执业药师考试西药药剂学笔记 (1)
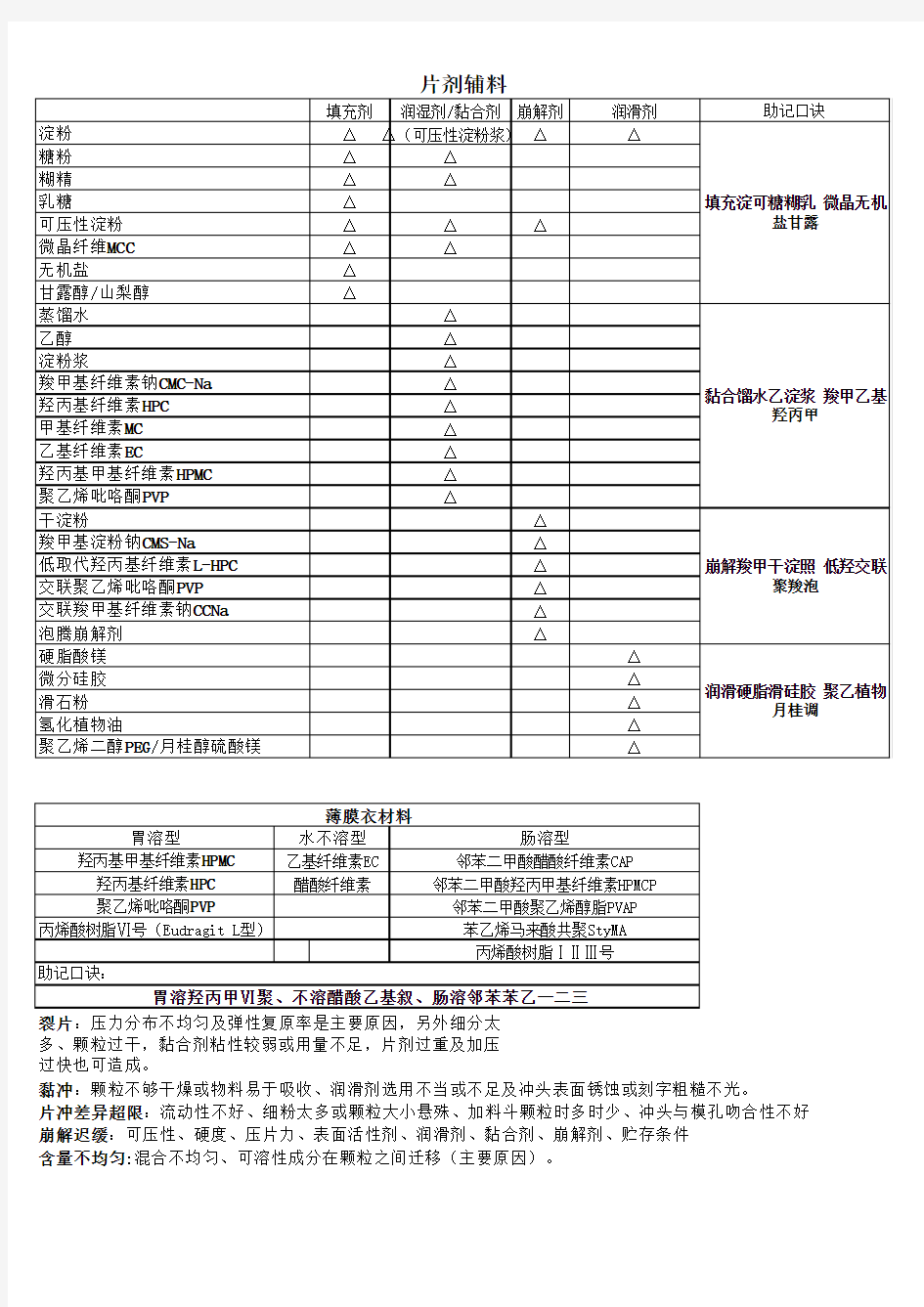

裂片:压力分布不均匀及弹性复原率是主要原因,另外细分太
多、颗粒过干,黏合剂粘性较弱或用量不足,片剂过重及加压
过快也可造成。
黏冲:颗粒不够干燥或物料易于吸收、润滑剂选用不当或不足及冲头表面锈蚀或刻字粗糙不光。
片冲差异超限:流动性不好、细粉太多或颗粒大小悬殊、加料斗颗粒时多时少、冲头与模孔吻合性不好崩解迟缓:可压性、硬度、压片力、表面活性剂、润滑剂、黏合剂、崩解剂、贮存条件
含量不均匀:混合不均匀、可溶性成分在颗粒之间迁移(主要原因)。
胶囊特点:1、掩盖不良嗅味、提高药物稳定性 2、提高生物利用度 3、弥补其他固体制剂的不足 4、延缓药物的释放和定位释放 不宜制成胶囊的药物:融化囊壁药物;易风化性药物;吸湿性强药物;易溶的有刺激性药物空胶囊制备流程:溶胶——蘸胶——干燥——拔壳——整理软囊壁组成增塑剂:甘油、山梨醇软胶囊制备方法:滴制法和压制法崩解时限:硬胶囊30min/软胶囊1h
滴丸剂常用基质:水溶性基质【PEG6000、PEG4000、泊洛沙姆、明胶】 非水溶性基质【硬脂酸、单硬脂酸甘油酯、氢化植物油】冷凝剂:液体石蜡、植物油、甲基硅油和水
制备要点:选择适宜的基质、确定合适的滴管内外口径、滴制过正中保持恒温、液压恒定、及时冷凝溶散时限:普通滴丸剂30min/包衣滴丸剂1h
小丸:药物与适宜的辅料均匀混合,制成球状或类球状固体制剂,可制成控释和缓释剂型小丸粒径:0.5-3.5mm
基质:油脂性基质【可可豆酯,多晶型α、β、βˊ、γ四种,其中β型最稳定。 半合成脂肪酸甘油酯【椰油酯、山苍子油酯、棕榈酸酯、脂肪酸丙二醇酯】 水溶性基质:1、甘油明胶(易滋生细菌,需抑菌剂)、
2、聚乙二醇类(不得与银盐、鞣酸、安替比林、奎宁、水杨酸类、苯佐卡因、氯碘喹啉、磺胺配伍
3、非离子型表面活性剂【聚氧乙烯40单硬脂酸酯类(Myri52)和泊洛沙姆(普朗尼克188)】
影响栓剂吸收的因素;
1、生理因素:距肛门2cm可避免肝首过,PH值7.4、直肠无粪便
2、理化性质:溶解度、粒径、脂溶性和解离度(酸性药物解离度>4.3或<
3、碱性药物<8.5或>10,快与慢3、基质和附加剂
置换价f:药物重量与同体积基质重量之比
药物需要基质重量x=(平均重量G—平均含药量W/置换价f)×拟制备的栓剂数量n
制备方法:热熔法和冷压法
融变时限:脂肪基质30min/水溶性基质1h 各剂型特殊评价
〖基质〗:1、油脂类基质【烃类(凡士林、固体石蜡、液体石蜡】凡士林特别适用不稳定抗生素,加入羊毛脂等增加吸水
【油脂类】【硅酮(不宜做眼膏基质,有刺激性)】【类脂类(羊毛脂、蜂蜡与鲸蜡】
2、乳状基质:①、【油包水W/O型与水包油O/W】禁用于糜烂、溃疡、水疱及脓疱症保湿剂:甘油、丙二醇和山梨醇 ②、乳状基质常用乳化剂和稳定剂
一价皂:O/W型,忌与阳离子表面活性剂及阳离子药物配伍多价皂:W/O型,
高级脂肪醇:十六醇和十八醇,弱性W/O型;增加稳定性和稠度
脂肪醇硫酸酯类:十二醇硫酸酯钠,为优良O/W型,系阴离子表面活性剂,不得与阳离子表面活性剂合用,遭破坏
③多元醇酯类:单硬脂脂肪酸甘油酯(W/O型)和脂肪酸山梨醇(司盘W/O)与聚山梨酯(吐温O/W) ④聚氧乙烯醚类:平平加O和乳化剂OP,两者属非离子表面活性剂O/W型乳化剂
3、水溶性基质:多用于润湿、糜烂创面,有利于分泌物排除,需加防腐剂。【甘油明胶、纤维素衍生物类(MC和CMC-Na)、PEG类】制备方法:研和法(小剂量)、熔和法(大剂量)和乳化法
特殊质量评价:微生物限度和无菌(烧伤或严重创伤的乳膏或软膏剂)
眼膏剂【无菌软膏剂】不得加入抑菌剂和抗氧剂
常用基质:黄凡士林、液体石蜡和羊毛脂混合比例8:1:1不溶性药物应先研成极细粉并通过9号筛凝胶剂【稠厚液体或半固体制剂】
常用基质:卡波姆(PH6-11有最大粘性和稠度)纤维素类衍生物(MC和CMC-Na)
气雾剂:含有药物溶液、乳状液或混悬液与适量的抛射剂共同封装于具有特定阀门系统容器的耐压容器内组成:药物、附加剂+抛射剂+耐压容器+阀门系统
特点:【优点】分布均匀、提高稳定性、避免首、提升用药顺应性、减少刺激、剂量准确 【缺点】成本高、易发生爆炸、有一定毒性、引起刺激或不适
栓剂【固体制剂】
软膏剂【半固体制剂】
气雾剂、膜剂和涂膜剂
分类:【分散系统】溶液型气雾剂(溶液),均相分散体,以雾滴喷出;混悬型气雾剂,非均相分散体(混悬液),以雾粒喷出; 乳剂型
气雾剂,非均相分散体(O/W或W/O型乳剂),以泡沫喷出。
胶囊【固体制剂】
滴丸剂:指固体或液体与适宜的基质加热熔融后溶解、乳化或混悬于基质中,再滴入不相混溶、互不作用的
冷凝液介质中,由于表面使用滴剂收缩成球状而成的制剂,主要供口服用
【相组成】二相气雾剂(气体和液体)和三相气雾剂(气体、固体和液体) 【医疗用途】吸入性气雾剂、皮肤黏膜气雾剂、空间消毒与杀虫气雾剂
气雾剂药物微粒大小:吸入性气雾剂雾滴(粒)大小控制在10μm以下,大多数应在5μm以下。
气雾剂的工艺流程:容器与阀门系统的处理与装配--药物配制与分装--填充抛射剂--质量检测--成品抛射剂的罐装:压罐法和冷压法
质量评价要点:泄漏率、每瓶总揿次、每揿主要含量、雾滴(粒)分布、喷出总量、无菌和微生物限度
有定量阀门的气雾剂检查:每瓶总揿次、每揿主药含量、雾滴(粒)分布非定量气雾剂检查:喷射速率和喷出总量
膜剂指药物与适宜的成膜材料加工制成的膜状制剂,可供口服、口含、舌下、粘膜、外用
成膜材料与附加剂:1/聚乙烯醇PVA(PVA05-88和PVA17-88)它们的醇解度均为88%,平均聚合度分别是500-600和1700-1800.
2/乙烯-醋酸乙烯共聚物EVA
3/附加剂:着色剂(色素、TiO2)增塑剂(甘油、山梨醇、丙二醇)脱膜剂(液体石蜡、甘油、硬脂酸、聚山梨酯-80)
涂膜剂;指药物溶解或分散于含膜材料溶剂中涂搽患处后形成薄膜的外用液体制剂成膜材料:聚乙烯醇、聚乙烯吡咯酮、乙基纤维素、聚乙烯醇缩甲乙醛。增塑剂:甘油、丙二醇、邻苯二甲酸二丁酯溶剂:乙醇
注射剂存在形式:溶液、乳状液、混悬液及临用前配成溶液或混悬液的粉末或浓溶液的无菌制剂
特点 【缺点】1、使用不便;2、注射疼痛;3、安全性不及口服制剂;4、制造过程复杂
给药途径(静脉滴注和推注(不得添加抑菌剂)、脊椎腔注射、肌内注射(1-5ml)/皮下注射(1-2ml)、皮内注射0.2ml 质量要求:无菌、无热源(重要指标)、可见异物、安全性、渗透性、PH值、稳定性、降压物质、澄清度、不溶性微粒
注射用水:【纯化水】饮用水经蒸馏法、离子交换法等制得的制药用水,不含附加剂,用作配制普通药物制剂的溶剂或实验用水
【注射用水】为纯化水经蒸馏所得的水,应符合细菌内毒素实验要求(无热源)
【灭菌注射用水】为注射用水按照注射剂生产工艺制备所得。不含任何添加剂,用于灭菌粉末的溶剂或注射剂稀释液注射用水质量要求:无热源和无菌
注射用水保存:在80℃以上保温、70℃以上保温循环存放、4℃一下状态存放。并在12小时内使用
注射用油:注射用大豆油规定为碘值126-140;皂角值188-195;酸值不大于0.1
酸值说明游离脂肪酸多少;碘值说明油中不饱和键多少;皂化值表示油中游离脂肪酸和结合成酯的脂肪酸多少
其他注射溶剂:乙醇、甘油、丙二醇、聚乙二醇、苯甲酸苄酯、二甲基乙酰胺
注射剂附加剂增溶剂、润湿剂和乳化剂:吐温、聚乙烯吡咯酮(PVP)、卵磷脂、普朗克尼
缓冲剂:醋酸、醋酸钠;枸橼酸、枸橼酸钠;乳酸;酒石酸、酒石酸钠。混悬剂:MC、CMC-Na、明胶
螯合剂:依地酸二钠(EDTA-2Na)
抗氧剂:亚硫酸钠、亚硫酸氢钠、焦亚硫酸氢钠、硫代硫酸钠、硫脲抑菌剂:三氯叔丁醇;苯甲醇;羟苯丁酯、丙酯;苯酚局麻剂:盐酸普鲁卡因、利多卡因渗透压调节剂:氯化钠、葡萄糖
热源:指微生物能引起恒温动物体温异常升高的物质。产生内毒素,由磷脂、脂多糖和蛋白质组成,脂多糖是内毒素的主要成分内毒素=热源=脂多糖 热源分子量一般为1×106
左右
热源性质: 耐热(180℃3-4分钟;250℃30-45分钟;650℃1分钟彻底破坏)
滤过性(体积小,1-5μm之间,一般均可通过,但活性炭可以吸附)水溶性(热源能溶于水)
不挥发性(蒸馏法去除热源的原理可被强酸强碱破坏
污染途径:注射用水带入(主要原因);辅料;输液器;容器用具管道和设备等带入
去除热源的方法:高温法、酸碱法、吸附法、超滤法(3.0-15nm超滤膜)、离子交换、凝胶虑过法、反渗透法
抛射剂的分类:氟氯烷烃(已禁用)、碳氢化合物(丙烷、正丁烷)、压缩气体(CO2)、氢氟氯烷烃与氢氟烷烃(三氟一氟乙烷HFA-134a
和七氟丙烷HFA-227)
膜剂和涂膜剂
注射剂
增加溶解度的方法:1、制成可溶性盐;2、引入亲水基因;3、加入助熔剂;4、使用混合溶剂(潜溶剂);5增加增溶剂虑过:指使固液混合物通过多孔介质,达到固-液分离的操作。分为介质滤过(固体<0.1%)和滤饼滤过(固体>0.1%)深层虑过包括:砂滤棒、垂熔玻璃漏斗、多孔陶瓷、石棉滤过板。
影响虑过因素:压力愈大虑速愈快;粘度愈大虑速愈慢;毛细管越细,阻力越大,不易虑过;虑速与滤层厚度成反比助滤剂:纸浆、硅藻油、活性炭滤器:砂滤棒
垂熔玻璃滤器(6号作无菌虑过),其化学性质稳定、滤过时无介质脱落、易于清洗微孔滤膜滤器:(种类)
醋酸纤维素膜:用于无菌虑过
硝酸纤维素膜:不耐酸碱、溶于有机溶剂,可在120℃、30分钟热压灭菌醋酸纤维与硝酸纤维混合酯膜:同硝酸纤维素膜
聚酰胺膜:适用于虑过弱酸、稀酸、碱类和普通溶剂
聚四氟乙烯膜:适用虑过酸性、碱性、有机溶剂,可耐260℃高温耐溶剂专用微孔膜
聚偏氟乙烯膜:具有耐氧化性和耐热性
可作除菌虑过用孔径为0.22μm
注射剂制备:原辅料准备、配制、灌封、灭菌、质量检查、包装
环境区划分:控制区和洁净区(精滤、灌封、冷却)
玻璃容器要求:无色透明;低膨胀系数、耐热性;耐热压力差;化学稳定性好;熔点低;不得有气泡、麻点及砂粒配制方法:稀配法和浓配法
注射剂的质量检查:1、可见异物(澄明度)检查
2、热原检查(家兔法和细菌内毒素检查法【鲎试验法】)
3、无菌检查
4、不溶性微粒检查
例:维生素C注射液:碳酸氢钠(ph调节剂)、依地酸二钠(金属络合剂)、亚硫酸钠(抗氧化剂)
概念:灭菌:杀灭所有微生物和细菌的芽孢;防腐:防止和抑制微生物生长繁殖;消毒:将病原微生物杀死。
D值:微生物耐热参数,系一定温度下细菌杀灭90%所需的时间,D值愈大,微生物耐热性越强。
Z值:灭菌温度系数,某一种微生物的D值下降一个对数单位,灭菌时间升高的值。即灭菌时间减少到原来的1/10所需要升高的温度。F值:以分为单位,常用于干热灭菌
F 0值仅用于热压灭菌,也可认为是以相当于121℃热压灭菌时杀死容器中全部微生物所需要的时间
灭菌法:
热压灭菌法所需温度:115℃(67kpa)30分钟、121℃(97kpa)20分钟;126℃(139kpa)15分钟
流通蒸汽灭菌
煮沸灭菌
煮沸30-60分钟,灭菌效果差,适用注射器、注射针等消毒
低温间歇灭菌
用流通蒸汽或60-80℃水加热1小时放置24小时再次灭菌,反复3-5次,适用于不耐高温的制剂火焰灭菌
干热空气灭菌法适用于耐高温玻璃制品、金属制品、以及不允许湿气穿透的油脂类和耐高温的粉末化学药品辐射灭菌
紫外线灭菌
适用无菌室及蒸馏水灭菌微波灭菌
适用水性注射液
虑过灭菌环氧乙烷等气体杀菌,适用粉末注射剂、不耐热的医用器具等苯扎溴铵溶液,用于其他灭菌辅助
无菌室灭菌
无菌操作
安瓿150-180℃,2-3小时干热灭菌;橡皮塞要121℃,1小时热压灭菌
输液可分为电解质输液、营养输液和胶体输液
按照GMP规定:一般洗涤、灌封室内洁净度为10000级,室内正压>4.9帕 洗瓶机、传送机、灌装机、盖膜、盖胶塞等关键部分,要求洁净度10000级或100级。输液从配置到灭菌以不超过4小时为宜。
干热灭菌
化学目的在于减少微生物数量,不能杀死芽孢,仅对繁殖
射线灭菌化学灭菌法
气体灭菌法
药液法常压下100℃流通蒸汽30-60分钟加热杀灭微生物的方法,本法不能保证杀灭全部芽孢,系非可靠灭菌
湿热灭菌
物理化学灭
菌法无菌操作法
输液质量要求:1、无菌,无热源;2、ph尽量等渗于血浆,控制在4-9范围;3、渗透压应等渗或偏高渗溶液;4、不得添加抑菌剂;5澄明
度符合
输液质量检查:1、澄明度;2不溶性微粒;3、热源、无菌检查;4、酸碱度及含量检查
例:
葡萄糖注射液:1、产生云雾状由于原料不纯,采用浓配法,滤膜滤过,加入适量的盐;2、ph值下降和颜色变黄,避免变色要严格控制灭
菌温度和时间,调节ph值在3.8-4.0较为稳定
静脉注射脂肪乳:乳化剂常用卵磷脂、豆磷脂及普朗尼克F-68,以卵磷脂为好,稳定剂常用油酸钠
右旋糖酐注射液:易夹杂热原,故活性炭用量较大。本品粘度高,需在较高温下虑过。不耐热。
血浆冰点降低为0.52;葡萄糖为0.09;氯化钠0.58
W(需要加入的药量=0.52-未经调整的药物冰点下降度/已调整等渗的药物1%(g/ml)溶液的冰点下降度数
例:用氯化钠配制100ml等渗溶液,需要多少氯化钠?1%:x%=0.58:0.52 x=1%×0.52%/0.58%=0.9%
渗透压调节剂:氯化钠和葡萄糖
等渗溶液:与血浆渗透压相等的溶液
等张溶液:与红细胞膜张力相等的溶液0.9%的氯化钠既是等渗溶液也是等张溶液。
注射剂的无痛化:常用止痛剂(利多卡因或0.5%三氯叔丁醇)
滴眼剂
质量要求1:ph值控制在5-9;2、渗透压相当于0.6-1.5%氯化钠溶液;3、无菌(角膜或手术用滴眼剂不得加入抑菌剂);4、可见异物【>50μm颗粒不得2粒并不得检出>90μm的粒子】;5、粘度在4.0-5.0;6、稳定性好
吸收途径:角膜和结合膜两条途径吸收。
无菌度的保持(眼用抑菌剂选择):
有机汞类:硝酸苯汞
季胺盐类:苯扎溴铵、苯扎氯铵
醇类:三氯叔丁醇
酯类:羟苯酯类(尼泊金
酸类:山梨醇
液体制剂
液体制剂质量要求:均匀相液体应该是澄明溶液,非均相液体制剂药物粒子应分散均匀,浓度准确等
液体溶剂常用溶剂
极性溶剂水、甘油、二甲基亚砜(产妇禁用)
半极性溶剂乙醇、丙二醇、PEG(分子量在1000以下为液体,超过1000为半固体或固体
非极性溶剂脂肪油、液体石蜡、醋酸乙酯
《中国药典》规定染菌数限量要求
口服给药、直肠给药:不得过1000个/g;液体制剂:不得过100个/ml,不得检出大肠杆菌
液体制剂、眼部给药、尿道、阴道、其他局部给药:不得过100个/g或ml或10平方厘米
局部给药:用于手术、烧伤及严重创面应符合无菌
常用防腐剂:
羟苯酯类(尼泊金类):丁酯最强
苯甲酸及其盐:0.25%苯甲酸和0.05-0.1%尼泊金合用对防止发霉和发酵最为理想
山梨酸
苯扎溴铵:阳离子表面活性剂】
醋酸氯已定
芳香水剂:指芳香挥发性药物的饱和或近饱和的水溶液,芳香水剂多数易分解、变质甚至霉变,故不宜大量配制
溶胶剂:固体药物微细粒子分散在水中形成的非均匀液体分散系统,微细粒子在1-100nm之间
性质光学性质;丁峰尔效应
电学性质:电泳现象
动力学性质:布朗运动
稳定性:热力学不稳定系统
制备方法;分散法【机械分散法、胶溶法和超声分散法】、凝聚法【物理凝聚法和化学凝聚法】
高分子溶剂:指高分子化合物溶解于溶剂中制成的均匀分散液体溶剂
性质:高分子渗透压:与高分子溶液浓度有关
高分子溶液的黏度和分子量
高分子溶液的稳定性【陈化现象:放置过程中自发的凝结而沉淀;絮凝现象:其他原因如盐类、ph值等使化合物凝结沉淀】
表面活性剂:具有很强表面活性并能使液体的表面张力显著下降的物质表面活性剂的种类:
皂角类硬脂酸钠、硬脂酸镁、硬脂酸钙、三乙醇胺皂
硫酸化物十二烷基硫酸钠
磺酸化物十二烷基苯磺酸
苯扎溴铵和苯扎氯铵卵磷脂
氨基酸型和甜菜碱型两性离子脂肪酸甘油酯W/O型乳剂辅助乳化剂蔗糖脂肪酸酯O/W型乳化剂、分散剂脂肪酸山梨坦(司盘)W/O型乳化剂
聚山梨酯(吐温)
O/W型乳化剂、增溶剂和润湿剂聚氧乙烯脂肪酸酯卖泽,作为O/W型乳化剂聚氧乙烯脂肪醇醚苄泽,作为O/W型乳化剂
聚氧乙烯一聚氧丙烯共聚物
特性:
临界胶束浓度;表面活性剂分子缔合形成胶束的最低浓度表面活性剂分子中亲油和亲水基团对油和水的综合亲和力
乳剂:两种互不相溶的两相液体混合,其中一相液体以液滴的状(分散相)分散于另一相液体中(分散介质)形成非均匀相液体分散体系。
乳剂中一相为水或水溶性溶液称为水相,以W表示,另一相与水不混溶的相称为油相,以O表示
微乳粒径在0.01-0.10μm范围,粒径在0.1-0.5μm范围称为亚微乳,为亚微乳时应控制在0.25-0.4μm范围内。
乳剂特点:分散度很大,药物吸收和药效发挥快,有利于提高利用度
水包油型可掩盖药物的不良臭味外用能改善对皮肤、粘膜的渗透性。
静脉注射乳注射剂注射后分布较快,药效高,有靶向性。
乳剂类型:O /W型和W/O型,W/O/W或O/W/O(多重乳剂)乳化剂种类:1、表面活性剂类乳化剂
阴离子:O/W硬脂酸钠、硬脂酸钾、油酸钠、油酸钾、十二烷基硫酸钠、十六烷基硫酸化蓖麻油,W/O硬脂酸钙阴离子:O/W单甘油脂肪酸酯,三甘油脂肪酸酯,吐温;W/O聚甘油硬脂酸酯,聚甘油油酸酯、司盘2、天然乳化剂:O/W阿拉伯胶,西黄蓍胶,明胶,卵黄; 杏树胶,3、固体微粒乳化剂
O/W:氢氧化镁、氢氧化铝、二氧化硅、皂土等W/O:氢氧化钙、氢氧化锌、硬脂酸镁
4、辅助乳化剂
增加水相粘度:MC、CMC-Na、HPC、海藻酸钠、琼脂、西黄蓍胶、阿拉伯胶、黄原胶等增加油相粘度:鲸琼醇、蜂蜡、单硬脂酸甘油酯、硬脂酸、硬脂醇等
乳化剂的选择:O/W型乳剂应选择HLB值在8-16的O/W型乳化剂,W/O型乳化剂应选择HLB值在3-6的W/O型乳化剂乳化形成必要条件:1、降低表面张力2、加入适宜的乳化剂3、形成牢固的乳化膜4、有适当的相体积比
乳剂的变化:分层出现分散粒子上浮或下沉现象,因密度差造成
絮凝分散相乳滴发生可逆的聚集现象,因电解质和离子型乳化剂的存在是主要原因 转相因某些条件变化而改变乳剂类型,因乳化剂的性质发生改变乳滴周围有乳化膜存在、乳化膜破坏导致乳滴变大称为合并,合并进一步发展使乳剂分为油水两相称破坏,是不可逆
混悬剂:难溶性固体药物以微粒状态分散于分散介质中形成的非均匀的液体制剂。
混悬剂中的药物微粒一般在0.5-10μm之间,小者可为0.1μm,大者可达50μm或更大。
混悬剂的物理稳定性:
1、混悬粒子的沉降速度:与微粒半径平方、微粒与分散介质的密度差成正比,与分散介质的粘度成反比。
2、微粒的荷电和水化
3、絮凝与反絮凝
乳化剂的制备:干胶法(植物油比例4:2:1,挥发油比例2:2:1,液体石蜡比例3:2:1),温胶法、新生皂法、两项交替法、机械法、微乳
制备、复核乳剂制备
合并并破坏
制成混悬剂的条件:凡是难溶性药物需制成液体制剂供临床用时;药物剂量超过溶解度而不能以溶剂形式应用时;两种溶液混合时药物溶解度降低而析出固体药物时;为了使药物产生缓释作用等条件下都可以考虑混悬剂。剧毒药物或剂量小的额药物不应制成混悬剂使用 Krafft点:离子型表面活性剂在溶液中随温度升高溶解增加,超过某一温度时溶解度急剧增大,这一温度称为Krafft点,该点越高的表面活性剂,临界胶束 浓度越小;它是离子型表面活性剂的特征值,也是表面活性剂应用温度的下限。
非离子表面活性剂泊洛沙姆(普朗尼克F68),作为O/W型乳化剂,适用于静脉乳剂极少乳化剂之一,能耐受高温和
低温冷冻
1、形成胶束
2、亲水亲油平衡值HLB
HLB值在3-8,表性活性剂适用于W/O型乳化剂,在8-16,使用O/W性乳化剂,作为增溶剂应在13-18,作为润湿剂应在7-9
3、增溶作用
昙点:指聚氧乙烯型非离子表面活性剂,温度升高可致聚氧乙烯链与水之间的氢键断裂,当温度上升到一定程度时,聚氧乙烯链可发生强烈脱水和收缩,使增溶空间减少,增溶能力下降,表面活性剂解离度急剧下降并析出,溶液出现浑浊,这一现象称为起昙。
阴离子表面活性剂阳离子表面活性剂
两性离子活性剂
4、结晶增长与转型
5、分散相的浓度和温度
混悬剂的稳定剂
混悬剂低分子助悬剂:甘油、糖浆剂等低分子化合物
高分子助悬剂:
天然高分子混悬剂:阿拉伯胶、西黄蓍胶、海藻琼钠
合成或半合成高分子助悬剂:CMC-Na、MC、HPC、HPMC、卡波姆、聚维酮、丙烯酸钠等
硅皂土
触变胶
润湿剂:聚山梨酯类、聚氧乙烯脂肪醇醚类、聚氧乙烯蓖麻油了类、磷脂类、泊洛沙姆等
絮凝剂与反絮凝剂
不同给药途径用液体制剂
合剂:以水为溶剂含有一种或一种以上药物成分的内服液体制剂
洗剂:指专供涂抹、敷于皮肤的外用液体制剂
搽剂:专供揉搽皮肤表面用的液体制剂
滴耳剂:指专供滴入耳腔内的外用液体制剂
滴鼻剂:指专供滴入鼻腔内使用的液体制剂
含漱剂:用于咽喉、口腔清洗的液体制剂
灌肠剂:经肛门灌入直肠使用的液体制剂
涂剂:指用纱布、棉花蘸取后涂搽皮肤、口腔或喉部黏膜的液体制剂
液体制剂的包装
内服液体标签:白底蓝字或黑字
外用液体制剂标签:白底红字或黄字
药物制剂的稳定性是评价药物制剂质量的重要指标之一
药物制剂基本要求是安全、有效、稳定
稳定性:化学稳定性:只药物由于水解氧化等因素发生降解,造成药物含量(效价)下降、产生有毒或副作用的降解产物、色泽发生改变物理稳定性:药物剂量发生物理变化,如混悬剂结块、结晶、乳剂分层、破裂、片剂的崩解度、溶出速度发生改变。
制剂中药物化学降解途径
1、水解:是药物降解的主要途径之一,属于此类的药物主要有酯类(普鲁卡因、对乙酰水杨酸)、内酯类(毛果芸香碱、华法
林)、酰胺类(氯霉素、青霉素类、头孢类、巴比妥类)药物等
2、氧化:也是药物降解常见的反应,属于此类的有酚类(肾上腺素、左旋多巴、吗啡、水杨酸钠)、烯醇类(维生素c)、吡
唑酮类(氨基比林、安乃近)、噻嗪类(盐酸氯丙嗪、异丙嗪)
3、其他反应:异构化、聚合、脱羧
影响药物制剂降解的因素
处方因素ph值的影响
广义酸碱化常用的缓冲剂如磷酸盐、醋酸盐、硼酸盐、枸橼酸盐及其相应的酸均为广义酸碱。
溶剂的影响
离子强度的影响
表面活性剂的影响
处方中辅料的影响
环境因素温度的影响
光线的影响
空气(氧)的影响
金属离子的影响
温度和水分的影响
包装材料的影响
稳定化的方法
改进剂型与生产工艺制成固体制剂、制成微囊或者包合物、采用直接压片或包衣工艺
制成稳定衍生物制成难溶性盐、酯类、酰胺类或高熔点衍生物。
加入干燥剂及改善包装
药物稳定性的试验方法
1、影响因素实验:高温试验(60℃温度下放置10天,于第5天和第10天取样)
高湿度实验(在25℃分别于相对湿度(90±5)%条件下放置10天,于第5天和第10天取样)
强光实验(在装有日光灯的光照箱内,于照度为4500±500)lx条件下放置10天,于第5天和第10天取样)
2、加速实验:探讨药物稳定性,3批供试品,在温度(40±2)℃,相对湿度(75±5)%条件下放置6个月
3、长期试验:制定药物有效期提供依据。3批供试品,在温度(25±2)℃,相对湿度(60±10)%条件下放置12个月,0/3/6/9/12个月取样
4、经典恒温法;用于新药申请。
5、药物有效期及贮存条件
阴凉处:不超过20℃;凉暗处:避光并不超过20℃,冷处:2-10℃,常温0-30℃。
重组人生长激素要求密闭,2-8℃保存
重组人工胰岛素要求遮光、密闭,﹣15℃一下保存,避免冰冻。
微型胶囊将固态药物或液态药物包裹在1-250μm的微小药库型胶囊
特点;1、提高药物稳定性
2、掩盖药物不良臭味及口味
3、防止药物在胃肠道失活
4、缓释或控释药物
5、使液态药物固态化
6、减少药物配伍禁忌
7、使药物浓集于靶区
常用囊材天然高分子囊材(明胶、阿拉伯胶、海藻酸盐、聚糖、蛋白质类)
半合成高分子囊材(CMC-Na、醋酸纤维素酞酸酯CAP、EC、MC)
合成高分子囊材
1)不受ph值影响的囊材:聚酰胺、硅橡胶
2)在一定ph值下溶解的囊材:聚丙烯酸树酯、聚乙烯醇
3)生物降解的合成聚合物:聚碳酯、聚氨基酸、聚乳酸PLA、乙酰酯丙交酯共聚物,聚乳酸-聚乙二醇崁段聚合物PLA-PEG。
微囊化的方法
物理法学法:单聚凝法、复聚凝法、溶剂-非溶剂法、改变温度发、液中干燥法
物理机械法:喷雾干燥法、喷雾冷冻法、空气混悬包衣法、多孔离心法、锅包衣法
化学法:界面缩聚法、辐射交联法
微囊的评价:微囊的囊型与粒径、微囊中药物含量、微囊的载药量与包封率、微囊中药物释放速率、有害有机溶剂限度检查
包合物由主分子和客分子两部分组成
包合过程是物理过程而不是化学过程,其稳定性主要取决于两者之间的范德华力。
包合物的材料
环糊精:α、β、γ-CYD三种,分别由6、7、8个葡萄糖分子构成,其中以β-CYD最为常用,分子量为1135.
环糊精衍生物:
水溶性环糊精衍生物:甲基衍生物、羟丙基衍生物、葡萄糖基衍生物
疏水性环糊精衍生物:乙基化β-CYD衍生物。
常用的包合方法:(饱和水溶液法、研磨法、冷冻干燥法、喷雾干燥法)
固体分散物指药物以一种形式分散在另一种水溶性或难溶性、肠溶性载体材料中形成固体分散体
释放原理药物以分子或微晶状态分散在载体材料形成的网状结构中,溶出时,药物必须首先扩散通过疏水性的网状结构骨架,故延缓释放。分散物载体材料:
水溶性载体材料
PEG类:适合熔融法、溶剂法制备固体分散物
聚维酮PVP类:适合溶剂法、研磨法制备固体分散物
表面活性剂类:适合熔融法和溶剂法制备固体分散物
有机酸类:与药物形成低共熔混合物。
糖类和醇类:与药物以氢键形成固体分散物,适用小剂量、熔点高的药物。
难溶性载体材料
维生素类:采用溶剂法制备固体分散物
聚丙烯树脂类:多采用溶剂法制备固体分散物
脂质类:适合熔融法制备。
肠溶性载体材料
维生素类:与药物制成肠溶性固体分散物。
聚丙烯树脂类:采用溶剂法制备肠溶性固体分散物。
固体分散物制备方法:熔融法、溶剂法、溶剂-熔融法、溶剂-喷雾(冷冻)干燥法、研磨法
缓释(非恒速)与控释(恒速释放)制剂
缓控释剂与普通口服制剂相比其主要特点:
1、对半衰期短的药物,可以减少给药次数、方便使用,提高患者的顺应性
2、血药浓度平稳,避免或减少小峰谷现象,有利于降低不良反应
3、减少用药总剂量,以最小剂量达到最大药效。
影响缓控释剂的因素
药物理化因素:剂量大小、解离度和水溶性、分配系数、稳定性
生物因素:生物半衰期、吸收、代谢。
缓控释剂的辅料多为高分子化合物:阻滞剂、骨架材料、增粘剂
阻滞剂指疏水性强的脂肪、腊类(生物型):蜂蜡、氢化植物油、硬脂醇、单硬脂酸甘油酯等作为溶蚀性骨架材料。
肠溶性阻滞剂:醋酸纤维素酞酸酯CAP、丙烯酸树脂L/S型、羟丙甲纤维素酞酸酯HPMCP、等
骨架材料:不溶性(EC、羟丙基丙烯酸酯、聚氯乙烯、聚乙烯、硅橡胶)
亲水胶体骨架(HPMC、MC、CMC-Na、PVP、卡波姆、海藻酸钠盐或钙盐等)
增粘剂:(明胶、PVP、CMC-Na、PVA、)
缓控释剂方法【制成溶解度小的盐或酯/与高分子化合物生成难溶性盐/控制粒子大小/将药物包藏于溶蚀性骨架或亲水性高分子材料中】
渗透泵原理:利用渗透泵原理制成的控释制剂,能均匀恒速地释放药物,其释放速率不受胃肠道可变因素影响,比骨架型缓释剂更优越膜内外渗透压的差别,药物由细孔持续流出。
致孔剂:PEG、PVP、PVA、十二烷基硫酸钠、糖或盐
渗透泵片由药物、半透膜材料(醋酸纤维素、乙基纤维素)、渗透压活性物质(氯化钠、乳糖、果糖、葡萄糖、甘露醇)和推动剂(分子量3000到500万的聚羟甲基丙烯酸烷基酯、分子量1万-36万的pvp、分子量20万-500万的聚氧乙烯)组成
经皮给药制剂TDDS:由毛细血管和淋巴管吸收进入体循环,广义指软膏剂、硬膏剂、贴剂,狭义指贴剂,能起全身作用
优点1、避免肝脏首过效应
2、减少给药次数
3、维持恒定需要浓度
4、给要方便,可随时中断给药
缺点1、仅限于剂量小药理作用强的药物
2、对皮肤有刺激性和过敏性
3、存在皮肤代谢和储库作用
组成:背衬层、药物贮库层、控释膜、粘附层和保护层
TDDS类型可分为膜控释型和骨架型两类
填充封闭型TDDS:控释膜以乙烯-醋酸乙烯共聚物EVA制得,压敏胶常用硅橡胶和丙烯酸酯类,代表药物:硝苯地平、芬太尼
复合模型TDDS:药物储库是将药物分散在聚异丁烯等压敏胶中,代表药物:东莨菪碱和可乐定
黏胶分散型TDDS:代表性药物::硝酸甘油Deponit
聚合物型TDDS:加入吸水垫,目的在于吸收和排出过量的汗液,使TDDS保持良好的粘附性,代表药物:硝酸甘油Nitro-Dur
微储库型TDDS
吸收与途径
药物吸收过程包括释放、穿透及吸收入血液三个阶段
吸收途径有2条:表皮途径和皮肤附属器
影响因素1、油性药物吸收大于水溶性药物
2、药物吸收与分子量成正比
3、低熔点药物容易通过皮肤
4、溶液态药物>混悬态药物、微粉>细粒、
经皮促进剂
1、二甲亚砜及同系物:二甲亚砜DMSO
2、氮酮类化合物:月桂氮卓酮
3、醇类、表面活性剂等
TDDS制备方法
1、涂膜复合工艺
2、填充热合工艺
3、骨架粘合工艺
质量评价:均匀度(±25%),释放度、微生物限度
靶向制剂
分类1、被动靶向制剂:>100nm的纳米囊与纳米球集于骨髓,<3μm时一般被肝、脾中巨噬细胞摄取,>7μm的微粒通常被肺截留
2、主动靶向制剂
3、物理化学靶向制剂
评价相对摄取率re、靶向效率te、峰浓度比ce,三者值越大,靶向性越好
被动靶向制剂
脂质体:将药物被类脂双分子层包封的微小泡囊。由磷脂为主要膜材并加入胆固醇等附加剂制成
特点;1、靶向性和淋巴定向性
2、缓释性
3、细胞亲和性与组织相容性
4、降低药物毒性
5、提高稳定性
脂质体两个重要理化性质:相变温度和荷电性
制备脂质体材料:磷脂和胆固醇
制备方法:注入法、薄膜分散法、超声波分散法、逆向蒸发法、冷冻干燥法
靶向乳剂:靶向性特点在于它对淋巴系统的亲和性
转运途径:血液、消化道、组织
微球药物与适合的高分子材料制成的球形或类球形骨架实体,粒径通常在1-250μm之间,一般制成混悬剂供注射或口服微球特性:靶向性和缓释性
纳米粒属于基质型骨架,纳米球粒径在10-1000nm范围,分散在类似胶体溶液中
制备方法:聚合法、天然高分子凝聚法、液中干燥法
主动靶向制剂
修饰的药物微粒载体
1、修饰的脂质体
长循环脂质体(PEG修饰)
免疫脂质体
配体修饰脂质体
2、修饰的微乳
3、修饰的微球
4、修饰的纳米粒
前体药物
物理化学靶向制剂
磁性靶向制剂热敏靶向制剂
拴塞靶向制剂ph敏感靶向制剂
结肠靶向制剂
生物药剂学:研究药物在体内吸收、分布、代谢与排泄过程,阐明药物的剂型因素、用药对象的生物因素与药效之间的关系的科学。药物跨膜转运药物吸收过程也就是一个膜转运的过程药物通过生物膜的转运方式:
4、膜动转运:分为胞饮和吞噬,膜动转运对蛋白质和多肽的吸收非常重要。
影响胃肠道吸收的因素生理性因素
胃肠液的成分与性质胃排空与胃蠕动循环系统影响食物影响
剂型因素
药物理化性质对吸收的影响
药物的剂型与给药途径对吸收的影响:口服制剂:水溶液>混悬剂>散剂>胶囊剂>片剂>包衣片剂各种注射剂药物释放速度排序:水溶液>水混悬液>油溶液>O/W乳剂>W/O乳剂>油混悬剂
药物动力学:药物体内药量随时间变化规律的科学隔室模型单室隔模型
二隔室模型:包括中央室、周边室多隔室模型
药物消除常数K:大多数药物从体内消除符合表观一级速度过程
生物半衰期t1/2,即体内药量或血药浓度下降一半所需要的时间,衡量药物消除速度快慢,t1/2=0.693/k 清除率Cl:在单位时间内消除掉相当于多少体积的流经血液中的药物。Cl=kv(v指表观分布容积)
单室模型静脉注射给药:在体内只有消除,按照一级过程进行,即药物消除速度与体内药量的一次方成正比。
dX/dt=-Kx X=X 0e -kt
logX=(-k/2.303)t+logX 0
单室模型静脉滴注
dX/dt=k 0-kx
X=k 0(1-e -kt )/k C=k 0(1-e-kt)/k
稳态血药浓度
C ss =k 0/Vk
稳态后停滴
C'=k 0e -kt /Vk
logC'=(-k/2.303)t'+k0/Vk
稳态前停药
C'=C T e -kt =[k 0(1-e -kT )/Vk]e -kt'/Vk logC'=(-k/2.303)t'+log[k 0(1-e -kT )/Vk]
血管外给药
C=K αFX 0/V(k α-k)(e kt -e k αt )
血药浓度-时间曲线下的面积AUC=FX 0/Vk 清除率Cl=FX 0/AUC 生物利用度
绝对生物利用度:F Ab =[AUC po /X 0(po)]/[AUC iv /X 0(iv )]×100%相对生物利用度:F Rel =[AUC 实验/X 0(实验)]/[AUC 参比/X 0(参比)]×100%
1、被动扩散:大多数药物通过这种方式透过生物膜。高浓度向低浓度顺浓度差转运,呈一级速度过程,不需要载体,也不消耗能量,无饱和现象和竞争抑制现象。转运途径:溶解扩散和限制扩散
2、主动转运:逆浓度差转运,需要消耗能量,与载体有关,可出现饱和现象;可与类似结构物质发生竞争现象;受代谢抑制剂影响,且有结构特和部位特异性。主动转运速度可以采用米氏方程式描述。
3、促进扩散:又称易化扩散,是指一些物质在细胞膜载体帮助下,由膜的高浓度一侧向低浓度一侧扩散或转运的过程。有饱和现象,透过速度符合米氏方程式,对转运物质有结构特异性要求,可被类似结构竞争抑制。与主动转运不同之处:促进不消耗能量,而且是顺浓度差。
单剂静脉是基础,e变对数找log
静滴要找k0值,静滴速度别忘记
生物利用度和生物等效性实验原理及原则
生物样品分析方法要求:1、专属性;2、定量下限;3、精密度与准确度;4、准确度高;5、样品稳定,提取回收率、质量控制等
普通制剂
受试者的选择:在人体内进行,应选择正常、健康的自愿受试者,年龄18-40周岁,男性,体重±10%,要求18-24例。应与受试者签订知情同意书。
参比制剂:首选考虑国内外已上市相同剂型的市场主导制剂作为标准参比制剂
受试制剂:受试与参比制剂实际含量差异在5%以内
实验设计:通常采用双周期交叉随机试验设计,每个周期之间洗净期通常为1周或2周。取样点至少取4个点,峰后取6个或以上,总采点不少于12个点。整个采样期时间至少应为3-5个半衰期。
药物动力学分析参数主要有生物半衰期t1/2、峰浓度C max、血药浓度-时间下滑面积AUC
药物制剂的配伍变化与相互作用
配伍使用的目的
1、协同作用;复方乙酰水杨酸、复方降压片
2、提高疗效,降低副作用等磺胺药+甲氧苄啶TMP联合应用,阿莫西林+克拉维酸联用
3、利用药物拮抗作用克服副作用:吗啡镇痛配伍阿托品
4、为预防或治疗合并症
配伍变化类型
物理变化溶解度变化
潮解、液化和结块
分散状态或粒径改变
化学变化
变色维生素c与烟酰胺;多巴胺与碳酸氢钠、氨茶碱或异烟肼与乳糖粉
混浊和沉淀
ph值改变水杨酸钠或苯巴比妥遇到酸或酸性药物
水解苯巴比妥钠水解产生无效的苯乙基乙酰脲,硫酸锌滴眼液加入少量的硼酸防止水解
生物碱盐黄连素与黄芩苷;鞣酸、碘、碘化钾遇到乌洛托品产生沉淀
复分解硫酸镁遇到钙盐、碳酸氢钠产生沉淀
产气溴化铵、氯化铵或乌洛托品与强碱性药物配伍;溴化铵与利尿剂配伍
分解破坏,疗效下降维生素b12和维生素c合用,环丙沙星与甲硝唑混合,红霉素与葡萄糖氯化钠混合
发生爆炸氯化钾与硫、高峰酸钾与甘油、强氧化剂与葡萄糖或蔗糖
不适合于与其他注射剂配伍的是:血液、甘露醇、脂肪乳
注射液配伍变化的主要原因
1、溶剂组成改变7、配合量
2、ph值改变8、混合顺序
3、缓冲容量9、反应时间
4、离子作用10、氧与二氧化碳影响
5、直接反应11、光敏感
6、盐析反应12、成分的纯度
配伍变化的处理方法
1、改变贮存条件
2、改变调配顺序
3、改变溶剂或添加助溶剂
4、调整ph值
5、调整有效成分或改变剂型
生物技术:又称生物工程,包括基因工程(含蛋白质工程)、细胞工程、发酵工程和酶工程
大多数是蛋白质或多肽类药物,临床使用剂量小,药理活性灵活,副作用少,很少有过敏反应,但稳定性差,在体内酸碱环境或酶存在下极易失活,不能口服只能注射给药,此类药物生物半衰期较短,从血中消失很快。
