江苏省会计从业资格考试 财经法规知识点汇总

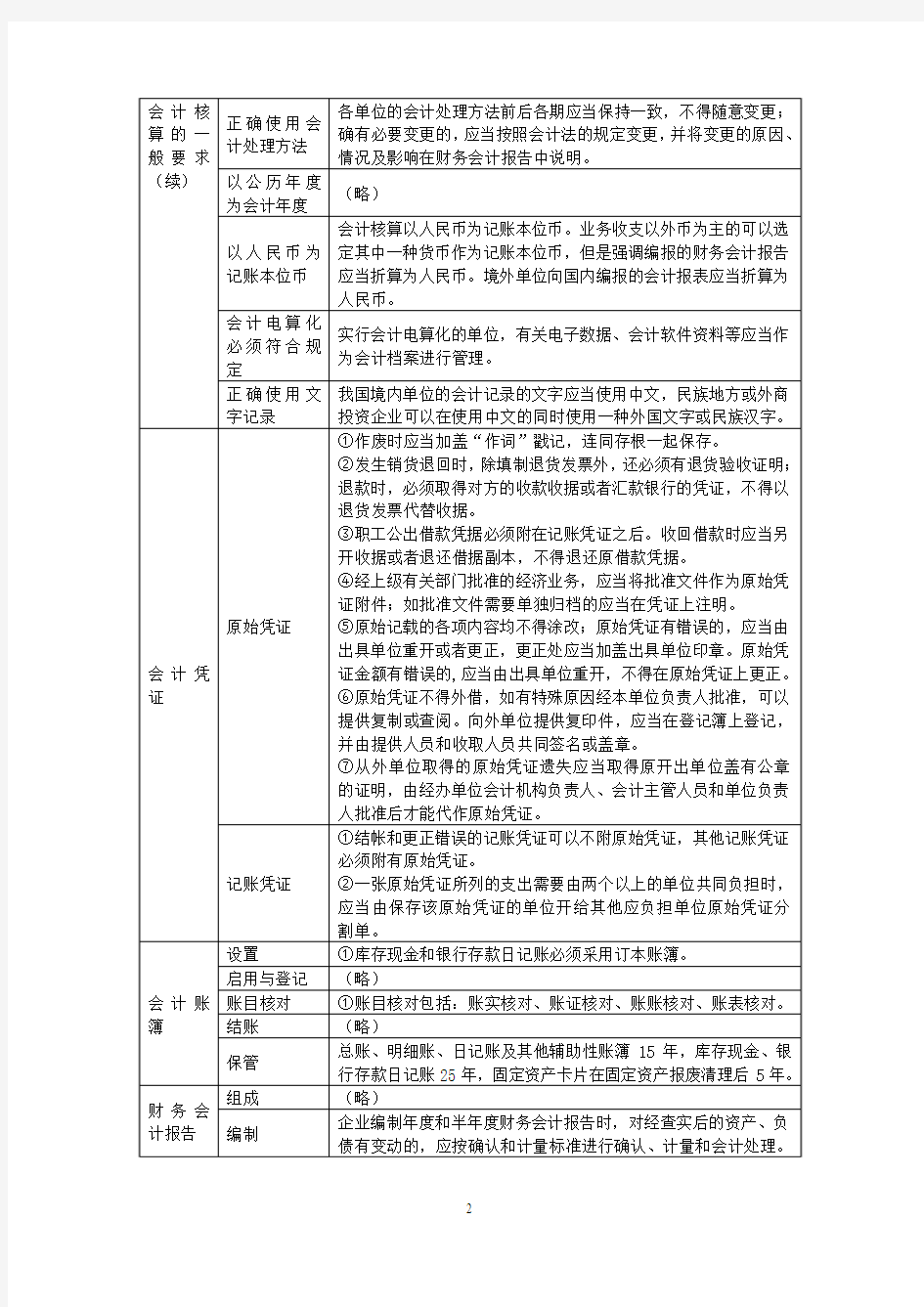
《财经法规与会计职业道德》知识点汇总第一章会计法律制度
七、会计法律制度案例分析(略)
第二章支付结算法律制度
二、银行结算账户
第三章税收征收管理法律制度
第四章会计职业道德
北京工商大学管理学考点重点知识点总结
一概述。 1.选择: A管理概念:特定的环境条件下,以人为中心,对组织所有拥有的资源进行有效的计划、组织、领导、控制、以便达到既定组织目标的过程。 B主体:人管理是组织中的管理,管理的载体是组织,由担任主管工作的人或小组来完成; 管理的对象:一切可调用的资源 管理的目标:有效率地完成组织既定目标,达成期望效果 管理的本质:活动或过程(分配、协调或过程) 管理的职能:获取信息、决策、计划、组织、领导、控制、和创新; 管理的核心:协调人际关系 C.评价管理工作有效性指标:效率,效果 D管理的科学与技术之争1.作为科学的管理,客观规律性,可检验性和系统性。2.作为艺术的管理,正是指管理是一门艺术,正是指管理者在管理实践过程中随地制宜地、创造性地运用管理技术和方法来解决管理问题,它有很强的技艺和技巧性。3.离不开扎实的管理理论知识,又离不开自身主观能动性和创造性的充分发挥。E.系统组织是(开放式)的 F组织与环境的关系包括两个方面:1.外部环境对组织的决定、制约和影响作用。2.组织对环境的消极被动的或者积极主动的适应。 组织环境分为一般环境和任务环境.____.一般环境,指对某一特定社会中一切组织都会发生影响、都会起作用,具有普遍意义的共有环境____任务环境,具有直接的、具体的和经常性的亦即特殊影响和特定环境。 G管理职能的拓展:1.决策是各项管理职能的核心2.创新是各项管理职能的灵魂3.协调是管理工作的本质要求H. pdca循环:提出者:美国戴明。p计划-d执行-c检查-a行动pdca循环的过程就是发现问题,解决问题的过程。pdca循环特点:1.大环带小环。2.阶梯式上升 I古典管理理论:1.泰罗——科学管理理论。三个基本出发点:1,科学管理的根本目的是谋求最高工作效率,即提高劳动生产率。2.用科学管理来代替传统的经验管理。3.科学管理的核心是要求管理人员和工人双方都实行重要的精神变革——心理革命 J法约尔十四条管理原则(1)劳动分工(2)权力和责任(3)纪律(4)统一指挥(5)统一领导(6)个人利益服从整体利益(7)员工报酬(8)集权原则(9)等级制度(10)秩序(11)公平(12)人员的稳定(13)首创精神(14)团结合作实质:统一指挥和等级制度 2.简答.A管理的六大职能:计划、组织、人力资源管理、领导、沟通、控制。 B按组织中所处层级,将管理者划分为: 高级管理者(决策层),中层管理者,高级管理决策的执行者(执行层),基层管理者(作业层) C管理者角色分为三大类:人际角色(代表人,领导者,联络者)信息传递(监督者,传播者,发言人)决策制定(企业家,混乱驾驭着,资源分配者,判断者) D管理者的技能1.技术技能(基层管理者最重要)。2.人事技能。(中层管理者)3.概念技能(1思想技能。2设计技能) E西方管理思想与管理理论的发展可以分为三个阶段:(1)古典管理理论阶段:泰罗开创的科学管理理论、法约尔所提出的一般管理理论,韦伯的理想的行政组织体系理论等 (2)近代的“人际关系”——梅奥人际关系学说的霍桑试验《工业文明的人类问题》“行为科学” (3)当代管理理论阶段:罗德3孔茨管理丛林,西蒙决策理论。法约尔管理过程权变管理,德鲁克经验管理,数量管理(管理科学,运营管理,管理信息) F:泰罗具体方法:1.科学作业管理2.计件付酬原理3.计划与作业分离原理。4.职能组织原理。5例外管理原理。。6.人事管理原则 G法约尔五大管理职能。计划、组织、指挥、协调、控制 H韦伯,组织权力的类型:@@@ 传统的权力形式(效率最低)@@@超凡的权力形式(对某人所持有的非凡性的热爱)@@@ 法理性的权力形式(最理想)
高考语文最常见的23个易错考点
高考语文最常见的23个易错考点 易错1 多音字误读 易错分析:正确识记多音字的读音,可以从这样几个方面入手。一是词性。如“刹”,共有chà和shā两个读音,作名词时读chà,作动词时读shā。二是词义。有些多音字的读音,单从词性上很难判断,可以以义辨音。如“纤”有xiān和qiàn两个读音,作形容词表示“细小”时读xiān,作名词表示拉船的绳子时读qiàn。三是语境。可以把多音字的几个读音尽可能放在具体的语言环境中来辨别,这样既能增加趣味性,又能提高记忆效果。如“商店打折(zhé),顾客抢购。一阵折(zhē)腾,累得住院。不但没赚,反而折(shé)本”。四是语体。书面语读音一般用于双音节词和成语中,口语读音常用于口头交际中,用于单音节词和少数表示日常生活事物的双音节词中。如“色”,书面语读音为sè,口语读音为shǎi。五是巧记。舍众取寡,以少推多。如“埋”只在“埋怨”中读mán,其余都读mái。记住一个“埋怨”,就记住“埋”在各种语境中的读音了。 易错2 音近字误读 易错分析:汉字中的同音字很多,这些字的声母、韵母和声调都完全一致。但如果其中的或声母,或韵母,或声调有细微的差别,就构成了音近字。命题者往往就在“近”与“同”上做文章。如果在平时学习中没能把容易混淆的音近字准确地区别开来,就会给解题增加难度。正确识记这些字的读音,需要日积月累的过程,把某类同音字集中起来记忆,会达到记住一串且印象深刻的效果。 易错3 形近字误读 易错分析:辨别形近字,要找出形近字之间的不同之处,从细微处加深印象,加强记忆。有很多可以采用口诀记忆法,如“戍、戌、戊、戎”可以编为“点戍(shù)横戌(xū)戊(wù)中空,十戈相合即为戎(rónɡ)”。应该说,对这类字音的识记,既要动脑筋求便捷,更要花工夫记忆,关键在于积累。而就具体题目来说,其中一定会有部分字音是我们已经正确掌握的。因此,审清题干,认真分析,结合字义,合理推断,运用比较排除的方法选出正确答案并非难事。 易错4 形声字误读 易错分析:形声字的“声旁”是表声的,但由于古今音的差异,现代汉语形声字中有70%左右已不能按其“声旁”确定读音了,它们中有的声母发生了变化,有的韵母发生了变化,有的声母和韵母都发生了变化。如果我们不注意这些变化,仍然按照“声旁”的读音去读,就会发生误读。在解答中无法判断时,一般形声字注音为“同声旁读音”的正确性小,注音为“不同声旁读音”的正确性大。所以,我们一方面要深入研究高考(论坛)试题,明了形声字读音设误的主要形式,即故意以声旁注音或故意以同一声旁不同形旁的字的常读音注音;另一方面要摒弃“汉字读半边,不会错上天”的错误想法,养成勤查字典词典的习惯,准确记忆,注重积累。 易错5 习惯性误读 易错分析:由于习惯原因,尤其是方言的原因,人们在生活中常常无意识地把一些字“约定俗成”地读错。如把“豇”读成ɡānɡ,把“埋怨”中的“埋”读成mái,把“涮”读成shuā,把“档”读成dǎnɡ等。普通话基本功不扎实,在解题时常常会受习惯的影响而作出错误的判断。养成说普通话的习惯是解决习惯性误读问题的最好方法。我们平时要有意识地注意这些习惯性误读字。一是注重分类整理。注意收集生活中的习惯性误读字,从易错点入手分声母、韵母、声调三类进行整理。二是讲究即时记忆。一经发现,即时记忆,今天掌握一点,明天掌握一点,积少成多,不能等收集到一定的量才去突击强记。三是注意适时复习。每隔一段时间就要拿出来看看、读读,反复记忆,加深印象,直到真正掌握。 易错6 混淆形近字
选修三易考知识点背诵
生物选修三易考知识点背诵 专题1 基因工程 基因工程的概念 基因工程是指按照人们的愿望,进行严格的设计,通过体外DNA重组和转基因技术,赋予生物以新的遗传特性,创造出更符合人们需要的新的生物类型和生物产品。基因工程是在DNA分子水平上进行设计和施工的,又叫做DNA重组技术。 (一)基因工程的基本工具 1.“分子手术刀”——限制性核酸切酶(限制酶) (1)来源: 主要是从原核生物中分离纯化出来的。 (2)功能: 能够识别双链DNA分子的某种特定的核苷酸序列,并且使每一条链中特定部位的两个核苷酸之间的磷酸二酯键断开,因此具有专一性。 (3)结果: 经限制酶切割产生的DNA片段末端通常有两种形式:黏性末端和平末端。 EcoRI限制酶的切割产生黏性末端,SmaI限制酶的切割产生平末端。 2.“分子缝合针”——DNA连接酶 DNA连接酶)的比较: (1)两种DNA连接酶(E·coliDNA连接酶和T 4- ①相同点:都缝合磷酸二酯键。 ②区别: E·coliDNA连接酶来源于大肠杆菌,只能将双链DNA片段互补的黏性末端之间的磷酸二酯键连接起来;而T DNA连接酶能缝合两种末端,但连接平末端的 4 之间的效率较低。 (2)与DNA聚合酶作用的异同: DNA聚合酶只能将单个核苷酸加到已有的核苷酸片段的末端,形成磷酸二酯键。DNA连接酶是连接两个DNA片段的末端,形成磷酸二酯键。 3.“分子运输车”——运载体 (1)载体具备的条件: ①能在受体细胞中复制并稳定保存。 ②具有一至多个限制酶切点,供外源DNA片段插入。 ③具有标记基因,供重组DNA的鉴定和选择。 (2)最常用的载体是质粒,它是一种裸露的、结构简单的、独立于细菌染色体之外,并具有自我复制能力的双链环状DNA分子。 (3)其它载体:噬菌体的衍生物、动植物病毒。 (二)基因工程的基本操作程序
高考化学必背基础知识点归纳
高考化学必背基础知识点归纳 1.注意加热方式 有机实验往往需要加热,而不同的实验其加热方式可能不一样。 ⑴酒精灯加热。 酒精灯的火焰温度一般在400~500℃,所以需要温度不太高的实验都可用酒精灯加热。教材中用酒精灯加热的有机实验是:“乙烯的制备实验”、“乙酸乙酯的制取实验”“蒸馏石油实验”和“石蜡的催化裂化实验”。 ⑵酒精喷灯加热。酒精喷灯的火焰温度比酒精灯的火焰温度要高得多,所以需要较高温度的有机实验可采用酒精喷灯加热。教材中用酒精喷灯加热的有机实验是:“煤的干馏实验”。 ⑶水浴加热。水浴加热的温度不超过100℃。教材中用水浴加热的有机实验有:“银镜实验(包括醛类、糖类等的所有的银镜实验)”、“ 硝基苯的制取实验(水浴温度为6 0℃)”、“酚醛树酯的制取实验(沸水浴)”、“乙酸乙酯的水解实验(水浴温度为70℃~80℃)”和“糖类(包括二糖、 淀粉和纤维素等)水解实验(热水浴)”。 ⑷用温度计测温的有机实验有:“硝基苯的制取实验”、“乙酸乙酯的制取实验”(以上两个实验中的温度计水银球都是插在反应液外的水浴液中,测定水浴的温度)、“乙烯的实验室制取实验”(温度计水银球插入反应液中,测定反应液的温度)和“
石油的蒸馏实验”(温度计水银球应插在具支烧瓶支管口处,测定馏出物的温度)。 2、注意催化剂的使用 ⑴ 硫酸做催化剂的实验有:“乙烯的制取实验”、 “硝基苯的制取实验”、“乙酸乙酯的制取实验”、“纤维素硝酸酯的制取实验”、“糖类(包括二糖、淀粉和纤维素)水解实验”和“乙酸乙酯的水解实验”。 其中前四个实验的催化剂为浓硫酸,后两个实验的催化剂为稀硫酸,其中最后一个实验也可以用氢氧化钠溶液做催化剂 ⑵铁做催化剂的实验有:溴苯的制取实验(实际上起催化作用的是溴与铁反应后生成的溴化铁)。 ⑶氧化铝做催化剂的实验有:石蜡的催化裂化实验。 3、注意反应物的量 有机实验要注意严格控制反应物的量及各反应物的比例,如“乙烯的制备实验”必须注意乙醇和浓硫酸的比例为1:3,且需要的量不要太多,否则反应物升温太慢,副反应较多,从而影响了乙烯的产率。 4、注意冷却 有机实验中的反应物和产物多为挥发性的有害物质,所以必须注意对挥发出的反应物和产物进行冷却。 ⑴需要冷水(用冷凝管盛装)冷却的实验:“蒸馏水的制取实验”和“石油的蒸馏实验”。
个人与团队管理各知识点
《个人与团队管理》各章知识点 第一单元自我规划 第1章:思考你的目标 1、什么是创造性思维方法,你的工作当中的哪些方面适合应用创造性思维方法? 创造性思维是指不依常规、寻求变异、想出新方法、建立新理论、从多方面寻求答案的开放式思维方式。头脑风暴法的规则遵循两个独立的阶段,这两个阶段不能同时进行。在我们的工作中,经常会遇到比如:制定目标、解决问题的情况,我们经常采用头脑风暴法。 例:培养创造型思维是培养创造能力的一个方面。(对) 2、什么是头脑风暴法?个人和集体使用头脑风暴进行创造性思维有什么区别和联系? 头脑风暴法(Brainstorming)是为了克服阻碍产生创造性方案的遵从压力的一种相对简单的方法,它利用一种思想产生过程,鼓励提出任何种类的方案设计思想,同时禁止对各种方案的任何批评。个人头脑风暴不会受到别人的干扰,但是思路狭窄;团队头脑风暴法能够集中很多人的意见,但是人们往往会有所顾虑。3、假如你现在面对职业或工作的选择,你会采用什么手段来面对这些选择? 具体情况具体对待。面对不同的情况,应该有不同的方法。一般来讲包括: 改变境遇 积极进取——使自己更加适应; 面对其他挑战,如参加训练和培训; 改善工作环境; 授权给其他人,让他们承担一些日常事务。 改变自己 检查自己的真实想法——嘴上说的和心中想的是否一致; 改变行为; 发展在其他领域的技能和能力 改变个人与工作之间的关系 适应工作; 将工作看作达到目标的方法; 通过降低问题的重要性来改变看法——更注重工作之余的生活。 离开 4、请思考你是如何制定自己的目标和计划的。 制定目标时首先应该分析自己的现状,考虑自己的选择,这种情况可以用个人头脑风暴法来进行,但是一定要遵循头脑风暴法的规则。 制定计划:可以按照计划的时间长短进行,长期计划一般是提纲挈领的;而短期的计划则是详细具体的,事情的时间、地点、人物等都应该具体详细。当然其他的方法也可以。 第2章:自我认知 1、什么是自我认知?在日常生活中你是怎样了解自己和他人的? 自我认知是情感智能框架中的一个方面,也就是了解自己的情感,主要包括:情感自我认知、正确的自我评估、自信等。一般通过测试,视个人情况而定,只要合理即可。 一般来说:与他人沟通,理解他人,换角度思考,反思自己的行为,接受各种反馈意见等都能帮助你去理解自己和他人。 例:情感智能框架中的认知包括( D )。
2020英语四级【易错知识点总结-常考易错题精选及解析
------------------------------------------------------------- 考点------ 可数名词的数 There are fifty _____ in our school. They are all friendly to us. A. woman teachers B. women teacher C. woman teacher D. women teachers 【易错选项】选A 【易错原因】复合名词变复数时, 忽视由man和woman构成的复合名词这一特殊形式。 【正确答案】D 【试题解析】由man和woman构成的复合名词变复数时,前后两个名词都要变成复数。 ------------------------------------------------------------- 考点------ 不可数名词 I'm so hungry. Please give me _____ to eat. A. three bread B. three pieces of bread
C. three pieces of breads 【易错选项】选C 【易错原因】未掌握不可数名词的数量表达。 【正确答案】B 【试题解析】bread为不可数名词,没有复数形式,表示数量时, 不能用数词直接来修饰,可借助表示数量单位的短语修饰。 ------------------------------------------------------------- 考点------ 名词所有格 ---What is _____ brother? ---He is a policeman A. Jim's and paul's B. Jim and Paul C. Jim and paul's 【易错选项】选A 【易错原因】混淆表示共有和各自拥有时的所有格结构。 【正确答案】C 【试题解析】由问句中的brother及答语中的He可知, 此处表示Jim
高中化学选修3知识点总结
高中化学选修3知识点总结 二、复习要点 1、原子结构 2、元素周期表和元素周期律 3、共价键 4、分子的空间构型 5、分子的性质 6、晶体的结构和性质 (一)原子结构 1、能层和能级 (1)能层和能级的划分 ①在同一个原子中,离核越近能层能量越低。 ②同一个能层的电子,能量也可能不同,还可以把它们分成能级s、p、d、f,能量由低到高依次为s、p、d、f。 ③任一能层,能级数等于能层序数。 ④s、p、d、f……可容纳的电子数依次是1、3、5、7……的两倍。 ⑤能层不同能级相同,所容纳的最多电子数相同。 (2)能层、能级、原子轨道之间的关系 每能层所容纳的最多电子数是:2n2(n:能层的序数)。 2、构造原理 (1)构造原理是电子排入轨道的顺序,构造原理揭示了原子核外电子的能级分布。 (2)构造原理是书写基态原子电子排布式的依据,也是绘制基态原子轨道表示式的主要依据之一。
(3)不同能层的能级有交错现象,如E(3d)>E(4s)、E(4d)>E(5s)、E(5d)>E(6s)、E(6d)>E(7s)、E(4f)>E(5p)、E(4f)>E(6s)等。原子轨道的能量关系是:ns<(n-2)f <(n-1)d <np (4)能级组序数对应着元素周期表的周期序数,能级组原子轨道所容纳电子数目对应着每个周期的元素数目。 根据构造原理,在多电子原子的电子排布中:各能层最多容纳的电子数为2n2 ;最外层不超过8个电子;次外层不超过18个电子;倒数第三层不超过32个电子。 (5)基态和激发态 ①基态:最低能量状态。处于最低能量状态的原子称为基态原子。 ②激发态:较高能量状态(相对基态而言)。基态原子的电子吸收能量后,电子跃迁至较高能级时的状态。处于激发态的原子称为激发态原子。 ③原子光谱:不同元素的原子发生电子跃迁时会吸收(基态→激发态)和放出(激发态→较低激发态或基态)不同的能量(主要是光能),产生不同的光谱——原子光谱(吸收光谱和发射光谱)。利用光谱分析可以发现新元素或利用特征谱线鉴定元素。 3、电子云与原子轨道 (1)电子云:电子在核外空间做高速运动,没有确定的轨道。因此,人们用“电子云”模型来描述核外电子的运动。“电子云”描述了电子在原子核外出现的概率密度分布,是核外电子运动状态的形象化描述。 (2)原子轨道:不同能级上的电子出现概率约为90%的电子云空间轮廓图称为原子轨道。s电子的原子轨道呈球形对称,ns能级各有1个原子轨道;p电子的原子轨道呈纺锤形,n p能级各有3个原子轨道,相互垂直(用p x、p y、p z表示);n d能级各有5个原子轨道;n f能级各有7个原子轨道。 4、核外电子排布规律 (1)能量最低原理:在基态原子里,电子优先排布在能量最低的能级里,然后排布在能量逐渐升高的能级里。 (2)泡利原理:1个原子轨道里最多只能容纳2个电子,且自旋方向相反。 (3)洪特规则:电子排布在同一能级的各个轨道时,优先占据不同的轨道,且自旋方向相同。 (4)洪特规则的特例:电子排布在p、d、f等能级时,当其处于全空、半充满或全充满时,即p0、d0、f0、p3、d5、f7、p6、d10、f14,整个原子的能量最低,最稳定。 能量最低原理表述的是“整个原子处于能量最低状态”,而不是说电子填充到能量最低的轨道中去,泡利原理和洪特规则都使“整个原子处于能量最低状态”。 电子数 (5)(n-1)d能级上电子数等于10时,副族元素的族序数=n s能级电子数 (二)元素周期表和元素周期律 1、元素周期表的结构 元素在周期表中的位置由原子结构决定:原子核外的能层数决定元素所在的周期,原子的价电子总数决定元素所在的族。 (1)原子的电子层构型和周期的划分 周期是指能层(电子层)相同,按照最高能级组电子数依次增多的顺序排列的一行元素。即元素周期表中的一个横行为一个周期,周期表共有七个周期。同周期元素从左到右(除稀有气体外),元素的金属性逐渐减弱,非金属性逐渐增强。 (2)原子的电子构型和族的划分 族是指价电子数相同(外围电子排布相同),按照电子层数依次增加的顺序排列的一列元素。即元素周期表中的一个列为一个族(第Ⅷ族除外)。共有十八个列,十六个族。同主族周期元素从上到下,元素的金属性逐渐增强,非金属性逐渐减弱。 (3)原子的电子构型和元素的分区 按电子排布可把周期表里的元素划分成5个区,分别为s区、p区、d区、f区和ds区,除ds区外,区的名称来自按构造原理最后填入电子的能级的符号。 2、元素周期律
高中化学学业水平考试必背知识点
20XX 年高中毕业会考 高中化学学业水平测试必修1、2必背考试点 1、化合价(常见元素的化合价): Na 、K 、Ag 、H :+1 F :—1 Ca 、Mg 、Ba 、Zn :+2 Cl :—1,+1,+5,+7 Cu :+1,+2 O :—2 Fe :+2,+3 S :—2,+4,+6 Al :+3 Mn :+2,+4,+7 N :—3,+2,+4,+5 2、氧化还原反应 定义:有电子转移(或者化合价升降)的反应 本质:电子转移(包括电子的得失和偏移) 特征:化合价的升降 氧化剂(具有氧化性)——得电子——化合价下降——被还原——还原产物 还原剂(具有还原性)——失电子——化合价上升——被氧化——氧化产物 口诀:得——降——(被)还原——氧化剂 失——升——(被)氧化——还原剂 四种基本反应类型和氧化还原反应关系: 3、金属活动性顺序表 K Ca Na Mg Al Zn Fe Sn Pb (H) Cu Hg Ag Pt Au 还 原 性 逐 渐 减 弱 4、离子反应 定义:有离子参加的反应 电解质:在水溶液中或熔融状态下能导电的化合物 非电解质:在水溶液中和熔融状态下都不能导电的化合物 离子方程式的书写步骤: 第一步:写。写出化学方程式 第二步:拆。易溶于水、易电离的物质拆成离子形式;难溶(如CaCO 3、BaCO 3、BaSO 4、AgCl 、AgBr 、 AgI 、Mg(OH)2、Al(OH)3、Fe(OH)2、Fe(OH)3、Cu(OH)2等),难电离(H 2CO 3、H 2S 、CH 3COOH 、HClO 、H 2SO 3、NH 3·H 2O 、H 2O 等),气体(CO 2、SO 2、NH 3、Cl 2、O 2、H 2等),氧化物(Na 2O 、MgO 、Al 2O 3等)不拆 第三步:删。删去方程式两边都有的离子 第四步:查。检查前后原子守恒,电荷是否守恒。 离子共存问题判断: ①是否产生沉淀(如:Ba 2+和SO 42-,Fe 2+和OH -); ②是否生成弱电解质(如:NH 4+和OH -,H +和CH 3COO -)
(完整)高中化学_全知识点总结记忆,推荐文档
高一化学各章必记知识点 第一章化学实验基本方法 一.化学实验基本方法 1、易燃易爆试剂应单独保存,防置在远离电源和火源的地方。 2、酒精小面积着火,应迅速用湿抹布扑盖;烫伤用药棉浸75%-95%的酒精轻涂伤处;眼睛的化学灼伤应立即用大量水清洗,边洗边眨眼睛。浓硫酸沾在皮肤上,立即用大量水清洗,最后涂上3%-5%的NaHCO3溶液。碱沾皮肤,用大量水清洗,涂上5%的硼酸溶液。 3、产生有毒气体的实验应在通风橱中进行。 4、防暴沸的方法是在液体中加入碎瓷片或沸石。 5、过滤是把难溶固体和水分离的方法;蒸发是把易挥发液体分离出来,一般都是为了浓缩结晶溶质。 6、粗盐含杂质主要有泥沙,CaCl2、MgCl2、Na2SO4等,需用的分离提纯方法是“钡碳先,碱随便,接过滤,后盐酸”的方法。 7、溶液中SO42-检验法是先加盐酸酸化,后加BaCl2溶液,如有白色沉淀产生,证明含有SO42-。 8、Cl-检验法是用AgNO3溶液和稀HNO3溶液,如有白色沉淀生成,则证明含Cl-;酸化的目的是防止碳酸银等沉淀的生成。 9、蒸馏是分离液液互溶物的方法,常见主要仪器是蒸馏烧瓶和冷凝器。温度计的水银球应放在蒸馏烧瓶的支管口附近,冷凝水流方向要注意逆流。 10、萃取是用某种物质在互不相溶的溶剂中溶解度的不同,从溶解度小的溶剂中转移到溶解度大的溶剂中的过程。一般萃取后都要分液,需用在分液漏斗中进行,后者操作时下层液体从下口放出,上层液体从上口倒出。 11、常见的有机萃取剂是CCl4和苯,和水混合后分层,分别在下层和上层。 12、Fe2+(浅绿色)、Fe3+(黄色)、Cu2+(蓝色)、MnO4-(紫或紫红色)、[Fe(SCN)]2+(血红色或红色);淀粉溶液+I2→显蓝色 溴、碘的单质在几种溶剂中的颜色: 单质水苯汽油、四氯化碳 溴橙黄→橙红橙红橙红 碘棕黄紫红紫红 13、仪器的洗涤 ⑴标准:仪器内壁水膜均匀附着,既不聚成水滴,也不成股流下,表示仪器已洗干净。 ⑵若附着不易用水洗净的物质时,应选不同的“洗涤剂”区别对待。如: 残 留 物洗 涤 剂 盐酸 久置石灰水的瓶壁上的白色固体 (CaCO3) 铁 锈盐酸 制氯气时残留的二氧化锰浓盐酸(温热) 久置FeCl3溶液的瓶壁上的沉淀(Fe2O3)盐酸 容器壁上附着的碘酒精或NaOH溶液 容器壁上附着的硫二硫化碳或热NaOH溶液 试管壁上的银镜稀硝酸 二、化学计量在实验中的应用 1、注意“同种微粒公式算”的途径
管理沟通知识点总结
第一部分管理沟通原理 1 沟通与管理沟通 沟通是人们分享信息,思想和情感的任何过程. *沟通在管理中的作用:激励,创新,交流,联系. *管理沟通是围绕企业经营而进行的信息,知识与情报的分享过程. *沟通过程由各种要素组成:发送―接受者,信息,渠道,噪音,反馈和环境. 发送―接收者:在大多数沟通中,人们是发送―接收者,即在同一时间即发送又接受. 信息是由一个发送―接收者要分享的思想和情感组成的. 渠道是信息经过的路径 反馈是发送―接收者相互间的反应. 噪音是阻止理解和准确解释信息的障碍.它分成种形式:外部噪音,内部噪音和语义噪音. 环境是沟通发生的地方.环境能对沟通产生重大影响 *外部噪音来自于环境,它阻碍听到或理解信息,如天气热,吵闹. *内部噪音发生在发送―接受者的头脑中,这时他们的思想和情感集中于在沟通以外的事情上. 2沟通是一种相互作用 沟通的相互作用不仅包括身体方面,也包括心理方面:印象是在沟通参与者的头脑中形成的,人们对另一个人的所思所想直接影响到他们的沟通. 沟通作为一种相互作用,包含三个重要的原理: 1)进行沟通的人连续的,同步的发出信息.即不管你在沟通中是否说话,你都积极地参与到信息的发送和接收中. 2)沟通事件由过去,现在和将来.即我们都依据自己的经验,情绪和期望对各种情形做出反应,这些要素使沟通情景复杂化. 3)沟通的参与者扮演相应的角色.即在沟通中我们扮演不同的的角色,无论这个角色是否由个人关系或社会所确立,不同的人会按不同的方式理解,这些不同的理解影响它们所导致的沟通. 3 管理沟通的种类 自身内沟通人际沟通小组中的沟通公共场合沟通跨文化沟通 *自身内沟通是发生在自身内部的沟通,它包括思想,情感和我们看待自己的方式. *跨文化沟通是两个或两个以上来自不同文化背景的人在任何时候相互作用而产生的沟通. 4 组织内部信息沟通网络 正式与非正式的沟通网络,非言语沟通 *正式沟通网络有链式,轮式,环式,全渠道式,Y式. *非正式沟通网络有单串型,饶舌型,机率型,集聚型. *非正式沟通是不受管理层控制的. 5 影响管理沟通的基本因素 1) 外在因素:组织结构;沟通环境.
化学中考易错易考知识点复习
化学中考易错易考知识 点复习 Company number:【WTUT-WT88Y-W8BBGB-BWYTT-19998】
2012中考化学易错易考知识点集锦 一、常见物质的俗称、名称、化学式 干冰二氧化碳CO2沼气天然气甲烷CH4 盐酸氢氯酸HCl大理石石灰石碳酸钙CaCO3 纯碱苏打碳酸钠Na2CO3小苏打碳酸氢钠NaHCO3 食盐氯化钠NaCl生石灰氧化钙CaO 澄清石灰水氢氧化钙溶液Ca(OH)2熟石灰消石灰氢氧化钙Ca(OH)2 火碱烧碱苛性钠氢氧化钠NaOH水银汞Hg 二、酸、碱、盐易漏化学性质 1、二氧化碳、二氧化硫、三氧化硫和可溶性碱反应。------为什么可溶性碱易变质的原因 2、二氧化碳、二氧化硫、二氧化硫和水反应生成酸。------烧煤为什么造成降酸雨的原因 3、干冰不是冰,纯碱不是碱(是盐,但微弱的碱性-------否定只有碱液才显碱性) 4、溶液导电的原因是溶液中存在自由移动的离子(酸碱盐的水溶液能导电------判断方法) 三、推断题中的一些特别知识(方法:找出特别的地方,看其左右的内容) 1、黑色固体有:氧化铜、炭粉、铁粉、二氧化锰、四氧化三铁 2、浅黄色粉末是:硫,红色(或紫红色)固体是金属铜 3、暗紫色固体是高锰酸钾,红色固体是红磷或氧化铁 4、能使澄清石水变浑浊的气体是二氧化碳 5、能使带火星木条复燃的气体是氧气 6、既有可燃性,又有还原性的物质有:氢气、一氧化碳、木炭 7、相对分子质量最小的氧化物是水 8、红褐色沉淀肯定是:Fe(OH)39、蓝色沉淀可能是Cu(OH)2或CuCO3 10、既不溶于水,也不溶于硝酸的白色沉淀有AgCl或BaSO4 11、白色沉淀可溶于酸,但有气泡放出的可能是不溶性碳酸盐(___CO3) 白色沉淀可溶于酸,但没有气泡放出的可能是不溶性碱(___OH) 12、固体和酸混合有气泡放出的物质可能是:碳酸盐+酸或活泼金属+酸 13、产物有三种的化学变化有两种:①高锰酸钾加热分解②碳酸盐和酸反应 14、燃烧同时有两种产物生成的物质是甲烷燃烧。 15、碱和盐中,除三价铁(黄色)、二价铁(浅绿色)、二价铜(蓝色)外, 其余物质:固体是白色,溶液是无色, 16、金属氧化物的性质主要有:①金属氧化物和酸反应;②还原剂和金属氧化物反应。 四、一些重要实验的注意事项 1、空气中氧气的测定: ①选用试剂燃烧后的产物必须是固态,能在空气中燃烧-------故选用红磷②最后所测结果偏小的原因有四:ⅰ、红磷不足,部分氧气没反应;ⅱ、装置气密性不好;ⅲ、最后所剩的气体没有完全冷却至室温 2、氧气的实验室制法 ①导气管伸入试管少许;②应根据酒精灯火焰来调节试管的高度;③试管口应略向下倾斜;④高锰酸钾制氧时,应在试管口放一小团棉花;⑤氯酸钾制氧气时,不能混有可燃物,否则会发生爆炸;⑥排水集气法时,应待气泡均匀冐出时才收集;⑦向上排空气法收集时,导气管应伸到集气瓶的底部;⑧排水法收集氧气结束时,最后先把导气管从水槽移出,后熄灭酒精灯。 3、二氧化碳的实验室制取 ①所选试剂是大理石和稀盐酸,不能说是碳酸钙和稀盐酸,酸不选用稀硫酸和浓盐酸-----想想为什么②长颈漏斗的使用:下端口应伸到液面以下③不能选用排水法来收集二氧化碳④简易装置的优点是:装置简单;节约药品;操作简便⑤带长颈漏斗的装置的优点是:随时增添液体 4、一氧化碳还原氧化铁实验 ①实验前,一氧化碳和要先检验纯度:可(可燃性气体)+助(助燃性气体)点燃可能会发生爆炸②加热前都要选通一会儿一氧化碳------赶出试管内的空气③实验结束时,先停止加热,断续通入一氧化碳至冷却-----为什么④尾气处理装置----为什么一氧化碳有毒,要防止污染环境,防止中毒,处理方法----燃烧或收集 5、电解水实验:①通入直流电②生成物的体积比为氢气:氧气==2:1③生成物的质量比为氢气:氧气==1:8④电解水实验说明水是由氢,氧两种元素组成的 6、白磷的保存:浸在水中-----为什么着火点低(40℃),易在空气中被氧化 7、称量氢氧化钠的质量:放到小烧杯中再称量-----为什么有强烈的腐蚀性,易潮解 8、浓硫酸的稀:把浓硫酸注入水中,要不断地搅拌 五、几个重要的活动探究: 1、质量守恒定律的探究:镁条燃烧时质量比原来估计的值低的原因有:①有部分产物变成白烟流失到空气中②有部分物质粘在坩埚钳上 2、粗盐的提纯:步骤:①溶解②过滤③蒸发注意事项:⑴过滤的注意事项“一贴二低三靠”一贴:(滤纸紧贴漏斗内壁)二低:(滤纸边缘低于漏斗口边缘,液面低于滤纸边缘)三靠:烧杯口紧靠玻璃棒
高中生物选修3知识点总结
选修3知识点复习 专题1 基因工程 (一)基因工程又叫基因拼接技术或DNA重组技术。原理是基因重组,操作水平是分子水平。优点:打破物种界限;定向地改造生物的遗传性状。 (二)基因工程的基本工具1.“分子手术刀”——限制性核酸内切酶(限制酶) (1)来源:主要从原核生物中分离纯化出来。 (2)功能:使每一条链中特定部位的两个核苷酸之间的磷酸二酯键断开(3)特点具有专一(特异)性。 (4)结果:经限制酶切割产生的DNA片段末端通常有两种形式:黏性末端和平末端。 2.“分子缝合针”——DNA连接酶 (1)两种DNA连接酶(E·coliDNA连接酶和T4-DNA连接酶)的比较: ①相同点:都缝合磷酸二酯键。②区别:E·coliDNA连接酶只能连接黏性末端;而T4DNA连接酶能缝合两种末端,但连接平末端的之间的效率较低。 (2)与DNA聚合酶作用的异同:DNA聚合酶只能将单个脱氧核苷酸加到已有的脱氧核苷酸片段的末端,形成磷酸二酯键。DNA连接酶是连接两个DNA片段的末端,形成磷酸二酯键。 3.“分子运输车”——载体(1)载体具备的条件:①能够稳定保存并复制;②有一至多个限制酶酶切位点③含有标记基因,便于筛选。④对受体细胞无害。 (2)最常用的载体是质粒,化学本质是DNA分子。(3)其它载体:λ噬菌体的衍生物、动植物病毒 (三)基因工程的基本操作程序第一步:目的基因的获取 1.目的基因主要是指编码蛋白质的结构基因。 3.人工合成目的基因的两个条件:基因比较小;核苷酸序列已知。 4.PCR技术扩增目的基因 (1)PCR是多聚酶链式反应的缩写,原理DNA双链复制。 (2)过程:第一步变性:加热至90~95℃,DNA解链,不需要解旋酶;第二步复性:冷却到55~60℃,引物结合到互补DNA链。变性和复性利用了DNA的热变性原理;第三步延伸:加热至70~75℃,热稳定DNA聚合酶从引物起始互补链的合成。 第二步:基因表达载体的构建基因表达载体的组成:除了目的基因外,还必须有启动子、终止子、标记基因等。启动子是RNA聚合酶识别和结合的部位。标记基因的作用:是为了鉴定受体细胞中是否含有目的基因,从而将含有目的基因的细胞筛选出来。常用的标记基因是抗生素基因。 第三步:将目的基因导入受体细胞常用的导入方法:将目的基因导入植物细胞:采用最多的方法是农杆菌转化法,其次还有基因枪法和花粉管通道法等。将目的基因导入动物细胞:最常用的方法是显微注射法。此方法的受体细胞多是受精卵。将目的基因导入微生物细胞:原核生物作为受体细胞的原因是繁殖快、多为单细胞、遗传物质相对较少,最常用的原核细胞是大肠杆菌,其转化方法是:先用Ca2+处理细胞,使其成为感受态细胞,再将重组表达载体DNA分子溶于缓冲液中与感受态细胞混合,在一定的温度下促进感受态细胞吸收DNA分子,完成转化过程。 第四步:目的基因的检测和鉴定 1.首先要检测转基因生物的染色体DNA上是否插入了目的基因,方法是采用DNA分子杂交技术。 2.其次还要检测目的基因是否转录出了mRNA,方法是分子杂交技术。 3.最后检测目的基因是否翻译成蛋白质,方法是从转基因生物中提取蛋白质,用相应的抗体进行抗原-抗体杂交。 4.有时还需进行个体生物学水平的鉴定。如:转基因抗虫植物是否出现抗虫性状。 (四)基因工程的应用 1.植物基因工程:抗虫、抗病、抗逆转基因植物,利用转基因改良植物的品质。 2.动物基因工程:提高动物生长速度;改善畜产品品质;用转基因动物生产药物:如乳腺生物反应器和膀胱生物反应器,方法是将目的基因导入哺乳动物的受精卵中,使其发育成转基因动物。 3.基因治疗是把正常基因导入病人的体内,使该基因的表达产物发挥功能,从而达到治疗的目的,这是治疗遗传病最有效的手段。 (五)蛋白质工程的概念:基因工程在原则上只能生产自然界已存在的蛋白质,蛋白质工程师在基因工程的基础上,延伸出来的第二代基因工程。基本途径是:从预期的蛋白质功能出发→设计预期的蛋白质结构→推测应有的氨基酸序列→找到相对应的脱氧核苷酸序列。 专题2 细胞工程 (一)植物细胞工程 1.植物组织培养技术(1)原理:植物细胞的全能性 (2)过程:离体的植物器官、组织或细胞脱分化愈伤组织再分化植物体
管理基础知识重点归纳
管理基础知识重点归纳(全) 一、管理 ■含义:1.管理是由管理者引导的活动 2.管理是在一定的环境条件下进行的 3.管理是为了实现组织目标 4.管理需要有效地动员和配置资源 5.管理具有基本职能 6.管理是一种社会实践活动 ■管理的特性:1.管理的二重性(自然属性和社会属性)首先是指管理的生产力属性和生产关系属性。管理工作既有科学性又有艺术性。 2.管理具有目标性。 3.管理具有组织性。 4.管理具有创新性。 ■管理的基本职能:计划 组织(组织设计、人员配备、组织运行) 领导 控制 ■管理的类型:按公共领域和非公共领域划分,现代管理分为公共管理和企业管理。 ■管理者的层次分为高层管理者、中层管理者、基础管理者。同时整个组织还包括一层作业人员。 ■按管理人员的领域分为综合管理人员和专业管理人员。 ■管理者的角色:人际角色(代表人角色、领导者角色、联络者角色)、信息角色(信息监视者、信息传播者、发言人)、决策角色(企业家、故障处理者、资源配置者、谈判者)。 ■管理者应具备的技能:技术技能;人际技能;概念技能。 ■管理环境之组织环境的分类:外部环境(一般环境和特殊环境);内部环境(人力资源、财力资源、物力资源和信息资源和各项管理手段完善与协调的程度) ■外部环境:一般环境(政治、经济、社会文化、技术、自然环境) 特殊环境(产品的用户、竞争对手、供应商、政府机构、社会团体)
■两种程度四种环境状况,美国的邓肯的静态(稳定)—动态(不稳定),简单—复杂得来。 ■SWOT(内外部环境综合分析):S优势、W劣势、O机会、T威胁。 二、决策 ■决策的本质:1.决策应有明确合理的目标; 2.决策必须有两个或两个以上的备选方案,但只能采取其中一个; 3.必须知道采用每种方案后可能出现的各种后果; 4.最后选取得方案,只能是“令人满意”或“足够好的”,而不可能是最优的。 5.决策的实质是为了谋求企业外部环境、内部条件和经营目标之间的动态平衡而作出的努力。 ■决策的特征:前瞻性;目标性;选择性;可行性;过程性;科学性;风险性。 ■决策的作用:决策时决定组织管理工作成败的关键; 决策时实施各项管理职能的保证。 ■决策的类型:1.按决策的重要程度,可分为战略决策、战术决策和业务决策。 2.按决策的重复程度,可分为程序化决策和非程序化决策。 3.按决策的信息可靠程度,可分为确定型、风险型和不确定型决策。 4.按照参与决策主体不同,可分为个人决策和群体决策。 ■决策的原则:满意原则;系统原则;信息原则;预测原则;比较优选原则;反馈原则;效益原则。 ■决策的制定过程:1.确定决策问题;2.确定目标;3.拟定备选方案;4.分析备选方案;5.选择最优方案。 ■决策的主要方法:1.定性决策方法:头脑风暴法;德尔菲法;哥顿法;名义群体法;电子会议法。 2.定量决策方法:确定型决策方法(盈亏平衡点法) 风险型决策法(“决策树”法) 不确定决策方法:冒险法(大中取大,乐观法则);保 守法(小中取大、悲观法则);折中法。 ■预测的程序:确定预测目标;收集和分析有关资料;选择预测方法;评价预测结果;编写预测报告。■预测方法:定性预测法(专家调查法;德尔菲法) 定量预测法(时间序列法;因果预测法) ■决策心理:1.光环效应(又称晕轮效应) 2.首因效应(“第一感”)
中考化学易错易考知识点总结
中考化学易错易考知识点总结 一、常见物质的俗称、名称、化学式 干冰二氧化碳CO2沼气天然气甲烷CH4 盐酸氢氯酸HCl 大理石石灰石碳酸钙CaCO3 纯碱苏打碳酸钠Na2CO3小苏打碳酸氢钠NaHCO3 食盐氯化钠NaCl 生石灰氧化钙CaO 澄清石灰水氢氧化钙溶液Ca(OH)2熟石灰消石灰氢氧化钙Ca(OH)2 火碱烧碱苛性钠氢氧化钠NaOH 水银汞Hg 二、酸、碱、盐易漏化学性质 1、二氧化碳、二氧化硫、三氧化硫和可溶性碱反应。------为什么可溶性碱易变质的原因 2、二氧化碳、二氧化硫、二氧化硫和水反应生成酸。------烧煤为什么造成降酸雨的原因 3、干冰不是冰,纯碱不是碱(是盐,但微弱的碱性-------否定只有碱液才显碱性) 4、溶液导电的原因是溶液中存在自由移动的离子(酸碱盐的水溶液能导电------判断方法) 三、推断题中的一些特别知识(方法:找出特别的地方,看其左右的内容) 1、黑色固体有:氧化铜、炭粉、铁粉、二氧化锰、四氧化三铁 2、浅黄色粉末是:硫,红色(或紫红色)固体是金属铜 3、暗紫色固体是高锰酸钾,红色固体是红磷或氧化铁 4、能使澄清石水变浑浊的气体是二氧化碳 5、能使带火星木条复燃的气体是氧气 6、既有可燃性,又有还原性的物质有:氢气、一氧化碳、木炭 7、相对分子质量最小的氧化物是水 8、红褐色沉淀肯定是:Fe(OH)39、蓝色沉淀可能是Cu(OH)2或CuCO3 10、既不溶于水,也不溶于硝酸的白色沉淀有AgCl或BaSO4 11、白色沉淀可溶于酸,但有气泡放出的可能是不溶性碳酸盐(___CO3) 白色沉淀可溶于酸,但没有气泡放出的可能是不溶性碱(___OH) 12、固体和酸混合有气泡放出的物质可能是:碳酸盐+酸或活泼金属+酸 13、产物有三种的化学变化有两种:①高锰酸钾加热分解②碳酸盐和酸反应 14、燃烧同时有两种产物生成的物质是甲烷燃烧。 15、碱和盐中,除三价铁(黄色)、二价铁(浅绿色)、二价铜(蓝色)外, 其余物质:固体是白色,溶液是无色, 16、金属氧化物的性质主要有:①金属氧化物和酸反应;②还原剂和金属氧化物反应。 四、一些重要实验的注意事项 1、空气中氧气的测定: ①选用试剂燃烧后的产物必须是固态,能在空气中燃烧-------故选用红磷②最后所测结果偏小的原因有四:ⅰ、红磷不足,部分氧气没反应;ⅱ、装置气密性不好;ⅲ、最后所剩的气体没有完全冷却至室温 2、氧气的实验室制法 ①导气管伸入试管少许;②应根据酒精灯火焰来调节试管的高度;③试管口应略向下倾斜;④高锰酸钾制氧时,应在试管口放一小团棉花; ⑤氯酸钾制氧气时,不能混有可燃物,否则会发生爆炸;⑥排水集气法时,应待气泡均匀冐出时才收集;⑦向上排空气法收集时,导气管应伸到集气瓶的底部;⑧排水法收集氧气结束时,最后先把导气管从水槽移出,后熄灭酒精灯。 3、二氧化碳的实验室制取 ①所选试剂是大理石和稀盐酸,不能说是碳酸钙和稀盐酸,酸不选用稀硫酸和浓盐酸-----想想为什么②长颈漏斗的使用:下端口应伸到液面以下③不能选用排水法来收集二氧化碳④简易装置的优点是:装置简单;节约药品;操作简便⑤带长颈漏斗的装置的优点是:随时增添液体 4、一氧化碳还原氧化铁实验 ①实验前,一氧化碳和要先检验纯度:可(可燃性气体)+助(助燃性气体)点燃可能会发生爆炸②加热前都要选通一会儿一氧化碳------赶出试管内的空气③实验结束时,先停止加热,断续通入一氧化碳至冷却-----为什么?④尾气处理装置----为什么?一氧化碳有毒,要防止污染环境,防止中毒,处理方法----燃烧或收集 5、电解水实验:①通入直流电②生成物的体积比为氢气:氧气==2:1 ③生成物的质量比为氢气:氧气==1:8 ④电解水实验说明水是由氢,氧两种元素组成的 6、白磷的保存:浸在水中-----为什么?着火点低(40℃),易在空气中被氧化 7、称量氢氧化钠的质量:放到小烧杯中再称量-----为什么?有强烈的腐蚀性,易潮解 8、浓硫酸的稀:把浓硫酸注入水中,要不断地搅拌 五、几个重要的活动探究: 1、质量守恒定律的探究:镁条燃烧时质量比原来估计的值低的原因有:①有部分产物变成白烟流失到空气中②有部分物质粘在坩埚钳上 2、粗盐的提纯:步骤:①溶解②过滤③蒸发注意事项:⑴过滤的注意事项“一贴二低三靠”一贴:(滤纸紧贴漏斗内壁)二低:(滤纸边缘低于漏斗口边缘,液面低于滤纸边缘)三靠:烧杯口紧靠玻璃棒上端;玻璃棒下端紧靠三层滤纸部分;漏斗下端口紧靠烧杯内壁)⑵蒸发的注意事项:蒸到出现较多固体析出时就要停止加热⑶三步中都要用到玻璃棒但作用不同:溶解时搅拌加快溶解;过滤时引流液体;蒸发时使受热均匀 六、物质的除杂 1、CO2(CO):把气体通过灼热的氧化铜 2、CO(CO2):通过足量的氢氧化钠溶液
