正极材料LiNi_0_5_Mn_1_5_O_4的合成及性能

收稿日期:2006-11-27。收修改稿日期:2007-01-09。中南大学博士后基金资助项目。
*
通讯联系人。E-mail:zxwang@mail.csu.edu.cn第一作者:季
勇,男,25岁,硕士研究生;研究方向:化学电源与新能源材料。
正极材料LiNi 0.5Mn 1.5O 4的合成及性能
季
勇
王志兴*
尹周澜
郭华军
彭文杰
李新海
(中南大学冶金科学与工程学院,长沙
410083)
摘要:采用低温固相法制备镍锰复合草酸盐,煅烧后生成的镍锰复合氧化物与Li2CO3混合,在空气中于700℃反应12h,得到LiNi0.5Mn1.5O4。通过XRD,SEM和恒电流充放电测试对样品进行了表征。XRD结果表明:复合草酸盐经390℃煅烧3h,生成了多相氧化物;合成的LiNi0.5Mn1.5O4为纯相,具有立方尖晶石结构。电化学测试结果表明,合成的样品在室温和高温(55℃)下,具有较好的电化学性能;大电流充放电时,具有良好的循环性能。关键词:锂离子电池;正极材料;LiNi0.5Mn1.5O4;倍率性能中图分类号:O614.111;O614.81+3;O614.7;TM912.9
文献标识码:A
文章编号:1001-4861(2007)04-0597-05
SynthesisandPropertyofCathodeMaterialLiNi0.5Mn1.5O4
JIYongWANGZhi-Xing*
YINZhou-Lan
GUOHua-Jun
PENGWen-Jie
LIXin-Hai
(SchoolofMetallurgicalScienceandEngineering,CentralSouthUniversity,Changsha410083)
Abstract:Compositeoxideofnickelandmanganesewaspreparedbycalcinationofcompositeoxalatesynthesised
bysolid-statereactionatlowtemperature.LiNi0.5Mn1.5O4wasthensynthesisedbyfiringthemixtureoftheas-preparedcompositeoxideandLi2CO3at700℃for12hoursinair.ThesamplewascharacterizedbyXRD,SEMandcharge-dischargetests.XRDpatternshowedthatthecompositenickelandmanganeseoxidepreparedat390℃for3hourswascomposedofseveralphases.ThesynthesizedLiNi0.5Mn1.5O4hadthepurespinelstructure.TheelectrochemicaltestshowedthatLiNi0.5Mn1.5O4deliveredgoodelectrochemicalperformancebothatroomtemperatureandhightemperature(55℃),anditshowedgoodcycleperformanceunderhighcurrentdensity.
Keywords:lithiumionbatteries;cathodematerial;LiNi0.5Mn1.5O4;ratecapability
尖晶石型LiMn2O4作为一种极具发展前途的锂离子电池正极材料得到了广泛的研究。但由于尖晶石型LiMn2O4正极材料充放电过程中伴随着Li+离子脱出嵌入发生的Jahn-Teller效应而导致的电极容量下降、容量衰减大、循环寿命短等缺点阻碍了其商品化应用。为了提高尖晶石型LiMn2O4正极材料的循环性能,人们在研究中发现,利用某些元素(如:
Co,Ni,Cr,Cu,Fe)对Mn元素进行部分取代会使尖
晶石相电极4V区的容量向更高的电位区移动,形
成一系列更高电位平台的尖晶石相的电极材料,如:
4.7V平台的LiNi0.5Mn1.5O4,4.8V平台的LiCrxMn2-xO4
(x=0.5,1),4.9V平台的Li2FeMn2O8以及5V平台的LiCoxMn2-xO4(x=0.5,1)和LiCuxMn2-xO4等[1 ̄3]。其中LiNi0.5Mn1.5O4具有较高的充放电容量,而且对电解液
的分解作用低,因而可作为一种新型高性能锂离子电池的电极材料。
目前合成LiNi0.5Mn1.5O4的方法较多,多采用液
相法,也有部分采用固相法直接合成的。
固相法[4,6]简单易行,但研究表明当反应温度达到700℃以上时,
会出现一个对应于Mn3+/Mn4+氧化还原的4.1V平台,这和在高温条件下反应会导致氧的缺失有关。液相法主要包括:溶胶-凝胶法[5,6]、共沉淀法[7]、复合碳
第4期2007年4月
Vol.23No.4Apr.,2007
无机化学学报
CHINESEJOURNALOFINORGANICCHEMISTRY
第23卷无机化学学报
酸盐法[8]等。本研究采用一种新的合成方法,即通过低温固相反应制备草酸盐前躯体,将前驱体在390
℃煅烧3h,得到颗粒细小的镍锰的复合氧化物。该氧化物再与Li
2
CO3混合,于700℃反应得到产物LiNi0.5Mn1.5O4。
1实验部分
按照一定物质的量比称取NiCl
2
?6H2O(分析纯)、MnCl2?4H2O(分析纯)和(NH4)2C2O4?H2O(分析纯)3种物质。其中,金属元素镍、锰的物质的量比为1∶3,草酸铵与总的金属元素的物质的量比为1.2∶1。草酸铵适当过量,以使低温固相反应更加充分。过量的草酸铵在前驱体煅烧时将分解除去。将各反应物放入研钵研磨,进行低温固相反应。研磨刚开始,反应即迅速进行,约2 ̄5min可完成。反应过程中,结晶水的释放使体系变得粘稠,随着研磨的继续进行,约0.5h后体系逐渐变得干燥。最终得到浅蓝色复合草酸盐粉末。经120℃干燥6h,再于空气中390℃煅烧3h,得到镍锰复合氧化物。采用ICP、EDS等检测方法分析了复合氧化物中镍锰元素的含量和区域分布情况。最后,将镍、锰元素与碳酸锂按照物质的量比为1∶3∶1.05混合(锂过量5%,以补偿在高温煅烧时,锂的挥发损失),在空气中,700℃煅烧12h,得到产
物LiNi
0.5
Mn1.5O4。
用XRD(Rint-2000,Rigaku)和SEM(JEOL,JSM-5600LV)分别表征样品的晶体结构和表面形貌。按照
质量比为8∶1∶1称量LiNi
0.5
Mn1.5O4与导电碳黑、PVDF,在溶剂NMP中混合成均匀浆料,均匀涂布于铝箔上。在80℃的真空箱中干燥制成正极片。在充满氩气的手套箱中装配成CR-2025型扣式电池:以锂片为负极,Cellgard2400聚丙烯多孔膜为隔膜,溶解于EC/EMC/DMC(体积比1∶1∶1)的1mol?L-1LiPF6为电解液。充放电为恒电流方式,电压限制在3.5 ̄4.9V范围内,在室温和高温(55℃)测试时,电流为1C倍率(150mA?g-1);在大电流充放电测试时,电流倍率分别为5C,10C。
2结果与讨论
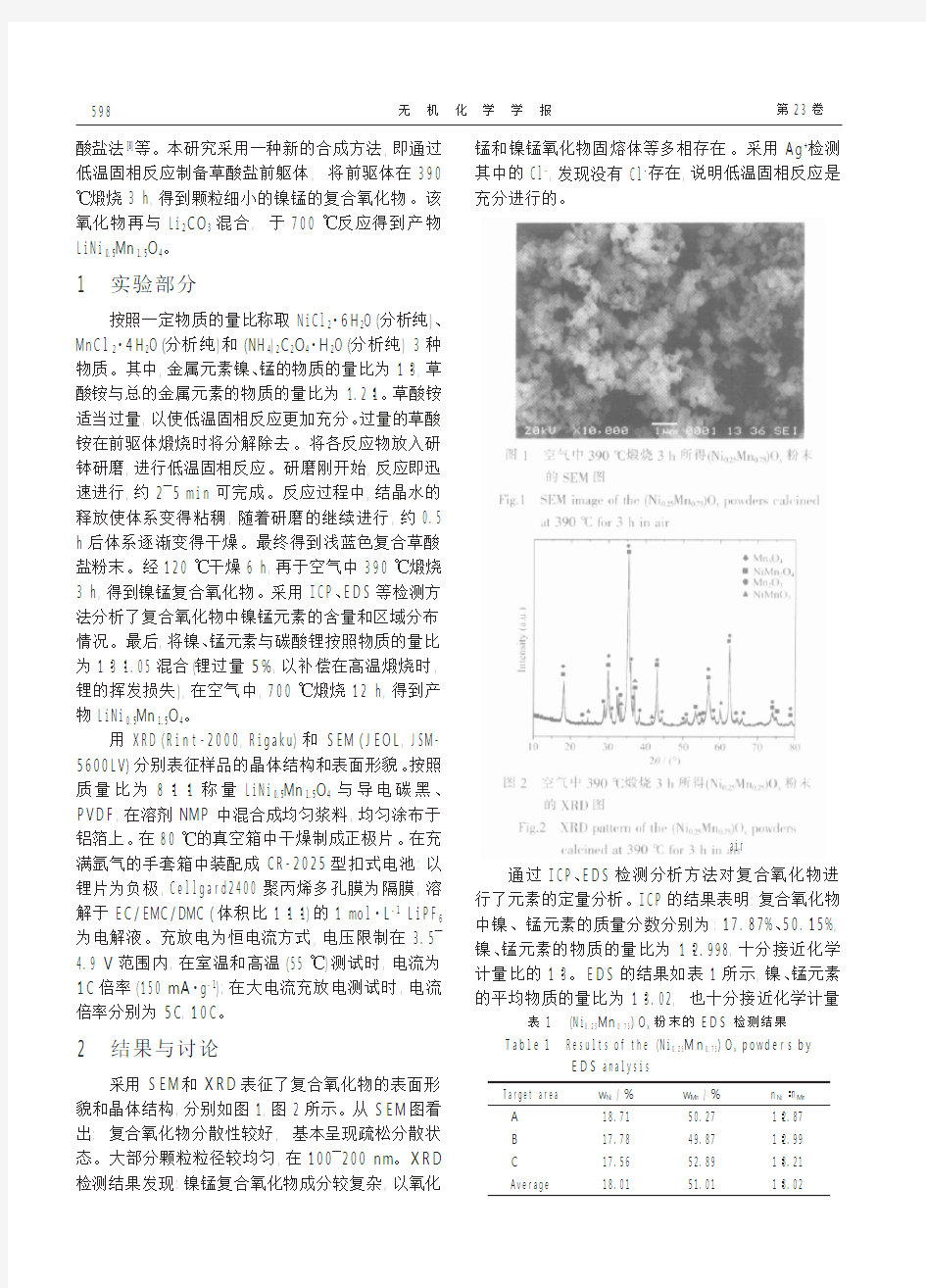
采用SEM和XRD表征了复合氧化物的表面形貌和晶体结构,分别如图1,图2所示。从SEM图看出:复合氧化物分散性较好,基本呈现疏松分散状态。大部分颗粒粒径较均匀,在100 ̄200nm。XRD检测结果发现:镍锰复合氧化物成分较复杂,以氧化锰和镍锰氧化物固熔体等多相存在。采用Ag+检测其中的Cl-,发现没有Cl-存在,说明低温固相反应是充分进行的。
通过ICP、EDS检测分析方法对复合氧化物进行了元素的定量分析。ICP的结果表明:复合氧化物中镍、锰元素的质量分数分别为:17.87%、50.15%,镍、锰元素的物质的量比为1∶2.998,十分接近化学计量比的1∶3。EDS的结果如表1所示,镍、锰元素的平均物质的量比为1∶3.02,也十分接近化学计量
TargetareawNi/%wMn/%nNi∶nMn
A18.7150.271∶2.87
B17.7849.871∶2.99
C17.5652.891∶3.21
Average18.0151.011∶3.02
图1空气中390℃煅烧3h所得(Ni
0.25
Mn0.75)Ox粉末
的SEM图
Fig.1SEMimageofthe(Ni0.25Mn0.75)Oxpowderscalcinedat390℃for3hinair
表1(Ni
0.25
Mn0.75)Ox粉末的EDS检测结果Table1Resultsofthe(Ni0.25Mn0.75)Oxpowdersby
EDSanalysis
图2空气中390℃煅烧3h所得(Ni
0.25
Mn0.75)Ox粉末
的XRD图
Fig.2XRDpatternofthe(Ni0.25Mn0.75)Oxpowders
calcinedat390℃for3hinair
598
第4期
季
勇等:正极材料LiNi0.5Mn1.5O4的合成及性能
比1∶3;镍、锰元素的区域分布基本比较均匀。由此可见,用低温固相前驱体法所制备的镍锰复合氧化物成分分布均匀,基本符合理论的化学计量比。
图3、图4分别是合成的LiNi0.5Mn1.5O4的SEM图和XRD图。由图3可以看出:样品结晶性好,晶型发育比较完善,呈现较规则的几何外形。虽然大量颗粒团聚在一起,但是颗粒粒径分布较均匀,粒径在300nm左右。
由图4可以看出,样品的XRD图与标准尖晶石型LiNi0.5Mn1.5O4完全吻合,衍射峰相当尖锐,说明合成的为纯相LiNi0.5Mn1.5O4,未含其他杂质。另外,进一步测得其晶格常数为a=0.8168nm,比较相关文献中的晶格常数可知,合成的LiNi0.5Mn1.5O4应该属于P4332空间群,Ni有序地取代了部分Mn原子(16d位分为4b位和12d位,Ni占有4b位,Mn
占有12d位),这可能是由于煅烧温度较低所引起的。
将合成的LiNi0.5Mn1.5O4在室温和高温(55℃)下进行电化学性能测试,充放电曲线和循环曲线如图5、
图6所示。由图5可见,合成的样品仅在4.7V附近有一个电压平台存在,该电压平台对应于Ni2+/Ni4+的氧化还原,4.1V附近电压平台基本消除,说明合成样品基本纯净,其XRD检测结果没有杂质峰也说明了这一点。通常由于合成温度较高时,
LiNi0.5Mn1.5O4会发生歧化反应,使得一部分Mn4+还原成Mn3+,充放电曲线上在4.1V会出现一个电压平台,对应于Mn3+/Mn4+的氧化还原。电化学测试表明:室温时,样品首次放电比容量达到129.7mA?g-1。合
图4
空气中700℃煅烧12h所得LiNi0.5Mn1.5O4粉末的XRD图
Fig.4XRDpatternoftheLiNi0.5Mn1.5O4powderscalcinedat700℃for12hinair
图3
空气中700℃煅烧12h所得LiNi0.5Mn1.5O4粉末的SEM图
Fig.3SEMimageoftheLiNi0.5Mn1.5O4powderscalcinedat700℃for12hinair
图6
空气中700℃煅烧12h的LiNi0.5Mn1.5O4在室温和高温(55℃)时150mA?g-1电流下的循环性能曲线
Fig.6CycleperformancesoftheLi/LiNi0.5Mn1.5O4(calcinedat700℃for12hinair)cellsataconstantcurrent
densityof150mA?g-1(1Crate)atroomtemperature
andhightemperature(55℃)
图5
空气中700℃煅烧12h的LiNi0.5Mn1.5O4室温时在150mA?g-1电流下的首次充放电曲线
Fig.5
Firstcharge-dischargecurvesoftheLi/LiNi0.5Mn1.5O4
(calcinedat700℃for12hinair)cellataconstant
currentdensityof150mA?g-1(1Crate)atroom
temperature
599
第23卷
无机化学学报成的样品在室温和高温(55℃)下,都拥有较好的电化学性能,循环性能较优越:经过30次循环后,仍能分别保持初始放电比容量的97%和95%以上。
另外,考察了合成的LiNi0.5Mn1.5O4在室温和高温(55℃)下每个循环周期的库仑效率,结果见表2、表3。从表中可以看出:不论是在室温还是高温(55
℃)下,每个循环周期的库仑效率都较高,说明电化
学反应的可逆性较好;而且随着循环次数增加,库仑效率略呈上升趋势,说明电池的活化越来越好。综合看来,材料的电化学循环性能优越。还可以发现:与高温下循环时的库仑效率相比较,室温下的库仑效率要略高一些。这可能与高温、高电压下电解液的分解有一定关系。
为了研究LiNi0.5Mn1.5O4在不同充放电倍率下的电化学性能,特别是大电流充放电时的电化学性能,在不同的倍率下进行充放电测试:1C,5C和10C,循环性能曲线如图7所示。测试结果表明:合成的
LiNi0.5Mn1.5O4具有良好的循环性能,大电流充放电时,循环性能也十分优越,循环100次后,仍能分别
图7
空气中700℃煅烧12h的LiNi0.5Mn1.5O4在室温时不同电流密度下的循环性能曲线
Fig.7CycleperformancesoftheLi/LiNi0.5Mn1.5O4(calcinedat700℃for12hinair)cellsatvariouscurrent
densitiesof150mA?g-1,750mA?g-1and1500mA?g-1(1C,5Cand10C)atroomtemperature
CycleEfficiency/%
CycleEfficiency/%
CycleEfficiency/%
192.21197.82198.3294.61297.92298.3395.91397.92398.2496.51498.02498.2597.01598.02598.4697.21698.12698.4797.31798.22798.3897.31898.32898.3997.51998.22998.310
97.7
20
98.3
30
98.3
表2
空气中700℃煅烧12h的LiNi0.5Mn1.5O4在室温时150mA?g-1电流下的循环效率
Table2
CycleefficienciesoftheLi/LiNi0.5Mn1.5O4(calcinedat700℃for12hinair)cellataconstantcurrent
densityof150mA?g-1(1Crate)atroomtemperature
Cycle
Efficiency/%
CycleEfficiency/%
CycleEfficiency/%
179.01195.42196.2288.71295.62296.5391.31395.82396.4492.71495.92496.6593.51596.02596.5694.21696.22696.6794.41796.22796.5894.91896.12896.79
95.11996.52996.610
95.3
20
96.3
30
96.7
表3
空气中700℃煅烧12h的LiNi0.5Mn1.5O4在高温(55℃)时150mA?g-1电流下的循环效率
Table3
CycleefficienciesoftheLi/LiNi0.5Mn1.5O4(calcinedat700℃for12hinair)cellataconstantcurrentdensityof150mA
?g-1(1Crate)athightemperature(55℃)600
第4期
保持初始放电容量的93.5%、90%和78.6%。另外可以发现:在10C倍率下进行大电流充放电时,前30个循环周期的容量衰减较快,这可能是在如此大电流下充放电时,正极材料的结构受到一定程度的破坏所引起的。但总的看来,材料的大电流充放电性能还是十分优良的。
3结论
利用低温固相反应法合成的镍锰复合氧化物,在空气中于700℃制备了锂离子电池正极材料LiNi0.5Mn1.5O4。得到的LiNi0.5Mn1.5O4为纯相,具有立方尖晶石结构。充放电测试表明,该材料仅在4.7V附近有充放电平台,在4.1V附近的电压平台基本消除。样品在室温和高温(55℃)下都具有较优越的循环性能:经过30次循环后,仍能分别保持初始放电比容量的97%和95%以上。样品在不同的充放电倍率下,循环性能都十分优越,拥有良好的大电流充放电性能:在1C,5C和10C的倍率下进行充放电测试时,循环100次后,仍能分别保持初始放电容量的93.5%、90%和78.6%。研究表明,通过细化反应物颗粒粒径,并在较低反应温度下反应制备,可以有效解决高温制备时出现的材料失氧问题,得到电化学性能优良的纯相LiNi
0.5
Mn1.5O4正极材料。
参考文献:
[1]AmineK,TukamotoH,YasudaH,etal.J.PowerSources,1997,68:604 ̄608
[2]ZhongQ,BonakdarpourA,ZhangM,etal.J.Electrochem.Soc.,1997,144(1):205 ̄213
[3]OhzukuT,TakedaS,IwanagaM.J.PowerSources,1999,81 ̄82:90 ̄94
[4]IdemotoY,NaraiH,KouraN.J.PowerSources,2003,119 ̄121:125 ̄129
[5]KimJH,MyungST,SunYK.ElectrochimActa,2004,49:219 ̄227
[6]WuX,KimSB.J.PowerSources,2002,109:53 ̄57
[7]AlcantaraR,JarabaM,LavelaP,etal.ElectrochimActa,2002,47:1829 ̄1835
[8]LeeYS,SunYK,OtaS,etal.ElectrochemCommun,2002,4(12):989 ̄994
季勇等:正极材料LiNi
0.5
Mn1.5O4的合成及性能601
磷酸铁锂正极材料稳定性探讨
磷酸铁锂正极材料稳定性探讨 张世杰副总工程师 中国电子科技集团公司第十八研究所 目录 引言 磷酸铁锂正极材料产业现状分析 目前磷酸铁锂正极材料批产存在的主要质量问题 产生质量问题的主要原因分析 如何提高磷酸铁锂批次稳定性 讨论 1、引言 采用磷酸铁锂正极材料制备的锂离子电池与其他正极材料制备的锂离子电池比较具有三个突出的特点:一是电池安全性好,电池在过充电、过放电、短路、针刺等试验条件下安全;二是电池充放电循环寿命长且容量保持率高,能够循环2000次且容量仍能保持90%;三是电池倍率放电能力强,可以几十倍率放电。因此,磷酸铁锂正极材料被公认为是动力锂离子电池理想正极材料,也成为世人关注的“热点”。
锂离子电池制造商在使用国产磷酸铁锂正极材料试验和生产电池过程发现:国产磷酸铁锂正极材料与国际先进同类产品相比仍有较大差距、一部分磷酸铁锂供应商提供的材料存在不同程度的质量问题、批次产品之间存在质量不稳定等问题。为此,国产磷酸铁锂正极材料质量一致性又成为人们关注的“焦点”。 如何迅速解决磷酸铁锂正极材料生产中存在的关键技术问题、工艺技术问题和产品质量问题?如何提高磷酸铁锂批生产过程产品批次不稳定问题?更是从事磷酸铁锂正极材料技术研究、产品开发、中试和批生产技术攻关工作者所面临的一大“难点”。 本报告正是针对以上人们关心和关注的问题,结合实际工作中遇到的问题,浅谈一些粗浅的见解。 2、磷酸铁锂正极材料产业现状分析 国内已经形成了一批磷酸铁锂正极材料生产商,产业初具规模,并把产品投向市场,提供给锂离子电池制造商使用。但是,大家普遍感到:目前国内磷酸铁锂正极材料批量生产技术还存在突出的工艺稳定性问题。突出表现在: 一些大的锂离子电池制造商从磷酸铁锂材料平均粒径、电极加工性、电极压实密度、实际比容量、循环寿命、倍率放电、温度特性、安全性等方面对国内几个磷酸铁锂材料供应商和Valence等国外供应商所提供的材料进行了非常系统的试验评价,客观的试验数据表明:国内磷酸铁锂批产产品与Valence等国外供应商产品比较仍有较大差距; 表1: Valence公司产品与国产产品3个主要指标对比
【干货】锂离子电池的的原理、配方和工艺流程,正极材料介绍
锂离子电池的的原理、配方和工艺流程,正极材料介绍 锂离子电池的的原理、配方和工艺流程 锂离子电池是一种二次电池(充电电池),它主要依靠Li+ 在两个电极之间往返嵌入和脱嵌来工作。随着新能源汽车等下游产业不断发展,锂离子电池的生产规模正在不断扩大。本文以钴酸锂为例,全面讲解锂离子电池的的原理、配方和工艺流程,锂电池的性能与测试、生产注意事项和设计原则。 一,锂离子电池的原理、配方和工艺流程; 一、工作原理 1、正极构造 LiCoO2 + 导电剂 + 粘合剂 (PVDF) + 集流体(铝箔) 2、负极构造
石墨 + 导电剂 + 增稠剂 (CMC) + 粘结剂 (SBR) + 集流体(铜箔) 3、工作原理 3.1 充电过程 一个电源给电池充电,此时正极上的电子e从通过外部电路跑到负极上,正锂离子Li+从正极“跳进”电解液里,“爬过”隔膜上弯弯曲曲的小洞,“游泳”到达负极,与早就跑过来的电子结合在一起。
正极上发生的反应为: 负极上发生的反应为: 3.2 电池放电过程 放电有恒流放电和恒阻放电,恒流放电其实是在外电路加一个可以随电压变化而变化的可变电阻,恒阻放电的实质都是在电池正负极加一个电阻让电子通过。由此可知,只要负极上的电子不能从负极跑到正极,电池就不会放电。电子和Li+都是同时行动的,方向相同但路不同,放电时,电子从负极经过电子导体跑到正极,锂离子
Li+从负极“跳进”电解液里,“爬过”隔膜上弯弯曲曲的小洞,“游泳”到达正极,与早就跑过来的电子结合在一起。 3.3 充放电特性 电芯正极采用LiCoO2 、LiNiO2、LiMn2O2,其中LiCoO2本是一种层结构很稳定的晶型,但当从LiCoO2拿走x个Li离子后,其结构可能发生变化,但是否发生变化取决于x的大小。 通过研究发现当x >0.5时,Li1-xCoO2的结构表现为极其不稳定,会发生晶型瘫塌,其外部表现为电芯的压倒终结。所以电芯在使用过程中应通过限制充电电压来控制Li1-xCoO2中的x值,一般充电电压不大于4.2V那么x小于0.5 ,这时Li1-xCoO2的晶型仍是稳定的。 负极C6其本身有自己的特点,当第一次化成后,正极LiCoO2中的Li被充到负极C6中,当放电时Li回到正极LiCoO2中,但化成之后必须有一部分Li留在负极C6中心,以保证下次充放电Li 的正常嵌入,否则电芯的压倒很短,为了保证有一部分Li留在负
磷酸铁锂正极材料制备方法比较
磷酸铁锂正极材料制备方法比较 A.固相法 一. 高温固相法 1.流程:传统的高温固相合成法一般以亚铁盐(草酸亚铁,醋酸铁,磷酸亚铁等) ,磷酸盐(磷酸氢二铵,磷酸二氢铵),锂盐(碳酸锂,氢氧化锂,醋酸锂及磷酸锂等)为原料,按LiFeP04分子式的原子比进行配料,在保护气氛(氮气、氩气或它们与氢气的混合气体)中一步、二步或三步加热,冷却后可得LiFeP04粉体材料。 例1: C.H.Mi等采用一:步加热法得到包覆碳的LiFeP04,其在30 C, 0.1 C 倍率下的初始放电容量达到160 mAh g-1 ;例2 : S.S.Zhang等采用二步加热法,以 FeC:2O4 2H2O和LiH2PO4为原料,在氮气保护下先于350~380 C加热5 h形成前驱体,再在800 C下进行高温热处理,成功制备了LiFePO4/C复合材料,产物在0.02 C倍率下的放 电容量为159 mAh g-1 ;例3 : A.S.Andersson等采用三步加热法,将由:Li2CO3、FeC2O4 2H2O 和(NH4)2HPO4组成的前驱体先在真空电炉中于300 C下预热分解,再在氮气保护下先于 450 C加热10 h,再于800 C烧结36 h,产物在放电电流密度为2.3 mA g-1时放电,室温初始放电容量在136 mAh g-1 左右;例4: Padhi 等以Li2CO3 , Fe(CH3COO)2 , NH4H2PO4 为原料,采用二步法合成了LiFePO4正极材料,其首次放电容量达110 mA h /g ; Takahashi 等以LiOH H2O, FeC2O4 2H2O , (NH4)2HPO4 为原料,在675、725、800 C下,制备出具有不同放电性能的产品,结果表明,低温条件下合成的产品放电容量较大;例5:韩国的Ho Chul Shin、Ho Jang等以碳酸锂、草酸亚铁、磷酸二氢铵为原料,添加5wt%的乙炔黑为碳源、以 At+5%H2为保护气氛,在700 C下煅烧合成10h,得到碳包覆的LiFePO4材料。经检测表明,用该工艺合成的LiFePO4制备的电池放电平台在3 4-3 5V之间,0 05C首次放电比容量为150mA h/g ;例 6 :高飞、唐致远等以醋酸锂、草酸亚铁、磷酸二氢铵为原料,聚乙烯醇为碳源。混料球磨所得粒径细小,分布的悬浊液。然后将悬浊液采用喷雾干燥的方法制得LiFePO4 前驱体,再通过高温煅烧合成LiFePO4/C正极材料,首次放电比容量最为139 4mA h/g,并具有良好的循环性能,经10C循环50次后,比容量仅下降0 15% ;例7:赵新兵、周鑫等以氢氧化锂、磷酸铁、氟化锂为原料,,聚丙烯为碳源,先在500 C下预烧,再在700 C下煅烧合成具有F掺杂的LiFePO酒精为球磨介质4/C材料,电化学测试结果表明,LiFePO3 98F0 02/C 具有最佳放电特性,在1C倍率充放电下比容量为146mA h/g。 2?优点:工艺简单、易实现产业化 3?缺点:颗粒不均匀;晶形无规则;粒径分布范围广;实验周期长;难以控制产物的批次 稳定性;在烧结过程中需要耗费大量的惰性气体来防止亚铁离子的氧化;所生产的LiFePO4 粉末导电性能不好,需要添加导电剂增强其导电性能 4?改性:添加导电剂(多用蔗糖,乙炔黑,聚乙烯醇,聚丙烯等碳源)增强其导电性能 二. 碳热还原法 1.流程:碳热还原法也是高温固相法中的一种,是比较容易工业化的合成方法,多数以氧化铁或磷酸铁做为铁源,配以磷酸二氢锂以及蔗糖等碳源,均匀混合后,在高温和氩气或氮气 保护下焙烧,碳将三价铁还原为二价铁,也就是通过碳热还原法合成磷酸铁锂。 例1:杨绍斌等以正磷酸铁为铁源,以葡萄糖、乙炔黑为碳源,采用碳热还原法合成橄榄石型磷酸铁锂。研究发现:双碳复合掺杂样品电性能最高为148.5 mAh/g,倍率放电性能仍具 有优势,10 C时容量保持率为88.1% ;例2 : Mich等以分析纯的FePO4和LiOH为原料,聚丙烯为还原剂,合成的材料在0.1 C及0.5 C倍率下首次放电比容量分别为160 mAh/g 和146.5 mAh/g ; 例3 : PP.Prosini 等以(NH4)2Fe(SO4)2和NH4H2PO4为原料首先合成FePO4,然后用LiI还原Fe3+,并在还原性气氛
锂电池几种正极材料的优缺点
锂电池几种正极材料的优缺点 锂离子电池的性能主要取决于所用电池内部材料的结构和性能。这些电池内部材料包括负极材料、电解质、隔膜和正极材料等。其中正、负极材料的选择和质量直接决定锂离子电池的性能与价格。因此廉价、高性能的正、负极材料的研究一直是锂离子电池行业发展的重点。负极材料一般选用碳材料,目前的发展比较成熟。而正极材料的开发已经成为制约锂离子电池性能进一步提高、价格进一步降低的重要因素。在目前的商业化生产的锂离子电池中,正极材料的成本大约占整个电池成本的40%左右,正极材料价格的降低直接决定着锂离子电池价格的降低。对锂离子动力电池尤其如此。比如一块手机用的小型锂离子电池大约只需要5克左右的正极材料,而驱动一辆公共汽车用的锂离子动力电池可能需要高达500千克的正极材料。 衡量锂离子电池正极材料的好坏,大致可以从以下几个方面进行评估:(1)正极材料应有较高的氧化还原电位,从而使电池有较高的输出电压;(2)锂离子能够在正极材料中大量的可逆地嵌入和脱嵌,以使电池有高的容量;(3)在锂离子嵌入/脱嵌过程中,正极材料的结构应尽可能不发生变化或小发生变化,以保证电池良好的循环性能;(4)正极的氧化还原电位在锂离子的嵌入/脱嵌过程中变化应尽可能小,使电池的电压不会发生显著变化,以保证电池平稳地充电和放电;(5)正极材料应有较高的电导率,能使电池大电流地充电和放电;(6)正极不与电解质等发生化学反应;(7)锂离子在电极材料中应有较大的扩散系数,便于电池快速充电和放电;(8)价格便宜,对环境无污染。 锂离子电池正极材料一般都是锂的氧化物。研究得比较多的有LiCoO2,LiNiO2,LiMn2O4,LiFePO4和钒的氧化物等。导电聚合物正极材料也引起了人们的极大兴趣。 1、LiCoO2 在目前商业化的锂离子电池中基本上选用层状结构的LiCoO2作为正极材料。其理论容量为274mAh/g,实际容量为140mAh/g左右,也有报道实际容量已达155mAh/g。该正极材料的主要优点为:工作电压较高(平均工作电压为3.7V)、充放电电压平稳,适合大电流充放电,比能量高、循环性能好,电导率高,生产工艺简单、容易制备等。主要缺点为:价格昂贵,抗过充电性较差,循环性能有待进一步提高。 2、LiNiO2
正极材料
【交流】锂电池几种正极材料的优缺点 作者: bibiaomian(站内联系TA)发布: 2010-12-01 锂离子电池的性能主要取决于所用电池内部材料的结构和性能。这些电池内部材料包括负极材料、电解质、隔膜和正极材料等。其中正、负极材料的选择和质量直接决定锂离子电池的性能与价格。因此廉价、高性能的正、负极材料的研究一直是锂离子电池行业发展的重点。负极材料一般选用碳材料,目前的发展比较成熟。而正极材料的开发已经成为制约锂离子电池性能进一步提高、价格进一步降低的重要因素。在目前的商业化生产的锂离子电池中,正极材料的成本大约占整个电池成本的40%左右,正极材料价格的降低直接决定着锂离子电池价格的降低。对锂离子动力电池尤其如此。比如一块手机用的小型锂离子电池大约只需要5克左右的正极材料,而驱动一辆公共汽车用的锂离子动力电池可能需要高达500千克的正极材料。 衡量锂离子电池正极材料的好坏,大致可以从以下几个方面进行评估:(1)正极材料应有较高的氧化还原电位,从而使电池有较高的输出电压;(2)锂离子能够在正极材料中大量的可逆地嵌入和脱嵌,以使电池有高的容量;(3)在锂离子嵌入/脱嵌过程中,正极材料的结构应尽可能不发生变化或小发生变化,以保证电池良好的循环性能;(4)正极的氧化还原电位在锂离子的嵌入/脱嵌过程中变化应尽可能小,使电池的电压不会发生显著变化,以保证电池平稳地充电和放电;(5)正极材料应有较高的电导率,能使电池大电流地充电和放电;(6)正极不与电解质等发生化学反应;(7)锂离子在电极材料中应有较大的扩散系数,便于电池快速充电和放电;(8)价格便宜,对环境无污染。 锂离子电池正极材料一般都是锂的氧化物。研究得比较多的有LiCoO2,LiNiO2,LiMn2O4,LiFePO4和钒的氧化物等。导电聚合物正极材料也引起了人们的极大兴趣。 1、LiCoO2 在目前商业化的锂离子电池中基本上选用层状结构的LiCoO2作为正极材料。其理论容量为274mAh/g,实际容量为140mAh/g左右,也有报道实际容量已达155mAh/g。该正极材料的主要优点为:工作电压较高(平均工作电压为3.7V)、充放电电压平稳,适合大电流充放电,比能量高、循环性能好,电导率高,生产工艺简单、容易制备等。主要缺点为:价格昂贵,抗过充电性较差,循环性能有待进一步提高。 2、LiNiO2 用于锂离子电池正极材料的LiNiO2具有与LiCoO2类似的层状结构。其理论容量为274
锂离子电池正极材料镍锰酸锂的制备及其电化学性能研究
目录 摘要................................................................................................................ I Abstract ......................................................................................................... III 第1章绪论 (1) 1.1 引言 (1) 1.2 锂离子电池的基本原理 (2) 1.3 锂离子电池正极材料研究概况 (3) 1.3.1 层状结构正极材料 (3) 1.3.2 聚阴离子型正极材料 (4) 1.3.3 尖晶石型正极材料 (5) 1.4 镍锰酸锂的制备方法 (6) 1.5 镍锰酸锂正极材料的缺陷及其改进 (8) 1.5.1 元素掺杂改性 (8) 1.5.2 表面包覆改性 (9) 1.5.3 形貌改性 (10) 1.5.4 晶面调控改性 (11) 1.6 论文主要研究内容及意义 (13) 第2章实验方法 (15) 2.1 实验所用药品及分析仪器 (15) 2.1.1 实验所用试剂及原料 (15) 2.1.2 实验仪器与设备 (15) 2.2 材料表征手段 (16) 2.2.1 X射线衍射(XRD) (16) 2.2.2 扫描电子显微镜(SEM) (16) 2.2.3 热重分析(TG) (16) 2.2.4 电化学性能测试 (17) 2.3 正极片的制备与电池组装 (17) 2.3.1 正极片的制备 (17) 2.3.2 纽扣半电池的组装 (17) 第3章纳米及纳微结构LiNi 0.5Mn 1.5 O 4 的制备及其性能研究 (18) 3.1 引言 (18) 3.2 实验部分 (18) 3.3 结果与讨论 (19) 3.4 本章小结 (26)
锂离子电池三元镍钴锰正极材料研究现状综述
三元系锂电池正极材料研究现状 摘要:综述了近年来锂离子电池层状Li-Ni-Co-Mn-O正极材料的研究进展,重点介绍了正极材料LiNi l/3Co l/3Mn l/3O其合成方法电化学性能以及掺杂、包覆改性等方面的研究结果。 三元系正极材料的结果: LiMn x Co y Ni1-x-y O2具有α-2NaFeO2层状结构。Li原子占据3a位置,Ni、Mn、Co随机占据3b位置,氧原子占据6c位置。其过渡金属层由Ni、Mn、Co 组成,每个过渡金属原子由6 个氧原子包围形成MO6 八面体结构,而锂离子嵌入过渡金属原子与氧形成的(MnxCo yNi1-x-y) O2层之间。在层状锂离子电池正极材料中均有Li+与过渡金属离子发生位错的趋势,特别是以结构组成中有Ni2+存在时这种位错更为突出。抑制或消除过渡金属离子在锂层中的位错现象是制备理想α-2NaFeO2结构层状正极材料的关键,在LiMn x Co y Ni1-x-y O2结构中, Ni2+的半径( rNi2+=0.069nm)与Li+的( rLi+=0.076nm)半径接近,因此晶体结构会发生位错,即过渡金属层中的镍原子占据锂原3a的位置,锂原子则进驻3b位置。在Li+层中,Ni2+的浓度越大,则Li+在层状结构中脱嵌越困难,电化学性能越差。而相对于LiNiO2及LiNi x Co1-x-y O2 ,LiMn x Co y Ni1-x-y O2中这种位错由于Ni 含量的降低而显著减少。同时由于Ni2 + 的半径( rNi2 + =0. 069nm) 大于Co3+ ( rCo3+ = 0. 0545nm) 和Mn4 + ( rMn4 + =0. 053nm) ,LiMnxCo yNi1 - x - yO2 的晶格常数有所增加。 由于充分综合镍酸锂的高比容量、钴酸锂良好的循环性能和锰酸
几种正极材料对比
锂电池的几种主要正极材料 1、锂电池正极材料主要有钴酸锂、镍酸锂、锰酸锂、磷酸铁锂、钒的氧化物和三元材料等。锂电池的性能主要取决于所用电池内部材料的结构和性能。这些电池内部材料包括正极材料、负极材料、电解液、隔膜和导电材料等。其中正、负极材料的选择和质量直接决定锂电池的性能与价格。因此廉价、高性能的正、负极材料的研究一直是锂电池行业发展的重点。负极材料一般选用碳材料,目前的发展比较成熟。而正极材料的开发已经成为制约锂电池性能进一步提高、价格进一步降低的重要因素。 在目前的商业化生产的锂电池中,正极材料的成本大约占整个电池成本的40%左右,正极材料价格的降低直接决定着锂电池价格的降低。对锂动力电池尤其如此。比如一块手机用的小型锂电池大约只需要5克左右的正极材料,而驱动一辆电动汽车用的锂动力电池可能需要高达500千克的正极材料。衡量锂电池正极材料的好坏,大致可以从以下几个方面进行评估: (1)正极材料应有较高的氧化还原电位,从而使电池有较高的输出电压;(2)锂离子能够在正极材料中大量的可逆地嵌入和脱嵌,以使电池有高的容量;(3)在锂离子嵌入/脱嵌过程中,正极材料的结构应尽可能不发生变化或小发生变化,以保证电池良好的循环性能; (4)正极的氧化还原电位在锂离子的嵌入/脱嵌过程中变化应尽可能小,使电池的电压不会发生显著变化,以保证电池平稳地充电和放电; (5)正极材料应有较高的电导率,能使电池大电流地充电和放电; (6)正极不与电解质等发生化学反应; (7)锂离子在电极材料中应有较大的扩散系数,便于电池快速充电和放电;(8)价格便宜,对环境无污染。 锂电池正极材料一般都是锂的氧化物。研究得比较多的有钴酸锂,镍酸锂,锰酸锂,磷酸铁锂和钒的氧化物等。导电聚合物正极材料也引起了人们的极大兴趣。 1.1、钴酸锂
动力电池各种正极材料性能比较
动力电池各种正极材料性能比较 来源:中国储能网 链接:https://www.360docs.net/doc/0b6692886.html,/tech/23760.html 动力电池各种正极材料性能比较 锂离子动力电池是目前最有潜力的车载电池,主要由正极材料、负极材料、隔膜、电解质等部分组成。目前负极材料的研发和生产已比较成熟。正极材料、隔膜和电解质是锂离子电池的核心材料,占据电池成本的70%;其中又以正极材料附加值最高,约占锂电池成本的30%。这三种核心材料的技术突破,将对锂离子动力电池的性能提升起到重要推动作用。 目前已批量应用于锂电池的正极材料主要有钴酸锂、镍酸锂、锰酸锂、钴镍锰酸锂(三元材料)以及磷酸铁锂。 钴酸锂:研究始于1980 年,20 世纪90 年代开始进入市场。它属于α-NaFeO2型层状岩盐结构,结构比较稳定 ,是一种非常成熟的正极材料产品,目前占据锂电池正极材料市场的主导地位。但由于其高昂的价格和较差的抗过充电性,使其使用寿命较短,而且钴有放射性,不利于环保,因此发展受到限制。 镍酸锂:氧化镍锂的价格较钴酸锂便宜,理论能量密度达276mAh/g,但制作难度大,且安全性和稳定性不佳 。技术上采用掺杂Co、Mn、Al、F 等元素来提高其性能。由于提高镍酸锂技术研究需考察诸多参数,工作量大,目前的进展缓慢。 锰酸锂:锰资源丰富、价格便宜,而且安全性较高、易制备,成为锂离子电池较为理想的正极材料。早先较 常用的是尖晶石结构的LiMn2O4,工作电压较高,但理论容量不高,与电解质的相容性不佳,材料在电解质中会缓慢溶解。近年新发展起来层状结构的三价锰氧化物LiMn2O4,其理论容量为286mAh/g,实际容量已达200mAh/g 左右,在理论容量和实际容量上都比LiMn2O4 大幅度提高,但仍然存在充放电过程中结构不稳定,以及较高工作温度下的溶解问题。 钴镍锰酸锂:即现在常说的三元材料,它融合了钴酸锂和锰酸锂的优点,在小型低功率电池和大功率动力电 池上都有应用。但该种电池的材料之一——钴是一种贵金属,价格波动大,对钴酸锂的价格影响较大。钴处于价格高位时,三元材料价格较钴酸锂低,具有较强的市场竞争力;但钴处于价格低位时,三元材料相较于钴酸锂的优势就大大减小。随着性能更加优异的磷酸铁锂的技术开发,三元材料大多被认为是磷酸铁锂未大规模生产前的过渡材料。 磷酸铁锂:在所有的正极材料中,LiFePO4 正极材料做成的锂离子电池在理论上是最便宜的。它的另一个特点 是对环境无污染。此外,它在大电流放电率放电(5~10C 放电)、放电电压平稳性、安全性、寿命长等方面都比其它几类材料好,是最被看好的电流输出动力电池。目前A123 公司已能将磷酸铁锂正极材料制造成均匀的纳米级超小颗粒,使颗粒和总表面积剧增,进一步体高了磷酸铁锂电池的放电功率和稳定性。 原文地址:https://www.360docs.net/doc/0b6692886.html,/tech/23760.html 页面 1 / 1
2017年锂电池正极材料分析报告
2017年锂电池正极材料深度 分析报告 (此文档为word格式,可任意修改编辑!) 2017年8月
正文目录 一.正极材料:锂电池的核“芯” (5) 1.1 正极材料为锂电池产业链的关键材料 (5) 1.2 传统的电池材料正不断被替换 (6) 1.3 上游涨价带动正极材料价格上涨 (9) 1.4 动力电池材料成为热点 (11) 二.下游市场需求旺盛,以动力型电池增长为主 (14) 2.1 3C市场增速放缓,需求平稳 (16) 2.2 动力型电池增长明显,需求旺盛 (18) 2.3 储能领域的应用逐渐增长 (21) 三.扩张时代,高镍三元为王 (23) 3.1 高能量密度三元材料需求增大 (23) 3.2 产能扩大加剧行业洗牌 (26) 3.3 正极材料中日韩三分天下 (27) 四.主要公司分析 (28) 4.1 杉杉股份 (28) 4.2 当升科技 (30) 4.3 格林美 (32)
图表目录 图表 1:锂离子电池结构 (5) 图表 2:电芯材料成本构成 (5) 图表 3:正极材料产业链(以含钴的材料为例) (6) 图表 4:正极材料性能统计 (7) 图表 5:中国正极材料细分产品产量 (8) 图表 6:中国正极材料产量 (8) 图表 7:中国正极材料产量结构 (9) 图表 8:磷酸铁锂价格变动趋势图(元/吨) (10) 图表 9:钴酸锂价格变动趋势图(元/吨) (10) 图表 10:部分正极材料价格涨跌表(万元/吨) (11) 图表 11:三元NCM523价格变动趋势图(元/吨) (11) 图表 12:常见正极材料合成示意图 (11) 图表 13:磷酸铁锂合成路线图 (12) 图表 14:三元材料合成路线图 (12) 图表 15:三元材料分型号产量占比(2016) (13) 图表 16:常见的三元正极材料性能表 (13) 图表 17:主要的正极材料厂商(2016) (13) 图表 18:主部分正极材料上市公司业绩(2016) (14) 图表 19:全球锂电市场规模(2011-2015,亿元) (15) 图表 20:中国锂电池产量和增速(2012-2016,Gwh) (15) 图表 21:中国锂电池产值和增速(2012-2016) (16) 图表 22:中国锂电池用途分类(2012-2015) (16) 图表 23:全球手机出货量(2011-2016,千部) (17) 图表 24:中国无人机市场规模产值(亿元) (18) 图表 25:中国智能穿戴市场规模(亿元) (18) 图表 26:全国动力电池用正极材料需求(2017-2020,万吨) (19) 图表 27:全国动力电池出货量(2012-2016,Gwh) (19)
正极材料材料制备
水热法制备金属氧化物表面改 性正极材料 研究意义: 目前许多正极材料都存在一些主要缺点,如钴酸锂的高成本与有限可逆比容量、锰酸锂的高温循环与储存性能差、镍钴锰酸锂三元材料的低压实密度、磷酸铁锂存在电子传导率低,锂离子传导率低等。
?电解液会有缓慢分解的现象,并且在高电压下的正极材料具有较强的氧化性,加速了电解液的分解,会产生一些有害的副产物;同时电解液还会浸蚀正极材料,这样电解液与正极材料相互作用会导致电池的自放电增大,循环性能变差,也影响到电池的安全性能。为了克服正极材料与电解液的相互作用,通常是采用表面包覆的方法避免正极材料和电解液的直接接触。?研究内容:本实验利用水热法制备氧化锌表面修饰正极材料
?实验原理: 锌盐溶液与NaOH 溶液混合,初期产生大量白色絮状物;振荡搅拌后白色絮状物迅速溶解,变为白色透明溶液。随着反应在水 热条件下进行生长基之间发生氧桥键 合作用,以及阴离子基团的质子化反应形成ZnO 晶核。 ↓????→????→?+- ZnO OH Zn NaOH NO Zn 水热反应过程 搅拌反应2423)()(-24)(OH Zn
?实验步骤: 1)称量:2)溶解:将与分别置于两只小烧杯中,搅拌使溶解。 3)混合:将缓慢地加入到盛有 溶液烧杯中,搅拌至溶液澄清,用pH 试纸测其pH 值为14。 4)反应:将加入到高压釜的内衬中,将混合液注入到其中,搅拌,将磁子放入内衬中,将高压釜放在150℃油浴中,并开启搅拌开关,反应1h 。2 2232,4,6)(3.0gLiCoO gNaOH O H NO gZn 2 3)(NO Zn NaOH 23)(NO Zn 2LiCoO NaOH
浅谈四大正极材料的压实密度
众所周知,压实密度一般受真密度和材料形貌结构的影响。 真密度 材料的压实密度主要受真密度影响比较大,不同材料的真密度分别为:钴酸锂:5.1,锰酸锂:4.2,磷酸铁锂3.6,三元材料受组成的不同,真密度有所变化,一般的111型,以美国3M的BC-618为例,约为4.8,所以按照真密度的由大到小来排列,四种材料的顺序如下:钴酸锂>三元>锰酸锂>磷酸铁锂,这也与目前压实密度的趋势完全一致,可见,真密度是影响一种材料压实的最大影响因素。 形貌结构 材料的表面光滑程度,二次颗粒内部空隙的大小,材料的规整程度,这些都是影响材料压实密度的因素,目前的钴酸锂是一次颗粒,这也就不存在二次颗粒内部间隙的影响,我公司的锰酸锂和三元材料也做成了类钴酸锂的一次颗粒(锰酸锂可以成为单晶,三元材料存在争议),也把压实密度分别提高到了锰酸锂(2.9-3.2),三元(3.7-3.9),至于磷酸铁锂,(比较特殊,会在倍率性能部分说明)由于材料的纳米化,限制了其压实的进一步提高,粒径分布是比较复杂的因素,合理的粒径分布可以适当的提高压实,这些可以一般可以根据自己的产品作相应的调整。 倍率性能 倍率性能属于电化学性能,与材料的客观的压实密度无关,但是考虑到在电池的应用中,就有必要细细说明。单纯从材料本身的倍率性能而言(排除粒径影响)锰酸锂>钴酸锂>三元材料>磷酸铁锂。为了保证材料的倍率性能,目前产业化的产品都在工艺上进行了调整,以保证其倍率性能,所以目前的D50一般的范围来说也是和材料自身倍率性成正比,自身倍率性(离子和电子传输能力)越好的产品,一般可以做到粒径越大,因为大的粒径可以保证材料的压实密度更高一些(虽然二者比例不是严格的对应),当然,特殊领域的追求高倍率产品属于例外。 所以,我们可以合理认为:倍率性能在一定程度上限制了压实密度的提高。 (补充:我们提高压实的途径:把产品做成类钴酸锂的一次颗粒 单晶一次颗粒的压实密度高于二次颗粒,这是毋庸置疑的,但是带来的新的问题就是可能影响倍率性能,因为倍率性能与锂离子在颗粒内部的传输速率相关性很大,一般粒径越小,传输速率越快(这也是磷酸铁锂必须纳米化的主要原因),普通的二次颗粒的小颗粒都是纳米级或者1微米以下,所以即使二次颗粒的粒径D50大于做到十几甚至几十微米,倍率性能依然不错,但是单晶一次颗粒的另一个好处是,自由长成的晶体表面很光滑,与导电剂接触很紧密,此外,高温下自由长成的晶体内部晶格缺陷很少,使里离子传输更加畅通,此外,我们把粒径做小(小于二次团聚颗粒)也有助于倍率性能的提高。以上为一次颗粒倍率性的说明)
镍钴锰三元正极制备方法
1镍钴锰三元正极材料结构特征 镍钴锰三元材料通常可以表示为:LiNixCoyMnzO2,其中x+y+z=1;依据3种元素的摩尔比(x∶y∶z比值)的不同,分别将其称为不同的体系,如组成中镍钴锰摩尔比(x∶y∶z)为1∶1∶1的三元材料,简称为333型。摩尔比为5∶2∶3的体系,称之为523体系等。 333型、523型和811型等三元材料均属于六方晶系的α-NaFeO2型层状岩盐结构,如图1。 镍钴锰三元材料中,3种元素的的主要价态分别是+2价、+3价和+4价,Ni为主要活性元素。其充电时的反应及电荷转移如图2所示。 一般来说,活性金属成分含量越高,材料容量就越大,但当镍的含量过高时,会引起Ni2+占据Li+位置,加剧了阳离子混排,从而导致容量降低。Co正好可以抑制阳离子混排,而且稳定材料层状结构;Mn4+不参与电化学反应,可提供安全性和稳定性,同时降低成本。 2镍钴锰三元正极材料制备技术的最新研究进展 固相法和共沉淀法是传统制备三元材料的主要方法,为了进一步改善三元材料电化学性能,在改进固相法和共沉法的同时,新的方法诸如溶胶凝胶、喷雾干燥、喷雾热解、流变相、燃烧、热聚合、模板、静电纺丝、熔融盐、离子交换、微波辅助、红外线辅助、超声波辅助等被提出。 2.1固相法
三元材料创始人OHZUKU最初就是采用固相法合成333材料,传统固相法由于仅简单采用机械混合,因此很难制备粒径均一电化学性能稳定的三元材料。为此,HE等、LIU等采用低熔点的乙酸镍钴锰,在高于熔点温度下焙烧,金属乙酸盐成流体态,原料可以很好混合,并且原料中混入一定草酸以缓解团聚,制备出来的333,扫描电镜图(SEM)显示其粒径均匀分布在0.2~0.5μm左右,0.1C(3~4.3V)首圈放电比容量可达161mAh/g。TAN等采用采用纳米棒作为锰源制备得到的333粒子粒径均匀分布在150~200nm。 固相法制得的材料的一次粒子粒径大小在100~500nm,但由于高温焙烧,一次纳米粒子极易团聚成大小不一的二次粒子,因此,方法本身尚待进一步的改进。 2.2共沉淀法 共沉淀法是基于固相法而诞生的方法,它可以解决传统固相法混料不均和粒径分布过宽等问题,通过控制原料浓度、滴加速度、搅拌速度、pH值以及反应温度可制备核壳结构、球形、纳米花等各种形貌且粒径分布比较均一的三元材料。 原料浓度、滴加速度、搅拌速度、pH值以及反应温度是制备高振实密度、粒径分布均一三元材料的关键因素,LIANG等通过控制pH=11.2,络合剂氨水浓度0.6mol/L,搅拌速度800r/min,T=50℃,制备得到振实密度达2.59g/cm3,粒径均匀分布的622材料(图3),0.1C(2.8~4.3V)循环100圈,容量保持率高达94.7%。 鉴于811三元材料具有高比容量(可达200mAh/g,2.8~4.3V),424三元材料则可提供优异的结构和热稳定性的特点。有研究者试图合成具有核壳结构的(核为811,壳层l为424)三元材料,HOU等采用分布沉淀,先往连续搅拌反应釜(CSTR)中泵入8∶1∶1(镍钴锰比例)的原料,待811核形成后在泵入镍钴锰比例为1∶1∶1的原料溶液,形成第一层壳层,然后再泵入组成为4∶2∶2的原溶液,最终制备得到核组成为811,具有壳组成为333、424的双层壳层的循环性能优异的523材料。4C倍率下,这种材料循环300圈容量保持率达90.9%,而采用传统沉淀法制备的523仅为72.4%。 HUA等采用共沉淀法制备了线性梯度的811型,从颗粒内核至表面,镍含量依次递减,锰含量依次递增,从表1可明显看到线性梯度分布的811三元材料大倍率下放电容量和循环性明显优于元素均匀分布的811型。
锂离子电池正极材料的合成及改性研究
目录 第一章绪论 (1) 1.1 引言 (1) 1.2 锂离子电池简介 (2) 1.2.1 锂离子电池的结构 (2) 1.2.2 锂离子电池的工作原理 (3) 1.3 锂离子电池研究进展 (4) 1.3.1 锂离子负极材料 (5) 1.3.2 锂离子正极材料 (7) 1.4 本论文的研究目的及内容 (14) 第二章实验试剂与实验技术 (20) 2.1实验药品与仪器 (20) 2.2 材料制备技术 (22) 2.3 材料的表征技术 (22) 2.3.1 X射线衍射分析(XRD) (22) 2.3.2 扫描电子显微镜(SEM) (22) 2.3.3 透射电子显微镜(TEM) (23) 2.3.4 拉曼光谱分析技术 (23) 2.3.5 X射线光电子能谱(XPS) (23) 2.4 电化学表征方法 (23) 2.4.1 充放电测试 (23) 2.4.2 循环伏安测试(CV) (24) 第三章富锂层状材料的结构和电化学性能研究 (25) 3.1 引言 (25) 3.2 0.6Li[Li1/3Mn2/3]O2 - 0.4LiNi(2+x)/6Mn(2+x)/6Co(1-x)/3O2 体系的研究 (26) 3.2.1 实验部分 (26) 3.2.1.1 材料的制备 (26) 3.2.1.2 性能表征 (26)
3.2.1.3 电化学性能测试 (27) 3.2.2 结果与讨论 (27) 3.2.3 小结 (35) 3.3 Li[Li0.2Ni0.17Mn0.56Co0.07]O2的ZnO 包覆 (35) 3.3.1 实验部分 (35) 3.3.1.1 材料的制备 (35) 3.3.1.2 性能表征 (36) 3.3.1.3 电化学性能测试 (36) 3.3.2 结果与讨论 (37) 3.3.2 小结 (39) 第四章高电压LiNi0.5Mn1.35Ti0.15O4材料的合成及改性 (42) 4.1 引言 (42) 4.2 实验部分 (43) 4.2.1 材料制备 (43) 4.2.2 性能表征 (44) 4.2.3 电化学性能测试 (44) 4.3 结果与讨论 (44) 4.4 本章小结 (52) 第五章结论 (55) 科研成果 (56) 致谢 (57)
氟化石墨烯用作一次锂电池正极材料的性能
文章编号:1007_8827(2015)01_0079_07 氟化石墨烯用作一次锂电池正极材料的性能 许耀,詹亮,王赟,王艳莉,施云海 (华东理工大学化学工程联合国家重点实验室特种功能高分子材料及其相关技术教育部重点实验室,上海200237) 摘要:以异丙醇/水二氟化石墨分别作试剂和原料,采用液相剥离法制备出氟化石墨烯三所制氟化石墨烯呈二维二无定型的多孔结构,其中F含量高达49.7%三氟化石墨烯丰富的C_F键及其超薄的二维纳米结构有利于Li+在充放电过程中的存储和扩散,因此所制氟化石墨烯具有优异的电化学性能,尤其有较大的功率密度三 关键词:氟化钠米石墨片;二维纳米结构;氟化石墨;一次锂电池 中图分类号:TQ127.1+1文献标识码:A 基金项目:国家自然科学基金(51472086,51002051);上海市自然科学基金(12ZR1407200). 通讯作者:詹亮,副教授.E_mail:zhanliang@https://www.360docs.net/doc/0b6692886.html,;施云海,副教授.E_mail:shi yunhai@https://www.360docs.net/doc/0b6692886.html, 作者简介:许耀,硕士研究生.E_mail:xuyaoxy@https://www.360docs.net/doc/0b6692886.html, Fluorinated graphene as a cathode material for high performance primary lithium ion batteries XU Yao,ZHAN Liang,WANG Yun,WANG Yan_li,SHI Yun_hai (State Key Laboratory of Chemical Engineering,Key Laboratory of Specially Functional Polymeric Materials and Related Technology(Ministry of Education),East China University of Science and Technology,Shanghai200237,China) Abstract:A free_standing fluorinated graphene(F_graphene)was fabricated by the simple liquid exfoliation of a fluorinated graphite(F_graphite)in a2_propanol/water mixture,and was used as the cathode material of primary lithium ion batteries.As_pre_ pared F_grapheneh as a very high fluorine content(49.7at%),and an amorphous_like two_dimensional nanostructure.These fea_ tures facilitate the rapid diffusion of lithium ions during discharging.The F_graphene exhibits better electrochemical performance, especially,a higher specific power density than the F_graphite. Keywords: Fluorinated graphene nanosheets;Two_dimensional nanostructure;Fluorinated graphite;Pprimary lithium batteries Received date:2014_07_13; Revised date:2015_01_17 Foundation item:National Science Foundation of China(51472086,51002051);Natural Science Foundation of Shanghai City (12ZR1407200). Corresponding author:ZHAN Liang,Associate Professor.E_mail:zhanliang@https://www.360docs.net/doc/0b6692886.html,; SHI Yun_hai,Associate Professor.E_mail:shi yunhai@https://www.360docs.net/doc/0b6692886.html, Author introduction:XU Yao,Master Student.E_mail:xuyaoxy@https://www.360docs.net/doc/0b6692886.html, English edition available online ScienceDirect(http://https://www.360docs.net/doc/0b6692886.html,/science/journal/18725805). DOI:10.1016/S1872_5805(15)60177_9 1 Introduction Fluorinated carbon(C x F)n has been extensively applied as active cathode materials for primary lithium battery[1_3].Generally,the(C x F)n materials are de_ rived from coke or graphite by reacting with fluorine gas at high temperature(600?)[4,5]or catalytically reacting with HF,F2and a volatile fluoride MF n such as IF5,BF3at room temperature[6_9].Theoretically, the carbon atoms in(C x F)n compounds are sp3hy_ bridized with F atoms forming pure covalent C_F bonding,i.e.the atomic F/C ratio is1(denoted as CF1).However,(C x F)n materials have some elec_trochemically inactive defects such as CF2groups if it is produced at high temperature[4,5].Additionally, the residual catalysts(IF5,IF6_,BF4_,ClHF_, FHF_)will be intercalated into the graphitic layers, significantly affect the electrochemical properties[10]. Importantly,due to kinetic limitations associated with the poor electrical conductivity of the strongly cova_ lent CF1,the battery can only run at medium dis_ charge current densities[11_13].Therefore,to meet the requirements of primary lithium batteries with a high power density for new applications such as for space long term exploratory missions,many efforts have been made to develop novel nanostructured(C x F)n 第30卷第1期 2015年2月新型炭材料 NEW CARBON MATERIALS Vol.30 No.1 Feb.2015
