工艺用水监护管理规程

目的:建立一个工艺用水质量监控管理规程,确保工艺用水的质量。
范围:适用于饮用水、纯化水等工艺用水的监控。
责任:QA监督员、水质检验员、水系统操作人员。
内容:
1.纯水系统新建或改建后必须经验证后方可使用,验证按《水系统验证方案》进
行。
2.水处理系统正常运行后,一般不停止工作,停用超过六个月,在正式生产三个星期前开启工艺用水处理系统并做3个周期(每七天为一周期)的监控,合格后方可投入使用。监控按《水系统验证方案》进行。
3.工艺用水日常监控
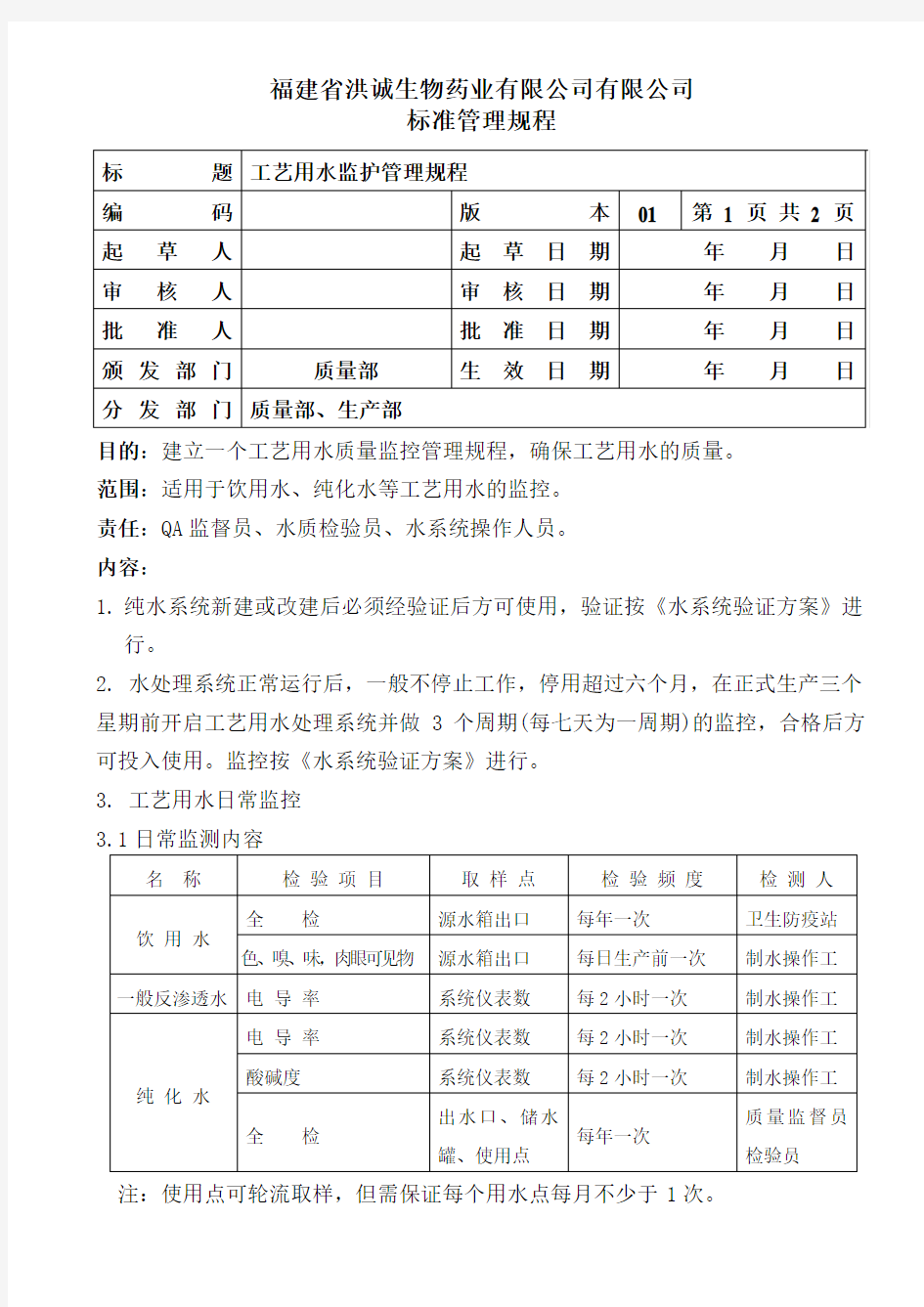
3.1日常监测内容
注:使用点可轮流取样,但需保证每个用水点每月不少于1次。
日常监测由QA负责监督。
3.2取样方法
按取样方案取样,但由于取检、化验等的因素,有时会出现个别点水质不合格的现象,这时必须考虑重新取样化验。
3.2.1在不合格的使用点再取1次样。
3.2.2重新化验不合格的指标。
重测这个指标必须合格。若不合格,则做出不合格判定,通知有关部门进行检查、维修,确保水质合格。
3.3标准依据分别为《饮用水质量标准》、《纯化水质量标准》
3.4水质检测按《水质检验操作规程》进行。
4.设备清洗、消毒
贮罐、输送纯水的管道应每月清洗并消毒一次。出现水质不合格应及时清洗消毒。
工艺用水管理制度
文件编号: 工艺用水管理规定 1.0 目的 明确规定工艺用水的监控和检查,保证工艺用水的质量。 2.0 适用范围 适用于本公司工艺用水的制备、检测、使用和设备维护。 3.0 职责 3.1生产采购部负责工艺用水的制备、使用及设备维护的管理。 3.2 技术质量部负责工艺用水的检测。 4.0 工作程序 4.1 工艺用水的分类a.饮用水 b.纯化水 4.2 工艺用水的制备: 4.2.1 由受过专业培训的人员按设备操作规程操作设备,按工艺制水要求进行制水。操作员需每天清洁设备和场地,保持制水室内卫生干净。 4.2.2工艺用水需通过管道输送至洁净区内的使用点,管道应为不锈钢或其它无毒材料制作。 4.3 工艺用水及使用范围及用量配置 4 3.1根据生产工艺要求,对需要使用工艺用水的对象作如下表规定: 4.3.2工艺用水的用量在确定年最大生产能力方案时,按最大用水量和保险系数确定其制水设备能力的配置要求。 4.3.3 生产采购部每年要根据现行的生产能力和用水设备的变化情况进行一次总用水量分析,若总用水量超出制水设备生产能力时,应补充制水设备或采取适应的措施,确保工艺用水能满足生产需求。
4.5 取样方式和取样点 4.5.4取样所用器具和方式确保不能对检测指标产生影响,如盛放做微生物限度的器具必须先进行灭菌。 4.6 工艺用水贮存要求 4.6.1饮用水不储存,直接使用市政自来水; 4.6.2纯化水在室温条件下可用不锈钢贮缸贮存,贮存时间不得超过36小时。 4.6.3购买的注射用水应在12小时内使用。 4.7 管道贮罐消毒 4.7.1输送、贮存纯化水的管道和贮罐每3个月清洗、消毒1次。 消毒方法:用适量的2.5%次氯酸钠溶液注入纯化水贮罐中,按在线清洗消毒方式打开各管道阀门,足量循环消毒30min后排放,停机浸泡30分钟,如此反复3次停止,后还是冲洗,冲洗完毕后,将清洗水箱残液排完,注入符合RO装置原水指标的水(即RO装置前级水),以清洗相同条件进行清洗消毒。或用预处理的低压冲洗条件来冲洗消毒。冲洗完毕后,按规定的运行方式进行低压冲洗和高压运行,最初产物排入地沟,到出水指标合格后。最后,在各使用点取样,按《中国药典》2010版附录纯化水规定的项目检验合格方可使用。 4.8 维护和保养 4.8.1制水设备的机械过滤器、活性炭过滤器应每周进行一次正洗、反洗,除去设备运行中截留的杂质。反洗时间约15分钟,正洗时间约5分钟。 4.8.2制水设备中的过滤器或滤膜应每3个月清洗一次,压差阻力太大导致产水量明显减少时应进更换。 4.8.3 RO膜应定期清洗(可视水质情况而定)。 4.8.4设备上的紫外线灯管累计使用不超过800小时应更换。 4.9 操作人员应做好相关的监测记录和维护保养记录,检测人员应做好水质检测并保存好记录。 5.0 相关记录 5.1《纯化水日常监测记录》 5.2《纯化水检测报告》
工艺管理制度
工艺管理制度 gz-scxb-15版本:a修改状态:0 XX年1月1日实施第一章总则第一条:为建立和健全工艺管理,加强生产责任制,严肃工艺纪律,以实现优质、高产、低耗、安全的目的,特制订本制度。第二条:工艺管理是生产技术管理的重要组成部份.其基本任务是:组织制定,执行各种产品的生产工艺技术规程及其它以此为中心的各项规程,督促、检查以生产工艺技术规程为中心的各项技术规程的执行情况,总结经验,改造生产技术,开展合理化建议的活动。并参与组织技术措施的实施;组织工艺查定和对工艺路线、工艺流程的技术经济评审,通过调查研究和生产实践,使各种规程制度不断得到修订和完善。第三条:工艺管理工作要同挖潜,革新、改造,以及新技术应用相结合,必须同提高产品质量,降低原材料消耗相结合;工艺管理还要与搞好环境保护,开展安全无事故活动相结合.第四条:工艺管理的日常工作:1、组织制订或修订产品或生产装置的工艺规程技术文件(并督促检查执行情况)。2、组织制订或修订各级工艺控制指标,操作指标,并督促检查执行情况。3、对现有的产品生产工艺,原材料消耗,以及中间控制进行定期的分析与评价,并提出改进意见和建议4、制订原始记录,工艺控制台帐、组织工艺技术分析5、开展合理化建议和技术改进活动。6、组织和参加工艺查定工作。7、配合技术情报,技术档案部门,收集和整理
国内外有关工艺技术资料。8、开展技术交流和协助开展技术教育活动。9、参加新产品技术鉴定工作。l0、参加制订和修订技术改造计划和长远规划工作。第二章工艺规程的编制和管理第五条:凡正式生产的产品和装置均需制订技术标准,工艺规程,岗位操作法和分析规程,均应该按规定的程序进行审查、批准,并给予受控编号后,方可贯彻执行.第六条:工艺规程是生产的法规,是各级生产指挥人员、生产技术管理人员开展工作的技术依据。工艺规程包括了产品的工艺路线和流程图,产品的质量,工艺和主要技经指标等基础资料。岗位操作法是按照工艺规程和生产实践经验组织编制的,是生产岗位操作人员必须共同遵守,执行的基本依据。工艺规程内容:一.产品概述1.产品名称、化学结构式、主要理化性质2.技术标准、产品质量规格、包装贮运方式3.主要用途、使用方法须知二.原辅材料1.原材料名称、规格及其主要指标检验方法2.辅助材料名称、规格及其主要指标检验方法3.其它材料名称、规格及其主要指标检验方法三.生产工艺过程1.工艺沿革(包括装置能力、技术进步等内容)2.化工工艺路线及其技术依据3.主要化学反应及副反应4.主要物料的平衡及流向5.工艺过程及流程图四.生产控制技术 1.配方和配料(可列配方编号、配方另立)2.工艺控制点示意图3.各项工艺操作指标4.主要生产工序的控制方法5.中间控制技术及检测手段6.其它五.原材料动力消耗定额六.安全生产技术1.使用、产生有毒有害物质一览表2.易燃易爆工序岗位一览表3.安全生产的贮存、
生产工艺用水管理规程
目的:规范工艺用水的管理,确保工艺用水的质量 范围:工艺用水 1.本公司工艺用水的分类 1.1 饮用水 1.2 纯化水 2.工艺用水的水质要求和检测 2.1 饮用水应符合《生活饮用水质量标准》GB 5750-851的要求,由市级卫生防疫部门每季度进行一次全检。 2.2 纯化水符合《中国药典》(2000年版)纯化水项下的有关规定,由公司质量保障部每周进行一次全检,制水岗位每二小时进行一次部分项目的检测。 3.工艺用水的用途(具体见产品工艺规程) 3.1 饮用水:非洁净区所有操作用水、制备纯化水的水源。 3.2 纯化水:洁净区(洁净管理区)所有操作用水。 4.工艺用水的制备或来源 4.1 饮紨水:经处理的深井水或直接取自城市自来水供水管网。 4.2 纯化水:饮用水经二级反渗透制得。 5.水质监控 5.1 工艺用水应制订质量标准和检验操作规程,内容包括各类水质的检查项
目、各类水质要求、取样部位及监测周期。 5.2 工艺用水的水质要按上述的时限规定定期检测,监控计划应根据验证结果来定。 6.工艺用水的储存、输送、清洁、消毒 6.1 饮用水可用镀锌管输送、一般容器常规储存、48小时内使用。 6.2纯化水的储存、输送和分配要有防止微生物滋生和污染的措施,其储存、输送、分配系统的材质宜为304不锈钢或工程塑料等;贮罐的通气口安装不脱落纤维的疏水性除菌滤器;室温下贮存时间不超过24小时。 6.3 纯化水保持动态循环使用,在室温下贮存、输送纯化水的设备、管道及静止管道(24h不流动者)应定期清洗、消毒。 6.4 与纯化水接触的不锈钢容器或管道在制作完毕后,应进行清洗脱脂钝化处理。 6.5 纯化水采用臭氧进行消毒。 7.生产工艺用水系统在安装竣工后及使用前应进行全面的验证,并且在运行一定周期后要进行再验证,以证明其制备系统的质量稳定性。
GMP-66工艺用水管理制度
1 目的 制订本公司工艺用水管理制度,加强工艺用水落石出的水质监护工作,保障生产的正常进行。 2 范围 适用于本公司工艺用水的管理。 3 定义 工艺用水是指药品生产工艺中使用的水,包括:饮用水、纯化水、注射用水。纯化水:为蒸馏法、离子交换法、反渗透法或其它适宜的方法制得的供药用的水,不含任何附加剂。注射用水:为去离子水或蒸馏水经蒸馏所得的水。 3 责任 3.1 技术部门负责制订工艺用水的水质标准。 3.2 生产车间制水岗位操作人员严格执行。 3.3 车间工艺员、质监员负责监督与检查。 5 内容 5.1 工艺用水的制备 5.1.1 饮用水由自来水公司供应。 5.1.2 纯化水由生产车间制水岗位按《纯化水制备工艺规程》进行纯化水的生产。 5.1.3 注射用水由生产车间制水岗位按《注射用水制备工艺规程》进行注射用水的生产。 5.2 工艺用水的监测管理 由质管部制订《工艺用水监测管理规定》,各车间、质管部门按此规定进行工艺用水的监测管理。《工艺用水监测管理规定》应包括工艺用水的检测项目、取样点和检测周期。
5.3 工艺用水的贮存和使用 5.3.1 纯化水贮罐、循环管道所用材质应为无毒、耐腐蚀的优质低碳不锈钢;注射用水贮罐、循环管道所用材质应为316L不锈钢。各管道的设计、安装应尽量避免死角、盲角;纯化水、注射用水贮罐的通气口应安装不脱落纤维的疏水性除菌滤器。 5.3.2 纯化水采用室温循环保存;注射用水采用65℃以上保温循保存。 5.3.3 各车间应按工艺要求正确选用工艺用水;作为工艺用水,纯化水应在制备后24小时内使用,注射用水应在制备后12小时内使用。 5.4 纯化水贮罐、输送管道应每周用双氧水消毒次;注射用水贮罐、输送管道应每周清洗,并用纯蒸汽水消毒一次。 6 工艺用水要求(见表1)
工艺用水管理规程
1.目的 加强对工艺用水质量的管理,确保工艺用水的制备和使用不对医疗器械产品质量造成影响。 2.范围 适用于本公司工艺用水的制备、检测、使用和设备维护。 3.职责 3.1.设备工程部负责工艺用水设备的维修。 3.2.生产部负责工艺用水的制备、使用及设备保养与维护。 3.3.质保部 3.3.1.负责工艺用水的取样、检测。 3.3.2.监督本规程的执行情况。 4.规程 4.1.定义 工艺用水是医疗器械产品实现过程中使用或接触的水的总称,以饮用水为源水,主要包括符合《中华人民共和国药典》规定的纯化水、注射用水和灭菌注射用水,还包括体外诊断试剂用纯化水、血液透析及相关治疗用水、分析实验室用水等。 工艺用水主要用于:可作为产品的组成成分;可用于试剂的配制;可用于零部件、半成品或外协件、成品、包装材料的清洁;可用于产品的检验;可用于洁净环境的清洁;可用于洁净室(区)内直接接触产品的工装、工位器具、设施设备的清洁;可用于洁净室(区)内工作服及人员的清洁等。 4.2.工艺用水的分类 根据《无菌医疗器具生产管理规范》YY0033-2000以及我公司生产的产品需要,我公司的工艺用水分为饮用水和纯化水两种。 4.3.工艺用水的水质要求 4.3.1.饮用水应符合《生活饮用水卫生标准》GB5749-2006的要求。 4.3.2.纯化水应符合《中国药典》(2015版)中纯化水的有关规定。 4.4.工艺用水的用途(具体见产品工艺规程) 4.4.1.饮用水:非洁净区所有生产工序用水、制备纯化水的水源。 4.4.2.纯化水:洁净区内设备、工装、工位器具、工作服的清洗;清洗液、消毒液和试剂的配制用水。
化工工艺管理制度
化工工艺管理制度 一、主题内容及适用范畴 本制度规定了化工工艺治理的内容要求和方法,适用于全厂化工生产活动中治理事项的治理。 二、化工工艺治理内容及要求 (一)化工操作人员对工艺文件(岗位操作法、岗位责任制等)熟练程度,要求达到工艺操作标准要求。 (二)化工操作人员对现场工艺流程熟练,要求达到工艺操作标准。 (三)化工操作人员对<<化工通用治理标准>>执行情形,要求符合标准。 (四)工艺记录报表、交接班记录填写情形是否按时、准确、整齐,保管妥善,符合原始记录治理标准。 (五)巡回检查制执行情形要求符合化工操作通用治理标准。 (六)工艺治理制度要求建立健全。 (七)工艺指标、定额消耗情形要求符合标准。 (八)工艺事故处理情形要求符合工艺事故治理标准。 (九)工艺台帐要求健全、完整。 (十)化工岗位清洁文明要求达到标准。 (十一)各单位化工工艺纪律执行情形要求直截了当与单位效益挂钩,执行经济责任制标准。 (十二)生产技术部负责每月五日前将上月化工工艺纪律执行情形考核 结果汇总上报。 三、化工工艺纪律检查方式及要求 (一)对化工艺纪律执行情形采取巡回检查。不定期抽查和定期全面检查三种方式。 (二)巡回检查由各化工车间主管生产工艺的副主任负责进行.每周至少一次,负责本车间范畴内所有化工岗位的检查,对不符合本标准要求的操作者有权禁止或停止其操作。
(三)不定期抽查由生产技术部负责进行,每月最少四次。检查范畴包括本单位所有化工岗位。对不符合本标准的操作人员有权停止其操作。 (四)定期全面检查由厂组织联合检查组负责进行,每季度一次。范畴包括所有化工岗位。对不符合本标准要求的操作人员有权停止其操作,并责令其所在单位进行批判教育。 (五)当班生产调度、生产班组长必须按点定时检查,生产调度随时抽查。对不符合本标准要求者应及时纠正或停止其操作。 (六)每次检查必须有检查纪录,作为执行经济责任制考核的依据。 开停车治理制度 为了加大开停车的打算性和严肃性,有效地增加生产时刻,提升开车效率,使全系统生产处于受控状态,做到清理和检修工作安全、及时、高效、完全,使各装置长周期、满负荷、连续、稳固运行,特制定复肥厂开停车治理制度。 一、复肥厂生产系统分为硫酸、磷酸过滤、浓缩、磷铵、一铵五个主统和氟钠、供电、供水、供汽(气)等辅助系统,除氟钠由磷酸车间按照每月的生产作业打算自主组织生产外,其它主辅系统的开停车,均纳入本制度之列。 二、打算开停车的治理制度 (一)辅助系统的开停车由调度室统一和谐和指挥,而主系统的开停车必须严格履行申请、审批程序。 (二)停车时刻在1小时之内,由当班班长电话报告调度室,并经当班
国家食品药品监督管理总局关于发布医疗器械工艺用水质量管理指南的通告年第号
国家食品药品监督管理总局关于发布医疗器械工艺用水质量管理指南的通告 (2016年第14号) 2016年01月29日为指导医疗器械生产企业做好工艺用水质量管理工作,提高工艺用水质量安全保证水平,根据《医疗器械生产监督管理办法》(国家食品药品监督管理总局令第7号)和《医疗器械生产质量管理规范》(国家食品药品监督管理总局公告2014年第64号)及相关附录,国家食品药品监督管理总局组织制定了《医疗器械工艺用水质量管理指南》,现予发布。 特此通告。 附件:医疗器械工艺用水质量管理指南 食品药品监管总局 2016年1月26日 医疗器械工艺用水质量管理指南
医疗器械生产企业应当按照《医疗器械生产质量管理规范》(国家食品药品监督管理总局公告2014年第64号)的要求,加强对工艺用水质量的管理,确保工艺用水的制备和使用不对医疗器械产品质量造成影响。 一、适用范围 本指南所指工艺用水是医疗器械产品实现过程中使用或接触的水的总称,以饮用水为源水,主要包括符合《中华人 标准的规定, 适应。 (三)应当确定工艺用水的传输形式,用量较大时应当通过管道输送至洁净室(区)的用水点。通过管道输送时,应当对工艺用水种类、流向进行标识。 (四)应当确保与工艺用水直接接触的储罐、输送管道的材质不对工艺用水造成污染和影响,设计安装方式应避免死角盲端,以防止微生物的滋生。
(五)应当对制水系统的安装、运行和性能等进行验证和确认,确保制水系统持续、稳定生产出符合标准、适合产品生产要求的工艺用水,并保存制水系统验证计划、方案、报告以及再确认等相关技术资料。 (六)应当保存制水系统的设计图纸、使用说明书、工艺用水制备流程图、技术文件等档案资料。 (七)应当确定工艺用水制备和检验的责任部门及岗位人员,岗位人员应当熟悉相关的法规,具备与岗位相适应的 录。 送管道等造成影响,并保存储罐、输送管道清洗消毒、验证等记录。 (十三)应当对制水系统进行定期维护。涉及需计量、校验的仪表、器具应当定期计量、校验,标识明显,并保存制水系统仪表、器具的计量、校验证书。委托制水系统厂家进行维护、清洗消毒的,应当与委托制水系统厂家签订协议,规定技术要求、质量要求等内容,明确双方所承担的质量责任,并保存相关记录。
工艺用水管理规程
目的:建立工艺用水的管理标准,明确规定工艺用水的管理内容。 范围:工艺用水的管理。 职责:质量管理部经理、生产管理部经理、工程设备部经理。 规程: 1水源卫生防护 1.1饮用水的管网不得和非饮用水的管网直接连接。 1.2饮用水、纯化水、注射用水等管道要避免穿过垃圾堆或毒物污染区。 1.3给水管道与污水管道交叉时,给水管道应铺设在污水管道上面,管外壁的净距不得小于0.4m,且不允许有接口重叠。与其它管道(煤气、电缆、其它液体)交叉时,其净距离不得小于0.15m。 1.4饮用水的清水池或水塔必须保证水的流动,避免死角,防止污染,便于清洗和透气。 1.5室内给水管配水出口不得被任何液体或杂质所淹没。 1.6室内给水管道不得铺设在排水沟、烟道或风道内,不得穿过大、小便槽(包括距槽0.5米以内的范围), 应设在排水管道上方。 1.7水箱设在便于维护、通风良好、不易结冻的地方,水箱应加盖,定期清洁。 1.8凡与水接触的给水设备、管道所用材料均不得污染水质。 2工艺用水:工艺用水水质按工艺要求确定,根据其使用目的灵活运用各种水处理技术,制出符合需要的工艺用水。 2.1 饮用水:来源为自来水,其水质必须符合国家生活饮用水水质标准GB5749-85《生活饮用水卫生标准》。饮用水可作为非无菌药品的设备、包装材料和器具的初洗用水和制备纯化水的水源。 2.1纯化水 2.2.1 定义:为饮用水经蒸馏法、离子交换法、反渗透法或其他适宜方法制备的水。其质量应符合中国药典纯化水项下的规定。 2.2.2 纯化水不含任何附加剂。可作为非无菌药品配料、洗瓶,注射剂、无菌制剂瓶子的初洗,制备注射用水水源。必要时亦用作非灭菌制剂用药材的提取溶剂。纯化水不得用于无菌滴眼剂的配制
工艺用水管理制度7
1目的 制订本公司工艺用水管理制度,加强工艺用水的水质监护工作,保障生产的正常进行。 2范围 适用于本公司工艺用水的管理。 3定义 工艺用水是指药品生产工艺中使用的水,包括:饮用水、纯化水、注射用水。纯化水:为蒸馏法、离子交换法、反渗透法或其它适宜的方法制得的供药用的水,不含任何附加剂。注射用水:为去离子水或蒸馏水经蒸馏所得的水。 3责任 3.1技术部门负责制订工艺用水的水质标准。 3.2生产车间制水岗位操作人员严格执行。 3.3车间工艺员、质监员负责监督与检查。 5内容 5.1工艺用水的制备 5.1.1饮用水由自来水公司供应。 5.1.2纯化水由生产车间制水岗位按《纯化水制备工艺规程》进行纯化水的生产。 5.1.3注射用水由生产车间制水岗位按《注射用水制备工艺规程》进行注射用水的生产。 5.2工艺用水的监测管理 由质管部制订《工艺用水监测管理规定》,各车间、质管部门按此规定进行MST新迈-07-00 第2页/共2页工艺用水
的监测管理。《工艺用水监测管理规定》应包括工艺用水的检测项目、取样点和检测周期。 5.3工艺用水的贮存和使用 531纯化水贮罐、循环管道所用材质应为无毒、耐腐蚀的优质低碳不锈钢;注射用水贮罐、循环管道所用材质应为 316L不锈钢。各管道的设计、安装应尽量避免死角、盲角;纯化水、注射用水贮罐的通气口应安装不脱落纤维的疏水性除菌滤器。 5.3.2纯化水采用室温循环保存;注射用水采用 65C以上保温循保存。 5.3.3各车间应按工艺要求正确选用工艺用水;作为工艺用水,纯化水应在制备后24小时内使用,注射用水应在制备后12小时内使用。 5.4纯化水贮罐、输送管道应每周用双氧水消毒一次;注射用水贮罐、输送管道应每周清洗,并用纯蒸汽水消毒一次。 6工艺用水要求(见表1) 表1
工艺用水管理规定
工艺用水管理规定 文稿归稿存档编号:[KKUY-KKIO69-OTM243-OLUI129-G00I-FDQS58-
文件编号: 工艺用水管理规定 1.0目的 明确规定工艺用水的监控和检查,保证工艺用水的质量。 2.0适用范围 适用于本公司工艺用水的制备、检测、使用和设备维护。 3.0职责 3.1生产采购部负责工艺用水的制备、使用及设备维护的管理。 3.2技术质量部负责工艺用水的检测。 4.0工作程序 4.1工艺用水的分类a.饮用水b.纯化水 4.2工艺用水的制备: 4.2.1由受过专业培训的人员按设备操作规程操作设备,按工艺制水要求进行制水。操作员需每天清洁设备和场地,保持制水室内卫生干净。 4.2.2工艺用水需通过管道输送至洁净区内的使用点,管道应为不锈钢或其它无毒材料制作。 4.3工艺用水及使用范围及用量配置 43.1根据生产工艺要求,对需要使用工艺用水的对象作如下表规定: 4.3.2工艺用水的用量在确定年最大生产能力方案时,按最大用水量和保险系数确定其制水设备能力的配置要求。 4.3.3生产采购部每年要根据现行的生产能力和用水设备的变化情况进行一次总用水量分析,若总用水量超出制水设备生产能力时,应补充制水设备或采取适应的措施,确保工艺用水能满足生产需求。
4.5取样方式和取样点 4.5.4取样所用器具和方式确保不能对检测指标产生影响,如盛放做微生物限度的器具必须先进行灭菌。 4.6工艺用水贮存要求 4.6.1饮用水不储存,直接使用市政自来水; 4.6.2纯化水在室温条件下可用不锈钢贮缸贮存,贮存时间不得超过36小时。 4.6.3购买的注射用水应在12小时内使用。 4.7管道贮罐消毒 4.7.1输送、贮存纯化水的管道和贮罐每3个月清洗、消毒1次。 消毒方法:用适量的2.5%次氯酸钠溶液注入纯化水贮罐中,按在线清洗消毒方式打开各管道阀门,足量循环消毒30min后排放,停机浸泡30分钟,如此反复3次停止,后还是冲洗,冲洗完毕后,将清洗水箱残液排完,注入符合RO 装置原水指标的水(即RO装置前级水),以清洗相同条件进行清洗消毒。或用预处理的低压冲洗条件来冲洗消毒。冲洗完毕后,按规定的运行方式进行低压冲洗和高压运行,最初产物排入地沟,到出水指标合格后。最后,在各使用点取样,按《中国药典》2010版附录纯化水规定的项目检验合格方可使用。4.8维护和保养 4.8.1制水设备的机械过滤器、活性炭过滤器应每周进行一次正洗、反洗,除去设备运行中截留的杂质。反洗时间约15分钟,正洗时间约5分钟。 4.8.2制水设备中的过滤器或滤膜应每3个月清洗一次,压差阻力太大导致产水量明显减少时 应进更换。 4.8.3RO膜应定期清洗(可视水质情况而定)。 4.8.4设备上的紫外线灯管累计使用不超过800小时应更换。 4.9操作人员应做好相关的监测记录和维护保养记录,检测人员应做好水质检测并保存好记录。 5.0相关记录
工艺用水管理制度
文件编号: 工艺用水管理规定 1.0目的 明确规定工艺用水的监控和检查,保证工艺用水的质量。 2.0 适用范围 适用于本公司工艺用水的制备、检测、使用和设备维护。 3.0 职责 3.1生产采购部负责工艺用水的制备、使用及设备维护的管理。 3.2 技术质量部负责工艺用水的检测。 4.0 工作程序 4.1 工艺用水的分类a.饮用水b.纯化水 4.2 工艺用水的制备: 4.2.1 由受过专业培训的人员按设备操作规程操作设备,按工艺制水要求进行 制水。操作员需每天清洁设备和场地,保持制水室内卫生干净。 4.2.2工艺用水需通过管道输送至洁净区内的使用点,管道应为不锈钢或其它无毒材料制作。 4.3 工艺用水及使用范围及用量配置 4 3.1根据生产工艺要求,对需要使用工艺用水的对象作如下表规定: 4.3.2 工艺用水的用量在确定年最大生产能力方案时,按最大用水量和保险系 数确定其制水设备能力的配置要求。 4.3.3 生产采购部每年要根据现行的生产能力和用水设备的变化情况进行一 次总用水量分析,若总用水量超出制水设备生产能力时,应补充制水设备或采取适应的措施,
确保工艺用水能满足生产需求。 4.4工艺用水的水质标准、监控方式、检测项目及要求、频次按下表规定: 4.5取样方式和取样点 4.5.1验证时对工艺用水的取样按其验证方案中的规定进行。 4.5.2纯化水日常监测时电导率采用在线测试或另行取样测试。 4.5.3全性能检测:分别从总出水口或总送水口、用点取样进行,各用水点轮流进行取样检测,每周进行1次。 4.5.4取样所用器具和方式确保不能对检测指标产生影响,如盛放做微生物限度的器具必须先进行灭菌。 4.6 工艺用水贮存要求 4.6.1饮用水不储存,直接使用市政自来水; 4.6.2纯化水在室温条件下可用不锈钢贮缸贮存,贮存时间不得超过36小时。 4.6.3购买的注射用水应在12小时内使用。 4.7管道贮罐消毒 4.7.1输送、贮存纯化水的管道和贮罐每3个月清洗、消毒1次。 消毒方法:用适量的2.5%次氯酸钠溶液注入纯化水贮罐中,按在线清洗消毒方式打开各管道阀门,足量循环消毒30min后排放,停机浸泡30分钟,如此反复3 次停止,后还是冲洗,冲洗完毕后,将清洗水箱残液排完,注入符合R0装置原 水指标的水(即RC装置前级水),以清洗相同条件进行清洗消毒。或用预处理的低压冲洗条件来冲洗消毒。冲洗完毕后,按规定的运行方式进行低压冲洗和高压运行,最初产物排入地沟,到出水指标合格后。最后,在各使用点取样,按《中国药典》2010版附录纯化水规定的项目检验合格方可使用。 4.8维护和保养 4.8.1制水设备的机械过滤器、活性炭过滤器应每周进行一次正洗、反洗,除去设备运行中截留的杂质。反洗时间约15分钟,正洗时间约5分钟。 4.8.2制水设备中的过滤器或滤膜应每3个月清洗一次,压差阻力太大导致产水量明显减少时
工艺用水管理规程(汇编)
规范工艺用水的质量监控及使用管理,确保生产用水符合GMP要求,保证药品质量。 2范围 适用于本公司饮用水、纯化水、注射用水(含纯蒸汽)的质量管理。 3职责 各车间制水岗位、质量管理部、生产制造部遵照执行。 4内容 4.1水源 饮用水水源:城市生活饮用水供水 纯化水水源:饮用水经软化 注射用水水源:纯化水 纯蒸汽水源:纯化水 4.2工艺用水质量标准 4.2.1饮用水应符合国家《生活饮用水卫生标准》的要求。 4.2.2纯化水、注射用水(含纯蒸汽)应符合《中华人民共和国药典》的质量标准。 4.3在线检测 4.3.1纯化水 制水操作人员每2小时检测一次储罐及混床出口或EDI出水口(二、三车间纯化水间)的电导率、酸碱度,每天检测一次总送水口和总回水口的电导率、酸碱度,每周检测一次活性炭过滤器后取样口的余氯,并做记录。二、三车间纯化水间在线监测原水电导率和温度、一级淡水电导率和温度、二级淡水电导率和温度、EDI出水电阻和温度,储罐总回水电导率。制水在岗人员每2小时记录一次总回水流量和循环泵运行状况。 4.3.2注射用水 a.制水岗位每2小时检测一次储罐及蒸馏水机出口的电导率、pH值,每天检测一次总送水口和总回水口的电导率、pH值,并做记录。一车间注射用水系统无TOC在线监测,加测易氧化物项,在线监测总回水口的温度;二、三车间注射用水系统在线监测原料水(纯化水)的电导率、温度,蒸馏水机出口的电导率和温度、总回水口的TOC、温度、电导率。制水在岗人员每2小时记录一次总回水流量和循环泵运行状况。 b.QA在当日用水前检测配液用水点细菌内毒素。 4.3.3纯蒸汽 在线监测原料水(纯化水)的电导率,纯蒸汽发生器的电导率和温度。制水岗位每天开机、关机时各一次检测纯蒸汽冷凝水的易氧化物和pH值。 4.4QC检测 4.4.1检测周期 4.4.1.1饮用水
007工艺用水管理制度
1 概述 明确规定工艺用水的监控和检查,保证工艺用水的质量。 2 范围 适用于本公司工艺用水的制备、检测和设备维护。 3 职责 3.1 生产技术科负责工艺用水的制备及设备维护的管理。 3.2 质管科负责工艺用水的检测。 4 管理内容和方法 4.1 工艺用水的分类a.饮用水 b.纯化水 c.注射用水 4.2 工艺用水的制备: 4.2.1由接受过专业培训的人员按设备操作规程操作设备,按制水工艺卡要求进行制水。操作员需每天清洁设备和场地,保持制水室内干净。 4.2.2工艺用水需通过管道输送至洁净区内的使用点,管道应为不锈钢或其他无毒材料制作。 4.3 工艺用水的使用范围及用量配置 4.3.2工艺用水的用量在确定年最大生产能力方案时,按最大用水量和保险系数确定其制水设备能力的配置要求。 4.3.3生产技术科每年需根据现行的生产能力和用水设备的变化情况进行一次总用
水量分析,若总用水量超出制水设备生产能力时,应补充制水设备或采取适应的措施,确保工艺用水能满足生产需求。 4.5 取样方式和取样点 4.5.1验证时对工艺用水的取样按其验证方案中的规定进行。 4.5.2纯化水日常监测时电导率采用在线测试,不另行取样测试。注射用水日常监测时从出水口取样进行。 4.5.3全性能检测分别从总出水口或总送水口、最远使用点取样进行,其他使用点轮流进行取样检测,每季度不少于1次。 4.5.4取样所用器具和方式应确保不能对检测指标产生影响,如盛放做微生物限度的器具必须先进行灭菌。 4.6 工艺用水贮存要求 4.6.1 饮用水不储存,直接使用市政自来水; 4.6.2纯化水在室温条件下可用不锈钢贮缸罐贮存,但最长贮存时间不超过24小时; 4.6.3注射用水临时制备在12小时内使用 4.7 管道贮罐消毒 4.7.1输送、贮存纯化水的管道和贮罐每周清洗、消毒1次。 消毒方法:a.关闭所有用水点,将贮罐内注入适量的纯化水,开启输送泵;b.将臭氧发生器启动,使产生出臭氧;c.当臭氧正常后,将通入臭氧的管道阀门打开,使
工艺规程管理制度4
l目的 规范本公司工艺规程的编制和修订方法、工艺规程的内容与格式,保证工 艺规程的贯彻执行。 2范围 适用于本公司各产品工艺规程的管理。 3责任 3.1生产技术部负责组织制订工艺规程管理制度,各相关部门遵照执行。 3.2公司主管副总经理负责审批产品工艺规程,并批准执行日期。 4定义 工艺规程是规定为生产一定数量产品所需原材料和包装材料的数量, 艺条件、操 以及工作要点、注意事项,包括生产过程质量控制的一个或一套文件;是对产品设计、处 方、工艺、标准、质量监控以及生产和包装全面规定性描述;是生产管理和质量监控的基准性文件,是制定批记录、批生产作业计划的重要依据。 5内容 5.1凡正式生产的产品都必须制订工艺规程,否则不能生产。 5.2编制工艺规程必须以法定标准和新产品审核文件为依据,按照GMP要求组织
编写,要科学地总结生产经验,采用先进技术,确保产品优质、指标先进、生产 安 全。 5.3产品工艺规程由技术部经理组织人员编写,由技术部经理审核,经主管副总经理批准后执行。工艺规程应有编写人、技术部经理、副总经理签字及批准执行 日 期。 5.4产品在试产前,应根据科研设计资料(包括引进技术)及现在情况编制试行 工艺规程,待生产正常后一年内在总结实践的基础上编制正式工艺规程。 5.5当遇到有工艺改革或变动时,工艺规程由技术部经理组织修订,其修订程序同制订程序。 5.6编制、修订工艺规程的若干规定 561各种工艺技术参数和技术经济定额的计量单位均按国家规定采用国际计 量单位。 5.6.2产品名称按中国药典或药监行政部门批准的法定名为标准。 5.6.3原材料名称一律采用化学名,适当附注商品名或其它通用别名。 5.6.4产品、中间体、原料分子量一律以最新国际原子量表计算,取两位小数。 5.7工艺规程的贯彻执行 5.7.1工艺规程批准后即正式颁布产并在批准的执行日期执行。 5.7.2工艺规程一经颁布,公司有关部门和员工必须严格执行,任何人不得擅自 改动和违反,对未经批准手续的不符合工艺规程的一切指示, 车间和工序操作人员应拒绝执行。 5.7.3各相关职能部门应提供工艺规程需求的设备、公用系统(电力、蒸汽、冷 冻、真空、压空、生产用水等)及合格的原材料和劳保设施、用品等一切工艺条
工艺用水监测管理规定
受控状态: 建立对工艺用水(饮用水、纯化水、注射用水)的质量控制监测项目、抽查频率及监测标准操作程序。 2范围 适用于本厂工艺用水的水质标准、水质监护的管理。 3责任 化验员、质监员、制水操作工。 4定义 工艺用水是指制剂生产中洗瓶、配料等工序,原料药生产的精制、洗涤等工序所用的水。按水质可分成饮用水、纯化水(即去离子水、蒸馏水)和注射用水。 5内容 5.1工艺用水系统监控工作由质监科负责。化验室定期对各种用水进行全项检测并出具检验报告书。纯化水、注射用水采用“批”管理,批号为6位阿拉伯 数字,前两位为年份、中间两位为月份,后两位为日期,如001008批纯化水表 示2000年10月8日生产的纯化水。 5.2车间制水工序操作员和质监科质监员按规定频次对各种水质进行必要的理 化项目测定,如:纯化水测定导电率(要求w 2卩S/cm)、氯离子等。 5.3取样点:制水点出口、用水点出口、贮水罐出口。 OS-太荔质-07-08-00 第2页/共2页
5.4取样检验时间和频次: 541节假日或停产一段时间后,开工之前应取样检验,符合规定后,方可使用 5.4.2发生异常情况或出现不符合规定的情况,应增加取样检验的频次。 5.4.3 一般正常生产情况下,饮用水每月检验部分项目一次,每年委托防疫站或自来水公司 全检一次;纯化水每2小时监测部分项目一次,每周全检一次。注射用水每2小时监测部分项目一次,每天全检一次。具体监控指标、检测频率和取样点见表: 5.5化验员和质监员、制水工应严格按各用水点水质的质量标准,取样操作规程和检验操作规程进行监测。 5.6水质检验记录,保存三年。 5.7水质检验报告书保存于质监科、制水部门。
工艺用水管理制度(新版)
When the lives of employees or national property are endangered, production activities are stopped to rectify and eliminate dangerous factors. (安全管理) 单位:___________________ 姓名:___________________ 日期:___________________ 工艺用水管理制度(新版)
工艺用水管理制度(新版) 导语:生产有了安全保障,才能持续、稳定发展。生产活动中事故层出不穷,生产势必陷于混乱、甚至瘫痪状态。当生产与安全发生矛盾、危及职工生命或国家财产时,生产活动停下来整治、消除危险因素以后,生产形势会变得更好。"安全第一" 的提法,决非把安全摆到生产之上;忽视安全自然是一种错误。 1.本厂采用去离子水法制得纯化水,即为去离子水。 2.制水设备由清洁工负责制备、清洁保养,由化验室负责再生、检测。 3.厂化验室负责对制出的去离子说进行每班一次的检验,并有记录。 4.去离子水使用范围包括:清洁工作服、鞋、帽,储水器清洗、洁净室、工作台面清洗、净化区的工位器具,消毒液配置等。 5.非洁净区工位器具、储水器清洗、注塑机的冷却用饮用水即可,无需用去离子水。 6.用去离子水制得的去离子水不得用在清洗与生产无关物品或浪费。 7.储水器应每隔本个月由清洁工进行消毒。其消毒规程为:1、先用去离子水清洗;2、冲干;3、用1%甲醛溶液消毒;4、用去离子说冲洗;5、水质检测。
8.制水量应能满足生产需要,并要有制水记录。工艺用水量分布情况 序号 用水项目 用水量㎏/日 备注 1 洗工作服、鞋、帽 280 去离子水 2 工位器具清洗 180 去离子水 3 人员洗手 50 去离子水
工艺用水管理制度
文件编号: 工艺用水管理规定
1.0 目的 明确规定工艺用水的监控和检查,保证工艺用水的质量。 2.0 适用范围 适用于本公司工艺用水的制备、检测、使用和设备维护。 3.0 职责 3.1生产采购部负责工艺用水的制备、使用及设备维护的管理。 3.2 技术质量部负责工艺用水的检测。 4.0 工作程序 4.1 工艺用水的分类a.饮用水 b.纯化水 4.2 工艺用水的制备: 4.2.1 由受过专业培训的人员按设备操作规程操作设备,按工艺制水要求进行制水。操作员需每天清洁设备和场地,保持制水室内卫生干净。 4.2.2工艺用水需通过管道输送至洁净区内的使用点,管道应为不锈钢或其它无毒材料制作。 4.3 工艺用水及使用范围及用量配置 4 3.1根据生产工艺要求,对需要使用工艺用水的对象作如下表规定: 4.3.2工艺用水的用量在确定年最大生产能力方案时,按最大用水量和保险系数确定其制水设备能力的配置要求。 4.3.3 生产采购部每年要根据现行的生产能力和用水设备的变化情况进行一次总用水量分析,若总用水量超出制水设备生产能力时,应补充制水设备或采取适应的措施,确保工艺用水能满足生产需求。
4.5 取样方式和取样点 4.5.1验证时对工艺用水的取样按其验证方案中的规定进行。 4.5.2纯化水日常监测时电导率采用在线测试或另行取样测试。 4.5.3全性能检测:分别从总出水口或总送水口、用点取样进行,各用水点轮流进行取样检测,每周进行1次。 4.5.4取样所用器具和方式确保不能对检测指标产生影响,如盛放做微生物限度的器具必须先进行灭菌。 4.6 工艺用水贮存要求 4.6.1饮用水不储存,直接使用市政自来水; 4.6.2纯化水在室温条件下可用不锈钢贮缸贮存,贮存时间不得超过36小时。 4.6.3购买的注射用水应在12小时内使用。 4.7 管道贮罐消毒 4.7.1输送、贮存纯化水的管道和贮罐每3个月清洗、消毒1次。 消毒方法:用适量的 2.5%次氯酸钠溶液注入纯化水贮罐中,按在线清洗消毒方式打开各管道阀门,足量循环消毒30min后排放,停机浸泡30分钟,如此反复3次停止,后还是冲洗,冲洗完毕后,将清洗水箱残液排完,注入符合RO装置原水指标的水(即RO装置前级水),以清洗相同条件进行清洗消毒。或用预处理的低压冲洗条件来冲洗消毒。冲洗完毕后,按规定的运行方式进行低压冲洗和高压运行,最初产物排入地沟,到出水指标合格后。最后,在各使用点取样,按《中国药典》2010版附录纯化水规定的项目检验合格方可使用。 4.8 维护和保养 4.8.1制水设备的机械过滤器、活性炭过滤器应每周进行一次正洗、反洗,除去设备运行中截留的杂质。反洗时间约15分钟,正洗时间约5分钟。 4.8.2制水设备中的过滤器或滤膜应每3个月清洗一次,压差阻力太大导致产水量明显减少时 应进更换。 4.8.3 RO膜应定期清洗(可视水质情况而定)。 4.8.4设备上的紫外线灯管累计使用不超过800小时应更换。
GMP工艺用水管理制度
目的:建立工艺用水日常监测和使用管理程序,确保工艺用水水质符合药品生产要求。 范围:公司内的饮用水、纯化水。 职责:生产部、质量部、生产车间、QA检查员。 内容: 1.工艺用水主要指制剂生产中容器清洗、配料等工序所使用的水。按水质可分成饮用水、纯化水和注射用水,本公司的工艺用水主要指的是饮用水和纯化水。 2.饮用水的管理 2.1 饮用水的水质应符合卫生部生活饮用水的标准。 2.2 饮用水应定期检测,每月检测部分项目一次。 2.3 饮用水的使用 2.3.1 药材的清洗、浸润、提取 2.3.2 非洁净区生产工具、容器、设备的清洗,洁净区生产工具、容器、设备的初洗。 3.纯化水的管理 3.1 纯化水系统安装竣工使用前应全面验证,使用一定周期后要进行再验证。 3.2 输送纯化水的管道应采用无毒、耐腐蚀、优质不锈钢管道,其设计安装应避免死角。 3.3 纯化水室温下采用无毒、耐腐蚀的不锈钢罐贮存,其贮存的时间不超过24小时。贮罐的通气口应安装不脱落纤维的蔬水性除菌
滤过器。 3.4 纯化水应符合中国药典2000年版标准 3.5 纯化水的使用 用于洁净区设备、生产工具的最终洗涤 3.6 纯化水的监控 3.6.1 纯化水开始制备时,应检查Cl-、电导率、PH值、NH4等,符合要求后,再经紫外杀菌进入纯水储罐中,制备过程中每隔2小时检查一次电导率、PH和NH4+值。 3.6.2 纯化水制水系统的出水口每周应检查全部项目一次。 3.6.3 设立纯水储罐的车间每月对纯水进水口检查纯化水全部项目一次。 3.7 纯化水储罐、管道的清洗消毒 3.7.1 每星期用流通蒸汽对贮罐、管道消毒一次。 3.7.2 每三月对纯化水储罐、管道清洗消毒一次。
工艺用水日常监测管理规程
工艺用水日常监测管理制度 目的:建立工艺用水日常监测管理规程。 范围:适用于全厂工艺用水的监测管理。 责任:制水操作人、QA人员负责实施,QA经理负责管理。 内容: 1.工艺用水主要是指制药生产中配料等工序、原料药的精制、洗涤等工序所用的水。 按水质不同分为饮用水、纯化水、注射用水等。各工序应根据工艺要求制订各自的用水标准,按规定使用。 2.制药工艺用水要求: 类别用途水质要求 (1)非无菌药品的设备、器具应符合卫生部生活用水 饮用水和包装材料的初洗标准GB5749—2006(2)制备纯水的水源 (1)非无菌药品的配料洗瓶 (2)注射剂、无菌冲洗剂瓶子 初洗 纯化水(3)非无菌原料药的精制应符合企业内控标准及现行版中国(4)制备注射用水的水源,药典标准 (用于配料和原料药精制时, 应控制杂菌数) 注射(1)胶塞、浓稀配罐、玻瓶精洗、容 器具及管道的最终洗涤;应符合企业内控标准及现行版(2)注射剂的配制;中国药典标准 用水 3.工艺用水的制备 3.1饮用水是自来水公司供应的符合饮用水标准的自来水。 3.2纯化水是以饮用水为水源,经蒸馏法、离子交换法,反渗透法后或其他适宜的方法制得供药用的水,不含任何附加剂。 3.3 注射用水以纯化水为水源,经蒸馏法制备的制药用水;水质必须符合《中国药典》 注射用水质量标准。 4.质量保证部QA人员应对生产工艺用水进行质量监控。 4.1一般饮用水需当地环保局或防疫站一年全检一次。每月对饮用水应按内控标准自
行检测一次。 4.2制水的部门要及时请验。 4.3由QA人员负责每周对纯化水进行取样,并将样品送交质量控制部QC人员进行全 项检测。 4.4工艺用水的检测项目及检测频次: 4.4.1纯化水 每2个小时检测一次:由操作工对总出水口进行电导率、酸碱度检测。 每周一次:由质量保证部对总送水口、总回水口、贮水罐及各使用点取样,送QC 人员全检,按《中国药典》2010年版二部“纯化水”项下项目检验。 细菌、霉菌和酵母菌总数:应符合有关规定。 4.4.2 QA人员每日检查一次制水记录,检查操作工是否按操作规程对水质进行检测。 发现水质异常立即采取措施。 4.4.3注射用水 4.4.3.1水质维护: A.注射用水系统必须经过验证合格后,方可投入使用,并进行严格的变更控制。 B.注射用水系统正常情况每年进行一次再验证,以确认验证状态是否漂移。 C.注射用水系统操作人员进行定期的清洗、消毒及设备维护等操作。 4.4.3.2水质监测: A 注射用水日常监测频次及检查项目: B.质量检验中心将检验结果交质量保证部,并由质量保证部在各用水点贴绿色合格 签,方可使用。 C.检验结果不符合要求,立即执行“偏差管理制度”,由质量保证部会同相关部门
工艺用水管理规程
工艺用水管理规程 1.目的:建立工艺用水管理制度,确保工艺用水质量符合规定。 2.适用范围:本公司所有的工艺用水。 3.责任人:质量技术部、生产供应部、工程设备管理中心、工艺用水的制水、使用、检测相关人员。 4.内容: 4.1工艺用水分类 4.1.1工艺用水是指制剂生产中容器清洗、配料等工序以及原料药生产中的精制、洗涤等工序所用的水。 4.1.2按水质分为饮用水、纯化水。 4.1.3本公司工艺用水为饮用水、纯化水。 4.2工艺用水的定义及适用范围 4.2.1饮用水是指经过处理、直接供给人体饮用的水;饮用水水质应符合卫生部生活饮用水标准(GB/T5750-2006); 4.2.2纯化水为反渗透法制得供药用的水,不含任何附加剂。水质应符合《中国药典2015年版二部》纯化水标准;纯化水可作为药品生产用水。 4.3纯化水贮存与输送: 4.3.1纯化水在室温下用优质不锈钢罐密封循环贮存,循环贮存周期不宜大于72小时。 4.3.2纯化水贮存在优质304不锈钢贮罐中,贮罐必须密闭,贮罐通气口应安装不脱落纤维的疏水性除菌过滤装置。 4.3.3输送纯化水的管道,管件,阀门应采用优质低碳不锈钢,并尽量减少支管和阀门,分配管线宜采用环形干线,防止死角滞留。 4.4水质监测 4.4.1饮用水每年送岳阳市城市水质监测站或岳阳市食品药品检验所作一次全检。 4.4.2公司每半年对饮用水作检测一次PH值、混浊度、总硬度、微生物检查。 4.4.3纯化水监测 纯化水制水工序在线监测一级、二级电导率、回水流速、回水电导率、酸碱度、并在纯化水制水间配备离线电导率检测仪,检测纯化水电导率,且每二小时做一次监测记录。 正常生产情况下,各使用点每一月轮流取样全检一次,纯化水贮罐、总送水口、总回水口每一周取样全检一次。 纯化水系统停用周期:需停一周以上才能停运。停运前纯化水循环系统里的纯化水需排净。
