硝酸钾溶解热数据处理
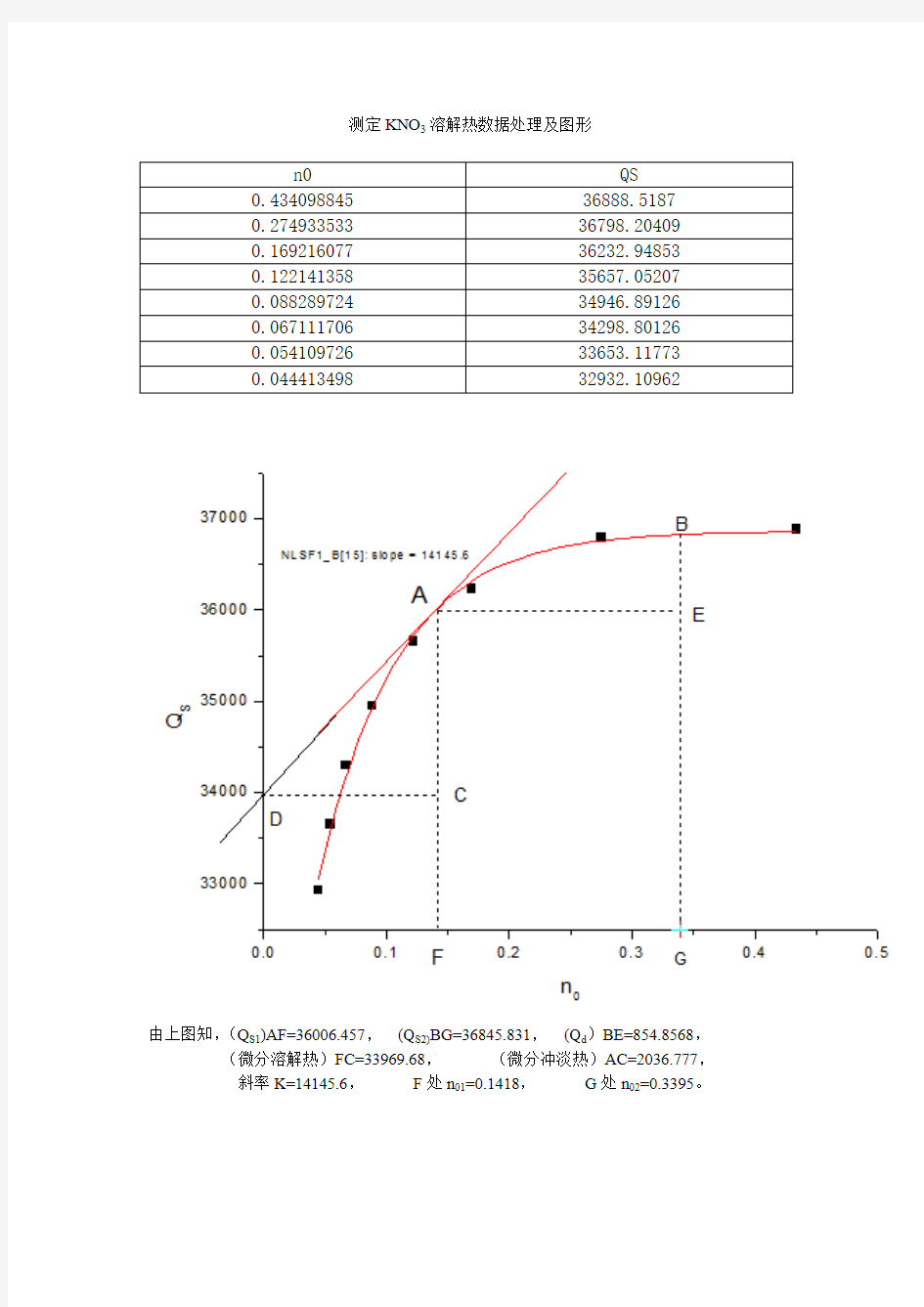
测定KNO3溶解热数据处理及图形
n0 QS
0.434098845 36888.5187
0.274933533 36798.20409
0.169216077 36232.94853
0.122141358 35657.05207
0.088289724 34946.89126
0.067111706 34298.80126
0.054109726 33653.11773
0.044413498 32932.10962
由上图知,(Q S1)AF=36006.457,(Q S2)BG=36845.831,(Q d)BE=854.8568,(微分溶解热)FC=33969.68,(微分冲淡热)AC=2036.777,
斜率K=14145.6,F处n01=0.1418,G处n02=0.3395。
溶解度的测定
硝酸钾溶解度得测定(方法1:结晶析出法) 实验原理: 先设计好不同溶质与溶剂得量,称量、混合、加热、搅拌使其溶解,降温并用温度计分别测定其开始析出晶体时得温度,即所得溶液为该温度下得饱与溶液,计算该温度下得溶解度。实验用品: 托盘天平(J0160,200g,0.2g),烧杯(J6124),大试管(J6104),玻璃棒(J6453),温度计(J6071,量程0~100℃),酒精灯(J6201),量筒(J6001,10ml),方座支架(J1102,带铁圈),石棉网(J6432),药匙(J6442),试管刷(J6471),硝酸钾(化学纯),蒸馏水。 实验步骤: 一、检查实验用品就是否齐全、完好。 二、硝酸钾得称取与溶解。 1、用托盘天平分别准确称取硝酸钾3.5g、1.5g、1.5g、2.0g、2.5g,称量过程详见分组实验三得步骤二。将称好得5份硝酸钾放在实验台上,并做标记。 2.在一支大试管中加入上面称取得3.5g硝酸钾。 3.用量筒准确量取10.0m1蒸馏水,加入大试管中。 4.在水浴中加热大试管,边加热边搅拌,至硝酸钾完全溶解(水浴温度不要太高,以刚好使硝酸钾溶解为宜,否则会使下一步结晶析出操作耗时过长) 三、硝酸钾得结晶。 1.自水浴中取出大试管,插入一支干净得温度计,用玻璃棒轻轻搅拌并摩擦试管壁,同时观察温度计得读数。当刚开始有晶体析出时,立即记下此时得温度t1,并填入下表中。 2.把试管再放入水浴中加热,使晶体全部溶解,然后重复两次上述实验步骤得操作,分别测定开始析出晶体时得温度t2、t3。将读数填入表格。 四、溶解度曲线得绘制。 1.依次向试管中再加入1.5g、1.5g、2.0g、2.5g硝酸钾(使试管中依次共有硝酸钾5.0g、6.5g、8.5g、11.0g),每次加入硝酸钾后都重复溶解、结晶实验步骤得操作,并将晶体开始析出时得温度读数填人表格。
溶解度的测定
硝酸钾溶解度的测定(方法1:结晶析出法)实验原理: 先设计好不同溶质和溶剂的量,称量、混合、加热、搅拌使其溶解,降温并用温度计分别测定其开始析出晶体时的温度,即所得溶液为该温度下的饱和溶液,计算该温度下的溶解度。 实验用品: 托盘天平(J0160,200g,0.2g),烧杯(J6124),大试管(J6104),玻璃棒(J6453),温度计(J6071,量程0~100℃),酒精灯(J6201),量筒(J6001,10ml),方座支架(J1102,带铁圈),石棉网(J6432),药匙(J6442),试管刷(J6471),硝酸钾(化学纯),蒸馏水。 实验步骤: 一、检查实验用品是否齐全、完好。 二、硝酸钾的称取和溶解。 1. 用托盘天平分别准确称取硝酸钾3.5g、1.5g、1.5g、 2.0g、 2.5g,称量过程详见分组实验三的步骤二。将称好的5份硝酸钾放在实验台上,并做标记。 2.在一支大试管中加入上面称取的3.5g硝酸钾。 3.用量筒准确量取10.0m1蒸馏水,加入大试管中。 4.在水浴中加热大试管,边加热边搅拌,至硝酸钾完全溶解(水浴温度不要太高,以刚好使硝酸钾溶解为宜,否则会使下一步结晶析出操作耗时过长) 三、硝酸钾的结晶。 1.自水浴中取出大试管,插入一支干净的温度计,用玻璃棒轻轻搅拌并摩擦试管壁,同时观察温度计的读数。当刚开始有晶体析出时,立即记下此时的温度t1,并填入下表中。
2.把试管再放入水浴中加热,使晶体全部溶解,然后重复两次上述实验步骤的操作,分别测定开始析出晶体时的温度t2、t3。将读数填入表格。 四、溶解度曲线的绘制。 1.依次向试管中再加入1.5g、1.5g、2.0g、2.5g硝酸钾(使试管中依次共有硝酸钾 5.0g、6.5g、8.5g、11.0g),每次加入硝酸钾后都重复溶解、结晶实验步骤的操作,并将晶体开始析出时的温度读数填人表格。 2.根据所得数据,以温度为横坐标,溶解度为纵坐标,绘制溶解度曲线图。 五、整理实验用品。 1.用试管刷清洗玻璃仪器。 2.整理实验用品,恢复实验前的摆放位置。 注意事项: 1.为了使测量结果准确,称取硝酸钾晶体的质量和量取倒入试管的蒸馏水的体积应尽量准确。 2.水浴加热时,烧杯里的水面不能低于试管里的液面。温度计应插在溶液的中部,使所示的温度具有代表性。 3.使试管里的液体升温时应采用水浴加热,而不能用酒精灯直接加热。
溶解热的测定实验报告
溶解热测定 姓名 学号 班级 实验日期 1 实验目的 (1)了解电热补偿法测定热效应的基本原理。 (2)用电热补偿法测定硝酸钾在水中的积分溶解热,通过计算或作图求出硝酸钾在水中的微分溶解热、积分溶解热和微分冲淡热。 (3)掌握用微机采集数据、处理数据的实验方法和实验技术。 2 实验原理 溶解热:恒温恒压下,物质的量为2n 的溶质溶于物质的量为1n 的溶剂(或溶于某浓度溶液)中产生的热效应,用Q 表示。 积分溶解热:恒温恒压下,1mol 溶质溶解于一定量的溶剂中形成一定浓度的溶液,整个过程产生的热效应。用s Q 表示。 微分溶解热:恒温恒压下,1mol 溶质溶于某一确定浓度的无限量的溶液中产生的热效应,以1 2n n Q ???? ????表示。 冲淡热:恒温恒压下,一定量的溶剂A 加到某浓度的溶液使之稀释所产生的热效应。 积分冲淡热:恒温恒压下,在含有1mol 溶质的溶液中加入一定量的溶剂,使之稀释成另一浓度的溶液的过程中产生的热效应,以d Q 表示。 微分冲淡热:恒温恒压下,1mol 溶剂加入到某一浓度无限量的溶液中所发生的热效应, 以21n n Q ???? ????或2 0n s n Q ???? ????表示。 它们之间关系可表示为: s Q n Q =2 令021n n n = 2 1002n s n s n Q n n Q Q ???? ????+???? ????= ()()0201n s n s d Q Q Q -= 积分溶解热s Q 可由实验测得,其他三种热效应则可通过0n Q s -曲线求得,曲线某点的切线的斜率为该浓度下的摩尔微分稀释热,切线与纵坐标的截距,为该浓度下的摩尔微分溶解热 (即OC )。显然,图中A 点的摩尔溶解热与B 点的摩尔溶解热之差为该过程的摩尔积分稀释热(即BE )。
溶解热测定
实验七 溶解热的测定 一、实验目的 1.掌握采用电热补偿法测定热效应的基本原理。 2.用电热补偿法测定硝酸钾在水中的积分溶解热,并用作图法求出硝酸钾在水中的微分溶解热、积分稀释热和微分稀释热。 3.掌握溶解热测定仪器的使用。 二、实验原理 物质溶解过程所产生的热效应称为溶解热,可分为积分溶解热和微分溶解热两种。积分溶解热是指定温定压下把1mol 物质溶解在n 0mol 溶剂中时所产生的热效应。由于在溶解过程中溶液浓度不断改变,因此又称为变浓溶解热,以△sol H 表示。微分溶解热是指在定温定压下把1mol 物质溶解在无限量某一定浓度溶液中所产生的热效应,以表示.在溶解过程中浓度可视为不变,因此又称为定浓度 溶解热,以0 ,,)(n p T sol n H ???表示,即定温、定压、定溶剂状态下,由微小的溶质增 量所引起的热量变化。 稀释热是指溶剂添加到溶液中,使溶液稀释过程中的热效应,又称为冲淡热。它也有积分(变浓)稀释热和微分(定浓)稀释热两种。积分稀释热是指在定温定压下把原为含1mol 溶质和n 01mol 溶剂的溶液冲淡到含n 02mol 溶剂时的热效应,它为两浓度的积分溶解热之差。微分稀释热是指将1mol 溶剂加到某一浓度的无 限量溶液中所产生的热效应,以n p T sol n H ,,0 )(???表示,即定温、定压、定溶质状态 下,由微小的溶剂增量所引起的热量变化。 积分溶解热的大小与浓度有关,但不 具有线性关系。通过实验测定,可绘制出一条积分溶解热△sol H 与相对于1mol 溶质的溶剂量n 0之间的关系曲线,如图1所示,其他三种热效应由△sol H~n 0曲线求得。 设纯溶剂、纯溶质的摩尔焓分别为H m1和H m2,溶液中溶剂和溶质的偏摩尔焓分别为H 1和H 2,对于由n 1mol 溶剂和n 2mol 溶质组成的体系,在溶质和溶剂未混合前,体系总焓为: 图1
初三化学 溶解度、结晶经典习题精编(附答案)
初三化学溶解度、结晶经典习题精编(附答案) 一、选择题 1、下表提供了硝酸钾固体在不同温度时的溶解度,则下列说法正确的是()温度/℃020406080硝酸钾的溶解度/g 13、3 31、6 63、9110169 A、在20℃时,向100 g水中加入40 g硝酸钾固体,能够得到140 g溶液 B、随着溶液温度不断升高,硝酸钾固体的溶解度呈现出不断减少的趋势 C、60℃时210 g硝酸钾饱和溶液降温到20℃,能析出 78、4 g硝酸钾晶体 D、在40℃时硝酸钾的饱和溶液中加入少量氯化钠固体,氯化钠不会溶解 2、下面是硝酸钾和氯化钠的溶解度曲线、下列说法中,不正确的是() A、硝酸钾的溶解度受温度的影响比氯化钠大 B、t1℃时,100 g硝酸钾饱和溶液中含有20 g 硝酸钾 C、t2℃时,氯化钠饱和溶液与硝酸钾饱和溶液中溶质的质量分数相同
D、温度高于t2℃时,硝酸钾的溶解度大于氯化钠的溶解度 3、已知氯化钠、硝酸钾在不同温度时的溶解度如下表:温度/℃102030405060溶解度/g氯化钠 35、8 36、0 36、3 36、6 37、0 37、3硝酸钾 20、9 31、6 45、8 63、9 85、5110依据上表数据和溶解度曲线判断,下列说法错误的是() A、能表示硝酸钾和氯化钠的溶解度曲线分别是甲和乙 B、t1℃时,氯化钠和硝酸钾的溶解度相等,在 36、0 g 至 36、3 g 之间 C、t2℃时,将接近饱和的丙物质的溶液升高温度,可使其变成饱和溶液 D、氯化钠中混有少量的硝酸钾,可采用降温结晶的方法提纯
说法不正确的是()温度/℃102030405060溶解度/g氯化钠 35、8 36、0 36、3 36、6 37、0 37、3硝酸钾 20、9 31、6 45、8 63、9 85、5110 A、氯化钠和硝酸钾的溶解度曲线在20℃~30℃温度范围内会相交 B、在20℃时,向68g饱和氯化钠溶液中加入32g水,此时溶液中溶质的质量分数为18% C、分别将20℃时一定质量的饱和氯化钠溶液、饱和硝酸钾溶液升温至40℃,此时硝酸钾溶液中溶质的质量分数大于氯化钠溶液 D、从含有少量氯化钠的饱和硝酸钾溶液中得到较多的硝酸钾晶体,可采用冷却硝酸钾热饱和溶液的方法
物理化学实验报告_溶解热的测定
物理化学实验报告 溶解热的测定 实验时间:2018年4月日 姓名:刘双 班级: 学号: 1.实验目的 (1)了解电热补偿法测量热效应的基本原理。 (2)用电热补偿法测定硝酸钾在水中的积分溶解热,通过计算或者作图求出硝酸钾在水中的微分溶解热、积分冲淡热和微分冲淡热。 (3)掌握微机采集数据、处理数据的实验方法和实验技术。 2.实验原理 物质溶解于溶剂过程的热效应称为溶解热,物质溶解过程包括晶体点阵的破坏、离子或分子的溶剂化、分子电离(对电解质而言)等过程,这些过程热效应的代数和就是溶解过程的热效应,溶解热包括积分(或变浓)溶解热和微分(或定浓)溶解热。把溶剂加到溶液中使之稀释,其热效应称为冲淡热。包括积分(或变浓)冲淡热和微分(或定浓)冲淡热。 溶解热Q:在恒温、恒压下,物质的量为n2的溶质溶于物质的量为n1的溶剂(或溶于某浓度的溶液)中产生的热效应。 积分溶解热Qs:在恒温、恒压下,1mol溶质溶于物质的量为n1的溶剂中产生的热效应。 微分溶解热(ee ee2)e 1 :在恒温、恒压下,1mol溶质溶于某一确定浓度的无限量的溶液中 的热效应。 冲淡热:在恒温、恒压下,物质的量为n1的溶剂加入到某浓度的溶液中产生的热效应。 积分冲淡热Q d:在恒温、恒压下,把原含1mol溶质和n02mol溶剂的溶液冲淡到含溶剂为n01mol时的热效应,为某两浓度的积分溶解热之差。 微分冲淡热(ee ee1) e2 或(eee ee0 ) e2 :在恒温、恒压下,1mol溶剂加入到某一确定浓度的无 限量的溶液中产生的热效应。 它们之间的关系可表示为:
dQ=(ee ee1) e2 ee1+( ee ee2 ) e1 ee2 上式在比值e1 e2 恒定下积分,得: e=(ee ee1 ) e2 e1+( ee ee2 ) e1 e2 ee2=ee,令:e1 n2 =e0,则有: ( ?Q ?n1 )=[ ?(n2Q s ?(n2n0) ]=( ?Q s ?n0 ) Q d=(ee)e01?(ee)e02 其中积分溶解热ee可以直接由实验测定,其他三种可以由ee?e0曲线求得。 欲求溶解过程中的各种热效应,应先测量各种浓度下的的积分溶解热。可采用累加的方法,先在纯溶剂中加入溶质,测出热效应,然后再这溶液中再加入溶质,测出热效应,根据先后加入的溶质的总量可计算出n0,而各次热效应总和即为该浓度下的溶解热。本实验测量硝酸钾溶解在水中的溶解热,是一个溶解过程中温度随反应的进行而降低的吸热反应,故采用电热补偿法测定。先测定体系的初始温度T,当反应进行后温度不断降低时,由电加热法使体系复原到起始温度,根据所耗电能求出热效应Q。 3.仪器和试剂 反应热测量数据采集接口装置: NDRH-1型,温度测量范围0~40℃,温度测量分辨率0.001℃,电压测量范围0~20V,电压测量分辨率0.01V,电流测量范围0~2A,电流测量分辨率0.01A。 精密稳流电源:YP-2B型。 微机、打印机。 量热计(包括杜瓦瓶,搅拌器,加热器,搅拌子)。 称量瓶8只,毛笔,研钵。 硝酸钾(A.R.) 4.实验操作 (1)取8个称量瓶,分别编号。 (2)取KNO3于研钵中,研磨充分。 (3)分别称量约 2.5、1.5、2.5、3.0、3.5、4.0、4.0、4.5g 研磨后的硝酸钾,放入 8 个称量瓶中,并精确称量瓶子与药品的总质量。记录下所称量的数据。
50℃时硝酸钾的溶解度
试题专页注册登录 揭秘试题背后的真相题文答案考点梳理举一反三 当前位置:魔方格>化学>固体溶解度>某实验室欲配制一定溶质质量分数的KNO3溶液,现实验室只有含少量.. 题文答案 题文 某实验室欲配制一定溶质质量分数的KNO3溶液,现实验室只有含少量NaCl的KNO3固体药品. (1)如图所示为KNO3和NaCl的溶解度曲线,50℃时,将85.5g固体药品溶于100g水中,得到的是KNO3的______溶液(填“饱和”或“不饱和”). (2)将KNO3提纯的方法是______. (3)小明用提纯后的KNO3固体配制1000g溶质质量分数为5%的KNO3溶液,其操作步骤是:计算、______、量取、溶解.经检测,小明所配溶液中KNO3溶质质量分数偏小,其原因可能是______. ①KNO3固体仍然不纯;②溶解前,烧杯中有水;③量取水时,俯视读数;④装瓶时,有少量溶液洒出. 魔方格 题型:填空题难度:中档来源:不详 答案(找作业答案--->>上魔方格) (1)50℃时硝酸钾的溶解度为85.5g即50℃时,将85.5g硝酸钾溶于100g水中正好达到饱和,而85.5g固体药品中由于含有少量氯化钠,所以硝酸钾的质量要小于85.5g,所以50℃时,将85.5g固体药品溶于100g水中,得到的是KNO3的不饱和溶液;故填:不饱和; (2)硝酸钾的溶解度受温度影响变化较大,所以将KNO3提纯的方法是降温结晶或冷却热的饱和溶液;故填:降温结晶或冷却热的饱和溶液; (3)配制溶液的步骤为:计算、称量、量取、溶解;KNO3固体仍然不纯会导致所配溶液中KNO3溶质质量分数偏小;②溶解前,烧杯中有水,说明说多了,也会导致所配溶液中KNO3溶质质量分数偏小;③用量筒量取水时俯视读数,量取到的液体偏少,即配得的质量分数会偏大;④装瓶时,有少量溶液洒出,不影响所配溶液中KNO3溶质质量分数.故填:称量;①②
溶解热的测定.
学号:201214140130 基础物理化学实验报告 实验名称:溶解热的测定 12级药学1班 实验人姓名:李楚芳 同组人姓名:罗媛兰婷 指导老师:李旭老师 实验日期:2014—06—13 湘南学院化学与生命科学系 一、实验目的: 1.了解ZR-2J溶解热测定仪的原理、构造和使用方法,掌握溶解热的测定技术。 2.懂得积分溶解热的定义及其在化学热力学运算中的作用。 二、主要实验原理,实验所用定律、公式以及有关文献数据: 1.在热化学中,关于溶解过程的热效应,引进下列几个基本概念。 溶解热在恒温恒压下,n2摩尔溶质溶于n1摩尔溶剂(或溶于某浓度的溶液)中产生的热效应,用Q表示,溶解热可分为积分(或称变浓)溶解热和微分(或称定浓)溶解热。 积分溶解热在恒温恒压下,一摩尔溶质溶于n0摩尔溶剂中产生的热效应,用Q s表示。
微分溶解热在恒温恒压下,一摩尔溶质溶于某一确定浓度的无限量的溶液 中产生的热效应,以表示,简写为。 2.积分溶解热(Q S)可由实验直接测定,其它三种热效应则通过Q S—n0曲线求得。 设纯溶剂和纯溶质的摩尔焓分别为H m(1)和H m(2),当溶质溶解于溶剂 变成溶液后,在溶液中溶剂和溶质的偏摩尔焓分别为H1 ,m 和H2 ,m ,对于由n1 摩尔溶剂和n2摩尔溶质组成的体系,在溶解前体系总焓为H。 H=n1H m(1)+n2H m(2) (1) 设溶液的焓为H′, H′=n1H1,m+n2H2,m (2) 因此溶解过程热效应Q为 Q =Δmix H=H - H= n1[H1。m –H m(1)]+n2[H2,m–H m(2)] =n1Δmix H m(1)+n2Δmix H m(2) (3) 式中,Δmix H m (1)为微分冲淡热,Δmix H m (2)为微分溶解热。根据上述定义,积分溶解热Q S为 (4) 在恒压条件下,Q=Δmix H,对Q进行全微分 (5) 上式在比值恒定下积分,得 (6)
实验四 溶解热的测定
实验四溶解热的测定 一、实验目的 1.用电热补偿法测定KNO3在不同浓度水溶液中的积分溶解热。 2.用作图法求KNO3在水中的微分冲淡热、积分冲淡热和微分溶解热。 二、预习要求 1.复习溶解过程热效应的几个基本概念。 2.掌握电热补偿法测定热效应的基本原理。 3.了解如何从实验所得数据求KNO3的积分溶解热及其它三种热效应。 4.了解影响本实验结果的因素有那些。 三、实验原理 1.在热化学中,关于溶解过程的热效应,引进下列几个基本概念。 溶解热在恒温恒压下,n2摩尔溶质溶于n1摩尔溶剂(或溶于某浓度的溶液)中产生的热效应,用Q表示,溶解热可分为积分(或称变浓)溶解热和微分(或称定浓)溶解热。 积分溶解热在恒温恒压下,一摩尔溶质溶于n0摩尔溶剂中产生的热效应,用Q s表示。 微分溶解热在恒温恒压下,一摩尔溶质溶于某一确定浓度的无限量的溶液 中产生的热效应,以表示,简写为。 冲淡热在恒温恒压下,一摩尔溶剂加到某浓度的溶液中使之冲淡所产生的热效应。冲淡热也可分为积分(或变浓)冲淡热和微分(或定浓)冲淡热两种。
积分冲淡热在恒温恒压下,把原含一摩尔溶质及n01摩尔溶剂的溶液冲淡到含溶剂为n02时的热效应,亦即为某两浓度溶液的积分溶解热之差,以Qd表示。 微分冲淡热在恒温恒压下,一摩尔溶剂加入某一确定浓度的无限量的溶液 中产生的热效应,以表示,简写为。 2.积分溶解热(Q S)可由实验直接测定,其它三种热效应则通过Q S—n0曲线求得。 设纯溶剂和纯溶质的摩尔焓分别为H m(1)和H m(2),当溶质溶解于溶剂变成溶液后,在溶液中溶剂和溶质的偏摩尔焓分别为H1,m和H2,m,对于由n1摩尔溶剂和n2摩尔溶质组成的体系,在溶解前体系总焓为H。 H=n1H m(1)+n2H m(2) (1) 设溶液的焓为H′, H′=n1H1,m+n2H2,m (2) 因此溶解过程热效应Q为 Q =Δmix H=H - H= n1[H1。m –H m(1)]+n2[H2,m–H m(2)] =n1Δmix H m(1)+n2Δmix H m(2) (3) (3)式中,Δmix H m (1)为微分冲淡热,Δmix H m (2)为微分溶解热。根据上述定义,积分溶解热Q S为 (4)
《溶液 溶解度》单元测试题(含答案)
《溶液溶解度》单元测试题(含答案) 一、溶液选择题 1.根据如图所示的溶解度曲线,判断下列说法正确的是 A.50℃时,分别将等质量的硝酸钾和氯化铵溶于适量的水恰好配成饱和溶液,所得溶液的质量前者比后者大 B.60℃时,把40g硝酸钾和40g氯化钾分别加入到50g水中,充分搅拌,降温至10℃ ,氯化钾析出的晶体质量多 C.70℃时,50g硝酸钠饱和溶液中所含溶剂质量:100g硝酸钾饱和溶液中所含溶剂质量 =1:2 D.80℃时,向与100g氯化钾饱和溶液相同质量的水中加入153g硝酸钠充分搅拌后,最终硝酸钠完全溶解 【答案】C 【解析】 A. 50℃时,硝酸钾的溶解度大于氯化铵的溶解度,所以50℃时,分别将等质量的硝酸钾和氯化铵溶于适量的水恰好配成饱和溶液,所需水的质量是硝酸钾小于氯化铵,所得溶液的质量前者比后者小,错误; B.60℃时,硝酸钾的溶解度是110g,50g水中最多溶解55g,40g硝酸钾硝酸钾全部溶解,60℃时,氯化钾的溶解度大于40g,小于50g,所以50g水中溶解氯化钾的质量少于25g,即60℃时形成的是饱和溶液,降温到10℃,硝酸钾的溶解度小于氯化钾的溶解度,所以硝酸钾析出的晶体质量多,错误; C. 70℃时,硝酸钠的溶解度等于硝酸钾的溶解度,所以它们的饱和溶液中溶质质量分数相等,溶液具有均一性,所以70℃时,50g硝酸钠饱和溶液中所含溶剂质量:100g硝酸钾饱和溶液中所含溶剂质量=1:2,正确; D. 80℃时,氯化钾的溶解度是50g,100g氯化钾饱和溶液中所含水的质量是: 100g×(1- 50g 50g100g )=2 3 ×100g,80℃时,硝酸钠的溶解度是150g,则 2 3 ×100g水最多
硝酸钾的制备知识讲解
硝酸钾的制备
硝酸钾的制备 一.实验目的 1.掌握无机制备中常用的过滤法,着重介绍减压过滤和热过滤。 2.练习加热溶解、蒸发浓缩、结晶等基本操作。 二.实验原理 1.KCl+ NaNO 3=KNO 3 +NaCl 2.当KCl和NaNO 3 溶液混合时,混合液中同时存在,由它们组成的四种盐,在不同的温度下有不同的溶解度,利用NaCl、KNO3的溶解度随温度变化而变化的差别,高温除去NaCl,滤液冷却得到KNO3。 表2.1.1 四种盐在水中的溶解度(g/100g H2O) 仅供学习与交流,如有侵权请联系网站删除谢谢2
仅供学习与交流,如有侵权请联系网站删除 谢谢3 三.主要仪器与试剂 1 仪器 烧杯 量筒 热过滤漏斗 减压过滤装置 电子天平。 2 试剂 NaNO 3(s)、KCl(s)。 四.操作步骤 操作 现象 解释 称8.5g 硝酸钠、7.5g 氯化 钾 加15mL 水,作记号,加热、搅拌、溶解; 溶解后得 到澄清无 色溶液 由于四种离子组成了四种盐,高温时氯化钠的溶解度最小,故要使盐溶解,首先由氯化钠的溶解度来考虑加水量。 从化学计量式知产物氯化钠的生成量为5.9g ,加 热至373K 时氯化钠溶解度为39.8g/100g H 2O ,需水 15g ,约相当于15mL 。 小火浓缩至原体积的2/3; 有圆粒状白色晶体生成 析出的晶体是氯化钠,反应生成的氯化钠为5.9g 。蒸发 浓缩溶液至原体积的2/3时,体系中有水 :15×2/3 = 10mL 。373K 时氯化钠溶解度39.8g /100g 水,10mL 水中 可溶解氯化钠4g ,故析出氯化钠5.9 - 4 = 1.9g 。因
冰的熔解热的测定实验报告
实验名称测定冰的熔解热 一、前言 物质从固相转变为液相的相变过程称为熔解。一定压强下晶体开始熔解时的温度称为该晶体在此压强下的熔点。对于晶体而言,熔解是组成物质的粒子由规则排列向不规则排列的过程,破坏晶体的点阵结构需要能量,因此,晶体在熔解过程中虽吸收能量,但其温度却保持不变。物质的某种晶体熔解成为同温度的液体所吸收的能量,叫做该晶体的熔解潜热。 二、实验目的 1、学习用混合量热法测定冰的熔解热。 2、应用有物态变化时的热交换定律来计算冰的溶解热。 3、了解一种粗略修正散热的方法——抵偿法。 三、实验原理 本实验用混合量热法测定冰的熔解热。其基本做法如下:把待测系统A和一个已知热容的系统B混合起来,并设法使它们形成一个与外界没有热量交换的孤立系统C (C=A+B).这样A(或B)所放出的热量,全部为B(或A)所吸收。因为已知热容的系统在实验过程中所传递的热量Q,是可以由其温度的改变△T 和热容C计算出来,即Q = C△T,因此待测系统在实验过程中所传递的热量也就知道了。 实验时,量热器装有热水(约高于室温10℃,占内筒容积1/2),然后放入适量冰块, 冰溶解后混合系统将达到热平衡。此过程中,原实验系统放热,设为Q 放 ,冰吸热溶成水, 继续吸热使系统达到热平衡温度,设吸收的总热量为Q 吸 。 因为是孤立系统,则有Q 放= Q 吸 (1) 设混合前实验系统的温度为T1,其中热水质量为m1(比热容为c1),内筒的质量为m2(比热容为c2),搅拌器的质量为m3(比热容为c3)。冰的质量为M(冰的温度和冰的熔点均认为是0℃,设为T0),数字温度计浸入水中的部分放出的热量忽略不计。设混
硝酸钾
《盐化工工艺学》 课程论文 论文题目:硝酸钾 学生姓名:刘波 学号: 201208014219 专业:化学工程与工艺班级:2012级盐气化工任课教师:黄美英 完成时间:2014年12月
目录 1生产简史 (1) 2硝酸钾的物化性质及用途 (1) 2.1物理化学性质 (1) 2.2硝酸钾的应用 (1) 2.3质量规格 (2) 3硝酸钾的生产方法 (2) 3.1合成法 (2) 3.2硝酸铵转化法(复分解法) (3) 3.3吸收法 (3) 3.4离子交换法 (3) 3.5转化法 (3) 4新工艺 (4) 4.1新工艺原理与流程[4] (4) 4.2主要设备选型及特点 (5) 4.2.1配料槽 (5) 4.2.2空气冷却结晶塔 (5) 4.2.3离心机 (6) 4.2.4溶解槽 (6) 4.2.5卧式冷却结晶器 (6) 4.2.6硝酸钾洗涤机 (6) 4.2.7干燥机组 (6)
4.2.8蒸发设备 (6) 4.3新工艺装置特点 (7) 4.4生产中应注意问题 (7) 结束语 (8) 致谢 (9) 参考文献 (10)
硝酸钾 【摘要】介绍了硝酸钾产品的生产简史及其主要物化性质、用途、国家标准、生产方法、典型生产方法的基本原理、工艺条件、工艺流程图以及相关的设备等。本文重点介绍一种硝酸钠转化法制取硝酸钾新工艺。该工艺根据传统硝酸钠生产硝酸钾经验,通过进一步试验与研究,对传统工艺与设备进行改造创新,实现连续工业化生产。 1生产简史 世界硝酸钾70%用于农业,以色列和美国产量最大,约占世界总量的四分之三,智利居第三位。1995年世界硝酸钾总能力约90万吨年,其中直接法的产量约占75%,中国硝酸钾现有生产能力约6万吨年,在建能力亦为6万吨年,其中约80%硝酸钾用于工业部门。 2硝酸钾的物化性质及用途 2.1物理化学性质 硝酸钾(钾硝石)是无水的白色粉末,在空气中不潮解。有时因带有杂质而显浅灰色。密度为2.11g/cm3334℃熔融,高于338℃,分解为亚硝酸钾和放出氧气。硝酸钾有两种晶体,即低温时,生成斜方形结晶;高温时生成菱形结晶。硝酸钾的溶解度随着硝酸浓度升高而降低,当达到最低值后,又升高;硝酸钾在水中的溶解度随着温度的升高而增大。纯品中含46.58%氧化钾和13.85%氮。硝酸钾易溶于水,而且溶解度随温度升高而急剧增加,在20℃时每100克水中可溶解31.2克,在100℃时可溶解247克。 硝酸钾是强氧化剂,与有机物接触能燃烧爆炸,运输、储存时注意安全。2.2硝酸钾的应用 硝酸钾是一种重要的无机化工原料,主要用于制造黑火药、火柴、玻璃制品、光化学玻璃、陶瓷制品、药品、食品等。 硝酸钾在农业上是一种优良的低氯二元钾肥,其主要优点有:①总营养成分 高达59%,其中约含13.5% ~13.9%硝基氮及44.6% ~ 46%的K2O;②当作为烟草、茶 叶肥时,硫酸钾中的SO42-会使烟草、茶叶中含硫量偏高,降低品位,而硝酸钾则不存在这个问题;③硝酸钾在水中溶解度高,不易挥发,是液体肥料的最佳配料;④
溶解热的测定(KNO3溶解热的测定)
KNO 3溶解热的测定 一、实验目的 1.用电热补偿法测定KNO 3在不同浓度水溶液中的积分溶解热。 2.用作图法求KNO 3在水中的微分冲淡热、积分冲淡热和微分溶解热。 二、预习要求 1.复习溶解过程热效应的几个基本概念。 2.掌握电热补偿法测定热效应的基本原理。 3.了解如何从实验所得数据求KNO 3的积分溶解热及其它三种热效应。 4.了解影响本实验结果的因素有那些。 三、实验原理 1.在热化学中,关于溶解过程的热效应,引进下列几个基本概念。 溶解热: 在恒温恒压下,n 2摩尔溶质溶于n 1摩尔溶剂(或溶于某浓度的溶液)中产生的热效应,用Q 表示,溶解热可分为积分(或称变浓)溶解热和微分(或称定浓)溶解热。 积分溶解热:在恒温恒压下,一摩尔溶质溶于n 0摩尔溶剂中产生的热效应,用s Q 表示。 微分溶解热:在恒温恒压下,一摩尔溶质溶于某一确定浓度的无限量的溶液中产生的热效应,以1,,2n p t n Q ???? ????表示,简写为1 2n n Q ???? ????。 冲淡热:在恒温恒压下,一摩尔溶剂加到某浓度的溶液中使之冲淡所产生的热效应。 冲淡热也可分为积分(或变浓)冲淡热和微分(或定浓)冲淡热两种。 积分冲淡热:在恒温恒压下,把原含一摩尔溶质及n 01摩尔溶剂的溶液冲淡到含溶剂为 n 02时的热效应,亦即为某两浓度溶液的积分溶解热之差,以d Q 表示。 微分冲淡热:在恒温恒压下,一摩尔溶剂加入某一确定浓度的无限量的溶液中产生的 热效应,以2,,1n p t n Q ???? ????表示,简写为2 1n n Q ???? ????。 2.积分溶解热(s Q )可由实验直接测定,其它三种热效应则通过s Q —n 0曲线求得。 设纯溶剂和纯溶质的摩尔焓分别为)1(m H 和)2(m H ,当溶质溶解于溶剂变成溶液后,在溶液中溶剂和溶质的偏摩尔焓分别为m H ,1和m H ,2,对于由1n 摩尔溶剂和2n 摩尔溶质组成的体系,在溶解前体系总焓为H 。 )2()1(21m m H n H n H += ( 1 ) 设溶液的焓为H ′, m m H n H n H ,22,11/+= ( 2 )
溶解度的测定
实验2 溶解度的测定 37 一 目的 藉由不同温度下测定物质的溶解度,以了解温度与溶解度之间的关系,并以图形表达之。 二 实验原理 溶质的溶解度会受到许多因素的影响,如溶质的本性、溶剂的种类、温度…等。即使是在同一种溶剂中,如图E2-1所示,不同的溶质在水中的溶解度也各不相同,硝酸钾在约22℃以下,其溶解度小于氯化钠,但高于此温度时,其溶解度则远大于氯化钠。大部分的固体溶质,其溶解度随着温度的增高而变大,但是如下图所示有些变化较大,有些则变化较小。 图E2-1中的各条曲线是如何画出来的?我们可以在高温下配制数支不同浓度的不饱和溶液,然后依序让试管内溶液的温度徐徐降低,直至溶液中有碎屑开始出现时,记录当时的温度,将其浓度换算即可得知该温度的溶解度,将数点不同温度下的溶解度在图形中相连,即可得相似的曲线。 三 实验器材 每組 器材(规格) 数量 器材(规格) 数量 天平 共享 中型试管(18 mm 口径) 4支 试管夹 1支 烧杯(600 mL ) 1个 量筒(25 mL ) 1个 电热板和磁搅拌子(或其他加热装置) 1组 温度计 1支 末端有环的铁丝(可自制) 1支 试管架 1座 溶解度的测定 如何使更多的固体溶到水中? 2 连结课本P.116 图E2-1 各种固体溶解度与温度关系
36高中化学(全)实验活动手册 四实验试药 每組 药品份量药品份量 水约20 mL 硝酸钾(KNO3)约14 g 五实验步骤 1 取600 mL烧杯,装热水 半满并置于电热板上,开 启电源,把火力调至最 小,加热烧杯内的水。 2 称取质量为2.0 g、3.0 g、 4.0 g和 5.0 g的硝酸钾倒入 四支试管。 3 再各加入5.0 g水于四支 试管。 4 将4支试管放入装水烧 杯中,以水浴法加热。 5 注意观察各试管内固体。 6 依序用试管夹将固体已 溶解的试管取出(其先后 顺序应为加了2.0 g、3.0 g、4.0 g和5.0 g硝酸钾 固体的试管),先进行下 一步骤,直到所有试管均 取出为止,关闭电热板的 电源。
物质的溶解度
溶解度计算1 姓名_________ 1、把50克20℃时的硝酸钾饱和溶液蒸干,得到12克硝酸钾。求20℃时硝酸钾的溶解度。 2、 70℃时,硝酸钾的溶解度为138克,配制饱和溶液时: (1)60克水最少需要加入硝酸钾多少克。 (2)13.8克硝酸钾最多可加入水多少克。 (3)70℃100克的硝酸钾饱和溶液里含硝酸钾多少克。 3、80℃时,硝酸钾的溶解度为169克,在此温度下将90.2克的硝酸钾溶解在60克水里,计算: (1)此溶液是饱和溶液还是不饱和溶液? (2)若用蒸发溶剂的方法使其达到饱和,需要蒸发多少克水? (3)若用增加溶质的方法使其达到饱和,应再加入硝酸钾多少克? 4、60℃时90克KNO3固体加入75克水后充分振荡,有7.5克没有溶解。求60℃时KNO3的溶解度。 5、已知60℃时溶解度为110克,有90克KNO3固体,加入75克水,能得到多少克溶液? 6、20℃,氯化钠的溶解度为36克。 (1)20℃,氯化钠溶液中有部分晶体未溶,加入25克水恰好将其溶解,问没有溶解的晶体有多少克? (2)将20℃氯化钠饱和溶液34克蒸干,可以得到晶体多少克? 8、20度时,50gA溶于水,形成200g不饱和溶液,现蒸发原水量的一半,溶液刚好达到饱和,求20度时A的溶解度。 9、20度时,已知氯化钠的溶解度时36g,现有27g食盐溶解在该温度下的200g水中,要使溶液达到饱和状态,问:(1)至少需要加入食盐多少克?(2)至少需要蒸发水多少克?10、20度时,将某固体物质60g完全溶解于水,制成200ml密度为1.5g/ml的饱和溶液,求20度时该物质的溶解度。 11、20度时,227g不饱和溶液,如果加入45g某物质或蒸发125g水都能达到饱和,则20度时该物质的溶解度时多少克? 12、一定温度下,Ag某固体溶质加入水中,制成Bg该溶质的饱和溶液,该物质在此温度下的溶解度是多少? 13、T度时的硝酸钾溶液200g,蒸发掉10g水后析出晶体4g,又蒸发10g水后析出晶体6g,再蒸发20g水析出晶体的质量是________________。 14、25℃时,M固体(硝酸钾)的溶液200克,当温度不变,蒸发掉20克水时,有5克M 析出;若再蒸发掉20克水时,有10克M析出;若又蒸发掉20克水时,可析出M物质的质量是_____,则25℃时M物质的溶解度______。 15、已知25℃时,50克水中需溶解12.5克硝酸钾才能达到饱和。现有一杯硝酸钾溶液500克,若要使其达到饱和需蒸发10克水,若改用加硝酸钾的方法,需加_____克硝酸钾才能使其达到饱和? 16、 30℃时,将A物质的溶液平均分成二等份,第一份恒温蒸发10克水,有1克A析出,第二次恒温蒸发25克水,有5克A析出,若第一份继续蒸发15克水,有____克晶体析出.则30℃时,A物质的溶解度为_______. 17、某温度下,将A物质的水溶液分成等量的2份,向第一份中加入9克A物质,充分搅拌,尚有1克固体不能溶解,将第二份溶液蒸发掉40克水,并恢复到原温度,溶液恰好饱和(无A析出),则A物质在该温度下的溶解度是_______。
物化实验报告:溶解热的测定-KCl、KNO3
华南师范大学实验报告 课程名称 物理化学实验 实验项目 溶解热的测定 【实验目的】 1.用量热计简单测定硝酸钾在水中的溶解热。 2.掌握贝克曼温度计的调节和使用。 【实验原理】 盐类的溶解往往同时进行着两个过程:一是晶格破坏,为吸热过程;二是离子的溶剂化,为放热过程。溶解热是这两种热效应的总和。最终是吸热还是放热,则由这两种热效应的相对大小来决定。 本实验在定压、不做非体积功的绝热体系中进行时,体系的总焓保持不变,根据热平衡,即可计算过程所涉及的热效应。 T C C W C W W M H m sol ??++-=?][322111 )( (3.1) 式中: m Sol H ?为盐在溶液温度和浓度下的积分溶解热,单位:kJ ·mo1–1; 1W 为溶质的质量,单位:kg ; T ?为溶解过程的真实温差,单位:K ; 2W 为水的质量,单位:kg ; M 为溶质的摩尔质量,单位:kg ·mo1–1 ; 21C C 、分别为溶质和水的比热,单位:11--?K kg kJ ; 度升 3C 为量热计的热容(指除溶液外,使体系温高1℃所需要的热量) ,单位:kJ 。 实验测得W 1、W 2、ΔT 及量热计的热容后,即 可按 图3.1溶解热测定装配图 1.磁力搅拌器; 2.搅拌磁子; 3.杜瓦瓶; 4.漏斗; 5.传感器; 6.SWC —IIC 数字贝克曼温度仪.
(3.1)式算出熔解热m Sol H 。 【仪器与药品 】 溶解热测量装置一套(如图3.1所示);500ml 量筒一个;KCl(A.R.) ;KNO 3(A.R.) 【实验步骤】 1.量热计热容的测定: 本实验采用氯化钾在水中的溶解热来标定量热计热容3C 。为此,先在干净的量热计中装入500m1蒸馏水,将与贝克曼温度计接好的传感器插入量热计中,放在磁力搅拌器上,启动搅拌器, 保持60-90转/分钟的搅拌速度,此时,数字显示应在室温附近,至温度变化基本稳定后,每分钟准确记录读数一次,连续8次后,打开量热计盖,立即将称量好的10克氯化钾(准确至0.01克)迅速加入量热计中,盖上盖,继续搅拌,每分钟记录一次读数,读取12次即可停止。然后用普通水银温度计测出量热计中溶液的温度,倒掉溶液。 2.硝酸钾溶解热的测定:用硝酸钾代替氯化钾重复上述实验,区别是称取硝酸钾的质量为7克(准确至0.01g)。完成一次实验后,溶液不倒掉。同样连续读数8次后,再向溶液中加入7克硝酸钾,再读取12次温度完成第二次测量。实验结束,倒掉溶液 【数据的处理】 1.各样品溶解前后温差的雷诺校正图
实验3_溶解热的测定
溶解热的测定 1 引言 1.1 实验目的 1. 测量硝酸钾在不同浓度水溶液的溶解热,求硝酸钾在水中溶解过程的各种热效应。 2. 掌握量热装置的基本组合及电热补偿法测定热效应的基本原理。 3. 复习和掌握常用的测温技术 1.2 实验原理 在热化学中,关于溶解过程的热效应,有以下几个基本概念 溶解热 在恒温恒压下,溶质B 溶于溶剂A (或溶于某浓度溶液)中产生的热效应,用Δsol H 表示 摩尔积分溶解热 在恒温恒压下,1 mol 溶质溶解于一定量的溶剂中形成一定浓度的溶液,整个过程的热效应,用Δsol H m 表示: Δsol H m = Δsol H B 式中:n B 是溶解于溶剂A 中的溶质B 的物质的量 摩尔微分溶解热 在恒温恒压下,1 mol 溶质溶于某一确定浓度的无限量的溶液中产生的热效应,以 ( ?Δsol H ?n B ) T,p,n A 表示,简写为(?Δsol H ?n B )n A 稀释热 在恒温恒压下,一定量的溶剂A 加到某浓度的溶液中使之稀释,所产生的热效应 摩尔积分稀释热 在恒温恒压下,在含有1 mol 溶质的溶液中加入一定量的溶剂,使之稀释成另一浓度的溶液,这个过程产生的热效应,以Δdil H m 表示: Δdil H m =Δsol H m2?Δsol H m1 摩尔微分稀释热 在恒温恒压下,1 mol 溶剂加入到某一浓度无限量的溶液中所发生的热效应 在恒温恒压下,对于指定的溶剂A 和溶质B ,溶解热的大小取决于A 和B 的物质的量,即 Δsol H =f(n A ,n B ) 取全微分 Δsol H =n A (eΔsol H A )n B +n B (eΔsol H B )n A
高中化学物质的量浓度溶液配制与硝酸钾的溶解度测定实验操作口诀
高中化学物质的量浓度溶液配制与硝酸钾的溶解度测定实验操作口诀 物质的量浓度溶液配制 算称量取步骤清,溶解转移再定容。室温洗涤莫忘记,摇匀标签便告成。 解释: 1. 算称量取步骤清,溶解转移再定容:这两句的意思说明了摩尔溶液配制的步骤是:计算、称量、(或量取)、溶解、转移、定容。 2. 室温洗涤莫忘记:" 室温" 的意思是说溶解时往往因溶解的放热而使溶液的温度升高,故必须冷至室温以后再转移定容。" 洗涤" 的意思是指移液后,必须用蒸馏水洗涤烧杯和玻璃棒(2-3 次),并将洗涤液皆并入容量瓶中,然后再定容。 3. 摇匀标签便告成:" 摇匀" 的意思是说定容后盖好瓶塞,用食指顶住瓶塞,用另一指手的手指托住瓶底,把容量瓶倒转和摇动多次,使溶液混合均匀;" 标签" 的意思是说要贴好标签,标明溶液浓度和配制的日期。 硝酸钾的溶解度测定实验 内地外高水浴热,温度计在试管中。溶液饱和防溅失,干燥器中冷却成。 解释: 1. 内地外高水浴热:意思是说配制硝酸钾的饱和溶液时,必须在水浴中加热,以利于控制温度;试管内的液面要低于热水的液面,这样使试管内的液体受热均匀和水浴的温度相同。 2. 温度计在试管中:意思是说配制饱和溶液时,温度计务必放在试管内,不得放在水浴中。
3. 溶液饱和防溅失:"溶液饱和"的意思是说必须使溶液达到饱和(为了保证溶液饱和,硝酸钾晶体可稍加过量搅拌,在5分钟内不溶解即可);"防溅失"的意思是说在蒸发溶液的过程中,注意不要溅失,要彻底蒸干,不要使硝酸钾粘在试管壁上。 4. 干燥器中冷却成:意思是说蒸干后的晶体连同蒸发皿必须放在干燥器中冷却[联想:硫酸铜晶体结晶水含量测定实验中的"质量变化重称量"。
有关溶解度的计算典型例题
有关溶解度的计算典型例题 [例1]已知15℃时碘化钾的溶解度为140g,计算在该温度下250g水中最多能溶解多少克碘化钾? [例2] 把20℃的282g硝酸钾饱和溶液加热,升温到60℃,需要加入多少克硝酸钾才能使溶液重新达到饱和?(已知20℃时硝酸钾的溶解度为31.6g,60℃时为110g)。 [例3]已知30℃时硝酸钾的溶解度为45.8g。在这温度时,某硝酸钾溶液500g中溶有硝酸钾137.4g。如果蒸发掉90g水后,再冷却到30℃,可析出多少克硝酸钾? [例4]有60℃时A物质的溶液100g,若温度不变,蒸发掉10g水时,有4gA的晶体析出(不含结晶水),再蒸发掉10g水时,又有6gA的晶体析出,求60℃时A物质的溶解度是多少。
[例5]在20℃时某物质的不饱和溶液50g,平均分成两等份。一份中加入0.7g该物质,另一份蒸发掉5g水,结果两份溶液都达饱和。那么该物质在此温度下的溶解度为多少克? [例6]一定温度下,取某固体物质的溶液mg,分成等质量的两份,将一份溶液恒温蒸发达饱和时,其质量减轻一半。给另一份溶液里加入原溶质的晶体(该晶体不含结晶水),当达饱和时,所加晶体的质量恰好是此份溶液质量的1/8,求此温度下该物质的溶解度。 [例7]某物质溶解度曲线如图所示。现有该物质的A、B两种不同浓度的不饱和溶液,当A冷却至10℃时有晶体析出,B在60℃时成为饱和溶液。若取10℃时A的100g饱和溶液,取60℃时B的50g饱和溶液混合得C溶液,则需降温到多少时能析出5g无水晶体?
[例8]某固体混合物中含有硝酸钾和不溶性杂质、把它们加入一定量的水中充分溶解,其结果如下表: 硝酸钾的溶解度见下表: 求:1.所加水的质量。2.该固体混合物中硝酸钾的质量。 [例9]80℃时把10g硝酸钾溶解于50g水中形成溶液。根据溶解度曲线(初中化学课本)和计算说明:①此溶液是否饱和?②如冷却降温到什么温度下才能达到饱和?③欲使其达到饱和(80℃),可采取哪些方法? [例10] 一定温度下,溶质的质量分数为a%的硝酸钾溶液取其等质量的溶液两份,在温度不变的情况下,将一份蒸发掉10g水,析出1g晶体,另一份蒸发掉12.5g水,析出2g晶体,求该温度下硝酸钾的溶解度。
