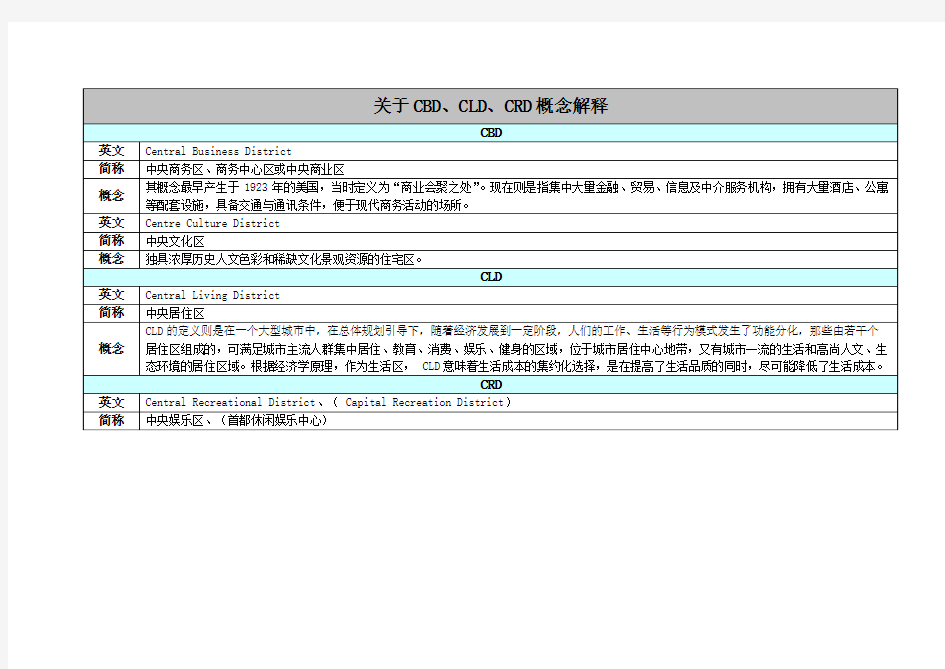
关于CBD、CLD、CRD概念解释
热力学概念名词解释
传热学名词解释 一、绪论 1.热流量:单位时间内所传递的热量 2.热流密度:单位传热面上的热流量 3.导热:物体各部分之间不发生相对位移时,依靠物质微粒(分子、原子或自由电子)的热运动而产生的热能传递,称为导热。 4.对流传热:流体流过固体壁时的热传递过程,就是热对流和导热联合用的热量传递过程,称为表面对流传热,简称对流传热。5.辐射传热:物体间通过热辐射而进行的热量传递,称辐射传热。6.总传热过程:热量从温度较高的流体经过固体壁传递给另一侧温度较低流体的过程,称为总传热过程,简称传热过程。 7.对流传热系数:单位时间内单位传热面当流体温度与壁面温度差为1K是的对流传热量,单位为W/(m2·K)。对流传热系数表示对流传热能力的大小。 8.辐射传热系数:单位时间内单位传热面当流体温度与壁面温度差为1K是的辐射传热量,单位为W/(m2·K)。辐射传热系数表示辐射传热能力的大小。 9.复合传热系数:单位时间内单位传热面当流体温度与壁面温度差为1K是的复合传热量,单位为W/(m2·K)。复合传热系数表示复合传热能力的大小。 10.总传热系数:总传热过程中热量传递能力的大小。数值上表 示传热温差为1K时,单位传热面积在单位时间内的传热量。
二、热传导 1.温度场:某一瞬间物体内各点温度分布的总称。一般来说,它是空间坐标和时间坐标的函数。 2.等温面(线):由物体内温度相同的点所连成的面(或线)。 3.温度梯度:在等温面法线方向上最大温度变化率。 4.热导率:物性参数,热流密度矢量与温度降度的比值,数值上等于1 K/m的温度梯度作用下产生的热流密度。热导率是材料固有的热物理性质,表示物质导热能力的大小。 5.导温系数:材料传播温度变化能力大小的指标。 6.稳态导热:物体中各点温度不随时间而改变的导热过程。 7.非稳态导热:物体中各点温度随时间而改变的导热过程。 8.傅里叶定律:在各向同性均质的导热物体中,通过某导热面积的热流密度正比于该导热面法向温度变化率。 9.保温(隔热)材料:λ≤0.12W/(m·K)(平均温度不高于350℃时)的材料。10.肋效率:肋片实际散热量与肋片最大可能散热量之比。 11.接触热阻:材料表面由于存在一定的粗糙度使相接触的表面之间存在间隙,给导热过程带来额外热阻。 12.定解条件(单值性条件):使微分方程获得适合某一特定问题 解的附加条件,包括初始条件和边界条件。 三、对流传热 1.速度边界层:在流场中壁面附近流速发生急剧变化的薄层。2.温度边界层:在流体温度场中壁面附近温度发生急剧变化的薄层。3.定性温度:确定换热过程中流体物性的温度。
化工热力学复习题
化工热力学复习题 1、等熵膨胀后的温度一定是。 2、汽轮机出口压力下降,会使朗肯循环的效率 3、在相同温度区间工作的制冷循环,以逆卡诺循环的制冷系数为(最大、最小、不定) 4、在制冷循环中,所用的装置有,, 5、理想气体的微分节流效应系数(Joule-Thomson系数)等于,这也意味着节流前后理想气体的温度(降低、升高、不变,不确定)。 6、理想气体节流膨胀后,节流效应系数μH效应。 7、在相同温度区间工作的蒸汽动力循环,以卡诺循环的热效率为(最大、最小、不定)。 8、消耗外功,实现热由低温区向高温区传递的逆向循环中,维持低于环境温度操作的叫循环,维持高于环境温度操作的叫循环或循环。 9、为提高朗肯循环热效率可采用: 11、朗肯循环由以下几个部分构成:。 12、节流膨胀是:。 13、热泵是指 14、制冷是将体系的温度降低到的操作。 三、名词解释 1、制冷 2、节流膨胀 3、干度 4、自由度 四、作图及简答 1、改进朗肯循环的途径有哪些? 2、请画出朗肯循环的示意图,并画出其在温熵图上的表示? 3、μJ的变化对截流后温度的变化有何影响? 4、试述蒸汽参数对朗肯循环热效率的影响? 5、画出双级复叠式制冷循环的实物图,指明设备的名称,并在TS图上作出制冷循环示意图 6、选择制冷剂应满足什么要求? 7、简述吸收制冷循环的过程并画流程图 8、简述复叠式制冷循环的特点。 9、影响朗肯循环热效率的主要因素是什么?为什么回热循环能提高循环的热效率? 10、卡诺循环中,冷热源温差越大,制冷系数是越大还是越小,为什么? 11、选择制冷剂时要求制冷剂在大气压力下沸点要低,为什么?
五、计算题 1、某制冷机中采用氨做制冷剂,以25℃的饱和液体进入节流阀,离开阀的温度为-20℃,试求:(1)节流过程的有效能损失。(2)当节流过程中制冷剂从环境吸收4.2kJ/kg热量时,有效能的损失。设P0=0.1Mpa,T0=27℃For NH3 4、蒸气动力循环中锅炉产生的蒸汽压力为60×105Pa,温度为500℃,该蒸汽经节流做绝热膨胀后压力降至40×105 Pa,然后进入汽轮机作可逆绝热膨胀到排气压力0.06×105 Pa.(1)画出T-S图、H-P图(2)乏汽的干度(3)气轮机对外做的功(4)热力学效率 5、某柴油机的功率为35KW,该机热力循环的最高热源温度为1800K,低温热源温度为300K,每Kg柴油燃烧后放热为42705KJ,试求柴油的最低消耗量。如果实际循环的热效率为相应卡诺循环的40%,则柴油消耗量为多少? 6、朗肯循环中水蒸气进气轮机的蒸气压力为50×105Pa,温度为360℃,乏气压力为0.1×105 Pa,为减少输出功率,采用锅炉出口的水蒸气先经过节流阀适当降压再送进气轮机膨胀作功,如果要求输出的功量降至正常情况的84%,问节流后进气轮机前的蒸汽状态?画出T-S 图 已知:P=50×105Pa, T=360℃时H=3188.7kj/kg,S=7.666 kj/kg.k P=0.1×105Pa时,饱和液体的H=191.83 kj/kg, S=0.6493 kj/kg.k 饱和蒸汽的H=2584.7 kj/kg, S=8.1502 kj/kg.k 7、朗肯循环中水蒸气进气轮机的蒸气压力为7000 kPa,温度为550℃,乏气压力为20 kPa, 汽轮机和泵的效率均为0.75,要求输出功率为100000 kW。 1)作出理想朗肯循环和实际朗肯循环TS图2)计算该循环的热效率3)确定蒸汽流量(吨/小时)
工程热力学名词解释专题
工程热力学名词解释专题 注:参考哈工大的工程热力学和西交大的工程热力学 第一章——基本概念 1、闭口系统:热力系与外界无物质交换的系统。 2、开口系统:热力系与外界有物质交换的系统。 3、绝热系统:热力系与外界无热量交换的系统。 4、孤立系统:热力系与外界有热量交换的系统。 5、热力平衡状态:热力系在没有外界作用的情况下其宏观性质不随时间变化的状态。 6、准静态过程:如果造成系统状态改变的不平衡势差无限小,以致该系统在任意时刻均无限接近于某个平衡态,这样的过程称为准静态过程 7、热力循环:热力系从某一状态开始,经历一系列中间状态后,又回复到原来状态。 8、系统储存能:是指热力学能、宏观动能、和重力位能的总和。 9、热力系统:根据所研究问题的需要,把用某种表面包围的特定物质和空间作为具体指定的热力学的研究对象,称之为热力系统。 第二章——热力学第一定律 1、热力学第一定律:当热能与其他形式的能量
相互转换时,能的总量保持不变。或者,第一类永动机是不可能制成的。 2、焓:可以理解为由于工质流动而携带的、并取决于热力状态参数的能量,即热力学能与推动功的总和。 3、技术功:技术上可资利用的功,是稳定流动系统中系统动能、位能的增量与轴功三项之和 4、稳态稳流:稳定流动时指流道中任何位置上的流体的流速及其他状态参数都不随时间而变化流动。第三章——热力学第二定律 1、可逆过程:系统经过一个过程后,如果使热力系沿原过程的路线反向进行并恢复到原状态,将不会给外界留下任何影响。 2、热力学第二定律:克劳修斯表述:不可能把热从低温物体转移到高温物体而不引起其他变化。开尔文普朗克表述:不可能从单一热源吸热而使之全部转变为功。 3、可用能与不可用能:可以转变为机械功的那部分热能称为可用能,不能转变为机械功的那部分热能称为不可用能。 4、熵流:热力系和外界交换热量而导致的熵的
工程热力学-名词解释
1.第一章基本概念及定义 2.热能动力装置:从燃料燃烧中得到热能,以及利用热能所得到动力的整套设备(包括辅助设备)统称热能动力装置。 3.工质:热能和机械能相互转化的媒介物质叫做工质,能量的转换都是通过工质状态的变化实现的。 4.高温热源:工质从中吸取热能的物系叫热源,或称高温热源。 5.低温热源:接受工质排出热能的物系叫冷源,或称低温热源。 6.热力系统:被人为分割出来作为热力学分析对象的有限物质系统叫做热力系统。 7.闭口系统:如果热力系统与外界只有能量交换而无物质交换,则称该系统为闭口系统。(系统质量不变) 8.开口系统:如果热力系统与外界不仅有能量交换而且有物质交换,则称该系统为开口系统。(系统体积不变) 9.绝热系统:如果热力系统和外界间无热量交换时称为绝热系统。(无论开口、闭口系统,只要没有热量越过边界) 10.孤立系统:如果热力系统和外界既无能量交换又无物质交换时,则称该系统为孤立系统。 11.表压力:工质的绝对压力>大气压力时,压力计测得的差数。 12.真空度:工质的绝对压力<大气压力时,压力计测得的差数,此时的压力计也叫真空计。 13.平衡状态:无外界影响系统保持状态参数不随时间而改变的状态。充要条件是同时到达热平衡和力平衡。 14.稳定状态:系统参数不随时间改变。(稳定未必平衡) 15.准平衡过程(准静态过程):过程进行的相对缓慢,工质在平衡被破环后自动恢复平衡所需的时间很短,工质有足够的时间来恢复平衡,随时都不致显著偏离平 衡状态,那么这样的过程就称为准平衡过程。它是无限接近于平衡状态的过程。 16.可逆过程:完成某一过程后,工质沿相同的路径逆行回复到原来的状态,并使相互作用所涉及的外界亦回复到原来的状态,而不留下任何改变。可逆过程=准 平衡过程+没有耗散效应(因摩擦机械能转变成热的现象)。 17.准平衡与可逆区别:准平衡过程只着眼工质内部平衡;可逆过程是分析工质与外界作用产生的总效果,不仅要求工质内部平衡,还要求工质与外界作用可以无 条件逆复。 18.功:功是热力系统通过边界而传递的能量,且其全部效果可表现为举起重物。 19.热量:热力系统与外界之间仅仅由于温度不同而通过边界传递的能量。 20.两者不同:功是有规则的宏观运动的能量传递,在做功的过程中往往伴随着能量形态的转化。热量则是大量微观粒子杂乱热运动的能量传递,传递过程中不出 现能量形态的转化。功转变成热量是无条件的而热量转变成功是有条件的。 21.正向循环(热动力循环):热能转化成机械能的循环叫做正循环,它使外界得到功Wnet。 22.逆向循环:工质在循环中消耗机械能(或其他能量)把热量从低温热源传给高温热源的过程称为逆循环,消耗外功。 23.第二章热力学第一定律 24.热力学第一定律:自然界中的一切物质都具有能量,能量不可能被创造,也不可能被消灭,但可以从一种形态转变为另一种形态,在能量的转换过程中能量的 总量保持不变。(热力学第一定律就是能量守恒和转换定律在热现象中的体现)。内能的改变方式有两个:做功和热传递ΔU = W + Q。 25.第一类永动机:不消耗能量便可以永远对外做功的动力机械。 26.热力学能(内能):分子间的不规则运动的内动能,分子间的相互作用的内位能,维持分子结构的化学能,原子核内部的原子能,电磁场作用下的电磁能等一 起构成热力学能。 27.总能(总存储能):内能(热力学能),外能(宏观运动动能及位能)的总和称总能。 28.推动功:工质在开口系统中流动而传递的功称为推动功mpv。 29.流动功:系统为维持工质流动所需的功称为流动功(推动功差p2V2-p1V1)。 30.技术功:机械能可以全部转变为技术上可以利用的功,称为技术功(技术上可资利用的功)。 31.体积功:工质因体积的变化与外界交换的功。 32.焓:在热力设备中,工质总是不断的从一处流到另一处,随着工质的移动而转移的能量,即热力学能和推动功之和u+pv。 33.稳定流动过程:流动过程中,开口系统内部及其边界上各点工质的热力参数及运动参数都不随时间而变,则这种流动过程称为稳定流动过程。反之,则为不稳 定流动过程或瞬变流动过程。 34.节流:工质流过阀门等设备时,流动界面突然收缩,压力下降,这种现象称为节流。 35.第三章气体和蒸汽的性质 36.标准大气压:在纬度45°的海平面上,当温度为0℃时,760毫米高水银柱产生的压强叫做标准大气压。 37.理想气体:1.分子间是弹性的、不具有体积的质点;2.分子间相互没有作用力。 38.摩尔气体常数:R=MRg=8.314 5 J/(mol·K),与气体种类状态都无关。Rg与气体种类有关,状态无关。Rg物理意义是1 kg某种理想气体定压升高1 K对外作 的功。 39.定压比热容Cp:压力不变的条件下,1kg物质在温度升高1K所需的热量称为定压比热容。 40.定容比热容Cv:体积不变的条件下,1kg物质在温度升高1K所需的热量称为定容比热容。Cp- Cv=Rg气体常数。Cp/Cv=γ比热容比。 41.湿饱和蒸汽:水蒸气和水的混合物称为湿饱和蒸汽。 42.干饱和蒸汽:即饱和蒸汽,水全部变成蒸汽,这个时候的蒸汽称为干饱和蒸汽 43.过热蒸汽:对饱和蒸汽继续定压加热,蒸汽温度升高,比体积增大,此时的蒸汽称为过热蒸汽。 44.饱和状态:当汽化速度=液化速度时,系统处于动态平衡,宏观上气、液两相保持一定的相对数量。 45.饱和温度:处于饱和状态的汽、液的温度相同称为饱和温度。 46.饱和压力:处于饱和状态的蒸汽的压力称为饱和压力。 47.过冷水:水温低于饱和温度时称为过冷水或未饱和水。 48.过热度:温度超过饱和温度之值称为过热度 49.汽化潜热:1kg质量的某种液相物质在汽化过程中所吸收的热量。简称汽化潜热(液体蒸发吸收的热量)。 50.第四章气体与蒸汽的基本热力 51.第五章热力学第二定律 52.热力学第二定律(克劳修斯说法):热不可能自发的、不付代价的从低温物体传至高温物体。 53.热力学第二定律(开尔文说法):不可能制造出从单一热源吸热,使之全部转化为功而不留下其他任何变化的热力发动机。 54.造成过程不可逆的两大因素:1、耗散效应。2、有限势差作用下的非准平衡变化。
浅谈抗震概念设计的重要性
浅谈抗震概念设计的重要性 摘要本文结合规范浅谈在抗震设计中概念设计的必要性、依据和来源、特点、应用 关键词总体地震效应薄弱层抗震设计概念设计 一、概述 目前,建筑抗震理论远未达到十分科学严密,单靠理论计算很难使建筑物具有良好的抗震能力,而着眼于建筑总体抗震能力的“概念设计”则愈来愈受到工程界的普遍重视,它在我国的抗震设计规范也开始有所体现。下面我就概念设计几点进行探讨。 二、抗震设计不确定因素 1. 地震发生的时间、地点和强度是不确定的,而且在某一次实际发生的地震中,方圆几千米区域内的地震加速度变化很大,表现出很强的离散型和不确定性。但实际设计时,往往是某一行政区域内所采用的地震作用参数确定的,例如,北京市为8度(0.2g,第一组,对于Ⅱ类场地设计特征周期为0.35s)设防区,上海为7度(0.1g,第一组,对于二类场地土为0.35s)设防区等,设计所采用的理论化结果和实际可能发生的地震作用之间不可能一致。就现阶段而言,结构抗震设计实际上只是一种校核或验算,即对给定结构的尺寸,给定预测的地震作用,验算结构是否满足强度和变形要求。即使考虑了结构构造措施的作用,也是在假定的地震作用条件下考虑的。由于地震的发生是未知的,一旦实际发生的地震大于预先假定的地震作用,结构就难以达到预先设计的安全性。 2. 结构理论本身也存在着许多不确定性,例如:结构构件材料性能、截面几何参数和计算模式的精度的不确定性导致结构构件抗力的不确定性,在结构整体分析中采用简化计算分析模型所引起的误差导致的不确定性,以及场地土类型的不确定性等。这些不确定性反映在工程设计方面,主要表现在以下几方面(1)结构分析的影响;(2)材料的影响;(3)阻尼系数的变化。(4)基础差异沉降的影响(5)地基承载力的影响(6)持续荷载的影响。 由此可见,由于地震作用的不确定性和复杂性,以及结构计算模型的基本假定与实际受力情况的不一致性,仅靠计算分析得出的数据进行的抗震设计即计算设计(或称为数值计算)所设计出的结构必然缺乏对不同地震作用的适应性,很难有效的控制结构的抗震性能。总结历次大地震灾害的经验教训,人们发现,在抗震设计时不能完全依赖计算,概念设计比计算设计更为重要,《建筑抗震设计规范》(GBJ 11-08)的条文说明中明确提出“结构抗震性能的决定因素是良好的概念设计”. 三、概念设计的定义及原则
化工热力学考试题目三
化工热力学考试题目3 一、选择题 1、关于化工热力学用途的下列说法中不正确的是( ) A 可以判断新工艺、新方法的可行性; B.优化工艺过程; C.预测反应的速率; D.通过热力学模型,用易测得数据推算难测数据,用少量实验数据推算大量有用数据; E.相平衡数据是分离技术及分离设备开发、设计的理论基础。 2、纯流体在一定温度下,如压力低于该温度下的饱和蒸汽压,则此物质的状态为( )。 A .饱和蒸汽 B.饱和液体 C .过冷液体 D.过热蒸汽 3、超临界流体是下列( )条件下存在的物质。 A.高于T c 和高于P c B.临界温度和临界压力下 C.低于T c 和高于P c D.高于T c 和低于P c 4、对单原子气体和甲烷,其偏心因子ω,近似等于( )。 A. 0 B. 1 C. 2 D. 3 5、关于化工热力学研究特点的下列说法中不正确的是( ) A 、研究体系为实际状态。 B 、解释微观本质及其产生某种现象的内部原因。 C 、处理方法为以理想态为标准态加上校正。 D 、获取数据的方法为少量实验数据加半经验模型。 E 、应用领域是解决工厂中的能量利用和平衡问题。 6、关于化工热力学研究内容,下列说法中不正确的是( ) A.判断新工艺的可行性。 B.化工过程能量分析。 C.反应速率预测。 D.相平衡研究 7、分) ,400K 的2N 1kmol 体积约为( ) A 3326L B 332.6L C 3.326L D 3 m 8、下列气体通用常数R 的数值和单位,正确的是( ) A K kmol m Pa ???/10314.83 3 B kmol K C K atm cm /3 ? D K kmol J ?/ 9、纯物质 PV 图临界等温线在临界点处的斜率和曲率都等于( )。 A. -1 B. 0 C.1 D. 不能确定 10、对理想气体有( )。 0)/.(??T P H B 0)/.(=??T P H C 0)/.(=??P T H D 11、对单位质量,定组成的均相流体体系,在非流动条件下有( )。 A . dH = TdS + Vdp B .dH = SdT + Vdp C . dH = -SdT + Vdp D. dH = -TdS -Vdp
工程热力学名词解释
热力系统:将所要研究的对象与周围环境分隔开来,这种人为分隔出来的研究对象,称之为热力系统。简称系统。边界:分隔系统与外界的分界面,作用:确定研究对象,将系统与外界分隔。 外界:边界以外与系统相互作用的物体,称为外界或环境。系统与外界作用通过分界面进行,有三种形式:功交换、热交换、物质交换。 闭口系统:没物质穿过边界的系统。又称为控制质量系统。 开口系统:有物质穿过边界的系统。 绝热系统:系统与外界无热量交换的系统。 孤立系统:系统与外界不发生任何能量传递和物质交换的系统。 热力状态:系统中某瞬间表现的工质热力性质的总状况。简称状态。热力状态反应大量分子热运动的平动特征。 平衡状态:系统在不受外界影响的条件下,系统内外同时建立了热和力平衡,这时系统的状态,称为平衡状态。 状态参数:描述工质状态特征的各种物理量。 基本状态参数:可以直接或间接地用仪表测量出来的参数。 比容:单位质量工质所具有的容积,称为工质的比容。 密度:单位容积的工质所具有的质量,称为工质的密度。 温度:描述热力平衡系统冷热状况的物理量。温度的数值标尺简称温标。 压力:垂直作用于器壁单位面积上的力。(也称压强) P=F/A 相对压力(表压力)=大气压力+绝对压力:以大气压力作为基准所表示的压力。 绝对压力:以绝对真空作为基准所表示的压力。状态参数。 道尔顿分压定律:混合气体总压力为P,等于各组成气体分压力Pi之和。 分容积:假象混合气体中组成气体具有混合气体相同温度和压力时,单独占有的容积。 准静态过程:由一系列非常接近平衡态的状态所组成的过程。(是理想化过程) 可逆过程:当系统进行正反两个过程后,系统与外界均能完全回复到初始状态的过程。反之为不可逆过程。(理想化过程)可逆过程实现条件(特征):1.过程势差无限小,即准静过程。2.没有耗散效应。 体积功:由于系统体积发生变化而通过界面向外界传递的机械功。(体积增大为膨胀功,体积减小为压缩功) 热力循环:工质从某一初态出发,经过一系列的中间状态变化,又回复到原来状态的全部过程。 理想气体:科学抽象的假象气体模型。气体分子是一些弹性的、不占有体积的质点,气体分子间无相互作用力。 比热容:单位物量的物质,温度升高或降低1K所吸收或放出的热量。 定容比热容:在定容情况下,单位物量的气体,温度变化1K所吸收或放出的热量。 定压比热容:在定容情况下,单位物量的气体,温度变化1K所吸收或放出的热量。Cp-Cv=R(适用于理想气体) 绝热指数(比热容比)κ:定压比热Cp与定体积比热Cv之比。 混合气体成分:混合气体中各组成气体的含量与混合气体总量的比值。分为:质量、容积、摩尔成分。 热力学第一定律:自然界一切物质都有能量,能量既不能被创造也不能被消灭,只能从一种形式转换成另一种形式,或从一个系统转移到另一个系统,而其总能量保持恒定。或者,第一类永动机是不可能制成的。 系统储存能(系统总能):是指热力学能(内能)、外部储存能(宏观动能和重力位能)的总和。 膨胀功(容积功):在压力差作用下,由于系统工质容积发生变化而传递的机械功。 轴功:系统通过机械轴与外界传递的机械功。 流动功(推动功):为推动流通通过控制界面而传递的机械功。 技术功:热力过程中可被直接用来做功的能量,膨胀功与流动功代数和。
化工热力学名词解释
化工热力学名词解释 1、(5分)偏离函数:* M M M R -= 指气体真实状态下的热力学性质M 与同一T ,P 下当气体 处于理想状态下热力学性质M* 之间的差额。 2、(5分)偏心因子: 000 .1)lg(7.0--==r T s r P ω 表示分子与简单的球形流体(氩,氪、氙) 分子在形状和极性方面的偏心度。 3、(5分)广度性质 4、(5分)R-K 方程(Redlich -Kwong 方程) 5、(5分)偏摩尔性质:偏摩尔性质 i j n P T i i n nM M ≠??=,,]) ([ 在T 、P 和其它组分量n j 均不变情况下,向无限多的溶液中加入1mol 的组分i 所引起的一系列热力学性质的变化。 6、(5分)超额性质:超额性质的定义是 M E = M -M id ,表示相同温度、压力和组成下,真实 溶液与理想溶液性质的偏差。ΔM E 与M E 意义相同。其中G E 是一种重要的超额性质,它与活度系数 7、(5分)理想溶液:理想溶液有二种模型(标准态):^ f i id = X i f i (LR ) 和 ^ f i id = X i k i (HL ) 有三个特点:同分子间作用力与不同分子间作用力相等,混合过程的焓变化,内能变化和体 积变化为零,熵变大于零,自由焓变化小于零。 8、(5分)活度: 化工热力学简答题 1、(8分)简述偏离函数的定义和作用。 偏离函数定义, * M M M R -= 指气体真实状态下的热力学性质M 与同一T ,P 下当气体处于理想状态下热力学性质M* 之间的差额。如果求得同一T ,P 下M R ,则可由理想气体的M* 计算真实气体的M 或ΔM 。 2、(8分)甲烷、乙烷具有较高的燃烧值,己烷的临界压力较低,易于液化,但液化石油气的主要成分既不是甲烷、乙烷也不是己烷,而是丙烷、丁烷和少量的戊烷。试用下表分析液化气成分选择的依据。
工程热力学名词解释专题
衡势差无限小,以致该系统在任意时刻均无限接工程热力学名词解释专题近于某个平衡态,这样的过程称为准静态过程 7、热力循环:热力系从某一状态开始,经历一参考哈工大的工程热力学和西交大的工程热注:系列中间状态后,又回复到原来状态。力学8、系统储存能:是指热力学能、宏观动能、和第一章——基本概念重力位能的总和。 9、热力系统:根据所研究问题的需要,把用某热力系与外界无物质交换的系统。1、闭口系统:种表面包围的特定物质和空间作为具体指定的热力系与外界有物质交换的系统。2、开口系统:热力学的研究对象,称之为热力系统。热力系与外界无热量交换的系统。3、绝热系统:、孤立系统:4热力系与外界有热量交换的系统。第二章——热力学第一定律、热力平衡状态:热力系在没有外界作用的情5、热力学第一定律:当热能与其他形式的能量1况下其宏观性质不随时间变化的状态。相互转换时,能的总量保持不变。或者,第一类、准静态过程:如果造成系统状态改变的不平6. 永动机是不可能制成的。第三章——热力学第二定律 、焓:可以理解为由于工质流动而携带的、并21、可逆过程:系统经过一个过程后,如果使热即热力学能与推动取决于热力状态参数的能量,力系沿原过程的路线反向进行并恢复到原状态,功的总和。将不会给外界留下任何影响。
、技术功:技术上可资利用的功,是稳定流动32、热力学第二定律:克劳修斯表述:不可能把系统中系统动能、位能的增量与轴功三项之和热从低温物体转移到高温物体而不引起其他变、稳态稳流:稳定流动时指流道中任何位置上4化。开尔文普朗克表述:不可能从单一热源吸热的流体的流速及其他状态参数都不随时间而变而使之全部 转变为功。 化流动。3、可用能与不可用能:可以转变为机械功的那部分热能称为可用能,不能转变为机械功的那部分热能称为不可用能。 、熵流:热力系和外界交换热量而导致的熵的4. 流动量5、熵产:由热力系内部的热产引起的熵的产生。)之:工作再两个恒温热源(和6、卡诺定理TT21第四章——气体的热力性质间的循环,不管采用什么工质,如果是可逆的,2T1、理想气体:分子本身不具有体积、分子间没,如果不是可逆的,其热效其热效率均为?11T2T有作用力的气体称为理想气体。。率恒小于?11T2、定压比热:单位质量的物质,在压力不变的工质在某一火用:、工质的对一定的环境而言,7条件下,作单位温度变化时相应的焓的变化。状态下所具有的热力学能中理论上可以转化为3、定容比热:单位质量的物质,在比体积不变可用能的部分。的条件下,作单位温度变化时相应的热力学能的、孤立系统的熵增原理:在孤立系内,一切实8变化。都朝着使系统熵增加的方际过程(不可逆过程)4、迈耶公式及使用条件:,适用于RCC??向进行,或者在极限情况下(可逆过程)维持系gpv00理想气体。统的熵不变。.
工程热力学 名词解释
1. 第一章 基本概念及定义 2. 热能动力装置:从燃料燃烧中得到热能,以及利用热能所得到动力的整套设备(包括辅助设备)统称热能动力装置。 3. 工质:热能和机械能相互转化的媒介物质叫做工质,能量的转换都是通过工质状态的变化实现的。 4. 高温热源:工质从中吸取热能的物系叫热源,或称高温热源。 5. 低温热源:接受工质排出热能的物系叫冷源,或称低温热源。 6. 热力系统:被人为分割出来作为热力学分析对象的有限物质系统叫做热力系统。 7. 闭口系统:如果热力系统与外界只有能量交换而无物质交换,则称该系统为闭口系统。(系统质量不变) 8. 开口系统:如果热力系统与外界不仅有能量交换而且有物质交换,则称该系统为开口系统。(系统体积不变) 9. 绝热系统:如果热力系统和外界间无热量交换时称为绝热系统。(无论开口、闭口系统,只要没有热量越过边界) 10. 孤立系统:如果热力系统和外界既无能量交换又无物质交换时,则称该系统为孤立系统。 11. 表压力:工质的绝对压力>大气压力时,压力计测得的差数。 12. 真空度:工质的绝对压力<大气压力时,压力计测得的差数,此时的压力计也叫真空计。 13. 平衡状态:无外界影响系统保持状态参数不随时间而改变的状态。充要条件是同时到达热平衡和力平衡。 14. 稳定状态:系统参数不随时间改变。(稳定未必平衡) 15. 准平衡过程(准静态过程):过程进行的相对缓慢,工质在平衡被破环后自动恢复平衡所需的时间很短,工质有足够的时间来恢复平衡,随时都不致显著偏离平衡状态,那么这样的过程就称为准平衡过程。它是无限接近于平衡状态的过程。 16. 可逆过程:完成某一过程后,工质沿相同的路径逆行回复到原来的状态,并使相互作用所涉及的外界亦回复到原来的状态,而不留下任何改变。可逆过程=准平衡过程+没有耗散效应(因摩擦机械能转变成热的现象)。 17. 准平衡与可逆区别:准平衡过程只着眼工质内部平衡;可逆过程是分析工质与外界作用产生的总效果,不仅要求工质内部平衡,还要求工质与外界作用可以无条件逆复。 18. 功:功是热力系统通过边界而传递的能量,且其全部效果可表现为举起重物。 19. 热量:热力系统与外界之间仅仅由于温度不同而通过边界传递的能量。 20. 两者不同:功是有规则的宏观运动的能量传递,在做功的过程中往往伴随着能量形态的转化。热量则是大量微观粒子杂乱热运动的能量传递,传递过程中不出现能量形态的转化。功转变成热量是无条件的而热量转变成功是有条件的。 21. 正向循环(热动力循环):热能转化成机械能的循环叫做正循环,它使外界得到功Wnet 。 22. 逆向循环:工质在循环中消耗机械能(或其他能量)把热量从低温热源传给高温热源的过程称为逆循环,消耗外功。 23. 第二章 热力学第一定律 24. 热力学第一定律:自然界中的一切物质都具有能量,能量不可能被创造,也不可能被消灭,但可以从一种形态转变为另一种形态,在能量的转换过程中能量的总量保持不变。(热力学第一定律就是能量守恒和转换定律在热现象中的体现)。内能的改变方式有两个:做功和热传递 ΔU = W + Q 。 25. 第一类永动机:不消耗能量便可以永远对外做功的动力机械。 26. 热力学能(内能):分子间的不规则运动的内动能,分子间的相互作用的内位能,维持分子结构的化学能,原子核内部的原子能,电磁场作用下的电磁能等一起构成热力学能。 27. 总能(总存储能):内能(热力学能),外能(宏观运动动能及位能)的总和称总能。 28. 推动功:工质在开口系统中流动而传递的功称为推动功mpv 。 29. 流动功:系统为维持工质流动所需的功称为流动功(推动功差p2V2-p1V1)。 30. 技术功:机械能可以全部转变为技术上可以利用的功,称为技术功(技术上可资利用的功)。 31. 体积功:工质因体积的变化与外界交换的功。 32. 焓:在热力设备中,工质总是不断的从一处流到另一处,随着工质的移动而转移的能量,即热力学能和推动功之和u+pv 。 33. 稳定流动过程:流动过程中,开口系统内部及其边界上各点工质的热力参数及运动参数都不随时间而变,则这种流动过程称为稳定流动过程。反之,则为不稳定流动过程或瞬变流动过程。 34. 节流:工质流过阀门等设备时,流动界面突然收缩,压力下降,这种现象称为节流。 35. 第三章 气体和蒸汽的性质 36. 标准大气压:在纬度45°的海平面上,当温度为0℃时,760毫米高水银柱产生的压强叫做标准大气压。 37. 理想气体:1.分子间是弹性的、不具有体积的质点;2.分子间相互没有作用力。 38. 摩尔气体常数:R=MRg=8.314 5 J/(mol ·K),与气体种类状态都无关。Rg 与气体种类有关,状态无关。Rg 物理意义是1 kg 某种理想气体定压升高1 K 对外作的功。 39. 定压比热容Cp :压力不变的条件下,1kg 物质在温度升高1K 所需的热量称为定压比热容。 40. 定容比热容Cv :体积不变的条件下,1kg 物质在温度升高1K 所需的热量称为定容比热容。Cp- Cv=Rg 气体常数。Cp/Cv=γ比热容比。 41. 湿饱和蒸汽:水蒸气和水的混合物称为湿饱和蒸汽。 42. 干饱和蒸汽:即饱和蒸汽,水全部变成蒸汽,这个时候的蒸汽称为干饱和蒸汽 43. 过热蒸汽:对饱和蒸汽继续定压加热,蒸汽温度升高,比体积增大,此时的蒸汽称为过热蒸汽。 44. 饱和状态:当汽化速度=液化速度时,系统处于动态平衡,宏观上气、液两相保持一定的相对数量。 45. 饱和温度:处于饱和状态的汽、液的温度相同称为饱和温度。 46. 饱和压力:处于饱和状态的蒸汽的压力称为饱和压力。 47. 过冷水:水温低于饱和温度时称为过冷水或未饱和水。 48. 过热度:温度超过饱和温度之值称为过热度 49. 汽化潜热:1kg 质量的某种液相物质在汽化过程中所吸收的热量。简称汽化潜热(液体蒸发吸收的热量)。 50. 第四章 气体与蒸汽的基本热力 51. 第五章 热力学第二定律 52. 热力学第二定律(克劳修斯说法):热不可能自发的、不付代价的从低温物体传至高温物体。 53. 热力学第二定律(开尔文说法):不可能制造出从单一热源吸热,使之全部转化为功而不留下其他任何变化的热力发动机。 54. 造成过程不可逆的两大因素:1、耗散效应。2、有限势差作用下的非准平衡变化。 55. 卡诺循环:工作于温度分别为1T 和2T 的两个热源之间的正向循环,由两个可逆定温过程和两个可逆绝热过程组成。 56. 概况性卡诺循环:双热源间的极限回热循环称为概括性卡诺循环。 57. 回热:用工质原本排出的热量加热工质本身的方法。 58. 熵产:由耗散热产生的熵增量叫做熵产。(闭口系内不可逆绝热过程中,存在不可逆因素引起耗散效应,使损失的机械能转化为热能被工质吸收,导致熵增大)。 59. 熵流:系统与外界换热量与热源温度的比值,称为熵流。 60. 孤立系统的熵增原理:孤立系统中的各种不可逆因素表现为系统的机械功损失,产生机械功不可逆地转化为热的效果,使孤立系统的熵增大。称为孤立系统的
化工热力学各章节习题
化工热力学各章节习题 第一章 绪论 一、选择题(共3小题,3分) 1、(1分)关于化工热力学用途的下列说法中不正确的是( ) A.可以判断新工艺、新方法的可行性。 B.优化工艺过程。 C.预测反应的速率。 D.通过热力学模型,用易测得数据推算难测数据;用少量实验数据推算大量有用数据。 E.相平衡数据是分离技术及分离设备开发、设计的理论基础。 2、(1分)关于化工热力学研究特点的下列说法中不正确的是( ) (A )研究体系为实际状态。 (B )解释微观本质及其产生某种现象的内部原因。 (C )处理方法为以理想态为标准态加上校正。 (D )获取数据的方法为少量实验数据加半经验模型。 (E )应用领域是解决工厂中的能量利用和平衡问题。 3、(1分)关于化工热力学研究内容,下列说法中不正确的是( ) A.判断新工艺的可行性。 B.化工过程能量分析。 C.反应速率预测。 D.相平衡研究 参考答案 一、选择题(共3小题,3分) 1、(1分)C 2、(1分)B 3、(1分)C 第二章 流体的PVT 关系 一、选择题(共17小题,17分) 1、(1分)纯流体在一定温度下,如压力低于该温度下的饱和蒸汽压,则此物质的状态为( )。 A .饱和蒸汽 B.饱和液体 C .过冷液体 D.过热蒸汽 2、(1分)超临界流体是下列 条件下存在的物质。 A.高于T c 和高于P c B.临界温度和临界压力下 C.低于T c 和高于P c D.高于T c 和低于P c 3、(1分)对单原子气体和甲烷,其偏心因子ω,近似等于 。 A. 0 B. 1 C. 2 D. 3 4、(1分)0.1Mpa ,400K 的2N 1kmol 体积约为__________ A 3326L B 332.6L C 3.326L D 33.263 m 5、(1分)下列气体通用常数R 的数值和单位,正确的是__________ A K kmol m Pa ???/10314.83 3 B 1.987cal/kmol K C 82.05 K atm cm /3 ? D 8.314K kmol J ?/
热力学概念名词解释
热力学概念名词解释
传热学名词解释 一、绪论 1.热流量:单位时间内所传递的热量 2.热流密度:单位传热面上的热流量 3.导热:物体各部分之间不发生相对位移时,依靠物质微粒(分子、原子或自由电子)的热运动而产生的热能传递,称为导热。 4.对流传热:流体流过固体壁时的热传递过程,就是热对流和导热联合用的热量传递过程,称为表面对流传热,简称对流传热。5.辐射传热:物体间通过热辐射而进行的热量传递,称辐射传热。6.总传热过程:热量从温度较高的流体经过固体壁传递给另一侧温度较低流体的过程,称为总传热过程,简称传热过程。 7.对流传热系数:单位时间内单位传热面当流体温度与壁面温度差为1K是的对流传热量,单位为W/(m2·K)。对流传热系数表示对流传热能力的大小。 8.辐射传热系数:单位时间内单位传热面当流体温度与壁面温度差为1K是的辐射传热量,单位为W/(m2·K)。辐射传热系数表示辐射传热能力的大小。 9.复合传热系数:单位时间内单位传热面当流体温度与壁面温度差为1K是的复合传热量,单位为W/(m2·K)。复合传热系数表示复合传热能力的大小。 10.总传热系数:总传热过程中热量传递能力的大小。数值 上表示传热温差为1K时,单位传热面积在单位时间内的传 热量。
二、热传导 1.温度场:某一瞬间物体内各点温度分布的总称。一般来说,它是空间坐标和时间坐标的函数。 2.等温面(线):由物体内温度相同的点所连成的面(或线)。3.温度梯度:在等温面法线方向上最大温度变化率。 4.热导率:物性参数,热流密度矢量与温度降度的比值,数值上等于1 K/m的温度梯度作用下产生的热流密度。热导率是材料固有的热物理性质,表示物质导热能力的大小。 5.导温系数:材料传播温度变化能力大小的指标。 6.稳态导热:物体中各点温度不随时间而改变的导热过程。 7.非稳态导热:物体中各点温度随时间而改变的导热过程。 8.傅里叶定律:在各向同性均质的导热物体中,通过某导热面积的热流密度正比于该导热面法向温度变化率。 9.保温(隔热)材料:λ≤0.12W/(m·K)(平均温度不高于350℃时)的材料。10.肋效率:肋片实际散热量与肋片最大可能散热量之比。 11.接触热阻:材料表面由于存在一定的粗糙度使相接触的表面之间存在间隙,给导热过程带来额外热阻。 12.定解条件(单值性条件):使微分方程获得适合某一特定 问题解的附加条件,包括初始条件和边界条件。 三、对流传热 1.速度边界层:在流场中壁面附近流速发生急剧变化的薄层。2.温度边界层:在流体温度场中壁面附近温度发生急剧变化的薄层。
结构抗震设计(试题及答案)
44、场地 参考答案: 指工程群体所在地,具有相似的反应谱特征。其范围相当于厂区,居民小区和自然村或不小于1.0 km2的平面面 45、反应谱 参考答案: 单自由度弹性体系在给定的地震作用下,某个最大反应量与体系自振周期的关系曲线 46、地震波 参考答案: -地震引起的振动以波的形式从震源向各个方向传播并释放能量,这就是地震波,地震波是一种弹性波 47、强柱弱梁 参考答案: 结构设计时希望梁先于柱发生破坏,塑性铰先发生在梁端,而不是在柱端。 48、动力自由度 参考答案: 简单的说就是自由度。是用了确定一个体系在振动过程中全部质量的位置所需独立几何参数的数目。 49、二阶效应 参考答案: 相对钢筋混凝土结构房屋,钢结构房屋较揉,容易产生较大的侧向变形。在这种情况下,重力荷载与侧向位也即所谓的二阶效应。 50、场地土的液化 参考答案: 饱和的粉土或砂土,在地震时由于颗粒之间的孔隙水不可压缩而无法排出,使得孔隙水压力增大,土体颗粒的部或全部处于悬浮状态,土体的抗剪强度接近于零,呈现出液态化的现象。 51、基本烈度 参考答案: 50年期限内,一般场地条件下,可能遭受超越概率10%的烈度值 52、等效剪切波速 参考答案: 若计算深度范围内有多层土层,则根据计算深度范围内各土层剪切波速加权平均得到的土层剪切波速即为等效剪 53、重力荷载代表值 参考答案: 结构抗震设计时的基本代表值,是结构自重(永久荷载)和有关可变荷载的组合值之和。
54、什么是楼层屈服强度系数?怎样判别结构薄弱层位置? 参考答案: 什么是楼层屈服强度系数?怎样判别结构薄弱层位置? 答:楼层屈服承载力系数是按构件实际配筋和材料强度标准值计算的楼层受剪承载力和按罕遇地震剪力的比值,它反映了结构中楼层的承载力与该楼层所受弹性地震剪力的相对关系。5分 薄弱层位置的确定:楼层屈服承载力系数沿高度分布均匀的结构可取底层为薄弱层;楼层屈服承载的结构,可取该系数最小的楼层和相对较小的楼层为薄弱楼层,一般不超过2~3处;单层厂房, 55、什么是鞭端效应,设计时如何考虑这种效应? 参考答案: 地震作用下突出建筑物屋面的附属小建筑物,由于质量和刚度的突然变小,受高振型影响较大,震为鞭端效应;(5分)设计时对突出屋面的小建筑物的地震作用效应乘以放大系数3,但此放大系 56、简述框架节点抗震设计的基本原则。 参考答案: 1、节点的承载力不应低于其连接构件的承载力; 2、多遇地震时节点应在弹性范围内工作; 3、罕遇地震时节点承载力的降低不得危及竖向荷载的传递; 4、梁柱纵筋在节点区内应有可靠的锚固; 5、节点配筋不应使施工过分困难。 57、什么是动力系数、地震系数和水平地震影响系数?三者之间有何关系? 参考答案: 动力系数是单质点弹性体系的最大绝对加速度反应与地震地面运动最大加速度的比值; 地震系数是地震地面运动最大加速度与重力加速度的比值; 水平地震影响系数是单质点弹性体系的最大绝对加速度反应与重力加速度的比值; 水平地震影响系数是地震系数与动力系数的乘积 58、简述两阶段三水准抗震设计方法 参考答案:
化工热力学名词解释讲课教案
化工热力学名词解释
化工热力学名词解释 1、(5分)偏离函数:* M M M R -= 指气体真实状态下的热力学性质M 与同一T , P 下当气体处于理想状态下热力学性质M* 之间的差额。 2、(5分)偏心因子: 000 .1)lg(7.0--==r T s r P ω 表示分子与简单的球形流体(氩, 氪、氙)分子在形状和极性方面的偏心度。 3、(5分)广度性质 4、(5分)R-K 方程(Redlich -Kwong 方程) 5、(5分)偏摩尔性质:偏摩尔性质 i j n P T i i n nM M ≠??=,,]) ([ 在T 、P 和其它组分量n j 均不变情况下,向无限多的溶液中加入1mol 的组分i 所引起的一系列热力学性质的变化。 6、(5分)超额性质:超额性质的定义是 M E = M -M id ,表示相同温度、压力和组成下,真实溶液与理想溶液性质的偏差。ΔM E 与M E 意义相同。其中G E 是一种重要的超额性质,它与活度系数 7、(5分)理想溶液:理想溶液有二种模型(标准态):^ f i id = X i f i (LR ) 和 ^ f i id = X i k i (HL ) 有三个特点:同分子间作用力与不同分子间作用力相等,混合过程的焓变化,内能变化和体积变化为零,熵变大于零,自由焓变化小于零。 8、(5分)活度: 化工热力学简答题 1、(8分)简述偏离函数的定义和作用。 偏离函数定义, * M M M R -= 指气体真实状态下的热力学性质M 与同一T ,P 下当气体处于理想状态下热力学性质M* 之间的差额。如果求得同一T ,P 下M R ,则可由理想气体的M* 计算真实气体的M 或ΔM 。 2、(8分)甲烷、乙烷具有较高的燃烧值,己烷的临界压力较低,易于液化,但液化石油气的主要成分既不是甲烷、乙烷也不是己烷,而是丙烷、丁烷和少量
