高考全国1卷化学选择题训练

高三化学选择题训练1
一、选择题(共7小题,每小题6分,满分42分)
7.食品添加剂关系到大家健康,下列物质中的添加剂作用不正确的是()
A.①B.②C.③D.④
8.下列与处理方法对应的反应方程式不正确的是()
A.工业上用水吸收NO2生产硝酸:3NO2 + H2O = 2HNO3 + NO
B.用氨水除去工业原料氯化铵中的氯化铁杂质:Fe3+ + 3OH- = Fe(OH)3↓
C.用熟石灰处理泄漏的液氯:2Ca(OH)2 +2Cl2 = CaCl2 + Ca(ClO)2 +2H2O
D.用明矾除去水中的悬浮颗粒物:Al3+ + 3H2O Al(OH)3(胶体) + 3H+
9.下列说法不正确的是()
A.乙二醇用于汽车防冻液
B.麦芽糖在水解前后均能发生银镜反应
C.1-氯丙烷和2-氯丙烷发生消去反应的产物不同
D.H2N—CH2—COOH的缩聚产物中含结构
10.短周期四种元素离子W2+、X -、Y2-、Z+的电子层结构相同。下列说法正确的是()A.原子序数:W>Z>X>Y
B.离子半径:r(W2+)>r(X一)>r(Y2-)>r(Z+)
C.Y的气态氢化物比X的气态氢化物稳定
D.氢氧化物碱性强弱:W(OH)2>ZOH
11.下图为Pt电极的氢氧燃料电池工作原理示意图,H2SO4为电解质溶液。有关说法不正
确的是()
A.a极为负极,电子由a极流向b极
B.a极的电极反应式是:H2 -2e- = 2H+
C.电池工作一段时间后,装置中c(H2SO4)增大
D.若将H2改为等物质的量CH4,O2的用量增多
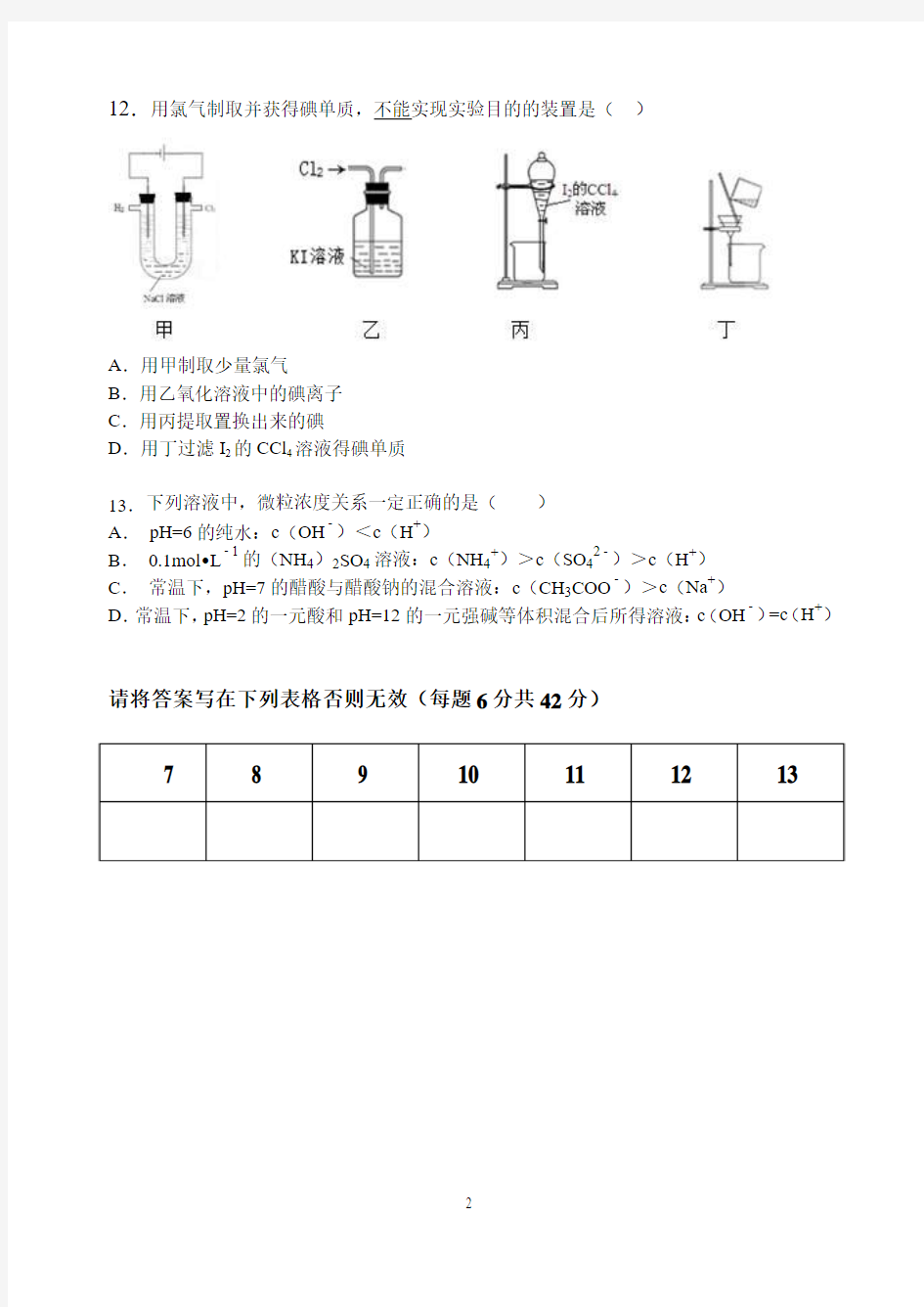
12.用氯气制取并获得碘单质,不能实现实验目的的装置是()
A.用甲制取少量氯气
B.用乙氧化溶液中的碘离子
C.用丙提取置换出来的碘
D.用丁过滤I2的CCl4溶液得碘单质
13.下列溶液中,微粒浓度关系一定正确的是()
A.pH=6的纯水:c(OH﹣)<c(H+)
B.0.1mol?L﹣1的(NH4)2SO4溶液:c(NH4+)>c(SO42﹣)>c(H+)
C.常温下,pH=7的醋酸与醋酸钠的混合溶液:c(CH3COO﹣)>c(Na+)
D.常温下,pH=2的一元酸和pH=12的一元强碱等体积混合后所得溶液:c(OH﹣)=c(H+)请将答案写在下列表格否则无效(每题6分共42分)
高三化学选择题训练2
一、选择题(共7小题,每小题6分,满分42分)
7.据《自然》杂志报道,在300~400℃的高温下,将砂糖(主要成分为蔗糖)等碳水化合物用加热的方法使其形成焦糖与碳之间的“半成品碳”状态,再放进硫酸溶液中高温加热,生成了一种叫“焦糖烯”的物质,其分子式为C36H50O25。下列有关说法正确的是A.向蔗糖中加入浓硫酸发生一系列反应,浓硫酸主要体现吸水性和酸性
B.“半成品碳”是碳元素的一种新单质,与C60都是碳元素的同素异形体
C.蔗糖的水解产物之一在碱性条件下加热,可与银氨溶液反应
D.焦糖烯是一种新型的烯烃,其能使溴的四氯化碳溶液褪色
8.下列有关实验装置进行的相应实验,能达到实验目的的是
A.用图1装置说明反应2NO2(g)N2O4(g) △H>0
B.用图2所示装置可制取大量的CO2气体
C.用图3装置制备Fe(OH)2并能较长时间观察其颜色
D.用图4所示装置可分离溴的四氯化碳溶液和水
9.下列有机物只有四种同分异构体的是
A.分子式为C4H10烷烃的二氯取代物
B.分子式为C3H9N的有机物,其中N原子以三个单键与其他原子相连
C.乙苯的二氯取代物 D.分子式为C4H8的有机物
10.以氨作为燃料的固体氧化物(含有O2-)燃料电池,具有全固态结构、能量效率高、
环保等特点,另外氨气含氢量高,不含碳,易液化,方便运输和贮存,是很好的氢源载体。其工作原理如图所示,下列关于氨固体氧化物燃料电池的说法正确的是
A.该电池工作时的总反应为:4NH3+5O2=4NO+6H2O
B.固体氧化物作为电池工作的电解质,其作用便于电子
在电池内移动
C. 电池工作时,在接触面上发生的电极反应为:
2NH3+3O2——6e—=N2+3H2O
D.外电路的电流方向为从电极a流向电极b
11.设N A为阿伏加德罗常数的值。下列说法正确的是
A.1. 6g由氧气和臭氧组成的混合物中含有氧原子的数目为0.1N A
B.标准状况下,1L戊烷充分燃烧后生成的气态产物的分子数为5/22. 4N A
C.pH=13的NaOH溶液中含有的OH-为0. 1mol
D.在过氧化钠与水的反应中,每生成0. 1mol氧气,转移电子的数目为0.4N A 12.短周期元素X、Y、Z的原子序数依次递增,其原子的最外层电子数之和为13,X与Y、Z位于相邻周期,Z原子最外层电子数是X原子内层电子数的3倍或者是Y原子最外层电子数的3倍,下列说法正确的是()
A.X的氢化物溶于水生成弱酸
B.Z的氢化物的水溶液在空气中存放不易变质
C.Y与X可生成Y3X2型化合物
D.Z的单质在氧气中燃烧可以生成两种酸性氧化物
13.高铁酸钾(K2FeO4)是一种高效多功能水处理剂,具有极强的氧化性,已知:4FeO42-+
10H2O4Fe(OH)3+8OH-+3O2↑。高铁酸钾常见制备方法之一是湿法制备:在一定条件下,Fe(NO3)3与NaClO反应生成紫红色高铁酸盐溶液。下列说法正确的是
A. K2FeO4在处理水的过程中所起的作用只有消毒杀菌
B.同浓度的高铁酸钾在pH=ll.50的水溶液中比中性溶液中稳定
C.湿法制备高铁酸钾,可以在酸性环境中顺利进行
D.湿法制备高铁酸钾,Fe(NO3)3与NaClO物质的量之比为3:2
请将答案写在下列表格否则无效(每题6分共42分)
高三化学选择题训练3
一、选择题(共7小题,每小题6分,满分42分)
7.下列有关化学用语表示正确的是()
①CSO的电子式:②次氯酸结构简式:H﹣Cl﹣O
③Cl﹣的结构示意图:④甲烷分子的比例模型:
⑤葡萄糖的实验式:CH2O ⑥原子核内有20个中子的氯原子:
⑦HCO3﹣的水解方程式为:HCO3﹣+H2O?CO32﹣+H3O+.
A.①④⑤ B.②③④⑥ C.③⑤⑥⑦ D.全部正确
8.甲酸香叶酯是一种食品香料.可以由香叶醇与甲酸发生酯化反应制得.下列说法中正
确的是()
A.香叶醇的分子式为C11H18O
B.香叶醇在浓硫酸、加热条件下可发生消去反应
C. 1 mol甲酸香叶酯可以与2 molH2发生加成反应
D.甲酸香叶酯分子中所有碳原子均可能共平面
9.短周期元素X、Y、Z、W的原子序数依次增大,X原子最外层电子数是其内层电子总数的3倍,Y原子最外层只有2个电子,Z单质可制成半导体材料,W与X属于同一主族.下列叙述正确的是()
A.元素X的简单气态氢化物的热稳定性比W的弱
B.元素W的最高价氧化物对应水化物的酸性逐渐比Z弱
C.原子半径的大小顺序:r Y>r Z>r W>r X
D.化合物YX、ZX2、WX3中化学键类型相同
10.已知:
①4NH3(g)+3O2(g)=2N2(g)+6H2O(g)△H=﹣1269kJ/mol
②
下列说正确的是()
A.断开1 mol O﹣O键比断开1 mol N﹣N键所需能量少448kJ
B.断开1 mol H﹣O键比断开1 mol H﹣N键所需能量相差约72.6kJ
C.由以上键能的信息可知H2O的沸点比NH3高
D.由元素非金属性的强弱可知H一O键比H一N键弱
11.已知25℃时,CaSO4在水中的沉淀溶解平衡曲线,如图所示,向100mL该条件下的CaSO4饱和溶液中,加入400mL 0.01mol/L的Na2SO4溶液,针对此过程的下列叙述正确的是()
A.溶液中析出CaSO4沉淀,最终溶液中c(SO42-)较原来大
B.溶液中无沉淀析出,溶液中c(Ca2+)、c(SO42-)都变小
C.溶液中析出CaSO4沉淀,溶液中c(Ca2+)、c(SO42-)都变小
D.溶液中无沉淀析出,但最终溶液中c(SO42-)较原来大
12.有芳香气味的C9H18O2在酸性条件下加热可水解产生相对分子质量相同的两种有机物,则符合此条件的C9H18O2的结构有()
A.8种B.14种C.16种D.18种
13.下述实验设计能够达到目的是()
请将答案写在下列表格否则无效(每题6分共42分)
高三化学选择题训练4
一、选择题(共7小题,每小题6分,满分42分)
7.下列说法或表达正确的是
A.乙醇、糖类和蛋白质都是人体必需的营养物质
B.NH4I的电子式:
C.石油是混合物,其分馏产品汽油也是混合物
D.陶瓷、水晶、水泥、玻璃都属于硅酸盐
8.用下列实验装置和方法进行相应实验,能达到实验目的的是
A.用甲装置制干燥的氨气
B.用乙装置收集并测量Cu与浓硝酸反应产生的气体及体积
C.用丙装置除去CO2中含有的少量HC1
D.用丁装置吸收NH3,并防止倒吸
9.有机物C4H8Cl2的结构中只含有一个甲基的同分异构体有几种(不考虑立体异构)A.3 B.4 C.7 D.8
10.下表中对离子方程式的评价不合理的是
11.设NA为阿伏加德罗常数,下列叙述中正确的是
A.足量铁在氯气中反应,l mol铁失去的电子数为2 NA
B.标准状况下22.4 L H2中含中子数为2 NA
C.1 L Imol/L的盐酸溶液中,所含氯化氢分子数为NA
D.常温下46 g NO2和N2O4混合气体中含有原子数为3NA 12.下列根据实验操作和现象所得出的结论正确的是
13.几种短周期元素的原子半径及主要化合价如下表:
下列叙述正确的是
A.离子半径:W<X B.气态氢化物的稳定性:Z>W C.化合物X3Z2中既含有离子键又含有共价键
D.最高价氧化物对应水化物的酸性:Z>Y
高三化学选择题训练5
一、选择题(共7小题,每小题6分,满分42分)
7.下列过程没有发生化学反应的是()
A.用活性炭去除冰箱中的异味
B.用热碱水清除炊具上残留的油污
C.用浸泡过高锰酸钾溶液的硅藻土保鲜水果
D.用含硅胶、铁粉的透气小袋与食品一起密封包装
8.联苯(两个苯环单键相连)的二氯代物有()
A.10种B.11种C.12种D.13种9.下列反应中,反应后固体物质质量不变的是()
A.氢气通过灼热的CuO粉末B.二氧化碳通过Na2O2粉末
C.铝与Fe2O3发生铝热反应D.将锌粒投入Cu(NO3)2溶液10.从矿物学资料查得,一定条件下自然界存在如下反应
14CuSO4+5FeS2+12H2O=7Cu2S+5FeSO4+12H2SO4.下列说法正确的是()A.Cu2S既是氧化产物又是还原产物
B.5molFeS2发生反应,有10mol电子转移
C.产物中的SO42﹣离子有一部分是氧化产物
D.FeS2只作还原剂
11.在恒温时,一固定容积的容器内发生如下反应:2NO2(g)?N2O4(g)达到平衡时,再向容器内通入一定量的NO2(g),重新达到平衡后,与第一次平衡时相比,NO2的体积分数()
A.不变B.增大C.减小D.无法判断12.一定温度下,下列溶液的离子浓度关系式正确的是()
A.pH=5的H2S溶液中,c(H+)=c(HS﹣)=1×10﹣5mol?L﹣1
B.pH=a的氨水溶液,稀释10倍后,其pH=b,则a=b+1
C.pH=2的H2C2O4溶液与pH=12的NaOH溶液任意比例混合:c(Na+)+c(H+)=c(OH﹣)+c(HC2O4﹣)
D.pH相同的①CH3COONa②NaHCO3③NaClO三种溶液的c(Na+):①>②>③
13.室温下,将1mol的CuSO4?5H2O(s)溶于水会使溶液温度降低,热效应为△H1,将1mol的CuSO4(s)溶于水会使溶液温度升高,热效应为△H2:CuSO4?5H2O受热分解的化学方程式为CuSO4?5H2O(s)CuSO4(s)+5H2O(l),热效应为△H3,则下列判断正确的是()
A.△H2>△H3B.△H1<△H3C.△H1+△H3=△H2D.△H1+△H2>△H3
7 8 9 10 11 12 13
全国卷高考化学选择题汇编
1.[化学常识]下列叙述正确的是A.锥形瓶可用作加热的反应器 B.室温下,不能将浓硫酸盛放在铝桶中 C.可以使用碱式滴定管量取高锰酸钾溶液 D.用蒸馏水润湿的试纸测溶液的pH,一定会使结果偏低 2.化学与生活密切相关,下列有关说法错误的是 A.用灼烧的方法可以区分蚕丝和人造纤维 B.食用油反复加热会产生稠环芳香烃等有害物质 C.加热能杀死流感病毒是因为蛋白质受热变性 D.医用消毒酒精中乙醇的浓度为85% 3.下列关于有机化合物的说法正确的是 A.2-甲基丁烷也称为异丁烷 B.由乙烯生成乙醇属于加成反应 C.C4H9Cl有3种同分异构体 D.油脂在酸性条件下水解叫做皂化反应 4.下列叙述错误的是 A.SO使溴水褪色与乙烯使KMnO溶液褪色的原理相同 B.制备乙酸乙酯时可用热的NaOH溶液收集产物以除去其中的乙酸 C.用饱和食盐水替代水跟电石反应,可以减缓乙炔的产生速率 D.用AgNO溶液可以鉴别KC1和KI 5.下列叙述中,错误 ..的是 A.苯与浓硝酸、浓硫酸共热并保持55~60℃反应生成硝基苯 B.苯乙烯在合适条件下催化加氢可生成乙基环己烷 C.乙烯和溴的四氯化碳溶液反应生成1,2-二溴乙烷
D.甲苯与氯气在光照下反应主要生成2,4-二氯甲苯 6、[离子方程]能正确表示下列反应的离子方程式是 A.用过量氨水吸收工业尾气中的SO2:2NH3·H20+SO22NH4++SO32-+H2O B.氯化钠与浓硫酸混合加热:H2SO4+2Cl-SO2↑+Cl2↑+H2O C.磁性氧化铁溶于稀硝酸:3Fe2++4H++NO3-3Fe3++NO↑+3H2O D.明矾溶液中滴入Ba(OH)2溶液使SO42-恰好完全沉淀: 2Ba2++3OH-+Al3++2SO42-2BaSO4↓+Al(OH)3↓ 7.下列离子方程式错误的是 A.向Ba(OH)2溶液中滴加稀硫酸:Ba2++2OH-+2H++SO42—=BaSO4↓+2H2O B.酸性介质中KMnO4氧化H2O2:2MnO4-+5H2O2+6H+=2Mn2++5O2↑+8H2O C.等物质的量的MgCl2、Ba(OH)2和HC1溶液混合:Mg2++2OH-=Mg(OH)2↓ D.铅酸蓄电池充电时的正极反应:PbSO4+2H2O-2e-=PbO2+4H++SO42— 8.[阿伏伽德罗常数]NA表示阿伏加德罗常数,下列叙述正确的是A.lmolFeI与足量氯气反应时转移的电子数为2N B.2L0.5mol?L硫酸钾溶液中阴离子所带电荷数为N C.1molNaO固体中含离子总数为4N A D.丙烯和环丙烷组成的42g混合气体中氢原子的个数为6N 9.设N A为阿伏加德罗常数值。下列有关叙述正确的是 A.14 g乙烯和丙烯混合气体中的氢原子数为2N A B.1molN2与4molH2反应生成的NH3分子数为2N A C.1molFe溶于过量硝酸,电子转移数为2N A D.标准状况下,2.24LCCl4含有的共价键数为0.4N A 10.设N A为阿伏加德罗常数,下列叙述中正确的是 A.0.1mo l·L-1的NH4NO3溶液中含有的氮原子数为0.2N A B.1mol氯气分别与足量铁和铝完全反应时转移的电子数均为3N A
课标高考化学选择题专项练习NA的计算与应用
选择题专项训练二N A的计算与应用 题型专项训练第31页 1.设N A为阿伏加德罗常数的值,下列叙述正确的是() A.常温下,1 L 0.1 mol·L-1 NH4NO3溶液中,氮原子数为0.2N A B.1 mol羟基中的电子数为10N A C.在含4 mol Si—O键的二氧化硅中,氧原子数为4N A ,22.4 L乙烯中C—H键数为4N A 答案:A 解析:常温下,1 L 0.1 mol·L-1 NH4NO3溶液中含有硝酸铵的物质的量为0.1 mol,氮原子数为 0.2N A,A正确;1 mol羟基中电子数为9N A,B错误;含4 mol Si—O键的二氧化硅的物质的量为1 mol,含有2 mol氧原子,氧原子数为2N A,C错误;常温常压V m>22.4 L·mol-1,22.4 L乙烯物质的量小于1 mol,D错误。 2.设N A表示阿伏加德罗常数的值,下列叙述中不正确的是() A.室温下,46 g NO2和N2O4的混合气体中含有N A个氮原子 B.1 mol 12C18O2中所含的中子数为26N A C.常温下,1 L 0.1 mol·L-1 CH3COONa溶液中含有的CH3COO-和Na+总数为0.2N A ,1 L pH=12的氨水中含有OH-的数目为0.01N A 答案:C 解析:NO2和N2O4的混合气体可以看作由基本结构单元NO2组成,则46 g混合气体中所含有的氮原子的物质的量为1 mol,含有N A个氮原子,A项正确;1 mol 12C18O2中所含的中子数为 (6+10×2)N A=26N A,B项正确;由于CH3COO-水解,则CH3COO-和Na+总数小于0.2N A,C项错误;常温下,pH=12的氨水中c(OH-)=0.01 mol·L-1,1 L pH=12的氨水中含有OH-的数目为0.01N A,D 项正确。 3.(2019福州高三检测)设N A为阿伏加德罗常数的值,下列叙述正确的是() A.1 L 0.2 mol·L-1亚硫酸钠溶液中H2SO3、HS O3-、S O32-的总数为0.2N A B.标准状况下,等物质的量的C2H4和CH4所含的氢原子数均为4N A C.向含1 mol FeI2的溶液中通入等物质的量的Cl2,转移的电子数为N A 的硫酸溶液中含氧原子数为0.4N A 答案:A 4.设N A为阿伏加德罗常数的值。下列说法正确的是() A.12 g金刚石晶体中含有的C—C键的数目为2N A B.1 L 1 mol·L-1 AlCl3溶液中含有的Al3+数目为N A C.在标准状况下,11.2 L氯气通入足量的NaOH溶液中转移电子数为N A 重水(D2O)含有的中子数为10N A 答案:A 解析:金刚石晶体中每个C平均占有两个C—C键,故12 g(1 mol)金刚石晶体中含有C—C的数目为2N A,A项正确;AlCl3溶液中由于Al3+水解,1 L 1 mol·L-1 AlCl3溶液中含有Al3+数目小于 N A,B项错误;标准状况下,11.2 L氯气通入足量的NaOH溶液中转移电子数为0.5N A,C项错误;1个D2O中含10个中子,18 g D2O小于1 mol,含中子数小于10N A,D项错误。 5.设N A表示阿伏加德罗常数的值,下列说法正确的是() A.标准状况下,1.12 L 1H2和0.2 g 2H2均含有0.1N A个质子 B.在同压不同温的情况下,质量相同的氧气和臭氧所含氧原子数不相同 C.标准状况下,11.2 L庚烷完全燃烧后生成的CO2分子数为3.5N A
高考化学选择题专题
潮阳一中明光学校高考化学选择题限时训练25(限时40分钟) ----------离子共存、离子方程式 一、单项选择题(每小题4分) 1、(2010广东理综7)能在溶液中大量共存的一组离子是 A . 4NH + 、Ag + 、34PO - 、Cl - B.3Fe +、H +、I -、 3HCO - C.K +、 + Na 、 -3NO 、 - 4MnO D.Al 3+、2+Mg 、2-4SO 、 2-3CO 2、(2011广东理综8)能在水溶液中大量共存的一组离子是 A. H +、I ―、NO 3―、SiO 32- B. Ag +、Fe 3+、Cl ―、SO 42― C.K +、SO 42-、Cu 2+、NO 3― D.NH 4+、OH -、Cl -、HCO 3- 3、(2010全国卷1)能正确表示下列反应的离子方程式是 A .将铜屑加入3+Fe 溶液中:3+2+2+2Fe +Cu=2Fe +Cu B .将磁性氧化铁溶于盐酸:+3+342Fe O +8H =3Fe +4H O C .将氯化亚铁溶液和稀硝酸混合:2++332Fe +4H +NO =Fe +2H O+NO -+↑ D .将铁粉加入稀硫酸中:+322Fe+6H =2Fe 3H ++↑ 4、(2010天津卷5)下列实验设计及其对应的离子方程式均正确的是 A .用F e C l 3溶液腐蚀铜线路板:Cu + 2F e 3+ = Cu 2+ + 2Fe 2+ B .Na 2O 2与H 2O 反应制备O 2 :Na 2O 2 + H 2O = 2N a + + 2O H - + O 2↑ C .将氯气溶于水制备次氯酸:C l 2 + H 2O = 2H + + Cl - + ClO - D .用浓盐酸酸化的K M n O 4溶液与H 2O 2反应,证明H 2O 2具有还原性: 2MnO 4- + 6H + + 5H 2O 2 = 2Mn 2+ + 5O 2↑ + 8H 2O 5、(2010安徽卷9)在pH=1的溶液中能大量共存的一组离子或分子是 A.Na +、Mg 2+、ClO —、NO 3— B. Al 3+、 NH 4+、 Br - 、Cl - C. K + 、Cr 2O 72- 、CH 3CHO 、 SO 42- D. Na +、K + 、SiO 32-、Cl - 6、(2010上海卷9)下列离子组一定能大量共存的是 A .甲基橙呈黄色的溶液中:I -、Cl -、NO 3-、Na + B .石蕊呈蓝色的溶液中:Na +、AlO 2-、NO 3-、HCO 3- C .含大量Al 3+的溶液中:K +、Na +、NO 3-、ClO - D .含大量OH 一的溶液中:CO 32-、Cl -、F -、K + 7、(2010上海卷19)下列反应的离子方程式正确的是 A .苯酚与碳酸钠溶液的反应 B .等体积、等浓度的Ca(HCO 3)2溶液和NaOH 溶液混合 223332222Ca HCO OH CaCO CO H O +---++??→↓++
近三年高考化学选择题(全国卷)
17-1 7.下列生活用品中主要由合成纤维制造的是 A.尼龙绳B.宣纸C.羊绒衫D.棉衬衣 8.《本草衍义》中对精制砒霜过程有如下叙述:“取砒之法,将生砒就置火上,以器覆之,令砒烟上飞着覆器,遂凝结累然下垂如乳,尖长者为胜,平短者次之。”文中涉及的操作方法是 A.蒸馏B.升华C.干馏D.萃取 9.已知(b )、(d )、(p)的分子式均为C6H6,下列说法正确的是 A.b的同分异构体只有d和p两种 B.b、d、p的二氯代物均只有三种 & C.b、d、p均可与酸性高锰酸钾溶液反应 D.b、d、p中只有b的所有原子处于同一平面 10.实验室用H2还原WO3制备金属W的装置如图所示(Zn粒中往往含有碳等杂质,焦性没食子酸溶液用于吸收少量氧气),下列说法正确的是 A.①、②、③中依次盛装KMnO4溶液、浓H2SO4、焦性没食子酸 溶液 B.管式炉加热前,用试管在④处收集气体并点燃,通过声音判断 气体纯度 C.结束反应时,先关闭活塞K,再停止加热 D.装置Q(启普发生器)也可用于二氧化锰与浓盐酸反应制备氯气 % 11.支持海港码头基础的防腐技术,常用外加电流的阴极保护法进行防腐,工作原理如图所示,其中高硅铸铁为惰性辅助阳极。下列有关表述不正确的是 A.通入保护电流使钢管桩表面腐蚀电流接近于零 B.通电后外电路电子被强制从高硅铸铁流向钢管桩 C.高硅铸铁的作用是作为损耗阳极材料和传递电流 D.通入的保护电流应该根据环境条件变化进行调整 12.短周期主族元素W、X、Y、Z的原子序数依次增大,W的简单氢化物可用作制冷剂,Y的原子半径是所有短周期主族元素中最大的。由X、Y和Z三种元素形成的一种盐溶于水后,加入稀盐酸,有黄色沉淀析出,同时有刺激性气体产生。下列说法不正确的是 A.X的简单氢化物的热稳定性比W强 ! B.Y的简单离子与X的具有相同的电子层结 构 C.Y与Z形成化合物的水溶液可使蓝色石蕊 试纸变红 D.Z与X属于同一主族,与Y属于同一周期 13.常温下将NaOH溶液添加到己二酸(H2X)溶 液中,混合溶液的pH与离子浓度变化的关系 如图所示。下列叙述错误的是 A.K SP(H2X)的数量级为10-6 B.曲线N表示pH与 2 (HX) lg (H X) c c 的变化关系
高考化学实验专题选择题训练(答案详解)
高考化学实验专题选择题训练 1.下列有关物质检验的实验操作与现象能得到对应结论的是( ) 操作现象结论 A 向某溶液中滴加稀NaOH溶液,将湿润的红色 石蕊试纸置于试管口 试纸不变蓝原溶液中无NH4+ B 向某无色溶液中滴加氯水和CCl4,振荡、静置下层溶液显紫色原溶液中有I﹣ C 用洁净铂丝蘸取某溶液进行焰色反应火焰呈黄色溶液中有K+ D 将某气体通入品红溶液中品红溶液褪色该气体一定是 SO2 2.将足量的X气体通入Y溶液中,实验结果与预测的现象一致的组合是 X气体Y溶液预测的现象 ①CO2饱和CaCl2溶液白色沉淀析出 ②SO2 Ba(NO3)2溶液白色沉淀析出 ③NH3AgNO3溶液白色沉淀析出 ④NO2Na2S溶液白色沉淀析出 A.只有①②③B.只有①②C.只有②D.②④ 3.水溶液X中只可能溶有Na+、Ca2+、Fe3+、AlO2-、SiO32-、SO32-、CO32-、SO42-中的若干种离子。某同学对该溶液迸行了如下实验: 下列判断正确的是 A.气体甲一定是纯净物B.沉淀甲是硅酸和硅酸钙的混合物C.Na+、AlO2-和SiO32-一定存在于溶液X中D.CO32-和SO42-一定不存在于溶液X中4.下列药品保存方法正确的是 A.短期保存Br2:盛于磨口的细口瓶中,并用水封,瓶盖严密。 B.锂、钠、钾都保存在煤油中,密封。 C.氨水、浓盐酸易挥发必须保存在棕色磨口细口瓶中。D.红磷无需密封保存。 5.下列实验中,所选装置不合理的是 A.分离Na2CO3溶液和CH3COOC2H5,选④B.用CCl4提取碘水中的碘,选③ C.用FeCl2溶液吸收Cl2,选⑤D.粗盐提纯,选①和② 6.下列实验方案能达到实验目的的是
高三化学化学-实验评价选择题专项测试及解析
课后作业---选择题专项微测二 微测5化学实验评价 1.某研究性学习小组讨论甲、乙、丙、丁四种实验装置的有关用法,其中正确的是() A.甲装置:可用来除去CO气体中的CO2气体 B.乙装置:可用来验证NaHCO3和Na2CO3的热稳定性 C.丙装置:可用来实验室制备乙酸乙酯 D.丁装置:可用来比较HCl、H2CO3和H2SiO3的酸性强弱 2.某化学小组同学用如图所示装置模拟工业制取SO3的过程,下列相关说法错误的是() A.装置c后应增加尾气处理装置 B.装置a只有干燥气体的作用 C.实验室制取SO2或O2可使用相同的气体发生装置 D.V2O5是催化剂并且也会参与反应 3.下列实验操作、现象和所得出的结论正确的是() 选项实验操作实验现象实验结论 A将HI溶液加入Fe(NO3)3溶液,充分反应后再加入CCl4混合振荡,静置溶液分层,下层液 体显紫红色 氧化性: Fe3+>I2 B取少量Mg(OH)2悬浊液,向其中滴加适量浓CH3COONH4溶液Mg(OH)2溶解CH3COONH4溶液 呈酸性 C 将浸透石蜡油的石棉放置在硬质试管底 部,加入少量碎瓷片并加强热,将生成 的气体通入酸性高锰酸钾溶液中 酸性高锰酸钾溶液 褪色 石蜡油分解产物中 含有不饱和烃 D将海带剪碎,灼烧成灰,加蒸馏水浸泡,取滤液滴加硫酸溶液,再加入淀粉溶液溶液变蓝 海带中含有丰富的 I2 4.根据下列实验操作与现象得出的结论正确的是() 选项实验操作与现象结论 A向滴有酚酞的碳酸钠溶液中加入少量氯化钡固 体,红色变浅 碳酸钠溶液中存在水解平衡 B向某溶液中逐渐通入CO2气体,先出现白色胶状 沉淀,继续通入CO2气体,白色胶状沉淀不溶解该溶液中一定含有AlO -2 C将润湿的淀粉碘化钾试纸置于集满某气体的集气 瓶口,试纸变蓝 该气体为氯气 D 向10mL0.5mol·L-1的氯化镁溶液中滴加5mL 2.4mol·L-1氢氧化钠溶液,产生白色沉淀,再滴 加氯化铜溶液,沉淀变蓝 K sp[Cu(OH)2]<K sp[Mg(OH)2]
2018年高考化学试卷(全国卷1)
2018年全国统一高考化学试卷(新课标Ⅰ) 一、选择题(共7小题,每小题6分,满分42分) 1.(6分)磷酸亚铁锂(LiFePO4)电池是新能源汽车的动力电池之一,采用湿法冶金工艺回收废旧磷酸亚铁锂电池正极片中的金属,其流程如下: 下列叙述错误的是() A.合理处理废旧电池有利于保护环境和资源再利用 B.从“正极片”中可回收的金属元素有Al、Fe、Li C.“沉淀”反应的金属离子为Fe3+ D.上述流程中可用硫酸钠代替碳酸钠2.(6分)下列说法错误的是() A.蔗糖、果糖和麦芽糖均为双糖 B.酶是一类具有高选择催化性能的蛋白质C.植物油含不饱和脂肪酸酯,能使Br2/CCl4褪色 D.淀粉和纤维素水解的最终产物均为葡萄糖 3.(6分)在生成和纯化乙酸乙酯的实验过程中,下列操作未涉及的是() A.B. C.D. 4.(6分)N A是阿伏加德罗常数的值,下列说法正确的是() A.16.25gFeCl3,水解形成的Fe(OH)3为胶体粒子数为0.1N A B.22.4L(标准状况)氩气含有的质子数为18N A C.92.0g甘油(丙三醇)中含有羟基数为1.0N A D.1.0molCH4与Cl2在光照下生成CH3Cl的分子数为1.0N A 5.(6分)环之间共用一个碳原子的化合物称为螺环化合物,螺(2,2)戊烷()是最单的一种,下列关于该化合物的说法错误的是() A.与环戊烯互为同分异构体 B.二氯化物超过两种 C.所有碳原子均处同一平面 D.生成1molC5H12,至少需要2molH2
6.(6分)主族元素W、X、Y、Z的原子序数依次增加,且均不大于20.W、X、Z最外层电子数之和为10;W与Y同族;W与Z形成的化台物可与浓硫酸反应,其生成物可腐蚀玻璃。下列说法正确的是() A.常温常压下X的单质为气态 B.Z的氢化物为离子化合物 C.Y和Z形成的化合物的水溶液呈碱性 D.W与Y具有相同的最高化合价 7.(6分)最近我国科学家设计了一种CO2+H2S协同转化装置,实现对天然气中CO2和H2S的高效去除。示意图如右所示,其中电极分别为ZnO@石墨烯(石墨烯包裹的ZnO)和石墨烯,石墨烯电极区发生反应为: ①EDTA﹣Fe2+﹣e﹣=EDTA﹣Fe3+ ②2EDTA﹣Fe3++H2S=2H++S+2EDTA﹣Fe2+该装置工作时,下列叙述错误的是() A.阴极的电极反应:CO2+2H++2e﹣═CO+H2O B.协同转化总反应:CO2+H2S═CO+H2O+S C.石墨烯上的电势比ZnO@石墨烯上的低 D.若采用Fe3+/Fe2+取代EDTA﹣Fe3+/EDTA﹣Fe2+,溶液需为酸性 二、解答题(共3小题,满分43分) 8.(14分)醋酸亚铬[(CH3COO)2Cr?2H2O]为砖红色晶体,难溶于冷水,易溶于酸,在气体分析中用作氧气吸收剂。一般制备方法是先在封闭体系中利用金属锌作还原剂,将三价铬还原为二价络;二价铬再与醋酸钠溶液作用即可制得醋酸亚铬。实验装置如图所示。回答下列问题: (1)实验中所用蒸馏水均需经煮沸后迅速冷却,目的是仪器a的名称是。(2)将过量锌粒和氯化铬固体置于c中,加入少量蒸馏水,按图连接好装置。打开K1、K2,关闭K3。 ①c中溶液由绿色逐渐变为亮蓝色,该反应的离子方程式为 ②同时c中有气体产生,该气体的作用是 (3)打开K3,关闭K1和K2.c中亮蓝色溶液流入d,其原因 是;d中析出砖红色沉淀。为使沉淀充分析出并 分离,需采用的操作是、洗涤,干燥。 (4)指出装置d可能存在的缺点
2020年高考化学选择题训练试题(附答案)
(每小题均为1到两个答案) 1.下列过程中不涉及化学变化的是() A. 可用石灰水保存新鲜鸡蛋 B. 在农业生产中常用福尔马林溶液浸种 HNO滴在皮肤 C. 甘油加水可作护肤剂 D. 如不慎将浓3 上,皮肤容易变黄 2.纤维素被称为第七营养素.食物中的纤维素虽然不能为人体提 供能量,但能促进肠道蠕动、吸附排出有害物质.从纤维素的化学成分看,它是一种() A.二糖B.多糖C.氨基酸D.脂肪 3.利用合成气(H2+CO)生产汽油、甲醇和氨等已经实现了工业 化,合成气也可合成醛、酸、酯等多种产物,下列表述正确的是 ①以合成气为原料的反应都是化合反应 ②改变合成气中CO与H2的体积比,可得到不同的产物 ③合成气的转化反应需在适当的温度和压强下通过催化完成 ④从合成气出发生成气态烃或醇类有机物是实现“煤变油”的在效途径 ⑤以合成气为原料的反应产物中不可能有烯烃或水 A.①②④B.②③④C.②④⑤D.③④⑤4.磷酸的结构式如右图所示,三分子磷酸可脱去两分子水生成三 聚磷酸(H5P3O10)。含磷洗衣粉中含有三聚磷酸,则该钠盐的
化学式及1mol此钠盐中P=O键的物质的量分别是 A.Na5P3O10 1mol B.Na3H2P3O102mol C.Na5P3O10 3mol D.Na2H3P3O10 4mol 5.下列说法正确的是 A.硫酸、纯碱、醋酸钠和生石灰分别属于酸、碱、盐和氧化物 B.蔗糖、硫酸钡和水分别属于非电解质、强电解质和弱电解质 C.活性炭、SO2和HClO都具有漂白作用,且漂白的化学原理相同 D.硫酸厂厂址的选择应靠近原料产地 6.下列热化学方程式书写正确的是 A.2SO2 + O2 ==== 2SO3△H=-196.6 kJ/mol B.H2(g)+O2(g)=== H2O (g) △H=-241.8 kJ C.2H2(g)+O2(g) === 2H2O(l) △H=-571.6 kJ/mol D.C(s) + O2(g) === CO2(g) △H= + 393.5 kJ/mol 7.已知土壤胶粒带负荷,在土壤里施用含氮量相等的下列肥料,肥 效较差的是 A.(NH4)2SO4 B.NH4HCO3 C.NH4NO3 D.NH4Cl 8.下列实验操作中错误的是 A 分液时,分液漏斗下层液体从下口放出,上层液体从上层倒出
至高考化学化学与生活选择题汇编
专题一化学与STSE历年高考真题集锦1.[2012·海南]化学与环境密切相关,下列有关说法正确的是() A.CO 2 属于大气污染物 B.酸雨是PH小于7的雨水 C.CO 2、NO 2 或SO 2 都会导致酸雨的形成D.大气中CO 2 含量的增加会导致温室效应加剧 2.[2012·江苏]化学在资源利用、环境保护等与社会可持续发展密切相关的领域发挥着积极的作用。下列做法与社会可持续发展理念相违背的是() A.改进汽车尾气净化技术,减少大气污染物的排放 B.开发利用可再生能源,减少化石燃料的使用 C.研发可降解高分子材料,减少“白色污染” D.过度开发矿物资源,促进地方经济发展 3.[2012·浙江]下列说法正确的是() A.油脂、淀粉、蔗糖和葡萄糖在一定条件都能发生水解反应 B.蛋白质是结构复杂的高分子化合物,分子中都含有C、H、O、N四种元素 C.棉、麻、羊毛及合成纤维完全燃烧都只生成CO 2和H 2 O D.根据分散质粒子的直径大小,分散系可分为溶液、浊液和胶体,浊液的分散质粒子大小介于溶液与胶体之间 4.[2012·广东]化学与生活息息相关,下列说法不正确的是() A 用食醋可除去热水壶内壁的水垢 B 淀粉、油脂和蛋白质都是高分子化合物 C 自行车钢架生锈主要是电化学腐蚀所致 D 新型复合材料使用手机,电脑等电子产品更轻巧,使用和新潮 5.[2012·四川]下列关于“化学与健康”的说法不正确的是() A.服用铬含量超标的药用胶囊会对人对健康造成危害 B.食用一定量的油脂能促进人体对某些维生素的吸收 C.“血液透析”利用了胶体的性质 D.光化学烟雾不会引起呼吸道疾病 6.[2012·天津]根据下列物质的化学性质,判断其应用错误 ..的是()A.酒精能使蛋白质变性,可用于杀菌消毒 B.CaO能与SO 2 反应,可作工业废气的脱硫剂 C.明矾水解时产生具有吸附性的胶体粒子,可作漂白剂 D.镧镍合金能大量吸收H 2 形成金属氢化物,可作储氢材料 7. [2012·北京]下列用品的有效成分及用途对应错误的是()
高考全国卷1化学试题附答案
2016年全国统一考试(新课标I 卷) 一、选择题: 7. 化学与生活密切相关。下列有关说法错误的是( ) A. 用灼烧的方法可以区分蚕丝和人造纤维 B. 食用油反复加热会产生稠环芳烃等有害物质 C. 加热能杀死流感病毒是因为蛋白质受热变性 D. 医用消毒酒精中乙醇的浓度为95% 8. 设A N 为阿伏加德罗常数值。下列有关叙述正确的是( ) A. 14g 乙烯和丙烯混合气体中的氢原子数为A 2N B. 1mol 2N 与4mol 2H 反应生成的3NH 分子数为A 2N C. 1mol Fe 溶于过量硝酸,电子转移数为A 2N D. 标准状况下,2.24L 4CCl 含有的共价键数为A 0.4N 9. 下列关于有机化合物的说法正确的是( ) A. 2-甲基丁烷也称为异丁烷 B. 由乙烯生成乙醇属于加成反应 C. 49C H Cl 有3种同分异构体 D. 油脂和蛋白质都属于高分子化合物 10. 下列实验操作能达到实验目的的是( ) A. 用长颈漏斗分离出乙酸与乙醇反应的产物 B. 用向上排空气法收集铜粉与稀硝酸反应产生的NO C. 配制氯化铁溶液时,将氯化铁溶解在较浓的盐酸中再加水稀释 D. 将2Cl 与HCl 混合气体通过饱和食盐水可得到纯净的2Cl 11. 三室式电渗析法处理含24Na SO 废水的原理如图所示,采用惰性电极,ab 、cd 均为离子 交换膜,在直流电场的作用下,两膜中间的+Na 和24SO - 可通过离子交换膜,而两端隔室中 离子被阻挡不能进入中间隔室。 下列叙述正确的是( ) A. 通电后中间隔室的24SO - 离子向正极迁移,正极区溶液pH 增大
2019届高三化学选择题专题—有机选择专题练习(最新整理)
有机化学基础(选择题)专题 1.下列关于有机物的叙述不正确的是 A.乙酸的分子模型可表示为 B.糖类、油脂、蛋白质都是高分子化合物 C.新制的氢氧化铜可以鉴别乙酸、葡萄糖和乙醇 D.丁酸和乙酸乙酯互为同分异构体 2.指甲花中存在的β-紫罗蓝酮属于一种萜类化合物,可作为合成维生素A 的原料。下列有关β-紫罗蓝 酮的说法正确的是 A.β-紫罗蓝酮的分子式为C10H14O B.分子中所有碳原子可能处于同一平面 C.与足量的H2反应后,分子中官能团的种类减少一种 D.和酸性KMnO4溶液、溴的四氯化碳溶液发生的反应类型相同 3.某有机物的结构简式见图,下列说法正确的是 A.不能发生消去反应 B.分子式为C14H15O6NBr C.不能使酸性高锰酸钾溶液褪色 D.在一定条件下与氢氧化钠溶液反应,1mol 该有机物最多消耗4 mol NaOH 4.某抗肿瘤药物中间体的合成路线如下。下列说法正确的是( ) A.吲哚的分子式为C8H6N B.苯甲醛中所有原子不可能全部共平面 C.可用新制氢氧化铜悬浊液区分苯甲醛和中间体 D.1mol 该中间体,最多可以与9mol 氢气发生加成反应 5.下列关于有机化合物的说法正确的是 A.分子式为C3H6Cl2的有机物有4 种同分异构体(不考虑立体异构) B.和互为同系物 C.乙炔和溴的四氯化碳溶液反应生成1,2-二溴乙烷 D.甲苯分子中所有原子都在同一平面上
6. 下列关于有机化合物的说法正确的是 A .丙烷的二氯取代物有 3 种 B . 和苯乙烯互为同系物 C .饱和(NH 4)2SO 4 溶液和福尔马林均可使蛋白质溶液产生沉淀,其原理相同 D .聚合物(—[ C H 2—CH 2—CH —CH 2—]n )可由单体 CH 3CH =CH 2 和 CH 2=CH 2 加聚制得 C |H 3 7. 已知互为同分异构体,下列说法不正确的是 A .盆烯可与酸性高锰酸钾溶液反应 B .苯与棱晶烷的一氯代物均只有一种 C .上述三种物质中,与甲苯互为同系物的只有苯 D .上述三种物质中,只有棱晶烷的所有原子不处于同一平面内 8. 增塑剂 DCHP 可由环己醇制得。环已醇和 DCHP 的结构简式如图所示,下列说法正确的是 A.DCHP 的分子式为 C 20H 14O 4 B 环已醇和 DCHP 的二氯代物均有 4 种 C.1molDCHP 水解时消耗 2mol NaOH D.环已醇分子中的所有碳原子可能共平面 9、某抗癌药物的结构简式如图所示,下列有关说祛正确的是 A.能发生取代、氧化、加聚反应 B.分子中所有原子可能共平面 C.与苯甲酸苯甲酯属同系物 D.水解生成酸的同分异构体中含有苯环且能发生银镜反应的有 3 种 10. 化合物 X 是一种药物合成的中间体,其结构简式如图所示。下列有关化合物 X 的说法正确的是 ( ) A. 化合物 X 的分子式为 C 16H 16O 6 HO HO B. 能发生加成反应、取代反应、消去反应 O C. 1mol 化合物 X 最多可与 5molNaOH 、7mol H 2、4molBr 2 发生反应 D. 可与 FeCl 3 溶液发生显色反应,但不能发生氧化反应 H 3C O O OH CH 3
2020年全国卷Ⅲ理综化学高考试题(含答案)
高考真题绝密★启用前 2020年普通高等学校招生全国统一考试 理科综合能力测试化学 注意事项: 1.答卷前,考生务必将自己的姓名、准考证号填写在答题卡上。 2.回答选择题时,选出每小题答案后,用铅笔把答题卡上对应题目的答案标号涂黑,如需改动,用橡皮擦干净后,再选涂其它答案标号。回答非选择题时,将答案写在答题卡上,写在本试卷上无效。 3.考试结束后,将本试卷和答题卡一并交回。 可能用到的相对原子质量:H 1 C 12 N 14 O 16 Mg 24 S 32 Fe 56 Cu 64 一、选择题:本题共13个小题,每小题6分。共78分,在每小题给出的四个选项中,只有一项是符合题 目要求的。 7.宋代《千里江山图》描绘了山清水秀的美丽景色,历经千年色彩依然,其中绿色来自孔雀石颜料(主要成分为Cu(OH)2·CuCO3),青色来自蓝铜矿颜料(主要成分为Cu(OH)2·2CuCO3)。下列说法错误的是A.保存《千里江山图》需控制温度和湿度 B.孔雀石、蓝铜矿颜料不易被空气氧化 C.孔雀石、蓝铜矿颜料耐酸耐碱 D.Cu(OH)2·CuCO3中铜的质量分数高于Cu(OH)2·2CuCO3 8.金丝桃苷是从中药材中提取的一种具有抗病毒作用的黄酮类化合物,结构式如下: 下列关于金丝桃苷的叙述,错误的是 A.可与氢气发生加成反应B.分子含21个碳原子 C.能与乙酸发生酯化反应D.不能与金属钠反应 9.N A是阿伏加德罗常数的值。下列说法正确的是 A.22.4 L(标准状况)氮气中含有7N A个中子
高考真题 B .1 mol 重水比1 mol 水多N A 个质子 C .12 g 石墨烯和12 g 金刚石均含有N A 个碳原子 D .1 L 1 mol·L ?1 NaCl 溶液含有28N A 个电子 10.喷泉实验装置如图所示。应用下列各组气体—溶液,能出现喷泉现象的是 气体 溶液 A . H 2S 稀盐酸 B . HCl 稀氨水 C . NO 稀H 2SO 4 D . CO 2 饱和NaHCO 3溶液 11.对于下列实验,能正确描述其反应的离子方程式是 A .用Na 2SO 3溶液吸收少量Cl 2:323SO -+Cl 2+H 2O = 23HSO -+2Cl -+24SO - B .向CaCl 2溶液中通入CO 2:Ca 2++H 2O+CO 2=CaCO 3↓+2H + C .向H 2O 2溶液中滴加少量FeCl 3:2Fe 3+ +H 2O 2=O 2↑+2H ++2Fe 2+ D .同浓度同体积NH 4HSO 4溶液与NaOH 溶液混合:4NH ++OH - =NH 3·H 2O 12.一种高性能的碱性硼化钒(VB 2)—空气电池如下图所示,其中在VB 2电极发生反应: 32442VB 16OH 11e VO 2B(OH)4H O ----+-=++该电池工作时,下列说法错误的是
2020年全国高考化学选择题专项攻关选择题专练(四)(解析版)
选择题专练(四) 7、化学与生产、生活密切相关。下列事实的解释正确的是 【答案】D 【解析】A中:Si是亲氧元素,在在自然界中不能稳定存在,A错。B中:在发动机内,高温下空气中的N2与O2发生反应生成氮氧化合物,不是汽油中含有氮元素,B错。C中:明矾不能杀菌消毒,C错。D:用惰性电极作辅助阳极,铁闸接外加电源的负极,作阴极,被保护,成为外加电流阴极保护法,D正确。选D。 8、N A表示阿伏加德罗常数的值。室温下,下列关于浓度均为0.1 mol/LNH4Cl、NH4Fe(SO4)2的两溶液的说法中正确的是 A.等体积的两溶液中含有的NH4+离子数目均小于0.1N A,且n(NH4+):NH4Fe(SO4)2>NH4Cl B.向1L 0.1 mol/L NH4Fe(SO4)2的加入足量Cu粉,转移电子数目0.2N A C.0.1 mol/L NH4Cl溶液中一定存在如下关系:c(NH4+)+c(NH3·H2O)=0.1mol/L D.加水稀释后,两溶液中c(OH-)均减小 【答案】C 【解析】等体积并不一定是指1L,,所以不能说NH4+的数目小于0.1N A,A错。B中的离子方程式为:Cu+2Fe3+=Cu2++2Fe2+,由此可知:0.1molFe3+参与反应转移电子0.1mol,B正确。C:.0.1 mol/L NH4Cl溶液的物料守恒为c(NH4+)+c(NH3·H2O)=0.1mol/L,C正确。NH4Cl、NH4Fe(SO4)2溶液呈酸性,加水稀释,c(H+)减小,故c(OH-)增大,D错。选C。 9、下列关于常见有机物的说法中,不正确的是 A.异戊烷的二氯代物的同分异构体有9种 B.油脂属于酯类,有可能使酸性高锰酸钾溶液褪色 C.乙醇能使酸性重铬酸钾溶液变色,被氧化生成CH3COOH D.苯和液溴的混合物中加入适量铁粉,振荡,导出的气体通入AgNO3溶液中,出现浅黄色沉淀, 【答案】A
高考化学易错易漏选择题专题训练
08高考化学易错易漏选择题专题训练(一) 总分共64分测试时间30分钟 一、选择题(本题包括8小题,每小题4分,共32分。每小题只有一个选项符合题意。) 1、对pH=3的醋酸溶液和pH=3的HCl溶液等体积混和后,溶液的PH值 A、PH<3 B、PH>3 C、PH=3 D、无法确定 2、常温下对pH=10的NaOH溶液和pH=4的HCl溶液中水的电离程度比较,下列叙述正确的是A、前者大B、后者大C、两者相等D、无法确定 3、将3.9g镁铝合金,投入到500mL2mol/L的盐酸中,金属完全溶解,再加入4mol/L的NaOH 溶液,若要生成的沉淀最多,加入的这种NaOH溶液的体积是 A、125mL B、200mL C、250mL D、560mL 4、将6.6g可能混有下列物质的(NH4)2SO4样品,在加热的条件下,与过量的NaOH反应, 可收集到2.15升NH3(密度为17克/22.4升),则样品中不可能含有的物质是 A.NH4HCO3,NH4NO3B.(NH4)2CO3,NH4NO3 C.NH4HCO3,NH4Cl D.NH4Cl,(NH4)2CO3 5、已知蓄电池在放电时起原电池的作用,充电时起电解池的作用。铅蓄电池在放电和充电 时发生的化学反应可用下式表示:Pb+PbO2+2H2SO42PbSO4+2H2O据此判断下列叙述正确的是 A.放电时负极电极反应式为:PbO2+4H+ + SO42-+2e-PbSO4+2H2O B.充电时阴极电极反应式为:PbSO4+2e-Pb+SO42- C.充电时,若要使1molPbSO4转变为Pb和PbO2,则需要通过2mol电子 D.放电时,H+向负极移动 6、某气体能使石蕊试液变红,能使酸性高锰酸钾溶液褪色,若通入溴水,可使溶液变浑浊。该气体是 A.CO2B.Cl2C.H2S D.SO2 7、FeSO4和Fe2(SO4)3的混合物中含硫的质量分数为a%,则含铁的质量分数为 A.2a% B.3a% C.1-2a% D.1-3a% 8、N A表示阿伏加德罗常数,下列叙述正确的是 A、1mol过氧化氢分子中共用电子对数为3N A B、常温常压下,22.4L的D2、H2组成的气体分子数为N A C、标准状况下,22.4LSO3中含有的氧原子数为3N A D、1molNa2O2与CO2充分反应转移的电子数为2N A 二、选择题(本题包括8小题,每小题4分,共32分。每小题只有一个或两个选项符合题 意。若正确答案包括一个选项,多选时,该题为0分;若正确答案包括两个选项,只选一个且正确的给2分,选两个且都正确的给4分,但只要选错一个,该小题就0分。)9、常温下,pH=9的CH3COONa 溶液由水电离出来的C(H+)为a,pH=9的NH3·H2O 溶液由水电离出来的C(H+)为b,下列a和b的关系正确的是 A.a=b B.a=104b C.b=10-4a D.a=10-4b 10、设N A代表阿伏加德罗常数,下列说法不正确的是 A、0.012kg13C中碳原子数为N A B、与S反应时,0.1molCu失去电子数为 0.1N A C、常温常压下,0.5摩尔CO2分子质量为22g D、7.8gNa2O2与足量CO2充分反应,转 移电子为0.1N A 11、下列说法正确的是 A、摩尔是物质的质量单位 B、氢气的摩尔质量是2g C、1molOH—的质量是17g D、气体摩尔体积就是1mol气体所占的体积 12、体积为1L的干燥容器内充入HCl气体后,测得容器中气体对氧气的相对密度为1.082, 用此气体进行喷泉实验,当喷泉停止后,进入容器中水的体积是: A、0.25L B.0.50L C.0.75L D.1.0L
高考全国卷1化学试题附答案-全国卷1
2016年全国统一考试(新课标I 卷) 一、选择题: 7. 化学与生活密切相关。下列有关说法错误的是( ) ?A.?用灼烧的方法可以区分蚕丝和人造纤维 B.?食用油反复加热会产生稠环芳烃等有害物质 ? C. 加热能杀死流感病毒是因为蛋白质受热变性 ? D.?医用消毒酒精中乙醇的浓度为95% 8. 设A N 为阿伏加德罗常数值。下列有关叙述正确的是( ) A.?14g 乙烯和丙烯混合气体中的氢原子数为A 2N B.?1mol 2N 与4mol 2H 反应生成的3NH 分子数为A 2N C. 1mol Fe 溶于过量硝酸,电子转移数为A 2N ?D. 标准状况下,2.24L 4CCl 含有的共价键数为A 0.4N 9. 下列关于有机化合物的说法正确的是( ) ?A. 2-甲基丁烷也称为异丁烷?B. 由乙烯生成乙醇属于加成反应 C.?49C H Cl 有3种同分异构体 D. 油脂和蛋白质都属于高分子化合物 10. 下列实验操作能达到实验目的的是( ) ?A. 用长颈漏斗分离出乙酸与乙醇反应的产物 B. 用向上排空气法收集铜粉与稀硝酸反应产生的NO C .?配制氯化铁溶液时,将氯化铁溶解在较浓的盐酸中再加水稀释 D. 将2Cl 与HCl 混合气体通过饱和食盐水可得到纯净的2Cl 11. 三室式电渗析法处理含24Na SO 废水的原理如图所示,采用惰性电极,a b、cd 均为离子交 换膜,在直流电场的作用下,两膜中间的+Na 和24SO - 可通过离子交换膜,而两端隔室中离子 被阻挡不能进入中间隔室。 下列叙述正确的是( ) ?A.?通电后中间隔室的24SO - 离子向正极迁移,正极区溶液pH 增大 ?B.?该法在处理含24Na SO 废水时可以得到NaOH 和24H SO 产品 ?C. 负极反应为+222H O 4O +4H e ===--,负极区溶液pH 降低 ?D.?当电路中通过1mol 电子的电量时,会有0.5mol 的2O 生成 12. 298K 时,在20.0mL 10.10mol L -?氨水中滴入10.10mol L -?的盐酸。溶液的pH 与所加盐酸 的体积关系如图所示。已知10.10mol L -?氨水的电离度为1.32%,下列有关叙述正确的是 ?A. 该滴定过程应该选择酚酞作为指示剂 ?B.?M 点对应的盐酸体积为20.0mL
2020年高考化学选择题专项训练题(含答案)
2020年高考化学选择题专项训练题 1.中国人民在悠久的历史中创造了绚丽多彩的中华文化,下列说法错误的是( ) A .“木活字”是由元代王祯创制的用于印刷的活字,“木活字”的主要成分是纤维素 B .“指南针”是我国古代四大发明之一,是由天然磁石制成,磁石的主要成分是Fe 2O 3 C .“苏绣”是用蚕丝线在丝绸或其他织物上绣出图案的工艺,蚕丝的主要成分是蛋白质 D .“黑陶”是一种传统工艺品,是用陶土烧制而成,其主要成分为硅酸盐 2.工业制备硝酸的反应之一为:3NO 2+H 2O=2HNO 3+NO 。用N A 表示阿伏加德罗常数,下列说法正确的是( ) A .室温下,22.4L NO 2中所含原子总数为3N A B .36g H 2O 中含有共价键的总数为2N A C .上述反应,生成1mol HNO 3转移电子的数目为N A D .标准状况下,11.2L NO 中所含电子总数为5N A 3.M 、N 两种化合物在医药方面有重要的作用,下列说法错误的是( ) A .N 的化学式为C 15H 20O 5 B .M 分子间能形成氢键,N 分子间不能形成氢键 C .M 中含有四种含氧官能团 D .1mol M 与溴水反应,最多消耗3mol Br 2 4.无水FeCl 2是常用还原剂,实验室中可以利用反应2FeCl 3+C 6H 5Cl 129C~135C ?? ?????→2FeCl 2+ C 6H 4Cl 2+HCl↑制取,已知:C 6H 5Cl 熔点-45℃,沸点132℃;C 6H 4Cl 2熔点53℃,沸点173℃。下列说法不正确的是( ) A .仪器a 的作用是冷凝、回流、导气
最新高考化学选择题专项训练(历年高考化学选择题分类汇编-共15个专题)
2016届高三选择题专项突破 第1集化学与生产、生活、科学、环境 1—1、下面有关发泡塑料饭盒的叙述,不正确的是 A.主要材质是高分子材料 B.价廉、质轻、保温性能好 C.适用于微波炉加热食品 D.不适于盛放含油较多的食品 2—1. 化学与社会、生产、生活紧密相关。下列说法正确的是 A.石英只能用于生产光导纤维B.从海水提取物质都必须通过化学反应才能实现C.为了增加食物的营养成分,可以大量使用食品添加剂D.“地沟油”禁止食用,但可以用来制肥皂 3—1. 化学与生活密切相关,下列说法不正确 ...的是() A.二氧化硫可广泛用于食品的增白B.葡萄糖可用于补钙药物的合成 C.聚乙烯塑料制品可用于食品的包装D.次氯酸钠溶液可用于环境的消毒杀菌 4—1.化学与生活密切相关,下列说法正确的是 A.聚乙烯塑料的老化是由于发生了加成反应 B.煤经过气化和液化等物理变化可以转化为清洁燃料 C.合成纤维、人造纤维及碳纤维都属于有机高分子材料 D.利用粮食酿酒经过了淀粉→葡萄糖→乙醇的化学变化过程 5—1、化学无处不在,下列与化学有关的说法,不正确的是() A、侯氏制碱法的工艺过程中应用了物质溶解度的差异 B、可用蘸浓盐酸的棉棒检验输送氨气的管道是否漏气 C、碘是人体必须微量元素,所以要多吃富含高碘酸的食物 D、黑火药由硫磺、硝石、木炭三种物质按一定比例混合制成 6—1、以下食品化学知识的叙述不正确的是 A、食盐可作调味剂,也可作食品防腐剂 B、新鲜蔬菜做熟后,所含维生素C会有损失 C、纤维素在人体内可水解为葡萄糖,故可做人类的营养物质 D、葡萄糖中的花青素在碱性环境下显蓝色,故可用苏打粉检验假红酒。 7—1.下列关于“化学与健康”的说法不正确的是 A、服用铬含量超标的药用胶囊会对人对健康造成危害 B、食用一定量的油脂能促进人体对某些维生素的吸收 C、“血液透析”利用了胶体的性质 D、光化学烟雾不会引起呼吸道疾病 8—1下列说法中正确的是 A.医用酒精的浓度通常为95% B.单质硅是将太阳能转化为电能的常用材料 C.淀粉、纤维素和油脂都属于天然高分子化合物 D.合成纤维和光导纤维都是新型无机非金属材料
