实验13 环己烯的制备
实验十三环己烯的制备
一、实验目的
1、熟悉环己醇在酸催化下的反应机理,掌握环己烯的制备方法;2、巩固分液漏斗的使用,复习分馏操作。
二、实验原理
OH
24
+H2O
三、试剂
环己醇,浓硫酸,食盐,无水氯化钙,5%碳酸钠溶液
四、实验步骤
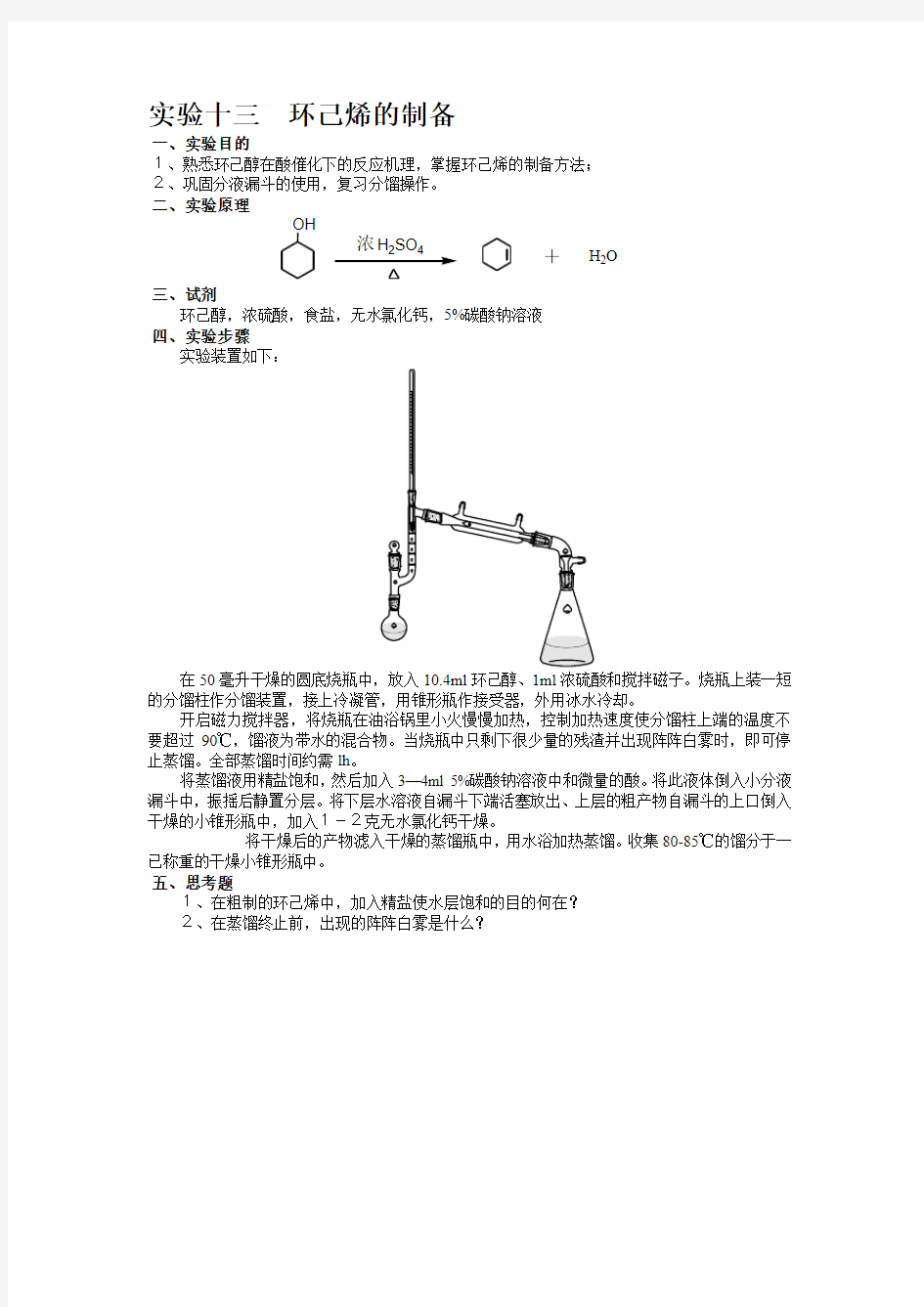
实验装置如下:
在50毫升干燥的圆底烧瓶中,放入10.4ml环己醇、1ml浓硫酸和搅拌磁子。烧瓶上装一短的分馏柱作分馏装置,接上冷凝管,用锥形瓶作接受器,外用冰水冷却。
开启磁力搅拌器,将烧瓶在油浴锅里小火慢慢加热,控制加热速度使分馏柱上端的温度不要超过90℃,馏液为带水的混合物。当烧瓶中只剩下很少量的残渣并出现阵阵白雾时,即可停止蒸馏。全部蒸馏时间约需lh。
将蒸馏液用精盐饱和,然后加入3—4ml 5%碳酸钠溶液中和微量的酸。将此液体倒入小分液漏斗中,振摇后静置分层。将下层水溶液自漏斗下端活塞放出、上层的粗产物自漏斗的上口倒入干燥的小锥形瓶中,加入1-2克无水氯化钙干燥。
将干燥后的产物滤入干燥的蒸馏瓶中,用水浴加热蒸馏。收集80-85℃的馏分于一已称重的干燥小锥形瓶中。
五、思考题
1、在粗制的环己烯中,加入精盐使水层饱和的目的何在?
2、在蒸馏终止前,出现的阵阵白雾是什么?
实验10环己酮的制备
酒泉职业技术学院《工科化学实验技术》学习领域教案NO:
课后分析及小结累计课时教研室主任签名 环己酮的制备一、教学要求:学习铬酸氧化法制环己酮的原理和方法。进一步了 解醇和酮之间的联系和区别。 二、预习内容:盐析实验原理抽虑操作2.3.1. 三、实验原理:铬酸是重要的铬酸最常用的方法是将伯醇和仲醇用铬酸氧化。实验室制备脂肪或脂环醛酮,%硫酸的混合物。仲醇用铬酸氧化是制备酮的最常用的方法。酮对氧化剂比较5040盐和-以免反应不易进一步氧化。稳定,铬酸氧化醇是一个放热反应,必须严格控制反应的温度, 2 过于激烈。环己酮主要用于合成尼龙-6或尼龙-66,还广泛用作溶剂,它尤其因对许多高聚物(如树脂、橡胶、涂料)的溶解性能优异而得到广泛的应用。在皮革工业中还用作脱脂剂和洗涤剂。 四、仪器与药品 仪器: 250ml圆底烧瓶、温度计、蒸馏装置、分液漏斗。 药品:浓硫酸、环己醇、重铬酸钠、草酸、食盐、无水碳酸钠。 四、实验步骤: 1.铬酸溶液的配制 在250mL烧杯中加入30mL水和5.5g重铬酸钠,搅拌使之全部溶解。然后在搅拌下慢慢加入4.5mL浓硫酸,将所得橙红色溶液冷却至30℃以下备用。
2. 氧化反应在250mL圆底烧瓶中加入5.5mL环己醇,然后取此铬酸溶液lml 加入圆底烧瓶中,充分振摇,这时可观察到反应温度上升和反应液由橙红色变为 继续向圆底墨绿色,表明氧化反应已经发生。溶(或重铬酸钾)烧瓶中滴加剩余的重铬酸钠保持控制滴加速度,液,同时不断振摇烧瓶,若超过此℃之间。烧瓶内反应液温度在60~65在圆底挠瓶中插温度时立即在冰水浴中冷却。这时温度并继续振摇反应瓶。入一支温度计,℃时,用水浴冷55徐徐上升,当温度上升到0.5h℃。大约却,并维持反应温度在60~65室温下当温度开始下降时移去冷水浴,左右,图1 普通蒸馏装置分钟左右,其间仍要间歇振摇反应瓶20放置则应加入少量草最后反应液呈墨绿色。如果反应液不能完全变成墨绿色,几次, 1mL)以还原过量的氧化剂。酸(0.5~1.0g或甲醇 进行蒸馏,)装置仪器(改用锥形瓶作接受器30mL3.在反应瓶中加入水,如图1环已这一步蒸馏操作实际上是一种简化了的水蒸气蒸馏。50mL馏出液。收集约。应注意馏出液的量不%)(95℃的恒沸混合物含环已酮38.4酮与水形成沸点为℃时为(31能太多,因为馏出液中含水较多,而环已酮在水中的溶解度较大也有少量环已酮溶于水而损失掉。,即使利用盐析效应,否则2.4g); 把馏出液用食盐水饱和,并将馏出液移至分液漏斗中,静止,分出有机相。4. 乙醚提取一次,将乙醚提取液与有机相合并,用无水硫酸镁干燥。15mL水相用在接液管的尾部接一通住水槽或室(15. 按图装置仪器,在水浴上蒸出乙醚 3 外的橡皮管,以便把易挥发、易燃的乙醚蒸气通入水槽的下水管内或引出室外),然后改用空气冷接管和接受器(如图2装置)继续蒸馏,收集150~155℃的馏分,产量3~4g。(产率66-72%)。 纯粹环己酮为无色透明液体,沸点155.7℃,相对密度d=0.9478,折光率1.4507。乙醚的凝固点-116.2℃,沸点34.5℃,相对密度0.7138(20/4℃)。
环己烯的制备__实验报告
主反应式: 可能的副反应:(难) 0H H + A 共沸点 64.9o C 、J 30.5% 69.5% 实验八 环己烯的制备 、实验目的: 1、 学习以浓磷酸催化环己醇脱水制备环己烯的原理和方法; 2、 初步掌握分馏、水浴蒸馏和液体干燥的基本操作技能 、实验原理:书 P158 烯烃是重要的有机化工原料。工业上主要通过石油裂解的方法制备烯烃,有时也利用醇在氧化铝等催 化剂存在下,进行高温催化脱水来制取,实验室里则主要用浓硫酸,浓磷酸做催化剂使醇脱水或卤代烃在 醇钠作用下脱卤化氢来制备烯烃。 本实验采用浓磷酸做催化剂使环已醇脱水制备环已烯。 三、主要试剂、产物的物理和化学性质 化学物质 相对分子质里 相对密度/d 420 沸点/ c 溶解度/g (100g 水)-1 环己醇 100 0.96 161.1 3.6 20c 磷酸 98 1.83 -1/2出0(213 C ) 2340 环己烯 82.14 0.89 83.3 微溶于水 环己醚 182.3 0.92 243 微溶于水 四、实 验装置 一般认为,该反应历程为 E i 历程,整个反应是可逆的:酸使醇羟基质子化,使其易于离去而生成正碳 离子,后者失去一个质子,就生成烯烃。 共沸点97施; 共彿点.西.纨“
仪器:50mL圆底烧瓶、分馏柱、直型冷凝管,100mL 分液漏斗、100mL锥形瓶、蒸馏头,接液管。 试剂:10.0g (10.4mL, O.lmol )环已醇,4mL浓磷酸, 氯化钠、 无水氯化钙、5%碳酸钠水溶液。 其它:沸石 1、投料 六、预习实验步骤、现场记录及实验现象解释 在50ml干燥的圆底烧瓶中加入10g环己醇、4ml浓磷酸和几粒沸石,充分摇振使之混合均匀,安装反应装置。 2、加热回流、蒸出粗产物产物 将烧瓶在石棉网上小火空气浴缓缓加热至沸,控制分馏柱顶部的溜出温度不超过90C,馏出液为带 水的混浊液。至无液体蒸出时,可升高加热温度(缩小石棉网与烧瓶底间距离),当烧瓶中只剩下很少残 液并出现阵阵白雾时,即可停止蒸馏。 3、分离并干燥粗产物 将馏出液用氯化钠饱和,然后加入3—4ml 5%的碳酸钠溶液中和微量的酸。将液体转入分液漏斗中, 振摇(注意放气操作)后静置分层,打开上口玻塞,再将活塞缓缓旋开,下层液体从分液漏斗的活塞放出,产物从分液漏斗上口倒入一干燥的小锥形瓶中,用 1 —2g无水氯化钙干燥。 4、蒸出产品 待溶液清亮透明后,小心滤入干燥的小烧瓶中,投入几粒沸石后用水浴蒸馏,收集80—85 C的馏分于 一已称量的小锥形瓶中。 六、产品产率的计算注意事项: 1、投料时应先投环己醇,再投浓磷酸;投料后,一定要混合均匀。 2、反应时,控制温度不要超过90Co 3、干燥剂用量合理。 4、反应、干燥、蒸馏所涉及器皿都应干燥。 5、磷酸有一定的氧化性,加完磷酸要摇匀后再加热,否则反应物会 被氧化。 6、环己醇的粘度较大,尤其室温低时,量筒内的环己醇若倒不干净,会影响 产率。 7、用无水氯化钙干燥时氯化钙用量不能太多,必须使用粒状无水氯化钙。粗产物干燥好后再蒸馏,蒸馏装置要预先干燥,否则前馏分多(环己 供参考
环己烯的制备实验报告
环己烯的制备实验报告 一、实验目的:利用环己醇以及其他相关的化学试剂来进行化学反应制备环己烯。 二、实验原理:化学反应式: 反应历程: 可能的副反应: 主要反应物,以及产物:环己醇(15g,也即是15.6ml)、1ml浓硫酸试剂、产物为、副产物为水,环己醚,以及环己醇、食盐Nacl、无水氯化钙、5%的碳酸钠水溶液。 其中环己醇的沸点为:163℃,纯粹环己烯的沸点为82.9℃。 三、实验仪器以及操作图: 实验仪器有:圆底烧瓶、铁架台,直型冷凝管、接受瓶、分液漏斗、温度计、橡胶塞、电炉、导管、接液管、水浴锅、锥形瓶、漏斗、烧杯、短的分馏柱、蒸馏头,电子天平。 四、实验步骤: 1、按照实验装置示意图从上到下、从左到右的顺序安装蒸馏装置,检查装置的气密性。 2、在50ml的圆底烧瓶里面加入15.6ml的环己醇,并加入1ml的浓硫酸,滴加时注意,防止浓硫酸烧伤手臂。并加入几粒沸石,充分摇匀后使之均匀混合。在烧瓶上装一短的分馏柱,接上冷凝管,把接受瓶浸在冷水中冷却。 3、将烧瓶在电炉上面用空气浴的方法加热,控制温度不超过90℃,分馏出的液体为带水的混浊液,到无液体蒸出而且在圆底烧瓶内有白雾出现的时候,停止蒸馏,此时记下蒸馏出产物的那段温度为85℃至90℃。 4、将蒸出的液体先加入食盐饱和,然后加入3——4ml5%的碳酸钠溶液进行中和微量的酸。将液体转入分液漏斗中,摇振后静置,直至有机相分离出来,然后用分液漏斗分理处需要的上层有机相,即为环己烯的粗产物。此时用1——2g无水氯化钙进行干燥,待溶液清亮透明后滤入重新洗净干燥后的烧瓶中,此时把锥形瓶洗干净并烘干称量干重。
5、将分离干燥后的滤液重新加入圆底烧瓶后,加入几粒沸石进行水浴加热,收集温度在80——85℃之间的馏分于已经称量干重的锥形瓶内,此时锥形瓶干重为51.6g。待蒸馏出只剩下很少部分液体时,且温度变化范围突然下降时,停止蒸馏,此时称量锥形瓶连同液体的质量,的数据为55.8g。 五、实验数据计算: 产物环己烯的质量=55.8g—51.6g=4.2g 生产出的环己烯的质量为4.2g。产率为4.2g/15g=28% 六、误差分析:产物过低的原因主要有: a.气密性不够,导致生成的环己烯有泄漏。 b.在转移液体以及过滤的时候液体有沾到器壁上,导致有损失。C.火力的大小有问题,导致加热不够稳定,火力过大时,导致生成环己烯的速率过快,从而来不及液化就散到容器外部。 七、思考题: 1、答案:加入食盐的目的就是为了降低环己烯的溶解度。 2、答案:由于反应进入末期时,绝大部分的环己醇已被反应生成环己烯,此时容器内生成剩余的环己烯很少,造成容器内蒸汽含量降低,蒸汽压不稳定,从而生成阵阵白雾。 3、答案:Cacl2+5H2O==Cacl2`5H2O 过滤的原因是因为五水氯化钙里面含有水,若不过滤则在第二次蒸馏时有水,是环己烯和水生成共沸物,从而影响环己烯的产量和纯度。 4、脱水产物: ①(CH3)2CHCH=CH2 ②(CH3)2C=CHCH3或者(CH3)2CHCH=CH2 ③(CH3)3CH=CH2 八、讨论: 1、本实验具有一定的危险性,在取浓硫酸时一定注意按照实验正规操作取浓硫酸。 2、要保证装置的气密性,防止出现严重的泄露。 3、第一次加热时可以是空气浴或者水浴加热,但是第二次的时候一定要水浴加热,防止温度变化范围太大。 4、各实验药品的添加顺序一定要正确,否则会影响实验的整个进程。 5、第一次蒸馏和第二次蒸馏的仪器有细微的差别,主要是短的分馏柱和分馏头的区别。
有机化学实验报告:环己酮的制备
环己酮的制备 华南师范:cai 前言: 环己酮,无色透明液体,分子量98.14 密度0.9478 g/mL 熔点?16.4 °C 沸点155.65 °C 在水中微溶;在乙醇中混溶。带有泥土气息,含有痕迹量的酚时,则带有薄荷味。不纯物为浅黄色,随着存放时间生成杂质而显色,呈水白色到灰黄色,具有强烈的刺鼻臭味。环己酮有致癌作用。环己酮是重要化工原料,是制造尼龙、己内酰胺和己二酸的主要中间体。也是重要的工业溶剂。也用作染色和褪光丝的均化剂,擦亮金属的脱脂剂,木材着色涂漆,可用环己酮脱膜、脱污、脱斑。 醇的氧化是制备醛酮的重要方法之一。本实验通氧化环己醇制备环己酮,氧化剂可以用铬酸或次氯酸,由于铬酸和它的盐价格比较贵,且会污染环境,用次氯酸或漂白粉来氧化醇可以避免这些缺点,产率也高。所以本实验采用次氯酸做氧化剂。 其他重要数据: 环己醇,有樟脑气味的无色粘性液体,熔点25.2℃沸点:160.9 ℃相对密度0.9624 环己酮和水形成恒沸点混合物,沸点95℃,含环己酮38.4%,溜出液中还有乙酸,沸程94~100℃。 反应方程式: 1、实验部分 1.1实验设备和材料 实验仪器:搅拌器、滴液漏斗、温度计、250mL三颈烧瓶、酒精灯、锥形瓶、冷凝管、蒸馏烧瓶、接液管、分液漏斗 实验药品:环已醇、次氯酸钠、冰醋酸、无水碳酸钠、无水硫酸镁、氯化铝、沸石、氯化钠、碘化钾淀粉试纸 1.2实验装置 反应装置蒸 馏装置分 液装置 1.3实验过程 混合反应:向装有搅拌器、滴 液漏斗和温度计的250mL三颈烧 瓶中依次加入5.2mL(5g,0.05 mol)环已醇和25mL冰醋酸。开 动搅拌器,在冰水浴冷却下,将 38mL次氯酸钠水溶液(约1.8mol/L)通过滴液漏斗逐滴加入反应瓶中,并使瓶内温度维持30~35℃,加完后搅拌5min,用碘化钾淀粉试纸检验应呈蓝色,否则应再补加5mL次氯酸钠溶液,以确保有过量次氯酸钠存在,使氧化反应完全。在室温下继续搅拌30min,加入饱和亚硫酸氢钠溶液至反应液对碘化钾淀粉试纸不显蓝色为至。 蒸馏粗产品:向反应混合物中加入30mL水、3g氯化铝和几粒沸石,在石棉网上加热蒸馏至馏出液无油珠滴出为至。 除杂干燥:在搅拌下向馏出液分批加入无水碳酸钠至反应液呈中性为止,然后加入精制食盐使之变成饱和溶液,将混合液倒入分液漏斗中,分出上层有机层;用无水硫酸镁干燥,过滤得到产物。
环己烯的制备思考题
环己烯的制备思考题 1、在粗制环己烯中加入精盐使水层达到饱和的目的何在? 答:目的是降低环己烯在水中的溶解;加饱和食盐水的目的是尽可能的除去粗产品中的水分,有利于分层。 2、在蒸馏终止前,出现的阵阵白雾是什么? 答:是浓磷酸由于反应物的减少而导致浓度增大而挥发的酸雾。 3、写出无水氯化钙吸水所起化学变化的反应式?为什么蒸馏前一定要将它过滤掉?答:CaCl2 +xH2O=CaCl 2?xH2O 常温下x 最大一般等于6。 蒸馏前若不将它过滤,会重新释放出H2O,使蒸馏产物中不可避免地混有少量水蒸气。 4、写出下列醇与浓硫酸进行脱水的反应产物。 a.3- 甲基-1-丁醇; b .3- 甲基-2-丁醇; c .3,3-二甲基-2-丁醇。 CH3 CH 3C=CHCH3 CH 3C=CHCH3 CH 3C=CCH3 CH3 CH3 CH3 补充: 1、用磷酸做脱水剂比用浓硫酸做脱水剂有什么优点? 答:(1)磷酸的氧化性小于浓硫酸,不易使反应物碳化;(2)无刺激性气体SO2放出。 2、如果你的实验产率太低,试分析主要在哪些操作步骤中造成损失? 答:(1)环己醇的粘度较大,尤其室温低时,量筒内的环己醇很难倒净而影响产率。(2)磷酸和环己醇混合不均,加热时产生碳化。(3)反应温度过高、馏出速度过快,使未反应的环己醇因于水形成共沸混合物或产物环己烯与水形成共沸混合物而影响产率。(4)干燥剂用量过多或干燥时间过短,致使最后蒸馏是前馏份增多而影响产率。 3、在环己烯制备实验中,为什么要控制分馏柱顶温度不超过73℃? 答:因为反应中环己烯与水形成共沸混合物(沸点70.8℃,含水10 %);环己醇与环己烯形成共沸混合物(沸点64.9℃,含环己醇30.5 %);环己醇与水形成共沸混合物(沸点97.8℃,含水80 %),因此,在加热时温度不可过高,蒸馏速度不易过快,以减少未反应的环己醇的蒸出。 4、当浓硫酸与环己醇混合时,为什么要充分摇匀? 答:浓硫酸与环己醇混合时应要充分摇匀,以免加热时使环己醇局部炭。 5、如果经干燥后蒸出的环己烯仍然浑浊,是何原因? 答:用无水氯化钙干燥的时间一般要在半个小时以上,并不时摇动。但实际实验中,由于时间关系,只能干燥5~10 分钟。因此,水可能没有除净的,在最后蒸馏时,会有较多的前馏分(环己烯和水的共沸物)蒸出,蒸出的环己烯会仍然浑浊。另外如果粗制品的最后一步蒸馏所用的仪器不干燥或干燥不彻底,则蒸出的产品将浑浊。 6、为什么蒸馏粗环已烯的装置要完全干燥? 答:因为环已烯可以和水形成二元共沸物,如果蒸馏装置没有充分干燥而带水,在蒸馏时则
己二酸制备
实验报告 尼龙66前体的制备 一、实验目的 1、学习由环己醇氧化制备环几酮和由环几酮氧化制备己二酸的基本原理。 2、掌握由环己醇氧化制备环己酮和由环己酮氧化制备己二酸的实验操作。 3、进一步了解盐析效应及萃取在分离有机化合物中的应用。 4、综合训练并掌握控温、减压抽滤、蒸馏、重结晶等操作技能。 二、实验原理 实验室制备脂肪和脂环醛、酮最常用的方法是将伯醇和仲醇用铬酸氧化。铬酸是重铬酸盐与40-50%硫酸的混合液。制备相对分子量低的醛,可以将铬酸滴加到热的酸性醇溶液中,以防止反应混合物中有过量的氧化剂存在,同时将较低沸点的醛不断蒸出,可以达到中等产率。尽管如此,仍有部分醛被进一步氧化成羧酸,并生成少量的酯。用此法制备酮,酮对氧化剂比较稳定,不易进一步被氧化。铬酸氧化醇是放热反应,必须严格控制反应温度以免反应过于剧烈。 本实验反应方程式为: 羧酸常用烯烃、醇、醛、酮等经硝酸、重铬酸钾的硫酸溶液或高锰酸钾等氧化来制备。本实验以环己酮为原料,在碱性条件下以高锰酸钾为氧化剂来制备己二酸,反应方程式: C 6H 10 O+MnO 4 -+2OH-→HOOC(CH 2 ) 4 COOH+MnO 2 +H 2 O 三、实验试剂和仪器装置: 1、仪器: 圆底烧瓶(250ml,100ml),烧杯(250ml,100ml) ,量筒(100ml ,10ml),,直型冷凝管,尾接管,蒸馏头,温度计,电热套,抽滤瓶,布氏漏斗,真空泵,蒸发皿,表面皿,分液漏斗,玻璃棒,石棉网,铁架台,酒精灯。 2、主要试剂: 浓H 2SO 4 ,Na 2 Cr 2 O 7 ,H 2 C 2 O 4 ,NaCl,无水MgSO 4 ,KMnO 4 ,NaOH10%,Na 2 SO 3
环己烯的制备
环己烯的制备 一、实验目的 1、学习、掌握由环己醇制备环己烯的原理及方法。 2、了解分馏的原理及实验操作。 3、练习并掌握蒸馏、分液、干燥等实验操作方法。 二、实验原理 OH 85%H 3PO 4+ H 2O OH 85%H 3PO 4 2 O + H 2O 主反应副反应 主反应为可逆反应,本实验采用的措施是:边反应边蒸出反应生成的环己烯和水形成的二元共沸物(沸点70.8℃,含水10%)。但是原料环己醇也能和水形成二元共沸物(沸点97.8℃,含水80%)。为了使产物以共沸物的形式蒸出反应体系,而又不夹带原料环己醇,本实验采用分馏装置,并控制柱顶温度不超过90℃。 反应采用85%的磷酸为催化剂,而不用浓硫酸作催化剂,是因为磷酸氧化能力较硫酸弱得多,减少了氧化副反应。 分馏的原理就是让上升的蒸汽和下降的冷凝液在分馏柱中进行多次热交换,相当于在分馏柱中进行多次蒸馏,从而使低沸点的物质不断上升、被蒸出;高沸点的物质不断地被冷凝、下降、流回加热容器中;结果将沸点不同的物质分离。详细的原理参见P88-89。 三、实验药品及物理常数 药品名称 分子量 (mol wt) 用 量 (ml 、g 、mol) 熔点 (℃) 沸点 (℃) 比重 (d 420) 水溶解度 (g/100ml) 环己醇 100.16 10ml (0.096mol ) 25.2 161 0.9624 稍溶于水 环己烯 82.14 83.19 0.8098 不溶于水 85%磷酸 98 5ml (0.08mol ) 42.35 1.834 易溶于水 其它药品 饱和食盐水、无水氯化钙
四、实验装置图 圆底烧瓶 刺形分馏柱 温度计 直形冷凝管 接引管 锥形瓶 蒸馏头 水浴 温度计 直形冷凝管 接引管 锥形瓶 图1 反应装置图2 蒸馏装置 图3 分液漏斗 五、实验流程图 10ml 环己醇5ml85%加样品摇匀 安装好仪器 加热反应分馏柱顶<90分去水层 粗产品无水等体积饱和食盐水洗涤 至出现白雾停止蒸馏 干燥 收集80-85度馏分产品称重,计算产率。 CaCl 2H 3PO 4 几粒沸石 ℃ 水浴蒸馏 六、实验步骤 在50毫升干燥的圆底(或茄形)烧瓶中,放入10ml 环己醇(9.6g ,0.096mol)、5ml85%磷酸,充分振摇、混合均匀。投入几粒沸石,按图1安装反应装置,用锥形瓶作接受器。 将烧瓶在石棉网上用小火慢慢加热,控制加热速度使分馏柱上端的温度不要超过90℃,馏出液为带水的混合物。当烧瓶中只剩下很少量的残液并出现阵阵白雾时,即可停止蒸馏。全部蒸馏时间约需40min 。 将蒸馏液分去水层,加入等体积的饱和食盐水,充分振摇后静止分层,分去水层(洗涤微量的酸,产品在哪一层?)。将下层水溶液自漏斗下端活塞放出、上层的粗产物自漏斗的上口倒入干燥的小锥形瓶中,加入1-2克无水氯化钙干燥。 将干燥后的产物滤入干燥的梨形蒸馏瓶中,加入几粒沸石,用水浴加热蒸馏。收集80-85℃的馏分于一已称重的干燥小锥形瓶中。产量4-5g 。 本实验约需4h 。 七、注意事项 1、环己醇在常温下是粘碉状液体,因而若用量筒量取时应注意转移中的损失。所以,取样时,最好先取环己醇,后取磷酸。 2、环己醇与磷酸应充分混合,否则在加热过程中可能会局部碳化,使溶液变黑。 3、安装仪器的顺序是从下到上,从左到右。十字头应口向上。 4、由于反应中环己烯与水形成共沸物(沸点70.8℃,含水l0%);环己醇也能与水形成共沸物(沸点97.8℃,含水80%)。因比在加热时温度不可过高,蒸馏速度不宜太快,以减少末作用的环己醇蒸出。文献要求柱顶控制在73℃左右,但反应速度太慢。本实验为了加快蒸出
环己酮的制备
有机化学实验报告 实验名称:环己酮的制备 学院:化学工程学院 专业:化学工程与工艺 班级: 姓名: 指导教师: 日期:2010年11月15日 一、实验目的 1、学习次氯酸氧化法制环己酮的原理和方法。 2、进一步了解醇和酮之间的联系和区别。 二、实验原理 醇类在氧化剂存在下通过氧化反应可被氧化为醛或酮。本实验用的环己醇属仲醇,因此氧化后生成环己酮。环己酮主要用于合成尼龙-6或尼龙-66,还广泛用作溶剂,它尤其因
对许多高聚物(如树脂、橡胶、涂料)的溶解性能优异而得到广泛的应用。在皮革工业中还用作脱脂剂和洗涤剂。 本实验用次氯酸钠做氧化剂,将环己醇氧化成环己酮。 三、主要试剂 环己醇、冰醋酸、次氯酸钠溶液(约1.8mol/L)、饱和亚硫酸氢钠溶液、氯化铝、碘化钾淀粉试纸、无水碳酸钠、氯化钠、无水硫酸镁、沸石 四、试剂用量规格 五、仪器装置 250mL三颈烧瓶、搅拌器、滴液漏斗、温度计、冷凝管、接受器、分液漏斗、烧杯、量筒、电热炉、石棉网、玻璃棒 图1 环己酮的反应装置
图2 环己酮的蒸馏提纯 六、实验步骤及现象 1、向装有搅拌器、滴液漏斗和温度计的250ml三颈烧瓶中依次加入5.2ml(5g,0.05mol)环己醇和25ml冰醋酸。开动搅拌器,在冰水浴冷却下,将38ml次氯酸钠溶液(约1.8mol/L)通过液滴漏斗逐渐加入反应瓶中,并使瓶内温度维持在30~35℃,加完后搅拌5min,用碘化钾淀粉试纸检验应呈蓝色,否则应再补加5ml次氯酸钠溶液,以确保有过量次氯酸钠存在,使氧化反应完全。在室温下继续搅拌30min,加入饱和亚硫酸氢钠溶液至发应液对碘化钾淀粉试纸不显蓝色为止。 2、向反应混合物中加入30ml水、3g氯化铝和几粒沸石,在石棉网上加热蒸馏至馏出液无油珠滴出为止。 3、在搅拌下向馏出液分批加入无水碳酸钠至反应液呈中性为止,然后加入精制食盐使之变成饱和溶液,将混合液倒入分液漏斗中,分出有机层,用无水硫酸镁干燥,蒸馏收集150~155℃馏分,计算产率。 七、实验结果 最终得到的环己酮为:1.6ml 产率为:1.6ml/5.2ml=30.77% 八、实验讨论 1、数据分析 产率相对较低,操作过程不够精细。 2、结果讨论 (1)、加热蒸馏得很充分,但是分液静置的时候时间不够长,导致环己酮的损失。 (2)、最后蒸馏的时候时间太短,不够充分,环己酮没有完全分离出来。 3、实际操作对实验结果的影响 (1)、反应温度要控制在30~35℃,此时收效较高,若温度低于30℃则不反应,温度
实验10环己酮的制备
酒泉职业技术学院《工科化学实验技术》学习领域教案
环己酮的制备 一、教学要求: 学习铬酸氧化法制环己酮的原理和方法。进一步了解醇和酮之间的联系和区别。 二、预习内容: 1.实验原理 2.抽虑操作 3.盐析 三、实验原理: 实验室制备脂肪或脂环醛酮,最常用的方法是将伯醇和仲醇用铬酸氧化。铬酸是重要的铬酸盐和40-50%硫酸的混合物。仲醇用铬酸氧化是制备酮的最常用的方法。酮对氧化剂比较稳定,不易进一步氧化。铬酸氧化醇是一个放热反应,必须严格控制反应的温度,以免反应
过于激烈。环己酮主要用于合成尼龙-6或尼龙-66,还广泛用作溶剂,它尤其因对许多高聚物(如树脂、橡胶、涂料)的溶解性能优异而得到广泛的应用。在皮革工业中还用作脱脂剂和洗涤剂。 四、仪器与药品 仪器: 250ml圆底烧瓶、温度计、蒸馏装置、分液漏斗。 药品:浓硫酸、环己醇、重铬酸钠、草酸、食盐、无水碳酸钠。 四、实验步骤: 1.铬酸溶液的配制 在250mL烧杯中加入30mL水和5.5g重铬酸钠,搅拌使之全部溶解。然后在搅拌下慢慢加入4.5mL浓硫酸,将所得橙红色溶液冷却至30℃以下备用。 2. 氧化反应在250mL圆底烧瓶中加入5.5mL环己醇,然后取此铬酸溶液lml 加入圆底烧瓶中,充分振摇,这时可观察到反应温度上升和反应液由橙红色变为 墨绿色,表明氧化反应已经发生。继续向圆底 烧瓶中滴加剩余的重铬酸钠(或重铬酸钾)溶 液,同时不断振摇烧瓶,控制滴加速度,保持 烧瓶内反应液温度在60~65℃之间。若超过此 温度时立即在冰水浴中冷却。在圆底挠瓶中插 入一支温度计,并继续振摇反应瓶。这时温度 徐徐上升,当温度上升到55℃时,用水浴冷 却,并维持反应温度在60~65℃。大约0.5h 左右,当温度开始下降时移去冷水浴,室温下图1 普通蒸馏装置 放置20分钟左右,其间仍要间歇振摇反应瓶几次,最后反应液呈墨绿色。如果反应液不能完全变成墨绿色,则应加入少量草酸(0.5~1.0g或甲醇1mL)以还原过量的氧化剂。 3.在反应瓶中加入30mL水,如图1装置仪器(改用锥形瓶作接受器)进行蒸馏,收集约50mL馏出液。这一步蒸馏操作实际上是一种简化了的水蒸气蒸馏。环已酮与水形成沸点为95℃的恒沸混合物(含环已酮38.4%)。应注意馏出液的量不能太多,因为馏出液中含水较多,而环已酮在水中的溶解度较大(31℃时为2.4g);否则,即使利用盐析效应,也有少量环已酮溶于水而损失掉。 4. 把馏出液用食盐水饱和,并将馏出液移至分液漏斗中,静止,分出有机相。水相用15mL乙醚提取一次,将乙醚提取液与有机相合并,用无水硫酸镁干燥。 5. 按图1装置仪器,在水浴上蒸出乙醚(在接液管的尾部接一通住水槽或室外的橡皮管,以便把易挥发、易燃的乙醚蒸气通入水槽的下水管内或引出室外),
环己烯的制备实验报告
OH H 3PO 4 + H 2O 实验八 环己烯的制备 一、实验目的: 1、 学习以浓磷酸催化环己醇脱水制备环己烯的原理和方法; 2、初步掌握分馏、水浴蒸馏和液体干燥的基本操作技能 二、实验原理:书P158 烯烃是重要的有机化工原料。工业上主要通过石油裂解的方法制备烯烃,有时也利用醇在氧化铝等催化剂存在下,进行高温催化脱水来制取,实验室里则主要用浓硫酸,浓磷酸做催化剂使醇脱水或卤代烃在醇钠作用下脱卤化氢来制备烯烃。 本实验采用浓磷酸做催化剂使环已醇脱水制备环已烯。 主反应式: 一般认为,该反应历程为E 1历程,整个反应 是可逆的:酸使醇羟基质子化,使其 易于离去而生 成正碳离子,后者失去一个质子,就生成烯烃。 可能的副反应:(难) 三、主要试剂、产物的物理和化学性质 化学物质 相对分子质量 相对密度/d 420 沸点/℃ 溶 解 度 /g(100g 水)-1 环己醇 100 3.620℃ 磷酸 98 -1/2H 2O(213℃) 2340 OH H OH 2-H 2 O
环己烯微溶于水 环己醚 243微溶于水 共沸物数据: 四、实验装置 仪器:50mL圆底烧瓶、分馏柱、直型冷凝管,100mL分液漏斗、100mL锥形瓶、蒸馏头,接液管。 试剂:10.0g(,)环已醇,4mL浓磷酸,氯化钠、无水氯化钙、5%碳酸钠水溶液。 其它:沸石 六、预习实验步骤、现场记录及实验现象解释 1、投料 在50ml干燥的圆底烧瓶中加入10g环己醇、4ml浓磷酸和几粒沸石,充分摇振使之混合均匀,安装反应装置。 2、加热回流、蒸出粗产物产物 将烧瓶在石棉网上小火空气浴缓缓加热至沸,控制分馏柱顶部的溜出温度不超过90℃,馏出液为带水的混浊液。至无液体蒸出时,可升高加热温度(缩小石棉网与烧瓶底间距离),当烧瓶中只剩下很少残液并出现阵阵白雾时,即可停止蒸馏。 3、分离并干燥粗产物 将馏出液用氯化钠饱和,然后加入3—4ml 5%的碳酸钠溶液中和微量的酸。将液体转入分液漏斗中,振摇(注意放气操作)后静置分层,打开上口玻塞,再将活塞缓缓旋开,下层液体从分液漏斗的活塞放出,产物从分液漏斗上口倒入一
环己酮肟实验报告
环己酮肟实验报告 篇一:环己酮的制备实验报告 20XX年11月19日 姓名///////////系年级20XX级应用化学系组别30同组者???科目有机化学题目环己酮的制备仪器编号 一、实验目的 1、学习铬酸氧化法制备环己酮的原理和方法。 2、通过醇转变为酮的实验,进一步了解醇和酮的联系和区别。 二、实验原理 实验室制备脂环醛酮,最常用的方法是将伯醇和仲醇用铬酸氧化。铬酸是重要的铬酸盐和40%~50%硫酸的混合物。仲醇用铬酸氧化是制备酮最常用的方法。酮对氧化剂比较稳定,不易进一步氧化。铬酸氧化醇是一个放热反应,必须严格控制反应的温度,以免反应过于剧烈。反应方程式为: Ho o 3 +na2cr2o7+4H2So4 + cr2(So4)3
+na2So4+ 7H2o 1 制备蒸馏装置 分液装置 精馏蒸馏装置 六、实验步骤 1、配制铬酸溶液:在200mL烧杯中加入30mL水和5.5g重铬酸钠,搅拌使之全部 溶解。然后在搅拌下慢慢加入 4.5mL浓硫酸,将所得橙红色溶液冷却到30℃以下备用; 2、250mL圆底烧瓶中加入5.3mL环己醇,然后一次加入配制好的铬酸溶液,并充分振摇使之混合均匀。用水浴冷却,控制反应温度在55~60℃。当温度开始下降时移去冷水浴,室温下放置0.5h,其间要间歇振摇反应瓶; 3、反应完毕后在反应瓶中加入30.0mL水和几粒沸石,改成蒸馏装置进行蒸馏。将环己酮和水一起蒸出来,直至馏出液不再浑浊再多蒸8~10mL,约收集馏出液25mL。 4、将馏出液用食盐饱和后转入分液漏斗中,分出有机相。水相用7.5mL乙醚提取一次,将乙醚提取液和有机相合并,用1~2g无水碳酸钾干燥;在水浴上蒸除乙醚,换空气冷凝管,蒸馏收集151~155℃馏分。
环己酮的制备实验报告
环己酮的制备实验报告 实验学专班姓指导日 机化学实验报告 名称:环己酮的制备 院:化学工程学院业:化学工程与工艺 级:化工12-4班名:王伟杰学号 12402010414 教师:张宗勇杨春风期: 有 一、实验目的 1、学习次氯酸氧化法制环己酮的原理和方法; 2、进一步了解醇和酮这件的联系和区别。 二、实验原理 用次氯酸钠作氧化剂,讲环己醇氧化成环己酮。 OH [O] O 三、主要试剂及仪器 试剂:环己醇(有樟脑气味的无色粘性液体,熔点:25.2℃,沸点: 160.9 ℃ 相对 密度:0.9624)、次氯酸钠、冰醋酸、无水碳酸钠、无水硫酸镁、氯化铝、沸石、氯化钠、碘化钾淀粉试纸。 仪器:搅拌器、滴液漏斗、温度计、250 ml三颈烧瓶、酒精灯、锥形瓶、冷凝管、蒸馏烧 瓶、接液管、分液漏斗。 四、试剂用量规格 五、实验仪器装置 反应装置蒸馏装置 分液装置空气冷凝蒸馏装置 六、实验步骤及现象 七、实验数据处理 环己醇的物质的量计算:n=m/M=5g/100g?mol-1=0.05mol 环己酮的物质的量计算:n′=m′/M′ 理论应该得出的环己酮的物质的量=实际环己醇的物质的量=0.05mol 环己酮产率=实际量/理论量 八、实验讨论
1、由于在第一次蒸馏时,溶液暴沸,所以将溶液过滤,除去沉积物,使得损失了大量 产品; 2、加热蒸馏不够充分,而且可能有部分蒸汽逸出,导致产品损失; 3、分液静置的时候时间不够长,导致产品损失; 4、最后蒸馏的时候时间太短,不够充分,使得环己酮没有完全分离出来。 九、注意事项 1、蒸馏时温度不宜升的过快,将导致溶液暴沸; 2、加入次氯酸不宜过多,否则中和时加入较多的亚硫酸氢钠,从而造成蒸馏时间过长; 3、盐析时,NaCl不宜加入太多,应该慢慢加入。
环己烯的制备实验报告
OH H3PO4 + H2O OH 共沸点 64.9o C 30.5% 69.5% OH 实验八环己烯的制备 计划学时:4学时 一、实验目的: 1、学习以浓磷酸催化环己醇脱水制备环己烯的原理和方法; 2、巩固分馏操作; 3、学习洗涤、干燥等操作。 二、实验原理: 烯烃是重要的有机化工原料。工业上主要通过石油裂解的方法制备烯烃,有时也利用醇在氧化铝等催化剂存在下,进行高温催化脱水来制取,实验室里则主要用浓硫酸,浓磷酸做催化剂使醇脱水或卤代烃在醇钠作用下脱卤化氢来制备烯烃。 本实验采用浓磷酸做催化剂使环已醇脱水制备环已烯。 主反应式: 一般认为,该反应历程为E1历程,整个反应是可逆的:酸使醇羟基质子化,使其易于离去而生成正碳离子,后者失去一个质子,就生成烯烃。 可能的副反应:(难) 三、主要仪器和试剂 仪器:50mL圆底烧瓶、分馏柱、直型冷凝管,100mL分液漏斗、100mL锥形瓶、蒸馏头,接液管。 试剂:10.0g(10.4mL,0.1mol)环已醇,4mL浓磷酸,氯化钠、无水氯化钙、5%碳酸钠水溶液。 四、试剂物理常数 1.查阅实验所涉及到的反应物、催化剂、产物、副产物(甚至溶剂,萃取剂等)的各种物理、化学 化学物质相对分子质量相对密度 /d420 沸点/℃溶解度/g(100g 水)-1 环己醇100 0.96 161.1 3.620℃ 磷酸98 1.83 -1/2H2O(213℃) 2340 环己烯82.14 0.89 83.3 微溶于水 环己醚182.3 0.92 243 微溶于水 共沸物数据: OH H OH-H 2 O H O H
五、实验装置 六、实验步骤: 1、投料 在50ml干燥的圆底烧瓶中加入10g环己醇、4ml浓磷酸和几粒沸石,充分摇振使之混合均匀,安装反应装置。 2、加热回流、蒸出粗产物产物 将烧瓶在石棉网上小火空气浴缓缓加热至沸,控制分馏柱顶部的溜出温度不超过90℃,馏出液为带水的混浊液。至无液体蒸出时,可升高加热温度(缩小石棉网与烧瓶底间距离),当烧瓶中只剩下很少残液并出现阵阵白雾时,即可停止蒸馏。 3、分离并干燥粗产物 将馏出液用氯化钠饱和,然后加入3—4ml 5%的碳酸钠溶液中和微量的酸。将液体转入分液漏斗中,振摇(注意放气操作)后静置分层,打开上口玻塞,再将活塞缓缓旋开,下层液体从分液漏斗的活塞放出,产物从分液漏斗上口倒入一干燥的小锥形瓶中,用1—2g无水氯化钙干燥。 4、蒸出产品 待溶液清亮透明后,小心滤入干燥的小烧瓶中,投入几粒沸石后用水浴蒸馏,收集80—85℃的馏分于一已称量的小锥形瓶中。 注意事项: 1、投料时应先投环己醇,再投浓磷酸;投料后,一定要混合均匀。 2、反应时,控制温度不要超过90℃。 3、干燥剂用量合理。 4、反应、干燥、蒸馏所涉及器皿都应干燥。 5、磷酸有一定的氧化性,加完磷酸要摇匀后再加热,否则反应物会
细胞生物学实验报告
染色体标本的制备及观察 泮力菁201100140091 2011级生物基地同组者:商倩倩 【实验目的】 1、掌握染色体标本制作的方法; 2、认识不同生物染色体的特征,学会制作染色体组形图; 【实验原理】 1、制作染色体标本的意义:A、生物学方面:根据染色体特征鉴别生物及种类(例如猫38;小鼠40;大鼠42;兔44;人46;马64;鸡和狗78);B、临床医学方面:主要用于遗传性疾病的诊断及研究(例如21三体综合症,卵巢退化症;睾丸退化症等)。因此,染色体阻性实验广泛应用与胎儿遗传性疾病早期诊断中(抽羊水做组型)。 2、染色体标本的制作原理:A、制作染色体标本的先决条件:细胞具有旺盛的分裂能力(选择活跃的组织:胸腺,骨髓,睾丸,小肠;施加药物使细胞分裂);设法得到大量的分裂中期细胞(秋水仙素)。B、重要点:PHA:促细胞分裂,使淋巴细胞返幼,变为淋巴母细胞;秋水仙素:破坏微管装配,使纺锤体不能形成,使大量细胞停止在分裂中期;低渗作用:水进入细胞内,细胞内容空间变大,染色体间的距离拉大,抑郁cs分散开;空气干燥:使细胞和cs展开;固定:用carnoy’s solution(甲醇:冰醋酸=3:1)作用是蛋白质变性,对染色体内的组蛋白讲,变性后硬度增加,保持了染色体的“即时形态”,对细胞膜蛋白讲,变性使细胞膜硬度增加,形成屏障作用,防止了细胞内物质的外溢和丢失。 3、本实验选择的实验材料是小鼠的睾丸。睾丸是雄性动物生殖细胞发育和成熟的部位,是产生精子的器官。睾丸内的曲细精管从外到内依次分布有精原细胞、初级精母细胞、次级精母细胞、精子细胞以及形态渐变中的精子。取睾丸将曲细精管中的细胞冲出后固定,然后制片染色,可以观察到动物生殖细胞减数分裂染色体的不同时相。如果提前给动物的腹腔注射秋水仙素溶液可抑制生殖细胞的正常分裂,增加了中期分裂细胞的数目,此方法可用来进行减数分裂过程中染色体的计数与观察。 睾丸染色体标本的制备,可以用来检测雄性个体生殖细胞是否受到周围环境污染或是否发生病变,是小型动物生殖学常规实验。 4、染色体标本的制作: ①观察:由于分裂期中期的染色体染色体凝集程度最高,因而我们应尽量使细胞停留在分裂期中期以便观察。 ②细胞:为尽量看到多的染色体,我们应当选取具有旺盛分裂能力的细胞,这样的细胞可以来自:胸腺、骨髓、睾丸、小肠等。我们在此实验中使用的是小鼠的精巢细胞。在做人的染色体标本时,我们使用的是血液里的淋巴细胞。 ③药物: PHA(植物细胞凝集素):PHA具有促进细胞凝集和分裂的作用。PHA 可以使血液中的淋巴细胞还原至淋巴母细胞(只存在于骨髓中);秋水仙素:秋水仙素可以破坏微管的组装,纺锤体不能形成,细胞分裂停在中期。与秋水仙素作用相同的药物还有长春花碱、鬼臼素、苯环己烯等。可以促进胃管组装的药物
环己酮肟的制备实验报告
环己酮肟的制备实验报告 篇一:环己酮肟的制备 实验二十六环己酮肟的制备 一实验目的 学习用酮和羟胺的缩合反应制备肟的方法 二实验原理: +nh2ohhcl+hcl 三主要试剂:盐酸羟胺2.5g(35mmol),环己酮 2.5g(2.7ml,25mmol). 四实验步骤: 在50ml的烧杯内将2.5g 盐酸羟胺溶解于7.5ml 水中(可 以微微加热)。然后慢慢用6mol/Lnaoh 水溶液中和(ph=8 左右)并冷却至室温。 五注意事项 1.反应回流后如溶液中有不溶性固体杂质,则可趁热减 压过滤。 篇二:环己酮肟的制备 环己酮肟的制备(cyclohexanoneoxime) 一、实验目的: 学习用酮和羟胺的缩合反应制备肟的方法 二、实验原理:o +nh2ohhcln+hcl
三、主要试剂: 盐酸羟胺2.5g(35mmol),环己酮2.5g(2.7ml,25mmol). 四、实验步骤:在50mlde 烧杯内将2.5g 盐酸羟胺溶解于7.5ml 水中(可以微微加热)。然后慢慢用6mol/Lnaoh 水溶液中和(ph=8 左右)并冷却至室温。将2.7ml 环己酮加入50ml 的圆底烧瓶中,加入4.0ml乙醇,在不断搅拌下,滴加上述羟胺溶液。加毕,回流20min, 回流后如溶液中有不溶性固体杂质,则趁热减压过滤。将滤液冷却,析出晶体,过滤,干燥,称重,计算产率(一般85%)。测定产品熔点,(产品的熔点88-89oc)。思考题及注意事项204.204.实验室使用或蒸馏乙醚时应注意哪些问题? 答:在实验室使用或蒸馏乙醚时,实验台附近严禁有明火。因为乙醚容易挥发,且易燃烧,与空气混和到一定比例时即发生爆炸。所以蒸馏乙醚时,只能用热水浴加热,蒸馏装置要严密不漏气,接收器支管上接的橡皮管要引入水槽或室外,且接收器外要用冰水冷却。另外,蒸馏保存时间较久的乙醚时,应事先检验是否含过氧化合物。因为乙醚在保存期间与空气接触和受光照射的影响可能产生二乙基过氧化物(c2h5ooc2h5),过氧化物受热.
环己烯的制备--实验报告
OH H 3PO 4 + H 2 O OH 共沸点 64.9o C 30.5% 69.5%OH 实验八 环己烯的制备 一、实验目的: 1、 学习以浓磷酸催化环己醇脱水制备环己烯的原理和方法; 2、初步掌握分馏、水浴蒸馏和液体干燥的基本操作技能 二、实验原理:书P158 烯烃是重要的有机化工原料。工业上主要通过石油裂解的方法制备烯烃,有时也利用醇在氧化铝等催化剂存在下,进行高温催化脱水来制取,实验室里则主要用浓硫酸,浓磷酸做催化剂使醇脱水或卤代烃在醇钠作用下脱卤化氢来制备烯烃。 本实验采用浓磷酸做催化剂使环已醇脱水制备环已烯。 主反应式: 一般认为,该反应历程为E 1历程,整个反应是可逆的:酸使醇羟基质子化,使其易于离去而生成正碳离子,后者失去一个质子,就生成烯烃。 可能的副反应:(难) 三、主要试剂、产物的物理和化学性质 化学物质 相对分子质量 相对密度/d 420 沸点/℃ 溶解度/g(100g 水)-1 环己醇 100 0.96 161.1 3.620 ℃ 磷酸 98 1.83 -1/2H 2O(213℃) 2340 环己烯 82.14 0.89 83.3 微溶于水 环己醚 182.3 0.92 243 微溶于水 共沸物数据: 四、实 验装置 OH H OH 2-H 2O H O H
仪器:50mL圆底烧瓶、分馏柱、直型冷凝管,100mL 分液漏斗、100mL锥形瓶、蒸馏头,接液管。 试剂:10.0g(10.4mL,0.1mol)环已醇,4mL浓磷酸, 氯化钠、无水氯化钙、5%碳酸钠水溶液。 其它:沸石 六、预习实验步骤、现场记录及实验现象解释 1、投料 在50ml干燥的圆底烧瓶中加入10g环己醇、4ml浓磷酸和几粒沸石,充分摇振使之混合均匀,安装反应装置。 2、加热回流、蒸出粗产物产物 将烧瓶在石棉网上小火空气浴缓缓加热至沸,控制分馏柱顶部的溜出温度不超过90℃,馏出液为带水的混浊液。至无液体蒸出时,可升高加热温度(缩小石棉网与烧瓶底间距离),当烧瓶中只剩下很少残液并出现阵阵白雾时,即可停止蒸馏。 3、分离并干燥粗产物 将馏出液用氯化钠饱和,然后加入3—4ml 5%的碳酸钠溶液中和微量的酸。将液体转入分液漏斗中,振摇(注意放气操作)后静置分层,打开上口玻塞,再将活塞缓缓旋开,下层液体从分液漏斗的活塞放出,产物从分液漏斗上口倒入一干燥的小锥形瓶中,用1—2g无水氯化钙干燥。 4、蒸出产品 待溶液清亮透明后,小心滤入干燥的小烧瓶中,投入几粒沸石后用水浴蒸馏,收集80—85℃的馏分于一已称量的小锥形瓶中。 六、产品产率的计算 注意事项: 1、投料时应先投环己醇,再投浓磷酸;投料后,一定要混合均匀。 2、反应时,控制温度不要超过90℃。 3、干燥剂用量合理。 4、反应、干燥、蒸馏所涉及器皿都应干燥。 5、磷酸有一定的氧化性,加完磷酸要摇匀后再加热,否则反应物会 被氧化。 6、环己醇的粘度较大,尤其室温低时,量筒内的环己醇若倒不干净,会 影响产率。 7、用无水氯化钙干燥时氯化钙用量不能太多,必须使用粒状无水氯化钙。粗产物干燥好后再蒸馏,蒸馏装置要预先干燥,否则前馏分多(环己
2020年环己烯制备实验报告
实验八环己烯的制备一、实验目的 1、学习以浓磷酸催化环己醇脱水制备环己烯的原理和方法; 2、初步掌握分馏、水浴蒸馏和液体干燥的基本操作技能二、实验原理书P158 烯烃是重要的有机化工原料。工业上主要通过石油裂解的方法制备烯烃,有时也利用醇在氧化铝等催化剂存在下,进行高温催化脱水来制取,实验室里则主要用浓硫酸,浓磷酸做催化剂使醇脱水或卤代烃在醇钠作用下脱卤化氢来制备烯烃。 本实验采用浓磷酸做催化剂使环已醇脱水制备环已烯。 主反应式 一般认为,该反应历程为E1历程,整个反应是可逆的酸使醇羟基质子化,使其易于离去而生成正碳离子,后者失去一个质子,就生成烯烃。 可能的副反应(难)三、主要试剂、产物的物理和化学性质化学物质相对分子质量相对密度/d42 沸点/℃溶解度/g(1g水)-1 环己醇 1 .96 161 62℃磷酸98 83 -1/2H2O(213℃) 234 环己烯 814 .89 83 微溶于水环己醚183 .92 243 微溶于水共沸物数据 四、实验装置仪器5mL圆底烧瓶、分馏柱、直型冷凝管,1mL分液漏斗、1mL锥形瓶、蒸馏头,接液管。 试剂1.g(1.4mL,.1mol)环已醇,4mL浓磷酸,氯化钠、无水氯化钙、5%碳酸钠水溶液。 其它沸石六、预习实验步骤、现场记录及实验现象解释 1、投料在5ml干燥的圆底烧瓶中加入1g环己醇、4ml浓磷酸和几粒沸石,充分摇振使之混合均匀,安装反应装置。 2、加热回流、蒸出粗产物产物将烧瓶在石棉网上小火空气浴缓缓加热至沸,控制分馏柱顶部的溜出温度不超过9℃,馏出液为带水的混浊液。至无液体蒸出时,可升高加热温度(缩小石棉网与烧瓶底间距离),当烧瓶中只剩下很少残液并出现阵阵白雾时,即可停止蒸馏。 3、分离并干燥粗产物将馏出液用氯化钠饱和,然后加入3—4ml 5%的碳酸钠溶液中和微量的酸。将液体转入分液漏斗中,振摇(注意放气操作)后静置分层,打开上口玻塞,再将活塞缓缓旋开,下层液体从分液漏斗的活塞放出,产物从分液漏斗上口倒入一干燥的小锥形瓶中,用1—2g无水氯化钙干燥。 4、蒸出产品待溶液清亮透明后,小心滤入干燥的小烧瓶中,投入几粒沸石后用水浴蒸馏,收集8—85℃的馏分于一已称量的小锥形瓶中。 六、产品产率的计算注意事项
