溶解度练习题

溶解度练习题
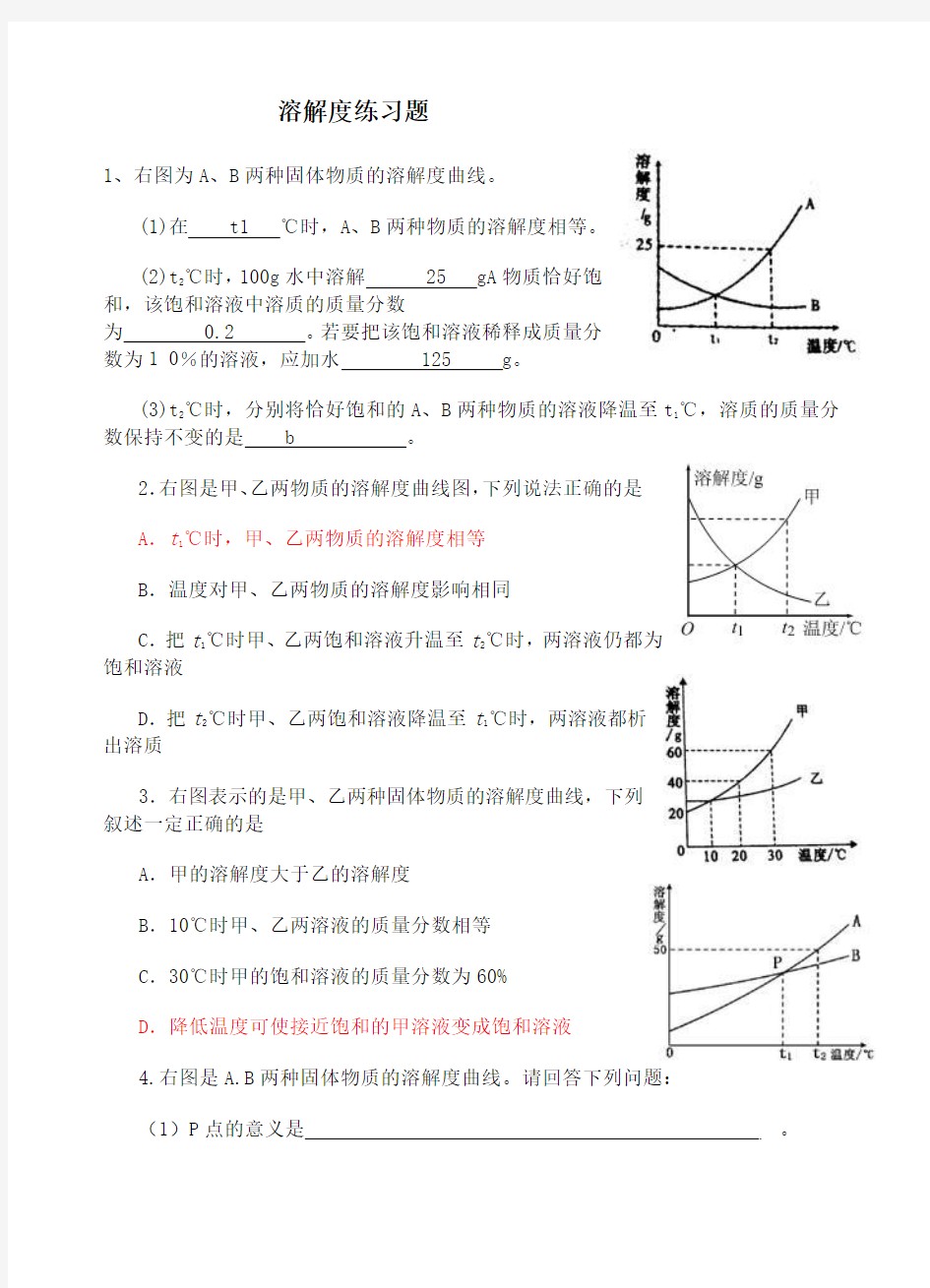
1、右图为A、B两种固体物质的溶解度曲线。
(1)在t1 ℃时,A、B两种物质的溶解度相等。
(2)t
2
℃时,100g水中溶解25 gA物质恰好饱和,该饱和溶液中溶质的质量分数
为0.2 。若要把该饱和溶液稀释成质量分数为1 0%的溶液,应加水125 g。
(3)t
2℃时,分别将恰好饱和的A、B两种物质的溶液降温至t
1
℃,溶质的质量分
数保持不变的是 b 。
2.右图是甲、乙两物质的溶解度曲线图,下列说法正确的是
A.t1℃时,甲、乙两物质的溶解度相等
B.温度对甲、乙两物质的溶解度影响相同
C.把t1℃时甲、乙两饱和溶液升温至t2℃时,两溶液仍都为
饱和溶液
D.把t2℃时甲、乙两饱和溶液降温至t1℃时,两溶液都析
出溶质
3.右图表示的是甲、乙两种固体物质的溶解度曲线,下列
叙述一定正确的是
A.甲的溶解度大于乙的溶解度
B.10℃时甲、乙两溶液的质量分数相等
C.30℃时甲的饱和溶液的质量分数为60%
D.降低温度可使接近饱和的甲溶液变成饱和溶液
4.右图是A.B两种固体物质的溶解度曲线。请回答下列问题:
(1)P点的意义是。
(2)t
2
℃时,将60g A物质放入100g水中,充分搅拌,所得溶液的质量
是150 g。
(3)将接近饱和的A物质的水溶液,变成饱和溶液的方法
有降低温度(答出一种即可)。
5、(3分)右图是a、b、c三种物质的溶解度曲线,a与c的溶解度曲线相交于P点。据图回答:
(1)P点的含义
是
(2)t
1
℃时30g a物质加入到50g水中不断搅拌,能
形成80g溶液吗?(填“能”或“不能”)。
(3)t
2
℃时,a、b、c三种物质的溶解度按由小到大的顺序排列的
是(填物质序号)。
6、(3分)向装有等量水的A、B、C烧杯中分别加入10g、25g、25gNaNO
3
固体,充分溶解后,现象如图一所示。
(1)烧杯中的溶液一定属于饱和溶液的是 b (填序号);
(2)图二能表示NaNO
3
溶解度曲线的是(填“甲”或“乙”);
(3)由图二分析,若分别将100g甲、乙的饱和溶液从t
2℃降温到t
1
℃,对所得
溶液的叙述正确的(填序号)。
A.甲、乙都是饱和溶液B.所含溶剂质量:甲<乙
C .溶液质量:甲>乙
D .溶质质量分数:甲>乙
i .要使w g 10%的NaCl 溶液的溶质的质量分数增至20%,可采用的方法是
A .再加入10w g 固体NaCl
B .蒸发浓缩成2w
g NaCl 溶液
C .蒸发掉一半溶剂
D .再加入2w g 25%的NaCl 溶液
ii .分别取等质量80℃的甲、乙两种化合物的饱和溶液,降温至20℃后,所析出的甲的质量比
乙的大(甲和乙均无结晶水)。下列关于甲、乙的溶解度的叙述中肯定正确的是
A .20℃时,乙的溶解度比甲的大
B .80℃时,甲的溶解度比乙的大
C .温度对乙的溶解度影响较大
D .温度对甲的溶解度影响较大
iii .右图是物质M 的溶解度曲线图,则P 点表示
A .饱和溶液
B .不饱和溶液
C .M 未完全溶解
D .无法配制
iv .(2005.11灌云县调研15)将40℃的饱和硫酸铜溶液升温至50℃,或者温
度仍保持在40℃而加入少量无水硫酸铜,在这两种情况下均保持不变的是
A .硫酸铜的溶解度
B .溶液中溶质的质量分数
C .溶液的质量
D .溶液中Cu 2+的数目
v .有一杯t ℃时的硝酸铵溶液,在该溶液中加入x g 硝酸铵晶体,充分搅拌后有y g 未溶;若将
原溶液加热蒸发掉2g 水再冷却至原温度,溶液恰好达到饱和,则t ℃时硝酸铵的溶解度
A .100x g
B .2200x y -+g
C .100()2x y -g
D .200x y -g vi .在烧杯中盛有10%的CaCl 2溶液,然后向烧杯中逐滴加入10%的Na 2CO 3溶液至不再生成沉
淀为止,过滤得到CaCO 3沉淀10g ,再将滤液蒸发掉90g 水后,所剩溶液的质量分数是多少?
A .11.7%
B .10%
C .9.2%
D .5.85%
vii .在25℃时,将某浓度的芒硝溶液分为等质量的两份溶液,一份加热蒸发掉20g 水后降至25℃
成为饱和溶液,另一份加入10g 芒硝晶体后也成为饱和溶液。则25℃时芒硝的溶解度是
A .20g
B .17.23g
C .30g
D .22.05g
viii .20℃时,将某盐R 的溶液蒸发掉10g 水,恢复到20℃,需在剩余溶液中加入6g R (无水),溶液达饱和;若将原溶液蒸发掉30g 水,则只需加入1g R (无水)就可以在20℃达到饱和,20℃时R 的溶解度为
A .20g
B .25g
C .30g
D .35g
ix .t ℃时,在V mL 密度为dg /cm 3的FeCl 3(相对分子质量为M )饱和溶液中,加入足量的NaOH
溶液,充分反应后过滤(假设滤液无损失),在滤液中加入适量硝酸使溶液呈中性后,再加入4mL 1.0 mol /L 的AgNO 3溶液恰好完全反应,则t ℃时FeCl 3的溶解度为
A .g M
dV M -3000400 B .g Vd M 15 C .g M Vd M -250100 D .g M Vd M -750100 x .某温度下,在100g 水中加入mg CuSO 4或加入ng CuSO 4·5H 2O ,均可使溶液恰好达到饱和,
则m 与n 的关系符合
A .m =n 250160
B .m =n n 925001600+
C .m =n n 1625001600+
D .m =n
n 2525001600+ xi .(2005.8启东中学8)t ℃时将某氢氧化钠溶液蒸发去8.2g 水后,恢复至t ℃析出5.8gNaOH ·H 2O
晶体。再蒸发去1.2g 水,恢复至t ℃,又析出5.8gNaOH ·H 2O 晶体,则t ℃时NaOH 的溶解度约为
A .40g
B .133.3g
C .333.3g
D .483.3g
xii .在t ℃时,取可溶物A 其浓度为a%的溶液100g ,蒸发掉p g 水,冷却到t ℃,析出A 的不含
结晶水的晶体g g ,则在t ℃时,A 的溶解度为
A .100()100a g a p ---g
B .100100()a g a g ---g
C .100100a a
-g D .100()a g a p --g xiii .在一定温度下,某无水盐R 在水中溶解度为23g ,向R 的饱和溶液中加入Bg 该无水盐,保
持温度不变,析出R 的结晶水合物Wg ,从原饱和溶液中析出溶质R 的质量为
A .23(W -
B )/123g B .23(W -B )/77g
C .23(W -B )/100g
D .(W -77B/23)/g
xiv .某温度下,氯化镁饱和溶液浓度为40%,在足量的此溶液中加入4.6g 无水氯化镁,最终析
出结晶水合物40.6g ,则该结晶水合物的化学式是
A .MgCl 2·7H 2O
B .MgCl 2·2H 2O
C .MgCl 2·6H 2O
D .MgCl 2·5H 2O
xv .已知20℃时,CuSO 4的溶解度为20g 。此温度下将36g 的无水硫酸铜放入100g 水中,充分
搅拌后,所得溶液的质量约为
A .136 g
B .120g
C .116g
D .108g
xvi .t ℃时,Na 2CO 3的溶解度为40 g ,现有饱和碳酸钠溶液Ag ,溶质质量分数为a %,向溶液中
投入碳酸钠固体10g ,静置后析出一定量晶体(Na 2CO 3·10H 2O ),加水使晶体全部溶解,所得溶液质量分数仍为a %,加入水的量是
A . 100g
B . 25g
C . (100-A )180/286g
D . 不能确定 xvii .某温度下,向一定质量的饱和石灰水中加入少量生石灰,并恢复到原温度,则
A .溶质的溶解度不变
B .溶液中溶质的质量增加
C.溶质的质量分数减少D.溶质的质量分数增大
xviii.Ca(OH)2在80℃时的溶解度为x g,20℃时溶解度为y g,取80℃时Ca(OH)2的饱和溶液
a g蒸发掉w g水后,再恢复至20℃,滤去折出固体,滤液中Ca(OH)2的质量分数为z%,
则x、y、z的关系正确的是
A.x>y>z B.y
xix.T℃时,bg固体A能完全溶解于水形成(a+b)g溶液。若固体A不含结晶水,也不与水反应;
则T℃时,A的溶解度肯定不可能是
A.100b
a g B.
200b
a g C.
100b
a b
+g D.
100()
a b
a
+
g
xx.某学生在10℃时取100g水配制成氯化钾的饱和溶液,又取50g水加入35.4g硝酸钠配成溶液,然后将两种溶液混合,发现有晶体析出。已知10℃时,氯化钾、硝酸钠、氯化钠、硝酸钾的溶解度依次为31g、80g、35.8g、20.9g。通过计算可推断出析出的晶体是
A.氯化钾B.硝酸钠C.氯化钠D.硝酸钾
xxi.浓度不等的两种硫酸溶液等质量混和时,其质量百分比浓度为a%,而等体积混和时为b%;
浓度不等的两种乙醇溶液等质量混和后,其质量百分比浓度也为a%,而等体积混和时为c%,则a、b、c间的关系是
A.a>b>c B.b>a>c C.c>a>b D.不可比较
xxii. (2005.4苏锡常镇一模15)已知:t℃时,某物质的不饱和溶液a g中含溶质m g。若溶液蒸发b g水并恢复到t℃时,析出溶质m1 g;若原溶液蒸发c g水并恢复到t℃时,则析出溶质m2 g。
若用S表示该物质在t℃时的溶解度,下式中正确的是
A.S=100m
a m
-g B.S=
2
100m
c g C.S=
12
100()
m m
b c
-
-g D.S=
1
100()
m m
a b
-
-g
xxiii. (2005.9南京调研10)在一定温度下,向15g蒸馏水中加入一包无水硫酸铜粉末,充分搅拌后过滤,得到一定质量的蓝色晶体和8.4g滤液。若此温度下无水硫酸铜的溶解度为40g,则此包无水硫酸铜的质量是
A.6.6g B.9g C.18.4g D.16g
xxiv. (2005.10丹阳市统测18)有一定质量的KNO
3
样品,在10℃下加蒸馏水使之充分溶解,残留固体的质量为250g。该实验在40℃下进行时,残留固体质量为120g,70℃时为20g。已知KNO3在不同温度下的溶解度:
下列对该样品的推断正确的是
A.样品为纯净物B.样品中混有不溶于水的杂质
C.样品中混有溶解度较大的杂质D.当温度在55℃左右时KNO3完全溶解
xxv. (2005.10泗阳中学14)Na
2
SO4溶液的溶解度曲线如图,
下列说法一定错误的是
A.A点表示Na2SO4溶液尚未达到饱和,但降温和加入
Na2SO4·H2O晶体都可使其饱和
B.B、C点表示t1℃时,Na2SO4溶液在B点的溶解度大
于在C点的溶解度
C.在C点时Na2SO4溶液降温或升温,都会使其溶液变浑浊
D.制取芒硝的最佳方法是在100℃时配成饱和溶液,再降温至0℃析出晶体
xxvi.有一种由CaCl2和NaCl组成的混和物,取34.8g溶于50g水使其充分溶解后,加入m g 某浓度的Na2CO3溶液恰好完全反应,生成20g沉淀。经过滤,所得滤液在t℃时刚好为饱和溶液(已知t℃时NaCl的溶解度为36g)。试求:(1)m值;(2)所加Na2CO3溶液的质量分数。
xxvii.将100g 15%的NaCl溶液稀释成10%的NaCl溶液,取稀释后的溶液11.7g与17g AgNO3溶液混合恰好完全反应。求:(1)稀释NaCl溶液时所加水的质量;(2)AgNO3溶液的溶质质量分数。
xxviii.将200g浓度为3.65%的稀盐酸加入到80g浓度为10%的NaOH溶液里恰好完全反应,(已知20℃时NaCl的溶解度为36g)试求:(1)反应后溶液中水的质量;(2)若将反应后所得溶液制成20℃时的饱和溶液,需蒸发掉多少克水?
xxix.30℃时将8.0g饱和硫酸铜溶液加水稀释至100mL,取出10mL溶液于试管中,加入过量的碘化钾溶液,发生以下反应:2Cu2++4I-=2CuI↓+ I2, 反应所生成的I2能够把20mL 0.05mol/L的
Na2S2O3溶液中的S2O2
3-全部氧化成S
4
O2
6
-,反应方程式为:I
2
+2S2O2
3
-=2I-+S
4
O2
6
-。请计算:30℃
时硫酸铜溶液的溶解度。
xxx.(2005.10泗阳中学26)进行下列实验:将过量Mg粉溶于100 mL 1.5 mol/L稀H
2
SO4中,反应结束后,滤去多余Mg粉,滤液在t℃下蒸发,当滤液质量为63 g时开始析出MgSO4·xH2O晶体,当析出晶体13.47g时,剩下滤液40g。请计算下列各小题:(1) 生成标准状况下的气体体积;(2) 开始析出MgSO4·xH2O晶体时溶液的质量分数;(3) t℃时该晶体的溶解度;(4) MgSO4·xH2O中的x
值。
溶液、溶解度知识点
初三化学:溶液、溶解度知识点梳理 要点梳理: 一、溶液 1.溶液的定义:一种或几种物质分散在另一种物质中,形成均一、稳定的混合物叫做溶液。 2,溶液的特征 (1)均一性:是制溶液各部分组成、性质完全相同。 (2)稳定性:是指外界条件不变(温度、压强等),溶剂的量不变时,溶液长期放置不会分层也不会析出固体或气体。 二、、饱和溶液与不饱和溶液 1,概念: (1)饱和溶液:在一定温度下、一定量的溶剂里,不能溶解某种绒织的溶液,叫做这种溶质的饱和溶液。 (2)不饱和溶液:在一定温度下、一定量的溶剂里,还能继续溶解某种溶质的溶液,叫做这种溶质的不饱和溶液。 2.饱和溶液与不饱和溶液的意义在于指明“一定温度”和“一定量的溶剂”,且可以相互转化: 饱和溶液不饱和溶液 三、、固体物质的溶解度以及溶解度曲线 1.概念: 在一定温度下,某固体物质在100g溶剂里达到饱和状态时,所溶解溶质的质量,叫做这种物质在这种溶解里的溶解度。 2.影响固体溶解度大小的因素 (1)溶质、溶剂本身的性质 (2)温度
3.溶解度曲线 (1)溶解度曲线的意义: ①溶解度曲线表示某物质在不同温度下的溶解度或溶解度随温度的变化情况。 ②溶解度曲线上的每一个点表示溶质在某一温度下的溶解度。此时,溶液必定是饱和溶液。 ③两条曲线的交叉点表示两种物质在该温度下具有相同的溶解度。在该温度下,这两种物质的饱和溶液中溶质的质量分数相等。 ④在溶解度曲线的下方的点,表示该温度下的溶液是该物质的不饱和溶液。 ⑤在溶解度曲线上方的点,表示该温度下的溶液是该物质的过饱和溶液,也就是说,在溶液中存在未溶解的溶质。 (2)溶解度曲线变化的规律 大多数固体物质的溶解度随温度的升高而增大,一般表现在曲线“坡度”比较“陡”,如硝酸钾;少数固体物质的溶解度受温度的影响较小,表现在曲线的“坡度”比较“平缓”,如氯化钠;极少数固体物质的溶解度随温度的升高而减小,表现在曲线的“坡度”下降,如熟石灰。 四、结晶的方法: (1)蒸发结晶(蒸发溶剂法):将固体溶质的溶液加热(或日晒,或在风力的作用下)使溶剂蒸发,使溶液又不饱和溶液转化为饱和溶液,再继续蒸发溶剂,使溶质从溶液中析出。适用范围:溶解度受温度变化影响不大的物质,如氯化钠。 (2)降温结晶(冷却热饱和溶液法)冷却热的饱和溶液,使溶质从溶液中结晶析出。适用范围:溶解度受温度变化影响较大的物质,如氯酸钾。
宏观经济学思考题及参考答案
宏观经济学思考题及参考答案(1) 第四章 基本概念:潜在GDP,总供给,总需求,AS曲线,AD曲线。 思考题 1、宏观经济学的主要目标是什么?写出每个主要目标的简短定义。请详细解释 为什么每一个目标都十分重要。 答:宏观经济学目标主要有四个:充分就业、物价稳定、经济增长和国际收支平衡。 (1)充分就业的本义是指所有资源得到充分利用,目前主要用人力资源作为充分就业的标准;充分就业本不是指百分之百的就业,一般地说充分就业允许的失业范畴为4%。只有经济实现了充分就业,一国经济才能生产出潜在的GDP,从而使一国拥有更多的收入用于提高一国的福利水平。 (2)物价稳定,即把通胀率维持在低而稳定的水平上。物价稳定是指一般物价水平(即总物价水平)的稳定;物价稳定并不是指通货膨胀率为零的状态,而是维持一种能为社会所接受的低而稳定的通货膨胀率的经济状态,一般指通货膨胀率为百分之十以下。物价稳定可以防止经济的剧烈波动,防止各种扭曲对经济造成负面影响。 (3)经济增长是指保持合意的经济增长率。经济增长是指单纯的生产增长,经济增长率并不是越高越好,经济增长的同时必须带来经济发展;经济增长率一般是用实际国民生产总值的年平均增长率来衡量的。只有经济不断的增长,才能满足人类无限的欲望。 (4)国际收支平衡是指国际收支既无赤字又无盈余的状态。国际收支平衡是一国对外经济目标,必须注意和国内目标的配合使用;正确处理国内目标与国际目标的矛盾。在开放经济下,一国与他国来往日益密切,保持国际收支的基本平衡,才能使一国避免受到他国经济波动带来的负面影响。 3,题略 答:a.石油价格大幅度上涨,作为一种不利的供给冲击,将会使增加企业的生产成本,从而使总供给减少,总供给曲线AS将向左上方移动。 b.一项削减国防开支的裁军协议,而与此同时,政府没有采取减税或者增加政府支出的政策,则将减少一国的总需求水平,从而使总需求曲线AD向左下方移动。 c.潜在产出水平的增加,将有效提高一国所能生产出的商品和劳务水平,从而使总供给曲线AS向右下方移动。 d.放松银根使得利率降低,这将有效刺激经济中的投资需求等,从而使总需求增加,总需求曲线AD向右上方移动。 第五章 基本概念:GDP,名义GDP,实际GDP,NDP,DI,CPI,PPI。 思考题: 5.为什么下列各项不被计入美国的GDP之中? a优秀的厨师在自己家里烹制膳食; b购买一块土地; c购买一幅伦勃朗的绘画真品; d某人在2009年播放一张2005年录制的CD所获得的价值; e电力公司排放的污染物对房屋和庄稼的损害;
初三化学溶解度曲线知识点(完整)知识讲解
初三化学溶解度曲线知识点(完整)
溶解度t/℃ 21m m 溶解度曲线知识点 一、正确理解溶解度曲线的含义 溶解度曲线就是在直角坐标系中,用来描述物质的溶解度随温度变化而变化的曲线。根据溶解度曲线可进行溶液的配制,混合物的分离与提纯,以及进行物质结晶或溶解的计算。下面,我们从溶解度曲线的特点入手,对溶解度作进一步的理解。 (一)点 1.曲线上的点:表示对应温度下该物质的溶解度。如:下图中a 表示A 物质在t 1℃时溶解度为m 1g 。 2.曲线上方的点:表示在对应温度下该物质的饱和溶液中存在不能继续溶解的溶质。如:图中b 表示在t 1℃时,A 的饱和溶液中有(m 2-m 1)g 未溶解的溶质。
3.曲线下方的点:表示在对应温度下该物质的不饱和溶液。如:图中C 表示在t 1℃时,A 的不饱和溶液中,还需要加入(m 1-m 3)g A 物质才达到饱和。 4.曲线交点:表示在对应温度下不同物质的溶解度相同。如图中d 表示在t 2℃,A 、B 两物质的溶解度都为m 4g 。 (二)线 如图中A 物质的溶解度随温度升高而明显增大,A 曲线为“陡升型”。如KNO 3等大多数固体物质。 图中B 物质的溶解度随温度变化不大,B 曲线为“缓升型”,如NaCl 等少数固体物质。 图中C 物质的溶解度随温度升高而减小,C 曲线为“下降型”,如气体及Ca(OH)2等极少数固体物质。 二、掌握溶解度曲线的应用 溶解度
1.溶解度曲线上的每一点,代表着某温度下某物质的溶解度,因此利用溶解度曲线可以查出某物质在不同温度下的溶解度,并根据物质的溶解度判断其溶解性。 2.可以比较在同一温度下不同物质溶解度的相对大小。 3.根据溶解度曲线的形状走向,可以看出某物质的溶解度随温度的变化情况。并根据此情况可以确定从饱和溶液中析出晶体或进行混合物分离提纯的方法。例如:某物质的溶解度曲线“陡”,表明该物质溶解度随温度变化明显,提纯或分离该物质时适合采用降温结晶法。某物质溶解度曲线“平缓”,提纯或分离该物质时适合采用蒸发溶剂法。 4.从溶解度曲线上的交点,可以判断哪些物质在该点所示的温度下具有相同的溶解度。 5.利用溶解度曲线可以确定一定质量的某物质的饱和溶液降温时析出晶体的质量。
溶解度(习题及答案)
溶解度(习题) 1.有关饱和溶液与不饱和溶液的叙述正确的是() A.饱和溶液不能再溶解任何物质 B.饱和溶液降温析出晶体后一定是饱和溶液 C.在一定温度下,稀溶液一定是不饱和溶液 D.饱和溶液与不饱和溶液之间不能相互转化 2.能证明20℃时的A溶液为饱和溶液的方法是() A.蒸干后得到溶质 A B.降 温到 0℃,有溶质 A 析出 C.加入少量溶质 A,振荡后不溶解 D.与同一温度下的 A 的饱和溶液混合,无明显现象 3.t℃时,向盛有 0.1 g 硝酸钾的试管中加入 10 g 水,充分振荡后 ,静置,试管底部仍有未溶解的晶体,下列对试管内上层清液的叙述正确的是() A.为t℃时的饱和溶液 B.为t℃时的不饱和溶液 C.溶质的质量为 0.1 g D. 不确定是否为饱和溶液 4.室温时,将100 g 氯化钠饱和溶液(无未溶解的晶体)平分 成甲、乙两份,然后向甲溶液中加入50 g 水,搅拌均匀后形成丙溶液,下列说法正确的是() A.甲、乙均为不饱和溶液 B.甲、乙均为饱和溶液 C.甲 、乙、丙均为不饱和溶液D.甲 、乙、丙均为饱和溶液 5.20℃时,将36 g NaCl 完全溶解在100 g 水中恰好形成饱和溶 液。下列叙述正确的是() A.20℃时,NaCl 的溶解度为 36 B.向该溶液中再加入 2 g NaCl,溶液质量为 138 g C.向该溶液中加入 10 g 水,溶液变成不饱和溶液 D.该溶液中溶质的质量分数为 36%
6.下表是 KCl 的部分溶解度数据,回答下列问题。 温度/℃0 20 40 60 溶解度/g 27.6 34.0 40.0 45.5 的溶解度为。 (2)40℃时,将50 g KCl 固体加入100 g 水中,所形成的溶液为(填“饱和”或“不饱和”)溶液, 溶液的质量为。 (3)60℃时,145.5 g KCl 饱和溶液降温至40℃,析出晶体的质量为。 7.如图是甲、乙两种物质的溶解度曲线,回答下列问题。 (1)20℃时,甲、乙两物质的溶解度大小关系为:甲 乙(填“>”、“<”或“=”)。 (2)20℃时,甲物质的饱和溶液中,溶质和溶剂的质量比为。 (3)将乙物质的不饱和溶液变为饱和溶液,可采用的方法是(写一种即可)。 8.如图是 A、B 两种物质的溶解度曲线,回答下列问题。 (1)t1℃时,将25 g A 加入到一定量水中制成饱和溶液,所得溶液的溶质质量分数为。 (2)t2℃时,A、B 两物质的饱和溶液中溶质质量分数大小关系为:A B(填“>”、“<”或“=”)。 (3)若将 A 物质从溶液中析出,采用的方法是________。
溶液 溶解度知识点总结
溶液溶解度知识点总结 一、溶液选择题 1.下表是NaCl、KNO3在不同温度时的溶解度: 温度/℃102030405060 NaCl35.836.036.336.637.037.3 溶解度/g KNO320.931.645.863.985.5110 据此数据,判断下列说法错误的是 A.KNO3和NaCl的溶解度曲线在20℃—30℃温度范围内会相交 B.在60℃时,KNO3的饱和溶液105g加入95g水后,溶液中溶质的质量分数为27.5%C.在20℃时,NaCl和KNO3固体各35g分别加入两只各盛有100g水的烧杯中,均不能形成饱和溶液 D.从含有少量NaCl的KNO3饱和溶液中得到较多的KNO3晶体,通常可采用冷却热饱和溶液的方法 【答案】C 【解析】 A、根据表格提供的数据可以发现,在20℃~30℃温度范围内硝酸钾和氯化钠存在溶解度相同的数值,KNO3和NaCl的溶解度曲线在20℃~30℃温度范围内会相交,错误; B、在60℃时,硝酸钾的溶解度为110g,则105g的KNO3饱和溶液,含有硝酸钾55g,加入95g 水后,溶液中溶质的质量分数=×100%=27.5%,错误;C、在20℃时,氯化钠的溶解度为36g,硝酸钾的溶解度为31.6g,NaCl 和KNO3固体各35g分别加入两只各盛有100g 水的烧杯中,氯化钠不能形成饱和溶液,硝酸钾形成饱和溶液,正确;D、硝酸钾的溶解度随温度的升高而变化很大,含有少量NaCl的KNO3饱和溶液中得到较多的KNO3晶体,通常采用冷却热的饱和溶液的方法,错误。故选C。 点睛:掌握溶解度随温度变化的特点以及饱和溶液中结晶析出晶体的方法是正确解答本题的关键。 2.实验室用KClO3制氧气并回收MnO2和KCl,下列操作不规范的是( ) A.用装置甲收集氧气 B.用装置乙溶解完全反应后的固体
(完整版)思考题及习题2参考答案
第2章思考题及习题2参考答案 一、填空 1. 在AT89S51单片机中,如果采用6MHz晶振,一个机器周期为。答:2μs 2. AT89S51单片机的机器周期等于个时钟振荡周期。答:12 3. 内部RAM中,位地址为40H、88H的位,该位所在字节的字节地址分别为 和。答:28H,88H 4. 片内字节地址为2AH单元最低位的位地址是;片内字节地址为A8H单元的最低位的位地址为。答:50H,A8H 5. 若A中的内容为63H,那么,P标志位的值为。答:0 6. AT89S51单片机复位后,R4所对应的存储单元的地址为,因上电时PSW= 。这时当前的工作寄存器区是组工作寄存器区。答:04H,00H,0。 7. 内部RAM中,可作为工作寄存器区的单元地址为 H~ H。答:00H,1FH 8. 通过堆栈操作实现子程序调用时,首先要把的内容入栈,以进行断点保护。调用子程序返回指令时,再进行出栈保护,把保护的断点送回到,先弹出的是原来中的内容。答:PC, PC,PCH 9. AT89S51单片机程序存储器的寻址范围是由程序计数器PC的位数所决定的,因为AT89S51单片机的PC是16位的,因此其寻址的范围为 KB。答:64 10. AT89S51单片机复位时,P0~P3口的各引脚为电平。答:高 11. AT89S51单片机使用片外振荡器作为时钟信号时,引脚XTAL1接,引脚XTAL2的接法是。答:片外振荡器的输出信号,悬空 12. AT89S51单片机复位时,堆栈指针SP中的内容为,程序指针PC中的内容为 。答:07H,0000H 二、单选 1. 程序在运行中,当前PC的值是。 A.当前正在执行指令的前一条指令的地址 B.当前正在执行指令的地址。 C.当前正在执行指令的下一条指令的首地址 D.控制器中指令寄存器的地址。 答:C 2. 判断下列哪一种说法是正确的?
溶液及溶解度学习知识点情况总结
中考化学溶液知识点总结 【考点1】溶液的概念和基本特征 一、溶液的概念 1.溶液:一种或几种物质分散到另一种物质里,形成均一的、稳定的混合物,叫做溶液。 2.溶液的组成:溶液是混合物,由溶质和溶剂组成。溶液的质量=溶质的质量+溶剂的质量;溶液的体积≠溶质体积+溶剂体积 溶质:被溶解的物质。可以是固体、液体或气体。一种溶液中的溶质可以是一种或多种物质。 溶剂:能溶解其他物质的物质。水是最常见的溶剂。汽油、酒精也可以作为溶剂。 二、溶液的基本特征 ①均一性:指溶液形成以后,溶液各部分的组成、性质完全相同。如溶液中部分的浓度、密度和颜色完全一样。 ②稳定性:外界条件不变是溶液长期放置,溶质不会从溶液中分离出来。 ③是混合物。 【规律】溶液的判别 (1)澄清透明不代表是无色的。 (2)均一稳定的液体不一定是溶液,如水。 【举例】硬水、空气、纯净水属于溶液;泥水,油水,蒸馏水不是溶液。 【技巧】溶质、溶剂的判定 ①通常不指明溶剂的溶液,一般是水溶液。 ②当固体、气体溶于液体时,固体、气体做溶剂,液体做溶剂。 ③当两种液体互相溶解时,量多的叫做溶剂,量少的叫做溶质。 ④当物质溶解发生化学变化时,一定要正确判断溶质。 ⑤溶质和溶剂是溶液所特有的概念,悬浊液和乳浊液不存在溶质和溶剂。 ⑥溶质质量是指溶液中已溶解溶质的质量。
影响物质溶解能力的因素: 1、相似相容,溶质和溶剂的性质相似,溶解能力越强。如:氯化钠易溶于水,难溶于油,碘易溶于汽油,那溶于水。 1、大部分物质稳定越高,溶解能力越强。 对于气体,压强越大溶解能力越强。 【考点2】溶液和浊液 1、浊液:包括乳浊液和悬浊液。 2、乳浊液:小液滴分散到液体里形成不均一的、不稳定的混合物叫乳浊液。 悬浊液:固体颗粒分散到液体里形成不均一的、不稳定的混合物叫悬浊液。 3、溶液和浊液的区别
溶解度专项练习题
溶解度练习题 1.下列说法正确的是() A.凡是均一的、稳定的液体都是溶液B.溶液都是无色透明的 C.可用水区分NaOH固体和NH4NO3固体D.面粉溶于水形成溶液 2.下列关于溶液的说法正确的是() A.一种溶液中只能有一种溶质B.澄清透明的液体就是溶液 C.溶液的各部分性质均相同D.溶液都具有导电性 3.下列关于溶液的说法正确的是() A.饱和溶液析出晶体后就变成不饱和溶液B.溶液中的溶质可以是一种或多种C.溶液上层的密度小,下层的密度大D.溶液一定是无色透明的 4.将下列固体分别溶解于水中,温度明显降低的是() A.硝酸铵B.氢氧化钠C.蔗糖D.氯化钠 5.已知在20℃时,氯化钠的溶解度为36g。在此温度下,20g水中最多能溶解氯化钠的质量为() A.36g B.C.D.10g 6.把一定质量的30%的某溶液加热蒸发10g水,冷却至20℃时有2g晶体析出,此时溶液的溶质质量分数为40%,则该物质在20℃是的溶解度是() A.20g B.C.40g D. 7.在4℃时,将100mL密度为cm3,溶质的质量分数为98%的浓硫酸与100mL的水均匀混合,待温度恢复到4℃时,下列关于混合后的溶液叙述正确的是() A.密度为cm3 B.溶质质量分数为% C.体积为200mL D.溶液的质量为280g 8.根据实验操作所绘制的图像中,正确的是() ①②③④ A.图①是高温煅烧石灰石,固体剩余物的质量与产生气体的质量关系 B.图②是向一定质量的水中不断加入蔗糖,加入固体质量与形成溶液质量的关系 C.图③是向等质量、等质量分数的稀硫酸中分别加入过量的金属镁与铝,加入金属质量与产生氢气质量的关系 D.图④是向一定质量铁粉中加入硫酸铜溶液,加入硫酸铜溶液与形成溶液总质量的9.下列图像与实验相符合的是() 固 体 质 量 /g 溶 液 质 量 /g 氢 气 质 量 /g Mg Al 溶 液 质 量 /g
初三化学溶解度知识点
《溶液》知识点 一、溶液的形成 二、溶解度 1、固体的溶解度 (1)溶解度定义:在一定温度下,某固态物质在100g溶剂里达到饱和状态时所溶解的质量 四要素:①条件:一定温度②标准:100g溶剂③状态:达到饱和④质量:单位:克 (2)溶解度的含义: 20℃时NaCl的溶液度为36g含义: 在20℃时,在100克水中最多能溶解36克NaCl 或在20℃时,NaCl在100克水中达到饱和状态时所溶解的质量为36克 (3)影响固体溶解度的因素:①溶质、溶剂的性质(种类)②温度 大多数固体物的溶解度随温度升高而升高;如KNO 3 少数固体物质的溶解度受温度的影响很小;如NaCl 极少数物质溶解度随温度升高而降低。如Ca(OH) 2 (4)溶解度曲线 ℃时A的溶解度为 80g 例:(1)t 3 (2)P点的含义在该温度时,A和C的溶解度 相同 (3)N点为 t ℃时A的不饱和溶液,可通过加 3 入A物质,降温,蒸发溶剂的方法使它变为饱和 (4)t ℃时A、B、C、溶解度由大到小的顺序C>B>A 1
(5)从A溶液中获取A晶体可用降温结晶的方法获取晶体。(6)从B的溶液中获取晶体,适宜采用蒸发结晶的方法获取晶体。 (7)t 2℃时A、B、C的饱和溶液各W克,降温到t 1 ℃ 会析出晶体的有A和B 无晶体析出 的有 C,所得溶液中溶质的质量分数由小到大依次为 A 思考题与习题 1 1- 1 回答以下问题: ( 1)半导体材料具有哪些主要特性? (2) 分析杂质半导体中多数载流子和少数载流子的来源; (3) P 型半导体中空穴的数量远多于自由电子, N 型半 导体中自由电子的数量远多于空穴, 为什么它们对外却都呈电中性? (4) 已知温度为15C 时,PN 结的反向饱和电流 I s 10 A 。当温度为35 C 时,该PN 结 的反向饱和 电流I s 大约为多大? ( 5)试比较二极管在 Q 点处直流电阻和交流电阻的大小。 解: ( 1)半导体的导电能力会随着温度、光照的变化或掺入杂质浓度的多少而发生显着改变, 即半导体具 有热敏特性、光敏特性和掺杂特性。 ( 2)杂质半导体中的多数载流子是由杂质原子提供的,例如 供一个自由电子,P 型半导体中一个杂质原子提供一个空穴, 浓度;少数载流子则是由热激发产生的。 (3) 尽管P 型半导体中空穴浓度远大于自由电子浓度,但 P 型半导体中,掺杂的杂质原子因获得一个价电子而变成带负电的杂 质离子(但不能移动),价 电子离开后的空位变成了空穴,两者的电量相互抵消,杂质半导体从总体上来说仍是电中性的。 同理, N 型半导体中虽然自由电子浓度远大于空穴浓度,但 N 型半导体也是电中性的。 (4) 由于温度每升高10 C ,PN 结的反向饱和电流约增大 1倍,因此温度为 35C 时,反向 饱和电流为 (5) 二极管在 Q 点处的直流电阻为 交流电阻为 式中U D 为二极管两端的直流电压, U D U on ,I D 为二极管上流过的直流电流, U T 为温度的 电压当量,常温下 U T 26mV ,可见 r d R D 。 1- 2 理想二极管组成的电路如题 1- 2图所示。试判断图中二极管是导通还是截止,并确定 各电路的输 出电压。 解 理想二极管导通时的正向压降为零, 截止时的反向电流为零。 本题应首先判断二极管的工 作状 态,再进一步求解输出电压。二极管工作状态的一般判断方法是:断开二极管, 求解其端口 电压;若该电压使二极管正偏, 则导通; 若反偏, 则截止。 当电路中有两只或两只以上二极管时, 可分别应用该方法判断每只二极管的工作状态。 需要注意的是, 当多只二极管的阳极相连 (共阳 极接法)时,阴极电位最低的管子将优先导通;同理,当多只二极管的阴极相连(共阴极接法) 时,阳极电位最高的管子将优先导通。 (a) 断开二极管 D ,阳极电位为12V ,阴极电位为6V ,故导通。输岀电压 U O 12V 。 (b) 断开二极管 D 1、D 2, D 1、D 2为共阴极接法,其阴极电位均为 6V ,而D 1的阳极电位 为9V , D 2的阳极电位为5V ,故D 1优先导通,将 D 2的阴极电位钳制在 7.5V ,D 2因反向偏置而 截止。输岀电压 U O 7.5V 。 N 型半导体中一个杂质原子提 因此 多子浓度约等于所掺入的杂质 P 型半导体本身不带电。因为在 溶解度练习题 1、右图为A、B两种固体物质的溶解度曲线。 (1)在℃时,A、B两种物质的溶解度相等。 (2)t 2 ℃时,100g水中溶解 gA物质恰好饱和,该饱和溶液中溶质的质量分数为。若要把该饱和溶液稀释成质量分数为1 0%的溶液,应加 水 g。 (3)t 2℃时,分别将恰好饱和的A、B两种物质的溶液降温至t 1 ℃,溶质的质量分 数保持不变的是。 2.右图是甲、乙两物质的溶解度曲线图,下列说法正确的是 A.t1℃时,甲、乙两物质的溶解度相等 B.温度对甲、乙两物质的溶解度影响相同 C.把t1℃时甲、乙两饱和溶液升温至t2℃时,两溶液仍都为 饱和溶液 D.把t2℃时甲、乙两饱和溶液降温至t1℃时,两溶液都析 出溶质 3.右图表示的是甲、乙两种固体物质的溶解度曲线,下列 叙述一定正确的是 A.甲的溶解度大于乙的溶解度 B.10℃时甲、乙两溶液的质量分数相等 C.30℃时甲的饱和溶液的质量分数为60% D.降低温度可使接近饱和的甲溶液变成饱和溶液 4.右图是A.B两种固体物质的溶解度曲线。请回答下列问题: (1)P点的意义是。 (2)t 2 ℃时,将60g A物质放入100g水中,充分搅拌,所得溶液的质量 是 g。 (3)将接近饱和的A物质的水溶液,变成饱和溶液的方法 有(答出一种即可)。 5、(3分)右图是a、b、c三种物质的溶解度曲线,a与c的溶解度曲线相交于P点。据图回答: (1)P点的含义 是 (2)t 1 ℃时30g a物质加入到50g水中不断搅拌,能 形成80g溶液吗?(填“能”或“不能”)。 (3)t 2 ℃时,a、b、c三种物质的溶解度按由小到大的顺序排列的 是(填物质序号)。 6、(3分)向装有等量水的A、B、C烧杯中分别加入10g、25g、25gNaNO 3 固体,充分溶解后,现象如图一所示。 (1)烧杯中的溶液一定属于饱和溶液的是(填序号); (2)图二能表示NaNO 3 溶解度曲线的是(填“甲”或“乙”); (3)由图二分析,若分别将100g甲、乙的饱和溶液从t 2℃降温到t 1 ℃,对所得 溶液的叙述正确的(填序号)。 A.甲、乙都是饱和溶液 B.所含溶剂质量:甲<乙 \ 1 / 第2讲溶解度应用及溶质质量分数 溶液的溶解度 1、 固体溶解度:在一定温度下,某固体物质在100g 溶剂里达到饱和状态时所溶解的质量。(符号 为S ,单位为g )。 溶解度含义:“20℃时NaCl 的溶解度为36g”的含义:在20℃时,NaCl 在100g 水中达到饱和状态时所溶解的质量为36g 。 2、四要素: ?温度——必须指明具体的温度,溶解度才有意义。?溶剂的质量是100g 。 ?固体溶解在溶剂中,必须达到饱和状态。? 溶解度的单位通常是g 。 3、影响固体溶解度的因素:(内因)溶质性质、溶剂性质;(外因)温度。 4、溶解度与溶解性 在20℃下,溶解度小于0.01g ,被称为难溶(或不溶);溶解度介于0.01~1g 之间,被称为微溶;溶解度介于1~10g 之间,被称为可溶;溶解度大于10g ,被称为易溶。 5、溶解度曲线的常见试题(右图) ?t 3℃时A 的溶解度为 80g 。 ?P 点的的含义是: 在t 2℃时,A 和C 的溶解度相同 。? N 点为 t 3℃时A 的不饱和溶液 ,可通过加入A 物质,降温或者蒸发溶剂的方法使它变为饱和。 曲线上的点代表对应温度的饱和溶液,曲线以下的点代表该物质对应温度的不饱和溶液。 加溶质相当于把点向正上方移动(但是点不能被移动到图线上方),加溶剂相当于向下竖直移动,降温相当于向左水平移动,升温相当于向右水平移动。 ?t 1℃时A 、B 、C 溶解度由大到小的顺序 B >C > A 。?从A 溶液中获取A 晶体可用 降温结晶 的方法获取晶体。 ?从B 的溶液中获取晶体,适宜采用 蒸发结晶 (冷却热饱和溶液)的方法获取晶体。? t 2℃ 时A 、B 、C 的饱和溶液各W 克,降温到t 1℃会析出晶体的有 A 和B ,无晶体析出的有 C ,所得溶液中溶质的质量分数由小到大依次为 A <C <B 。? 除去A 中的泥沙用 过滤 法;A 中混有少量的B ,提纯A 用降温结晶(冷却热饱和溶液);B 中混有少量的A ,提纯B 用蒸发结晶。 80 · · t 2 3N t /℃ S/g P A B C 难溶 管理学思考题及参考答案 第一章 1、什么是管理? 管理:协调工作活动过程(即职能),以便能够有效率和有效果地同别人一起或通过别人实现组织的目标。 2、效率与效果 效率:正确地做事(如何做) 效果:做正确的事(该不该做) 3、管理者三层次 高层管理者、中层管理者、基层管理者 4、管理职能和(或)过程——职能论 计划、组织、控制、领导 5、管理角色——角色论 人际角色:挂名首脑、领导人、联络人 信息角色:监督者、传播者、发言人 决策角色:企业家、混乱驾驭者、资源分配者、谈判者 6、管理技能——技能论 用图表达。 高层管理概念技能最重要,中层管理3种技能都需要且较平衡,基层管理技术技能最重要。 7、组织三特征? 明确的目的 精细的结构 合适的人员 第二章 泰罗的三大实验: 泰罗是科学管理之父。记住3个实验的名称:1、搬运生铁实验,2、铁锹实验,3、高速钢实验 4、吉尔布雷斯夫妇 动作研究之父 管理界中的居里夫妇 5、法约尔的十四原则 法约尔是管理过程理论之父 记住“十四原则”这个名称就可以了。 6、法约尔的“跳板” 图。 7、韦伯理想的官僚行政组织组织理论之父。6维度:劳动分工、权威等级、正式甄选、非个人的、正式规则、职业生涯导向。 8、韦伯的3种权力 超凡的权力 传统的权力 法定的权力。 9、巴纳德的协作系统论 协作意愿 共同目标 信息沟通 10、罗伯特·欧文的人事管理 人事管理之父。职业经理人的先驱 11、福莱特冲突论 管理理论之母 1)利益结合、 2)一方自愿退让、 3)斗争、战胜另一方 4)妥协。 12、霍桑试验 1924-1932年、梅奥 照明试验、继电器试验、大规模访谈、接线试验 13、朱兰的质量观 质量是一种合用性 14、80/20的法则 多数,它们只能造成少许的影响;少数,它们造成主要的、重大的影响。 15、五项修炼 自我超越 改善心智 共同愿景 团队学习 系统思考 第三章 1、管理万能论 管理者对组织的成败负有直接责任。 2、管理象征论 是外部力量,而不是管理,决定成果。 3、何为组织文化 组织成员共有的价值观和信念体系。这一体系在很大程度上决定成员的行为方式。 4、组织文化七维度 溶解度曲线中考试题解析 【知识点的认识】 所谓固体溶解度曲线如图所示: 就是用纵坐标表示溶解度(用字母S表示,单位为克/g),横坐标表示温度(用字母t表示,单位为℃),根据物质在不同温度时的溶解度不同,画出的物质溶解度随温度变化的曲线。固体溶解度曲线的作用可从点、线、面和交点四方面来理解。具体如下: 1.点,溶解度曲线上的每个点(即饱和点)表示的是某温度下某种物质的溶解度。即曲线上的任意一点都对应有相应的温度和溶解度。温度在横坐标上可以找到,溶解度在纵坐标上可以找到。溶解度曲线上的点有三个方面的作用: (1)根据已知的温度可以查出有关物质的溶解度; (2)根据物质的溶解度也可以查出它所对应的温度; (3)可以判断或比较相同温度下,不同物质溶解度的大小(或饱和 溶液中溶质的质量分数的大小)。 2.线,溶解度曲线表示某物质在不同温度下的溶解度或溶解度随温度的变化情况。曲线的坡度越大,说明溶解度受温度影响越大;反之,说明受温度影响较小。溶解度曲线也有三个方面的应用: (1)根据溶解度曲线,可以看出物质的溶解度随着温度的变化而变化的情况。一般规律是:大部分固体随温度升高溶解度增大,如硝酸钾;只有少数固体溶解度受温度影响不大,如食盐(氯化钠);极少数物质溶解度随温度升高反而减小,如熟石灰。 (2)根据溶解度曲线,判断或比较某一物质在不同温度下的溶解度大小。 (3)根据溶解度曲线,选择分离、提纯某些可溶性混合物的方法(即选用蒸发结晶还是降温结晶);并且,还可以判断或比较析出晶体的质量大小(即曲线越陡,析出的晶体就越多)。 3.面,对于曲线下部面积上的任何点,依其数据配制的溶液为对应温度时的不饱和溶液;曲线上部面积上的点,依其数据配制的溶液为对应温度时的饱和溶液,且溶质有剩余。如果要使不饱和溶液(曲线下部的一点)变成对应温度下的饱和溶液,方法有两种:第一种方法是向该溶液中添加适量的溶质使之到达曲线上;第二种方法是蒸发掉过量的溶剂。 3.交点,两条溶解度曲线的交点表示该点所示的温度下,两物质的溶解度是相同的;并且,此时两种物质饱和溶液的溶质质量分数也相同的。 【命题方向】 溶液溶解度练习题经典 一、溶液选择题 1.甲、乙、丙三种固体物质的溶解度曲线如图所示,下列叙述正确的是() A.t1℃时将等质量的乙、丙溶于水中,分别配成饱和溶液,所得溶液质量:乙=丙 B.将t1℃时甲、丙的饱和溶液升温到t2℃,两种溶液中溶质的质量分数相等 C.要将接近饱和的丙溶液变为饱和溶液,可以采用降温或蒸发的方法 D.t3℃时,将三种物质的饱和溶液恒温蒸发等量水后,析出溶质的质量顺序:甲>丙>乙【答案】A 【解析】A、t1℃时,乙的溶解度等于甲,将等质量的甲、乙分别配成饱和溶液,所需要的水的质量相等,故所得溶液质量甲=乙,故正确; B、将t1℃时甲、丙的饱和溶液升温到t2℃,甲的溶解度随温度的升高而增大,故溶液组成不变,而丙的溶解度随温度的升高而减小,会析出晶体,溶质质量分数会减小,但t2℃是丙的溶解度大于t1℃时甲的溶解度,故两种溶液中溶质的质量分数丙大于甲,故错误; C、由溶解度曲线可知,丙的溶解度随着温度的降低而增大,因此要将接近饱和的丙溶液变为饱和溶液,可以采用升温或蒸发的方法,故正确; D、t3℃时三种物质的溶解度关系为甲>乙>丙,将t3℃时三种物质的饱和溶液恒温蒸发等量水后,析出溶质的质量甲>乙>丙,故错误。 点睛: 根据固体的溶解度曲线可以:①查出某物质在一定温度下的溶解度,从而确定物质的溶解性,②比较不同物质在同一温度下的溶解度大小,从而判断饱和溶液中溶质的质量分数的大小,③判断物质的溶解度随温度变化的变化情况,从而判断通过降温结晶还是蒸发结晶的方法达到提纯物质的目的。 2.如图是甲、乙、丙三种固体物质的溶解度曲线,下列说法错误的是() A.t2℃时,甲、乙两种物质的溶解度相等 B.甲的溶解度随温度的升高而增大 C.分别将t3℃时甲、乙、丙的饱和溶液降温至t1℃,则所得的三种溶液中溶质的质量分数 溶解度 1、固体的溶解度 (1)溶解度的定义:在一定温度下,某固态物质在100g溶剂里达到饱和状态时所溶解的质量 四要素:①条件:一定温度②标准:100g溶剂③状态:达到饱和④质量:溶解度的单位:克 (2)溶解度的含义:20℃时NaCl的溶液度为36g含义: 在20℃时,在100克水中最多能溶解36克NaCl 或在20℃时,NaCl在100克水中达到饱和状态时所溶解的质量为36克 (3)影响固体溶解度的因素:①溶质、溶剂的性质(种类)②温度 大多数固体物的溶解度随温度升高而升高;如KNO3 少数固体物质的溶解度受温度的影响很小;如NaCl 极少数物质溶解度随温度升高而降低。如Ca(OH)2 例: (4)溶解度曲线 (1)t3℃时A的溶解度为80g (2)P点的的含义在该温度时,A和C的溶解度相同 (3)N点为t3℃时A的不饱和溶液,可通过加入A 物质,降温,蒸发溶剂的方法使它变为饱和 (4)t1℃时A、B、C、溶解度由大到小的顺序C>B>A (5)从A溶液中获取A晶体可用降温结晶的方法获取 晶体。 (6)从B的溶液中获取晶体,适宜采用蒸发结晶的方法获取晶体 (7)t2℃时A、B、C的饱和溶液各W克,降温到t1℃会析出晶体的有A和B 无晶体析出的有 C (8)除去A中的泥沙用过滤法;分离A与B(含量少)的混合物,用结晶法 2、气体的溶解度 (1)气体溶解度的定义:在压强为101kPa和一定温度时,气体溶解在1体积水里达到 饱和状态时的气体体积。 (2)影响因素:①气体的性质②温度(温度越高,气体溶解度越小) ③压强(压强越大,气体溶解度越大) 3、混合物的分离 (1)过滤法:分离可溶物+ 难溶物 (2)结晶法:分离几种可溶性物质 结晶的两种方法蒸发溶剂,如NaCl(海水晒盐) 降低温度(冷却热的饱和溶液,如KNO3) 蒸发结晶(蒸发溶剂法):将固体溶质的溶液加热(或日晒,或在风力的作用下)使溶剂蒸发,使溶液由不饱和溶液转化为饱和溶液,再继续蒸发溶剂,使溶质从溶液中析出。适用范围:溶解度受温度变化影响不大的物质,如氯化钠。 降温结晶(冷却热饱和溶液法):冷却热的饱和溶液,使溶质从溶液中结晶析出。适用范围:溶解度受温度变化影响较大的物质,如氯酸钾。 第一章思考题及参考答案 1. 无多余约束几何不变体系简单组成规则间有何关系? 答:最基本的三角形规则,其间关系可用下图说明: 图a 为三刚片三铰不共线情况。图b 为III 刚片改成链杆,两刚片一铰一杆不共线情况。图c 为I 、II 刚片间的铰改成两链杆(虚铰),两刚片三杆不全部平行、不交于一点的情况。图d 为三个实铰均改成两链杆(虚铰),变成三刚片每两刚片间用一虚铰相连、三虚铰不共线的情况。图e 为将I 、III 看成二元体,减二元体所成的情况。 2.实铰与虚铰有何差别? 答:从瞬间转动效应来说,实铰和虚铰是一样的。但是实铰的转动中心是不变的,而虚铰转动中心为瞬间的链杆交点,产生转动后瞬时转动中心是要变化的,也即“铰”的位置实铰不变,虚铰要发生变化。 3.试举例说明瞬变体系不能作为结构的原因。接近瞬变的体系是否可作为结构? 答:如图所示AC 、CB 与大地三刚片由A 、B 、C 三铰彼此相连,因为三铰共线,体系瞬变。设该 体系受图示荷载P F 作用,体系C 点发生微小位移 δ,AC 、CB 分别转过微小角度α和β。微小位移 后三铰不再共线变成几何不变体系,在变形后的位置体系能平衡外荷P F ,取隔离体如图所 示,则列投影平衡方程可得 210 cos cos 0x F T T βα=?=∑,21P 0 sin sin y F T T F βα=+=∑ 由于位移δ非常小,因此cos cos 1βα≈≈,sin , sin ββαα≈≈,将此代入上式可得 21T T T ≈=,()P P F T F T βαβα +==?∞+, 由此可见,瞬变体系受荷作用后将产生巨大的内力,没有材料可以经受巨大内力而不破坏,因而瞬变体系不能作为结构。由上分析可见,虽三铰不共线,但当体系接近瞬变时,一样将产生巨大内力,因此也不能作为结构使用。 4.平面体系几何组成特征与其静力特征间关系如何? 答:无多余约束几何不变体系?静定结构(仅用平衡条件就能分析受力) 有多余约束几何不变体系?超静定结构(仅用平衡条件不能全部解决受力分析) 瞬变体系?受小的外力作用,瞬时可导致某些杆无穷大的内力 常变体系?除特定外力作用外,不能平衡 5. 系计算自由度有何作用? 答:当W >0时,可确定体系一定可变;当W <0且不可变时,可确定第4章超静定次数;W =0又不能用简单规则分析时,可用第2章零载法分析体系可变性。 6.作平面体系组成分析的基本思路、步骤如何? 答:分析的基本思路是先设法化简,找刚片看能用什么规则分析。 溶解度/g t/℃ 21m m m m 溶解度曲线知识点 一、正确理解溶解度曲线的涵义 溶解度曲线就是在直角坐标系中,用来描述物质的溶解度随温度变化而变化的曲线。根据溶解度曲线可进行溶液的配制,混合物的分离与提纯,以及进行物质结晶或溶解的计算。 点 ① 曲线上的点:表示对应温度下该物质的溶解度。如:下图中a 表示 A 物质在t 1℃时溶解度为m 1g 。 曲线上方的点:表示在对应温度下该物质的饱和溶液中存在 不能继续溶解的溶质。如:图中b 表示在t 1℃时,A 的饱和溶液中有 (m 2-m 1)g 未溶解的溶质。 曲线下方的点:表示在对应温度下该物质的不饱和溶液。如: 图中C 表示在t 1℃时,A 的不饱和溶液中,还需要加入(m 1-m 3)gA 物质才达到饱和。 ②曲线交点:表示在对应温度下不同物质的溶解度相同。如图中d 表示在t 2℃,A 、B 两物质的溶解度都为m 4g 。 2、线 如图中A 物质的溶解度随温度升高而明显增大,A 曲线为“陡升型”。 如KNO 3等大多数固体物质: 图中B 物质的溶解度随温度变化不大,B 曲线为“缓升型”, 如NaCl 等少数固体物质。 图中C 物质的溶解度随温度升高而减小,C 曲线为“下降型”,如气体及Ca(OH)2等极少数固体物质。 二、掌握溶解度曲线的应用 1. 溶解度曲线上的每一点,代表着某温度下某物质的溶解度,因此利用溶解度曲线可以查出某物质在不同温度下的溶解度,并根据物质的溶解度判断其溶解性。 2. 可以比较在同一温度下不同物质溶解度的相对大小。 3. 根据溶解度曲线的形状走向,可以看出某物质的溶解度随温度的变化情况。并根据此情况可以确定从饱和溶液中析出晶体或进行混合物分离提纯的方法。例如:某物质的溶解度曲线“陡”,表明该物质溶解度随温度变化明显,提纯或分离该物质时适合采用降温结晶法。某物质溶解度曲线“平缓”,提纯或分离该物质时适合采用蒸发溶剂法。 4. 从溶解度曲线上的交点,可以判断哪些物质在该点所示的温度下具有相同的溶解度。 5. 利用溶解度曲线可以确定一定质量的某物质的饱和溶液降温时析出晶体的质量。 溶解度曲线专题练习 1. 甲、乙两物质的溶解度曲线如图所示,下列说法正确的是 溶解度/g 度 最新溶液溶解度知识点题型经典 一、溶液选择题 1.某固体物质的溶解度曲线如图所示,在100g水中加入120g固体,充分搅拌,在不同温度下存在①②③④四种状态.对这四种状态的描述正确的是 A.状态①为不饱和溶液, 状态②③④均为饱和溶液 B.状态①降温至10℃,有110g晶体析出 C.各状态的溶质质量分数:①>②>③>④ D.将状态②加水200g再降温至40℃可达到状态③ 【答案】A 【解析】 A、溶解度曲线上的点对应是该温度的饱和溶液,溶解度曲线下方的点对应是该温度的不饱和溶液,①在溶解度曲线的下方为90℃该物质不饱和溶液,②③④在溶解度曲线上为一定温度下的饱和溶液,正确; B、10℃时,该物质的溶解度为20g,此时100g水能溶解20g 溶质;状态①降温至10℃,有(120g-20g)=100g晶体析出,错误; C、状态①的质量分数 = 120 100120 g g g + ×100%=54.5 %;②③④在溶解度曲线上为一定温度下的饱和溶液,一定温 度下,饱和溶液的溶质质量分数= s 100s + ×100%,状态②的质量分数 = 120 100120 g g g + ×100%=54.5 %;状态③的质量分数= 65 10065 g g g + ×100%=39.3 %;状态④ 的质量分数= 35 10035 g g g + ×100%=25.9 %;各状态的溶质质量分数:④=③>②>①;错 误;D、将状态②加水200g时,溶液中有水300g,溶质120g,再降温至40℃时,若可达 到状态③,则40℃时该物质的溶解度为40g,根据溶解度曲线可知40℃时,该物质的溶解度大于60g,错误。故选A。 点睛:一定温度下,饱和溶液的溶质质量分数= s 100s + ×100%。 2.氯化铵和硝酸钾溶解度曲线如图所示,下列叙述正确的是( ) A.50℃时,氯化铵的溶解度大于硝酸钾 B.a℃时,氯化铵与硝酸钾溶液的质量分数相等 C.将60℃的硝酸钾饱和溶液降温会变为不饱和溶液 D.40℃时,50g水中加入50g硝酸钾,充分搅拌,得到质量分数约为39%的硝酸钾溶液【答案】D 【解析】 【分析】 【详解】 A、从图中看出,50℃时,硝酸钾的溶解度大于氯化铵的,故A不正确; B、a℃时,硝酸钾和氯化铵的溶解度曲线相交,此时两物质的溶解度相等,则其饱和溶液的溶质质量分数相等,其不饱和溶液的质量分数是否相等无法确定,故B不正确; C、硝酸钾的溶解度随温度的升高明显增大,将60℃时硝酸钾饱和溶液降温后会析出晶体,剩余的溶液仍然是低温下的饱和溶液,故C不正确; D、40℃时,硝酸钾的溶解度为64g,则50g水中最多溶解硝酸钾32g,所得溶液的溶质质 量分数为 32g 100%39% 32g+50g ?≈,故D正确。 故选D。 3.甲、乙、丙三种物质的溶解度曲线如图所示。下列说法错误的是( )思考题与习题答案
(完整版)溶解度练习题
高中化学 溶解度知识点总结
管理学思考题及参考答案
溶解度曲线中考试题解析
溶液 溶解度练习题经典
(完整)初中化学溶解度知识点,推荐文档
第1章思考题及参考答案
溶解度曲线知识点及习题
最新溶液 溶解度知识点题型经典
