化学元素符号表与化学式
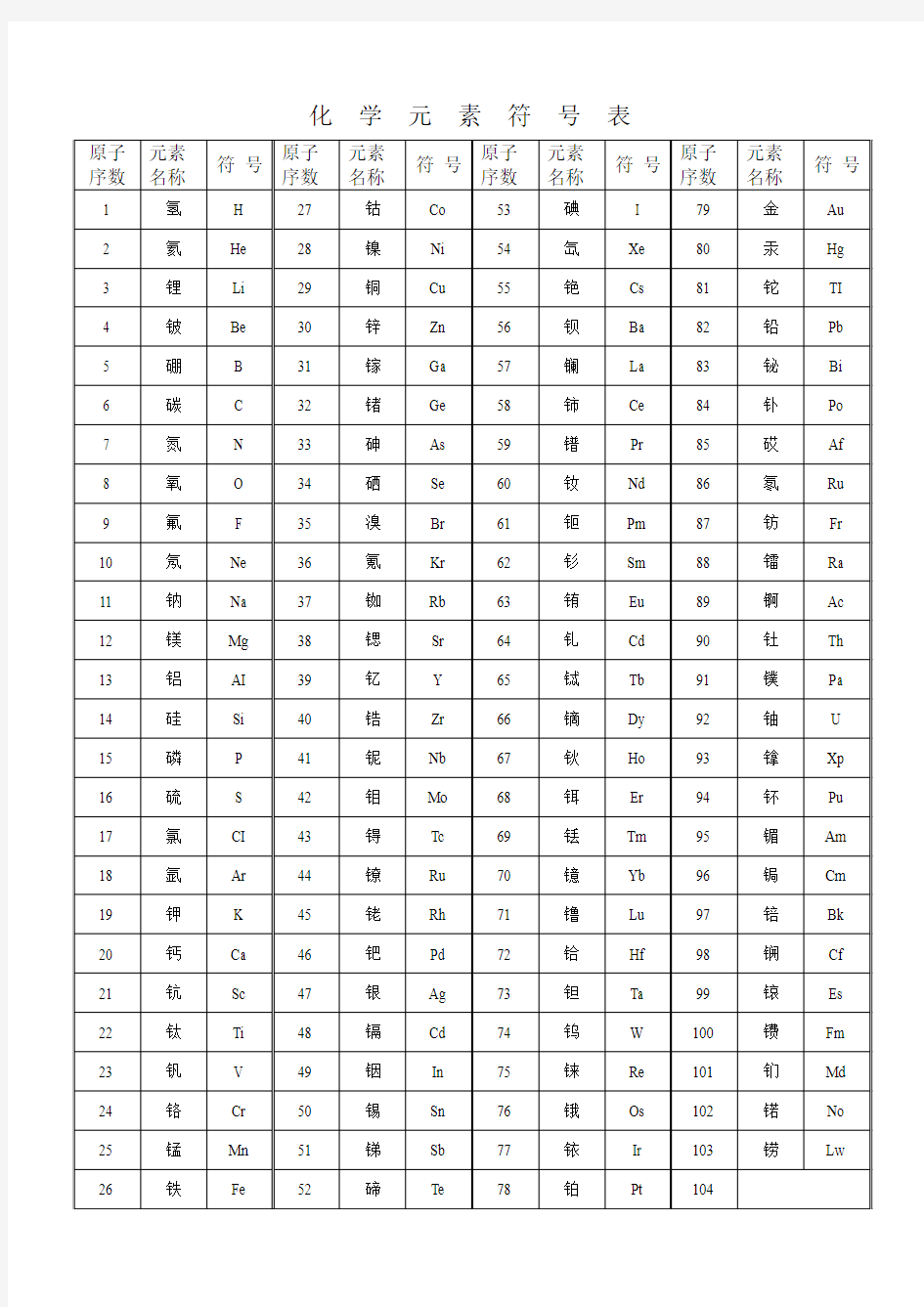

化学元素符号表
化合反应
1、镁在空气中燃烧:2Mg + O2 点燃2MgO
2、铁在氧气中燃烧:3Fe + 2O2 点燃Fe3O4
3、铝在空气中燃烧:4Al + 3O2 点燃2Al2O3
4、氢气在空气中燃烧:2H2 + O2 点燃2H2O
5、红磷在空气中燃烧:4P + 5O2 点燃2P2O5
6、硫粉在空气中燃烧:S + O2 点燃SO2
7、碳在氧气中充分燃烧:C + O2 点燃CO2
8、碳在氧气中不充分燃烧:2C + O2 点燃2CO
9、二氧化碳通过灼热碳层:C + CO2 高温2CO
10、一氧化碳在氧气中燃烧:2CO + O2 点燃2CO2
11、二氧化碳和水反应(二氧化碳通入紫色石蕊试液):CO2 + H2O === H2CO3
12、生石灰溶于水:CaO + H2O === Ca(OH)2
13、无水硫酸铜作干燥剂:CuSO4 + 5H2O ==== CuSO4?5H2O
14、钠在氯气中燃烧:2Na + Cl2点燃2NaCl
分解反应
15、实验室用双氧水制氧气:2H2O2 MnO2 2H2O+ O2↑
16、加热高锰酸钾:2KMnO4 加热K2MnO4 + MnO2 + O2↑
17、水在直流电的作用下分解:2H2O 通电2H2↑+ O2 ↑
18、碳酸不稳定而分解:H2CO3 === H2O + CO2↑
19、高温煅烧石灰石(二氧化碳工业制法):CaCO3 高温CaO + CO2↑
置换反应
20、铁和硫酸铜溶液反应:Fe + CuSO4 == FeSO4 + Cu
21、锌和稀硫酸反应(实验室制氢气):Zn + H2SO4 == ZnSO4 + H2↑
22、镁和稀盐酸反应:Mg+ 2HCl === MgCl2 + H2↑
23、氢气还原氧化铜:H2 + CuO 加热Cu + H2O
24、木炭还原氧化铜:C+ 2CuO 高温2Cu + CO2↑
25、甲烷在空气中燃烧:CH4 + 2O2 点燃CO2 + 2H2O
26、水蒸气通过灼热碳层:H2O + C 高温H2 + CO
27、焦炭还原氧化铁:3C+ 2Fe2O3 高温4Fe + 3CO2↑
其他
28、氢氧化钠溶液与硫酸铜溶液反应:2NaOH + CuSO4 == Cu(OH)2↓ + Na2SO4
29、甲烷在空气中燃烧:CH4 + 2O2 点燃CO2 + 2H2O
30、酒精在空气中燃烧:C2H5OH + 3O2 点燃2CO2 + 3H2O
31、一氧化碳还原氧化铜:CO+ CuO 加热Cu + CO2
32、一氧化碳还原氧化铁:3CO+ Fe2O3 高温2Fe + 3CO2
33、二氧化碳通过澄清石灰水(检验二氧化碳):Ca(OH)2 + CO2 ==== CaCO3 ↓+ H2O
34、氢氧化钠和二氧化碳反应(除去二氧化碳):2NaOH + CO2 ==== Na2CO3 + H2O
35、石灰石(或大理石)与稀盐酸反应(二氧化碳的实验室制法):CaCO3 + 2HCl === CaCl2 + H2O + CO2↑
36、碳酸钠与浓盐酸反应泡沫灭火器原理: Na2CO3 + 2HCl === 2NaCl + H2O + CO2↑
一.物质与氧气的反应:
(1)单质与氧气的反应:
1. 镁在空气中燃烧:2Mg + O2 点燃2MgO
2. 铁在氧气中燃烧:3Fe + 2O2 点燃Fe3O4
3. 铜在空气中受热:2Cu + O2 加热2CuO
4. 铝在空气中燃烧:4Al + 3O2 点燃2Al2O3
5. 氢气中空气中燃烧:2H2 + O2 点燃2H2O
6. 红磷在空气中燃烧:4P + 5O2 点燃2P2O5
7. 硫粉在空气中燃烧:S + O2 点燃SO2
8. 碳在氧气中充分燃烧:C + O2 点燃CO2
9. 碳在氧气中不充分燃烧:2C + O2 点燃2CO
(2)化合物与氧气的反应:
10. 一氧化碳在氧气中燃烧:2CO + O2 点燃2CO2
11. 甲烷在空气中燃烧:CH4 + 2O2 点燃CO2 + 2H2O
12. 酒精在空气中燃烧:C2H5OH + 3O2 点燃2CO2 + 3H2O
二.几个分解反应:
13. 水在直流电的作用下分解:2H2O 通电2H2↑+ O2 ↑
14. 加热碱式碳酸铜:Cu2(OH)2CO3 加热2CuO + H2O + CO2↑
15. 加热氯酸钾(有少量的二氧化锰):2KClO3 ==== 2KCl + 3O2 ↑
16. 加热高锰酸钾:2KMnO4 加热K2MnO4 + MnO2 + O2↑
17. 碳酸不稳定而分解:H2CO3 === H2O + CO2↑
18. 高温煅烧石灰石:CaCO3 高温CaO + CO2↑
三.几个氧化还原反应:
19. 氢气还原氧化铜:H2 + CuO 加热Cu + H2O
20. 木炭还原氧化铜:C+ 2CuO 高温2Cu + CO2↑
21. 焦炭还原氧化铁:3C+ 2Fe2O3 高温4Fe + 3CO2↑
22. 焦炭还原四氧化三铁:2C+ Fe3O4 高温3Fe + 2CO2↑
23. 一氧化碳还原氧化铜:CO+ CuO 加热Cu + CO2
24. 一氧化碳还原氧化铁:3CO+ Fe2O3 高温2Fe + 3CO2
25. 一氧化碳还原四氧化三铁:4CO+ Fe3O4 高温3Fe + 4CO2
四.单质、氧化物、酸、碱、盐的相互关系
(1)金属单质+ 酸-------- 盐+ 氢气(置换反应)
26. 锌和稀硫酸Zn + H2SO4 = ZnSO4 + H2↑
27. 铁和稀硫酸Fe + H2SO4 = FeSO4 + H2↑
28. 镁和稀硫酸Mg + H2SO4 = MgSO4 + H2↑
29. 铝和稀硫酸2Al +3H2SO4 = Al2(SO4)3 +3H2↑
30. 锌和稀盐酸Zn + 2HCl === ZnCl2 + H2↑
31. 铁和稀盐酸Fe + 2HCl === FeCl2 + H2↑
32. 镁和稀盐酸Mg+ 2HCl === MgCl2 + H2↑
33. 铝和稀盐酸2Al + 6HCl == 2AlCl3 + 3H2↑
(2)金属单质+ 盐(溶液)------- 另一种金属+ 另一种盐
34. 铁和硫酸铜溶液反应:Fe + CuSO4 === FeSO4 + Cu
35. 锌和硫酸铜溶液反应:Zn + CuSO4 === ZnSO4 + Cu
36. 铜和硝酸汞溶液反应:Cu + Hg(NO3)2 === Cu(NO3)2 + Hg (3)碱性氧化物+酸-------- 盐+ 水
37. 氧化铁和稀盐酸反应:Fe2O3 + 6HCl === 2FeCl3 + 3H2O
38. 氧化铁和稀硫酸反应:Fe2O3 + 3H2SO4 === Fe2(SO4)3 + 3H2O
39. 氧化铜和稀盐酸反应:CuO + 2HCl ==== CuCl2 + H2O
40. 氧化铜和稀硫酸反应:CuO + H2SO4 ==== CuSO4 + H2O
41. 氧化镁和稀硫酸反应:MgO + H2SO4 ==== MgSO4 + H2O
42. 氧化钙和稀盐酸反应:CaO + 2HCl ==== CaCl2 + H2O
(4)酸性氧化物+碱-------- 盐+ 水
43.苛性钠暴露在空气中变质:2NaOH + CO2 ==== Na2CO3 + H2O 44.苛性钠吸收二氧化硫气体:2NaOH + SO2 ==== Na2SO3 + H2O 45.苛性钠吸收三氧化硫气体:2NaOH + SO3 ==== Na2SO4 + H2O 46.消石灰放在空气中变质:Ca(OH)2 + CO2 ==== CaCO3 ↓+ H2O 47. 消石灰吸收二氧化硫:Ca(OH)2 + SO2 ==== Ca SO3 ↓+ H2O
(5)酸+ 碱-------- 盐+ 水
48.盐酸和烧碱起反应:HCl + NaOH ==== NaCl +H2O
49. 盐酸和氢氧化钾反应:HCl + KOH ==== KCl +H2O
50.盐酸和氢氧化铜反应:2HCl + Cu(OH)2 ==== CuCl2 + 2H2O
51. 盐酸和氢氧化钙反应:2HCl + Ca(OH)2 ==== CaCl2 + 2H2O
52. 盐酸和氢氧化铁反应:3HCl + Fe(OH)3 ==== FeCl3 + 3H2O
53.氢氧化铝药物治疗胃酸过多:3HCl + Al(OH)3 ==== AlCl3 + 3H2O
54.硫酸和烧碱反应:H2SO4 + 2NaOH ==== Na2SO4 + 2H2O
55.硫酸和氢氧化钾反应:H2SO4 + 2KOH ==== K2SO4 + 2H2O
56.硫酸和氢氧化铜反应:H2SO4 + Cu(OH)2 ==== CuSO4 + 2H2O
57. 硫酸和氢氧化铁反应:3H2SO4 + 2Fe(OH)3==== Fe2(SO4)3 + 6H2O
58. 硝酸和烧碱反应:HNO3+ NaOH ==== NaNO3 +H2O
(6)酸+ 盐-------- 另一种酸+ 另一种盐
59.大理石与稀盐酸反应:CaCO3 + 2HCl === CaCl2 + H2O + CO2↑ 60.碳酸钠与稀盐酸反应: Na2CO3 + 2HCl === 2NaCl + H2O + CO2↑ 61.碳酸镁与稀盐酸反应: MgCO3 + 2HCl === MgCl2 + H2O + CO2↑ 62.盐酸和硝酸银溶液反应:HCl + AgNO3 === AgCl↓ + HNO3
63.硫酸和碳酸钠反应:Na2CO3 + H2SO4 === Na2SO4 + H2O + CO2↑
64.硫酸和氯化钡溶液反应:H2SO4 + BaCl2 ==== BaSO4 ↓+ 2HCl
(7)碱+ 盐-------- 另一种碱+ 另一种盐
65.氢氧化钠与硫酸铜:2NaOH + Cu SO4 ==== Cu(OH)2↓ + Na2SO4
66.氢氧化钠与氯化铁:3NaOH + FeCl3 ==== Fe(OH)3↓ + 3NaCl
67.氢氧化钠与氯化镁:2NaOH + MgCl2 ==== Mg(OH)2↓ + 2NaCl
68. 氢氧化钠与氯化铜:2NaOH + CuCl2 ==== Cu(OH)2↓ + 2NaCl
69. 氢氧化钙与碳酸钠:Ca(OH)2 + Na2CO3 === CaCO3↓+ 2NaOH
(8)盐+ 盐----- 两种新盐
70.氯化钠溶液和硝酸银溶液:NaCl + AgNO3 ==== AgCl↓ + NaNO3
71.硫酸钠和氯化钡:Na2SO4 + BaCl2 ==== BaSO4↓ + 2NaCl
五.其它反应:
72.二氧化碳溶解于水:CO2 + H2O === H2CO3
73.生石灰溶于水:CaO + H2O === Ca(OH)2
74.氧化钠溶于水:Na2O + H2O ==== 2NaOH
75.三氧化硫溶于水:SO3 + H2O ==== H2SO4
76.硫酸铜晶体受热分解:CuSO4?5H2O 加热CuSO4 + 5H2O
77.无水硫酸铜作干燥剂:CuSO4 + 5H2O ==== CuSO4?5H2
化学方程式反应现象应用
2Mg+O2点燃或Δ2MgO 剧烈燃烧.耀眼白光.生成白色固体.放热.产生大量白烟白色信号弹
2Hg+O2点燃或Δ2HgO 银白液体、生成红色固体拉瓦锡实验
2Cu+O2点燃或Δ2CuO 红色金属变为黑色固体
4Al+3O2点燃或Δ2Al2O3 银白金属变为白色固体
3Fe+2O2点燃Fe3O4 剧烈燃烧、火星四射、生成黑色固体、放热4Fe + 3O2高温2Fe2O3
C+O2 点燃CO2 剧烈燃烧、白光、放热、使石灰水变浑浊
S+O2 点燃SO2 剧烈燃烧、放热、刺激味气体、空气中淡蓝色火焰.氧气中蓝紫色火焰
2H2+O2 点燃2H2O 淡蓝火焰、放热、生成使无水CuSO4变蓝的液体(水)高能燃料
4P+5O2 点燃2P2O5 剧烈燃烧、大量白烟、放热、生成白色固体证明空气中氧气含量
CH4+2O2点燃2H2O+CO2 蓝色火焰、放热、生成使石灰水变浑浊气体和使无水CuSO4变蓝的液体(水)甲烷
和天然气的燃烧
2C2H2+5O2点燃2H2O+4CO2 蓝色火焰、放热、黑烟、生成使石灰水变浑浊气体和使无水CuSO4变蓝的液体(水)氧炔焰、焊接切割金属
2KClO3MnO2 Δ2KCl +3O2↑ 生成使带火星的木条复燃的气体实验室制备氧气
2KMnO4Δ K2MnO4+MnO2+O2↑ 紫色变为黑色、生成使带火星木条复燃的气体实验室制备氧气
2HgOΔ2Hg+O2↑ 红色变为银白、生成使带火星木条复燃的气体拉瓦锡实验
2H2O通电2H2↑+O2↑ 水通电分解为氢气和氧气电解水
Cu2(OH)2CO3Δ2CuO+H2O+CO2↑绿色变黑色、试管壁有液体、使石灰水变浑浊气体铜绿加热
NH4HCO3ΔNH3↑+ H2O +CO2↑ 白色固体消失、管壁有液体、使石灰水变浑浊气体碳酸氢铵长期暴露空气中会消失
Zn+H2SO4=ZnSO4+H2↑ 有大量气泡产生、锌粒逐渐溶解实验室制备氢气
Fe+H2SO4=FeSO4+H2↑ 有大量气泡产生、金属颗粒逐渐溶解
Mg+H2SO4 =MgSO4+H2↑ 有大量气泡产生、金属颗粒逐渐溶解
2Al+3H2SO4=Al2(SO4)3+3H2↑ 有大量气泡产生、金属颗粒逐渐溶解
F e2O3+3H2 Δ 2Fe+3H2O 红色逐渐变为银白色、试管壁有液体冶炼金属、利用氢气的还原性
Fe3O4+4H2 Δ3Fe+4H2O 黑色逐渐变为银白色、试管壁有液体冶炼金属、利用氢气的还原性
WO3+3H2Δ W +3H2O 冶炼金属钨、利用氢气的还原性
MoO3+3H2 ΔMo +3H2O 冶炼金属钼、利用氢气的还原性
2Na+Cl2Δ或点燃2NaCl 剧烈燃烧、黄色火焰离子化合物的形成、
H2+Cl2 点燃或光照2HCl 点燃苍白色火焰、瓶口白雾共价化合物的形成、制备盐酸
CuSO4+2NaOH=Cu(OH)2↓+Na2SO4 蓝色沉淀生成、上部为澄清溶液质量守恒定律实验
2C +O2点燃2CO 煤炉中常见反应、空气污染物之一、煤气中毒原因
2C O+O2点燃2CO2 蓝色火焰煤气燃烧
C + CuO 高温2Cu+ CO2↑ 黑色逐渐变为红色、产生使澄清石灰水变浑浊的气体冶炼金属
2Fe2O3+3C 高温4Fe+ 3CO2↑ 冶炼金属
Fe3O4+2C高温3Fe + 2CO2↑ 冶炼金属
C + CO2 高温2CO
CO2 + H2O = H2CO3 碳酸使石蕊变红证明碳酸的酸性
H2CO3 ΔCO2↑+ H2O 石蕊红色褪去
Ca(OH)2+CO2= CaCO3↓+ H2O 澄清石灰水变浑浊应用CO2检验和石灰浆粉刷墙壁
CaCO3+H2O+CO2 = Ca(HCO3)2 白色沉淀逐渐溶解溶洞的形成,石头的风化
Ca(HCO3)2Δ CaCO3↓+H2O+CO2↑ 白色沉淀、产生使澄清石灰水变浑浊的气体水垢形成.钟乳石的形成
2NaHCO3ΔNa2CO3+H2O+CO2↑ 产生使澄清石灰水变浑浊的气体小苏打蒸馒头
CaCO3 高温C aO+ CO2↑ 工业制备二氧化碳和生石灰
CaCO3+2HCl=CaCl2+ H2O+CO2↑ 固体逐渐溶解、有使澄清石灰水变浑浊的气体实验室制备二氧化碳、除水垢
Na2CO3+H2SO4=Na2SO4+H2O+CO2↑ 固体逐渐溶解、有使澄清石灰水变浑浊的气体泡沫灭火器原理
Na2CO3+2HCl=2NaCl+ H2O+CO2↑ 固体逐渐溶解、有使澄清石灰水变浑浊的气体泡沫灭火器原理
MgCO3+2HCl=MgCl2+H2O+CO2↑ 固体逐渐溶解、有使澄清石灰水变浑浊的气体
CuO +COΔ Cu + CO2 黑色逐渐变红色,产生使澄清石灰水变浑浊的气体冶炼金属
Fe2O3+3CO高温2Fe+3CO2 冶炼金属原理
Fe3O4+4CO高温3Fe+4CO2 冶炼金属原理
WO3+3CO高温W+3CO2 冶炼金属原理
CH3COOH+NaOH=CH3COONa+H2O
2CH3OH+3O2点燃2CO2+4H2O
C2H5OH+3O2点燃2CO2+3H2O 蓝色火焰、产生使石灰水变浑浊的气体、放热酒精的燃烧
Fe+CuSO4=Cu+FeSO4 银白色金属表面覆盖一层红色物质湿法炼铜、镀铜
Mg+FeSO4= Fe+ MgSO4 溶液由浅绿色变为无色Cu+Hg(NO3)2=Hg+ Cu (NO3)2
Cu+2AgNO3=2Ag+ Cu(NO3)2 红色金属表面覆盖一层银白色物质镀银
Zn+CuSO4= Cu+ZnSO4 青白色金属表面覆盖一层红色物质镀铜
Fe2O3+6HCl=2FeCl3+3H2O 铁锈溶解、溶液呈黄色铁器除锈
Al2O3+6HCl=2AlCl3+3H2O 白色固体溶解
Na2O+2HCl=2NaCl+H2O 白色固体溶解
CuO+2HCl=CuCl2+H2O 黑色固体溶解、溶液呈蓝色
ZnO+2HCl=ZnCl2+ H2O 白色固体溶解
MgO+2HCl=MgCl2+ H2O 白色固体溶解
CaO+2HCl=CaCl2+ H2O 白色固体溶解
NaOH+HCl=NaCl+ H2O 白色固体溶解
Cu(OH)2+2HCl=CuCl2+2H2O 蓝色固体溶解
Mg(OH)2+2HCl=MgCl2+2H2O 白色固体溶解
Al(OH)3+3HCl=AlCl3+3H2O 白色固体溶解胃舒平治疗胃酸过多
Fe(OH)3+3HCl=FeCl3+3H2O 红褐色沉淀溶解、溶液呈黄色
Ca(OH)2+2HCl=CaCl2+2H2O
HCl+AgNO3= AgCl↓+HNO3 生成白色沉淀、不溶解于稀硝酸检验Cl—的原理
Fe2O3+3H2SO4= Fe2(SO4)3+3H2O 铁锈溶解、溶液呈黄色铁器除锈
Al2O3+3H2SO4= Al2(SO4)3+3H2O 白色固体溶解
CuO+H2SO4=CuSO4+H2O 黑色固体溶解、溶液呈蓝色
ZnO+H2SO4=ZnSO4+H2O 白色固体溶解
MgO+H2SO4=MgSO4+H2O 白色固体溶解
2NaOH+H2SO4=Na2SO4+2H2O
Cu(OH)2+H2SO4=CuSO4+2H2O 蓝色固体溶解
Ca(OH)2+H2SO4=CaSO4+2H2O
Mg(OH)2+H2SO4=MgSO4+2H2O 白色固体溶解
2Al(OH)3+3H2SO4=Al2(SO4)3+3H2O 白色固体溶解
2Fe(OH)3+3H2SO4=Fe2(SO4)3+3H2O 红褐色沉淀溶解、溶液呈黄色
Ba(OH)2+ H2SO4=BaSO4↓+2H2O 生成白色沉淀、不溶解于稀硝酸检验SO42—的原理BaCl2+ H2SO4=BaSO4↓+2HCl 生成白色沉淀、不溶解于稀硝酸检验SO42—的原理
Ba(NO3)2+H2SO4=BaSO4↓+2HNO3 生成白色沉淀、不溶解于稀硝酸检验SO42—的原理Na2O+2HNO3=2NaNO3+H2O 白色固体溶解
CuO+2HNO3=Cu(NO3)2+H2O 黑色固体溶解、溶液呈蓝色
ZnO+2HNO3=Zn(NO3)2+ H2O 白色固体溶解
MgO+2HNO3=Mg(NO3)2+ H2O 白色固体溶解
CaO+2HNO3=Ca(NO3)2+ H2O 白色固体溶解
NaOH+HNO3=NaNO3+ H2O
Cu(OH)2+2HNO3=Cu(NO3)2+2H2O 蓝色固体溶解
Mg(OH)2+2HNO3=Mg(NO3)2+2H2O 白色固体溶解
Al(OH)3+3HNO3=Al(NO3)3+3H2O 白色固体溶解
Ca(OH)2+2HNO3=Ca(NO3)2+2H2O
Fe(OH)3+3HNO3=Fe(NO3)3+3H2O 红褐色沉淀溶解、溶液呈黄色
3NaOH + H3PO4=3H2O + Na3PO4
3NH3+H3PO4=(NH4)3PO4
2NaOH+CO2=Na2CO3+ H2O 吸收CO、O2、H2中的CO2、
2NaOH+SO2=Na2SO3+ H2O 2NaOH+SO3=Na2SO4+ H2O 处理硫酸工厂的尾气(SO2)
FeCl3+3NaOH=Fe(OH)3↓+3NaCl 溶液黄色褪去、有红褐色沉淀生成
AlCl3+3NaOH=Al(OH)3↓+3NaCl 有白色沉淀生成
MgCl2+2NaOH = Mg(OH)2↓+2NaCl
CuCl2+2NaOH = Cu(OH)2↓+2NaCl 溶液蓝色褪去、有蓝色沉淀生成
CaO+ H2O = Ca(OH)2 白色块状固体变为粉末、生石灰制备石灰浆
Ca(OH)2+SO2=CaSO3↓+ H2O 有白色沉淀生成初中一般不用
Ca(OH)2+Na2CO3=CaCO3↓+2NaOH 有白色沉淀生成工业制烧碱、实验室制少量烧碱
Ba(OH)2+Na2CO3=BaCO3↓+2NaOH 有白色沉淀生成
Ca(OH)2+K2CO3=CaCO3↓ +2KOH 有白色沉淀生成
CuSO4+5H2O= CuSO4?H2O 蓝色晶体变为白色粉末
CuSO4?H2OΔ CuSO4+5H2O 白色粉末变为蓝色检验物质中是否含有水
AgNO3+NaCl = AgCl↓+Na NO3 白色不溶解于稀硝酸的沉淀(其他氯化物类似反应)应用于检验溶液中的氯离子
BaCl2 + Na2SO4 = BaSO4↓+2NaCl 白色不溶解于稀硝酸的沉淀(其他硫酸盐类似反应)应用于检验硫酸根离子
CaCl2+Na2CO3= CaCO3↓+2NaCl 有白色沉淀生成
MgCl2+Ba(OH)2=BaCl2+Mg(OH)2↓ 有白色沉淀生成
CaCO3+2HCl=CaCl2+H2O+CO2 ↑
MgCO3+2HCl= MgCl2+H2O+ CO2 ↑
NH4NO3+NaOH=NaNO3+NH3↑+H2O 生成使湿润石蕊试纸变蓝色的气体应用于检验溶液中的铵根离子
NH4Cl+ KOH= KCl+NH3↑+H2O 生成使湿润石蕊试纸变蓝色的气体
一、化学元素表巧记口诀复习过程
一、化学元素表巧记 口诀
一、化学元素表巧记口诀 (一)、元素符号有来由,拉丁名称取字头;第一个字母要大写,附加字母小写后。 对比碳C,铜Cu,N氮、P磷、S硫; Si硅、氧是O,铝A1、铅Pb; Ba钡、钨W, Ag是银、Zn锌; I碘、K钾、Br溴, H是氢、U是铀; Fe铁、Na钠, Mg镁、Ca钙; Hg汞、金Au,Sn锡、Sb锑; 氯Cl、钻Co,元素符号要熟记。 (二)、化学元素符号歌(外文按英语字母发音读) 碳是C,磷是P,铅的符号是Pb。 Cu铜,Ca钙,钨的符号W。 H氢,S硫,硅的符号Si。 金Au,银Ag,镁的符号Mg。 钠Na,氖Ne,汞的符号Hg。 硼是B,钡Ba,铁的符号Fe。 锌Zn,锰Mn,锡的符号Sn。 钾是K,碘是I,氟的符号是F。 氧是O,氮是N,溴的符号是Br。 Al铝,Cl氯,锑的符号Sb。(三)常见元素符号名称歌(可边写边读)(写)C H O N Cl S P,(读)碳氢氧氮氯硫磷。(写)K Ca Na Mg Al FeZn,
(读)钾钙钠镁铝铁锌。(写)Br I Mn Ba Cu Hg Ag,(读)溴碘锰钡铜汞银。(写)Sb Si Sn Pb W和Au,(读)锑硅锡铅钨和金 二、前二十种元素 氢氦锂铍硼,碳氮氧氟氖; 钠镁铝硅磷,硫氯氩钾钙。 三、常见元素的化合价 (一) 一价元素氢锂钠钾银,二价元素氧钙钡镁锌; 三价铝,四价硅。还有变价元素往后推 铜汞一二来铁二三,正二正四本是碳 磷是双三外加五,最难记的氮锰氯 氯价通常显负一,还有正价一五七; 锰显正价二四六,最高价数也是七。 (二) 钾钠银氢正一价,钙镁钡锌正二价; 一二铜汞二三铁,三铝四硅五氮磷; 二四六硫二四碳,金正非负单质零。 (三) 一价钾钠银氢氟,二价钙镁和钡锌; 铝价正三氧负二,以上价态要记真; 铜一二来铁二三,碳硅二四要记全; 硫显负二正四六,负三正五氮和磷; 氯价通常显负一,还有正价一五七;
化学元素符号快速记忆方法
化学元素符号快速记忆方法 导读:我根据大家的需要整理了一份关于《化学元素符号快速记忆方法》的内容,具体内容:元素符号是国际通用的化学用语,它是学习化学不可缺少的重要工具。记住化学元素符号也是学习化学的基础。下面是由我给大家带来关于化学元素符号的快速记忆方法,希望对大家有帮助!化学...元素符号是国际通用的化学用语,它是学习化学不可缺少的重要工具。记住化学元素符号也是学习化学的基础。下面是由我给大家带来关于化学元素符号的快速记忆方法,希望对大家有帮助! 化学元素符号的快速记忆方法 一、拼音法 钠(Na)、钡(Ba)、氟(F)、钨(W)、锂(Li):这些元素名称的汉语拼音与该元素的元素符号相似。 如钠元素(Na),"钠"的汉语拼音为n; 钡元素(Ba),"钡"的读音由汉语拼音"b"的发音与英语字母"a"的发音拼成; 氟元素(F),"氟"的读音的声母为"f", 钨元素(W),"钨"的汉语拼音的声母为"w"; 锂元素(Li),"锂"的汉语拼音为"lǐ". 二、形象法 有些元素的元素符号可采用形象的方法记忆. 钨元素(W),可以联想白炽灯内的钨丝,酷似"W"形;
硫元素(S),可以联想起弯弯曲曲的小溪中的流水,形如"S"状; 氧元素(O),可以联想圆圆的太阳形状; 钾元素(K),可以联想到剪指甲时张开的剪刀的形状. 三、谐音法 如金元素(Au),可以设想这样的情景:有人突然看到地上有一块金光闪闪的金子,他一定会情不自禁地发出"哎哟"的惊叹声,这"哎哟"的发音不正是英文字母"Au"的发音吗? 四、韵语法 ①按字母对比记忆法. "A"开头,金银铝氩, "B"字开头钡和溴,钙铜碳氯先写"C", "M"领头锰和镁. 常用元素符号按英文字母顺序对比记忆: A:Ag(银)、Al(铝)、Ar(氩)、Au(金). B:Be(铍)、B(硼)、Ba(钡). C:C(碳)、Cl(氯)、Ca(钙)、Cu(铜). F:F(氟) H:H(氢)、He(氦)、Hg(汞). I:I(碘). K:K(钾). L:Li(锂). M:Mg(镁)、Mn(锰).
常用化学元素符号表
创作编号: GB8878185555334563BT9125XW 创作者:凤呜大王* 常用分子式 氮气:N2氢气:H2甲烷:CH4氧气:O2 氨:NH3水:H2O 一氧化碳:CO 二氧化碳:CO2 硫:S 二氧化硫:SO2硫代硫酸钠:Na2S2O3 铁:Fe 二价铁离子:Fe2+三价铁离子:Fe3+硫酸钠:Na2SO4
磷酸三钠:Na3PO4碳酸钠:Na2CO3 碳酸钙:CaCO3碳酸氢钠:NaHCO3氢氧化钠:NaOH 盐酸:HCL 碳酸氢铵:NH4HCO3硝酸:HNO3 硫酸:H2SO4尿素:CO(NH2) 碳酸:H2CO3 化学需氧量:COD 高锰酸钾:KMnO4锰酸钾:K2MnO4 缩二尿:NH2CONHCONH2硝酸银:AgNO3硫酸铜:CuSO4 碳酸丙稀脂(碳丙液):C3H6CO3甲醇:CH3OH 乙醇:CH3CH2OH 甲醛:HCHO 一甲氨:NH2CH3二甲氨:NH(CH3)2 三甲氨:N(CH3)3三氧化二铝:AL2O3三氧化二铁:Fe2O3 氧化铜:CuO 氯化钠:NaCL 一、初中化学常见混合物的重要成分 1、空气:氮气(N2)和氧气(O2) 2、水煤气:一氧化碳(CO)和氢气(H2) 3、煤气:一氧化碳(CO) 4、天然气:甲烷(CH4) 5、石灰石/大理石:(CaCO3) 6、生铁/钢:(Fe) 7、木炭/焦炭/炭黑/活性炭:(C) 8、铁锈:(Fe2O3) 二、初中化学常见物质俗称 1、氯化钠(NaCl):食盐 2、碳酸钠(Na2CO3) :纯碱,苏打,口碱 3、氢氧化钠(NaOH):火碱,烧碱,苛性钠 4、氧化钙(CaO):生石灰 5、氢氧化钙(Ca(OH)2):熟石灰,消石灰 6、二氧化碳固体(CO2):干冰 7、氢氯酸(HCl):盐酸 8、碱式碳酸铜(Cu2(OH)2CO3):铜绿 9、硫酸铜晶体(CuSO4 .5H2O):蓝矾,胆矾 10、甲烷(CH4):沼气 11、乙醇(C2H5OH):酒精 12、乙酸(CH3COOH):醋酸 13、过氧化氢(H2O2):双氧水 14、汞(Hg):水银 15、碳酸氢钠(NaHCO3):小苏打 三、物质的除杂 1、CO2(CO):把气体通过灼热的氧化铜,
初中化学常见的元素符号
常见的元素符号: 氢氦锂铍硼,碳氮氧氟氖,钠镁铝硅磷,硫氯氩钾钙。锰钡碘H He Li Be B , C N O F Ne , Na Mg Al Si P , S Cl Ar K Ca 。Mn Ba I 金属活动性顺序:钾钙钠镁铝,锌铁锡铅氢铜汞银铂金 K Ca Na Mg Al, Zn Fe Sn Pb(H),Cu Hg Ag Pt Au 常见元素的化合价:金正,非负,单质零,氢+1,氧-2,正负总价和为零。 钾钠银氢+1价,钙镁钡锌+2价;氟氯溴碘-1价,通常氧是-2价; 铜+1,+2铝+3;铁有+2,+3 硅+4; 2,4,6硫 2,4碳; 氮磷-3,+5最常见;2,4,6,7锰变价;单质中元素零价要记清。化学式: 单质:氢气H2氧气O2氮气N2氯气Cl2氖气Ne碳 C 铜Cu铁Fe 化合物:氧化物:一氧化碳CO二氧化碳CO2五氧化二磷P2O5二氧化硫SO2二氧化锰MnO2三氧化二铁Fe2O3四氧化三铁Fe3O4 氧化亚铁FeO氧化镁MgO氧化钙CaO三氧化二铝Al2O3 氧化汞HgO氧化铜CuO 酸:盐酸HCl硫酸H2SO4硝酸HNO3碳酸H2CO3磷酸H3PO4碱:氢氧化钠NaOH氢氧化钙Ca(OH)2氢氧化钡Ba(OH)2氢氧化钾KOH 氢氧化铁(红褐色)Fe(OH)3氢氧化铜(蓝色)Cu(OH)2 盐:氯化钠NaCl氯化镁MgCl2氯化铝AlCl3 氯化钾 KCl氯化铁FeCl3氯化亚铁FeCl2氯化锌ZnCl2 氯化钡BaCl2氯化铜CuCl2氯化银AgCl(盐酸盐) 碳酸钙CaCO3碳酸钠Na2CO3碳酸钾K2CO3碳酸钡BaCO3 硫酸亚铁FeSO4硫酸铁Fe2(SO4)3硫酸钠Na2SO4硫酸镁MgSO4 硫酸铝Al2(SO4)3硫酸铜CuSO4硫酸锌ZnSO4硫酸钡BaSO4 硝酸银AgNO3硝酸汞Hg(NO3)2硝酸锌Zn(NO3)2硝酸钡Ba(NO3)2 -1硝酸、氢氧根,-2碳酸、硫酸根,-3记住磷酸根,+1价的是铵根。
常用化学元素符号表
二、常用化学元素符号表 三、常用金属材料容重表 四、常用工业材料比重表
中碳钢(含碳0.4%) 高碳钢(含碳1%)高速钢(含钨9%)高速钢(含钨18%)不锈钢(含铬13%)62-1锡黄铜 60-1锡黄铜 77-2铝黄铜 60-1-1铝黄铜 58-2锰黄铜 59-1-1铁黄铜 80-3硅黄铜 4-3锡青铜 4-4-2.5锡青铜 4-4-4锡青铜 6.5~0.1锡青铜 4~0.3锡青铜 五号防锈铝 廿一号防锈铝 一号硬铝 三号硬铝 十一号硬铝 十二号硬铝 十四号硬铝 二号锻铝 四号锻铝 五号锻铝 八号锻铝 九号锻铝 4-1铸锌铝合金 锡 铅板 工业镍 15-20锌白铜 43-0.5锰白铜 40-1.5锰白铜 28-2.5-1.5镍铜合金9镍铬合金 锡基轴承合金7.82 7.81 8.3 8.7 7.75 8.45 8.45 8.6 8.2 8.5 8.5 8.6 8.8 8.79 8.9 8.8 8.9 2.65 2.73 2.75 2.73 2.84 2.8 2.8 2.69 2.65 2.75 2.8 2.8 6.9 7.3~7.5 11.37 8.9 8.6 8.89 8.90 8.8 8.72 7.34~7.75 74-3铅黄铜 63-3铅黄铜 59-1铅黄铜 90-1锡黄铜 70-1黄铜锡 3-12-5铸锡青铜 5-5-5铸锡青铜 6-6-3铸锡青铜 5铝青铜 7铝青铜 9-2铝青铜 9-4铝青铜 10-3-1.5铝青铜 2铍青铜 3-1硅青铜 铝板 二号防锈铝 二号锻铝 四号超硬铝 五号铸造铝合金 六号铸造铝合金 七号铸造铝合金 十三号铸造铝合金 十五号铸造铝合金 工业镁 锌板 铸锌 10-5锌铝合金 4-3铸锌铝合金 钴 钛 3钨钴合金 6钨钴合金 8钨钴合金 5钨钴钛合金 15钨钴钛合金 汞 锰 铬 8.70 8.5 8.5 8.8 8.54 8.69 8.8 8.82 8.2 7.8 7.63 7.6 7.5 8.23 8.47 2.73 2.67 2.8 2.8 2.55 2.60 2.65 2.67 2.95 1.74 7.2 6.86 6.3 6.75 8.9 4.51 14.9~15.3 14.6~15.0 14.4~14.8 12.3~13.2 11.0~11.7 13.6 7.43 7.19
常用化学元素符号表
常用分子式 氮气:N2氢气:H2甲烷:CH4氧气:O2 氨:NH3水:H2O 一氧化碳:CO 二氧化碳:CO2 硫:S 二氧化硫:SO2硫代硫酸钠:Na2S2O3 铁:Fe 二价铁离子:Fe2+三价铁离子:Fe3+硫酸钠:Na2SO4磷酸三钠:Na3PO4碳酸钠:Na2CO3 碳酸钙:CaCO3碳酸氢钠:NaHCO3氢氧化钠:NaOH 盐酸:HCL 碳酸氢铵:NH4HCO3硝酸:HNO3 精品
硫酸:H2SO4尿素:CO(NH2) 碳酸:H2CO3 化学需氧量:COD 高锰酸钾:KMnO4锰酸钾:K2MnO4 缩二尿:NH2CONHCONH2硝酸银:AgNO3硫酸铜:CuSO4 碳酸丙稀脂(碳丙液):C3H6CO3甲醇:CH3OH 乙醇:CH3CH2OH 甲醛:HCHO 一甲氨:NH2CH3二甲氨:NH(CH3)2 三甲氨:N(CH3)3 三氧化二铝:AL2O3三氧化二铁:Fe2O3 氧化铜:CuO 氯化钠:NaCL 一、初中化学常见混合物的重要成分 1、空气:氮气(N2)和氧气(O2) 2、水煤气:一氧化碳(CO)和氢气(H2) 3、煤气:一氧化碳(CO) 4、天然气:甲烷(CH4) 5、石灰石/大理石:(CaCO3) 6、生铁/钢:(Fe) 7、木炭/焦炭/炭黑/活性炭:(C) 8、铁锈:(Fe2O3) 二、初中化学常见物质俗称 1、氯化钠(NaCl):食盐 2、碳酸钠(Na2CO3) :纯碱,苏打,口碱 3、氢氧化钠(NaOH):火碱,烧碱,苛性钠 4、氧化钙(CaO):生石灰 5、氢氧化钙(Ca(OH)2):熟石灰,消石灰 6、二氧化碳固体(CO2):干冰 7、氢氯酸(HCl):盐酸 8、碱式碳酸铜(Cu2(OH)2CO3):铜绿 9、硫酸铜晶体(CuSO4 .5H2O):蓝矾,胆矾 10、甲烷(CH4):沼气 11、乙醇(C2H5OH):酒精 12、乙酸(CH3COOH):醋酸 13、过氧化氢(H2O2):双氧水 14、汞(Hg):水银 15、碳酸氢钠(NaHCO3):小苏打 三、物质的除杂 1、CO2(CO):把气体通过灼热的氧化铜, 2、CO(CO2):通过足量的氢氧化钠溶液 3、H2(水蒸气):通过浓硫酸/通过氢氧化钠固体 4、CuO(C):在空气中(在氧气流中)灼烧混合物 5、Cu(Fe) :加入足量的稀硫酸 6、Cu(CuO):加入足量的稀硫酸 精品
常用化学元素符号表
常用化学元素符号 元素名称符号元素名称符号元素名称符号铬Cr铌Nb铅Pb 镍Ni钽Ta铋Bi 硅Si氢H锕Ac 锰Mn碳C铈Ce 铝Al氧O铍Be 磷P钠Na铯Se 钨W镁Mg锆Zr 钼Mo硫S镧La 钒V氯Cl钡Ba 钛T钾K汞Hg 铜Cu锌Zn钙Ca 铁Fe银Ag碘I 硼B锡Sn溴Br 钴Co锑Sb氟F 氮N金Au烯土Re 常用分子式 氮气:N2氢气:H2甲烷:CH4氧气:O2 氨:NH3水:H2O 一氧化碳:CO 二氧化碳:CO2 硫:S 二氧化硫:SO2硫代硫酸钠:Na2S2O3 铁:Fe 二价铁离子:Fe2+三价铁离子:Fe3+硫酸钠:Na2SO4 磷酸三钠:Na3PO4碳酸钠:Na2CO3 碳酸钙:CaCO3碳酸氢钠:NaHCO3氢氧化钠:NaOH 盐酸:HCL 碳酸氢铵:NH4HCO3硝酸:HNO3 硫酸:H2SO4尿素:CO(NH2) 碳酸:H2CO3 化学需氧量:COD 高锰酸钾:KMnO4锰酸钾:K2MnO4 缩二尿:NH2CONHCONH2硝酸银:AgNO3硫酸铜:CuSO4 碳酸丙稀脂(碳丙液):C3H6CO3甲醇:CH3OH 乙醇:CH3CH2OH 甲醛:HCHO 一甲氨:NH2CH3二甲氨:NH(CH3)2 三甲氨:N(CH3)3 三氧化二铝:AL2O3三氧化二铁:Fe2O3 氧化铜:CuO 氯化钠:NaCL 一、初中化学常见混合物的重要成分 1、空气:氮气(N2)和氧气(O2)
2、水煤气:一氧化碳(CO)和氢气(H2) 3、煤气:一氧化碳(CO) 4、天然气:甲烷(CH4) 5、石灰石/大理石:(CaCO3) 6、生铁/钢:(Fe) 7、木炭/焦炭/炭黑/活性炭:(C) 8、铁锈:(Fe2O3) 二、初中化学常见物质俗称 1、氯化钠(NaCl):食盐 2、碳酸钠(Na2CO3) :纯碱,苏打,口碱 3、氢氧化钠(NaOH):火碱,烧碱,苛性钠 4、氧化钙(CaO):生石灰 5、氢氧化钙(Ca(OH)2):熟石灰,消石灰 6、二氧化碳固体(CO2):干冰 7、氢氯酸(HCl):盐酸 8、碱式碳酸铜(Cu2(OH)2CO3):铜绿 9、硫酸铜晶体(CuSO4 .5H2O):蓝矾,胆矾 10、甲烷(CH4):沼气 11、乙醇(C2H5OH):酒精 12、乙酸(CH3COOH):醋酸 13、过氧化氢(H2O2):双氧水 14、汞(Hg):水银 15、碳酸氢钠(NaHCO3):小苏打 三、物质的除杂 1、CO2(CO):把气体通过灼热的氧化铜, 2、CO(CO2):通过足量的氢氧化钠溶液 3、H2(水蒸气):通过浓硫酸/通过氢氧化钠固体 4、CuO(C):在空气中(在氧气流中)灼烧混合物 5、Cu(Fe) :加入足量的稀硫酸 6、Cu(CuO):加入足量的稀硫酸 7、FeSO4(CuSO4): 加入足量的铁粉 8、NaCl(Na2CO3):加入足量的盐酸 9、NaCl(Na2SO4):加入足量的氯化钡溶液 10、NaCl(NaOH):加入足量的盐酸 11、NaOH(Na2CO3):加入足量的氢氧化钙溶液 12、NaCl(CuSO4):加入足量的氢氧化钡溶液 13、NaNO3(NaCl):加入足量的硝酸银溶液 14、NaCl(KNO3):蒸发溶剂 15、KNO3(NaCl):冷却热饱和溶液。 16、CO2(水蒸气):通过浓硫酸
化学元素表带拼音
第 02 号元素: 氦 [化学符号]He, 读“亥”第 03 号元素: 锂 [化学符号]Li, 读“里”第 04 号元素: 铍 [化学符号]Be, 读“皮”第 05 号元素: 硼 [化学符号]B, 读“朋” 第 06 号元素: 碳 [化学符号]C, 读“炭” 第 07 号元素: 氮 [化学符号]N, 读“淡” 第 08 号元素: 氧 [化学符号]O, 读“养” 第 09 号元素: 氟 [化学符号]F, 读“弗” 第 10 号元素: 氖 [化学符号]Ne, 读“乃”第 11 号元素: 钠 [化学符号]Na, 读“纳”第 12 号元素: 镁 [化学符号]Mg, 读“美”第 13 号元素: 铝 [化学符号]Al, 读“吕”第 14 号元素: 硅 [化学符号]Si, 读“归”第 15 号元素: 磷 [化学符号]P, 读“邻” 第 16 号元素: 硫 [化学符号]S, 读“流” 第 17 号元素: 氯 [化学符号]Cl, 读“绿”第 18 号元素: 氩 [化学符号]Ar,A, 读“亚”第 19 号元素: 钾 [化学符号]K, 读“甲” 第 20 号元素: 钙 [化学符号]Ca, 读“丐”第 21 号元素: 钪 [化学符号]Sc, 读“亢”第 22 号元素: 钛 [化学符号]Ti, 读“太”第 23 号元素: 钒 [化学符号]V, 读“凡”
第 25 号元素: 锰 [化学符号]Mn, 读“猛”第 26 号元素: 铁 [化学符号]Fe, 读“铁”第 27 号元素: 钴 [化学符号]Co, 读“古”第 28 号元素: 镍 [化学符号]Ni, 读“臬”第 29 号元素: 铜 [化学符号]Cu, 读“同”第 30 号元素: 锌 [化学符号]Zn, 读“辛”第 31 号元素: 镓 [化学符号]Ga, 读“家”第 32 号元素: 锗 [化学符号]Ge, 读“者”第 33 号元素: 砷 [化学符号]As, 读“申”第 34 号元素: 硒 [化学符号]Se, 读“西”第 35 号元素: 溴 [化学符号]Br, 读“秀”第 36 号元素: 氪 [化学符号]Kr, 读“克”第 37 号元素: 铷 [化学符号]Rb, 读“如”第 38 号元素: 锶 [化学符号]Sr, 读“思”第 39 号元素: 钇 [化学符号]Y, 读“乙”第 40 号元素: 锆 [化学符号]Zr, 读“告”第 41 号元素: 铌 [化学符号]Nb, 读“尼”第 42 号元素: 钼 [化学符号]Mo, 读“目”第 43 号元素: 碍 [化学符号]Tc, 读“得”第 44 号元素: 钌 [化学符号]Ru, 读“了”第 45 号元素: 铑 [化学符号]Rh, 读“老”第 46 号元素: 钯 [化学符号]Pd, 读“巴”
化学元素符号注音及记忆法
1 元素周期表读音 1氢(qīng 2氦(hài 3锂(lǐ 4铍(pí 5 硼(p?ng HHeLiBeB 6碳(tàn 7氮(dàn 8氧(yǎng 9氟(fú 10 氖(nǎi CNOFNe 11钠(nà 12镁(měi 13铝(lǚ 14硅(guī 15 磷(lín NaMgAlSiP 16硫(liú 17氯(lǜ 18氩(yà 19钾(jiǎ 20钙(gài SClArKCa 21钪(kàng 22钛(tài 23 钒(fán 24铬(ga 25锰(měng ScTiVCrMn 26铁(tiě 27钴(gǔ 28 镍(nia 29 铜(t?ng 30 锌(xīn FeCoNiCuZn 31镓(jiā 32锗(zhě 33砷(shēn 34硒(xī 35溴(xiù GaGeAsSeBr 36 氪(ka 37铷(rú 38锶(sī 39钇(yǐ 40锆(gào KrRbSrYZr 41铌(ní 42 钼(mù 43锝(d? 44钌(liǎo 45铑(lǎo NbMoTcRuRh 46钯(bǎ 47银(yín 48镉(g? 49铟(yīn 50锡(xī PdAgCdInSn 51锑(tī 52碲(dì 53 碘(diǎn 54氙(xiān 55铯(sa SbTeIXeCs 56钡(bai 57镧(lán 58铈(shì 59镨(pǔ 60 钕(nǚ BaLaCePrNd 61 钷(pǒ 62钐(shān 63铕(yǒu 64 钆(gá 65铽(ta PmSmEuGdTb 66镝(dī 67钬(huǒ 68 铒(ěr 69铥(diū 70 镱(yì DyHoErTmYb 71镥(lǔ 72铪(hā 73 钽(tǎn 74钨(wū 75铼(lái LuHfTaWRe 76锇(? 77铱(yī 78铂(b? 79 金(jīn 80汞(gǒng OsIrPtAuHg 2
化学 元素符号表示的量
温州龙文教育 科学 学科导学案(第 次课) 教师: 邓云峰 学生: 年级: 九 日期:15. 星期: 时段: 课 题 化学 4 元素符号表示的量 教学目标 本节知识中计算相对分子质量、化合价中各元素质量比,以及一定量物质中某元素的质 量同现实生活结合起来考查,作为近几年中考命题中的热点,特别是关注社会热点和新闻报 道中的化学问题,以此为线索进行的命题设计是以信息为载体,以考查基础知识为目的的信 息迁移能力。 教学重点 相对分子质量、化合价中各元素质量比,以及一定量物质中某元素的质量计算 教学难点 相对分子质量、化合价中各元素质量比,以及一定量物质中某元素的质量计算 教学方法 基础知识点复习,考点精讲,讲练结合,课后巩固 学习内容与过程 第7节:元素符号表示的量(1) 【知识梳理】 1.相对原子质量 以一种碳原子(碳—12)的质量1/12作为标准,把其他原子的质量跟这个标准相比较所得的比值,叫做这种原子的相对的原子质量。 注意:根据最新国家计量标准,相对原子质量的单位符号为“1”,“1”不用明确写出,因此,相对质量是有单位的。以下的相对分子质量的单位也为“1”。 2.相对分子质量 化学式中各原子的相对原子质量的总和就是相对分子质量。 3.相对分子质量的典型计算 (1)CO 2的相对分子质量 =12+16×2=44; (2)2CO 2相对分子质量总和 =2(12+16×2)=88; (3)Ca(OH)2的相对分子质量 =40+(16+1)×2=74 (4)SO 42-的相对分子质量 =32+16×4=96; (5)CuSO 4·5H 2O 的相对分子质量 =64+32+16×4+5×(1×2+16)=250 相对原子质量=———————————— 一个该原子的质量 1/12(一个碳原子的质量) =—————————— 一个该原子的质量 1.661×10-27千克
实用文库汇编之初中化学常见的元素符号
*作者:角狂风* 作品编号:1547510232155GZ579202 创作日期:2020年12月20日 实用文库汇编之常见的元素符号: 氢氦锂铍硼,碳氮氧氟氖,钠镁铝硅磷,硫氯氩 钾钙。锰钡碘 H He Li Be B , C N O F Ne , Na Mg Al Si P , S Cl Ar K Ca 。Mn Ba I 金属活动性顺序:钾钙钠镁铝,锌铁锡铅氢铜汞银铂金 K Ca Na Mg Al, Zn Fe Sn Pb(H),Cu Hg Ag Pt Au 常见元素的化合价:金正,非负,单质零,氢+1,氧-2,正负总价和为零。 钾钠银氢+1价,钙镁钡锌+2价;氟氯溴碘-1 价,通常氧是-2价; 铜+1,+2铝+3;铁有+2,+3 硅+4; 2,4, 6硫 2,4碳; 氮磷-3,+5最常见;2,4,6,7锰变价;单 质中元素零价要记清。 化学式: 单质:氢气H2氧气O2氮气N2氯气Cl2氖气Ne碳 C 铜Cu铁Fe 化合物:氧化物:一氧化碳CO二氧化碳CO2五氧化 二磷P2O5 二氧化硫SO2二氧化锰MnO2三氧化二铁Fe2O3四 氧化三铁Fe3O4氧化亚铁FeO氧化镁MgO氧
化钙CaO三氧化二铝Al2O3氧化汞HgO 氧化铜CuO 酸:盐酸HCl硫酸H2SO4硝酸HNO3碳酸H2CO3磷酸H3PO4 碱:氢氧化钠NaOH氢氧化钙Ca(OH)2氢氧化钡Ba(OH)2氢氧化钾KOH 氢氧化铁(红褐色)Fe(OH)3氢氧化铜(蓝色)Cu(OH)2盐:氯化钠NaCl氯化镁MgCl2氯化铝AlCl3氯化钾 KCl氯化铁FeCl3氯化亚铁FeCl2氯化锌ZnCl2 氯化钡BaCl2氯化铜CuCl2氯化银AgCl (盐酸盐) 碳酸钙CaCO3碳酸钠Na2CO3碳酸钾K2CO3碳酸钡BaCO3 硫酸亚铁FeSO4硫酸铁Fe2(SO4)3硫酸钠Na2SO4硫酸镁MgSO4 硫酸铝Al2(SO4)3硫酸铜CuSO4硫酸锌ZnSO4硫酸钡BaSO4 硝酸银AgNO3硝酸汞Hg(NO3)2硝酸锌Zn(NO3)2 硝酸钡Ba(NO3)2 硝酸铝Al(NO3)3硝酸铁Fe(NO3)3硝酸铜Cu(NO3)2
初三化学元素周期表及符号知识点学习
初三化学元素周期表及符号知识点学习 元素符号是打开化学之门的第一把钥匙,是学习化学不可缺少的工具,它将直接关系到今后学习化学式、化学方程式等化学用语的书写和运用,必须熟练掌握,下面就元素符号的学习谈谈看法。 一、明确元素符号定义:表示元素的拉丁文符号,是国际通用的。 二、了解元素符号表示的意义:元素符号表示一种元素,还表示这种元素的一个原子。 三、注意元素符号的书写:用元素的拉丁文名称的第一个大写字母表示元素,当几种元素的拉丁文名称的第一个字母相同时,就用附加元素拉丁文名称的另一个小写字母的方法来表示。如钙、铜、氯的拉丁文第一个字母都是C,为了以示区别,分别在第一个大写字母C的后面附加了小写的a、u、l即组成了钙(Ca)、铜(Cu)、氯(Cl)的元素符号,当一种元素由两种符号组成时,书写时应遵循先大后小、高低有序的原则,即前面一个符号一定要写大写字母,后一个符号一定要写小写字母。如钴元素只能写成Co不能写成CO,镁元素只能写面Mg不能写成mg或MG。 四、掌握记忆元素符号的方法:刚刚学习化学的同学,总觉得元素符号特别难记,很零散,没有规律,怎样能熟记元素符号呢?下面介绍两类方法供参考。
(一)分散识记 元素符号的系统学习安排在教材第二章第三节,为了减轻元素符号集中识记的负担,可从第一节绪言课开始,对所接触到的元素符号进行分散识记,如绪言课中就可识记:镁(Mg)、铜(Cu)、碳(C)、氢(H)、氧(O);学习空气时,就识记氮(N)、氦(He)、氖(Ne)、氩(Ar)等;学习氧气的性质制法时就记住氯(Cl)、钾(K)、锰(Mg)、硫(S)、磷(P)、铁(Fe)等,以后每学一节就识记几种,这样积少成多,元素符号学习就会水到渠成。
人教版初中化学讲义——8元素、元素符号与元素周期表
授课内容 T 元素 C 元素符号 T 元素周期表简介 教学目的与目标 1、了解元素的概念及元素符号所代表的意义,学会看元素周期表 2、通过联想记忆,认识和记忆元素符号;通过元素周期表的学习,培养归纳总结的能力 3、通过元素学习进行从微观到宏观认识方法的教育,树立量变引起质变的辩证唯物主义观 教学内容 我们日常生活中所说的“加碘食盐”、“补钙”、“补锌”等,这里面的“碘、钙、锌”是指的什么呢? 从古到今,人们都在不断地探究世界上的万物是由什么组成的,在学习了原子和原子结构之后,我们也有了一定的了解。通过不断地科学探究证明,组成物质的基本成分就是元素,那我们这节课就开始探索元素的神秘之旅。 【元素】 1、概念:具有相同质子数(或核电荷数)的一类原子的总称。 注意:元素是一类原子的总称;这类原子的质子数相同 因此:元素的种类由原子的质子数决定,质子数不同,元素种类就不同。 (元素就像英文字母,虽然本身不是特别多,但却能组成百千 万的物质。) 2、元素的分布: ①地壳中含量前五位的元素:氧、硅、铝、铁、钙 ②空气中前二位的元素:氮、氧 知识梳理 课堂导入
③生物细胞中含有较多的元素:氧、碳、氢、氮 3、元素的分类:元素分为金属元素、非金属元素和稀有气体元素 4、原子、分子、元素、物质间的联系 5.原子和元素的区别与联系:
原子元素 区别1. 粒子(成员) 2. 既讲种类,又讲个数 3. 从微观角度描述分子的构成或物质的构成 1、粒子的总称(集体) 2. 只讲种类,不讲个数 3. 从宏观角度描述物质的组成 联系元素的概念建立在原子的基础上,原子的核电荷数(即核内的质子数)决定元素的种类相似化学反应前后元素和原子的种类都不会改变 1、豆类、动物肝脏中含有丰富的铁和锌,这里的“铁”、“锌”是指() A 原子B.分子C.元素D.单质 2、今有四种粒子的结构示意图,下列说法正确的是() A.它们表示四种元素 B.②离子有二个电子层 C.④表示的元素是非金属元素 D.①④表示的是阳离子 3、某原子结构示意图如图,有关它的说法错误的是() A.它的核内有12个质子 B.它属于非金属元素 C.它有3个电子层 D.它的最外层有2个电子 4、下列粒子(微粒)中不能直接构成物质的是() A.原子B.分子C.离子D.电子 基础演练
化学元素性质大全
化学元素性质大全
1H 原子序数:1 元素符号:H 元素中文名称:氢 元素英文名称:Hydrogen 相对原子质量:1.008 核内质子数:1 核外电子数:1 核电核数:1 质子质量:1.673E-27 质子相对质量:1.007 所属周期:1 所属族数:IA 摩尔质量:1 氢化物:无 氧化物:H2O 最高价氧化物:H2O 密度:0.08988 熔点:-259.14 沸点:-252.87
外围电子排布:1s1 核外电子排布:1 颜色和状态:无色气体 原子半径:0.79 常见化合价+1,-1 发现人:卡文迪许 发现时间和地点:1766 英格兰 元素来源:在地球上和地球大气中只存在极稀少的游离状态氢,锌与稀盐酸反映制取是一种办法,电解水方法。 元素用途:导热能力特别强,跟氧化合成水。氢气球。氢能源。 工业制法:电解水2H2O=O2+2H2 实验室制法:锌与稀盐酸反映Zn+2HCl=ZnCl2+H2 其他化合物:H2O-水H2S-硫化氢HCl-氯化氢HBr-氢溴酸H2SO4-硫酸NH3-氨气CH4-甲烷 扩展介绍:利用氢的同位素氘和氚的原子核聚变时产生的能进行杀伤和破坏的炸弹,其威力比原子弹大得多 2He 原子序数:2 元素符号:He 元素中文名称:氦 元素英文名称:Helium 相对原子质量:4.003 核内质子数:2 核外电子数:2 核电核数:2 质子质量:3.346E-27 质子相对质量:2.014 所属周期:1 所属族数:0 摩尔质量:4 氢化物: 氧化物: 密度:0.1785 熔点:-272.0 沸点:-268.6 外围电子排布:1s2 核外电子排布:2 颜色和状态:无色气体 原子半径:0.49 常见化合价:0 发现人:严森、洛克耶、拉姆塞、克利夫 发现时间和地点:1895 苏格兰/瑞典 元素来源:存在于整个宇宙中
2020年常用化学元素符号表
作者:非成败 作品编号:92032155GZ5702241547853215475102 时间:2020.12.13 常用分子式 氮气:N2氢气:H2甲烷:CH4氧气:O2 氨:NH3水:H2O 一氧化碳:CO 二氧化碳:CO2 硫:S 二氧化硫:SO2硫代硫酸钠:Na2S2O3 铁:Fe 二价铁离子:Fe2+三价铁离子:Fe3+硫酸钠:Na2SO4磷酸三钠:Na3PO4碳酸钠:Na2CO3 碳酸钙:CaCO3碳酸氢钠:NaHCO3氢氧化钠:NaOH 盐酸:HCL 碳酸氢铵:NH4HCO3硝酸:HNO3
硫酸:H2SO4尿素:CO(NH2) 碳酸:H2CO3 化学需氧量:COD 高锰酸钾:KMnO4锰酸钾:K2MnO4 缩二尿:NH2CONHCONH2硝酸银:AgNO3硫酸铜:CuSO4 碳酸丙稀脂(碳丙液):C3H6CO3甲醇:CH3OH 乙醇:CH3CH2OH 甲醛:HCHO 一甲氨:NH2CH3二甲氨:NH(CH3)2 三甲氨:N(CH3)3 三氧化二铝:AL2O3三氧化二铁:Fe2O3 氧化铜:CuO 氯化钠:NaCL 一、初中化学常见混合物的重要成分 1、空气:氮气(N2)和氧气(O2) 2、水煤气:一氧化碳(CO)和氢气(H2) 3、煤气:一氧化碳(CO) 4、天然气:甲烷(CH4) 5、石灰石/大理石:(CaCO3) 6、生铁/钢:(Fe) 7、木炭/焦炭/炭黑/活性炭:(C) 8、铁锈:(Fe2O3) 二、初中化学常见物质俗称 1、氯化钠(NaCl):食盐 2、碳酸钠(Na2CO3) :纯碱,苏打,口碱 3、氢氧化钠(NaOH):火碱,烧碱,苛性钠 4、氧化钙(CaO):生石灰 5、氢氧化钙(Ca(OH)2):熟石灰,消石灰 6、二氧化碳固体(CO2):干冰 7、氢氯酸(HCl):盐酸 8、碱式碳酸铜(Cu2(OH)2CO3):铜绿 9、硫酸铜晶体(CuSO4 .5H2O):蓝矾,胆矾 10、甲烷(CH4):沼气 11、乙醇(C2H5OH):酒精 12、乙酸(CH3COOH):醋酸 13、过氧化氢(H2O2):双氧水 14、汞(Hg):水银 15、碳酸氢钠(NaHCO3):小苏打 三、物质的除杂
常用化学元素符号表.
常用化学元素符号 常用分子式 氮气:N2氢气:H2甲烷:CH4氧气:O2 氨:NH3水:H2O 一氧化碳:CO 二氧化碳:CO2硫:S 二氧化硫:SO2硫代硫酸钠:Na2S2O3 铁:Fe 二价铁离子:Fe2+三价铁离子:Fe3+硫酸钠:Na2SO4磷酸三钠:Na3PO4碳酸钠:Na2CO3 碳酸钙:CaCO3碳酸氢钠:NaHCO3氢氧化钠:NaOH 盐酸:HCL 碳酸氢铵:NH4HCO3硝酸:HNO3 硫酸:H2SO4尿素:CO(NH2) 碳酸:H2CO3
化学需氧量:COD 高锰酸钾:KMnO4锰酸钾:K2MnO4缩二尿:NH2CONHCONH2硝酸银:AgNO3硫酸铜:CuSO4碳酸丙稀脂(碳丙液):C3H6CO3甲醇:CH3OH 乙醇:CH3CH2OH 甲醛:HCHO 一甲氨:NH2CH3二甲氨:NH(CH3)2三甲氨:N(CH3)3三氧化二铝:AL2O3三氧化二铁:Fe2O3 氧化铜:CuO 氯化钠:NaCL
1 H 氢1.0079化学元素周期表 2 He 氦 4.0026 3 Li 锂6.941 4 Be 铍 9.0122 5 B 硼 10.811 6 C 碳 12.011 7 N 氮 14.007 8 O 氧 15.999 9 F 氟 18.998 10 Ne 氖 20.17 11 Na 钠22.989812 Mg 镁 24.305 13 Al 铝 26.982 14 Si 硅 28.085 15 P 磷 30.974 16 S 硫 32.06 17 Cl 氯 35.453 18 Ar 氩 39.94 19 K 钾39.09820 Ca 钙 40.08 21 Sc 钪 44.956 22 Ti 钛 47.9 23 V 钒 50.9415 24 Cr 铬 51.996 25 Mn 锰 54.938 26 Fe 铁 55.84 27 Co 钴 58.9332 28 Ni 镍 58.69 29 Cu 铜 63.54 30 Zn 锌 65.38 31 Ga 镓 69.72 32 Ge 锗 72.5 33 As 砷 74.922 34 Se 硒 78.9 35 Br 溴 79.904 36 Kr 氪 83.8 37 Rb 铷85.46738 Sr 锶 87.62 39 Y 钇 88.906 40 Zr 锆 91.22 41 Nb 铌 92.9064 42 Mo 钼 95.94 43 Tc 锝 (99) 44 Ru 钌 161.0 45 Rh 铑 102.906 46 Pd 钯 106.42 47 Ag 银 107.868 48 Cd 镉 112.41 49 In 铟 114.82 50 Sn 锡 118.6 51 Sb 锑 121.7 52 Te 碲 127.6 53 I 碘 126.905 54 Xe氙 131.3 55 Cs 铯132.905 56 Ba 钡 137.33 57-71 La-Lu 镧系 72 Hf 铪 178.4 73 Ta 钽 180.947 74 W 钨 183.8 75 Re 铼 186.207 76 Os 锇 190.2 77 Ir 铱 192.2 78 Pt 铂 195.08 79 Au 金 196.967 80 Hg 汞 200.5 81 Tl 铊 204.3 82 Pb 铅 207.2 83 Bi 铋 208.98 84 Po 钋 (209) 85 At 砹 (201) 86 Rn 氡 (222) 87 Fr 钫(223) 88 Ra 镭 226.03 89-103 Ac-Lr 锕系 104 (261) 105 (262) 106 (263) 107 (262) 108 (265) 109 (266)
化学元素表带拼音
第02 号元素: 氦[化学符号]He, 读“亥”第03 号元素: 锂[化学符号]Li, 读“里”第04 号元素: 铍[化学符号]Be, 读“皮”第05 号元素: 硼[化学符号]B, 读“朋” 第06 号元素: 碳[化学符号]C, 读“炭” 第07 号元素: 氮[化学符号]N, 读“淡” 第08 号元素: 氧[化学符号]O, 读“养” 第09 号元素: 氟[化学符号]F, 读“弗” 第10 号元素: 氖[化学符号]Ne, 读“乃”第11 号元素: 钠[化学符号]Na, 读“纳”第12 号元素: 镁[化学符号]Mg, 读“美”第13 号元素: 铝[化学符号]Al, 读“吕”第14 号元素: 硅[化学符号]Si, 读“归”第15 号元素: 磷[化学符号]P, 读“邻” 第16 号元素: 硫[化学符号]S, 读“流” 第17 号元素: 氯[化学符号]Cl, 读“绿”第18 号元素: 氩[化学符号]Ar,A, 读“亚”第19 号元素: 钾[化学符号]K, 读“甲” 第20 号元素: 钙[化学符号]Ca, 读“丐”第21 号元素: 钪[化学符号]Sc, 读“亢”第22 号元素: 钛[化学符号]Ti, 读“太”第23 号元素: 钒[化学符号]V, 读“凡”
第25 号元素: 锰[化学符号]Mn, 读“猛”第26 号元素: 铁[化学符号]Fe, 读“铁”第27 号元素: 钴[化学符号]Co, 读“古”第28 号元素: 镍[化学符号]Ni, 读“臬”第29 号元素: 铜[化学符号]Cu, 读“同”第30 号元素: 锌[化学符号]Zn, 读“辛”第31 号元素: 镓[化学符号]Ga, 读“家”第32 号元素: 锗[化学符号]Ge, 读“者”第33 号元素: 砷[化学符号]As, 读“申”第34 号元素: 硒[化学符号]Se, 读“西”第35 号元素: 溴[化学符号]Br, 读“秀”第36 号元素: 氪[化学符号]Kr, 读“克”第37 号元素: 铷[化学符号]Rb, 读“如”第38 号元素: 锶[化学符号]Sr, 读“思”第39 号元素: 钇[化学符号]Y, 读“乙”第40 号元素: 锆[化学符号]Zr, 读“告”第41 号元素: 铌[化学符号]Nb, 读“尼”第42 号元素: 钼[化学符号]Mo, 读“目”第43 号元素: 碍[化学符号]Tc, 读“得”第44 号元素: 钌[化学符号]Ru, 读“了”第45 号元素: 铑[化学符号]Rh, 读“老”第46 号元素: 钯[化学符号]Pd, 读“巴”
初中化学元素符号顺口溜和记忆口诀
20个必记:氢氦锂铍硼碳氮氧氟氖钠镁铝硅磷硫氯氩钾钙(5个一记会好记点)
一、实验操作 1、粉末状药品的取用 粉末药品药匙取,也可倒在纸槽里; 横放试管送底部,直立试管落到低。 或:一斜二送三直立。 2、块状药品的取用 块状药品镊子夹,绝对不能手来拿; 横持试管把药放,慢慢竖起向下滑。 或:一横二放三慢竖。 3、液体药品的取用 取下瓶塞倒放桌,标签朝心右手握; 口口紧挨要倾斜,倒完液体原处搁。 4、液体药品的量取 量筒平放实验桌,先倒后滴至刻度; 平视凹液最低处,三线一齐为读数。
或:一倒二滴三读数。 5、用滴管取用药品 轻拿滴管胶头处,手捏滴管橡胶头; 垂直滴入容器中,切忌管头触器口。 或:两管直立,莫触内壁; 滴管悬空,滴入正中。 6、托盘天平的使用 天平用前调零点,左物右码记心间; 砝码要用镊子夹,由大到小顺序拿; 一般药品垫纸称,腐蚀药品杯中放; 称完天平要复原,游码移回到零点。 或:一放平、二调零,三加砝码四进行; 砝码要用镊子取,左物右码须记清。 7、酒精灯的使用 酒精不能燃着加,对火可能危险发; 酒精灯焰分三层,外焰温度为最大; 熄灯要用灯帽盖,切记嘴吹酿火灾; 万一失火燃起来,抹布立刻来扑盖。 8、试管中的固体加热 药品斜铺试管底,受热均匀面积大; 管口略比管底低,防水倒流试管炸; 试管夹持中上部,根据外焰定高度; 均匀预热试管后,集中外焰把热加。 9、试管中的液体加热 加热常用试管夹,夹在试管中上部; 试管加液三分一,药液体积不超它; 移动试管预热前,应把外壁水擦干; 管口不朝你我他,四十五度为最佳。 10、仪器的洗涤 一般容器用水洗,内壁附物用刷洗; 壁内若有不溶物,盐酸溶碱纯碱脂; 仪器洗净有标准,水不成股不聚滴。 二、前二十种元素 氢氦锂铍硼,碳氮氧氟氖; 钠镁铝硅磷,硫氯氩钾钙。 三、常见元素的化合价 (一) 钾钠银氢正一价,钙镁钡锌正二价; 一二铜汞二三铁,三铝四硅五氮磷; 二四六硫二四碳,金正非负单质零。 (二) 一价钾钠银氢氟,二价钙镁和钡锌; 铝价正三氧负二,以上价态要记真; 铜一二来铁二三,碳硅二四要记全;
化学元素符号
初高中衔接------- (一) -----常见的元素符号 【课程标准与考试要求】学会常见的元素符号的写法,记住一些常见的元素符号。 【学习目标】1、学会常见的元素符号的写法。 2、了解元素符号所表示的意义。 【重、难点】认识并正确书写常见的元素符号 【预习案】 【教材自学】元素符号 (1)通过阅读教材,请同学们写出1-20号元素的元素符号: (2)意义:①表示一种;②表示这种元素的。 ③对于金属、固体非金属、稀有气体的元素符号还表示。 例:N表示的意义有:和。 例:Fe表示的意义有:和、。 如果在元素符号前面添加系数,就只表示该元素的原子个数,不能表示该元素。如H既表示氢元素又能表示一个氧原子,而2H只能表示;3Fe表示;若要表示5个 镁原子可记为:,7个氯原子可记为: 【微课助学】 观看微视频《元素符号书写规则》,填写下表。 【在线测学】预习结束后,通过平板电脑完成本课的“预习自测”。 【自学反思】 我的 收获 我的 疑问
( ) 【探究案】 1、试写出下列物质的元素符号:钒、铬、锰、钡、镍、溴、碘、钨、锡、砷 2、试写出金属的活动性顺序的元素符号及汉字: 【归纳小结】回顾本节所学知识,归纳知识结构。 【训练案】 1、下列符号中,既能表示某种元素及该元素的一个原子,还能表示某种物质的是() A、H B、Al C、Fe3+ D、N2 2.下列符号中,表示一个原子,又表示一种元素,还表示一种物质的是() A.C60 B.2H C.2N2 D.Fe 3.下列符号中,表示2个氢原子的是() A.H2 B.2H C.H2O D.2H2 4. 指出下列各符号的意义: N 2N H2 5.用化学符号表示: 2个氯气分子:,氮气:, 2个铝原子:_________; 4个硫酸分子:,氧元素:,3个氧分子:________; 【自我反思】 我的 收获 我的 疑问
