家教专用1111化学公式定理大全9(化学反应速率_化学平衡)

1.化学反应速率
[化学反应速率的概念及其计算公式]
(1)概念:化学反应速率是用来衡量化学反应进行的快慢程度,通常用单位时间内反应物浓度的减少或生成物浓度的增加来表示.单位有mol ·L -
1·min
-1
或mol ·L -
1·s -
1
(2)计算公式:某物质X 的化学反应速率:
))
或时间变化量()
的浓度变化量(m in )(1s L mol X X -?=
ν 注意 ①化学反应速率的单位是由浓度的单位(mol ·L -
1)和时间的单位(s 、min 或h)决定的,可以是
mol ·L -
1·s -
1、mol ·L -
1·min
-1
或mol ·L -
1·h -
1,在计算时要注意保持时间单位的一致性.
②对于某一具体的化学反应,可以用每一种反应物和每一种生成物的浓度变化来表示该反应的化学反应速率,虽然得到的数值大小可能不同,但用各物质表示的化学反应速率之比等于化学方程式中相应物质的化学计量数之比.如对于下列反应: mA + nB = pC + qD
有:)(A ν∶)(B ν∶)(C ν∶)(D ν=m ∶n ∶p ∶q 或:
q
D p
C n
B m
A )
()
()
()
(νννν=
=
=
③化学反应速率不取负值而只取正值.
④在整个反应过程中,反应不是以同样的速率进行的,因此,化学反应速率是平均速率而不是瞬时速率.
[有效碰撞] 化学反应发生的先决条件是反应物分子(或离子)之间要相互接触并发生碰撞,但并不是反应物分子(或离子)间的每一次碰撞都能发生化学反应.能够发生化学反应的一类碰撞叫做有效碰撞.
[活化分子] 能量较高的、能够发生有效碰撞的分子叫做活化分子.
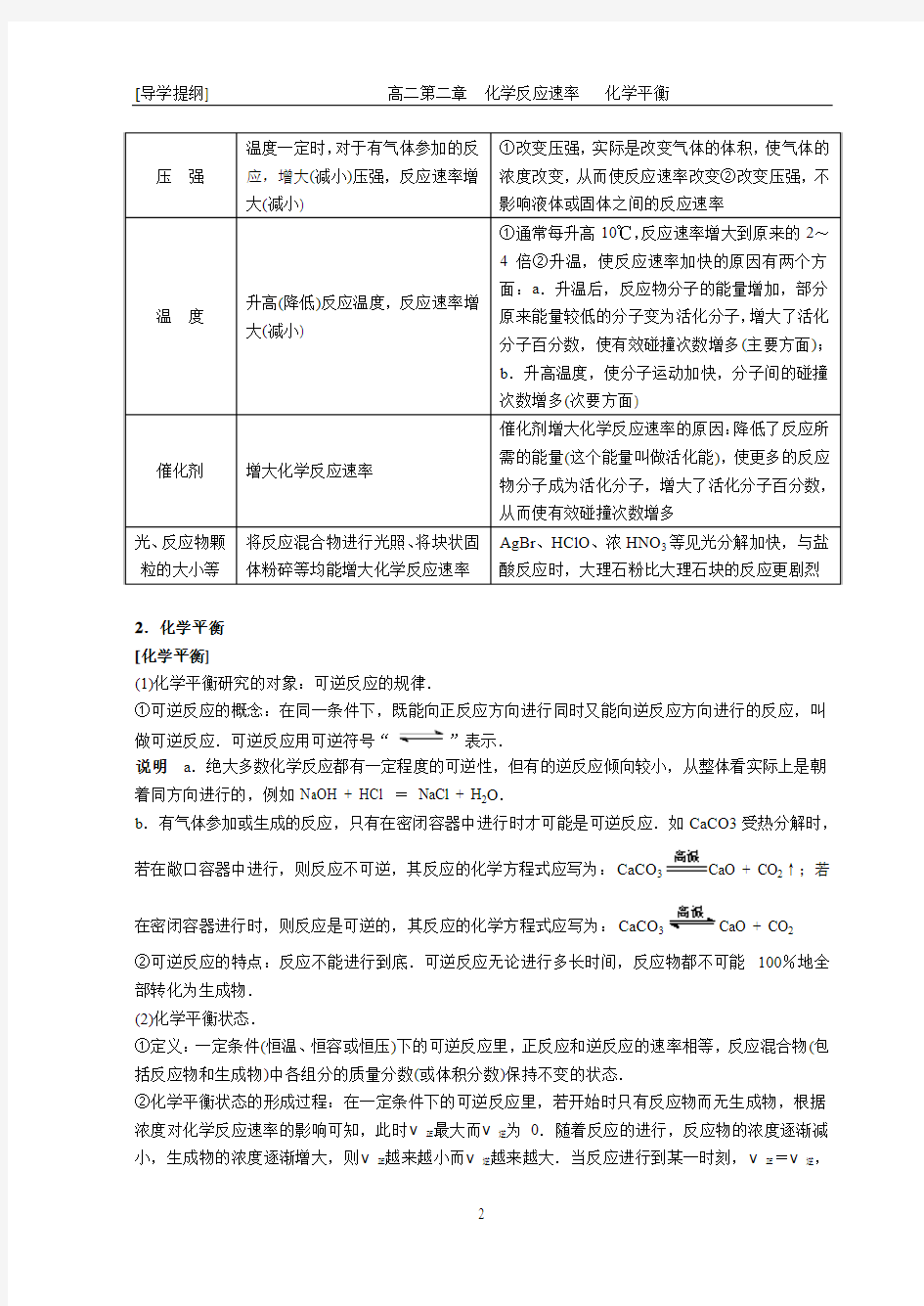
说明 ①活化分子不一定能够发生有效碰撞,活化分子在碰撞时必须要有合适的取向才能发生有效碰撞.②活化分子在反应物分子中所占的百分数叫做活化分子百分数.当温度一定时,对某一反应而言,活化分子百分数是一定的.活化分子百分数越 大,活化分子数越多,有效碰撞次数越多. [影响化学反应速率的因素]
2.化学平衡 [化学平衡]
(1)化学平衡研究的对象:可逆反应的规律.
①可逆反应的概念:在同一条件下,既能向正反应方向进行同时又能向逆反应方向进行的反应,叫
说明 a .绝大多数化学反应都有一定程度的可逆性,但有的逆反应倾向较小,从整体看实际上是朝着同方向进行的,例如NaOH + HCl = NaCl + H 2O .
b .有气体参加或生成的反应,只有在密闭容器中进行时才可能是可逆反应.如CaCO3受热分解时,若在敞口容器中进行,则反应不可逆,其反应的化学方程式应写为:CaCO 3CaO + CO 2↑;若在密闭容器进行时,则反应是可逆的,其反应的化学方程式应写为:CaCO 3
CaO + CO 2
②可逆反应的特点:反应不能进行到底.可逆反应无论进行多长时间,反应物都不可能100%地全部转化为生成物. (2)化学平衡状态.
①定义:一定条件(恒温、恒容或恒压)下的可逆反应里,正反应和逆反应的速率相等,反应混合物(包括反应物和生成物)中各组分的质量分数(或体积分数)保持不变的状态.
②化学平衡状态的形成过程:在一定条件下的可逆反应里,若开始时只有反应物而无生成物,根据浓度对化学反应速率的影响可知,此时ν正
最大而ν
逆
为0.随着反应的进行,反应物的浓度逐渐减
小,生成物的浓度逐渐增大,则ν
正
越来越小而ν逆
越来越大.当反应进行到某一时刻,ν正
=ν
逆
,
各物质的浓度不再发生改变,反应混合物中各组分的质量分数(或体积分数)也不再发生变化,这时就达到了化学平衡状态.
(3)化学平衡的特征:
①“动”:化学平衡是动态平衡,正反应和逆反应仍在继续进行,即ν正=ν逆≠0.
②“等”:达平衡状态时,ν正=ν逆,这是一个可逆反应达平衡的本质.ν正=ν逆的具体含意包含两个方面:a.用同一种物质来表示反应速率时,该物质的生成速率与消耗速率相等,即单位时间内消耗与生成某反应物或生成物的量相等;b.用不同物质来表示时,某一反应物的消耗速率与某一生成物的生成速率之比等于化学方程式中相应物质的化学计量数之比.
③“定”:达平衡时,混合物各组分的浓度一定;质量比(或物质的量之比、体积比)一定;各组分的质量分数(或摩尔分数、体积分数)一定;对于有颜色的物质参加或生成的可逆反应,颜色不改变.同时,反应物的转化率最大.
对于反应前后气体分子数不相等的可逆反应,达平衡时:气体的总体积(或总压强)一定;气体的平均相对分子质量一定;恒压时气体的密度一定(注意:反应前后气体体积不变的可逆反应,不能用这个结论判断是否达到平衡).
④“变”.一个可逆反应达平衡后,若外界条件(浓度、温度、压强)改变,使各组分的质量(体积、摩尔、压强)分数也发生变化,平衡发生移动,直至在新的条件下达到新的平衡(注意:若只是浓度或压强改变,而ν正仍等于ν逆,则平衡不移动).反之,平衡状态不同的同一个可逆反应,也可通过改变外界条件使其达到同一平衡状态.
⑤化学平衡的建立与建立化学平衡的途径无关.对于一个可逆反应,在一定条件下,反应无论从正反应开始,还是从逆反应开始,或是正、逆反应同时开始,最终都能达到同一平衡状态.具体包括:a.当了T、V一定时,按化学方程式中各物质化学式前系数的相应量加入,并保持容器内的总质量不变,则不同起始状态最终可达到同一平衡状态.
b.当T、P一定(即V可变)时,只要保持反应混合物中各组分的组成比不变(此时在各种情况下各组分的浓度仍然相等,但各组分的物质的量和容器内的总质量不一定相等),则不同的起始状态最终也可达到同一平衡状态.
如在恒温、恒压时,对于可逆反应:N2 + 3H3,在下列起始量不同情况下达到的是同一平衡状态.
c.对于反应前后气体体积相等的可逆反应,不论是恒温、恒容或是恒温、恒压,在不同的起始状态下,将生成物“归零”后,只要反应物的物质的量之比不变,就会达到同一平衡状态.
如:H2(g) + I2(g) 等.
[判断化学平衡状态的依据]
高中物理公式定理定律知识点整理归纳
高中物理公式定理定律知识点整理归纳 高中物理公式定理定律知识点整理归纳 一、质点的运动------直线运动 1)匀变速直线运动 1.平均速度v平=s/t(定义式) 2.有用推论vt2-vo2=2as 3.中间时刻速度vt/2=v平=(vt+vo)/2 4.末速度vt=vo+at 5.中间位置速度vs/2=[(vo2+vt2)/2]1/2 6.位移s=v平 t=vot+at2/2=vt/2t 7.加速度a=(vt-vo)/t{以vo为正方向,a与vo同向(加速)a>0;反向则a<0} 8.实验用推论δs=at2{δs为连续相邻相等时间(t)内位移之差} 9.主要物理量及单位:初速度(vo):m/s;加速度(a):m/s2;末速度(vt):m/s;时间(t)秒(s);位移(s):米(m);路程:米;速度单位换 算:1m/s=3.6km/h。 注:(1)平均速度是矢量;(2)物体速度大,加速度不一定 大;(3)a=(vt-vo)/t只是量度式,不是决定式; (4)其它相关内容:质点.位移和路程.参考系.时间与时刻;速度与速率.瞬时速度。 2)自由落体运动 1.初速度vo=0 2.末速度vt=gt 3.下落高度h=gt2/2(从vo位置向 下计算)4.推论vt2=2gh 注:(1)自由落体运动是初速度为零的匀加速直线运动,遵循匀变速直线运动规律;
(2)a=g=9.8m/s2≈10m/s2(重力加速度在赤道附近较小,在高山处比平地小,方向竖直向下)。 (3)竖直上抛运动 1.位移s=vot-gt2/2 2.末速度vt=vo-gt(g=9.8m/s2≈10m/s2) 3.有用推论vt2-vo2=-2gs 4.上升最大高度hm=vo2/2g(抛出点算起) 5.往返时间t=2vo/g(从抛出落回原位置的时间) 注: (1)全过程处理:是匀减速直线运动,以向上为正方向,加速度取负值; (2)分段处理:向上为匀减速直线运动,向下为自由落体运动,具有对称性; (3)上升与下落过程具有对称性,如在同点速度等值反向等。 二、质点的运动----曲线运动、万有引力 1)平抛运动 1.水平方向速度:vx=vo 2.竖直方向速度:vy=gt 3.水平方向位移:x=vot 4.竖直方向位移:y=gt2/2 5.运动时间t=(2y/g)1/2(通常又表示为(2h/g)1/2) 6.合速度vt=(vx2+vy2)1/2=[vo2+(gt)2]1/2 合速度方向与水平夹角β:tgβ=vy/vx=gt/v0 7.合位移:s=(x2+y2)1/2, 位移方向与水平夹角α:tgα=y/x=gt/2vo 8.水平方向加速度:ax=0;竖直方向加速度:ay=g
高级中学数学公式定理汇总
高中数学公式结论大全 1. ,. 2.. 3. 4.集合的子集个数共有个;真子集有个;非空子集有个;非空的真子集有 个. 5.二次函数的解析式的三种形式 (1)一般式; (2)顶点式;当已知抛物线的顶点坐标时,设为此式 (3)零点式;当已知抛物线与轴的交点坐标为时,设为此式 4切线式:。当已知抛物线与直线相切且切点的横坐标为时,设为此式 6.解连不等式常有以下转化形式 . 7.方程在内有且只有一个实根,等价于或。 8.闭区间上的二次函数的最值 二次函数在闭区间上的最值只能在处及区间的两端点处取得,具体如下:
(1)当a>0时,若,则; ,,. (2)当a<0时,若,则, 若,则,. 9.一元二次方程=0的实根分布 1方程在区间内有根的充要条件为或; 2方程在区间内有根的充要条件为 或或; 3方程在区间内有根的充要条件为或 . 10.定区间上含参数的不等式恒成立(或有解)的条件依据 (1)在给定区间的子区间形如,,不同上含参数的不等式(为参数)恒成立的充要条件是。 (2)在给定区间的子区间上含参数的不等式(为参数)恒成立的充要条件是 。
(3) 在给定区间 的子区间上含参数的不等式(为参数)的有解充要条件是 。 (4) 在给定区间 的子区间上含参数的不等式(为参数)有解的充要条件是 。 对于参数及函数.若恒成立,则;若恒成立,则;若有解,则 ;若 有解,则 ;若 有解,则 . 若函数无最大值或最小值的情况,可以仿此推出相应结论 11.真值表 12.常见结论的否定形式 原结论 反设词 原结论 反设词 是 不是 至少有一个 一个也没有 都是 不都是 至多有一个 至少有两个 大于 不大于 至少有个 至多有个 小于 不小于 至多有个 至少有 个 对所有,成立 存在某,不成立 或 且 对任何,不成立 存在某,成立 且 或 p q 非p p或q p且q 真 真 假 真 真 真 假 假 真 假 假 真 真 真 假 假 假 真 假 假
高中化学定律公式
高中化学定律和公式 一、物质的量的单位——摩尔 物质的量实际上表示含有一定数目粒子的集体。它的符号是n 。 我们把含有×1023个粒子的任何粒子集体计量为1摩尔,摩尔简称摩,符号mol 。 物质的量(n )、粒子个数(N )和阿伏加德罗常数(A N )三者之间的关系用符号表示:n= A N N (1)定义:单位物质的量的物质所具有的质量叫做摩尔质量。符号M 。 物质的量(n )、物质的质量(m)和摩尔质量(M )三者间的关系: 3.物质的量(mol )= 1()()g g mol 物质的质量摩尔质量 符号表示:n=M m 在相同条件下(同温、同压)物质的量相同的气体,具有相同的体积。在标准状况下(0 ℃、101 kPa)1 mol 任何气体的体积都约是 L 。 1.气体摩尔体积 单位物质的量的气体所占的体积叫气体摩尔体积。符号为m V m V V n (V 为标准状况下气体的体积,n 为气体的物质的量) 单位:L/mol 或(L·mol -1) m 3/mol 或(m 3·mol -1)
定义:以单位体积溶液里所含溶质B 的物质的量来表示的溶液组成的物理量,叫做溶质B 的物质的量浓度。用符号B C 表示,单位mol·L -1(或mol/L )。表达式:B B n C V =
c(浓溶液)·V(浓溶液)=c(稀溶液)·V(稀溶液) 1、 原子核的构成 原子是由原子中心的原子核和核外电子组成,而核外电子是由质子和中子组成。 1个电子带一个单位负电荷;中子不带电;1个质子带一个单位正电荷 核电荷数(Z) == 核内质子数 == 核外电子数 == 原子序数 2、质量数 将原子核内所有的质子和中子的相对质量取近似整数值加起来,所得的数值,叫质量数。 质量数(A )= 质子数(Z )+ 中子数(N )==近似原子量 X A Z ——元素符号 质量数——核电荷数——(核内质子数)表示原子组成的一种方法 a ——代表质量数; b ——代表质子数既核 电荷数; c ——代表离子的所带电荷数; d ——代表化合价 e ——代表原子个数 请看下列表示 a b +d X c+e 3、 阳离子 aW m+ :核电荷数=质子数>核外电子数,核外电子数=a -m 阴离子 b Y n-:核电荷数=质子数<核外电子数,核外电子数=b +n
高中数学《立体几何》重要公式、定理
高中数学《立体几何》重要公式、定理 1.证明直线与平面的平行的思考途径 (1)转化为直线与平面无公共点; (2)转化为线线平行; (3)转化为面面平行. 2.证明直线与直线的平行的思考途径 (1)转化为判定共面二直线无交点; (2)转化为二直线同与第三条直线平行; (3)转化为线面平行; (4)转化为线面垂直; (5)转化为面面平行. 3.证明直线与直线的垂直的思考途径 (1)转化为相交垂直; (2)转化为线面垂直; (3)转化为线与另一线的射影垂直; (4)转化为线与形成射影的斜线垂直. 4.证明直线与平面垂直的思考途径 (1)转化为该直线与平面内任一直线垂直; (2)转化为该直线与平面内相交二直线垂直; (3)转化为该直线与平面的一条垂线平行; (4)转化为该直线垂直于另一个平行平面; (5)转化为该直线与两个垂直平面的交线垂直. 5.证明平面与平面平行的思考途径 (1)转化为判定二平面无公共点; (2)转化为线面平行; (3)转化为线面垂直. 6.证明平面与平面的垂直的思考途径 (1)转化为判断二面角是直二面角; (2)转化为线面垂直. 7.空间向量的加法与数乘向量运算的运算律 (1)加法交换律:a +b=b +a . (2)加法结合律:(a +b)+c=a +(b +c). (3)数乘分配律:λ(a +b)=λa +λb . 8.共线向量定理 对空间任意两个向量a 、b(b ≠0 ),a ∥b ?存在实数λ使a=λb . P A B 、、三点共线?||AP AB ?AP t AB =?(1)OP t OA tOB =-+. ||AB CD ?AB 、CD 共线且AB CD 、不共线?AB tCD =且AB CD 、不共线. 9.共面向量定理 向量p 与两个不共线的向量a 、b 共面的?存在实数对,x y ,使p ax by =+. 推论 空间一点P 位于平面MAB 内的?存在有序实数对,x y ,使MP xMA yMB =+, 或对空间任一定点O ,有序实数对,x y ,使OP OM xMA yMB =++. 10.平面向量加法的平行四边形法则向空间的推广 始点相同且不在同一个平面内的三个向量之和,等于以这三个向量为棱的平行六面体的以公共始点为始点的对角 线所表示的向量. 11.对空间任一点O 和不共线的三点A 、B 、C ,满足OP xOA yOB zOC =++(x y z k ++=),则当1k =时,对于空间任一点O ,总有P 、A 、B 、C 四点共面;当1 k ≠
高中物理公式定理定律
高中物理公式定理定律 一、质点的运动(1)------直线运动 1)匀变速直线运动 1.平均速度V平=s/t(定义式) 2.有用推论Vt2-Vo2=2as 3.中间时刻速度Vt/2=V平=(Vt+Vo)/2 4.末速度Vt=Vo+at 5.中间位置速度Vs/2=[(Vo2+Vt2)/2]1/2 6.位移s=V平t=Vot+at2/2=Vt/2t 7.加速度a=(Vt-Vo)/t {以Vo为正方向,a与Vo同向(加速)a>0;反向则a<0} 8.实验用推论Δs=aT2 {Δs为连续相邻相等时间(T)内位移之差} 9.主要物理量及单位:初速度(Vo):m/s;加速度(a):m/s2;末速度(Vt):m/s;时间(t)秒(s);位移(s):米(m);路程:米;速度单位换算:1m/s=3.6km/h。 注: (1)平均速度是矢量; (2)物体速度大,加速度不一定大; (3)a=(Vt-Vo)/t只是量度式,不是决定式; (4)其它相关内容:质点、位移和路程、参考系、时间与时刻〔见第一册P19〕/s--t图、v--t 图/速度与速率、瞬时速度〔见第一册P24〕。 2)自由落体运动 1.初速度Vo=0 2.末速度Vt=gt 3.下落高度h=gt2/2(从Vo位置向下计算) 4.推论Vt2=2gh 注: (1)自由落体运动是初速度为零的匀加速直线运动,遵循匀变速直线运动规律; (2)a=g=9.8m/s2≈10m/s2(重力加速度在赤道附近较小,在高山处比平地小,方向竖直向下)。 (3)竖直上抛运动 1.位移s=Vot-gt2/2 2.末速度Vt=Vo-gt (g=9.8m/s2≈10m/s2) 3.有用推论Vt2-Vo2=-2gs 4.上升最大高度Hm=Vo2/2g(抛出点算起) 5.往返时间t=2Vo/g (从抛出落回原位置的时间) 注: (1)全过程处理:是匀减速直线运动,以向上为正方向,加速度取负值; (2)分段处理:向上为匀减速直线运动,向下为自由落体运动,具有对称性; (3)上升与下落过程具有对称性,如在同点速度等值反向等。 二、质点的运动(2)----曲线运动、万有引力 1)平抛运动 1.水平方向速度:Vx=Vo 2.竖直方向速度:Vy=gt 3.水平方向位移:x=Vot 4.竖直方向位移:y=gt2/2 5.运动时间t=(2y/g)1/2(通常又表示为(2h/g)1/2) 6.合速度Vt=(Vx2+Vy2)1/2=[Vo2+(gt)2]1/2 合速度方向与水平夹角β:tgβ=Vy/Vx=gt/V0
化学平衡状态
考纲要求 1.了解化学反应的可逆性及化学平衡的建立。2.掌握化学平衡的特征。3.理解外界条件(浓度、温度、压强、催化剂等)对化学平衡的影响,能用相关理论解释其一般规律。 考点一可逆反应与化学平衡建立 1.可逆反应 (1)定义 在同一条件下既可以向正反应方向进行,同时又可以向逆反应方向进行的化学反应。 (2)特点 ①二同:a.相同条件下;b.正、逆反应同时进行。 ②一小:反应物与生成物同时存在;任一组分的转化率都小于(填“大于”或“小于”)100%。 (3)表示 在方程式中用“”表示。 2.化学平衡状态 (1)概念 一定条件下的可逆反应中,正反应速率与逆反应速率相等,反应体系中所有参加反应的物质的质量或浓度保持不变的状态。 (2)化学平衡的建立
(3)平衡特点 深度思考 1.正误判断,正确的打“√”,错误的打“×” (1)2H2O电解 2H2↑+O2↑为可逆反应( ) 点燃 (2)可逆反应不等同于可逆过程。可逆过程包括物理变化和化学变化,而可逆反应属于化学变化( ) (3)化学反应达到化学平衡状态时正、逆反应速率相等,是指同一物质的消耗速率和生成速率相等,若用不同物质表示时,反应速率不一定相等( ) (4)一个可逆反应达到的平衡状态就是这个反应在该条件下所能达到的限度( ) 2SO3(g) ΔH=2.向含有2 mol的SO2的容器中通入过量氧气发生2SO2(g)+O2(g)催化剂 加热 -Q kJ·mol-1(Q>0),充分反应后生成SO3的物质的量 2 mol(填“<”、“>”或“=”,下同),SO2的物质的量 0 mol,转化率 100%,反应放出的热量Q kJ。 题组一极端假设,界定范围,突破判断 1.一定条件下,对于可逆反应X(g)+3Y(g)2Z(g),若X、Y、Z的起始浓度分别为c1、c2、c3(均不为零),达到平衡时,X、Y、Z的浓度分别为mol·L-1、mol·L-1、mol·L-1,
高中数学公式大全由易到难
乘法与因式分解 a^2-b^2=(a+b)(a-b) a^3+b^3=(a+b)(a^2-ab+b^2) ? a^3-b^3=(a-b(a^2+ab+b^2) 三角不等式|a+b|≤|a|+|b| |a-b|≤|a|+|b| |a|≤b<=>-b≤a≤b |a-b|≥|a|-|b| -|a|≤a≤|a| 一元二次方程的解-b+√(b^2-4ac)/2a -b-√(b^2-4ac)/2a 根与系数的关系X1+X2=-b/a X1*X2=c/a 注:韦达定理 判别式 b^2-4ac=0 注:方程有两个相等的实根 b^2-4ac>0 注:方程有两个不等的实根 b^2-4ac<0 注:方程没有实根,有共轭复数根 三角函数公式 两角和公式 sin(A+B)=sinAcosB+cosAsinB sin(A-B)=sinAcosB-sinBcosA cos(A+B)=cosAcosB-sinAsinB cos(A-B)=cosAcosB+sinAsinB tan(A+B)=(tanA+tanB)/(1-tanAtanB) tan(A-B)=(tanA-tanB)/(1+tanAtanB) cot(A+B)=(cotAcotB-1)/(cotB+cotA) cot(A-B)=(cotAcotB+1)/(cotB-cotA) 倍角公式 tan2A=2tanA/[1-(tanA)^2] cos2a=(cosa)^2-(sina)^2=2(cosa)^2 -1=1-2(sina)^2 半角公式 sin(A/2)=√((1-cosA)/2) sin(A/2)=-√((1-cosA)/2) cos(A/2)=√((1+cosA)/2) cos(A/2)=-√((1+cosA)/2) tan(A/2)=√((1-cosA)/((1+cosA)) tan(A/2)=-√((1-cosA)/((1+cosA)) cot(A/2)=√((1+cosA)/((1-cosA)) cot(A/2)=-√((1+cosA)/((1-cosA)) 和差化积 2sinAcosB=sin(A+B)+sin(A-B) 2cosAsinB=sin(A+B)-sin(A-B) ) 2cosAcosB=cos(A+B)-sin(A-B) -2sinAsinB=cos(A+B)-cos(A-B)
高中物理公式大全
高中物理公式、规律汇编表 一、力学公式 1、胡克定律: F = Kx(x 为伸长量或压缩量,K 为倔强系数,只与弹簧的原长、粗细和材料有关) 2、重力:G = mg(g 随高度、纬度、地质结构而变化) 3 、求 F 1、F2两个共点力的合力的公式: F=F2+ F2+ 2F F COS F2F 1212 合力的方向与F1成α角: αθ F2sin tgα= F1 F1+ F2cos 注意:(1)力的合成和分解都均遵从平行四边行法则。 (2)两个力的合力范围:?F1-F2? ≤F≤F1+F2 (3)合力大小可以大于分力、也可以小于分力、也可以等于分力。 4、两个平衡条件: (1)共点力作用下物体的平衡条件:静止或匀速直线运动的物体,所受合外力 为零。 ∑F=0或∑F x=0∑F y=0 推论:[1]非平行的三个力作用于物体而平衡,则这三个力一定共点。 [2]几个共点力作用于物体而平衡,其中任意几个力的合力与剩余几个力 (一个力)的合力一定等值反向 ( 2 )有固定转动轴物体的平衡条件:力矩代数和为零. 力矩:M=FL (L为力臂,是转动轴到力的作用线的垂直距离) 5、摩擦力的公式: (1 )滑动摩擦力:f= μN 说明:a、N为接触面间的弹力,可以大于G;也可以等于G;也可以小于G b、μ为滑动摩擦系数,只与接触面材料和粗糙程度有关,与接触面 积大小、接触面相对运动快慢以及正压力N无关. (2 ) 静摩擦力:由物体的平衡条件或牛顿第二定律求解,与正压力无关. 大小范围:O≤f静≤f m(f m为最大静摩擦力,与正压力有关) 说明: a 、摩擦力可以与运动方向相同,也可以与运动方向相反,还可以与运动方向成一定夹角。 b、摩擦力可以作正功,也可以作负功,还可以不作功。 c、摩擦力的方向与物体间相对运动的 方向或相对运动趋势的方向相反。d、静止的物体可以受滑动摩擦力的作用,运动的物体可以 受静摩擦力的作用。 6、浮力:F= ρVg(注意单位) 7、万有引力:F=G m1m2 r 2 (1).适用条件(2) .G 为万有引力恒量 (3) .在天体上的应用:(M 一天体质量R 一天体半径 g 一天体表面重力 加速度) a 、万有引力=向心力 Mm = m V 22 4 2 G= m(R+h) =m(R+h) (R+h)2(R+h)2T 2 b、在地球表面附近,重力=万有引力 - 1 -
重点高中化学定律公式
高中化学定律和公式 、物质的量的单位——摩尔 物质的量实际上表示含有一定数目粒子的集体。它的符号是 n 23 我们把含有 6.02 ×10 个粒子的任何粒子集体计 量为 物质的量( n )、粒子个数( N )和阿伏加德罗常数( N A )三者之间的关系 用符号表示: 1)定义:单位物质的量的物质所具有的质量叫做摩尔质量。符号 M 物质的量( n )、物质的质量 (m )和摩尔质量( M )三者间的关系 : 在相同条件下 (同温、同压)物质的量相同的气体,具有相同的体积。在标准状况下 (0 ℃、101kPa )1mol 任何气体的体积都约是 22.4L 。 1. 气体摩尔体积 单位物质的量的气体所占的体积叫气体摩尔体积。符号为 V m V m V (V 为标准状况下气体的体积, n -1 3 3 -1 n 为气体的物质的量 )单位: L/mol 或(L ·mol -1)m 3/mol 或(m 3· mol -1) 定义: 以单位体积溶液里所含溶质 B 的物质的量来表示的溶液组成的物理量,叫做溶质 B 的 物质 的量浓度。用符号 C B 表示,单位 mol · L -1(或 mol/L )。C B n B 1 摩尔,摩尔简称摩,符号 mol N n= N A 3.物质的量( mol )= 摩尔物质质量 的质(g 量·m (g ol )-1)符号表示 n= m
c(浓溶液)· V(浓溶液)=c(稀溶液)·V(稀溶液) 1、原子核的构成 原子是由原子中心的原子核和核外电子组成,而核外电子是由质子和中子组成。 1 个电子带一个单位负电荷;中子不带电;1 个质子带一个单位正电荷 核电荷数(Z)== 核内质子数==核外电子数==原子序数 2、质量数 将原子核内所有的质子和中子的相对质量取近似整数值加起来,所得的数值,叫质量数质量数(A)=质子数(Z)+中子数(N)==近似原子量 m+ 3、阳离子a W :核电荷数=质子数>核外电子数,核外电子数=a-m n- 阴离子b Y :核电荷数=质子数<核外电子数,核外电子数=b+n 元素主要化合价变化规律性 二、电子式 在元素符号的周围用小黑点(或×)来表示原子最外层电子的式子叫电子式。如Na、Mg、
高中数学定理公式大全
抛物线:y = ax *+ bx + c 就是y等于ax 的平方加上bx再加上c a > 0时开口向上 a < 0时开口向下 c = 0时抛物线经过原点 b = 0时抛物线对称轴为y轴 还有顶点式y = a(x+h)* + k 就是y等于a乘以(x+h)的平方+k -h是顶点坐标的x k是顶点坐标的y 一般用于求最大值与最小值 抛物线标准方程:y^2=2px 它表示抛物线的焦点在x的正半轴上,焦点坐标为(p/2,0) 准线方程为x=-p/2 由于抛物线的焦点可在任意半轴,故共有标准方程y^2=2px y^2=-2px x^2=2py x^2=-2py 圆:体积=4/3(pi)(r^3) 面积=(pi)(r^2) 周长=2(pi)r 圆的标准方程(x-a)2+(y-b)2=r2 注:(a,b)是圆心坐标 圆的一般方程x2+y2+Dx+Ey+F=0 注:D2+E2-4F>0 (一)椭圆周长计算公式 椭圆周长公式:L=2πb+4(a-b) 椭圆周长定理:椭圆的周长等于该椭圆短半轴长为半径的圆周长(2πb)加上四倍的该椭圆长半轴长(a)与短半轴长(b)的差。 (二)椭圆面积计算公式 椭圆面积公式:S=πab 椭圆面积定理:椭圆的面积等于圆周率(π)乘该椭圆长半轴长(a)与短半轴长(b)的乘积。 以上椭圆周长、面积公式中虽然没有出现椭圆周率T,但这两个公式都是通过椭圆周率T 推导演变而来。常数为体,公式为用。 椭圆形物体体积计算公式椭圆的长半径*短半径*PAI*高 三角函数: 两角和公式 sin(A+B)=sinAcosB+cosAsinB sin(A-B)=sinAcosB-sinBcosA cos(A+B)=cosAcosB-sinAsinB cos(A-B)=cosAcosB+sinAsinB tan(A+B)=(tanA+tanB)/(1-tanAtanB) tan(A-B)=(tanA-tanB)/(1+tanAtanB) cot(A+B)=(cotAcotB-1)/(cotB+cotA) cot(A-B)=(cotAcotB+1)/(cotB-cotA) 倍角公式 tan2A=2tanA/(1-tan2A) cot2A=(cot2A-1)/2cota
高中物理公式定理定律概念大全
高中物理公式定理定律概念大全 第一章运动的描述 一、质点( A) (1)没有形状、大小,而具有质量的点。 (2)质点是一个理想化的物理模型,实际并不存在。 (3)一个物体能否看成质点,并不取决于这个物体的大小,而是看在所研究的问题中物体 的形状、大小和物体上各部分运动情况的差异是否为可以忽略的次要因素,要具体问题具体分析。 二、参考系(A) (1)物体相对于其他物体的位置变化,叫做机械运动,简称运动。 (2)在描述一个物体运动时,选来作为标准的(即假定为不动的)另外的物体,叫做参考系。 对参考系应明确以下几点: ①对同一运动物体,选取不同的物体作参考系时,对物体的观察结果往往不同的。 ②在研究实际问题时,选取参考系的基本原则是能对研究对象的运动情况的描述得到尽量 的简化,能够使解题显得简捷。 ③因为今后我们主要讨论地面上的物体的运动,所以通常取地面作为参照系。 三、路程和位移(A) (1)位移是表示质点位置变化的物理量。路程是质点运动轨迹的长度。 (2)位移是矢量,可以用以初位置指向末位置的一条有向线段来表示。因此,位移的大小 等于物体的初位置到末位置的直线距离。路程是标量,它是质点运动轨迹的长度。因此其大小与运动路径有关。 (3)一般情况下,运动物体的路程与位移大小是不同的。只有当质点做单一方向的直线运 动时,路程与位移的大小才相等。图2-1-1 中质点轨迹 ACB的长度是路程, AB 是位移 S。 C C B B A A 图 2-1-1 (4)在研究机械运动时,位移才是能用来描述位置变化的物理量。路程不能用来表达物体 的确切位置。比如说某人从 O点起走了 50m路,我们就说不出终了位置在何处。 四、速度、平均速度和瞬时速度(A) (1)表示物体运动快慢的物理量,它等于位移s 跟发生这段位移所用时间t 的比值。即v=s/t 。速度是矢量,既有大小也有方向,其方向就是物体运动的方向。在国际单位制中, 速度的单位是( m/s)米/秒。 (2)平均速度是描述作变速运动物体运动快慢的物理量。 = 定义 v s/t 为物体在这段时间(或 这段位移)上的平均速度。平均速度也是矢量,其方向就是物体在这段时间内的位移的方向。(3)瞬时速度是指运动物体在某一时刻(或某一位置)的速度。从物理含义上看,瞬时速度指某一时刻附近极短时间内的平均速度。瞬时速度的大小叫瞬时速率,简称速率。
高中化学定律公式
高中化学定律公式Revised on November 25, 2020
高中化学定律和公式 一、物质的量的单位——摩尔 物质的量实际上表示含有一定数目粒子的集体。它的符号是n 。 我们把含有×1023 个粒子的任何粒子集体计量为1摩尔,摩尔简称摩,符号mol 。 物质的量(n )、粒子个数(N )和阿伏加德罗常数(A N )三者之间的关系用符号表示:n= A N N (1)定义:单位物质的量的物质所具有的质量叫做摩尔质量。符号M 。 物质的量(n )、物质的质量(m)和摩尔质量(M )三者间的关系: 3.物质的量(mol )= 1 ()()g g mol 物质的质量摩尔质量 符号表示:n=M m 在相同条件下(同温、同压)物质的量相同的气体,具有相同的体积。在标准状况下(0 ℃、101 kPa)1 mol 任何气体的体积都约是 L 。 1.气体摩尔体积 单位物质的量的气体所占的体积叫气体摩尔体积。符号为m V m V V n = (V 为标准状况下气体的体积,n 为气体的物质的量) 单位:L/mol 或(L·mol -1 ) m 3 /mol 或(m 3 ·mol -1 ) 定义:以单位体积溶液里所含溶质B 的物质的量来表示的溶液组成的物理量,叫做溶质B 的物质的量浓度。用符号B C 表示,单位mol·L -1(或mol/L )。表达式:B B n C =
c(浓溶液)·V(浓溶液)=c(稀溶液)·V(稀溶液) 1、原子核的构成 原子是由原子中心的原子核和核外电子组成,而核外电子是由质子和中子组成。 1个电子带一个单位负电荷;中子不带电;1个质子带一个单位正电荷 核电荷数(Z) == 核内质子数 == 核外电子数 == 原子序数 2、质量数 将原子核内所有的质子和中子的相对质量取近似整数值加起来,所得的数值,叫质量数。 质量数(A)= 质子数(Z)+ 中子数(N)==近似原子量 3、阳离子a W m+:核电荷数=质子数>核外电子数,核外电子数=a-m 阴离子b Y n- :核电荷数=质子数<核外电子数,核外电子数=b+n
高中物理全部公式大全汇总
[转] 高中所有物理公式整理,参考下的。 超级全面的物理公式!!!很有用的说~~~(按照咱们的物理课程顺序总结的)1)匀变速直线运动 1.平均速度V平=s/t(定义式) 2.有用推论Vt2-Vo2=2as 3.中间时刻速度Vt/2=V平=(Vt+Vo)/2 4.末速度Vt=Vo+at 5.中间位置速度Vs/2=[(Vo2+Vt2)/2]1/2 6.位移s=V平t=Vot+at2/2=Vt/2t 7.加速度a=(Vt-Vo)/t {以Vo为正方向,a与Vo同向(加速)a>0;反向则a<0} 8.实验用推论Δs=aT2 {Δs为连续相邻相等时间(T)内位移之差} 注: (1)平均速度是矢量; (2)物体速度大,加速度不一定大; (3)a=(Vt-Vo)/t只是量度式,不是决定式; 2)自由落体运动 1.初速度Vo=0 2.末速度Vt=gt 3.下落高度h=gt2/2(从Vo位置向下计算) 4.推论Vt2=2gh
(3)竖直上抛运动 1.位移s=Vot-gt2/2 2.末速度Vt=Vo-gt (g=9.8m/s2≈10m/s2) 3.有用推论Vt2-Vo2=-2gs 4.上升最大高度Hm=Vo2/2g(抛出点算起) 5.往返时间t=2Vo/g (从抛出落回原位置的时间) 1)平抛运动 1.水平方向速度:Vx=Vo 2.竖直方向速度:Vy=gt 3.水平方向位移:x=Vot 4.竖直方向位移:y=gt2/2 5.运动时间t=(2y/g)1/2(通常又表示为(2h/g)1/2) 6.合速度Vt=(Vx2+Vy2)1/2=[Vo2+(gt)2]1/2 合速度方向与水平夹角β:tgβ=Vy/Vx=gt/V0 7.合位移:s=(x2+y2)1/2, 位移方向与水平夹角α:tgα=y/x=gt/2Vo 8.水平方向加速度:ax=0;竖直方向加速度:ay=g 2)匀速圆周运动 1.线速度V=s/t=2πr/T 2.角速度ω=Φ/t=2π/T=2πf 3.向心加速度a=V2/r=ω2r=(2π/T)2r 4.向心力F心=mV2/r=mω2r=mr(2π/T)2=mωv=F合 5.周期与频率:T=1/f 6.角速度与线速度的关系:V=ωr
高中化学常用计算公式
1. 有关物质的量(mol )的计算公式 (1)物质的量(mol 即n= M m ;M 数值上等于该物质的相对分子(或原子)质量 (2)物质的量(mol )= )(个微粒数(个)mol /1002.623 ? 即n=A N N N A 为常数6.02×1023,应谨记 (3)气体物质的量(mol 即n= m g V V 标, V m 为常数22.4L ·mol -1,应谨记 (4)溶质的物质的量(mol )=物质的量浓度(mol/L )×溶液体积(L )即n B =C B V aq (5)物质的量(mol )=)反应热的绝对值()量(反应中放出或吸收的热mol KJ KJ / 即n=H Q ? 2. 有关溶液的计算公式 (1)基本公式 ①溶液密度(g/mL 即ρ = aq V m 液 ②溶质的质量分数=%100) g g ?+溶剂质量)((溶质质量)溶质质量(=) ) g g 溶液质量(溶质质量(×100% 即w= 100%?液质m m =剂质质m m m +×100% ③物质的量浓度(mol/L 即C B=aq B V n (2)溶质的质量分数、溶质的物质的量浓度及溶液密度之间的关系: ①溶质的质量分数100%(g/mL) 1000(mL)(g/mol) 1(L)(mol/L)????= 溶液密度溶质的摩尔质量物质的量浓度 即C B = B M ρω 1000 ρ单位:g/ml (3)溶液的稀释与浓缩(各种物理量的单位必须一致): 原则:稀释或浓缩前后溶质的质量或物质的量不变! ①浓溶液的质量×浓溶液溶质的质量分数=稀溶液的质量×稀溶液溶质的质量分数 即浓m 稀稀浓ωωm =
高中数学公式定理定律大全
高中数学公式大全 (最全面,最详细) 高中数学公式大全 抛物线: y = ax *+ bx + c 就是 y 等于 ax 的平方加上 bx 再加上 c a > 0 时开口向上 a < 0 时开口向下 c = 0 时抛物线经过原点 b = 0 时抛物线对称轴为 y 轴 还有顶点式 y = a ( x+h) * + k 就是 y 等于 a 乘以( x+h)的平方 +k -h 是顶点坐标的 x k 是顶点坐标的 y 一般用于求最大值与最小值抛物线标准方程 :y^2=2px 它表示抛物线的焦点在 x 的正半轴上 , 焦点坐标为 (p/2,0) 方程为 x=-p/2 由于抛物线的焦点可在任意半轴 , 故共有标准方程 准线y^2=2px y^2=-2px x^2=2py x^2=-2py 圆:体积 =4/3(pi )(r^3) 面积=(pi)(r^2) 周长=2(pi)r
圆的标准方程 (x-a)2+(y-b)2=r2 注:(a,b )是圆心坐标圆的一般方程 x2+y2+Dx+Ey+F=0 注: D2+E2-4F>0 (一)椭圆周长计算公式 椭圆周长公式: L=2πb+4(a -b) 椭圆周长定理:椭圆的周长等于该椭圆短半轴长为半径的圆周长 (2πb)加上四倍的该椭圆长半轴长( a)与短半轴长( b)的差。 (二)椭圆面积计算公式 椭圆面积公式: S=πab 椭圆面积定理:椭圆的面积等于圆周率(π)乘该椭圆长半轴长 ( a)与短半轴长( b)的乘积。 以上椭圆周长、面积公式中虽然没有出现椭圆周率 T,但这两个 公式都是通过椭圆周率 T 推导演变而来。常数为体,公式为用。 椭圆形物体体积计算公式椭圆的长半径*短半径*PAI* 高 三角函数: 两角和公式 sin(A+B)=sinAcosB+cosAsinB sin(A-B)=sinAcosB-sinBcosA cos(A+B)=cosAcosB-sinAsinB cos(A-
高中物理公式规律大全
高中物理基本规律及公式 一、力学 1、匀变速直线运动规律: (1)速度公式:at v v +=0 (2)位移公式:202 1at t v x + = (3)速度-位移公式:ax v v 22 02=- (4)平均速度公式: 2 02t v v v v =+= (5)在连续相等的时间T 内的位移之差为一恒定值,即2 aT x =? 2、胡克定律: kx F = (x 为伸长量或压缩量) 3、两个力的合力范围: ? F 1-F 2 ? ≤F ≤ F 1 +F 2 4、摩擦力公式: (1) 滑动摩擦力: f =μF N (F N 为正压力) (2) 静摩擦力: O <f 静≤f max (f max 为最大静摩擦力,与正压力有关) 5、物体平衡条件:静止或做匀速直线运动的物体,所受合外力为零。 或 6、牛顿第二定律: ma F =合 或 x x ma F = y y ma F = 7、平抛运动:初速度水平,只受重力。 性质:匀变速曲线运动 平抛运动可分解为水平方向的匀速直线运动和竖直方向的自由落体运动。 平抛速度求解:???==gt v v v y x 0 t 秒末的合速度2 2y x v v v += 速度的方向0 tan v gt v v x y = = β 平抛运动的位移:?? ? ??==2021gt y t v x t 秒末位移: 位移方向:0 2tan v gt x y == α 8、圆周运动:①线速度大小 T r t l v π2=??= ,方向在圆周上该点的切线方向. ②角速度:T t πθω2=??= ,(单位:rad/s ) ③ ωωr v v =的关系:与 ④周期T :匀速圆周运动的物体运动一周所用的时间. T =1/f ⑤向心加速度:r T r v r a n 2 22 2?? ? ??===πω,方向总与运动方向(即v 方向)垂直. 0=合F 0=x F 0 =y F 4 22 20224 1t g t v y x S + =+=
高中化学公式大全
高中化学常用公式总结 1. 有关物质的量(mol )的计算公式 (1)物质的量(mol )()= 物质的质量物质的摩尔质量() g g mol / (2)物质的量(mol )() = ?微粒数(个) 个6021023 ./mol (3)气体物质的量(mol )= 标准状况下气体的体积() .(/) L L mol 224 (4)溶质的物质的量(mol )=物质的量浓度(mol/L )×溶液体积(L ) 2. 有关溶液的计算公式 (1)基本公式 ①溶液密度(g/mL )= 溶液质量溶液体积()() g mL ②溶质的质量分数()= ?+溶质质量溶质质量溶剂质量(g g ) () 100% ③物质的量浓度(mol/L )= 溶质物质的量溶液体积() () mol L (2)溶质的质量分数、溶质的物质的量浓度及溶液密度之间的关系: ①溶质的质量分数= ????物质的量浓度溶质的摩尔质量溶液密度(mol /L)1(L)(g /mol) 1000(mL)(g /mL) 100% ②物质的量浓度= ???1000(mL)(g /mL)(g /mol)1(L) 溶液密度溶质的质量分数 溶质摩尔质量 (3)溶液的稀释与浓缩(各种物理量的单位必须一致): ①浓溶液的质量×浓溶液溶质的质量分数=稀溶液的质量×稀溶液溶质的质量分数(即溶质的质量不变) ②浓溶液的体积×浓溶液物质的量浓度=稀溶液的体积×稀溶液物质的量浓度[即c (浓)·V (浓)=c (稀)·V (稀)] (4)任何一种电解质溶液中:阳离子所带的正电荷总数=阴离子所带的负电荷总数(即整个溶液呈电中性) 3. 有关溶解度的计算公式(溶质为不含结晶水的固体) (1)基本公式: ① 溶解度饱和溶液中溶质的质量溶剂质量(g)100(g) (g) (g) =
高中数学课本中的定理公式结论的证明
数学课本中的定理、公式、结论的证明 数学必修一 第一章 集合(无) 第二章 函数(无) 第三章 指数函数和对数函数 1.对数的运算性质: 如果 a > 0 , a 1, M > 0 ,N > 0, 那么 (1)log ()log log a a a MN M N =+; (2)log log -log a a a M M N N =; (3)log log ()n a a M n M n R =∈. 根据指数幂的运算性质证明对数的运算性质 证明:(性质1)设log a M p =,log a N q =,由对数的定义可得 p M a =,q N a =, ∴p q p q MN a a a +=?=, ∴log ()a MN =p q +, 即证得log log log a a a MN M N =+. 证明:(性质2)设log a M p =,log a N q =, 由对数的定义可得 p M a =,q N a =, ∴ q p q p a a a N M -==, ∴q p N M a -=log , 即证得log log -log a a a M M N N =. 证明(性质3)设log a M p =,由对数的定义可得 p M a =, ∴n np M a =, ∴log n a M np =, 即证得log log n a a M n M =.
第四章函数应用(无) 数学必修二 第一章立体几何初步 直线与平面、平面与平面平行、垂直的判定定理与性质定理的证明. 1、直线与平面平行的判定定理 若平面外一条直线与此平面内一条直线平行,则该直线与此平面平行. 2、平面与平面平行的判定定理 如果一个平面内有两条相交直线都平行于另一个平面,那么这两个平面平行.
高中物理公式定理定律概念大全
高中物理公式定理定律概念大全 必修一 第一章 运动的描述 一、质点(A ) (1)没有形状、大小,而具有质量的点。 (2)质点是一个理想化的物理模型,实际并不存在。 (3)一个物体能否看成质点,并不取决于这个物体的大小,而是看在所研究的问题中物体的形状、大小和物体上各部分运动情况的差异是否为可以忽略的次要因素,要具体问题具体分析。 二、参考系(A ) (1)物体相对于其他物体的位置变化,叫做机械运动,简称运动。 (2)在描述一个物体运动时,选来作为标准的(即假定为不动的)另外的物体,叫做参考系。 对参考系应明确以下几点: ①对同一运动物体,选取不同的物体作参考系时,对物体的观察结果往往不同的。 ②在研究实际问题时,选取参考系的基本原则是能对研究对象的运动情况的描述得到尽量的简化,能够使解题显得简捷。 ③因为今后我们主要讨论地面上的物体的运动,所以通常取地面作为参照系。 三、路程和位移(A ) (1)位移是表示质点位置变化的物理量。路程是质点运动轨迹的长度。 (2)位移是矢量,可以用以初位置指向末位置的一条有向线段来表示。因此,位移的大小等于物体的初位置到末位置的直线距离。路程是标量,它是质点运动轨迹的长度。因此其大小与运动路径有关。 (3)一般情况下,运动物体的路程与位移大小是不同的。只有当质点做单一方向的直线运动时,路程与位移的大小才相等。图2-1-1中质点轨迹ACB 的长度是路程,AB 是位移S 。 (4)在研究机械运动时,位移才是能用来描述位置变化的物理量。路程不能用来表达物体的确切位置。比如说某人从O 点起走了50m 路,我们就说不出终了位置在何处。 四、速度、平均速度和瞬时速度(A ) (1)表示物体运动快慢的物理量,它等于位移s 跟发生这段位移所用时间t 的比值。即v=s/t 。速度是矢量,既有大小也有方向,其方向就是物体运动的方向。在国际单位制中,速度的单位是(m/s )米/秒。 (2)平均速度是描述作变速运动物体运动快慢的物理量。定义v =s/t 为物体在这段时间(或这段位移)上的平均速度。平均速度也是矢量,其方向就是物体在这段时间内的位移的方向。 A B C A B C 图2-1-1
重点高中化学定律公式
高中化学定律和公式 一、物质的量的单位——摩尔 物质的量实际上表示含有一定数目粒子的集体。它的符号是n 。 我们把含有6.02×1023 个粒子的任何粒子集体计量为1摩尔,摩尔简称摩,符号mol 。 物质的量(n )、粒子个数(N )和阿伏加德罗常数(A N )三者之间的关系用符号表示:n= A N N
c(浓溶液)·V(浓溶液)=c(稀溶液)·V(稀溶液) 1、 原子核的构成 原子是由原子中心的原子核和核外电子组成,而核外电子是由质子和中子组成。 1个电子带一个单位负电荷;中子不带电;1个质子带一个单位正电荷 核电荷数(Z)==核内质子数==核外电子数==原子序数 在元素符号的周围用小黑点(或×)来表示原子最外层电子的式子叫电子式。如Na 、Mg 、Cl 、O 的电子式我们可分别表示为: 1、表示原子 ‥ ‥ ∶ ‥
Na××Mg×?Cl?O? 习惯上,写的时候要求对称。 电子式同样可以用来表示阴阳离子,例如 2、表示简单离子: 阳离子:Na+Mg2+Al3+ 阴离子:[∶S∶]2-[∶Cl∶]-[∶O∶]2- ①.电子式最外层电子数用?(或×)表示; ②. . 4、. 吸放热与能量关系 一、原电池的定义:将化学能转化为电能的装置. 1、原电池的工作原理 正极:铜片上:2H + +2e-=H2↑(还原反应) 负极:锌片上:Zn-2e-=Zn 2+ (氧化反应) 氧化还原反应:Zn+2H + =Zn 2+ +H2↑该电极反应就是Zn+2H + =Zn 2+ +H2↑一、化学反应的速率 ‥ ‥ ‥‥ ‥ ‥ ‥‥ ‥
1、定义:单位时间内反应物的浓度减少或生成物浓度的增加来表示 2、单位:mol/L·smol/L·min 3、表达式:v(A)==t A c ??)( △c(A)表示物质A 浓度的变化,△t 表示时间 (2)对于反应mA(g)+nB(g) pC(g)+qD(g)来说,则有q V p V n V m V D C B A === 烷烃燃烧的通式 2分馏--- 裂化---1- 4。 5、△H (3)△H=中和热的定义是在稀溶液中,酸跟碱发生中和反应而生成1molH 2O 时的反应热叫中和热。 【实验】实验2-3:在50mL 烧杯中加入0.50mol/L 的盐酸,测其温度。另用量筒量取 50mL0.55mol/LNaOH 溶液,测其温度,并缓缓地倾入烧杯中,边加边用玻璃棒搅拌。观察反应中溶 液温度的变化过程,并作好记录。
