热重分析及综合热分析

实验七 热重分析及综合热分析
一、目的与要求
1.了解热重分析的仪器装置及实验技术。
2.了解差热分析的仪器装置及实验技术。
3熟悉综合热分析的特点,掌握综合热曲线的分析方法。 4.测绘矿物的热重曲线和差热分析曲线,解释曲线变化的原因。 二、原理
1 热重分析的仪器结构与分析方法
热重分析法是在程序控制温度下,测量物质的质量随温度变化的一种实验技术。 热重分析通常有静态法和动态法两种类型。
静态法又称等温热重法,是在恒温下测定物质质量变化与温度的关系,通常把试样在各给定温度加热至恒重。该法比较准确,常用来研究固相物质热分解的反应速度和测定反应速度常数。
动态法又称非等温热重法,是在程序升温下测定物质质量变化与温度的关系,采用连续升温连续称重的方式。该法简便,易于与其他热分析法组合在一起,实际中采用较多。
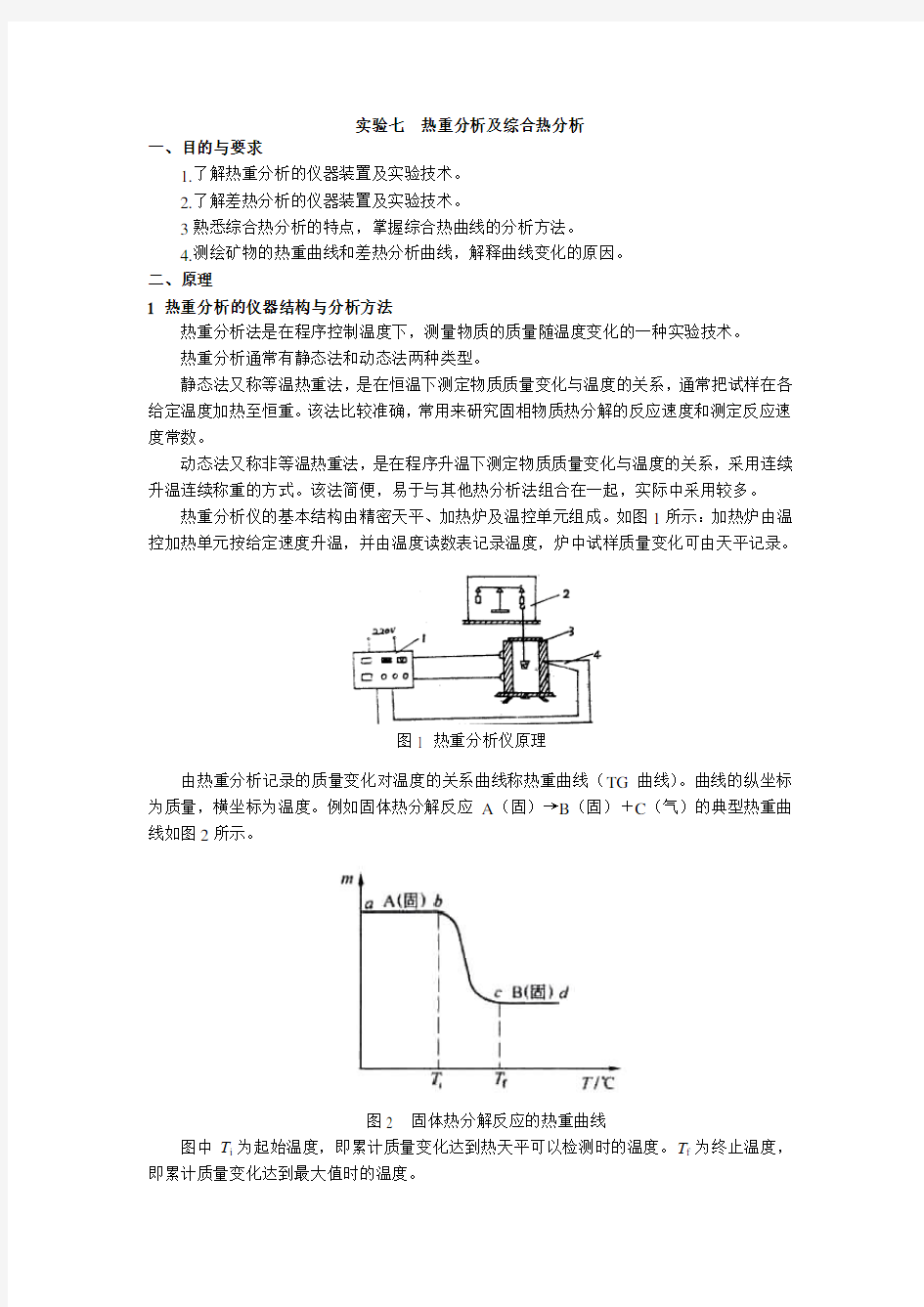
热重分析仪的基本结构由精密天平、加热炉及温控单元组成。如图1所示:加热炉由温控加热单元按给定速度升温,并由温度读数表记录温度,炉中试样质量变化可由天平记录。
由热重分析记录的质量变化对温度的关系曲线称热重曲线(TG 曲线)。曲线的纵坐标为质量,横坐标为温度。例如固体热分解反应A (固)→B (固)+C (气)的典型热重曲线如图2所示。
图2 固体热分解反应的热重曲线
图中T i 为起始温度,即累计质量变化达到热天平可以检测时的温度。T f 为终止温度,即累计质量变化达到最大值时的温度。
图1 热重分析仪原理
热重曲线上质量基本不变的部分称为基线或平台,如图2中ab 、cd 部分。
若试样初始质量为W 0,失重后试样质量为W 1,则失重百分数为(W 0-W 1)/W 0×100%。 许多物质在加热过程中会在某温度发生分解、脱水、氧化、还原和升华等物理化学变化而出现质量变化,发生质量变化的温度及质量变化百分数随着物质的结构及组成而异,因而可以利用物质的热重曲线来研究物质的热变化过程,如试样的组成、热稳定性、热分解温度、热分解产物和热分解动力学等。例如含有一个结晶水的草酸钙(CaC 2O 4·H 2O )的热重曲线如图3,CaC 2O 4·H 2O 在100℃以前没有失重现象,其热重曲线呈水平状,为TG 曲线的第一个平台。在100℃和200℃之间失重并开始出现第二个平台。这一步的失重量占试样总质量的12.3%,正好相当于每molCaC 2O 4·H 2O 失掉1molH 2O ,因此这一步的热分解应按
O H O CaC O H ·O CaC 242℃
200℃100242 ~ +????→?
进行。在400℃和500℃之间失重并开始呈现第三个平台,其失重量占试样总质量的18.5%,相当于每molCaC 2O 4分解出1molCO ,因此这一步的热分解应按
CO CaCO O CaC 3℃500 ℃40042~ +????→?
进行。在600℃和800℃之间失重并出现第四个平台,其失重量占试样总质量的30%,正好相当于每molCaC 2O 4分解出1molCO 2,因此这一步的热分解应按
2℃800 ℃60042CO CaO O CaC ~ +????→?
进行。
可见借助热重曲线可推断反应机理及产物。
图3 CaC 2O 4·H 2O 的热重曲线
2、综合热分析
DTA 、DSC 、TG 等各种单功能的热分析仪若相互组装在一起,就可以变成多功能的综合热分析仪,如DTA -TG 、DSC -TG 、DTA -TMA (热机械分析)、DTA -TG -DTG (微商热重分析)组合在一起。综合热分析仪的优点是在完全相同的实验条件下,即在同一次实验中可以获得多种信息,比如进行DTA -TG -DTG 综合热分析可以一次同时获得差热曲线、热重曲线和微商热重曲线。根据在相同的实验条件下得到的关于试样热变化的多种信息,就可以比较顺利地得出符合实际的判断。
综合热分析的实验方法与DTA 、DSC 、TG 的实验方法基本类同,在样品测试前选择好测量方式和相应量程,调整好记录零点,就可在给定的升温速度下测定样品,得出综合热曲线。
综合热曲线实际上是各单功能热曲线测绘在同一张记录纸上,因此,各单功能标准热曲线可以作为综合热曲线中各个曲线的标准。利用综合热曲线进行矿物鉴定或解释峰谷产生的
原因时,可查阅有关的图谱。
图4示出了某种粘土的综合热曲线,它包括加热曲线、差热曲线、热重曲线和收缩曲线。根据综合热分析可知,该粘土的主要谱形与高岭石(Al2O3·2SiO2·2H2O)相符,故其矿物组成以高岭石为主。差热曲线两个显著的吸热峰,第一个吸热峰从200℃以下开始发生至260℃达峰值,热重曲线上对应着这一过程质量损失3.7%,而收缩曲线表明这一过程体积变化不大,所以这一吸热峰对应的是高岭石失去吸附水、层间水的过程。第二吸热峰从540℃开始至640℃达顶峰,这一过程质量损失达1.31%,而体积收缩1.4%,这一过程的强烈的吸热效应相当于高岭石晶格中OH-根脱出或结晶水排除,致使晶格破坏,偏高岭石(Al2O3·2SiO2)分解成无定形的Al2O3与SiO2。当温度升高到1000℃左右,无定形的Al2O3结晶成-Al2O3和部分微晶莫来石,使差热谱上出现强烈的放热效应,此时质量无显著变化,体积却显著收缩,从3.19%达8.67%。加热到1240℃又出现一放热峰,同时体积从9.68%迅速收缩到14.4%,这显然又是一个结晶想的出现,据研究系非晶质SiO2与γ-Al2O3化合成莫来石(Al2O3·2SiO2)结晶所致。
图4 粘土的综合热曲线
1-加热曲线;2-差热曲线;3-热重曲线;4-收缩曲线在综合热分析技术中,DTA-TG组合是最普通最常用的一种,DSC-TG组合也常用。根据试样物理或化学过程中所产生的质量与能量的变化情况,DTA(DSC)和TG所对应的过程可作出大致的判断,如表1所示。表中“+”表示有,“-”表示无,在进行综合热曲线分析时可作为参考。
表1 DTA(DSC)和TG对反应过程的判断
三、仪器装置
四、操作步骤:
1. 试样准备
试样的用量与粒度对热重曲线有较大的影响。因为试样的吸热或放热反应会引起试样温度发生偏差,试样用量越大,偏差越大。试样用量大,逸出气体的扩散受到阻碍,热传递也受到影响,使热分解过程中TG曲线上的平台不明显。因此,在热重分析中,试样用量应在仪器灵敏度范围内尽量小。
试样的粒度同样对热传递气体扩散有较大影响。粒度不同会使气体产物的扩散过程有较大变化,这种变化会导致反应速率和TG曲线形状的改变,如粒度小,反应速率加快,TG 曲线上反应区间变窄。粒度太大总是得不到好的TG曲线的。
总之,试样用量与粒度对热重曲线有着类似的影响,实验时应选择适当。一般粉末试样应过200-300目筛,用量在1g左右为宜。
2. 热重分析的样品测试步骤
①将样品铂金坩埚用毛刷刷净,挂于天平挂丝上,精确称量其重量,记录其重量(注意勿使小坩埚及挂丝与炉壁相碰)。
②取下铂金坩埚盛入一定量的试样于铂金坩埚内(约0.5~1g),挂于吊丝上,再精确称其重量,算出其样品重量。
③盖好挡热板,注意勿与吊丝相碰,接通加热电源,调压使升温速度约为10℃/分匀速升温。
④温度指示仪表指于50℃时开始称量重量,此后每隔50℃左右称量一次,但在发生重量改变剧烈的温度区间应缩小称量温度间隔10℃称量一次。
⑤升温至750℃时,实验结束,关闭天平,关闭各仪器开关,切断电源。
3差热分析仪的操作步骤
①打开放大器电源开关,记录仪开关,进行预热;
②把炉体轻轻取下,确定差热电偶两工作端各自所应盛放的样品(本实验参比样品为煅
烧氧化铝,测量样品为左云土);装好样品,关好电炉盖;
③检查系统是否正常,打印机是否状态良好,设定基线;
图6 差热分析仪
图5 失重实验装置
④在“采样”程序中设定各参数,升温速率设定12℃/分升温;
⑤1200℃实验结束,按程序关闭各仪器开关,实验结束。
五、实验和数据处理
1.选择与DTA实验中测试的同种矿物,用静态法测绘TG曲线。
2.选择DTA实验相同测试条件和同种矿物,测绘DTA-TG综合热曲线,解释曲线
上能量和质量变化的原因,并与单功能DTA、TG曲线对照峰谷形状、温度及特点。
六、思考题
1. 升温速度对热重曲线形状有何影响?
2. 影响质量测量准确度的因素有哪些?在实验中可采取哪些措施来提高测量准确度?
3. 从晶体结构预测高龄土和滑石的差热曲线有何区别?
差热分析__实验报告
差热分析 一、实验目的 1. 用差热仪绘制CuSO4·5H2O等样品的差热图。 2. 了解差热分析仪的工作原理及使用方法。 3. 了解热电偶的测温原理和如何利用热电偶绘制差热图。 二、实验原理 物质在受热或冷却过程中,当达到某一温度时,往往会发生熔化、凝固、晶型转变、分解、化合、吸附、脱附等物理或化学变化,并伴随着有焓的改变,因而产生热效应,其表现为物质与环境(样品与参比物)之间有温度差。差热分析就是通过温差测量来确定物质的物理化学性质的一种热分析方法。 差热分析仪的结构如下图所示。它包括带有控温装置的加热炉、放置样品和参比物的坩埚、用以盛放坩埚并使其温度均匀的保持器、测温热电偶、差热信号放大器和信号接收系统(记录仪或微机)。差热图的绘制是通过两支型号相同的热电偶,分别插入样品和参比物中,并将其相同端连接在一起(即并联,见图5-1)。A 两支笔记录的时间—温度(温差)图就称为差热图,或称为热谱图。 图5-1 差热分析原理图 图5-1 典型的差热图从差热图上可清晰地看到差热峰的数目、位置、方向、宽度、高度、对称性以及峰面积等。峰的数目表示物质发生物理化学变化的次数;峰的位置表示物质发生变化的转化温度(如图5-2中T B);峰的方向表明体系发生热效应的正负性;峰面积说明热效应的大小。相同条件下,峰面积大的表示热效应也大。在相同的测
定条件下,许多物质的热谱图具有特征性:即一定的物质就有一定的差热峰的数目、位置、方向、峰温等,因此,可通过与已知的热谱图的比较来鉴别样品的种类、相变温度、热效应等物理化学性质。因此,差热分析广泛应用于化学、化工、冶金、陶瓷、地质和金属材料等领域的科研和生产部门。理论上讲,可通过峰面积的测量对物质进行定量分析。 本实验采用CuSO 4·5H 2O ,CuSO 4·5H 2O 是一种蓝色斜方晶系,在不同温度下,可以逐步失水: CuSO 4·5H 2O CuSO 4·3H 2O CuSO 4·H 2O CuSO 4 (s ) 从反应式看,失去最后一个水分子显得特别困难,说明各水分子之间的结合能力不一样。 四个水分子与铜离子的以配位键结合,第五个水分子以氢键与两个配位水分子和SO 4 2-离子结合。 加热失水时,先失去Cu 2+ 左边的两个非氢键原子,再失去Cu 2+ 右边的两个水分子,最后失去以氢键连接在SO 4 2- 上的水分子。 三、仪器试剂 差热分析仪1套;分析物CuSO 4·5H 2O ;参比物α-Al 2O 3。 四、实验步骤 1、 开启仪器电源开关,将各控制箱开关打开,仪器预热。开启计算机开关。 2、参比物(α-Al 2O 3)可多次重复利用,取干净的坩埚,装入CuSO 4·5H 2O 样品、装满,再次加入CuSO 4·5H 2O 将坩埚填满,备用。 3、抬升炉盖,将上步装好的CuSO 4·5H 2O 样品放入炉中,盖好炉盖。 4、打开计算机软件进行参数设定,横坐标2400S 、纵坐标300℃、升温速率
热重分析
高聚物的差热热重分析DTA/TG原理 高聚物的差热热重分析DTA/TG原理 差热分析,简称DTA,是将被测试样加热或冷却时,由于温度导致试样内部产生物理或化学变化,追踪热量变化的一种分析方法。热重分析,简称TG,是将被测试样加热,由于温度导致试样重量变化的分析方法。综合热分析仪是具有微机数据处理系统的热重—差热联用热分析仪器,是一种在程序温度(等速升降温、恒温和循环)控制下,测量物质的质量和热量随温度变化的分析仪器。常用以测定物质在熔融、相变、分解、化合、凝固、脱水、蒸发、升华等特定温度下发生的热量和质量变化,广泛应用于无机、有机、石化、建材、化纤、冶金、陶瓷、制药等领域,是国防、科研、大专院校、工矿企业等单位研究不同温度下物质物理、化学变化的重要分析仪器。差热分析作为一种重要的热分析手段已广为应用,它可以研究高聚物对热敏感的各种化学及物理过程,物理变化如:玻璃化转变、晶型转变、结晶过程、熔融、纯度变化等;化学变化如:加聚反应、缩聚反应、硫化、环化、交联、固化、氧化、热分解、辐射变化等。需指出,由于高聚物的物理或化学变化对热敏感的特性是很复杂的,所以常需要结合其它实验方法如动态力学试验、气质联用等对差热分析热谱图进行深入研究,从而进一步探讨高聚物的结构和性能间的关系。 仪器由热天平主机、加热炉、冷却风扇、微机温控单元、天平放大单元、微分单元、差热放大单元、接口单元、气氛控制单元、PC微机、打印机等组成。 实验时,将试样和惰性参比物(在测定的温度范围内不产生热效应的热惰性物质,常用?-氧化铝、石英粉、硅油等)置于温度均匀分布的坩埚(样品池)的适当位置,将坩埚(样品池)组合于加热炉中,控制其等速升温或降温。在此变温过程中,若试样发生物理或化学变化,则在对应的温度下吸收或放出热量改变其温度,使试样和参比物之间产生一定的温度(ΔT)。将ΔT 放大,记录试样与参比物的温度ΔT随温度T的变化,即ΔT~T曲线。此曲线通常称为差热曲线或差热热谱。 刚开始加热时,试样和参比物以相同温度升温,不产生温度差ΔT=0,差热曲线上为平直的基线。当温度上升到试样产产玻璃化转时,大分子的链段开始运动。试样的热容发生明显的变化,由于热容增大需要吸收更多的热量,因而试样的温度落后于参比物的温度,产生了温度差,于是差热曲线上方出现一个转折,该转折对应的温度,即玻璃化转变温度(Tg)若试样是能结晶的并处于过冷的无定形状态,则在玻璃温度以上的适当温度进行结晶,同时放出大量的热量,此时试样温度较参比物上升快,差热曲线上表现为放热峰。再进一步加热,晶体开始熔融面需要吸收热量,试样温度暂时停止上升,与参比物之间产生了温度差,其差热曲线在相反方向出现吸热峰。当熔融完成后,加于试样的热能在使试样温度升高,直到等于参比物的温度,于是二者的温度差又为零,回复到基线位置,将熔融峰顶点对应的温度记作熔点(T m);继续加热试样可能发生其他变化,如氧化、分解(氧化是放热反应,分解是吸热反应)。因此,根据差热曲线可以确定高聚物的转变和特征温度。
热重分析实验报告
热重分析实验报告
————————————————————————————————作者: ————————————————————————————————日期: ?
材料与建筑工程学院实验报告 课程名称: 材料物理性能 专业:材料科学与工程 班级: 2013级本科 姓名:张学书 学号: 3
指导老师:谢礼兰老师 贵州师范大学学生实验报告 成绩 实验一:STA449F3同步热分析仪的结构原理及操作方法 一、实验目的 1、熟悉同步热分析仪的基本原理。 2、了解STA449 F3型同步热分析仪的构造原理及性能。 3、学习STA449 F3型同步热分析仪的操作方法。 二、实验原理 差示扫描量热法(DSC)是指在加热的过程中,测量被测物质与参比物之间的能量差与温度之间的关系的一种方法技术。图1-1为功率补偿式DSC仪器示意图:
图1-1 功率补偿式D SC 示意图 1.温度程序控制器; 2.气氛控制;3.差热放大器;4.功率补偿放大器;5.记录仪 当试样发生热效应时,譬如放热,试样温度高于参比物温度,放置在它们下面的一组差示热电偶产生温差电势U ΔT ,经差热放大器放大后送入功率补偿放大器,功率补偿放大器自动调节补偿加热丝的电流,使试样下面的电流Is减小,参比物下面的电流IR 增大,而Is +IR 保持恒定。降低试样的温度,增高参比物的温度,使试样和参比物之间的温差ΔT 趋于零。上述热量补偿能及时,迅速完成,使试样和参比物的温度始终维持相同。 设两边的补偿加热丝的电阻值相同,即RS =RR=R,补偿电热丝上的电功率为PS=IR 和P R=IR 。当样品没有热效应时,PS=P R;当样品存在热效应时,PS 和PR 的差ΔP能反映样品放(吸)热的功率: ΔP= PS-PR= IR -IR=(I S+IR)( I S-IR)R =(IS+IR ) ΔV =I ΔV? (1) 由于总电流IS+IR 为恒定,所以样品的放(吸)热的功率ΔP只和ΔV 成正比, 3 1 2 4 5
最新差热分析DTA实验报告
差热分析DTA 一、实验目的 掌握热分析方法─差热分析法基本原理和分析方法。 了解差热分析和热重分析仪器的基本结构和基本操作。 二、差热分析基本原理 差热分析法(Differential Thermal Analysis,DTA)是在程序控温下测量样品和参比物的温度差与温度(或时间)相互关系的一种技术。 物质在加热或冷却过程中会发生物理或化学变化,同时产生放热或吸热的热效应,从而导致样品温度发生变化。因此差热分析是一种通过热焓变化测量来了解物质相关性质的技术。样品和热惰性的参比物分别放在加热炉中的两个坩埚中,以某一恒定的速率加热时,样品和参比物的温度线性升高;如样品没有产生焓变,则样品与参比物的温度是一致的(假设没有温度滞后),即样品与参比物的温差DT=0;如样品发生吸热变化,样品将从外部环境吸收热量,该过程不可能瞬间完成,样品温度偏离线性升温线,向低温方向移动,样品与参比物的温差DT<0;反之,如样品发生放热变化,由于热量不可能从样品瞬间逸出,样品温度偏离线性升温线,向高温方向变化,温差DT>0。上述温差DT(称为DTA 信号)经检测和放大
以峰形曲线记录下来。经过一个传热过程,样品才会回复到与参比物相同的温度。 在差热分析时,样品和参比物的温度分别是通过热电偶测量的,将两支相同的热电偶同极串联构成差热电偶测定温度差。当样品和参比物温差DT=0,两支热电偶热电势大小相同,方向相反,差热电偶记录的信号为水平线;当温差DT10,差热电偶的电势信号经放大和A/D换,被记录为峰形曲线,通常峰向上为放热,峰向下为吸热。差热曲线直接提供的信息主要有峰的位置、峰的面积、峰的形状和个数,通过它们可以对物质进行定性和定量分析,并研究变化过程的动力学。峰的位置是由导致热效应变化的温度和热效应种类(吸热或放热)决定的,前者体现在峰的起始温度上,后者体现在峰的方向上。不同物质的热性质是不同的,相应的差热曲线上的峰位置、峰个数和形状也不一样,这是差热分析进行定性分析的依据。分析DTA 曲线时通常需要知道样品发生热效应的起始温度,根据国际热分析协会(ICTA)的规定,该起始温度应为峰前缘斜率最大处的切线与外推基线的交线所对应的温度T(如图2),该温度与其它方法测得的热效应起始温度较一致。DTA峰的峰温Tp虽然比较容易测定,但它既不反映变化速率到达最大值时的温度,也与放热或吸热结束时的温度无关,其物理意义并不明确。此外,峰的面积与
热分析技术及其在高分子材料研究中的应用
第33卷第3期2008年9月 广州化学 Guangzhou Chemistry V ol.33, No.3 Sept., 2008 热分析技术及其在高分子材料研究中的应用 翁秀兰1,2 (1. 福建师范大学化学与材料学院,福建福州350007; 2. 福建省高分子材料重点实验室,福建福州350007) 摘要:简要介绍了热分析技术——热重法、差热分析、差示扫描量热法、热机械分析法和动态 机械热分析法等及其在高分子材料领域的广泛应用。热分析技术的方法具有快速、方便等优点, 在高分子材料的研究中发挥着重要作用。 关键词:热分析;高分子材料;应用 中图分类号:O657.99 文献标识码:A 文章编号:1009-220X(2008)03-0072-05 热分析技术是在程序控制温度下测量样品的性质随温度或时间变化的一组技术,它在定性、定量表征材料的热性能、物理性能、机械性能以及稳定性等方面有着广泛地应用。热分析技术已渗透到物理、化学、化工、石油、冶金、地质、建材、纤维、塑料、橡胶、有机、无机、低分子、高分子、食品、地球化学、生物化学等各个领域。 在高分子材料研究领域,随着高分子工业的迅速发展,为了研制新型的高分子材料与控制高分子材料的质量和性能,测定高分子材料的熔融温度、玻璃化转变温度、混合物的组成、热稳定性等是必不可少的[1-2]。在这些参数的测定中,热分析是主要的分析工具。 热分析技术主要包括:热重分析法(TG)、差热分析法(DTA)、差示扫描量热法(DSC)、热机械分析法(TMA)、动态热机械分析法(DMA)等。本文简要介绍了热分析技术及其发展前景及其在高分子材料研究领域的应用。 1 TG及其在高分子材料方面的应用 热重法(TG)是在程序温度控制下测量试样的质量随温度或时间变化的一种技术。热重分析主要研究在惰性气体中、空气中、氧气中材料的热的稳定性、热分解作用和氧化降解等化学变化;还广泛用于研究涉及质量变化的所有物理过程,如测定水分、挥发物和残渣,吸附、吸收和解吸,气化速度和气化热,升华速度和升华热;有填料的聚合物或共混物的组成等[3]。 1.1 高分子材料的组分测定 热重法测定材料组分,方法简便、快速、准确,经常用于进行高分子材料组分分析。通过热重曲线可以把材料尤其是高聚物的含量、含碳量和灰分测定出来,而对于高分子材料的混合物,如果各组分的分解温度范围不同的话,则可以利用TG来确定各个组分的含量[4]。 收稿日期:2007-11-13 作者简介:翁秀兰(1980-),女,福建福清人,研究实习员,负责热分析仪器及从事光催化研究。
热重分析实验报告
热重分析实验报告 南昌大学实验报告 学生姓名: _______ 学号: _______专业班级:__________ 实验类型:?演示?验证 ?综合?设计?创新实验日期:2013-04-09 实验成绩: 热重分析 一、实验目的 1.了解热重分析法的基本原理和差热分析仪的基本构造; 2.掌握热重分析仪的使用方法; 3.测定硫酸铜晶体试样的差热谱图,并根据所得到的差热谱图,分析样品在加热过程中发生的化学变化。 二、实验原理 热重法(TG)是在程序控制温度的条件下测量物质的质量与温度关系的一种技术。热重分析仪主要由天平、炉子、程序控温系统、记录系统等几个部分构成。最常用的测量的原理有两种,即变位法和零位法。所谓变位法,是根据天平梁倾斜度与质量变化成比例的关系,用差动变压器等检知倾斜度,并自动记录。零位法是采用差动变压器法、光学法测定天平梁的倾斜度,然后去调整安装在天平系统和磁场中线圈的电流,使线圈转动恢复天平梁的倾斜,即所谓零位法。由于线圈转动所施加的力与质量变化成比例,这个力又与线圈中的电流成比例,因此只需测量并记录电流的变化,便可得到质量变化的曲线。 热重实验仪器主要由记录天平、炉子、程序控温装置、记录仪器和支撑器等几个部分组成,其中最主要的组成部分是记录天平,它基本上与一台优质的分析天平相同,如准确度、重现性、抗震性能、反应性、结构坚固程度以及适应环境温度
变化的能力等都有较高的要求。记录天平根据动作方式可以分为两大类:偏转型和指零型,无论哪种方式都是将测量到的重量变化用适当的转换器变成与重量变化成比例的电信号,并可以将得到的连续记录转换成其他方式,如原始数据的微分、积分、对数或者其他函数等,用来对实验的多方面热分析。在上述方法中又以指零型天平中的电化学法适应性更强。发生重量变化时,天平梁发生偏转,梁中心的纽带同时被拉紧,光电检测元件的偏转输出变大,导致吸引线圈中电流的改变。在天平一端悬挂着一根位于吸引线圈中的磁棒,能通过自动调节线圈电流时天平梁保持平衡态,吸引线圈中的电流变化与样品的重量变化成正比,由计算机自动采集数据得到 TG 曲线。燃烧失重速率曲线 DTG 可以通过对曲线的数学分析得到。 热重分析原理如下图所示: 三、实验仪器及试剂 HCT-2 型 TG-DTA 综合热分析仪、镊子、五水硫酸铜晶体等 四、实验步骤 1、打开炉子,将左右两个陶瓷杆放入瓷坩埚容器,关好炉子在操作界面上调零。 2、将坩埚放在天平上称量,记下数值P1,然后将测试样放入已称坩埚中称量,记下试样的初始质量。 3、将称好的样品坩埚放入加热炉中吊盘内。 4、调整炉温,选择好升温速率。 5、开启冷却水,通入惰性气体。 6、启动电炉电源,使电源按给定的速率升温。 7、观察测温表,每隔一定时间开启天平一次,读取并记录质量数值。 8、测试完毕,切断电源,待温度降低至100摄氏度时切断冷却水。 五、实验结果及数据处理
差热分析_实验报告
学生实验报告 实验名称差热分析 姓名:学号:实验时间: 2011/5/20 一、实验目的 1、掌握差热分析原理和定性解释差热谱图。 2、用差热仪测定和绘制CuSO4·5H2O等样品的差热图。 二、实验原理 1、差热分析原理 差热分析是测定试样在受热(或冷却)过程中,由于物理变化或化学变化所产生的热效应来研究物质转化及花絮而反应的一种分析方法,简称DTA(Differential Thermal Analysis)。 物质在受热或者冷却过程中个,当达到某一温度时,往往会发生熔化、凝固、晶型转变、分解、化合、吸收、脱附等物理或化学变化,因而产生热效应,其表现为体系与环境(样品与参比物之间)有温度差;另有一些物理变化如玻璃化转变,虽无热效应发生但比热同等某些物理性质也会发生改变,此时物质的质量不一定改变,但温度必定会变化。差热分析就是在物质这类性质基础上,基于程序控温下测量样品与参比物的温度差与温度(或时间)相互关系的一种技术。 DTA的工作原理(图1 仪器简易图)是在程序温度控制下恒速升温(或降温)时,通过热偶点极连续测定试样同参比物间的温度差ΔT,从而以ΔT对T 作图得到热谱图曲线(图2 差热曲线示意图),进而通过对其分析处理获取所需信息。 图1 仪器简易图
实验仪器实物图 图2 差热曲线示意图 在进行DTA测试是,试样和参比物分别放在两个样品池内(如简易图所示),加热炉以一定速率升温,若试样没有热反应,则它的温度和参比物温度间温差ΔT=0,差热曲线为一条直线,称为基线;若试样在某温度范围内有吸热(放热)反应,则试样温度将停止(或加快)上升,试样和参比物之间产生温差ΔT,将该信号放大,有计算机进行数据采集处理后形成DTA峰形曲线,根据出峰的温度 及其面积的大小与形状可以进行分析。 差热峰的面积与过程的热效应成正比,即 ΔH。式中,m为样品质量;b、d分别为峰的 起始、终止时刻;ΔT为时间τ内样品与参比物的温差;
实验二 热重-差热分析法
实验二热重-差热分析法 一、实验目的 1.掌握热重和差热分析的基本原理。 2.学习热重和差热分析仪的操作。 3.学会定性解释差热谱图。 4.用差热仪测定绘制CuSO4·5H2O的DTA曲线,分析其水分子的脱去顺序。 二、实验原理 差热分析(DTA)是在程序控制温度下,建立被测量物质和参比物的温度差与温度关系的一种技术。数学表达式为 △T=Ts-Tr=f(T或t) 其中:Ts ,Tr分别代表试样及参比物温度;T是程序温度;t是时间。记录的曲线叫差热曲线或DTA曲线。
本实验以α – Al2O3作为参比物质,记录CuSO4·5H2O的DTA曲线,从而考察其失去五分子结晶水的情况。 物质受热时,发生化学变化,质量也就随之改变,测定物质质量的变化也就随之改变,测定物质质量的变化就可研究其变化过程, 热重法(TG)是在程序控制温度下,测量物质质量与温度关系的一种技术,热重法实验得到的曲线称为热重曲线(TG曲线)。 三、实验仪器: 差热分析仪 由加热炉、试样容器、热电偶、温度控制系统及放大、记录系统等部分组成。 四、实验步骤: 1.依次开启稳压电源、工作站、气体流量计、主机(开关均在后面)、电脑,打开氮气瓶,使之压力为0.5MP。 2.打开炉子,手动在左右两个陶瓷杆放入铝坩埚容器,关好炉子,在操作界面上调零,仪器自动扣除了空坩埚的重量。 3.打开炉子取出样品坩埚容器将约5-10mg的样品研成粉末放入铝坩埚容器。 4.打开软件TA-60WS Collection Monitor 点击measure,出现measure parameter,在这里我们可以设置所需要的程序温度,然后点击Start,要我们文件保存在哪里。 5.单击Start。 6.仪器测定结束。 四、结果处理 1.仪器结束后,打开软件TA60,找到要保存的结果文件。 2.依次找到重量线,热线,程序升温线。
南京大学-差热分析实验报告
差热分析 近代物理实验 一.实验目的 1?掌握差热分析的基本原理及测量方法。 2?学会差热分析仪的操作,并绘制CuSO4 5H2O等样品的差热图。 3?掌握差热曲线的处理方法,对实验结果进行分析。 二.实验原理 1、差热分析基本原理 物质在加热或冷却过程中,当达到特定温度时,会产生物理或化学变化,同时产生吸热和放热 的现象,反映了物质系统的焓发生了变化。在升温或降温时发生的相变过程,是一种物理变化,一般来说由固相转变为液相或气相的过程是吸热过程,而其相反的相变过程则为放热过程。在各种化学变化中,失水、还原、分解等反应一般为吸热过程,而水化、氧化和化合等反应则为放热过程。差热分析利用这一特点,通过对温差和相应的特征温度进行分析,可以鉴别物质或研究有关的转化温度、热效应等物理化学性质,由差热图谱的特征还可以用以鉴别样品的种类,计算某些反应的活化能和反应级数等。 在差热分析中,为反映微小的温差变化,用的是温差热电偶。在作差热鉴定时,是将与参比物 等量、等粒级的粉末状样品,分放在两个坩埚内,坩埚的底部各与温差热电偶的两个焊接点接触,与两坩埚的等距离等高处,装有测量加热炉温度的测温热电偶,它们的各自两端都分别接人记录仪的回路中在等速升温过程中,温度和时间是线性关系,即升温的速度变化比较稳定,便于准确地确定样品反应变化时的温度。样品在某一升温区没有任何变化,即也不吸热、也不放热,在温差热电偶的两个焊接点上不产生温差,在差热记录图谱上是一条直线,已叫基线。如果在某一温度区间样 品产生热效应,在温差热电偶的两个焊接点上就产生了温差,从而在温差热电偶两端就产生热电势差,经过信号放大进入记录仪中推动记录装置偏离基线而移动,反应完了又回到基线。吸热和放热效应所产生的热电势的方向是相反的,所以反映在差热曲线图谱上分别在基线的两侧,这个热电势的大小,除了正比于样品的数量外,还与物质本身的性质有关。 将在实验温区内呈热稳定的已知物质与试样一起放入一个加热系统中,并以线性程序温度对它们加热。如以AI2O3为参比物,它在整个试验温度内不发生任何物理化学变化,因而不产生任何热
实验差热热重
实验5 热重、差热分析实验 一.实验目的与基本要求 1.在固相反应中,通过对材料基本性质的了解,利用其基本性质参数,试设计出一条合理的温度曲线,利用综合热分析仪(ZRY-1P、ZRY-2P)对其进行测试分析,通过对比,得到最优烧结方案。 2.理解热重分析和差热分析的基本原理。 3.了解高温综合热分析仪(ZRY-2P)的组成及组成各系统的基本工作原理。 4.掌握高温综合热分析仪的具体测量方法。 5.当各种固体氧化物、盐类发生熔融、相变、分解、化合、脱水、凝固、蒸发、升华等特定过程时,对其进行热重分析和差热分析。 6.对实验数据进行处理,根据得到的一系列热重曲线(TG)、微分热重曲线(DTG)和差热曲线(DTA),对物质发生的具体过程进行热分析。 二.实验原理与温度曲线的设计 固相反应是一系列合金、传统硅酸盐材料以及新型无机功能材料生产过程中的基础反应。固相反应是固体参与直接化学反应并起化学变化,同时至少在固体内部或外部的一个过程中起控制作用的反应。固相反应除固体间的反应外也包括有气、液相参与的反应。例如金属氧化、碳酸盐、硝酸盐和草酸盐等的热分解反应、粘土矿物的脱水反应以及煤的干馏等反应。 固相反应的共同特点有:首先,固体质点(原子、离子或分子)间具有很大的作用键力,故固态物质的反应活性通常较低,速度较慢。其次,在低温时固体在化学上一般是不活泼的,因而固相反应通常需在高温下进行。而且由于反应发生在非均一系统,传热和传质过程都对反应速度有重要影响。而伴随反应的进行,反应物和产物的物理化学性质将会变化,并导致固体内部温度和反应物浓度分布及其物性的变化,这都可能对传热、传质和化学反应过程产生影响。 在具体的反应中为了得到预定的产物,使反应向着希望的方向进行,各种固体氧化物、盐类发生熔融、相变、分解、化合、脱水、凝固、蒸发、升华等特定过程需要适当的温度和持续时间,在对具体反应物基本性质的了解,利用其基本性质参数的基础上,试设计出一条适宜的温度曲线,利用高温综合热分析仪(ZRY-2P)对其进行测试,通过对实验结果的分析比较,得到最优温度方案。 综合热分析仪是具有微机数据处理系统的热重-差热联用热分析仪器,是一种在程序温度(等速升温、
《差热分析》报告
实验二差热分析 姓名 ________ 学号 ________ 院系 ________
差热分析 一引言 差热分析 (Differential Thermal Analysis. 简称 DTA) 就是通过温差测量来确定物质的物理 化学性质的一种热分析方法。本文通过实验讨论了如何分析DTA 的结果以获得有效的信息,并阐述了影响差热分析效果的各种因素。 二实验原理 物质在受热或冷却过程中,当达到某一温度时,往往会发生熔化、凝固、晶型转变、分 解、化合、吸附、脱附等物理或化学变化,并伴随着有焓的改变,因而产生热效应,其表现 为物质与环境 (样品与参比物 )之间有温度差。差热分析( DTA )是在程序控制温度下,测量物质与参比物之间的温度差与温度关系的一种技术。 DTA 曲线是描述试样与参比物之间的 温差(T)随温度或时间的变化关系。在DTA 实验中,试样温度的变化是由于相转变或反 应的吸热或放热效应引起的。如:相转变、熔化、结晶结构的转变、升华、蒸发、脱氢反应、断裂或分解反应、氧化或还原反应、晶格结构的破坏和其它化学反应。一般说来,相转变、 脱氢还原和一些分解反应产生吸热效应;而结晶、氧化等反应产生放热效应。
图 1 差热分析的原理图(1- 参比物 ; 2- 试样 ; 3- 炉体 ; 4- 热电偶)图2试样和参比物的升温曲线DTA 的原理如图 1 所示。将试样和参比物分别放入坩埚,置于炉中以一定速率ν=dT/dt 进行程序升温,以T s、T r表示各自的温度,设试样和参比物(包括容器、温差电偶等)的热 容量 C s、C r不随温度而变。则它们的升温曲线如图2所示。 若以T=T s-T r对 t 作图,所得 DTA 曲线如图3所示,在0-a 区间, T 大体上是一致的,形成DTA 曲线的基线。随着温度的增加,试样产生了热效应(例如相转变 ),则与参比物间的温差变大,在DTA 曲线中表现为峰。显然,温差越大,峰也越大,试样发生变化的 次数多,峰的数目也多,所以各种吸热和放热峰的个数、形状和位置与相应的温度可用来定 性地鉴定所研究的物质,而峰面积与热量的变化有关。 图 3DTA 吸热转变曲线 在热量测量中应用的最为广泛的计算式是Speil 式: t2Tdt= m a H A t1g s 式中 ma 是试样中活性物的质量,△H 是试样中活性物的焓变,g 是与仪器有关的系数,反映了仪器的几何形状试样和参比物在仪器中安置的方式对热传导的影响,λs 是试样的热导系数,△T 是试样和参比物的温度差,当g 和 s 作为常数处理时上式可以改写为:
热分析技术在金属材料研究中的应用解读
研究生课程论文 (2014 -2015 学年第一学期) 热分析技术在金属材料研究中的应用 提交日期:2014年12月 1 日研究生签名: 学号学院材料科学与工程学院 课程编号课程名称材料的物性及其测试技术 学位类别硕士任课教师 教师评语: 成绩评定:分任课教师签名:年月日
热分析技术在金属材料研究中的应用 摘要:介绍了热分析技术的一些常用的热分析方法,如热重分析、差热分析、差示扫描量热分析、热膨胀等;同时阐述了热分析技术在金属材料中的应用,如测定金属材料的相变的临界温度以及对磁性材料居里温度的测量,及相变的热效应等。 关键词:热分析技术金属材料研究应用 Application of thermal analysis technique in the research of metallic materials Jing Deng School of Materials Science and Engineering, South China University of Technology Abstract: The application of the thermal analysis technique and some commonly methods were introduced, such as thermogravimetry analysis (TGA), differential thermal analysis (DTA), differential scanning calorimetry (DSC), thermodilatometry and so on. The application of the thermal analysis technology in metallic materials was introduced, for example, to measure phase transition critical temperature of the metallic materials and the Curie temperature of the magnetic material and the thermal effect of the phase transition. Keywords: thermal analysis technique; metallic materials; research; application 1、前言 热分析是在程序控制温度下测量物质的物理性质与温度之间对应关系的一项技术。主要包括如下三个方面的内容:一是物质要承受程序控温的作用,即以一定的速率等速升温或降温;二是要选择一观测的物理量P,该物理量可以是热学、磁学、力学、电学、声学和光学的等;三是测量物理量P随温度T的变化,往往不能直接给出两者之间的函数关系[1]。 热分析主要用于研究物理变化(晶型转变、熔融、升华和吸附等)和化学变化(脱水、分解、氧化和还原等)。热分析不仅提供热力学参数,而且还能给出有参考价值的动力学数据。因此,热分析在材料研究和选择上,在热力学和动力学的理论研究上都是很重要的分析手段[2]。 按照测量的物理性质,国际热分析协会(ICTA)将现有的热分析技术分类[3-4],具体见表1。热分析技术种类繁多,应用甚广,本文将介绍主要的热分析技术及其在金属材料研究中的主要应用。 表1 ICTA关于热分析技术的分类 测试性质方法名称英文全称缩名称质量热重法Thermogravimetry Analysis TGA 等压质量变化测定Isobaric Mass-change Determination 逸出气检测Evolved Gas Detection EGD 逸出气分析Evolved Gas Analysis EGA 放射热分析Emanation Thermal Analysis TEA
试验11高聚物的差热热重分析
实验11 高聚物的差热热重分析 一、目的要求 1.了解差热分析的原理 2.通过实验掌握差热分析的实验技术 3.使用差热分析仪测定高聚物的T g、T m 二、原理 差热分析,简称DTA,是将被测试样加热或冷却时,由于温度导致试样内部产生物理或化学变化,追踪热量变化的一种分析方法。热重分析,简称TG,是将被测试样加热,由于温度导致试样重量变化的分析方法。ZRY系列综合热分析仪是具有微机数据处理系统的热重—差热联用热分析仪器,是一种在程序温度(等速升降温、恒温和循环)控制下,测量物质的质量和热量随温度变化的分析仪器。常用以测定物质在熔融、相变、分解、化合、凝固、脱水、蒸发、升华等特定温度下发生的热量和质量变化,广泛应用于无机、有机、石化、建材、化纤、冶金、陶瓷、制药等领域,是国防、科研、大专院校、工矿企业等单位研究不同温度下物质物理、化学变化的重要分析仪器。差热分析作为一种重要的热分析手段已广为应用,它可以研究高聚物对热敏感的各种化学及物理过程,物理变化如:玻璃化转变、晶型转变、结晶过程、熔融、纯度变化等;化学变化如:加聚反应、缩聚反应、硫化、环化、交联、固化、氧化、热分解、辐射变化等。需指出,由于高聚物的物理或化学变化对热敏感的特性是很复杂的,所以常需要结合其它实验方法如动态力学试验、气质联用等对差热分析热谱图进行深入研究,从而进一步探讨高聚物的结构和性能间的关系。 仪器由热天平主机、加热炉、冷却风扇、微机温控单元、天平放大单元、微分单元、差热放大单元、接口单元、气氛控制单元、 PC微机、打印机等组成。 实验时,将试样和惰性参比物(在测定的温度范围内不产生热效应的热惰性物质,常用?-氧化铝、石英粉、硅油等)置于温度均匀分布的坩埚(样品池)的适当位置,将坩埚(样品池)组合于加热炉中,控制其等速升温或降温。在此变温过程中,若试样发生物理或化学变化,则在对应的温度下吸收或放出热量改变其温度,使试样和参比物之间产生一定的温度(ΔT)。将ΔT放大,记录试样与参比物的温度ΔT随温度T的变化,即ΔT~T曲线。此曲线通常称为差热曲线或差热热谱。 刚开始加热时,试样和参比物以相同温度升温,不产生温度差ΔT=0,差热曲线上为平直的基线。当温度上升到试样产产玻璃化转时,大分子的链段开始运动。试样的热容发生明显的变化,由于热容增大需要吸收更多的热量,因而试样的温度落后于参比物的温度,产生了温度差,于是差热曲线上方出现一个转折,该转折对应的温度,即玻璃化转变温度(Tg)若试样是能结晶的并处于过冷的无定形状态,则在玻璃温度以上的适当温度进行结晶,同时放出大量的热量,此时试样温度较参比物上升快,差热曲线上表现为放热峰。再进一步加热,晶体开始熔融面需要吸收热量,试样温度暂时停止上升,与参比物之间产生了温度差,其差
差热分析实验报告概论
差热分析实验报告 赵启峰 131120132 摘要:本实验报告阐述了差热分析的基本原理、实验及数据处理方法,以三氧化二铝作为参照物,分别测量了锡样品和五水硫酸铜样品的差热曲线并对其进行了分析,最后对实验结果进行了讨论。 关键词:差热曲线锡五水硫酸铜 引言 差热分析(DTA)是在程序控制下测量物质和参比物之间的温度差与温度(或时间)关系的一种技术。描述这种关系的曲线称为差热曲线或DTA曲线。由于试样和参比物之间的温度差主要取决于试样的温度变化,因此就其本质来说,差热分析是一种主要与焓变测定有关并借此了解物质有关性质的技术。 实验目的 (1)了解差热分析的基本原理和实验基本步骤。 (2)测量五水硫酸铜和锡的差热曲线,并简单计算曲线峰的面积。 实验原理 物质在加热或冷却过程中会发生物理变化或化学变化,与此同时,往往还伴随吸热或放热现象。伴随热效应的变化,有晶型转变、沸腾、升华、蒸发、熔融等物理变化,以及氧化还原、分解、脱水和离解等化学变化。另有一些物理变化,虽无热效应发生但比热容等某些物理性质也会发生改变,这类变化如玻璃化转变等。物质发生焓变时质量不一定改变,但温度是必定会变化的。差热分析正是在物质这类性质基础上建立的一种技术。 若将在实验温区内呈热稳定的已知物质(参比物)和试样一起放入加热系统中(图1),并以线性程序温度对它们加热。在试样没有发生吸热或放热变化且与程序温度间不存在温度滞后时,试样和参比物的温度与线性程序温度是一致的。若试样发生放热变化,由于热量不可能从试样瞬间导出,于是试样温度偏离线性升温线,且向高温方向移动。反之,在试样发生吸热变化时,由于试样不可能从环境瞬间吸取足够的热量,从而使试样温度低于程序温度。只有经历一个传热过程试样才能回复到与程序温度相同的温度。 图1 加热和测定试样与参比物温度的装置示意图 在试样和参比物的比热容、导热系数和质量等相同的理想情况,用图1装置测得的试样和参比物的温度及它们之间的温度差随时间的变化如图2所示。图中参比物的温度始终与程序温度一致,试样温度则随吸热和放热过程的发生而偏离程序温度线。当T S-T R=ΔT为零时,
材料热重分析
材料热重分析 中国科学院广州化学研究所分析测试中心 ---李工--136--0304-4558 材料热分析是在程序温度控制下测量材料的物理性质与温度关系的一类技术。如释放出结晶水和挥发性物质,热量的吸收或释放,增重或失重,发生热-力学变化和热物理性质和电学性质变化等。它在定性、定量表征材料的热性能、物理性能、机械性能以及稳定性等方面 有着广泛地应用。 热分析技术已渗透到物理、化学、化工、石油、冶金、地质、建材、纤维、塑料、橡胶、有机、无机、低分子、高分子、食品、地球化学、生物化学等各个领域。 材料热分析主要检测项目: 熔点 结晶温度 热解性能 燃烧性能 结晶度 热阻等 熔融热焓 结晶热焓 导热系数 线膨胀系数 玻璃化转变温度 PCB板爆板时间T260与T288 测试方法: 1.比热容(specific heat capacity) –DSC法 DSC是在程序控制温度下,测量样品的热流随温度或时间变化而变化的技术。因此,利用此技术,可以对样品的热效应,如玻璃化转变、熔融、固-固转变、化学反应等进行研究。 玻璃化转变温度(Tg)-DSC法 2.TGA TGA是在程序控制温度下,测量样品的质量随温度或时间变化而变化的技术,利用此技术可以研究诸如挥发或降解等伴随有质量变化的过程。如果采用TGA-MS或TGA-FTIR的联用技术,还可以对挥发出的气体进行分析,从而得到更加全面和准确的信息。
3.TMA (热机械分析仪) TMA是测量样品在温度或时间以及外加力的作用下尺寸的变化。材料在温度变化时会有物性上的变化,如收缩膨胀、软化等,为了解在温度变化下的物性常使用的工具之一,而TMA主要是量测样品在温度变化下时的膨胀收缩现象,藉此可量得Tg(玻璃转化温度)或是CTE(膨胀系数)等数据。以TMA针对Tg以及CTE量测,对于一般电子产业、复合材料、高分子、玻璃、陶瓷、PCB印刷电路板产业制程的控制与改善,颇有帮助。
热重法分析实验报告
现代分析测试技术实验报告 实验名称:热重法分析一水草酸钙的差热 姓名:学号:专业:有机化学 实验日期:2017.10.10 指导老师:成绩: 一、实验目的: 1、掌握热重分析法的一般原理; 2、了解热重分析使用方法; 3、掌握热分析谱图的解析方法。 二、工作原理: 1、根据热电偶的测量原理,将一个热电偶制成传感器,将微量的样品置于传感器上,放入特殊的炉子内按一定的规律加热,当样品在一定的温度下发生吸放热的物理变化时,通过传感器就可以探测出样品温度的变化,进而通过专业的热分析软件,处理得出温度变化的数据或图形,根据图形再判断材料有可能发生的各种相变。 2、将传感器和样品构成的支架系统同时放在天平上, 当样品在一定的温度下发生重量的变化时,天平就可以立刻反应出来,通过专业的热分析软件,处理得出重量变化的数据或图形,同样根据图形再判断材料有可能发生的各种内在成分的变化。 3、将两张图放在一块,可以同时测试物质的重量和差热随温度的变化,进而在材料的物化分析方面得到更多的信息。 三、实验仪器和药品: 1、仪器:热重分析仪TG209F1(德国耐驰仪器制造有限公司)、直径为6mm的氧化铝坩埚 2、主要试剂:CaC2O4·H2O
四、实验操作步骤: 1、提前2小时检查恒温水浴的水位(保持液面低于顶面2cm );打开电源开关,在面板上启动运行,设定的温度值应比环境温度高约10---15℃,同时注意有无漏水现象; 2、依次打开电源开关:显示器、电脑主机、仪器测量单元、控制器,以及测量单元上的天平电源开关; 3、实验使用氮气,调节低压输出压力为0.03-0.05Mpa ; 4、在电脑上打开对应的TG209测量软件,待自检通过后,检查仪器设置;打开炉盖,将支架升起,放入空坩埚;待程序正常结束后冷却后,打开炉子取出坩埚,将样品平整放入后(以不超过1/3容积约10mg 为好)称重,然后打开基线文件,选择基线加样品的测量模式,编程运行,结束温度值为910℃; 5、待样品温度降至100℃以下时,先将支架升起方可打开炉盖,拿出坩埚; 6、不使用仪器时正常关机顺序依次为:关闭软件、退出操作系统、关电脑主机、显示器、仪器控制器、天平电源、测量单元。 五、数据记录与处理: 1、根据得到的曲线,读出试样质量发生变化前后的值及其所对应的温度,分析CaC 2O 4·H 2的TG 曲线上质量变化的原因: 一水合草酸钙100200300400500600700800温度 /℃40 5060 708090100TG /%质量变化: -13.15 %质量变化: -19.51 %质量变化: -30.32 %起始点: 156.3 ℃起始点: 452.0 ℃起始点: 730.6 ℃[1]
草酸钙的热重差热分析
草酸钙的热重差热分析文件排版存档编号:[UYTR-OUPT28-KBNTL98-UYNN208]
综合热分析法测定草酸钙 【实验目的】 (1)掌握热重-差热分析原理和ZCT-A型综合热分析仪的操作方法,了解其应用范围。 (2)对草酸钙进行热重及差热分析,测量化学分解反应过程中的分解温度。 (3)测量物质在加热过程中所发生的物理化学变化,绘制相应曲线,从而研究材料的反应过程。 【实验原理】 热分析是物理化学分析的基本方法之一。综合热分析研究物质在加热过程中发生相变或其他物理化学变化时所伴随的能量、质量和体积等一系列的变化,可以确定其变化的实质或鉴定矿物。热分析技术种类很多,比较常用的方法有(1)差热法(DTA),(2)热重法(TG)[包括微分热重(DTG)],(3)差示扫描量热法(DSC)。 (1)热重分析 热重分析是在程序控制温度下,测量物质质量与温度关系的一种技术。热重法实验得到的曲线称为热重(TG)曲线。TG曲线以温度作横坐标,以试样的失重作纵坐标,显示试样的绝对质量随温度的恒定升高而发生的一系列变化。这些变化表征了试样在不同温度范围内发生的挥发组分的挥发,以及在不同温度范围内发生的分解产物的挥发。如图1、图 2 CaC 2O 4 ·H 2 O的热重曲线,有三个非常明显的失重阶段。第一个阶段表 示水分子的失去,第二个阶段表示CaC 2O 4 分解为CaCO 3 ,第三个阶段表示
CaCO 3分解为CaO 。当然,CaC 2O 4·H 2O 的热失重比较典型,在实际上许多 物质的热重曲线很可能是无法如次明了地区分为各个阶段的,甚至会成为一条连续变化地曲线。这时,测定曲线在各个温度范围内的变化速率就显得格外重要,它是热重曲线的一阶导数,称为微分热重曲线[图1也现示出了CaC 2O 4·H 2O 的微分热重曲线(DTG )]。微分热重曲线能很好地 显示这些速率地变化。 图1 CaC 2O 4·H 2O 的TG-DSC 曲线(文献图) 图2 CaC 2O 4·H 2O 的TG 曲线(文献图) (2)差热分析(DTA )和差示扫描量热分析(DSC ) 差热分析(DTA )是在试样与参比物处于控制速率下进行加热或冷却地环境中,在相同地温度条件时,记录两者之间地温度差随时间或温度地变化。差示扫描量热分析(DSC )记录地则是在二者之间建立零温度差所需地能量随时间或温度的变化。 差热分析和差示扫描量热分析所得到的谱图或曲线常画成在恒定加热或冷却的速率下随时间或温度变化的形式,其横坐标相应于时间或温度,作差热分析测量时,纵坐标为试样与参比物之温差,而作差示扫描量热分析时,纵坐标为试样池与参比池之功率差(d ΔC/dt )。从图1可以看出,CaC 2O 4·H 2O 的DSC 曲线(DTA 曲线与DSC 曲线相似)有三个向 上的峰,分别表示CaC 2O 4·H 2O 热分解时发生了三个吸热反应。所以DSC (或DTA )反映的是所测试样在不同的温度范围内发生的一系列伴随着热现象的物理或化学变化。换言之,凡是有热量变化的物理和化学现象都
