金纳米粒子信号放大探针检测细胞浓度

金纳米粒子信号放大探针检测细胞浓度
2016-09-10 12:49来源:内江洛伯尔材料科技有限公司作者:研发部
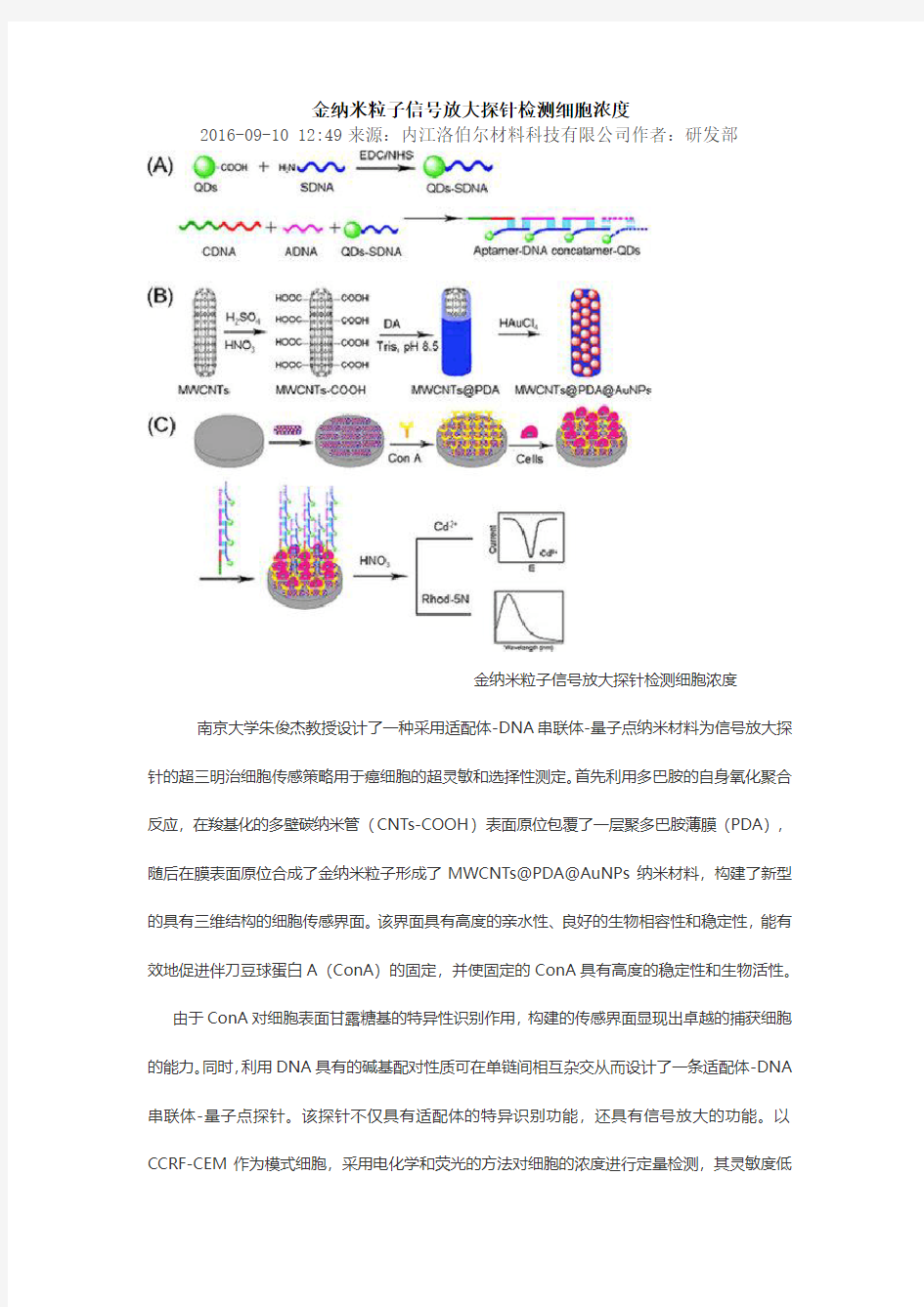
金纳米粒子信号放大探针检测细胞浓度南京大学朱俊杰教授设计了一种采用适配体-DNA串联体-量子点纳米材料为信号放大探针的超三明治细胞传感策略用于癌细胞的超灵敏和选择性测定。首先利用多巴胺的自身氧化聚合反应,在羧基化的多壁碳纳米管(CNTs-COOH)表面原位包覆了一层聚多巴胺薄膜(PDA),随后在膜表面原位合成了金纳米粒子形成了MWCNTs@PDA@AuNPs纳米材料,构建了新型的具有三维结构的细胞传感界面。该界面具有高度的亲水性、良好的生物相容性和稳定性,能有效地促进伴刀豆球蛋白A(ConA)的固定,并使固定的ConA具有高度的稳定性和生物活性。
由于ConA对细胞表面甘露糖基的特异性识别作用,构建的传感界面显现出卓越的捕获细胞的能力。同时,利用DNA具有的碱基配对性质可在单链间相互杂交从而设计了一条适配体-DNA 串联体-量子点探针。该探针不仅具有适配体的特异识别功能,还具有信号放大的功能。以CCRF-CEM作为模式细胞,采用电化学和荧光的方法对细胞的浓度进行定量检测,其灵敏度低
至50 cells mL-1。这一策略为癌细胞灵敏测定提供了新的途径,进一步为癌症的诊断和治疗提供了帮助。
金纳米探针
【摘要】由于金纳米粒子(AuNPs)具有与大小、形状和聚集程度相关的物理和化学特性,被广泛应用于各种生物分析和生物医学检测技术中,并发展成具有高选择性、高灵敏度的生物分析检测手段。以AuNPs为探针的分析方法通常具有简单、快速、灵敏度高的优点,并能应用于实际样品检测. 【关键词】金纳米粒子;探针;合成与修饰; 1 引言 纳米技术与化学、生物学、物理学和医学等领域的结合,对分析科学和生命科学领域的超灵敏检测和成像方法的发展起着越来越重要的 作用。由于AuNPs具有独特的光学性质(表面等离子体吸收和共振光散射)、易进行表面修饰以及良好的生物相容性(通常认为裸AuNPs 是无生物毒性的,而修饰后的AuNPs的生物毒性由其配体决定),因此功能化AuNPs的应用领域不断被拓宽,特别是其在生物分析和生物医药等领域的应用引起了人们广泛关注[2,3]。本文综述了生物分子修饰的AuNPs探针的合成及其在检测金属离子、小分子、DNA、蛋白质和细胞内分析等方面的新进展,以若干应用实例突显一些技术突破及发展趋势。 2 金纳米粒子的合成、稳定性和功能化 2.1 金纳米粒子的合成方法 金纳米粒子的制备方法可分为化学法和物理法。化学法是以金的化合物为原料,在还原反应生成金纳米粒子时控制粒子的生长,使其维持纳米尺度。化学合成法包括氧化还原法、电化学法、晶种法、模板法、
微乳液法、微波合成法和光化学法等,其中最具代表性并被广泛应用的有:(1)Turkevich-Frens法,即在100 ℃下,通过改变还原剂(柠檬酸钠)和三价金的化合物(氯金酸或氯金酸钠)的比例来控制AuNPs 粒径的大小,从而获得粒径在10~60 nm范围内且分散性较好的AuNPs。该方法制备程序简单,且包裹在AuNPs表面的柠檬酸根容易被其它配体置换(如巯基修饰的DNA等);(2)Brust-Schiffrin 法,即在两相(液/液)体系或单相体系中,以四正辛基溴化铵(TOAB)为相转移剂,将三价金的化合物(氯金酸或氯金酸钠)转移到有机相中,以烷基硫醇为稳定剂,NaBH4为还原剂,制备粒径为1~8 nm的AuNPs;硫醇/金盐的比例越大、加入还原剂速度越快,冷却溶液可以制得尺寸更小和单分散性更好的粒子,进一步通过配体交换反应改变AuNPs表面的配体而实现其功能化;(3)聚合物保护法:通常以含有聚乙二醇、硫醇或硫醚基团的聚合物为配体,以NaBH4为还原剂,制备水溶性或具有疏水性的粒径小于10 nm的AuNPs。聚合物稳定剂决定纳米粒子的溶解性;例如,采用硫醚或硫醇修饰的聚合物配体(烷基硫醚终端修饰的聚甲基丙烯酸等)一步法合成了具有高分散性的粒径小于5 nm的AuNPs,粒子的大小和分散性可以通过改变聚合物的结构、浓度和配体上能与金属结合的基团个数来控制,并且可以将粒径为1.1~1.7 nm的无荧光纳米粒子转变为荧光纳米粒子。物理法是利用各种技术将块状固体金分散为金纳米粒子,包括真空沉积法、电分散法、激光消融法等[12]。物理法容易控制AuNPs的形状并能获得图案化的AuNPs的阵列,但通常需要特殊的设备和技术,
二氧化硅生物荧光纳米颗粒的制备与应用
第33卷第4期湖南农业大学学报(自然科学版) Vol.33 No.4 2007年8月Journal of Hunan Agricultural University (Natural Sciences) Aug.2007 文章编号:1007-1032(2007)04-0496-04 二氧化硅生物荧光纳米颗粒的制备与应用 谢文刚a,b (湖南农业大学a.理学院;b.东方科技学院,湖南长沙 410128) 摘要:以荧光染料(联吡啶钌配合物)为核,二氧化硅为外壳制备了荧光纳米颗粒.电镜检测结果显示,合成的二氧化硅纳米颗粒粒径为(20±3) nm,分布均匀,形态规则.对荧光纳米颗粒进行生物修饰得到荧光探针,以DNA碱基配对原则为基础建立检测DNA的方法,利用激光扫描共聚焦显微镜研究玻片上的荧光信号和荧光强度.结果表明,该方法不仅可定量检测到4.4×10-8 mol/L的目标DNA3,而且可定性检测目标DNA3、单碱基错配DNA4及随机序列DNA5,为发展DNA检测技术提供了新的思路. 关键词:荧光纳米颗粒;核酸探针;DNA检测 中图分类号: O644 文献标识码:A Synthesis and application of silicon dioxide biological fluorescent nanoparticles XIE Wen-gang a,b (a. College of Sciences;b. College of Orient Science Technology,HNAU,Changsha 410128,China) Abstract:The Fluorescence-doped silicon nanoparticles were synthesized in a microemulsion system of triton-100 /cyclohexane/ ammonia hydroxide and characterized by techniques of electron microscopy.Nanoparticles were modified with biotin-DNA1 in order to obtain fluorescence probe.A method to monitor target DNA3 was set up on the basis of princile of DNA base complementary. Fluorescence signals were monitored by laser-scanning confocal microscopy for the detection of surface-bound fluorescent nanoparticles.The results showed that target DNA3 of 4.4×10-8 mol/L can be monitored by this method,which can also identify target DNA3 and single base unmatched DNA4 and random DNA5 effectively.The method potentially serves as a useful platform in a number of biomedical applications where accurate and sensitive gene analysis is critical. Key words:biological fluorescent nanoparticles;nucleic acid probe;DNA detect 生命体内痕量活性物质的分析与检测对获取生命过程中的化学与生物信息、了解生物分子及其结构与功能的关系、阐释生命活动的机理以及疾病的诊断都具有重要意义[1-3].生物荧光纳米颗粒的成功研制为在复杂的环境中进行最佳的单分子研究提供了条件.生物荧光纳米颗粒的粒径为1~100 nm,具有巨大的比表面、尺寸量子效应和化学反应活性,使其与生物体有特殊的相互作用,并得到了广泛应用,如可实现对SmIgG+ B淋巴细胞、HepG 肝癌细胞、WA系统性红斑狼疮疾病细胞和白血病特征细胞等的识别[4-5].但生物荧光纳米颗粒在DNA检测方面的应用鲜有报道[6].为此,笔者利用微乳液法制备二氧化硅纳米颗粒,并对其进行生物修饰,以DNA-DNA的特异识别与结合作用为基础,以三明治结构为模型(勿需对检测对象进行标记) ,研究了生物荧光纳米颗粒在DNA检测中的应用,旨在为发展新型DNA检测技术提供依据. 1 材料与方法 1.1 试验材料 联吡啶钌配合物([Ru(II)(bpy)3]2+.6H2O,Fluka 公司),链霉亲和素(美国Sigma公司),DNA片段(上海生工生物试剂有限公司合成).所用DNA的序列如下: 收稿日期:2007-01-10 基金项目:湖南农业大学基础科学基金(62020206002)作者简介:谢文刚(1966-),男,湖南吉首人,硕士,副教授,主要从事生物无机化学方面的研究.
基于金纳米粒子探针可视化检测基因点突变
基于金纳米粒子探针可视化检测基因点突变 2016-06-30 12:47来源:内江洛伯尔材料科技有限公司作者:研发部 纳米金识别单链和双链DNA过程示意图 基因点突变分析是分子生物学的一个重要话题. 在传统的点突变检测方法中,常采用各种标记探针, 如放射性元素探针、荧光色素探针及酶标记探针等; 或采用各种染色方法, 例如溴化乙锭(ethidium bromide,EB)染色. 这些技术大都存在着操作复杂、费时或费用昂贵等缺点, 因此发展一种简便、快速、低成本的基因检测方法具有重要意义. 目前, 纳米金(gold nanoparticles, Au-nps)作为一种新型的色团报告分子已被应用于基因检测中. 一方面,纳米金具有高的消光系数.例如, 尺径为 13和50 nm的金颗粒在波长为520 nm处的消光系数分别为2.7×108和1.5×1010 mol?L-1?cm-1, 它比常规有机发光团分子的消光系数高3~5个数量级; 另一方面, 纳米金的光学性质依赖于粒子直径以及间距, 由于纳米金胶颜色与粒子的聚集程度有密切关系, 根据其聚集程度的不同, 颜色可由酒红色逐渐变成粉色,紫色或灰色等. 纳米金表面修饰一段寡核苷酸序列制成纳米金探针, 在靶基因序列识别及单核苷酸多态性(single nucleotide polymorphism,SNP)分析中取得了显著的效果, 其中Mirkin等在纳米金探针的应用上开展了一系列具有开创性的工作. Rothberg等在2004年发展了一种新颖的纳米金比色基因检测(colorimetric detection)方法. 该法直接采用纳米金作为比色报告基团, 根据单链DNA (single-stranded DNA, ss-DNA)和双链DNA (double-stranded DNA, ds-DNA)与纳米金存在不同的静电作用, 即可实现对特定基因序列的识别及单核苷酸多态性的分析. 该法的检测原理如图所示. 单链和双链DNA具有不同的结构, 因此与纳米金存在不同的静电作用力; 单链DNA与纳米金之间存在的范德华力使单链DNA能够被吸附到纳米金颗粒表面,且吸附的速率与单链长度及环境温度有关; 而双链DNA 由于其骨架中带负电的磷酸根基团(PO43-)暴露在外, 与表面带负电荷的纳米金颗粒之间存在静电斥力, 使双链不能被吸附到纳米金颗粒表面. 表面吸附了DNA的纳米金能在较高浓度的盐溶液中不发生聚集. 因此, 纳米金在盐溶液的调控下能够比色识别单链和双链DNA, 进而达到判断基因是否发生杂交及分析单核苷酸多态性的目的. 等位基因特异性扩增(Allele-specificamplification,ASA)是利用DNA延伸过程中3'端碱基的特殊重要性所设计的扩增技术, 用于对已知突变基因进行检测, 是聚合酶链式反应(polymerase chainreaction, PCR)技术应用的发展. 等位特异性
SERS标记的金纳米棒探针用于免疫检测
2009年第67卷化学学报V ol. 67, 2009第14期, 1603~1608 ACTA CHIMICA SINICA No. 14, 1603~1608 * E-mail: jwhu@https://www.360docs.net/doc/994523279.html, Received March 2, 2009; revised April 5, 2009; accepted May 7, 2009.
1604化学学报V ol. 67, 2009 荧光谱峰较宽, 信号的选择性相对较差; 若用荧光分子标记, 还存在光解和光致褪色现象, 因而荧光标记技术亦有其局限性. 基于表面增强拉曼散射(SERS)的SERS 标记技术是一种光谱标记技术, 始建立于20世纪80年代末[8]. 它利用金或银等贵金属纳米颗粒来增强/放大表面吸附的拉曼活性分子的拉曼信号(即SERS), 以拉曼活性分子的SERS信号作为读出示踪信号. 近年来随着纳米科技的快速发展, SERS标记技术已引起了国内外科学家的广泛关注[9,10]. 首先, 拉曼光谱具有高度的分子特征性, 且谱峰窄, 能减小不同分子间的谱峰重叠. 其次, 在多元检测中一种波长的激发光就能激发出不同的拉曼活性分子的谱峰. 第三, SERS信号很少受光漂白的影响, 可在一定程度上为获得较好的SERS信号而延长积分时间. 第四, SERS信号不象荧光分子那样易发生自淬灭现象, 可通过增加拉曼活性分子数目来提高信号强度, 从而提高免疫检测的灵敏度. 目前, SERS免疫检测呈现几个基本的发展趋势[11]. 第一, 如何解决SERS标记免疫探针在固体基底上非特异性吸附造成的“假阳性”问题. SERS免疫检测的基本方法是标记抗体, 待测抗原和俘获抗体之间形成“三明治”夹心结构. 理想情况下, 探针上的抗体通过抗体和抗原之间的特异性免疫反应连接到俘获抗体上. 除此以外的吸附为非特异性吸附, 由此造成假阳性和背景信号升高等. 通常可利用牛血清白蛋白来封闭固体基底上的空位以减少非特异性吸附. 第二, 实现从单组分到多组分检测. Ni等[12]最早尝试了双组分检测. 国内顾仁敖课题组[13]也成功地进行了二组分检测, 并初步进行了三组分检测的尝试[11]. 第三, SERS探针的表面修饰. SERS 纳米探针的表面修饰可以减少标记分子从纳米颗粒表面脱落, 提高信号的稳定性, 并能有效减少探针的非特异性吸附问题. 除此以外, 探针还应具备水溶性、抗团聚和生物亲和性的特点. 目前, 表面修饰的发展趋势是从第一代裸纳米颗粒探针[12~15]到第二代的SiO2修饰的探针[10], 再到第三代高分子包覆的纳米探针[16]. 我们在前期的工作中已明确: 可将胶体的空间稳定理论作为设计制备各类纳米探针的理论依据[17], 即将生物亲和性高分子吸附在纳米颗粒/探针上, 以其提供的空间稳定来取代探针原来的电荷稳定机制. 由于稳定机制不同, 高分子稳定的纳米探针可以耐受高浓度盐等苛性条件而不团聚, 还可提供水溶性和生物亲和性等诸多优异的性能. 第四, 提高免疫检测的灵敏度. 由前述SERS免疫检测的基本方法可知, 提高免疫检测灵敏度实际上就是要提高SERS信号强度. 因此通常选择具有较大拉曼散射截面的分子作为标记分子. 除此以外, 另一个方案是全面借鉴SERS领域的研究成果, 采用具有较强增强能力的纳米颗粒来制备探针. 如Porter等[18]采用60 nm 的金颗粒来制备SERS免疫探针. Cao等[19]和徐等[20,21]则利用银染色技术来提高SERS信号. Cui等[22]采用表面具有孔洞的银核金壳颗纳米粒子来制备探针. Ji等[23]则采用金核银壳纳米颗粒来制备探针, 可通过改变Au/Ag 核与壳的厚度从而获得强的SERS信号. Sanles-Sobrido 等[24]采用颗粒聚集体来制备探针. 金纳米棒有着独特的光学性质, 并且在医学、传感和化学分离等方面有很好的应用前景, 近年来已成为人们研究的热点[25]. 金纳米棒有两个等离子体共振(SPR)吸收带: 横向SPR吸收峰和纵向SPR吸收峰, 其中纵向等离子体吸收峰的位置可以随其长径比的增大而逐渐红移[25]. 金纳米棒SPR的这种可调性使其能作为很好的SERS基底. 因为按照SERS的电磁场增强机制, 当激发光和SPR共振时, 可以最大程度提高单个纳米颗粒的增强能力[26]. 我们最近的实验和理论计算也证实: 当金纳米棒纵向SPR与632.8 nm的激发光耦合时, 其增强能力确实比耦合程度小或没有耦合时强[27]. 因而, 我们制备了长径比为2.5的金纳米棒, 使其纵向SPR和632.8 nm的激发光耦合. 并以此金纳米棒来制备SERS纳米探针, 进行SERS免疫检测研究. 1 实验部分 1.1 实验试剂 氯金酸、十六烷基三甲基溴化铵(CTAB)、硼氢化钠、硝酸银、抗坏血酸(AA)均为分析纯, 购自上海国药集团化学试剂有限公司. N,N'-二环己基碳酰亚胺(DCC)为分析纯, 购自上海共价化学科技有限公司. 对巯基苯甲酸(MBA)、3,3'-二硫代二丙酸(99%)、N-羟基丁二酰亚胺(NHS)购自Aldrich公司. 羊抗鼠IgG、小鼠IgG、牛血清蛋白(BSA), PBS缓冲液(pH=7.2)购自北京鼎国生物技术有限责任公司. α-甲氧基-ω-巯基聚乙二醇(mPEG-SH, M W=5000)由北京建凯科技有限公司特定合成. 四氢呋喃(THF)、丙酮、正己烷购自天津大茂化学试剂有限公司. 玻璃镀金基底由中国科学院安徽光学精密机械研究所提供. 先在清洗干净的玻璃片基底上真空镀上Ni-Cr层, 其上再镀上金. 实验用水为Mini-Q超纯水, 电阻率大于18.0 MΩ?cm-1. 1.2 3,3'-二硫代二丙酸丁二酰亚胺酯(DSP)的制备 0.4836 g 3,3'-二硫代二丙酸(2.3 mmol)溶于50 mL THF中, 向其中加入0.575 g (5 mmol) NHS, 在0 ℃下再加入1.03 g DCC (5 mmol), 在冰浴条件下搅拌反应36 h. 过滤除去副产物N,N'-二环己基脲(DCU), 将滤液旋转蒸发除去THF. 用丙酮/正己烷重结晶两次后得到白色固
荧光上上转换纳米粒子做近红外荧光探针
荧光上上转换纳米粒子做近红外荧光探针 由于在生物医学研究和临床治疗上的需求,光学成像技术在生物成像的应用方面发展迅猛,各种新手段、新材料、新方法不断涌现。近年来,随着各种功能强大的荧光探针的快速发展(如半导体纳米粒子、荧光蛋白、荧光有机分子等),光学成像技术已经越来越广泛的应用于生物体内成像研究。但是,由于需要光作为成像的信息源,生物组织对光的高散射和高吸收成为制约光学成像技术在生物体内成像的主要障碍。一般来讲,生物组织对可见区(350-700nm)和红外区(>1000nm)具有最强的吸收。相反,生物组织对近红外区(650-1000nm)光的吸收最少,因此近红外光可以穿透生物组织的距离最大。采用近红外荧光探针可以对深层的组织和器官进行探测和成像,这是可见区荧光探针所不能比拟的。我们在设计新一代荧光探针时必须考虑如何将探针的激发光和发射光调控到近红外区。 迄今为止,近红外荧光探针的种类非常有限,几乎全部属于有机荧光染料,而有机荧光染料作为生物体内荧光探针有很多缺点:第一,有机荧光染料容易被光漂白,不能长时间使用;第二,有机染料不适合同时多色成像,大多数染料只能被特定的波长有效激发,需要多个激发光源才能实现多色显示;第三,激发和发射波长不够稳定,容易随周围环境(如PH、温度等)而变化。为了克服这些缺点,人们正在发展用无机荧光纳米半导体粒子(量子点)来作为新一代荧光探针。与有机荧光染料相比,量子点具有很多优势:首先,量子点具有宽带吸收峰和很窄的发射峰,通过控制粒径可以得到从紫光到近红外的各种发光;其次,具有很高的荧光量子产率,发光稳定,不易被光漂白;并且,量子点容易实现修饰,可以在表面修饰各种有机分子和生物分子,进行生物检测和成像,一个量子点还可以修饰很多靶向分子。目前,发射近红外光的CdTe, CdS,HgS和CdSe 量子点已经作为近红外荧光探针应用在近红外生物细胞和组织成像研究上。然而,目前采用的这些量子点在生物成像中仍然存在一些问题。最主要的问题就是量子点的毒性,如量子点中含有的Cd, P和Hg等均对生物体有很大伤害。此外,量子点需要高能量的紫外或近紫外光激发,在采集荧光探针信号的同时,生物组织在高能量光源的激发下的产生自身荧光也会极大干扰荧光探针的信号,造成信噪比变差,从而不能检测深层生物组织的信号。长时间暴露在高能光源下还会造成生物组织的光损伤、蛋白质破坏和细胞死亡等。因此,开发新一代近红外荧光纳米粒子必须满足以下几个条件: 1.制备方法简便,绿色无污染,原料成本低。 2.发光稳定,不会被光漂白。 3.荧光量子产率高。
无机纳米材料简介
无机纳米材料简介 无机纳米材料是纳米材料从物质的类别来划分出的一种纳米材料。指其组成的主体是无机物质。 无机纳米材料主要包括:纳米氧化物、纳米复合氧化物、纳米金属及合金,以及其他无机纳米材料。 一、纳米氧化物: 纳米氧化物指的是粒径达到纳米级的氧化物,比如纳米二氧化钛 (T25),纳米二氧化硅(SP30),纳米氧化锌(JE01),纳米氧化铝(L30),纳米氧化锆,纳米氧化铈,纳米氧化铁等等。 纳米氧化物的基本技术指标包含:粒径,含量,比表面积,pH, 以及一些金属成分的含量。 纳米氧化物在催化领域的应用 纳米催化剂具有表面效应,吸附特性及表面反应等特性,因此纳米催化剂在催化领域的应用十分广泛。实际上,国际上已把纳米粒子催化剂称为第四代催化剂。我国目前在纳米材料的研究应用水平在某些方面处于世界领先地位,已实现产业化的SiO2(如VK-SP30)、CaCO3、TiO2(如VK-T25)、ZnO等少数几个品种,这些制备出来的纳米材料在催化领域中主要用于两个方面:一是直接用作主催化剂,二是作为纳米催化剂载体制成负载型催化剂使用。国际现在企业主要有杜邦,德固赛,国内的有杭州万景等企业生产纳米氧化物系列的产品。 2.1 石油化工催化领域 由于纳米材料颗粒的大小可以人工控制,又由于尺寸小,比表面积大,表面的键态和颗粒内部不同及表面原子配位不全等,从而导致表面的活性部位增加。另外,随着粒径的减小,表面光滑程度变差,形成了凹凸不平的原子台阶,这样就增加了化学反应的接触面。利用纳米微粒的高比表面积和高活性这些特性,可以显著提高催化效率。例如,纳米Ni粉可将有机化学加氢和脱氢反应速度提高15倍;超细Pt粉、碳化钨粉是高效的加氢催化剂;在甲醛氧化制甲醇反应中,使用纳米SiO2,选择性可提高5倍,利用纳米Pt催化剂,放在TiO2担体上,通过光照,使甲醇水溶液制氢产率
无机纳米材料在生物医学的应用
无机纳米材料在生物医学的应用 班级:材料科学与工程(1)班 姓名:何丽莉 学号:201473030107
摘要:主要介绍了几种介绍了介孔二氧化硅、纳米碳等非金属类纳米材料,以及磁性铁、氧化铈、银纳米粒子、金纳米粒子、镍等金属类纳米材料,比较了不同来源无机纳米材料的发展、特点、优势,明确了无机纳米材料具有环境友好、成本低、生物相容性好及低毒性等特点,综述了无机纳米材料在生物医药、临床诊断、疾病预防等生物医学方面的研究与应用。 关键词:无机纳米材料生物医学 Abstract: This paper mainly introduces several kinds of the mesoporous silica, nano carbon and other non metal nano materials, and magnetic iron, cerium oxide, silver nanoparticles, gold nanoparticles, nickel and other metal nano materials, compared the development of different sources of inorganic nano materials, features, advantages, the inorganic nano material is environmentally friendly low cost, good biocompatibility and low toxicity characteristics, the application of inorganic nano materials in the biomedical, clinical diagnosis, disease prevention research and application in biomedicine. Keywords: inorganic nano materials biomedicine
金纳米颗粒聚集以及金纳米探针 微阵列技术研究进展
金纳米颗粒聚集以及金纳米探针-微阵列技术研究进展 逄键涛 文思远 王升启# (军事医学科学院放射与辐射医学研究所,北京100850) 摘 要 金纳米颗粒 (GNP )探针正引起科学家们越来越多的兴趣。本文主要综述了基于GNP 自组装聚集反应的生物检测和微阵列-金标银染检测的最新进展,对GNP 在电化学等其他领域的研究前沿也进行了探讨。引用文献41篇。 关键词 金纳米颗粒,微阵列,生物检测,评述 2005-08-10收稿;2005-12-03接受 本文系国家863资助项目(No.2004BA519A46) 1 引 言 金纳米颗粒(GNP )是直径为0.8~250nm [1]的缔合胶体,具有纳米表面效应、量子效应、宏观量子 隧道效应。按粒子尺寸和聚集情况,GNP 可显示不同的颜色,已被广泛用于光学、电学、电子显微镜检 测的生物分子标记[2]。单个纳米颗粒的尺寸和颗粒间的组装形式,使胶体Au 溶液表现出不同的整体 特征。生物分子可参与到GNP 的聚集和组装过程中, 从而干扰GNP 的原始组装方式。通过胶体Au 溶液最终的物理状态(如颜色、吸光度等)可得到参与组装的生物分子的“质、量”特征,达到检测的目的。另外,GNP 逐渐在生物芯片检测中显现出应用前景。生物芯片技术本身是纳米尺度的分子操作和组装技术,芯片诊断、纳米检测等技术可以在此得到良好的融合。本文着重就GNP 自组装以及GNP 探针-微阵列技术进展作一综述。 2 生物分子辅助的GNP 聚集和组装 2.1 DNA-GNP 探针 灵敏度高、特异性强、快速简单、低成本是生物检测的重要指标。基于GNP 聚集反应的分子诊断方法能满足这些要求。Mirkin 发现DNA 特异杂交可使DNA-Au 颗粒自组装为复合结构,开创了GNP 用 于生物检测的新领域[3]。GNP 经巯基修饰的短链DNA 修饰成为编码探针[4],溶液中加入目标互补 DNA 后,纳米颗粒发生有序、可逆的聚集反应[5]。聚集后溶液颜色发生红7桃红7紫色变化,几小时出 现桃灰色沉淀(DNA-胶体金沉淀)。该现象是DNA 介导的胶体-胶体键合,其过程是可逆的。系统在没有优化的情况下能检测10fmol 的寡核苷酸。 DNA 修饰的GNP 以非交联结构聚集,对于颗粒表面结合的杂交体末端错配有很好的选择性[6],可 对单核苷酸多态性(SNP )进行检测。5个人瘤细胞系的基因组DNA 的检测结果与传统方法(质谱、直接测序)一致。这种方法不需要复杂的设备,为SNP 医护现场诊断、个性化医疗提供了可能。Storhoff 等[7]研究了GNP 距离和光学性质的关系,开发出“杂交-读出”的比色检测方法,鉴别核酸序列。DNA 修饰的金纳米探针识别核酸目标分子后发生颜色变化,可检测到zmol (10-21mol )级的核酸,不需要目 标分子的扩增或信号放大。S?nnichsen 等[8]采用等离子体耦合对金银纳米颗粒间距进行测量,研究了 金银纳米颗粒二聚体的实时组装以及单个DNA 分子杂交的动力学。 “等离子体标尺”可连续监控分子间距离上限达到70nm ,时间超过50min 。 2.2 非标记DNA 检测 双链DNA (dsDNA )比单链DNA (ssDNA )表面负电荷堆积程度高,并且dsDNA 的双螺旋结构使氮(N )、硫(S )等对GNP 亲和性高的原子包埋更深,所以ssDNA 和dsDNA 对GNP 有不同吸附力。 Li 等[9,10]据此设计了基于Au 颗粒聚集反应的核酸杂交比色检测方法。ssDNA 可吸附负电荷纳米金颗第34卷 2006年6月 分析化学(FENXI HUAXUE ) 评述与进展 Chinese Journal of Analytical Chemistry 第6期 884~888
金纳米粒子探针的合成及应用(一)
金纳米粒子探针的合成及应用(一) 作者:马立娜刘殿骏王振新 【摘要】由于金纳米粒子(AuNPs)具有与大小、形状和聚集程度相关的物理和化学特性,被广泛应用于各种生物分析和生物医学检测技术中,并发展成具有高选择性、高灵敏度的生物分析检测手段。以AuNPs为探针的分析方法通常具有简单、快速、灵敏度高的优点,并能应用于实际样品检测。本文综述了目前生物分子修饰的AuNPs探针的合成及其在检测金属离子、小分子、DNA、蛋白质和细胞内分析等方面的应用。 【关键词】金纳米粒子;探针;合成与修饰;评述 AbstractDuringlastdecade,goldnanoparticled(AuNPs)-basedassayshavebeenwell-developedandwidelyusedinbiologicalanalys isandbiomedicaldetectionbecauseAuNPshaveuniquephysicalandchemicalpropertieswhichdepend onthesize,shapeanddegreeofaggregation.TheAuNPs-basedassayshavealreadybeenemployedfordetectingpra cticalsampleswithhighsimplicityandselectivity.Thisreviewdiscussestherecentlydevelopmentofthes ynthesisandbiologicalmolecularfunctionalisationofAuNPsandtheirapplicationsontheheavymetallic cations,smallorganiccompounds,nucleicacidsandproteinsdetectionandcellularanalysis. KeywordsGoldnanoparticles;Probe;Synthesisandfunctionalization;Chemicalsensing;Review 1引言 纳米技术与化学、生物学、物理学和医学等领域的结合,对分析科学和生命科学领域的超灵敏检测和成像方法的发展起着越来越重要的作用1~5]。由于AuNPs具有独特的光学性质(表面等离子体吸收和共振光散射)、易进行表面修饰以及良好的生物相容性(通常认为裸AuNPs 是无生物毒性的,而修饰后的AuNPs的生物毒性由其配体决定),因此功能化AuNPs的应用领域不断被拓宽,特别是其在生物分析和生物医药等领域的应用引起了人们广泛关注2,3]。本文综述了生物分子修饰的AuNPs探针的合成及其在检测金属离子、小分子、DNA、蛋白质和细胞内分析等方面的新进展,以若干应用实例突显一些技术突破及发展趋势。 2金纳米粒子的合成、稳定性和功能化 2.1金纳米粒子的合成方法 金纳米粒子的制备方法可分为化学法和物理法。化学法是以金的化合物为原料,在还原反应生成金纳米粒子时控制粒子的生长,使其维持纳米尺度。化学合成法包括氧化还原法、电化学法、晶种法、模板法、微乳液法、微波合成法和光化学法等2],其中最具代表性并被广泛应用的有:(1)Turkevich-Frens法6,7],即在100℃下,通过改变还原剂(柠檬酸钠)和三价金的化合物(氯金酸或氯金酸钠)的比例来控制AuNPs粒径的大小,从而获得粒径在10~60nm范围内且分散性较好的AuNPs。该方法制备程序简单,且包裹在AuNPs表面的柠檬酸根容易被其它配体置换(如巯基修饰的DNA等)2,4];(2)Brust-Schiffrin法8,9],即在两相(液/液)体系或单相体系中,以四正辛基溴化铵(TOAB)为相转移剂,将三价金的化合物(氯金酸或氯金酸钠)转移到有机相中,以烷基硫醇为稳定剂,NaBH4为还原剂,制备粒径为1~8nm的AuNPs;硫醇/金盐的比例越大、加入还原剂速度越快,冷却溶液可以制得尺寸更小和单分散性更好的粒子,进一步通过配体交换反应改变AuNPs表面的配体而实现其功能化;(3)聚合物保护法:通常以含有聚乙二醇、硫醇或硫醚基团的聚合物为配体,以NaBH4为还原剂,制备水溶性或具有疏水性的粒径小于10nm的AuNPs。聚合物稳定剂决定纳米粒子的溶解性;例如,文献10,11]采用硫醚或硫醇修饰的聚合物配体(烷基硫醚终端修饰的聚甲基丙烯酸等)一步法合成了具有高分散性的粒径小于5nm的AuNPs,粒子的大小和分散性可以通过改变聚合物的结构、浓度和配体上能与金属结合的基团个数来控制,并且可以将粒径为1.1~1.7nm的无荧光纳米粒子转变为荧光纳米粒子。
金纳米棒的表面改性及其在生物医学领域的应用
进展评述 金纳米棒的表面改性及其在生物医学领域的应用 杨玉东 徐菁华 杨林梅 (沈阳工业大学理学院 沈阳 110870) 摘 要 各向异性的金纳米棒由于具有独特的光学性质,在生物医学领域得到了日益广泛的应用。本文综述了金纳米棒的表面改性及其在生物标记与识别、生物成像、癌症诊断和光热治疗等领域中的应用。 关键词 金纳米棒 表面改性 生物医学 Prepara ti on s and Surface M od i f i ca ti on s of Gold Nanorods for B i om ed i ca l Appli ca ti on s Yang Yudong,Xu J inghua,Yang L inmei (Shenyang University of Technol ogy,Shenyang110870) Abstract Because of its unique op tical p r operties,the anis otr op ic gold nanor ods have been widely used in bi omedical.The surface modificati ons of gold nanor ods and their app licati ons in the fields of bi omedical including bi orecogniti on,bi ol ogical i m aging,and cancer diagnosis and phot other mal therapy are su mmarized. Keywords Gold nanor ods,Surface modificati on,B i omedical 各向异性的金纳米棒(Gold nanor ods,Au NR s),由于其长径比可调,具有化学和光学上的各向异性[1],作为一类新的金纳米粒子已经引起材料科学和生命科学领域的巨大兴趣。在可见光区和近红外区,Au NR s具有横向和纵向表面等离子体共振峰(Surface Plas mon Res onance,SPR)[2~3],且在近红外区的等离子体表面的纵向吸收峰可实现人为调控,对光有强的吸收,以更高效率发出荧光和更强的散射光。 近红外光在生物化学和医学领域的应用中是一个强有力的工具,近红外波长范围正是生物组织具有的光学窗口。使用Au NR s和近红外光不仅能够在体外和体内两次发光成像[4],而且近红外激光照射可以控制Au NR s与质粒DNA络合物中的质粒DNA的释放[5]。另外,笔者还发现[6],近红外激光照射可将Au NR s重新塑型到球形纳米粒子。这种光照反应对于新型的基因传递具有潜在的作用。因此,Au NR s作为细胞成像的探针、光热治疗的载体或基因传递的功能材料是可行的[7,8]。 在应用于生物化学和医学领域中时,要求包含Au NR s在内的各种纳米粒子具有生物相容性和胶体稳定性。在Au NR s制备方法中,十六烷基三甲基溴化铵(CT AB)不仅是支持电解质,而且还是Au NR s的稳定剂和保护剂,得到的Au NR s表面都吸附有CT AB涂层[9]。但是,Au NR s溶液中的CT AB具有高毒性[10],会干扰生物过程,阻碍Au NR s与生物分子的偶联[11]。为了改进Au NR s的生物相容性,如何消除CT AB的影响、实现生物修饰是Au NR s在涉及生物体系应用中需要解决的关键问题。本文重点论述Au NR s的表面修饰及其在生物医学领域中的应用,并展望了它的发展趋势和应用前景。 Au NR s的表面改性有两种途径:一是表面改性材料与粒子表面依靠化学键结合,这通常是指一些小分子化合物;二是用主要包括表面活性剂、高分子材料、DNA生物分子及二氧化硅等有机或无机材料直接包裹Au NR s。 2009204215收稿,2009206229接受
点印迹法中的金纳米粒子探针
点印迹法中的金纳米粒子探针 2016-09-04 12:17来源:内江洛伯尔材料科技有限公司作者:研发部 金纳米粒子探针 这种分析方法主要利用金纳米粒子本身具有颜色,对白色基底(如硝化纤维膜)上点样点处的待检测物,进行染色定量分析。金纳米粒子表面需要修饰上,特定可以和待检测物结合的探针分子;待检测物通过吸附或其他方法附着固定在基底上,形成含有不同量待检测物的点样点。基底上样品点之外部分进行了封闭,尽量减少金纳米粒子在表面的非特异性吸附造成的干扰。将点样点在分散有修饰探针分子的金纳米粒子溶液中进行孵育,充分结合后取出,此时依据点样点上所固定的待检测物的量多少,结合了相应数量的金纳米粒子。再将点样点浸泡在银离子溶液中,银离子会在金纳米粒子表面沉积,使原有的颜色进一步加深,而结合的金纳米粒子越多,银沉积的也越多,有利于进一步增加信号灵敏度。 台湾国立台北大学Chun-Yen Huang等人利用点印迹法进行了免疫检测。他们合成了表面修饰有可以结合待检测分子的抗体(即探针分子)的金纳米粒子。检测时,将一定体积含有待检测分子的溶液滴在白色硝化纤维膜上,待检测分子可以吸附固定于膜表面;然后将膜在含有修饰了探针分子的金纳米粒子溶液中孵育,通过待检测分子-抗体的结合将金纳米粒子连接固定到膜表面。膜上金纳米粒子颜色越深,则该点样点处待检测分子越多,由此可以实现定量检测。
为了进一步增加检测灵敏度,他们在金纳米粒子表面沉积银,放大检测信号。实验比较表明,通过银沉积放大,可以将检测灵敏度提高1000倍(从100 amol 到100 zmol)。这个方法可以扩展到很多免疫检测上,只要在金纳米粒子表面修饰合适的抗体作为探针分子。 长春应用化学研究所汪尔康小组通过点印记阵列的方法,实现了对蛋白质凝血酶的简便、快速和灵敏的检测。该工作的一个特点是使用点印记法,另一个特点为采用适配子作为蛋白质检测探针。适配子一般是指具有特定序列,能特异性结合生物分子,如蛋白质或者小分子的单链DNA。蛋白质与对应适配子的结合,具有可以比拟“抗原-抗体结合”的特异性和结合常数,而适配子的合成、纯化非常简单,因此近年来适配子被普遍应用于蛋白质的检测。Wang等首先合成了粒径约13nm的金纳米粒子,再将其表面修饰上凝血酶的适配子。检测时,将含有待检测物凝血酶的溶液滴在硝化纤维膜(nitrocellulose membrane)上。凝血酶通过静电、疏水作用而固定在硝化纤维膜表面,再将膜上空余部分用10%牛血清白蛋白(BSA)封闭,减少其后金纳米粒子的非特异性吸附。然后,将硝化纤维膜浸泡在含有适配子修饰的金纳米粒子溶液中孵育。此时金纳米粒子便会和硝化纤维膜表面的凝血酶结合,凝血酶越多,结合的金纳米粒子越多,则该处颜色越深。经过银沉积到金纳米粒子上,可以进一步增加检测灵敏度。他们还检测了模拟实际样品的凝血酶含量,发现含有低于8%的血浆不会明显降低检测效果,但是10%以上的血浆会干扰检测。 以上点印迹法的检测灵敏度有了很大提高,但是仍需要训练有素的专业人员进行检测操作。为了进一步提高方法的实用性,有必要简化操作过程,降低复杂程度,以便日常家庭中的使用。
纳米金的应用
纳米金的应用 拓少杰 (陕西理工学院化学与环境科学学院应用化学1202班,陕西汉中723001) 指导教师:吴睿 [摘要]纳米金作为纳米家族的重要成员,除了具有纳米材料的一般性质外,还具有良好的光学特性、生物相容性及催化活性等独特的物理、化学性质。纳米金这些特殊的性质,使其在化学、生物、医药、食品等领域具有广泛的应用。本文重点就纳米金在食品安全检测领域、生物医药领域的应用作了详细综述,并对其未来的发展进行了展望。 [关键词]纳米金;应用;食品安全检测;生物医学 The application of gold nanoparticles ShaojieTuo (Grade12, Class 1202, Major in AppliedChemistry, School of Chemical & Environment science, Shaanxi University of Technology, Hanzhong 723001, Shaanxi) Tutor: Rui Wu Abstract: As animportant member of the nanoparticle family, gold nanoparticles have the general properties of nanometer materials and other good unique physical and chemical properties such as optical properties, biocompatibility, catalytic activity. Gold nanoparticles have a wide range of applications in the chemical, biomedicine, food and other fields.Based on these special properties, we mainly reviewed the application of gold nanoparticles in the field of Food safety inspection and biomedicine, as well asthe development in the future was prospected. Key words: gold nanoparticles; application; Food safety inspection;biomedicine 引言 纳米材料是指三维空间中至少有一维处于纳米尺度范围或由它们作为基本单元构成的材料[1]。纳米金是纳米材料的一种,为金的纳米级颗粒,直径一般在1 ~ 100 nm之间。纳米金的发展可追溯到16世纪现代化学的奠基人Paracelsus将制备得到的“饮用金”用于精神类疾病的治疗。而在1857年,英国科学家法拉第发现将少量电解质加入到氯金酸还原出的含纳米金的溶液中后,溶液会由红变蓝,最后变为无色,而当他在溶液中加入一些大分子物质(如明胶等)后,便可阻止该现象的发生。法拉第的这个发现为后来纳米金的应用奠定了牢固的科学基础[2]。 1 纳米金的性质 纳米金具有非常特殊的光学性质,主要表现在对光的吸收和散射两方面。当其吸收光时,由于表面等离子体共振的存在,一方面可以使纳米金将光能高效的转换为热能,另一方面也会根据纳米金粒径、形状的不同而产生不同的颜色变化。而当其发生光散射时,不仅会发生等离子体共振散射,还能增强拉曼散射的信号强度。此外,纳米金与其他荧光物质作用时表现出荧光增强和荧光淬灭两
