大鼠肝脏解剖图解
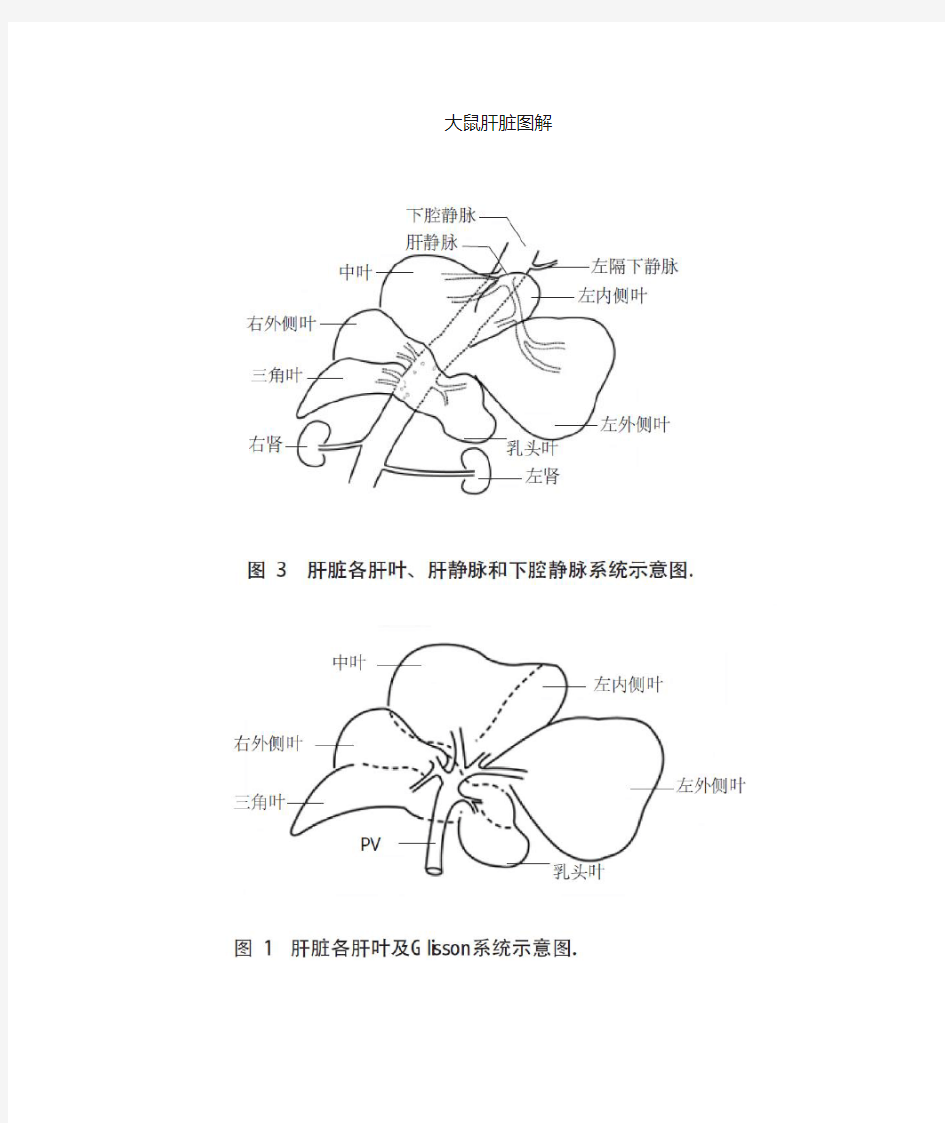
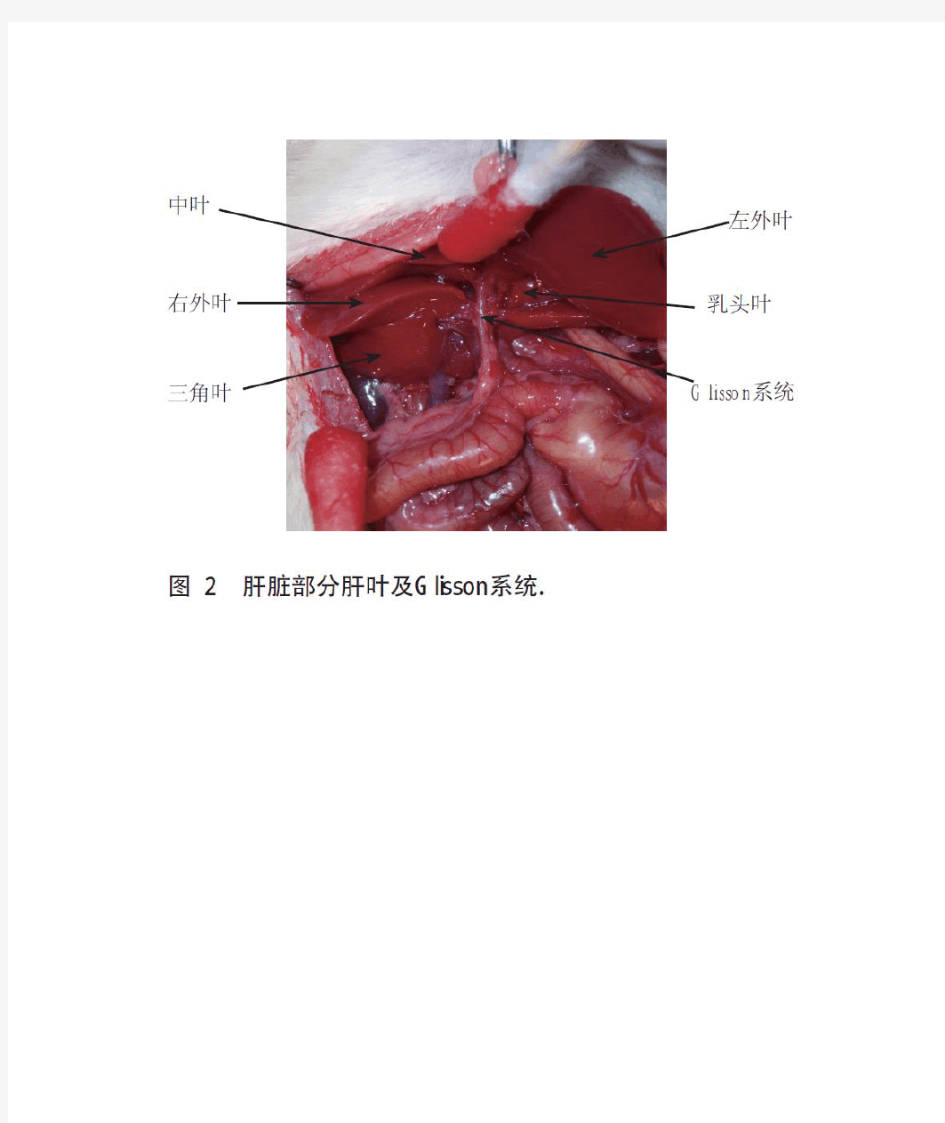
大鼠肝脏图解
大鼠系统解剖简述
第一章皮肤 一、皮肤由表皮、真皮和皮下组织构成。 二、皮肤腺有皮脂腺、汗腺和乳腺。 1、皮脂腺分布在毛囊周围。口角部、肛门、包皮和乳头周围有特化的皮脂腺。 2、汗腺,大鼠的汗腺只局限于足垫的皮肤。 3、乳腺 数量大鼠的乳腺共有6对,胸部3对,腹部1对,鼠蹊部2对。个别的大鼠有5对或者7对。 大小和形态随大鼠的年龄和性周期有明显的变化。 部位包埋在皮下组织中,由结缔组织隔与胸壁和腹壁松松地相连。 第二章骨 一.脊柱大鼠的脊柱由57 —61块脊椎骨组成,包括颈椎7、胸椎13、腰椎& 荐锥 4、尾锥27 —31块。锥式C7T13L6S4Cy27—31。骨性标志为第二胸椎,其棘突最高,超过其它脊椎骨。 1、颈椎和其它哺乳动物一样,恒为7块,全无肋骨相连,横突上具有横突孔,供锥动脉通过。 2、胸椎13块,椎骨的长度由前向后逐渐增加(由2毫米增加到4毫米),锥管的直径平均为3.3毫米,较颈部的锥管为狭窄。 3、腰椎6块,每块锥体的长度比较一致,约 6 —7毫米。锥管直径由前面的 4 毫米向后逐渐缩小至2毫米。 二、胸骨 共分为6节,最前一节为胸骨柄,第二到第五节称为胸骨体,最后一节为剑突,棒状的剑突后面接一盘状的剑状软骨。胸骨柄长约10毫米。 第三章肌肉系统(省略) 第四章消化系统 消化系统包括消化管及附属消化器官。消化管可分为口腔、食管、胃、小肠和大肠等部。附属消化器官有齿、舌、唾液腺、肝和胰。 第一节消化管
、口腔1、舌全长约30毫米,不具有正中系带,但是有两条侧系带。 一、食管 分为颈、胸、腹三部。成年大鼠食管的颈-胸段长度约75毫米,腹段通过膈的食管裂孔在膈后的长度约15毫米,食管外径约2毫米。 位置:食管主要是沿气管背侧走行,仅在颈部稍偏左侧。 一、胃 位置:横位于腹腔的左前部,其壁面几乎完全为肝的左叶所覆盖。 大小:胃重为体重的0.5% ,属单室胃。 形态:胃小弯朝向背前方,食管在其中部入胃。胃大弯朝向腹后方,其边缘 有双层的口袋状大网膜。贲门部外观呈半透明状,内壁有粘液腺。 三、小肠 1、十二指肠 长度:长约100毫米。 位置:从幽门发出向右后行,再折向前终于右侧。可分为降支(向右后行)、横支(水平部)、升支(向前行),它们构成一个不完全的环,包围着部分胰腺。 颜色:淡红色。 2、空肠 长度:为小肠的最长部分,大约有700—1000毫米。 位置形态:盘旋在腹腔的右方腹侧部。 3、回肠 长度:较短,约有40毫米。 位置形态:以三角形的系膜回盲褶与盲肠的末端相连,向盲肠的开口与结肠的起始部紧密相接。 二、大肠 1、盲肠 长度:是介于小肠与盲肠之间的一个大的盲囊。长约60毫米,直径约10毫米。位置:通常位于腹腔的左后部。盲肠呈锥体形,分为基部、体部和尖端。 2、结肠 长度:长约100毫米。
实验报告-大鼠
姓名:薛桂凤学号:132015200300 实验报告(二) 一、实验目的: 1.掌握大鼠的抓取和固定。 2.掌握大鼠的编号与标记方法。 3.掌握大鼠的常用实验方法。 4.掌握大鼠的常用麻醉方法。 5.掌握大鼠的安死术。 6.掌握大鼠的釆血方法。 7.了解小鼠的采尿、粪的方法。 8.了解小鼠各种脏器标本的采集方法。 二、实验器材:SD大鼠、电子称、手套、实验托盘、固定板、烧杯、注射器(3支)、 剪刀、镊子、灌胃针头、毛细管、酒精棉球、5%水合氯醛、生理盐水 三、实验内容 1.抓取:两种方法。第一种方法:右手食指和中指夹住大鼠颈部,使其头部固定,右 手拇指及无名指分别在大鼠前爪下抓住大鼠身体。第二种方法类似单手抓取小鼠的 方法,用右手拇指及其余四指并捏住大鼠颈部背部皮肤。 2.称重:小鼠放在烧杯中称重(去除烧杯重量),记录小鼠体重210g。 3.鉴别大鼠性别:观察生殖器雄性大鼠的阴囊非常明显。 4.编号:染色法:逆毛方向涂上有色斑点,顺序由左到右,由上向下,用两种颜色 可标记99只动物。 5.给药: (1)皮下注射小于1ml/100g(俯卧固定,左手拇指和食指捏住皮肤提起,右手持针沿纵轴方向刺入皮肤,阻力消失后回抽无血注入药物,拔针)(2)皮内注射小于0.1ml (麻醉后进行,先备皮)(俯卧固定,与皮肤平行刺入捏起的皮肤,阻力大,注射药物局部有皮丘后停留片刻后拔针)(3)腹腔注射0.01-0.02ml/g(仰面固定,在腹正中线两侧腹股沟平行的位置30-45°进针,挑起皮肤和肌肉,回抽无血,注药) (4)灌胃1-2ml/100g (大鼠固定身体呈一条直线,灌胃针头顺着上颚插入咽部,先少量注药证明未入气管后继续给药) 6.釆血:尾尖釆血法、眼眶静脉丛釆血法、心脏釆血法(麻醉后) 。 7.大鼠的采尿、粪的方法 (1)少量采集:在抓取固定时受到刺激排出少量尿液和粪便 (2)长期大量采集:使用代谢笼 8.麻醉:根据大鼠体重计算麻醉药物用量5%水合氯醛按300mg/kg,给药,计算药 量为 1.26ml,ip 麻醉小鼠,观察小鼠麻醉期。 (1)全身麻醉的第一期(随意兴奋期):出现运动和运动失调;35秒 (2)全身麻醉的第二期(不随意兴奋期):是由意识完全丧失至深而规则的自动 呼吸开始时止;2分30秒 (3)全身麻醉的第三期:角膜反射由迟钝渐趋消失,翻正反射消失,疼痛反射 消失; 9.安死术:颈椎脱臼法:用左手按住动物的头部于实验台上,右手抓住尾根部,快速、 不间断地向后、略向上使劲拉,以致脊椎脱臼,脊髓与脑干断离而死亡。 10.解剖:观察大鼠的脏器解剖结构
犬肝脏及附属管道的应用解剖
【摘要】目的:系统的整理犬肝脏及其附属管道的解剖学数据,为建立各种犬动物模型提供依据. 方法:戊巴比妥钠腹腔注射麻醉,取上腹部正中切口入腹,充分暴露肝脏,原位测量肝脏各叶径线及附属管道的长度和外径;切取肝脏,测量肝静脉及肝短静脉;切断各叶肝蒂,称各肝叶质量. 结果:原位观察68例,测量数据62份;离体观察43例,称重资料33份. 犬肝脏分为7叶,各肝叶形态、比例及质量较为恒定,具有独立的Glisson系统和肝静脉系统,肝动脉、肝静脉、胆道分支特殊,脾静脉一般分为上极和下极2支. 结论:成功的建立了犬肝脏及其附属管道的解剖学数据库,为以后建立各种犬动物模型奠定了基础. 【关键词】狗;肝;应用解剖 0引言 犬经常被用来制作各种动物模型,如门脉高压模型[1-2]、肝切除模型、肝硬化模型、肝衰模型、肝移植模型[3]等. 然而关于犬肝脏及附属管道的解剖没有系统研究报道. 为对后续有关犬肝脏、胆道的实验研究奠定基础,我们对68只家犬肝脏及附属管道进行了系统地的解剖学研究. 1材料和方法 1.1材料西安地区健康成年杂种犬68只,雌雄不限,最小犬龄20 mo,最大犬龄63 mo,平均犬龄(31.6±3.7) mo,平均质量(11.9±3.1) kg;器械包括常规的解剖学工具、磅秤(最小量程0.5 kg),天平(最小量程1 g),小分规及刻度尺(最小刻度1 mm)等. 1.2方法戊巴比妥钠(30 mL/L, 1 mL/kg)腹腔注射麻醉. 取上腹部正中切口入腹,自动拉钩向两侧牵开腹壁,游离肝胃韧带,左右三角韧带,充分暴露肝脏. 对肝脏进行解剖学观察,测量肝脏各叶径线,并对肝脏附属管道的长度和外径进行测量. 离体观测:处死动物,取下肝脏,保持其完整性,游离肝静脉及肝短静脉,观察第二肝门及第三肝门;切断各叶肝蒂,分别称各叶肝重. 本研究对犬所做处理符合西安交通大学伦理委员会相关规定并得到许可. 观测项目为肝脏位置及其与周围脏器的毗邻关系;肝分叶及形态;肝脏各叶径线及重量百分比;肝脏的韧带;肝脏附属管道. 统计学处理:数据以x±s表示. 统计学软件采用SPSS11.5数据包. 2结果 原位观察68例,测量数据62份. 离体观察43例,获称质量资料33份. 各观测项目结果如下. 2.1位置及毗邻犬肝脏位于横膈以后腹腔头侧. 尾状叶以凹陷切迹面与右肾相毗邻,两者间有肝肾韧带. 左外侧叶体积最大,隔小网膜遮盖舌叶(尾状叶乳头)、胃小弯、其左缘和食道相邻. 左中央叶遮盖左外侧叶右1/2. 方叶位于左中央叶和右中央叶之间,没有和别的肝叶相互遮盖. 右中央叶遮盖右外侧叶左1/2. 右外侧叶遮盖尾状叶. 左中央叶、方叶和右中央叶遮盖第一肝门. 胆囊附着于右中央叶左下方,与方叶右侧相邻. 肝下缘和肠道相邻.
大鼠解剖图
图Ⅷ-31左心房与左心室The left atrium and left ventricle 11左心房left atrium 12左心室left ventricle 13肺动脉右支right branch of pulmonary artery 14肺静脉pulmonary vein 15前腔静脉precavalvein 16肺动脉左支left branch of pulmonary art 7tery 17后腔静脉postcaval vein 18心中静脉 middle cardiac vein 19头臂动脉brachiocephalic artery 20主动脉弓aortic arch 21乳头肌papillary muscles 22左颈总动脉left common carotid artery 23左锁骨下动脉left subclavian artery 24右前腔静脉right precaval vein 25心外膜extracardium
图Ⅷ-56前肢内侧面The anterior limb. Medial aspect
图Ⅷ-57后肢内侧面(1)The posterior limb. Medial aspect(1) 1腋神经axillary nerve 2桡神经radial nerve 3头静脉cephalic vein 4正中神经median nerve 5正中动脉median artery 6肌支muscular branch 7尺神经ulnar nerve 8臂动脉brachial artery 9胸长神经long thoracic nerve 10胸外侧动脉external thoracic artery I1颈总动脉common carotid artery 12主动脉弓aorta arch 13左心耳left auricle 14右心耳right auricle 15食管esophagus 16胸主动脉thoracic aorta 17腹壁浅动脉superficial epigastric artery 18腹壁浅静脉superficial epigastric vein 19隐动脉saphenous artery 20隐大静脉great saphenous vein
实验报告-大鼠
姓名:薛桂凤学号: 实验报告(二) 一、实验目的: 1.掌握大鼠的抓取和固定。 2.掌握大鼠的编号与标记方法。 3.掌握大鼠的常用实验方法。 4.掌握大鼠的常用麻醉方法。 5.掌握大鼠的安死术。 6.掌握大鼠的釆血方法。 7.了解小鼠的采尿、粪的方法。 8.了解小鼠各种脏器标本的采集方法。 二、实验器材:SD大鼠、电子称、手套、实验托盘、固定板、烧杯、注射器(3支)、 剪刀、镊子、灌胃针头、毛细管、酒精棉球、5%水合氯醛、生理盐水 三、实验内容 1.抓取:两种方法。第一种方法:右手食指和中指夹住大鼠颈部,使其头部固定,右 手拇指及无名指分别在大鼠前爪下抓住大鼠身体。第二种方法类似单手抓取小鼠的 方法,用右手拇指及其余四指并捏住大鼠颈部背部皮肤。 2.称重:小鼠放在烧杯中称重(去除烧杯重量),记录小鼠体重210g。 3.鉴别大鼠性别:观察生殖器雄性大鼠的阴囊非常明显。 4.编号:染色法:逆毛方向涂上有色斑点,顺序由左到右,由上向下,用两种颜色 可标记99只动物。 5.给药: (1)皮下注射小于1ml/100g(俯卧固定,左手拇指和食指捏住皮肤提起,右手持针沿纵轴方向刺入皮肤,阻力消失后回抽无血注入药物,拔针)(2)皮内注射小于(麻醉后进行,先备皮)(俯卧固定,与皮肤平行刺入捏起的皮肤,阻力大,注射药物局部有皮丘后停留片刻后拔针) (3)腹腔注射(仰面固定,在腹正中线两侧腹股沟平行的位置30-45°进针,挑起皮肤和肌肉,回抽无血,注药) (4)灌胃1-2ml/100g (大鼠固定身体呈一条直线,灌胃针头顺着上颚插入咽部,先少量注药证明未入气管后继续给药) 6.釆血:尾尖釆血法、眼眶静脉丛釆血法、心脏釆血法(麻醉后) 。 7.大鼠的采尿、粪的方法 (1)少量采集:在抓取固定时受到刺激排出少量尿液和粪便 (2)长期大量采集:使用代谢笼 8.麻醉:根据大鼠体重计算麻醉药物用量5%水合氯醛按300mg/kg,给药,计算药 量为,ip 麻醉小鼠,观察小鼠麻醉期。 (1)全身麻醉的第一期(随意兴奋期):出现运动和运动失调;35秒 (2)全身麻醉的第二期(不随意兴奋期):是由意识完全丧失至深而规则的自动 呼吸开始时止;2分30秒 (3)全身麻醉的第三期:角膜反射由迟钝渐趋消失,翻正反射消失,疼痛反射 消失; 9.安死术:颈椎脱臼法:用左手按住动物的头部于实验台上,右手抓住尾根部,快速、 不间断地向后、略向上使劲拉,以致脊椎脱臼,脊髓与脑干断离而死亡。 10.解剖:观察大鼠的脏器解剖结构
大鼠和小鼠解剖图谱(照片版)
图Ⅷ-1整体骨骼侧面观The skeleton. Lateral View 图Ⅷ-2整体骨骼左前面观The skeleton. Left anterior view 1肋骨rib 2胸椎thoracic vertebra 3颈椎cervical vertebra 4颅骨cranium 5肩胛骨scapula 6肱骨hiimeius 7桡骨radius 8尺骨ulna 9掌骨metacarpal bone 10指骨digital bone 11腰椎lumbar vertebra 12髂骨ilium 13尾骨coccyx 14股骨femur 15髌骨patella 16腓骨fubula 17胫骨tibia 18跖骨metatarsal bone 19趾骨digital bone
图Ⅷ-4头骨侧面The skull. Lateral aspect
图Ⅷ-6下颌骨侧面The mandible. Lateral aspect
1枕骨occipital bone 2顶间骨interparietal bone 3矢状缝sagittal suture 4颧骨malar bone 5上颌骨maxillary bone 6前颌骨premaxillary bone 7枕外嵴external occipital creat 8顶骨parietal bone 9额骨frontal bone 10鼻骨nasal bone 11鼻间缝internasal suture 12前筛孔preethmoid pore 13蝶腭孔sphenopalatine foramen 14门齿 incisor tooth 15下颌骨mandible 16视神经孔optic foramen 17枕骨occipital bone 18茎突styloid process 19外耳道external acoustic meatus 20颞骨temporal bone 21 腭裂patoschisis 22臼齿molar tooth 23腭骨palatine bone 24翼孔pterygoid apertures 25破裂孔foramen lacerum 26枕大孔foramen magnum 27腭后孔posterior palatine foramen 28鼻后孔posterior nasal apertures 29卵圆孔foramen ovale 30鼓骨tympanic bone 31舌下神经孔hypoglossal foramen 32下颌联合mandibular symphysis 33颏孔mental foramen 34冠状突coronoid process 35下颌支ramus of mandible 36角状突process of horn 37下颌孔mandibular foramen 38翼肌窝pterygoid fossa 39髁突condylar process
大鼠的生物学特性和解剖学特点
大鼠的生物学特性和解剖学特点 1.大鼠性哺乳钢,啮齿目,鼠科,大鼠属动物。 2.繁殖快。大鼠2月龄时性成熟,性周期4天左右,妊娠期20(19~22),哺乳期21天,每天产仔平均8只,为全年、多发情性动物。 3.喜啃咬、夜间活动、肉食,白天喜欢挤在一起休息,晚上活动大,吃食多,因此白天除实验必须抓取外,一般不要抓弄它。食性广泛,喜吃各种煮熟的动物肉。对光照较敏感。 4.性情较凶猛、抗病力强。大鼠门齿较长,激恕、袭击抓捕时易咬手,尤其是哺乳期的母鼠更凶些,常会主动咬工作人员喂饲时伸入鼠笼的手。对外环境适应性强,成年鼠很少患病。一般情况下侵袭性不强,可在一笼内大批饲养,也不会咬人。 5.无胆囊:大鼠、鸽、鹿、马、驴、象等动物没有胆囊,它们的总胆肝管括约肌的阻力很少,肝分泌的胆汁通过总胆管进入十二指肠,受十二指肠端括约肌的控制。 6.不能呕吐:因此药理实验时应予注意。 7.垂体一肾上腺系统功能发达,应激反应灵敏。行为表现多样,情绪敏感。 8.视觉、嗅觉较灵敏,做条件反射等实验反应良好,但对许多药物易产生耐药性。 9.大鼠血压和血管阻力对药物反应敏感,但对强心甙的作用较猫敏感性低671倍。10.肝脏再生能力强,切除60~70%的肝叶仍有再生能力。 11.对营养、维生素、氨基酸缺乏敏感,可发生典型的缺乏症状。体内可以合成维生素C。 12.对炎症反应灵敏。它的眼角膜无血管。 13.生长发育期长,长骨长期有骨骺线存在,不骨化。 14.成年雌鼠在动情周期不同阶段,阴道粘膜可发生典型变化,采用阴道涂片法(Yaginal Smear Test)来观察性周期中阴道上皮细胞的变化,可推知性周期各个时期中卵巢、子宫状态与垂体激素的变动。 15.大鼠(包括小鼠)心电图中没有S-T段,甚至有的导联也不见T波,如有T波也是与S波紧挨着,或在R波降支上即开始,以致看不到等电线的S-T段。但心电图其他成分稳定,重复性好。豚鼠以上较大的动物均有明显的S-T段,在选择动物品种时应以注意。 16.大鼠垂体较脆弱地附着在漏斗下部,不需要很大的吸力就可以除去而不破坏鞍膈和脑膜,适宜于制作去垂体模型。大鼠也很适于作肾上腺和卵巢等内分泌腺切除手术。 17.大鼠肠道较短,盲肠较大,但盲肠功能不发达。不耐饥饿,肠内能合成维生素C。双子宫。胸部和鼠蹊部各有三对乳头。胰腺十分分散,位于胃和十二指肠弯曲处。染色体为21对,寿命3~4年。 18.大鼠的体温39(38.5~39.5)℃,心跳频率475(370~580)次/分,呼吸频率85.5(66~114)次/分,通气量7.3(5-10.1)ml/分,潮气量0.86(0.6~1.25)ml,耗氧量2000mm3/g体重,麻醉时收缩压116(88~138)mmHg红细胞总数8.9(7.2~9.6)百万mm3,血红蛋白14.8(12~17.5)g/100ml血,白细胞总数:5000~15000/mm3,血小板10~30万/mm3,血容量占体重的7.4%,红细胞比重1.090,总蛋白7.2(6.9~7.6)g%。
实验动物学实验报告大鼠,小鼠,小鼠的基本实验操作,大鼠的基本实验操作
实验一小鼠的基本实验操作 一、实验目的:通过实际操作,掌握小鼠的一般操作方法,包括小鼠的抓拿、标记、给药(灌 胃、腹腔注射、皮下、肌肉、尾静脉注射)、取血(眶后静脉丛,摘眼球)、脊椎脱臼法处死、大体解剖。 二、实验动物:昆明小鼠2只(1雌1雄) 三、实验步骤 1、抓取与固定,标记 2、去毛 3、给药:消化道、腹腔注射、尾静脉注射 4、取血:眼眶后静脉丛、尾静脉、眼球摘除法、断头法 5、麻醉:氯胺酮腹腔麻醉 6、处死:脊椎脱臼法 7、解剖: 雄性:睾丸、附睾、输精管、鼠蹊腺(在膀胱下方,胶质状,透明) 雌性:双角子宫、卵巢 肾上腺、胆囊、甲状腺、胃、肝脏、脾、肺、肾、心脏、甲状腺 四、实验结果 1、抓取与固定标记: 抓取:抓小鼠的尾根部 固定:抓住小鼠的尾根部,让小鼠在粗糙平面上爬行,后拉尾跟部,右手的拇 指与食指抓住小鼠两耳及其间的颈部皮肤,小指与无名指将尾巴固定在手掌面。并标记: 2、灌胃法:左手抓取小鼠固定后,右手持特制灌胃针,沿一侧口角进针,紧贴咽后壁,头后仰以便伸直消化道,进针2/3后灌生理盐水0、5ml 3、注射给药: 腹腔注射: 从下腹部的两侧进针 ,进针时针与腹部成45°。进针后稍微晃动针,如无粘滞感则可注射药物 尾静脉注射:一人固定小鼠,另一人用左手中指与拇指将尾拉直,食指托住尾部,在尾动脉位置进针注射0、5ml生理盐水。注射完毕拔出针头,用无菌棉球压迫止血。 4、采血 从眼角内侧0、5cm处进针 眼球摘除法:左手抓取用固定小鼠,右手持弯头镊在眼球根部将眼球摘除,头朝下,眼眶内血迅速流出。 5、麻醉: 0、5%氯胺酮腹腔麻醉:本小鼠重22g,按100mg/kg的药量给药,2分钟麻醉成功 6、处死: 脊椎脱臼法:按住头部,将尾根部向后上方以短促的力量拉即可致死 7、解剖: 雄性:寻找到睾丸、附睾、输精管、鼠蹊腺 雌性:双角子宫、卵巢 3、7、2 肾上腺:米粒大小 胰腺:位于胃下方,类似于脂肪组织,浑浊状 3、7、4 ,胆囊:芝麻大小,浅绿色,半透明,
实验大鼠取材方案
实验大鼠取材方案 [取材内容] 1.取大鼠静脉血,分离血浆、血清,-80℃保存。 2.取大鼠门静脉血,分离血清,-80℃保存。 3.取大鼠甲状腺组织,制备甲状腺电镜观察标本,其余组织液氮冰冻保存备用。 4.取大鼠胸腺组织,制备胸腺组织电镜观察标本、免疫组化观察标本,其余组织液氮冰冻 保存备用。 5.取大鼠肺组织,制备肺组织电镜观察标本、免疫组化观察标本,其余组织分装液氮冰冻 保存备用。 6.取大鼠肝脏组织,制备肝脏组织电镜观察标本、免疫组化观察标本,其余组织分装液氮 冰冻保存备用。 7.取大鼠胰腺组织,制备胰腺组织电镜观察标本、免疫组化观察标本,其余组织分装液氮 冰冻保存备用。 8.取大鼠肠系膜淋巴结组织,制备肠系膜淋巴结免疫组化观察标本,其余组织液氮冰冻保 存。 9.取大鼠胃部组织,制备胃粘膜组织电镜观察标本、免疫组化观察标本,其余组织分装液 氮冰冻保存备用。 10.取大鼠空肠组织,制备肠道粘膜组织电镜观察标本、免疫组化观察标本,其余组织分装 液氮冰冻保存备用。 11.取大鼠回肠组织,制备肠道粘膜组织电镜观察标本、免疫组化观察标本,其余组织分装 液氮冰冻保存备用。 12.取大鼠肾组织,制备左肾组织电镜观察标本、免疫组化观察标本,右肾组织液氮冰冻保 存备用。 13.取大鼠肾上腺组织,左侧制备肾上腺组织免疫组化观察标本,右侧肾上腺液氮冰冻保存 备用。 14.取大鼠睾丸组织,左侧制备电镜观察标本、免疫组化观察标本,右侧睾丸液氮冰冻保存 备有。 [试剂及药品] 戊巴比妥钠或10%水合氯醛、75%酒精、生理盐水、多聚甲醛或福尔马林液、3%戊二醛磷酸盐缓冲液(PBS0.01mol/LP pH7.4)或4%戊二醛、肝素钠、器械液(器械清洗消毒液) [器材] 备皮刀、解剖台、弯盘、组织剪、眼科剪、手术刀柄、刀片、小号弯式血管钳、蚊式血管钳、眼科镊、无损伤血管夹、聚乙烯管、三通管、丝线、培养皿、天平、一次性离心管(5ml、
大鼠取材方案
实验大鼠取材方案 [取材内容] 1. 取大歸脉血分离血衆血清-80 C保存。 2. 取大鼠门静脉血分离血清-80 C保存。 3. 取大鼠甲状腺组织.制备甲状腺电镜观察标本其余组织液氮冰冻保存备用〃 4. 取大鼠胸腺组织制备胸腺组织电镜观察标本、免疫组化孵标本其余组织液氮冰冻保存备用。 5. 取大鼠肺组织制备肺组织电镜观察标本,免疫组化观察标本其余组织分装液氮冰搽 保存备用。 6. 取大鼠肝脏组级制备肝脏组织电镜观察标本、免疫组化观察标本其余组织分装液氮冰冻保存备用。 7. 取大鼠觴组级制备康腺组织电镜观察标芯免疫组化观察标本其余组织分装液氮 冰冻保存备用。 8. 取大鼠肠系膜淋巴结组织制备肠系膜淋巴结免疫组化观察标本其余组织液氮冰冻保存。 9. 取鳩胃部组级制备胃粘膜组织电飙察标本免疫组化观察标本其余组织分装液氮冰冻保存备用。 10. 取大鼠空肠组级制备肠道粘膜组级电镜观察标本■免疫组化观集标本其余组级分装
液氮冰冻保存备用。 11. 取大鼠回肠组织制备肠道粘膜组织电镜观舉标技免疫组化观察标本其余组 织分装 液氮冰冻保存备用。 12. 取大關组织制备左肾组级电镜观察标本、免疫组化观察标本右肾组织液氮 冰探保 存备用。 13. 取大嵐肾上腺组织左侧制备肾上腺组级免疫组化观察标本右侧肾上腺液氮冰冻保 存 备用。 14. 取大鼠睾丸组级左侧制备电镜观察标本、免疫组化观察标本右侧睾丸液氮冰冻保存 备有。 [试剂及药品] 戊巴比妥钠或10%水合氯醛、75%酒精、生理盐水、多聚甲醛或福尔马林液、 3 应二醛 磷酸 盐缓冲液(PBS0.01mol/LP pH7.4)或 4 戍二肚肝素撤m器械清洗消毒液 [器材] 备皮刀、解剖台、弯盘、组织剪、眼科剪、手术刀柄、刀片、小号弯式血管钳、蚊式血管钳、 眼科镊、无损伤血管夹、聚乙烯管、三通管、丝线、培养皿、天平、一次性离2ml、1.5ml 、冻存氤肝麹真空采血管、微量移液議高速敲杠注射器10ml、5ml、
大鼠解剖方面的资料
1. 外观大鼠外观与小鼠相似,但个体较大。一般成年大鼠体长不小于18-20cm。尾上覆有短毛和环状角质鳞片,数量多于200片。上下颌各有两个切齿和六个臼齿,共16颗牙齿。齿式为(1003/1003)×2。 2. 大鼠骨骼约105-108块,大鼠的生长发育期长,长骨长期有骨骺存在,不骨化。切齿终生不断生长,大鼠需不断啃咬磨牙以维持其长度恒定,故垫料中应有部分小木块供其啃咬。 3. 大鼠唾液腺包括腮腺、颌下腺和舌下腺。分别位于下颌骨后缘至锁骨的腹外侧、下颌骨后缘和胸腔入口的腹侧、颌下腺口侧。颈区肩胛部间沉积的脂肪组织呈腺体状,称为冬眠腺,在产热中起着重要作用。 4. 胃由前后两部分组成,前胃为无腺区,后胃为有腺区,前后两部分由一个界限嵴分开,食管通过界限嵴的一个褶进入胃小弯,此褶是大鼠不能呕吐的原因。 5. 肠道分为十二指肠、空肠、回肠、盲肠、结肠、直肠。其中小肠最长,约114cm(102-126),盲肠较长,约6-8cm。 6. 肝脏呈紫红色,占体重的比例大,约为体重的1/25,由四叶组成(右侧叶、中叶、左叶和尾叶)。肝脏的再生能力强,经部分肝切除术后仍可再生。成年大鼠切除肝2/3,在一周内肝脏生长最快,三周内肝脏重量可恢复到接近正常。大鼠无胆囊,各肝叶的胆管会合成胆总管,开口于十二指肠。胰脏位于胃和十二指肠的弯曲处,呈淡粉色,形状不规则,似脂肪。 7. 心脏重量约占体重的1/30-1/20,由左心房、左心室、右心房、
右心室组成。左心室发出主动脉弓,由此分出无名动脉、左颈总动脉、左锁骨下动脉。无名动脉又分出右颈总动脉和右锁骨下动脉。主动脉弓到心脏背侧沿脊柱下行,形成背主动脉,背主动脉再分支到髂部和四肢。 8. 肺脏为海绵状,淡粉色,位于胸腔中部,分为左、右两部分。左肺为一个大叶,右肺分为4叶(前叶、中叶、副叶、后叶)。 9. 肾脏呈暗红色、蚕豆状,位于腹腔背侧脊柱两侧。每侧肾都和一条白色细长的输尿管相连,输尿管下接膀胱。 10. 大鼠的神经系统与人类相似,亦包括中枢神经系统和周围神经系统两部分。中枢神经包括脑和脊髓,周围神经包括脑神经、脊神经、植物神经。脑分为大脑、间脑、中脑、小脑和延脑,大鼠的大脑很发达,中脑较小。由脑发出的神经叫脑神经,共12对。脊神经和植物神经和其它动物相似。 实验用大鼠解剖生理学 一、概述 每年约使用3千5百万只鼠应用于研究和测试。使用实验大鼠进行的研究包括老化,肿瘤neoplasia,药效与毒性,含特定菌之动物gnotobiology,龋齿的研究,脂质新陈代谢,维他命之作用,行为,酒精中毒和肝脏硬化,关节炎,苯酮尿症(phenylketonuria),黄疸,果糖不耐症,高血压、胚胎学,畸胎畸形学,肾性尿崩症及传染性疾病等皆可使用大鼠进行研究。 二、解剖构造
小鼠肝脏取材步骤
小鼠肝脏组织取材步骤 小鼠肝脏组织取材步骤,并列出完成此次实验所需要的试剂、仪器、材料等相关物品及实验人员安排情况。 材料:小鼠 试剂:DMEM 戊巴比妥钠 75%酒精 PBS 器械消毒液戊二醛 仪器:解剖台备皮刀弯盘组织剪眼科剪手术刀柄刀片血管钳眼科镊 培养皿无菌手套 实验人员安排:小鼠养殖管理组准备工作组实验操作组 实验步骤: 1. 取材前夜禁食,自由饮水。 2. 小鼠称重,按照50mg/kg的比例用5ml的注射器配合针头抽取戊巴比妥钠备用。 3. 正左手的小指和无名指抓住大鼠的尾巴,另外三个手指抓住大鼠的颈部,使大鼠头部向向下。这样腹腔中的器官就会自然倒向胸部,防止注射器刺入时损伤大肠、小肠等器官。右手持注射器,从腹部近腿根处刺入后再腹部皮下穿行深入,动作轻柔,缓慢注射。注射完药物后,缓缓拔出针头,手指按住针口对小鼠腹部轻柔按摩,促进麻醉药物的吸收,掐小鼠尾部检测小鼠麻醉程度。 4.将小鼠四肢固定于解剖台上,暴露小鼠整个胸部和腹部,修剪去腹部毛发,75%酒精消毒。 5.沿腹侧正中线自阴茎上源由下而上剪开腹部皮肤直至剑突,向两侧钝性剥开皮肤与皮下组织,暴露腹壁浅肌层。沿白线钝性分离腹壁肌肉,剪开腹膜,暴露腹腔,将肝脏向上翻起,显露肝门,眼科剪剪除肝脏周围结缔组织和血管。 6.结扎剪断肝门管道系统,钝锐结合完整取出大鼠肝脏,放置于无菌培养皿,生理盐水冲洗,称重并记录。①切取肝左叶约1mm×1mm×1mm组织3块,3-戊二醛磷酸盐缓冲液(PBS0.01mol/LP pH 7.4)或4-戊二醛固定;②左叶肝组织浸入多聚甲醛或福尔马林液中固定;③右叶肝组织称重记录分装后全部放置于无菌冻存管液氮冰冻保存备用。 7.切取肝左叶约1mm×1mm×1mm组织3块,3-戊二醛磷酸盐缓冲液(PBS0.01mol/LP pH7.4)或4-戊二醛固定;左叶肝组织浸入多聚甲醛或福尔马林液中固定;右叶肝组织称重记录分装后全部放置于无菌冻存管液氮冰冻保存备用。
动物实验报告修订稿
动物实验报告 集团文件发布号:(9816-UATWW-MWUB-WUNN-INNUL-DQQTY-
实验动物学实验报告学院: 学号: 姓名 时间: 实验一:小鼠实验 一、实验目的 1、掌握小鼠抓取、固定的基本方法; 2、掌握小鼠的雌雄鉴别方法; 3、掌握小鼠的标记方法; 4、掌握小鼠的基本采血技术; 5、掌握小鼠的常用给药方法; 6、掌握小鼠的解剖方法,熟悉内部脏器的自然位置; 二、实验材料 1、实验动物:每组两只雌鼠,两只雄鼠; 2、实验器械及试剂:鼠笼;小鼠固定器和小鼠固定板;眼科剪;眼科镊;解剖刀;1ml注射器;毛细玻璃管;灌胃针;苦味酸染料;葡萄糖液;2%水合氯醛; 三、实验内容及方法 1、小鼠的抓取和固定 抓取时先用右手抓取鼠尾提起,置于鼠笼或实验台向后拉,在其向前爬行时,用左手拇指和食指抓住小鼠的两耳和颈部皮肤,将鼠体置于左手心中,把后肢拉直,以无名指按住鼠
尾,小指按住后腿即可。这种在手中固定方式,能进行实验动物的灌胃、皮下、肌肉和腹腔注射以及其他实验操作。 2、小鼠的雌雄鉴别 雄鼠的阴囊明显,雄鼠可见阴道开口和五对乳头。幼鼠或仔鼠则主要从外生殖器与肛门的距离判定,近者为雌,远者为雄。另外,雌鼠肛门和生殖器之间有一无毛小沟,而雄鼠则在肛门和生殖器之间长毛。 3、小鼠的标记方法 1)耳孔法 用耳号钳在耳上打洞或者用剪刀在耳边缘剪缺口,左耳为十位,右耳为个位。 2)剪趾法 适用于出生一周以内新生仔鼠; 3)染色法 用毛笔将苦味酸涂在动物的不同部位,注意逆着毛发生长方向刷。 4、小鼠的基本采血 1)剪尾采血 当所需血量很少时采用本法。固定动物并历出鼠尾,将鼠尾在45℃温水中浸泡数分钟,也可用酒精棉球涂擦,使局新血管扩张。将鼠尾擦干,再用刀片剪去1-2mm,让血液滴入盛器或直接用吸取,同时自尾根部向尾尖按摩。取血后,先用棉球压迫止血并立即用6%液体火棉胶涂于尾巴伤口处,使伤口外结一层火棉胶薄膜,保护伤口。也可采用切割尾静脉的方法采血,三根尾势脉可交替切割,并自尾尖向尾根方向切割,每次可取0.2~0.3ml 血,切割后用棉球压迫止血。这种采血方法在大鼠进行较好,可以较长的间隔时间连续取血,进行血常规检查。 2)眼眶后静脉丛取血
大鼠系统解剖简述(干货)
大鼠系统解剖简述 第一章皮肤 一、皮肤由表皮、真皮和皮下组织构成。 二、皮肤腺有皮脂腺、汗腺和乳腺。 1、皮脂腺分布在毛囊周围。口角部、肛门、包皮和乳头周围有特化的皮脂腺。 2、汗腺,大鼠的汗腺只局限于足垫的皮肤。 3、乳腺 数量大鼠的乳腺共有6对,胸部3对,腹部1对,鼠蹊部2对。个别的大鼠有5对或者7对. 大小和形态随大鼠的年龄和性周期有明显的变化。 部位包埋在皮下组织中,由结缔组织隔与胸壁和腹壁松松地相连。 第二章骨 一。脊柱大鼠的脊柱由57-61块脊椎骨组成,包括颈椎7、胸椎13、腰椎6、荐锥4、尾锥27—31块。锥式C7T13L6S4Cy27-31.骨性标志为第二胸椎,其棘突最高,超过其它脊椎骨。 1、颈椎和其它哺乳动物一样,恒为7块,全无
肋骨相连,横突上具有横突孔,供锥动脉通过。 2、胸椎13块,椎骨的长度由前向后逐渐增加 (由2毫米增加到4毫米),锥管的直径平均为 3。3毫米,较颈部的锥管为狭窄。 3、腰椎 6块,每块锥体的长度比较一致,约6-7 毫米。锥管直径由前面的4毫米向后逐渐缩小至2 毫米。 二、胸骨 共分为6节,最前一节为胸骨柄,第二到第五 节称为胸骨体,最后一节为剑突,棒状的剑突后面 接一盘状的剑状软骨。胸骨柄长约10毫米。 第三章肌肉系统(省略) 第四章消化系统 消化系统包括消化管及附属消化器官。消化管可 分为口腔、食管、胃、小肠和大肠等部。附属消 化器官有齿、舌、唾液腺、肝和胰。 第一节消化管 一、口腔 1、舌全长约30毫米,不具有正中系带,但是有两条侧系带。 一、食管 分为颈、胸、腹三部。成年大鼠食管的颈-胸段
长度约75毫米,腹段通过膈的食管裂孔在膈后的长度约15毫米,食管外径约2毫米. 位置:食管主要是沿气管背侧走行,仅在颈部稍偏左侧。 一、胃 位置: 横位于腹腔的左前部,其壁面几乎完全为肝的左叶所覆盖。 大小:胃重为体重的0.5%,属单室胃。 形态:胃小弯朝向背前方,食管在其中部入胃.胃大弯朝向腹后方,其边缘有双层的口袋状大网膜.贲门部外观呈半透明状,内壁有粘液腺. 三、小肠 1、十二指肠 长度:长约100毫米. 位置:从幽门发出向右后行,再折向前终于右侧.可分为降支(向右后行)、横支(水平部)、升支(向前行),它们构成一个不完全的环,包围着部分胰腺。 颜色:淡红色。 2、空肠 长度:为小肠的最长部分,大约有700-1000毫米。
大鼠系统解剖简述
大鼠系统解剖简述
第一章皮肤 一、皮肤由表皮、真皮和皮下组织构成。 二、皮肤腺有皮脂腺、汗腺和乳腺。 1、皮脂腺分布在毛囊周围。口角部、肛门、包皮 和乳头周围有特化的皮脂腺。 2、汗腺,大鼠的汗腺只局限于足垫的皮肤。 3、乳腺 数量大鼠的乳腺共有6对,胸部3对,腹部1对,鼠蹊部2对。个别的大 鼠有5对或者7对。 大小和形态随大鼠的年龄和性周期有明显的变化。 部位包埋在皮下组织中,由结缔组织隔与胸壁和腹壁松松地相连。 第 二章骨 一.脊柱大鼠的脊柱由57-61块脊椎骨组成,包括颈椎7、胸椎13、腰椎6、荐锥4、 尾锥27-31块。锥式C7T13L6S4Cy27 -31。骨性标志为第二胸椎,其棘突最 高,超过其它脊椎骨。 1、颈椎和其它哺乳动物一样,恒为7块,全无 肋骨相连,横突上具有横突孔,供锥动 脉通过。 2、胸椎13块,椎骨的长度由前向后逐渐增加(由 2毫米增加到4毫米),锥管的直径平 均为3.3毫米,较颈部的锥管为狭窄。 3、腰椎6块,每块锥体的长度比较一致,约6
-7毫米。锥管直径由前面的4毫米向 后逐渐缩小至2毫米。 二、胸骨 共分为6节,最前一节为胸骨柄,第二到第五 节称为胸骨体,最后一节为剑突,棒状 的剑突后面接一盘状的剑状软骨。胸骨 柄长约10毫米。 第三章肌 肉系统(省略) 第四章消 化系统 消化系统包括消化管及附属消化器官。消化管可 分为口腔、食管、胃、小肠和大肠等部。 附属消化器官有齿、舌、唾液腺、肝和 胰。 第一节消化管 一、口腔 1、舌全长约30毫米,不具有正中系带, 但是有两条侧系带。 一、食管 分为颈、胸、腹三部。成年大鼠食管的颈-胸段长度约75毫米,腹段通过膈的食管裂孔在膈后的长度约15毫米,食管外径约2毫米。 位置:食管主要是沿气管背侧走行,仅在颈部稍偏左侧。 一、胃 位置:横位于腹腔的左前部,其壁 面几乎完全为肝的左叶所覆盖。 大小:胃重为体重的0.5%,属单室 胃。
大鼠生物学特性和解剖生理特点
大鼠生物学特性和解剖生理特点 1.大鼠性哺乳钢,啮齿目,鼠科,大鼠属动物。 2.繁殖快。大鼠2月龄时性成熟,性周期4天左右,妊娠期20 天(19~22天),哺乳期21天,每天产仔平均8只,为全年、多发情性动物。 3.喜啃咬、夜间活动、肉食,白天喜欢挤在一起休息,晚上活动大,吃食多,因此白天除实验必须抓取外,一般不要抓弄它。食性广泛,喜吃各种煮熟的动物肉。对光照较敏感。 4.性情较凶猛、抗病力强。大鼠门齿较长,激恕、袭击抓捕时易咬手,尤其是哺乳期的母鼠更凶些,常会主动咬工作人员喂饲时伸入鼠笼的手。对外环境适应性强,成年鼠很少患病。一般情况下侵袭性不强,可在一笼内大批饲养,也不会咬人。 5.无胆囊:大鼠、鸽、鹿、马、驴、象等动物没有胆囊,它们的总胆肝管括约肌的阻力很少,肝分泌的胆汁通过总胆管进入十二指肠,受十二指肠端括约肌的控制。 6.不能呕吐:因此药理实验时应予注意。 7.垂体一肾上腺系统功能发达,应激反应灵敏。行为表现多样,情绪敏感。 8.视觉、嗅觉较灵敏,做条件反射等实验反应良好,但对许多药物易产生耐药性。 9.大鼠血压和血管阻力对药物反应敏感,但对强心甙的作用较猫敏感性低671倍。
10.肝脏再生能力强,切除60~70%的肝叶仍有再生能力。 11.对营养、维生素、氨基酸缺乏敏感,可发生典型的缺乏症状。体内可以合成维生素C。 12.对炎症反应灵敏。它的眼角膜无血管。 13.生长发育期长,长骨长期有骨骺线存在,不骨化。 14.成年雌鼠在动情周期不同阶段,阴道粘膜可发生典型变化,采用阴道涂片法(Yaginal Smear Test)来观察性周期中阴道上皮细胞的变化,可推知性周期各个时期中卵巢、子宫状态与垂体激素的变动。15.大鼠(包括小鼠)心电图中没有S-T段,甚至有的导联也不见T波,如有T波也是与S波紧挨着,或在R波降支上即开始,以致看不到等电线的S-T段。但心电图其他成分稳定,重复性好。豚鼠以上较大的动物均有明显的S-T段,在选择动物品种时应以注意。16.大鼠垂体较脆弱地附着在漏斗下部,不需要很大的吸力就可以除去而不破坏鞍膈和脑膜,适宜于制作去垂体模型。大鼠也很适于作肾上腺和卵巢等内分泌腺切除手术。 17.大鼠肠道较短,盲肠较大,但盲肠功能不发达。不耐饥饿,肠内能合成维生素C。双子宫。胸部和鼠蹊部各有三对乳头。胰腺十分分散,位于胃和十二指肠弯曲处。染色体为21对,寿命3~4年。18.大鼠的体温39℃(38.5~39.5℃),心跳频率475次/分(370~580次/分),呼吸频率85.5次/分(66~114次/分),通气量7.3 ml/分(5~10.1ml/分),潮气量0.86 ml (0.6~1.25ml),耗氧量2000mm3/g 体重,麻醉时收缩压116(88~138)mmHg红细胞总数8.9百万mm3
肝硬化大鼠肝脏组织病理学及血流动力学变化档
肝硬化大鼠肝脏组织病理学及血流动力学变化 作者:乔伟1,2,鲁建国1,王青1,李鹏超1 作者单位:(1. 第四军医大学唐都医院普外科,陕西西安710038;2. 西安市铁路中心医院普外科,陕西西安710054) 【摘要】目的通过建立大鼠肝硬化模型,了解肝硬化形成过程中门静脉血流动力学的变化。 方法雄性健康SD大鼠100只随机等分为5组:4个实验组(80只,每组20只)采用腹腔及皮下注射四氯化碳(CCl4),同时饮用酒精溶液进行诱导;对照组(20只)给予普通饮水和饲料。 分别于2、4、7、10周后观察肝脏的组织病理学改变及门静脉血流动力学变化。结果肝硬化过程中肝细胞经历变性、坏死、纤维组织增生及假小叶的形成;血流动力学检测指标发生 相应变化,平均动脉压(MAP)表现为逐渐下降,门静脉压力(PVP)、下腔静脉压(IVCP)及门静脉阻力(PVR)表现为逐渐升高,门静脉血流量(PVF)表现为先升高后下降,内脏血管阻力 (SVR)表现为先下降后升高。结论本方法可建立稳定的肝硬化门脉高压症模型,且适于大批量制作;在大鼠肝硬化门脉高压形成过程中门静脉血流动力学及肝组织病理学均发生了变 化,可用于肝硬化门脉高压症方面的相关研究。 【关键词】肝硬化;门脉高压;组织病理学;血流动力学;大鼠 Histopathological and hemodynamic changes of rats with liver cirrhosisQIAO Wei1,2, LU Jian guo1, WANG Qing1, LI Peng chao1 (1. Department of General Surgery, Tangdu Hospital, Fourth Military Medical University, Xi an 710038; 2. Department of General Surgery, Xi an Railway Center Hospital, Xi an 710054, China)ABSTRACT: Objective To investigate the hemodynamic changes during the progression of portal hypertension (PHT) by establishing a model of liver cirrhosis in rats. Methods Totally 100 healthy male SD rats were assigned to 5 groups randomly (1 control group and 4 experimental groups with 20 rats in each group). Animal model of cirrhosis was established by subcutaneous injection of carbon tetrachloride (CCl4) and drinking alcohol. Rats in control group were given water and forage. The changes in the portal hemodynamics during the pathological process of liver tissues were observed after 2, 4, 7 and 10 weeks. Results During the formation of experimental cirrhosis, the hepatocytes of rats underwent 4 processes: degeneration, necrosis, fibrosis and pseudolobular proliferation. The hemodynamic changes were observed: the mean arterial pressure declined gradually after injection, but the portal venous pressure, the inferior vena cava pressure and the portal vascular resistance increased slowly. The portal venous flow reduced after ascending whereas the splanchnic vascular resistance increased after descending. Conclusion This method can establish a
