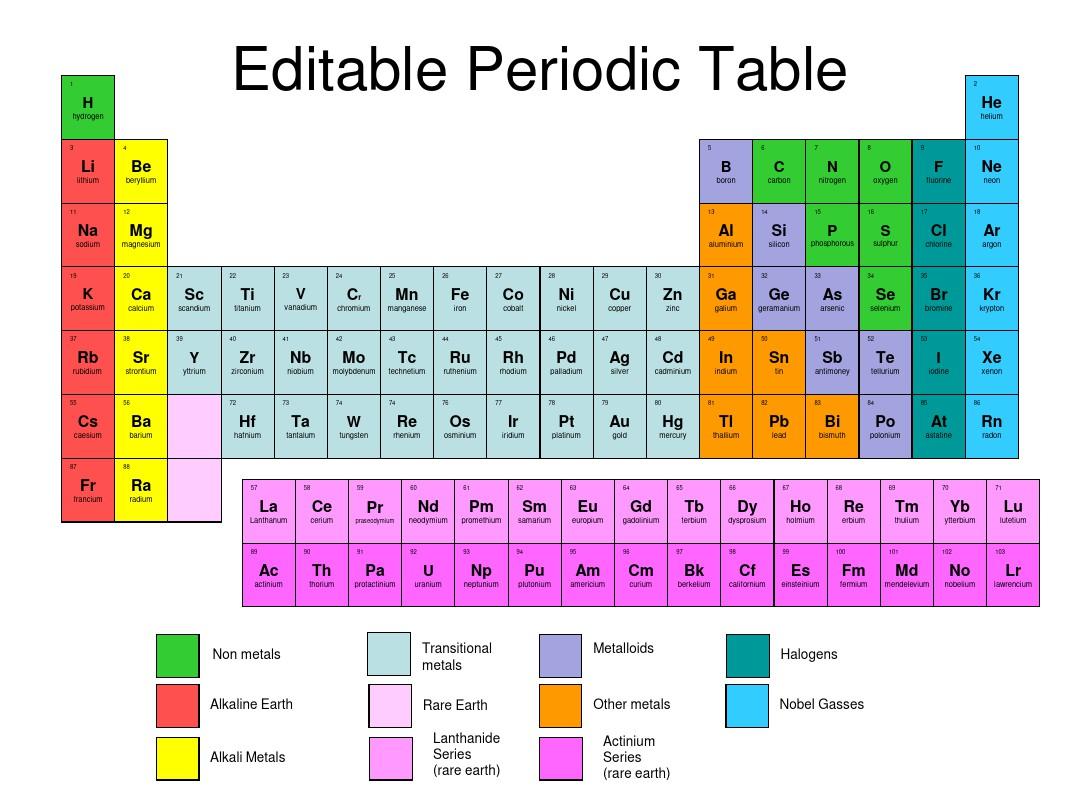
可编辑化学元素周期表PPT模板
化学元素周期表,元素周期律精读笔记!!
化学元素周期表,元素 周期律精读笔记!! -CAL-FENGHAI.Network Information Technology Company.2020YEAR
一.元素周期表 1.原子序数=核电荷数=核内质子数=核外电子数 2.主族元素最外层电子数=主族序数 3.电子层数=周期序数 4.碱金属元素:密度逐渐增大,熔沸点逐渐变大,自上而下反应越来越剧烈 银白色金属,密度小,熔沸点低,导电导热性强 5.判断元素金属性强弱的方法: 单质与水(酸)反应置换出氢的难易程度 最高价氧化物的水化物(氢氧化物)的碱性强弱 单质间的置换 6.卤族元素:密度逐渐增大,熔沸点逐渐升高 与氢气反应剧烈程度越来越弱,生成氢化物稳定性渐弱 7.判断元素非金属性强弱的方法: 与氢气生成气态氢化物的难易程度以及氢化物的稳定性 最高价氧化物的水化物的酸性 单质间的置换 8.质量数:核内所有质子和中子的相对质量取近似整数相加 9.核素:具有一定数目质子和一定数目的中子的一种原子 10.同位素:质子数相同而中子数不同的同一元素的不同原子互称为同位素 天然稳定存在的同位素,无论是游离态还是化合态各同位素所占的原子个数百分比一般是不变的 在相同状况下,各同位素的化学性质基本相同(几乎完全一样),物理性质有所不同 12.原子相对原子质量=1个原子的质量/(1/12 C12的原子质量) 13.原子的近似相对原子质量=质量数 14.元素的相对原子质量=各同位素的相对原子质量的平均值= A·a%+B·b%… 15.元素的近似相对原子质量=各同位素质量数的平均值= A·a%+B·b%… 二.元素周期律 1.K、L、M、N、O、P、Q(1,2,3,4,5,6,7,)层数越大,电子离核越远,其 能量越高 2.能量最低原理 3.各电子层最多容纳电子数:2n^2 4.最外层不超过8,次外层18,倒数第三层32 5.原子半径:同周期主族元素,原子半径从左到右逐渐减小 同主族元素,元素原子半径从上到下逐渐增大 6.元素性质的周期性变化是元素原子的核外电子排布的周期性变化的结果 (实质) 7.同一周期元素,电子层数相同,从左到右,核电荷数增多,原子半径减 小,失电子的能力逐渐减弱,得电子的能力逐渐增强 8.同一主族,自上而下,元素的金属性逐渐增强,非金属性逐渐减弱,最外 层电子数相同,电子层数增多,原子半径增大 9.最高正价=最外层电子数最低负价=8—最外层电子数 10.各周期元素种类:2,8,8,18,32,32
(完整word版)高中化学元素周期表练习题
高中化学元素周期表练习题 一、选择题 1.YBa2Cu8O x(Y为元素钇)是磁悬浮列车中的重要超导材料,关于8939Y的说法不正确的是( ) A.属于金属元素 B.质子数与中子数之差为50 C.原子的核外电子数是39 D.8939Y和9039Y是两种不同的核素 2.简单原子的原子结构可用下图形象地表示: 其中●表示质子或电子,○表示中子,则下列有关①②③的叙述正确的组合是( ) a.①②③互为同位素 b.①②③互为同素异形体 c.①②③是三种化学性质不同的粒子 d.①②③具有相同的质量数 e.①②③具有相同的质量 f.①②③是三种不同的原子 A.a、f B.b、c C.d、e D.e、f 3.某元素X的原子序数为52,下列叙述正确的是( ) A .X的主要化合价是-2、+4、+6 B. X可以形成稳定的气态氢化物 C .X的最高价氧化物对应水化物的酸性比HBrO4的酸性强 D .X原子的还原性比碘原子强 4.将两种元素铅和氪的原子核对撞,获得了一种质子数为118、中子数为175的超重元素,该元素原子核内的中子数和核外电子数之差为() A.57 B.47 C.61 D.293 5.元素周期表前四周期的元素中,同一周期的两种主族元素原子的核外电子数差值不可能为() A.6 B. 8 C. 11 D.16 6.砷为第4周期第ⅤA族元素,根据它在元素周期表中的位置推测,砷不可能具有的性质是( ) A.砷在通常情况下是固体 B.可以存在-3、+3、+5等多种化合价 C.As2O5对应水化物的酸性比H3PO4弱D.砷的氧化性比磷强 7.X和Y属短周期元素,X原子的最外层电子数是次外层电子数的一半,Y位于X的前一周期,且最外层只有一个电子,则X、Y形成的化合物的化学式可表示为() A XY2 B XY C XY3 D X2Y3
化学元素周期表word版(可打印)
ⅠA 1 H 氢 1.0079 ⅡA ⅢA Ⅳ3 Li 锂 4 Be 铍 5 B 硼 碳
6.941 9.0122 10.811 1.1 11 Na 钠 22.9898 12 Mg 镁 24.305 ⅢB ⅣB ⅤB ⅥB ⅦB Ⅷ ⅠB Ⅱ B 13 Al 铝 26.982 1 S 硅2.8 19 K 钾 20 Ca 钙 21 Sc 钪 22 Ti 钛 23 V 钒 24 Cr 铬 25 Mn 锰 26 Fe 铁 27 Co 钴 28 Ni 镍 29 Cu 铜 30 Zn 锌 31 Ga 镓 3 G 锗
39.098 40.08 44.956 47.9 50.9415 51.996 54.938 55.84 58.9332 58.69 63.54 65.38 69.72 7.37 Rb 铷 85.467 38 Sr 锶 87.62 39 Y 钇 88.906 40 Zr 锆 91.22 41 Nb 铌 92.9064 42 Mo 钼 95.94 43 Tc 锝 99 44 Ru 钌 101.07 45 Rh 铑 102.906 46 Pd 钯 106.42 47 Ag 银 107.86 8 48 Cd 镉 112.41 49 In 铟 114.82 5 S 锡1855 56 Ba 57-71 72 Hf 73 Ta 74 W 75 Re 76 Os 77 Ir 78 Pt 铂 79 Au 80 Hg 81 Tl 8 P
Cs 铯 132.905 钡 137.33 La -L u 镧系 铪 178.4 钽 180.947 钨 183.8 铼 186.207 锇 190.2 铱 192.2 195.08 金 196.967 汞 200.5 铊 204.3 铅2 787 Fr 钫 (2 23) 88 Ra 镭 226.03 89-103 Ac -L r 锕系 104 Rf (261) 105 Db (262) 106 Sg (263) 107 Bh (262) 108 Hs (265) 109 Mt (266) 110 Uu n (269) 111 Uu u (272) 112 Uu b (277) 113 Uu t 1U 57-757 La 58 Ce 59 Pr 60 Nd 61 Pm 62 Sm 63 Eu 64 Gd 65 Tb 66 Dy 67 Ho 68Er
化学元素周期表word版,可打印
1 H氢 1.0079 3 Li 4 Be 锂铍 6. 9419."0122 11 Na12 Mg 钠镁 2 2." 9824."305化学元素周期表2 He氦 4.00265 B6 C7 N8 O9 F10 Ne硼碳氮氧氟氖10." 81112." 01114." 00715." 99918." 99820."1713 Al14 Si15 P16 S17 Cl18 Ar铝硅磷硫氯氩26." 98228." 08530."
0635." 45339."9429 Cu铜6 3."5430 Zn锌6 5."3831 Ga镓6 9."7232 Ge33 As34 Se35 Br36 Kr锗砷硒溴氪 72." 574." 92278." 979." 90483."851 Sb锑 121."752 Te53 I 54 Xe氙碲碘13 1."312 7." 6126."905 85 At砹(201)86 Rn氡(222)19 K20 Ca21 Sc22 Ti23 V24 Cr25 Mn26 Fe27 Co28 Ni钾钙钪钛钒铬锰铁钴镍 3 9." 09840."
95647." 950." 941551." 99654." 93855." 8458." 933258."6937 Rb38 Sr39 Y40 Zr41 Nb42 Mo 铷锶钇锆铌钼 8 5." 46787." 6288." 90691." 2292." 906495."94 55 Cs56 Ba57-71 铯钡La-Lu 13 2." 905137."33镧系43 Tc44 Ru45 Rh46 Pd47 Ag48 Cd49 In50 Sn锝钌铑钯银镉铟锡
[精]高中化学元素周期表知识点详解(最新整理)
一.元素周期表的结构 第一节元素周期表 周期序数=核外电子层数主族序数=最外层电子数 原子序数=核电荷数=质子数=核外电子数 短周期(第1、2、3 周期) 周期:7 个(共七个横行) 周期表长周期(第4、5、6、7 周期) 主族7 个:ⅠA-ⅦA 族:16 个(共18 个纵行)副族 7 个:IB-ⅦB 第Ⅷ族 1 个(3 个纵行) 零族(1 个)稀有气体元素 ?【练习】 1.主族元素的次外层电子数(除氢) A.一定是8 个B.一定是2 个 C.一定是18 个D.是2 个、8 个或18 个 2.若某ⅡB 族元素原子序数为x,那么原子序数为x+1 的元素位于 A.ⅢB 族B.ⅢA 族C.ⅠB 族D.ⅠA 族 3.已知A 元素原子的最外层电子数是次外层电子数的3 倍,B 元素原子的次外层电子数是最外层电子数的2 倍,则A、B 元素 A.一定是第二周期元素B.一定是同一主族元素 C.可能是二、三周期元素D.可以相互化合形成化合物 二.元素的性质和原子结构 (一)碱金属元素: 1.原子结构相似性:最外层电子数相同,都为个 递变性:从上到下,随着核电核数的增大,电子层数增多 2.碱金属化学性质的相似性:4Li + O2点燃 点燃Li2O 2Na + O2Na2O2 相似。2 Na + 2H2O =2NaOH + H2↑2K + 2H2O =2KOH + H2↑ 2R + 2 H2O =2 ROH + H2↑ 产物中,碱金属元素的化合价都为+1价。 结论:碱金属元素原子的最外层上都只有个电子,因此,它们的化学性质 3.碱金属化学性质的递变性: 递变性:从上到下(从Li 到Cs),随着核电核数的增加,碱金属原子的电子层数逐渐增多,原子核对最外层电子的引力逐渐减弱,原子失去电子的能力增强, 即金属性逐渐增强。所以从Li 到Cs 的金属性逐渐增强。 结论:1)原子结构的递变性导致化学性质的递变性。 2)金属性强弱的判断依据:与水或酸反应越容易,金属性越强;最高价氧化物 对应的水化物(氢氧化物)碱性越强,金属性越强。 4.碱金属物理性质的相似性和递变性: 1)相似性:银白色固体、硬度小、密度小(轻金属)、熔点低、易导热、导电、有展性。 2)递变性(从锂到铯): ①密度逐渐增大(K 反常)②熔点、沸点逐渐降低
化学元素周期表】的口诀
快速记住【化学元素周期表】的口诀 (一) N 氮O 氧S 硫,C 碳P 磷金Au;K 钾I 碘Al 铝,钨的符号W。…… (二) H He Li Be B (氢氦锂铍硼) C N O F Ne (碳氮氧氟氖) Na Mg Al Si P (钠镁铝硅磷) S Cl Ar K Ca (硫氯氩钾钙) 五个五个背,比较顺口。 (三) 化合价: 一价请驴脚拿银,(一价氢氯钾钠银) 二价羊盖美背心。(二价氧钙镁钡锌) 一价钾钠氢氯银,二价氧钙钡镁锌; 三铝四硅五价磷,二三铁、二四碳; 一至五价都有氮,铜汞二价最常见。 正一铜氢钾钠银,正二铜镁钙钡锌; 三铝四硅四六硫,二四五氮三五磷; 一五七氯二三铁,二四六七锰为正; 碳有正四与正二,再把负价牢记心; 负一溴碘与氟氯,负二氧硫三氮磷。 初中常见原子团化合价口决: 负一硝酸氢氧根,负二硫酸碳酸根, 还有负三磷酸根,只有铵根是正一。 氢氦锂铍硼,碳氮氧氟氖; 钠镁铝硅磷,硫氯氩钾钙。 记化合价,我们常用下面的口诀: 一价氢氯钾钠银,二价钙镁钡氧锌。
二铜三铝四七锰,二四六硫二四碳, 三价五价氮与磷,铁有二三要记清。 记金属活动性顺序表可以按照下面的口诀来记: 钾钙钠镁铝、锌铁锡铅氢、铜汞银铂金。 (四) 自编的小故事口诀,10分钟全背 在背诵之前先用2分钟时间看一个不伦不类的小故事: 侵害 从前,有一个富裕人家,用鲤鱼皮捧碳,煮熟鸡蛋供养着有福气的奶妈,这家有个很美丽的女儿,叫桂林,不过她有两颗绿色的大门牙(哇,太恐怖了吧),后来只能嫁给了一个叫康太的反革命。刚嫁入门的那天,就被小姑子号称“铁姑”狠狠地捏了一把,亲娘一生气,当时就休克了。 这下不得了,娘家要上告了。铁姑的老爸和她的哥哥夜入县太爷府,把大印假偷走一直往西跑,跑到一个仙人住的地方。 这里风景优美:彩色贝壳蓝蓝的河,一只乌鸦用一缕长长的白巾牵来一只鹅,因为它们不喜欢冬天,所以要去南方,一路上还相互提醒:南方多雨,要注意防雷啊。 看完了吗?现在我们把这个故事浓缩一下,再用6分钟时间,把它背下来。 侵害 鲤皮捧碳蛋养福奶 那美女桂林留绿牙 嫁给康太反革命 铁姑捏痛新嫁者 生气休克 如此一告你 不得了 老爸银哥印西提 地点仙 (彩)色贝(壳)蓝(色)河 但(见)乌(鸦)(引)来鹅 一白巾供它牵 必不爱冬(天) 防雷啊!
化学元素周期表变化规律
页脚. 主族元素原子依次增大 同 同周期相同 主 族 依 同周期依次增多 相 次 同 增 由 同周期依次减小(0族除外) 多 小 到 同 大 主 族 由 小 到 大 同周期最高正价依次升高负价=n-8(F 除外) 同周期金属性逐渐减弱非金属性增强 同周期增强 同周期酸性逐渐增强碱性减弱 同主族酸性减弱碱性增强 同主族逐渐减弱 同主族金属性逐渐增强;非金属性逐渐 减弱 同主族最高正价相同 原子半径 核电荷数 电子层数 最外层电子数 化合价 金属性非金属性 气态氢化物稳定性 最高价氧化物对应水化物酸碱性
元素周期表中元素及其化合物的递变性规律 1 原子半径 (1)除第1周期外,其他周期元素(惰性气体元素除外)的原子半径随原子序数的递增而减小; (2)同一族的元素从上到下,随电子层数增多,原子半径增大。 注意:原子半径在VIB族及此后各副族元素中出现反常现象。从钛至锆,其原子半径合乎规律地增加,这主要是增加电子层数造成的。然而从锆至铪,尽管也增加了一个电子层,但半径反而减小了,这是与它们对应的前一族元素是钇至镧,原子半径也合乎规律地增加(电子层数增加)。然而从镧至铪中间却经历了镧系的十四个元素,由于电子层数没有改变,随着有效核电荷数略有增加,原子半径依次收缩,这种现象称为“镧系收缩”。镧系收缩的结果抵消了从锆至铪由于电子层数增加到来的原子半径应当增加的影响,出现了铪的原子半径反而比锆小的“反常”现象。 2 元素化合价 (1)除第1周期外,同周期从左到右,元素最高正价由碱金属+1递增到+7,非金属元素负价由碳族-4递增到-1(氟无正价,氧无+6价,除外); (2)同一主族的元素的最高正价、负价均相同 (3) 所有单质都显零价 3 单质的熔点 (1)同一周期元素随原子序数的递增,元素组成的金属单质的熔点递增,非金属单质的熔点递减; (2)同一族元素从上到下,元素组成的金属单质的熔点递减,非金属单质的熔点递增 4 元素的金属性与非金属性 (1)同一周期的元素电子层数相同。因此随着核电荷数的增加,原子越容易得电子,从左到右金属性递减,非金属性递增; (2)同一主族元素最外层电子数相同,因此随着电子层数的增加,原子越容易失电子,从上到下金属性递增,非金属性递减。 5 最高价氧化物和水化物的酸碱性 元素的金属性越强,其最高价氧化物的水化物的碱性越强;元素的非金属性越强,最高价氧化物的水化物的酸性越强。 6 非金属气态氢化物 元素非金属性越强,气态氢化物越稳定。同周期非金属元素的非金属性越强,其气态氢化物水溶液一般酸性越强;同主族非金属元素的非金属性越强,其气态氢化物水溶液的酸性越弱。 7 单质的氧化性、还原性 一般元素的金属性越强,其单质的还原性越强,其氧化物的阳离子氧化性越弱;元素的非金属性越强,其单质的氧化性越强,其简单阴离子的还原页脚.
化学元素周期表和化合价口诀
不论你是中学生还是中学生的家长,都可以试试。算好了,只要10分钟时间。 在背诵之前先用2分钟时间看一个不伦不类的小故事: 侵害 从前,有一个富裕人家,用鲤鱼皮捧碳,煮熟鸡蛋供养着有福气的奶妈,这家有个很美丽的女儿,叫桂林,不过她有两颗绿色的大门牙(哇,太恐怖了吧),后来只能嫁给了一个叫康太的反革命。刚嫁入门的那天,就被小姑子号称“铁姑”狠狠地捏了一把,新娘一生气,当时就休克了。 这下不得了,娘家要上告了。铁姑的老爸和她的哥哥夜入县太爷府,把大印假偷走一直往西跑,跑到一个仙人住的地方。 这里风景优美:彩色贝壳蓝蓝的河,一只乌鸦用一缕长长的白巾牵来一只鹅,因为它们不喜欢冬天,所以要去南方,一路上还相互提醒:南方多雨,要注意防雷啊。 看完了吗?现在我们把这个故事浓缩一下,再用6分钟时间,把它背下来。 侵害 鲤皮捧碳蛋养福奶 那美女桂林留绿牙 嫁给康太反革命 铁姑捏痛新嫁者
生气休克 如此一告你 不得了 老爸银哥印西提 地点仙 (彩)色贝(壳)蓝(色)河 但(见)乌(鸦)(引)来鹅 一白巾供它牵 必不爱冬(天) 防雷啊! 好了,现在共用去8分钟时间,你已经把元素周期表背下来了,不信?那你再用余下的2分钟,对照一下: 第一周期:氢氦 ---- 侵害 第二周期:锂铍硼碳氮氧氟氖 ---- 鲤皮捧碳蛋养福奶 第三周期:钠镁铝硅磷硫氯氩 ---- 那美女桂林留绿牙 第四周期:钾钙钪钛钒铬锰 ---- 嫁给康太反革命 铁钴镍铜锌镓锗 ---- 铁姑捏痛新嫁者 砷硒溴氪 ---- 生气休克 第五周期:铷锶钇锆铌 ---- 如此一告你
钼锝钌 ---- 不得了 铑钯银镉铟锡锑 ---- 老爸银哥印西提 碲碘氙 ---- 地点仙 第六周期:铯钡镧铪 ----(彩)色贝(壳)蓝(色)河 钽钨铼锇 ---- 但(见)乌(鸦)(引)来鹅 铱铂金汞砣铅 ---- 一白巾供它牵 铋钋砹氡 ---- 必不爱冬(天) 第七周期:钫镭锕 ---- 防雷啊! ( 唉,没办法,这么难记的东东,又必须要背,就只能这样了。其实,任何一门学科的知识都可以化为各种特殊方法来记忆,熟能生巧就能极大提高学习效率,如果每个人都能学好快速阅读记忆那该多好啊!) 以上是横着按周期背。下面是竖着按族背: 氢锂钠钾铷铯钫请李娜加入私访(李娜什么时候当皇上啦) 铍镁钙锶钡镭媲美盖茨被累(呵!想和比尔.盖茨媲美,小心累着) 硼铝镓铟铊碰女嫁音他(看来新郎新娘都改名了) 碳硅锗锡铅探归者西迁 氮磷砷锑铋蛋临身体闭 氧硫硒碲钋养牛西蹄扑
化学元素周期表word版(可打印)
89-103 Ac-Lr 锕系 89 Ac 锕 227.03 90 Th 钍 232.04 91 Pa 镤 231.04 92 U 铀 238.03 93 Np 镎 237.05 94 Pu 钚 244 95 Am 镅 243 96 Cm 锔 247 97 Bk 锫 247 98 Cf 锎 251 99 Es 锿 254 100 Fm 镄 257 101 Md 钔 258 102 No 锘 259 103 Lr 铹 260 ⅠA 1 H 氢1.0079 ⅡA ⅢA ⅣA ⅤA ⅥA ⅦA 2 He 氦 4.0026 3 Li 锂 6.941 4 Be 铍 9.0122 5 B 硼 10.811 6 C 碳 12.011 7 N 氮 14.007 8 O 氧 15.999 9 F 氟 18.998 10 Ne 氖 20.17 11 Na 钠22.9898 12 Mg 镁 24.305 ⅢB ⅣB ⅤB ⅥB ⅦB ⅧⅠB ⅡB 13 Al 铝 26.982 14 Si 硅 28.085 15 P 磷 30.974 16 S 硫 32.06 17 Cl 氯 35.453 18 Ar 氩 39.94 19 K 钾39.098 20 Ca 钙 40.08 21 Sc 钪 44.956 22 Ti 钛 47.9 23 V 钒 50.9415 24 Cr 铬 51.996 25 Mn 锰 54.938 26 Fe 铁 55.84 27 Co 钴 58.9332 28 Ni 镍 58.69 29 Cu 铜 63.54 30 Zn 锌 65.38 31 Ga 镓 69.72 32 Ge 锗 72.5 33 As 砷 74.922 34 Se 硒 78.9 35 Br 溴 79.904 36 Kr 氪 83.8 37 Rb 铷85.467 38 Sr 锶 87.62 39 Y 钇 88.906 40 Zr 锆 91.22 41 Nb 铌 92.9064 42 Mo 钼 95.94 43 Tc 锝 99 44 Ru 钌 101.07 45 Rh 铑 102.906 46 Pd 钯 106.42 47 Ag 银 107.868 48 Cd 镉 112.41 49 In 铟 114.82 50 Sn 锡 118.6 51 Sb 锑 121.7 52 Te 碲 127.6 53 I 碘 126.905 54 Xe氙 131.3 55 Cs 铯132.905 56 Ba 钡 137.33 57-71 La-Lu 镧系 72 Hf 铪 178.4 73 Ta 钽 180.947 74 W 钨 183.8 75 Re 铼 186.207 76 Os 锇 190.2 77 Ir 铱 192.2 78 Pt 铂 195.08 79 Au 金 196.967 80 Hg 汞 200.5 81 Tl 铊 204.3 82 Pb 铅 207.2 83 Bi 铋 208.98 84 Po 钋 (209) 85 At 砹 (201) 86 Rn 氡 (222) 87 Fr 钫(223) 88 Ra 镭 226.03 89-103 Ac-Lr 锕系 104 Rf (261) 105 Db (262) 106 Sg (263) 107 Bh (262) 108 Hs (265) 109 Mt (266) 110 Uun (269) 111 Uuu (272) 112 Uub (277) 113 Uut 114 Uuq 57-71 La-Lu 镧系 57 La 镧 138.905 58 Ce 铈 140.12 59 Pr 镨 140.91 60 Nd 钕 144.2 61 Pm 钷 147 62 Sm 钐 150.4 63 Eu 铕 151.96 64 Gd 钆 157.25 65 Tb 铽 158.93 66 Dy 镝 162.5 67 Ho 钬 164.93 68 Er 铒 167.2 69 Tm 铥 168.934 70 Yb 镱 173.0 71 Lu 镥 174.96
精高中化学元素周期表知识点详解
第一节 元素周期表 一.元素周期表的结构 周期序数=核外电子层数 主族序数=最外层电子数 原子序数 = 核电荷数 = 质子数 = 核外电子数 短周期(第1、2、3周期) 周期:7个(共七个横行) 周期表 长周期(第4、5、6、7周期) 主族7个:ⅠA-ⅦA 族:16个(共18个纵行)副族7个:IB-ⅦB 第Ⅷ族1个(3个纵行) 零族(1个)稀有气体元素 【练习】 1.主族元素的次外层电子数(除氢) A .一定是8个 B .一定是2个 C .一定是18个 D .是2个、8个或18个 2.若某ⅡB 族元素原子序数为x ,那么原子序数为x +1的元素位于 A .Ⅲ B 族 B .ⅢA 族 C .ⅠB 族 D .ⅠA 族 3.已知A 元素原子的最外层电子数是次外层电子数的3倍,B 元素原子的次外层电子数是最外层电子数的2倍,则A 、B 元素 A .一定是第二周期元素 B .一定是同一主族元素 C .可能是二、三周期元素 D .可以相互化合形成化合物 二.元素的性质和原子结构 (一)碱金属元素: 1.原子结构 相似性:最外层电子数相同,都为_______个 递变性:从上到下,随着核电核数的增大,电子层数增多 2.碱金属化学性质的相似性: 4Li + O 2 Li 2O 2Na + O 2 Na 2O 2 2 Na + 2H 2O = 2NaOH + H 2↑ 2K + 2H 2O = 2KOH + H 2↑ 2R + 2 H 2O = 2 ROH + H 2 ↑ 产物中,碱金属元素的化合价都为+1价。 结论:碱金属元素原子的最外层上都只有_______个电子,因此,它们的化学性质相似。 3.碱金属化学性质的递变性: 递变性:从上到下(从Li 到Cs ),随着核电核数的增加,碱金属原子的电子层数逐渐增多,原子核对最外层电子的引力逐渐减弱,原子失去电子的能力增强,即金属性逐渐增强。所以从Li 到Cs 的金属性逐渐增强。 结论:1)原子结构的递变性导致化学性质的递变性。 2)金属性强弱的判断依据:与水或酸反应越容易,金属性越强;最高价氧化物对应的水化物(氢氧化物)碱性越强,金属性越强。 4.碱金属物理性质的相似性和递变性: 1)相似性:银白色固体、硬度小、密度小(轻金属)、熔点低、易导热、导电、有展性。 2)递变性(从锂到铯): ①密度逐渐增大(K 反常) ②熔点、沸点逐渐降低 点燃 点燃
化学元素周期表(word版)
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 ⅠA元素周期表(word版)0 1 1 H 氢 1.0079 ⅡA固态液态气态人造元素金属非金属ⅢAⅣAⅤAⅥAⅦA 2 He 氦 4.0026 23 Li 锂 6.941 4 Be 铍 9.0122 5 B 硼 10.811 6 C 碳 12.011 7 N 氮 14.007 8 O 氧 15.999 9 F 氟 18.998 10 Ne 氖 20.17 3 11 Na 钠 22.9898 12 Mg 镁 24.305 ⅢBⅣBⅤBⅥBⅦBⅧBⅠBⅡB 13 Al 铝 26.982 14 Si 硅 28.085 15 P 磷 30.974 16 S 硫 32.06 17 Cl 氯 35.453 18 Ar 氩 39.94 4 19 K 钾 39.098 20 Ca 钙 40.08 21 Sc 钪 44.956 22 Ti 钛 47.9 23 V 钒 50.9415 24 Cr 铬 51.996 25 Mn 锰 54.938 26 Fe 铁 55.84 27 Co 钴 58.9332 28 Ni 镍 58.69 29 Cu 铜 63.54 30 Zn 锌 65.38 31 Ga 镓 69.72 32 Ge 锗 72.5 33 As 砷 74.922 34 Se 硒 78.9 35 Br 溴 79.904 36 Kr 氪 83.8 5 37 Rb 铷 85.467 38 Sr 锶 87.62 39 Y 钇 88.906 40 Zr 锆 91.22 41 Nb 铌 92.9064 42 Mo 钼 95.94 43 Tc 锝 99 44 Ru 钌 101.07 45 Rh 铑 102.906 46 Pd 钯 106.42 47 Ag 银 107.868 48 Cd 镉 112.41 49 In 铟 114.82 50 Sn 锡 118.6 51 Sb 锑 121.7 52 Te 碲 127.6 53 I 碘 126.905 54 Xe 氙 131.3 6 55 Cs 铯 132.905 56 Ba 钡 137.33 57-71 La-Lu 镧系 72 Hf 铪 178.4 73 T a 钽 180.947 74 W 钨 183.8 75 Re 铼 186.207 76 Os 锇 190.2 77 Ir 铱 192.2 78 Pt 铂 195.08 79 Au 金 196.967 80 Hg 汞 200.5 81 Tl 铊 204.3 82 Pb 铅 207.2 83 Bi 铋 208.98 84 Po 钋 (209) 85 At 砹 (201) 86 Rn 氡 (222) 7 87 Fr 钫 (223) 88 Ra 镭 226.03 89-103 Ac-Lr 锕系 104 Rf (261) 105 Db (262) 106 Sg (263) 107 Bh (262) 108 Hs (265) 109 Mt (266) 110 Uun (269) 111 Uuu (272) 112 Uub (277) 113 Uut 114 Uuq
高一化学元素周期表同步练习题及答案
2019高一化学元素周期表同步练习题及答案在化学学习的过程中,同步训练非常重要,可以帮助查缺补漏,小编为大家准备了2019高一化学元素周期表同步练习题及答案,供大家参考学习,希望对大家有所帮助! 一、选择题(每小题只有1个选项符合题意) 1.下列关于元素周期表的说法,错误的是A.元素周期表是元素按原子量大小排列而成的 B.从第一周期到第三周期元素,其原子的价电子数和族数是一致的 C.主族元素中(氢除外)族序数越小的元素,其最高价氧化物的水化物碱性越强 D.元素周期表是元素周期律的具体表现形式 3.下列各组中的元素用原子序数表示,其中都属于主族的一组元素是 A.2、4、6 B.19、20、21 18、16、、C.1、35 D.84.主族元素在周期表中的位置取决于元素原子的 A.原子量和核外电子数 B.电子层数和最外层电子数 C.原子量和最外层电子数 D.电子层数和次外层电子数页 1 第
5.在周期表中金属和非金属的分界线附近能找到 A.制农药的元素 B.制催化剂的元素 C.做半导体的元素 D.制耐高温合金材料的元素 二、选择题(每小题有1或2个选项符合题意) 6.下列关于周期表中第三周期元素性质从左到右变化趋势的叙述,错误的是 A.最高正价依次升高 B.气态氢化物稳定性逐渐增强 C.原子半径逐渐增大 D.最高价氧化物对应的水化物碱性逐渐减弱,酸性逐渐增强 7.下列气态氢化物中,按稳定性由强到弱的顺序排列的是 A.HI、HBr、HCl、HF B.HCl、H2S、PH3、SiH4 C.H2O、H2S、HCl、HBr D.HF、H2O、NH3、CH4 8.下列各组元素最高价氧化物对应水化物碱性渐弱,酸性渐强的是 A.NaOH、Mg(OH)2、H3PO4、H2SO4 HClO4H2SO4NaOH、、B.KOH、C.Be(OH)2、Ca(OH)2、HBrO4、HClO4D.Mg(OH)2、Ba(OH)2、H3PO4、H2SO4页 2 第 9.同主族3种元素X、Y、Z,已知它们的最高价氧化物对应水化物的酸性HXO4HZO4则下列判断正确的是 气态氢化物稳定性HXA.原子半径XZ B. C.非金属性XZ D.气态氢化物还原性HXHZ10.R元素的原子有3个电子层,M
2020年中考化学专题训练《元素周期表单元格题》(word版含答案)
2020年中考化学专题训练《元素周期表单元格题》 一、选择题: 1、近期热映的《复仇者联盟4》引发了不小的观影潮,深受观众喜爱的钢铁侠早期利用金属钯(Pd)制造出方舟反应炉来维持生命,如图是钯元素的相关信息,下列说法正确的是() A.钯原子在化学反应中易得到电子 B.钯原子核内有46个质子 C.钯元素的相对原子质量为106.4g D.钯原子结构示意图中x=8 2、我国的北斗导航卫星系统处于世界领先地位,它采用了铷原子钟提供精确时间。根据如图信息,判断下列说法中错误的是() A.铷原子内含有37个质子 B.铷原子易得电子变成阴离子 C.铷元素属于金属元素 D.铷元素的相对原子质量为85.47 3、在“宏观-微观-符号”之间建立联系是化学学科特有的思维方式。对下列图示信息的分析不正确的是() A.图①是硅原子的结构示意图 B.图②对应的元素原子的核外电子数为11 C.若图③中x的值为8,则其粒子符号为O2- D.图②④对应元素组成的化合物是由分子构成的
4、如图是钌元素在元素周期表中的信息,下列说法正确的是() A.钌元素的相对原子质量为101.1g B.钌的原子序数为44 C.钌原子的最外层电子数是8 D.钌在化学反应中容易得到电子 5、我国科学家最新研制出一种新型石墨烯-铝电池,手机使用这种电池,充电时间短,待机时间长。碳、铝元素的相关信息如图,有关说法正确的是() A.它们的化学性质相同 B.碳原子的核外有4个电子 C.铝的原子序数为13 D.铝的相对原子质量为26.98g 6、我国最新发布四种人造新元素的中文名称,其中115号镆元素的“镆”取自古代剑名“镆铘”,下列有关该元素信息(如图)的说法正确的是() A.镆铘剑中含有镆元素 B.镆原子的核内中子数为115 C.镆元素的相对原子质量为288g D.“Mc”表示镆这种物质、镆元素、1个镆原子 7、如图是钠元素和氯元素在元素周期表中的信息和有关的4种粒?结构示意图,下列说法正确的是() A.钠、氯都属于?属元素 B.氯化钠是由 a、c两种粒?构成的 C.氯的相对原?质量是35.45g