第九章 羧酸及其衍生物

第九章 羧酸及其衍生物
[目的要求]:
1. 掌握羧酸及衍生物的结构和命名。
2. 掌握羧酸及其衍生物的性质。
3. 理解羧酸及其衍生物的相互转化
4. 了解羧酸及其衍生物的用途。
§9—1 羧酸 一、 羧酸的结构、分类和命名
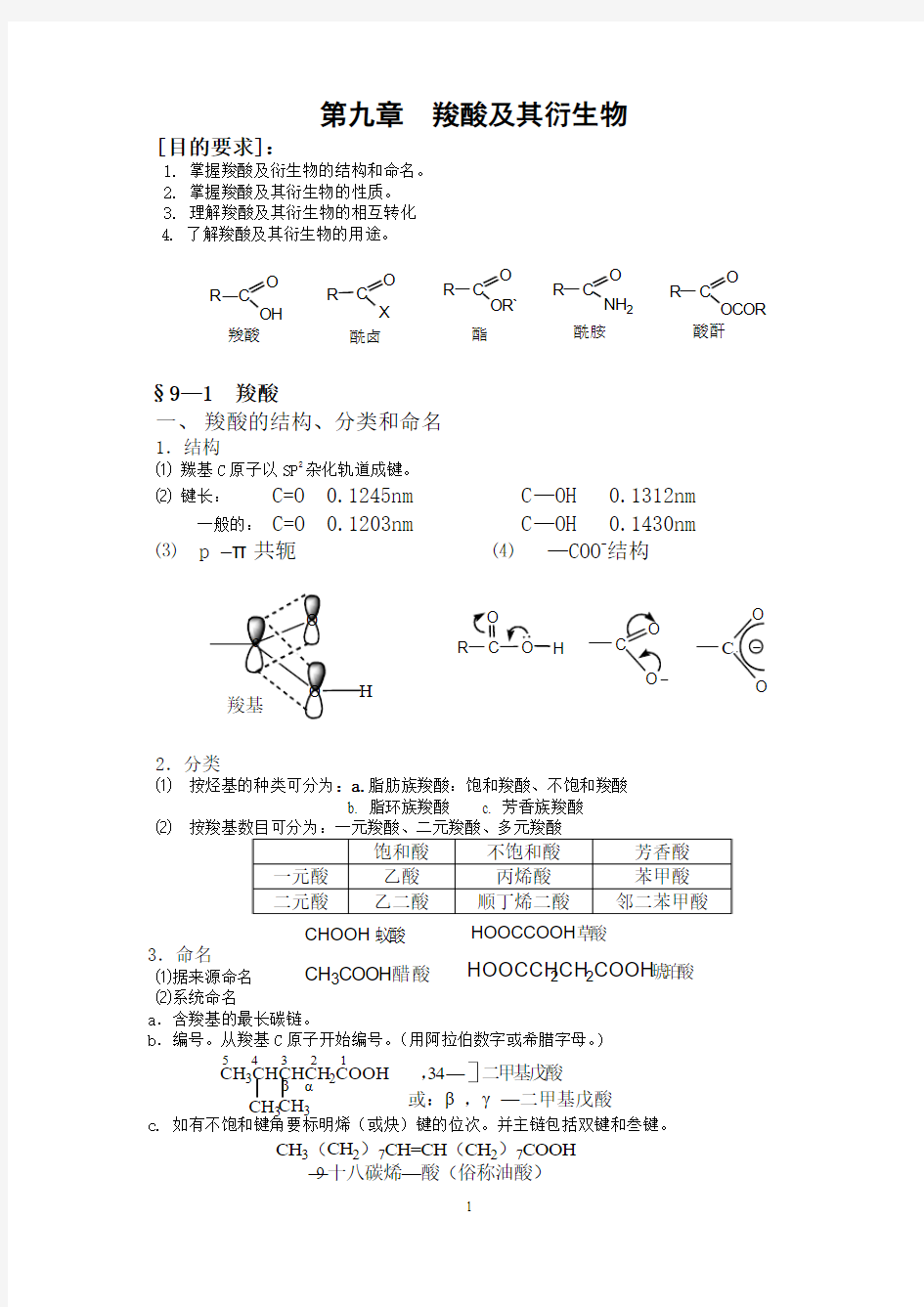
1.结构
⑴ 羰基C 原子以SP 2
杂化轨道成键。
⑵ 键长: C=O 0.1245nm C —OH 0.1312nm 一般的: C=O 0.1203nm C —OH 0.1430nm
⑶ p –π共轭 ⑷ —COO -结构
2.分类
⑴ 按烃基的种类可分为:a.脂肪族羧酸:饱和羧酸、不饱和羧酸
b. 脂环族羧酸
c. 芳香族羧酸
⑵
3.命名
⑴据来源命名
⑵系统命名
a .含羧基的最长碳链。
b .编号。从羧基C 原子开始编号。(用阿拉伯数字或希腊字母。)
c. 如有不饱和键角要标明烯(或炔)键的位次。并主链包括双键和叁键。 R C O
OH R C
X R
C O OR`
R
C
O NH 2
R
C
O
OCOR 羧酸酯
酸酐
酰卤
酰胺
R
C
O
O H
CHOOH 蚁酸
CH 3COOH 醋酸HOOCCOOH 草酸
HOOCCH 2CH 2COOH 琥珀酸CH 3CHCHCH 2COOH 3,4—二甲基戊酸
CH 3CH 3
或:β,γ—二甲基戊酸5 4 3 2 1β α
CH 3(CH 2)7CH=CH (CH 2)7COOH 9—十八碳烯—酸(俗称油酸)
d. 脂环族羧酸。简单的在脂环烃后加羧酸二字,复杂的环可作为取代基。
e.芳香酸可作脂肪酸的芳基取代物命名。
f.多元羧酸:选择含两个羧基的碳链为主链,按C 原子数目称为某二酸。
二、 羧酸的性质 ⒈物理性质
⑴ 沸点:高于分子量相近的醇。
乙醇分子间氢键键能为25KJ/mol ;甲酸分子间氢键键能为30 KJ/mol 。
⑵溶解性:随着烃基的增大溶解度(水中)减小。羰基是亲水基团,可与水形成氢键。 ⑶气味:甲、乙、丙酸有较强的刺鼻气味,水溶液有酸味。
4—9碳原子酸有难闻的酸臭味。 高级脂肪酸无气味,挥发性很低。 ⑷状态: 十个碳原子以下的饱和一元酸是液体。 高级脂肪酸是蜡状固体。 二元脂肪酸和芳香酸都是结晶固体。
⑸比重:一元羧酸:甲酸、乙酸比重大于1;其它羧酸的比重小于1。
二元羧酸、芳香羧酸的比重大于1。
2.化学性质
⑴ 酸性 羧酸能使兰色石蕊试纸变红色。 a. 与碱中和生成盐和水
b. PK a 甲酸的PK a =3.76;乙酸的 PK a =4.76;其它饱和一元酸的PK a =4.76—5之间。
COOH CH 2CH 2CH 2COOH 环已基甲酸4—环已基丁酸COOH CH 2CH 2CH 2COOH 4—苯基丁酸苯甲酸CH 2COOH α—
萘乙酸
O
H 酸性
R C O
OH 酰基
羧基
CH 3COOH CH 3COONa H 2O NaOH CaO 2RCOOH RCOO )2Ca H 2O ++++苯甲酸的乙醚溶液醚层水层苯甲酸H +
2RCOOH +Na 2CO 32RCOONa CO 2H 2O ++HCOOH CH 3COOH CH 3CH 2COOH Me 2CHCOOH Me 3CCOOH PKa 3.76 4.76 4.78 4.86 5.03C R
O H O
C R O H
c.诱导效应对羧酸酸性的影响
⑵ 羧酸中羟基的反应
a.酰卤的生成 ①
②
③
b. 酸酐的生成
R H C O
CH 3O C O 甲基的供电性,使负电
荷更集中而不稳定。
Cl O O Cl -的吸电性,使负
电荷分散而稳定。
HOOCCH 2COOH PK a1 2.83 ; PK a2 5.69
一元羧酸的分子间脱水产物二元羧酸的分子内脱水产物
酸酐
C
OH
O R C
O R +
C O O
R C O
R
H 2O
+
OH
R C O
酯酰胺
酰卤
酸酐
X
R O NH 2
R
O OR
R
O OCOR
R O
Cl 3CCOOH 〉Cl 2CHCOOH 〉ClCH 2COOH 〉CH 3COOH
PKa 0.64 1.30 2.86 4.76PKa 2.81 4.05 4.50 4.81CH 3CH 2CHCOOH CH 3CHCH 2COOH ClCH 2CH 2CH 2COOH CH 3CH 2CH 2COOH
>>>C
O R +
PCl 3
H 3PO 3亚磷酸
C
Cl O +
200℃分解
C
O
R C
Cl
O R +SOCl 2SO 2↑
HCl ↑
+
+
C
OH
O R +
++
POCl 3三氯氧磷
PCl 5
C
Cl
O
R HCl ↑沸点107℃
c. 酯化的生成
酸催化下,酯化反应一般按酰氧键断裂历程进行。
·酯化反应不是简单的取代反应,而是酸催化的加成—消除反应历程。
d.酰胺的生成
⑶还原反应
⑷烃基上的取代反应
A.α—
H的卤代反应(红磷或光照)
B.芳烃上取代
⑸二元羧酸
酸性:第一个
H+
受热分解
A.草酸、丙二酸加热失羧
CH3COOH+NH3COONH4CH3CONH
羧酸铵盐酰胺腈
CH3COOH CH
2
COOH
Br2PBr3
CBr3COOH
Br
红磷 P+
RCOOH RCH2OH
LiA lH4
COOH
COOH
150℃HCOOH CO
2
+
H2C CO2
CH3COOH
熔点以上时分解
140~160℃
+
COOH
COOH△
C
O
O
C O
COOH
COOH
H2
H2C
H2
H2C C
O
O
C O
+
C
OH
O
R H+C OH
R
+OH
OH
OH
H
R`C OH
OH
R
R`O H
+
C
R
OR`
2
C
R OR`C
O
R OR`+
H+
+
OH
OH
C
H3C
O
O CH2CH
H
+18
O
C
R
O
CH2CH3
18
+H2O
COOH
+Br2
FeCl3
COOH
Br
B . 丁二酸、戊二酸加热失水成环(酸酐)
C . 已二酸、庚二酸加热同时脱羧失水,成环酮
三、重要的羧酸 ⒈甲酸
结构
特性
⑴ 甲酸的酸性显著高于其它饱和一元酸。 ⑵ 甲酸具有还原性,能发生银镜反应。 ⑶ 甲酸也能使高锰酸钾溶液退色。 ⑷ 甲酸与浓硫酸加热,则分解生成二氧化碳和水。 ⑸ 甲酸具有杀菌力,可作消毒或防腐剂。
⒉ 乙酸
⒊ 苯甲酸
⒋ 乙二酸(草酸):具有还原性,易被氧化成二氧化碳和水 ⒌ 丁二酸
6.邻苯二甲酸
7.丁烯二酸:顺反异构体。 ⑴ 熔点 反式 〉顺式
⑵ 燃烧热 顺式 〉反式 (顺式没有反式稳定)
⑶ 顺、反的关系
⑷ 酸性: Ka 1 顺式 〉反式
Ka 2 反式 〉顺式
§9—2 羧酸衍生物 一、 命名
⒈酰卤:
H C OH O HCOOH CO 2
2SO
4
△H 2O
+
C
Cl
O
苯甲酰氯
C O
C O O 邻苯二甲酸酐
COOH H 2C COOH H 2C △
O O O
C
C H 2O +△
COOH H 2C C H 2H 2C COOH
O O O
C C H 2O +COOH C H 2COOH H 2C H 2C H 2C △
O H 2O +CO 2
+△COOH
C H 2COOH
H 2C H 2C C H 2
H 2C O H 2O +CO 2+HX
COOH
HOOC
H
H
COOH COOH
H
H
O O C
C
⒉酸酐: 称“酐”或“某酸酐”或“某酐”
⒊ 酯: 根据相应的羧酸和醇来命名。酸的部分包括酰基C 原子。
⒋ 酰胺:和酰卤相似,据相应的酰基来命名。
二、 物理性质
⒈沸点:分子量相近的衍生物比较,酰卤、酸酐和酯,由于它们分子间不能形成氢键,所以沸点一般比分子量相近的羧酸低。酰氨分子中含有氨基,它们分子间能形成氢键。
由于酰氨分子间缔合能力较强,因此沸点甚至比相应的羧酸还要高。 ⒉ 密度:酸酐的密度 〉1;脂肪族一元羧酸酯的密度均〈 1; 二元羧酸酯和芳酸酯的密度均 〉1。
H 3C C
Cl
O
乙酰氯
H 3CH C H 2C H 2C C
Cl
O
H 3C
4-甲基戊酰氯γ-甲基戊酰氯O
O C C
H 3C H 3C 乙酸酐
O
C O O C
苯甲酸酐
O
O
O C
C
丁二酸酐
H C NH 2
O
C NH 2O 苯甲酰胺C NMe 2O N ,N-二甲苯甲酰胺
甲酰胺H C
O CH 2CH 3O H 3C C
O CH 2CH 3O H 3C C O CH=CH O C O CH 2Ph
O H 3C C C H 2OCH 2CH 3O
C O OCH 2CH 3EtO C O
H 2C C O H 2C CH CH 2ONO 2
ONO 2ONO 2甲酸乙酯乙酸乙酯
乙酸乙烯酯苯甲酸苄酯(或苯甲酸苯甲酯)丙二酸二乙酯乙酰乙酸乙酯 丙三醇三硝酸酯(或甘油三硝酸酯)
N C R
O H N C
R O H H H
⒊ 水溶性:酰氯强烈水解,放出大量的HCl 及热量。 低级酰胺可溶于水。
三、 化学性质 ⒈羰基的反应
⑴ 水解
特点: a.产物均有羧酸生成。
b.活性:酰卤 〉酸酐 〉酯 〉酰胺
⑵醇解
特点:a.醇解产物是酯。
b.反应活性: 酰卤 〉酸酐 〉酯 〉酰胺
c.酰氯和酸酐是活泼的酰基化剂。
⑶氨解
a. 产物是酰胺。
b. 反应活性: 酰卤 〉酸酐 〉酯 〉酰胺
c. 重要的溴化试剂—
NBS
R C Cl
O R C O
R C NH 2
O R C O O R C OR'O
+RCOOH HCl NH 4+
H 2O
+ H 2O 剧烈反应
+ H 2O
+ H 2O
△
H 或OH H 或OH △
H 或OH △,长时间回流
+++2RCOOH RCOOH RCOOH R'OH R C Cl O R C O
R C NH 2O R C O O R C OR'O +++NH 32NH 3NH 3R'NH 2(过量)R C NH 2O R C NH 2O R C NH 2O △+++++NH 4Cl △△H 3C C NH 2O R C NHR'O CH 3CH 2OH NH 3O O O
+
NH 3
△
NH O O
Br 2
N O
O
Br N-溴代丁二酰亚胺
(NBS)
R C Cl O
R C O
R C NH 2
O R C O O R C OR'O
++++剧烈反应
△
CH 3CH 2NH 3
HCl
RCOOH ++
++
R C O
OC 2H 5R C O
CH 3CH 2OH
CH 3CH 2OH CH 3CH 2OH
OC 2H 5R C O
OC 2H 5R'OH R C O
OC 2H 5
水解、醇解、氨解的历程—加成消除可表示为:
2.酰胺的特殊反应
⑴酸碱性
⑵ Hofmam 降解反应 可制备少一个C 原子的伯胺。 3.酯缩合反应(Claisen 缩合)
两分子乙酸乙酯在EtONa 作用下起缩合反应生成β—羰基酯。
四、 自然界的羧酸衍生物 §9—3碳酸衍生物
一、 碳酰氯(光气)
1. 物性 毒性很强。沸点8.3℃,常温下为气体。
R C
O Nu
+R +R C
O Nu
A -
R 2CH 3 CONH 2HCl Na
CH 3CONH 2·HCl ↓CH 3CONHNa H 2↑
+乙醚+乙醚
CH 3 CONH 2+C O
C O
NH Na +乙醚
C O C O
N - Na +H 2O
+
CH 3CO OC 2H 5H-CH 2COOEt
EtO Na
CH 3CO CH 2COOEt EtOH
++H 3C O
C C
O
H 3C O
CH 2COOEt
H 3C C O
CH 2COOEt
+EtO -
乙酰乙酸乙酯
R CO NH 2NaOX 2NaOH RNH 2Na 2CO 3NaX +++++H 2O C HO OH
C O
H 2N NH 2C Cl
Cl C H 2N NH 2碳酸碳酰氯碳酰胺
胍
NH
H 3C O S 酶H 2C O
S 酶
3C O
H 2
C O S 酶
+酯缩合
-还原3C CH HO
H 2C C O
S 酶脱水
H 3C H
C
H
C C O
S 酶
还原
H 3C
C H 2
H 2C O
S 酶水解丁酸
2. 制备
3. 化性
⑴ 水解 ⑵ 氨解
⑶ 付—克反应
⑷ 醇解
二、尿素
⒈物性:白色结晶固体;熔点135℃;易溶于水和乙醇,不溶于氯仿和乙醚。
⒉化性:
⑴ 成盐
⑵ 水解
⑶ 放氮反应
⑷ 双缩脲反应
二缩脲在碱性溶液中与极稀的硫酸铜溶液能产生紫红色的颜色反应,这种颜色反应叫做缩二缩脲反应。
⒊制备
三、胍 极强的碱。
CO
Cl 2
+200℃
活性碳
C O
Cl
Cl 2S 2O 5Cl 2
+二氯五氧化二硫
COCl 2+H 2O
CO 22HCl
+COCl 2+2HCl
NH CO(NH 2)2
+C O
Cl +C C O CO(NH 2)2HNO 3CO(NH 2)2·HNO 3↓+硝酸脲(结晶固体不溶于水
)
CO(NH 2)232↑Na 2CO 3+CO 2↑++2NH 32NH 4Cl CO(NH 2)2+2HONO
2N 2↑3H 2O +CO 2↑+CO(NH 2)2+3NaBr 2H 2O 2N 2↑+CO 2↑++H 2NCONH 2NH 3
2NCONHCONH 2+H 2NCONH 2150℃+CO 2+NH 3(过量)
加压
180℃H 2NCONH 2
COCl 2ROH
ClCOOR 氯甲酸酯
碳酸酯ROH H 2N C NH
NH 2
H O
H 2N C O
NH 2
C H 2N
NH 2胍
NH
《有机化学》第十一章羧酸及其衍生物的结构与性质
第十一章羧酸及其衍生物的结构与性质 引言 羧基(一;.r -)是羧酸的官能团,是由羰基和羟基组成的。由于羰基的碳氧双键与羟基氧原子的共轭效应的作用,使羟基中氧原子电子向羰基转移,羟基的氢易离解而显酸性。羧基中羟基也能被其它基团取代生成羧酸衍生物。羧基是吸电子基,a- H 具有活性,可以被卤代。此外羧酸还能被还原和发生 脱羧反应。 [I 这里所讨论的羧酸衍生物主要是指羧基中羟基被取代后生成的酰卤(R-c-x),酸酐 O 0 11 II ((ACOb°b,酯(R^C-OR'),酰胺(R-C-NH2)以及由酰胺脱水后生成的产物腈(RCN) 在羧酸衍生物中羰基与卤素,酰胺基,烷氧基和氨基相连,由于卤素,氧原子和氮原子的负电性以及孤对 电子的作用,使羰基碳上正电性不同,因此它们发生亲核反应性质也有差另U。羧酸衍生物还能发生还原反 应。 11.1羧酸的酸性 羧酸是弱酸,能与强碱反应生成盐: RCOOH + MaOH ---------------------------- R COONa + 羧酸酸性的强弱与所连的基团有关,连吸电子基团的羧酸酸性较强,而连供电子基团的酸性相对较弱。如下列化合物酸性强弱顺序为: ① CH3CH2CHCOOH > CH3CHCH2COOH > CH2CH2CH2COOH CI 01 01 11.2羧酸衍生物的生成 羧基中的羟基被卤素、酰胺基、烷氧基和氨基取代形成酰卤、酸酐、酯和酰胺等羧酸衍生物。 1、酰卤的形成 CI3CCOOH CHCI3CCOOH CH3CICOOH COOH COOH COOH COOhi COOH CH3OCHj NO2
羧酸及其衍生物
第11章羧酸及其衍生物 11.1 基本要求 1.掌握常见的羧酸及其衍生物的命名规则。 2.掌握羧酸酸性的变化规律,羟基的取代反应、α-H的卤代以及一元和二元羧酸的脱羧反应,羧酸及其衍生物的还原反应。 3.比较羧酸衍生物的水解、醇解、氨解反应,弄清它们之间以及与羧酸之间相互转化的规律,理解和掌握亲核加成-消除的反应机理。 4.基本掌握羟基酸、α-酮酸、β-酮酸的重要化学性质。 11.2 基本内容 Ⅰ.羧酸 1.羧酸的结构和性质 羧基中的碳原子是sp2杂化,是平面构型。其中羰基与羟基之间存在p-π共轭效应,使羰基碳原子上的电正性削弱,不利于亲核试剂的进攻(与醛、酮相比)。同时使得羟基氧原子上的电子云密度降低,使氢原子易于解离,表现出酸性。由于羧基的吸电子效应,还使其α-H有一定的活泼性(小于醛、酮)。羧酸是强极性分子,其沸点大于同碳原子数的醇。2.羧酸的化学性质 C 酸性 H 氢的反应 羰基碳原子上的亲核反应 (1)酸性 羧酸的酸性比碳酸强,可与碳酸钠或碳酸氢钠作用生成羧酸钠: NaHCO3 RCOOH +RCOONa + CO2 + H2O 羧酸的酸性一般比无机酸弱,当向羧酸盐中加入无机酸后,羧酸又可游离出来。 RCOONa+ HCl RCOOH + NaCl 羧酸的酸性强弱受整个分子结构的影响,主要是诱导效应和共轭效应这两个因素的作用。 (a)诱导效应(I) 凡是具有-I效应的基团,即能使羧基电子云密度降低的基团,都会使羧酸的酸性增强。 酸性:ICH2COOH < BrCH2COOH < ClCH2COOH < FCH2COOH CH3CH2CH2COOH < CH2=CHCH2COOH < HC CCH2COOH HCOOH > CH3COOH > CH3CH2COOH > (CH3)2CHCOOH > (CH3)3CCOOH
11._羧酸及其衍生物
第十一章羧酸及其衍生物1. 完成下列各组反应,写出主要的反应产物:
2. 写出下列反应的主产物:
3. 两个什么样的化合物缩合后再酸化会得到下列各产物? 4. 给下列反应式填入适当的试剂: 5. 回答下列问题: 1)比较下列各酯水解的反应相对活性: 2)比较下列各个酯氨解反应的相对活性:
3)比较化合物的酸性强弱顺序: 3. 两个什么样的化合物缩合后再酸化会得到下列各产物? 4. 给下列反应式填入适当的试剂:
5. 回答下列问题: 1)比较下列各酯水解的反应相对活性: 2)比较下列各个酯氨解反应的相对活性: 3)比较化合物的酸性强弱顺序: 8. 某化合物(E) 的分子式为C5H6O3,(E)和乙醇作用得到两个互为异构体(F)和(G),将(F)和(G)分别与亚硫酰氯作用后,再与乙醇作用得到相同的化合物(H),试推测(E)(F)(G)(H)的构造式,并写出各步反应式。 9. 一个中性化合物C7H13O2Br,与羟氨和苯肼均没有反应。IR 谱在2850-2950cm-1区域有吸收峰,而在3000cm-1以上区域没有吸收峰,另外一个较强的吸收峰在1740cm-1。NMR 谱在δ=1.0(3H)三重峰;δ=1.3(6H)二重峰;δ=2.1(2H)多重峰;δ=4.2(1H) 三重峰;δ=4.6(1H) 多重峰。请推测此化合物的结构。
10. 化合物A, 分子式为C9H10O3。它不溶于水、稀HCl 及稀NaHCO3溶液,但能溶于NaOH 液。A 与稀NaOH 共热后,冷却酸化得一沉淀B,分子式为C7H6O3,B 能溶于NaHCO3溶液并放出气体,B 与FeCl3 溶液作用给出紫色,B 在酸性介质中可以进行水蒸气蒸馏,写出A,B 的构造式及各步反应式。 11. 写出化合物的A-F 正确构造式。 12. 推测化合物A-F 的结构。
《有机化学》练习题(大学)(九)羧酸及其衍生物
第十四章 羧酸及其衍生物 一选择题 1. 比较化合物乙酸(I)、乙醚(II)、苯酚(III)、碳酸(IV)的酸性大小是: (A) I>III>II>IV (B) I>II>IV>III (C) I>IV>III>II (D) I>III>IV>II 2. 下列反应应用何种试剂完成 (A) LiAlH 4 (B) NaBH 4 (C) Na + EtOH (D) Pt/H 2 3. 比较取代羧酸FCH 2COOH(I),ClCH 2COOH(II),BrCH 2COOH(III),ICH 2COOH(IV)的酸性大小是: (A) I>II>III>IV (B) IV>III>II>I (C) II>III>IV>I (D) IV>I>II>III 4.戊二酸受热(300 C)后发生什么变化 (A) 失水成酐 (B) 失羧成一元酸 (C) 失水失羧成环酮 (D) 失水失羧成烃 5. 哪种羧酸衍生物具有愉快的香味 (A) 酸酐 (B) 酰氯 (C) 酰胺 (D) 酯 6. 有强大爆炸力的三硝基甘油属于下列哪类物质: (A) 酸 (B) 碱 (C) 脂 (D) 酯 7. 增塑剂DBP(邻苯二甲酸二丁酯)是由下列哪两种物质合成的: (A) 丁醇和邻苯二甲酸酐(B) 丁酸和邻苯二酚 (C) 邻苯二甲酸酐和氯丁烷 (D) 邻苯二酚和甲酸丁酯 8.下列反应经过的主要活性中间体是: (A) 碳正离子(或离子对中,碳原子为正电一端) (B) 碳负离子(及烯醇盐负离子碎片) (C) 卡宾(即碳烯Carbene) (D) 乃春(即氮烯Nitrene) (E) 苯炔(Benzyne) 9. 下列反应经过的主要活性中间体是: (A) 碳正离子(或离子对中碳原子为正电一端) (B) 碳负离子(及烯醇盐负离子碎片) (C) 卡宾(即碳烯Carbene) (D) 氮宾(即氮烯Nitrene) (E) 苯炔(Benzyne) 10. Claisen 酯缩合的缩合剂是强碱 ,用以增长碳链.从反应活性中心看,它们是 (A) 一个羧酸酯出羰基,一个醛出-C (B) 一个羧酸酯出羰基,一个醇出-C (C) 两个羧酸酯,一个出羰基,一个出-C (D) 两个醛或酮,一个出羰基,一个出-C 11. 可以进行分子内酯缩合的二酯是: (A) 丙二酸二乙酯 (B) 丁二酸二乙酯 (C) 对苯二甲酸二乙酯 (D) 己二酸二乙酯 12. 乙酰基水杨酸(Aspirin )的结构是下列何种 2CO 2 +NH 2CONH 2 EtOOCCH 2CH 2CH 2CH 2CO 2Et O CO 2Et NaOEt EtOH CH 3O O O O COOH COOH CH 2C C O A . COOH B . C . D . CH 3 CH 3C O CH
第九章羧酸及其衍生物
第9章 羧酸及其衍生物 本章重点介绍羧酸及其衍生物的结构、分类和命名;羧酸的酸性及其影响因素;羧酸衍生物的形成及其机制;二元羧酸的某些特征反应;羧酸衍生物的亲核取代反应及其机制;碳酰胺及其衍生物的性质。 分子中含有羧基( 或简写为-COOH )的化合物称为羧酸(carboxylic acid ),其 通式为RCOOH (甲酸R=H )。羧基(carboxyl )是羧酸的官能团,它是有机化合物中同一个碳原子上的最高氧化形式,因此羧酸对一般氧化剂是稳定的。 羧酸羧基中的羟基被其它原子或基团取代后生成的化合物称为羧酸衍生物(carboxylic acid derivative )。重要的羧酸衍生物有酰卤、酸酐、酯和酰胺。 羧酸及其衍生物广泛存在于动植物体内,它们与人类生活密切相关。日常生活中,洗涤用的肥皂是高级脂肪酸的钠盐;食用醋是含有2%乙酸的水溶液;食用油是羧酸甘油酯。在生物体内,某些羧酸是动植物代谢的重要物质,它们参与了动植物的生命过程,具有重要生理活性;某些羧酸衍生物是许多昆虫幼虫的激素,能控制昆虫的发育。在医药工业上,羧酸常用作合成药物的原料或中间体,有些药物本身就是羧酸或其衍生物,因此羧酸及其衍生物是一类与医药关系十分密切的有机物。 你在学习完本章节后,应能回答以下问题: 1.羧酸的分类和命名方法有几种? 2.羧基中存在着什么电子效应?羧酸在性质上如何反映出羧基结构中存在着这种电子效应的? 3.羧酸的酸性强弱取决于哪些因素,有何规律? 4.什么叫酯化反应?不同结构的醇与羧酸酯化反应的机制是否相同?可否写出反应机制? 5.不同的二元酸受热时所发生的反应有何差异? C O OH
羧酸及羧酸衍生物地重要反应及重要反应机理
第六章羧酸及羧酸衍生物的性质及重要反应机理 一、羧酸的化学性质 1.酸性 羧酸具有酸性,诱导、共轭、场效应等对酸性强弱有影响。利用羧酸的酸性可以制备羧酸酯和羧酸盐。 2.亲核取代反应 这是羧酸在一定条件下转变成羧酸生物的反应。大多数亲核取代反应是通过加成-消除历程完成的。 3.还原反应 羧酸能被LiAlH4和B2H6还原成相应的伯醇。 4.α-H的卤化(Hell-Volhard-Zelinsky反应)
通过控制卤素的用量可以制备一元或多元的卤代羧酸,并进一步制备羟基酸和氨基酸。5.脱羧反应 羧酸在适当的条件下,一般都能发生脱羧反应,这是缩短碳链的反应。通常的脱羧反应表示如下: A为-COOH、-CN、-(C=O)R、-NO2、-CX3、-C=O、C6H5-等吸电子基团时,脱羧反应相当容易进行。此外还有一些特殊的脱羧方法。 二元羧酸的脱羧规律是:乙二酸、丙二酸、加热失羧,丁二酸、戊二酸加热是水生成分子酸酐,己二酸、庚二酸加热是水、失羧生成环酮。根据以上反应可以得出一个结论,在有机反应中有成环可能时,一般易形成五元环或六元环。这称为布朗克(Blanc)规则。 二、羧酸衍生物的化学性质 1.亲核取代反应 这是羧酸衍生物的转换反应。转换的活性顺序为: RCOX>CRCOOOCR>RCOOR′>RCONR2 酸和碱都能催化反应。
2.与有机金属化合物的反应 选用空阻大的酰卤,反应能控制在酮的阶段。选用甲酸酯,可以制备对称二级醇。选用碳酸酯,可制备三个烃基相同的三级醇。二元酸的环状酸酐可用来制备酮酸。酰胺氮上有活泼氢,一般不宜使用。 3.还原反应 一般还原反应归纳于下表: 反应物还原剂 NaBH4LiAlH4催化氢化B2H6 RCOCl Rosenmund 法 RCHO + + RCH2OH RCOOOCR + + + + 2RCH2OH RCOOR′+ + 特殊催化剂+ RCH2OH R′OH RCONH2+ + 特殊催化剂 + RCH2NH2 RCN + + RCH2NH2 其他重要反应如:Claison缩合、Reformatsky反应、Darzens反映、Perkin反应、Bouveault-Blanc 反应、酮醇反应、酯的热裂等见重要反应机理。 三、羧酸和羧酸衍生物的制备 1.羧酸的制备
第十章羧酸及其衍生物答案
第十章羧酸及其衍生物答案 1.略 2.(1)乙二酸>丙二酸>甲酸>乙酸>苯酚 (2)F3CCOOH>ClCH2COOH>CH3COOH>C6H5OH>C2H5 OH 3. (1)乙酸 乙醇 乙醛托伦试剂 银镜 NaHCO3 CO 2 4.(1)A.H3+O,B.SOCl2,C.NH3,D.P2O5/△,F. NaOBr/NaOH,G.H2, Pd-BaSO 4 (3) NH3; NH2CONHCONH2
O O O (3) (4) O O O
O (5)CHO+ C2H5OH
中靠氯原子近的羧基的酸性较强。 13. (1)CH3CH2O-的碱性较强。因CH3COO-负离子的负电荷平均分配在两个氧原子上;CH3CH2O-负离子的负电荷定域在一个氧原子上,较不稳定,与质子作用的倾向性较大。 (2)CH3CH2CH2COO->ClCH2CH2COO-(由于Cl的诱导作用而较稳定)。 (3) ClCH2CH2COO-较强;CH3CHClCOO-中,Cl靠近—COO-中心而较稳定。 (4)FCH2COO-较强;F2CHCOO-含有两个F原子之故。 (5)CH3CH2CH2COO-较强;HC≡CCH2COO-中HC≡C—吸电子诱导效应之故。
反应式略。 15. A. CH3COOCH=CH2 B.CH3CH=COOCH3 反应式略。 18.
CH CNa CH 3I CH 3C CH CH 3CH=CH 2 Br 2 CCl 4 CH 3CHBrCH 2Br CH 2 (COOC 2 H 5) 2 C 2H 5ONa CH(COOC 2H 5)2CH(COOC 2H 5)2CH 3CHBrCH 2Br CH 3CHCH 2-CH(COOC 2H 5)2 CH(COOC 2H 5)2 H 3O+ +H 2 ,Lindlar --2+目标产物 3) H CNa CH 3I CH 3C CH CH 3CH=CH 2 Br 2 CCl 4CH 3CHBrCH 2Br CH 2(COOC 2H 5)2C 2H 5ONa CH(COOC 2H 5)2CH(COOC 2H 5)2CH 3CHBrCH 2Br CH 3CHCH 2-CH(COOC 2H 5)2 CH(COOC 2H 5)2H 3O++H 2,Lindlar --2+ 目标产物 3) Br 2CCl 4 CH 2BrCH 2Br CH 2(COOC 2H 5) C 2H 5ONa CH(COOC 2H 5)CH(COOC 2H 5)CH 2BrCH 2Br CH 2CH 2-CH(COOC 2H 5)2CH(COOC 2H 5)2 C 2H 5OH H + CH 2=CH 2 --2+4)
第十五章羧酸、羧酸衍生物
第十五章羧酸、羧酸衍生物(一) 一、羧酸 [教学目的]: 1、熟悉羧酸的命名和分类 2、掌握羧酸的物理性质和化学性质 [教学重点和难点]: 酸的化学性质 羧酸衍生物的生成 脱羧反应 羧酸的酸性 [课堂组织]:羧酸(carboxylic acids)的官能团是羧基(carboxyl group), ,简写为-COOH 或-CO2H。羧酸结构中最简单的是一元羧酸,其它 羧酸的结构与其相似。 一元羧酸的通式为RCO2H,其中R为氢或烃基。 两分子羧酸容易通过氢键缔合成二缔合体: 在固态、液态和中等压力的气态下一元羧酸主要以二缔合体的形式存在,在稀溶液中或高温蒸汽中二缔合体离解。 一元羧酸二缔合体用物理方法测定的键长、键角平均值为: C=O 123pm,∠OCO 122-123°, C-O 136pm, O-H…O 260-270pm 在甲酸()分子中,所有的原子在同一平面内。 可以认为羧基碳原子为杂化。一元羧酸的分子轨道模型见图(a) 羧酸在水溶液中电离成羧酸根负离子:
羧酸根中两个C-O键是等同的,其键长在126pm左右(用羧酸盐测定)。因此,在羧酸根中羧基碳原子P电子和两个氧原子上的p电子是共轭的,可用共振式表示: 羧酸根中的负电荷平均分配在两个氧原子上。羧酸根的分子轨道模型见图(b)。 羧酸分子中羟基氧原子上的孤电子对也与羰基上的电子共轭,其结构可用共振式表示: 几个经典结构式中正负电荷分离的能量较高,在共振杂化体中的贡献较小。羧酸分子中碳-氧双键的键长与醛酮分子中的碳-氧双键相近。 15.1羧酸 15.1.1命名 根据羧酸分子中所含羧基的数目可分为一元羧酸(monocarboxylic acids)、二元羧酸(dicarboxylic acids)等;根据烃基的结构不同,又可分为饱和羧酸、不饱和羧酸或芳香酸;根据不饱和羧酸中不饱和键与羧基的位置不同,又可分为共轭羧酸和非共轭羧酸等。 在系统命名法中含碳链的羧酸是以含羧基的最长碳链为主链,从羧基碳原子开始进行编号,根据主链上碳原子的数目称为某酸,以此作为母体,然后在母体名称的前面加上取代基的名称和位置。例如: 含碳环的羧酸则是将环作为取代基命名。例如: 许多羧酸存在于天然产物中,因此,还有历史上流传下来的反映其来源的习惯名。例如:甲酸、乙酸和苯甲酸又分别称为蚁酸、醋酸和安息酸。
第八章羧酸、羧酸衍生物和取代酸
第八章羧酸、羧酸衍生物和取代酸问题八 9-1按酸性次序排列下列化合物: COOH NH 2 COOH OCH3 COOH CH3 COOH Br (1) (2) (3) (4) 解: 9-2由乙醇合成α-氯代丁酸(无机试剂任选)。 解: 9-3按照水解活性的大小次序排列下列化合物,并说明原因。 (1)乙酰胺(2)醋酸酐(3)乙酰氯(4)乙酸乙酯 解:题中给出的四种羧酸衍生物的水解反应是双分子酰氧键断裂的亲核加成-消除机理,用下列通式表示这四种化合物:CH3C O Y Y=Cl,OCCH3,OC2H5,NH2 如果C=O基团中碳原子的正电性越强,离去基团的离去倾向越大,反应物的活性也就越大。综合诱导效应和共轭效应,C=O基团中碳原子的正电性和离去基团的离去倾向次序为:乙酰氯>乙酸酐>乙酸乙酯>乙酰胺,所以水解反应的活性次序为:乙酰氯>乙酸酐>乙酸乙酯>乙酰胺。 9-4以丙腈为原料合成乙胺(无机试剂任选)。 解: 9-5试完成由丙酸→α-氯代丙酸→α-羟基丙酸→丙酮酸的转化。 解:
习题八 1. 用系统命名法命名下列化合物: (1)CH 2OH COOH (2) (8)(7) (5) (6)(4)(3)(9)(10) OCH 2COOH Cl Cl COOH (11) (12) C = C Br Cl COOH C 2H 5 CH 3CHCH 2CH 2CHCOOH CH 3 C 2H 5CH 3 CH CH COOH O H COOH H C HOO O C CH 3 O COOH H C OCH 2 O CH 2 CHCH 2COOH CH 3 OH CH 2COOH O C NHCH 3O 解:(1) 2,5-二甲基庚酸 (2) (2E , 4E )-2,4-己二烯酸 (3) (E )-2-乙基-3-氯-3-溴丙烯酸 (4) 3-羟甲基苯甲酸 (5) 2,3-环氧丁酸 (6) 2-(2,4-二氯苯氧基)乙酸 (7) (1S ,2S )-1,2-环丙基二甲酸 (8) 乙酸-2-羧基苯酯 (乙酰水杨酸) (9) 甲酸苯甲酯(甲酸苄酯) (10) 3-甲基-4-环己基丁酸 (11) 5-羟基-1-萘乙酸 (12) N-甲基氨基甲酸苯酯 2. 写出下列化合物的结构式: (1)2,3-二甲基戊酸 (2)对苯二甲酸 (3)延胡索酸 (4)(S )-α-溴丙酸 (5)顺-12-羟基-9-十八碳烯酸 (6)3-甲基邻苯二甲酸酐 (7)异丁酸异丙酯 (8)丁酸酐 (9)丁二酸酐 (10)间硝基苯乙酰溴 (11)乙二醇二乙酸酯 (12)己二酸单酰胺 解:
第十一章羧酸及其衍生物
第十章羧酸及其衍生物 【教学重点】 羧酸及其衍生物的化学性质、丙二酸二乙酯和乙酰乙酸乙酯在合成上的应用。【教学难点】 诱导效应、酰基上的亲核取代反应机理。 【教学基本内容】 羧酸的结构;羧酸的制备方法;羧酸及其衍生物的物理性质;羧酸的化学性质——羧酸的酸性及影响酸性强度的因素(诱导效应、共轭效应和场效应);羧酸衍生物的生成;羧基的还原反应;脱羧反应;α-氢原子的卤代反应。 羟基酸的制备方法(卤代酸水解、羟基腈水解、Refomatsky反应)、羟基酸的化学性质——酸性、脱水反应、α-羟基酸的分解。 羧酸衍生物的化学性质——酰基上的亲核取代反应(水解、醇解、氨解)及其反应机理;还原反应;与Grignard反应;酰胺氮原子上的反应(酰胺的酸碱性、脱水反应、Hofmann降解反应)。 乙酰乙酸乙酯的制备方法(Claisen酯缩合);乙酰乙酸乙酯的化学性质——酮式-烯醇式互变异构、酸式分解和酮式分解;乙酰乙酸乙酯在合成上的应用。 丙二酸二乙酯的制备及在合成上的应用。 Ⅰ目的要求 羧酸是含有羧基(—COOH)的含氧有机化合物,我们平常所说的有机酸就是指的这类化合物。 所谓羧酸衍生物,包括的化合物种类很多,诸如羧酸盐类、酰卤类、酯类(包括内酯、交酯、聚酯等)、酸酐类、酰胺类(包括酰亚胺、内酰胺)等都是羧酸衍生物,有人甚至把腈类也包括在羧酸衍生物的范围之内。其实,比较常见的而又比较重要的是酰卤、酸酐、酯和酰胺这四类化合物。羧酸盐与一般无机酸盐在键价类型上没大区别,不作专门介绍。至于腈类,将放在含氮化合物中加以介绍。这四类化合物都是羧酸分子中,因酰基转移而产生的衍生物,所以又叫羧酸的酰基衍生物。 羧酸及其衍生物RCOL(L:-OH、-X、-OOCR′、-OR′、-NH2)在许多重要天然产物的构成以及在生物代谢过程中均占有重要地位。本章将以饱和一元脂肪酸为重点,讨论羧酸及其衍生物的结构和性质。 鉴于乙酰乙酸乙酯和丙二酸二乙酯在有机合成上的重要地位,本章作概括介绍。希望学生在此基础上,探讨设计合成路线的一般方法。 本章学习的具体要求 1、掌握羧酸的结构与性质之间的关系。 2、掌握羧酸衍生物的主要化学性质。 3、了解羧酸衍生物的亲核取代反应机理。 4、掌握羧酸与羧酸衍生物之间相互转变条件。 5、了解卤代酸、羟基酸的特性。
大学有机化学第十章羧酸及其衍生物
第十章 羧酸及其衍生物 10.1用系统命名法命名(如有俗名请注出)或写出结构式 a. (CH 3)2CHCOOH b. OH COOH c. d.CH 3CHCH 2COOH Br e.CH 3CH 2CH 2COCl f.(CH 3CH 2CH 2CO)2O g. h.CH 3CH 2CH 2OCOCH 3 i. CONH 2 j. HOOCC=CCOOH k. 邻苯二甲酸二甲酯 l. 甲酸异丙酯 CH 3CH=CHCOOH CH 3 CH 2COOC 2H 5 n. 尿素 o. 草酸 p. 甲酸 q. 琥珀酸 r. 富马酸 s. 苯甲酰基 t. 乙酰基 答案:a. 2-甲基丙酸 (异丁酸) b. 邻羟基苯甲酸(水杨酸) c. 2-丁烯酸 d 3-溴丁酸 e. 丁酰氯 f. 丁酸酐 g. 丙酸乙酯 h. 乙酸丙酯 i. 苯甲酰胺 j. 顺丁烯二酸 s. C O t. H 3C O k. COOCH 3 COOCH 3 l. HCOOCH(CH 3)2 m.CH 3CH 2CONHCH 3 n.NH 2CONH 2o.HCOOH p.HOOCCH 2CH 2COOH q.HOOCCOO H r.HOOC C C H COOH 10.2 将下列化合物按酸性增强的顺序排列: a. CH 3CH 2CHBrCO 2H b. CH 3CHBrCH 2CO 2H c. CH 3CH 2CH 2CO 2H d. CH 3CH 2CH 2CH 2OH e. C 6H 5OH f. H 2CO 3 g. Br 3CCO 2H h. H 2O 答案: 酸性排序 g > a > b > c > f > e > h > d 10.3写出下列反应的主要产物 a. 22724 b.(CH 3)2CHOH + COCl H 3C c. HOCH 2CH 2COOH LiAlH 4 d.NCCH 2CH 2CN + H 2O NaOH H + e. CH 2COOH CH 2COOH Ba(OH)2 f. CH 3COCl + CH 3 AlCl 3 g. (CH 3CO)2O +OH h. CH 3CH 2COOC 2H 5 NaOC 2H 5
第十章 羧酸及其衍生物
第十章 羧酸及其衍生物 1.命名下列化合物或写出结构式 OH COOC 2H 5 (1) (2) COCl C 2H 5O O O (3) (4)丁二酰亚胺;(5)α-甲基丙烯酸甲酯;(6)亚油酸;(7)柠檬酸;(8)苹果酸; 解: (1) 邻羟基苯甲酸乙酯 (2) 对乙氧基苯甲酰氯 (3) γ-戊内酯 (4) N H O O (5) CH 2=CCH 3COOCH 3 (7) (6) HOOCCH 22COOH OH COOH O OH (8)HOOCCH(OH)CH 2COOH 2.写出丙酸与下列试剂反应的主要产物。 (1) NaHCO 3 (2) SOCl 2,Δ (3)(CH 3CO)2O ,Δ (4)C 2H 5OH ,少量浓H 2SO 4,Δ (5)NH 3,Δ (6)LiAlH 4,干醚,然后H 3O + (7)B 2H 6-THF ,然后H 2O (8)HgO,Br 2, Δ (9) 催化量P ,Cl 2,Δ (10)PBr 3, Δ 解:(1) CH 3CH 2CONa (2) CH 3CH 2COCl (3) CH 3CH 2COOCCH 3 (4) CH 3CH 2COOCH 2CH 3 (5) CH 3CH 2CONH 2 (6) CH 3CH 2CH 2OH (7) CH 3CH 2CH 2OH (8) CH 3CH 2Br (9) CH 3CH 2CH 2Cl (10) CH 3CH 2COBr 3.写出丙酰氯与下列试剂反应的主要产物 (1)H 2O ,Δ (2)C 2H 5OH ,Δ (3)C 6H 5OH ,Δ (4)CH 3NH 2,Δ (5)C 6H 5NH 2,Δ (6)H 2,Pd (7) H 2,Pd/BaSO 4,S-喹啉 (8)2CH 3CH 2MgBr,干醚,然后H 3O + (9)(C 2H 5)2CuLi / Et 2O (10)(CH 3CH 2CH 2)2CuLi,乙醚 解: (1) CH 3CH 2COOH (2) CH 3CH 2COOC 2H 5 (3) CH 3CH 2COOC 6H 5 (4) CH 3CH 2CONHCH 3 (5) CH 3CH 2CONHC 6H 5 (6) CH 3CH 2CH 2OH (7) CH 3CH 2CHO (8) CH 3CH 2COH(CH 2CH 3)2 (9) CH 3CH 2COC 2H 5 (10) CH 3CH 2COCH 2CH 2CH 3 4.写出苯甲酰胺与下列试剂反应的主要产物 (1)H 2O ,H +,Δ (2)H 2O ,HO -,Δ (3)C 2H 5OH ,H +,Δ (4)LiAlH 4,乙醚,然后H 3O + (5)P 2O 5,Δ 解: (1) (2)(3) (4) (5) COOH COO - COOC 2H 5 CH 2NH 2 CN 5.用简单的化学方法鉴别下列各组化合物 (1)A .甲酸 B.丙酸 C.丙二酸 D. 丙烯酸 (2)A .甲基丙烯酸甲酯 B.乙酸丁酯 C. 丁酸乙酯
羧酸及其衍生物 四川大学
第七章醛酮醌 一、学习要求 1.掌握醛酮的结构及命名。 2.掌握醛酮的主要化学性质及异同点。 3.了解醌的结构、命名和化学性质。 二、本章要点 (一)醛和酮 1.结构醛和酮分子中均含有羰基。羰基与氢和烃基相连(甲醛除外)的有机化 。羰基与两个烃基相连的有机化合物称为 酮,通式为 。羰基中碳原子为SP2杂化,由于氧的电负性较大,因此羰基是极性不饱和基团。 2.命名IUPAC法是选择含羰基的最长碳链作母体,从羰基碳原子开始给主链编号,根据主链碳原子数称为某醛或某酮。对于酮,还要标明酮基的位次,以此作为母体名。再将取代基、双键或叁键的位置编号和名称写在母体名称前。 3.物理性质在常温下,除甲醛为气体外,其它醛、酮为液体或固体。醛、酮是极性分子,分子之间存在着偶极-偶极之间的相互作用,从而使醛、酮的沸点高于相对分子质量相近的烷烃和醚。醛、酮分子中羰基氧原子可与水分子中的氢原子形成氢键,故含碳数较低的醛、酮易溶于水,但随着分子中烃基碳原子数增多,水中的溶解度逐渐降低。 4.化学性质羰基是极性不饱和基团,可发生亲核加成。又由于羰基的-I效应,使α-H有一定活性,可发生一些反应。 (1)亲核加成:羰基中碳原子带部分正电荷,易受到亲核试剂的进攻而发生加成反应。反应通式为: C R R' δδ +- :A C R R'Nu - C R R'Nu O A +
羰基亲核加成反应的活性大小,主要取决于羰基碳上连接的原子或原子团的电子效应和空间效应。羰基碳原子上的正电性越强,亲核反应越易进行;羰基所连的烃基越多或体积越大,反应越难进行。不同结构的醛、酮进行亲核加成时,反应活性次序为: ①与氢氰酸加成:醛、脂肪族甲基酮和小于8个碳原子的环酮能与氢氰酸加成,生成α-羟基腈(又称为α-氰醇)。 ②与亚硫酸氢钠加成:醛、脂肪族甲基酮以及8个碳以下的环酮可与饱和亚硫酸氢钠溶液(40%)作用,生成α-羟基磺酸钠。 ③与醇加成:在干燥氯化氢的催化下,醛能和一分子醇发生亲核加成,生成不稳定的半缩醛,再继续与一分子醇脱水而生成稳定的缩醛。酮较难发生此反应。 ④与水加成:醛、酮可与水加成形成水合物,但这种水合物是一种同碳二元醇化合物,极不稳定,很易失水又形成羰基,因此反应平衡主要偏向反应物一方。若羰基与强的吸电子基团相连,羰基碳上的正电性增大,则可以与水加成形成较稳定的水合物。 ⑤氨的衍生物加成:所有羰基化合物均可与氨的衍生物加成,但加成产物很不稳定,易发生分子内脱水,生成含有碳氮双键的化合物。 (2)α-活泼氢的反应 ①羟醛缩合反应:在稀碱作用下,有α-氢的醛可发生羟醛缩合反应,生成β-羟基醛,反应的结果使主碳链增长两个碳原子。含有α氢的酮在碱催化下也能发生羟酮缩合反应,但酮的羟酮缩合反应比醛难。 ②卤代反应和卤仿反应:在碱催化下,醛、酮的α-氢容易被卤素(Cl 2、Br 2 、I 2)取代,生成α-多卤代醛、酮。具有三个α-氢结构的化合物,在碱性条件下,与卤素作用或与次卤酸钠溶液作用时,甲基上的三个α-氢都会被卤素取代,生成α-三卤代醛、酮,三卤代醛、酮在碱溶液中发生碳碳键断裂,生成卤仿和少一个碳原子的羧酸盐,此反应称为卤仿反应。此外具有 结构的醇也能发生卤仿反应。 (3)还原反应: 醛、酮分子中的羰基可以被还原,但所用还原剂不同,生成的产物也不同。 在金属铂、镍和钯催化下与氢气作用时,羰基被还原成醇羟基,若分子中有其他不饱和基团,将同时被还原。 用金属氢化物(氢化铝锂 LiAlH 4,氢硼化钠NaBH 4)还原醛或酮时,羰基被还原成 CH 3CH R (H)C O H H C O H CH C O H C 6H 5 C O CH CH 3 O C O C 6H 5CH 3C O C 6H 5 C 6H > > > > >>
第九章羧酸及其衍生物
第9章 羧酸及其衍生物 本章重点介绍羧酸及其衍生物的结构、分类和命名;羧酸的酸性及其影响因素;羧酸衍生物的形成及其机制;二元羧酸的某些特征反应;羧酸衍生物的亲核取代反应及其机制;碳酰胺及其衍生物的性质。 分子中含有羧基( 或简写为-CO OH )的化合物称为羧酸(carbox yl ic a cid ),其通式为RCOOH (甲酸R=H)。羧基(car boxyl )是羧酸的官能团,它是有机化合物中同一个碳原子上的最高氧化形式,因此羧酸对一般氧化剂是稳定的。 羧酸羧基中的羟基被其它原子或基团取代后生成的化合物称为羧酸衍生物(ca rb oxyl ic a cid d eriv ative)。重要的羧酸衍生物有酰卤、酸酐、酯和酰胺。 羧酸及其衍生物广泛存在于动植物体内,它们与人类生活密切相关。日常生活中,洗涤用的肥皂是高级脂肪酸的钠盐;食用醋是含有2%乙酸的水溶液;食用油是羧酸甘油酯。在生物体内,某些羧酸是动植物代谢的重要物质,它们参与了动植物的生命过程,具有重要生理活性;某些羧酸衍生物是许多昆虫幼虫的激素,能控制昆虫的发育。在医药工业上,羧酸常用作合成药物的原料或中间体,有些药物本身就是羧酸或其衍生物,因此羧酸及其衍生物是一类与医药关系十分密切的有机物。 你在学习完本章节后,应能回答以下问题: 1.羧酸的分类和命名方法有几种? 2.羧基中存在着什么电子效应?羧酸在性质上如何反映出羧基结构中存在着这种电子效应的? 3.羧酸的酸性强弱取决于哪些因素,有何规律? 4.什么叫酯化反应?不同结构的醇与羧酸酯化反应的机制是否相同?可否写出反应机制? 5.不同的二元酸受热时所发生的反应有何差异? 6.羧酸衍生物的水解、醇解和氨解属于什么反应类型,反应机制如何?它们的活性次序如C O OH
第十章羧酸及其衍生物
第13章 羧酸 学习要求: 1. 掌握羧基的结构和羧酸的化学性质 2. 掌握诱导效应和共轭效应对羧酸酸性的影响 3. 掌握羧酸的制备方法以及重要的羧酸的主要用途 4. 掌握二元羧酸取代羧酸的特性反应 分子中含有羧基(-COOH )的一类化合物称为羧酸(Carboxylic acid )。羧基是羰酸 的官能团。除甲酸外,羧酸可看作是烃的羧基衍生物,其通式为:按羧基所连的烃基种类不同,羧酸可分为脂肪族羧酸、脂环族羧酸和芳香族羧酸。按烃基是否饱和,可分为饱和羧酸和不饱和羧酸。按羧酸分子中所含羧基的数目不同,又可分为一元羧酸、二元羧酸、三元羧酸等。二元及二元以上羧酸统称为多元羧酸。 羧基中的碳原子也是sp 2杂化方式成键的,它用三个sp 2杂化轨道分别与-OH的氧原子,羰基的氧原子和一个烃基的碳原子(也可以是一个氢原子)以σ键相结合,且这三个σ键在同一平面内。羰基碳原子上未参与杂化的p 轨道与羰基氧原子的p 轨道相互交盖而形成π键。-OH氧原子上的带有未共用电子对的p 轨道可以与π键形成p -π共轭体系,发生电子离域。 R H .. 13.1 羧酸的物理性质 甲酸、乙酸、丙酸是具有刺激性臭味的液体,丁酸至壬酸是具有腐败气味的油状液体,癸酸以上的正构羧酸是无臭的固体。脂肪族二元羧酸和芳香族羧酸都是结晶固体。 由于羧酸是个亲水基团,可和水形成氢键。甲酸至丁酸能与水混溶。从戊酸开始随相对分子质量增加,分子中非极性烃基增大,水溶性迅速降低。癸酸以上的羧酸不溶于水。脂肪族一元羧酸一般都能溶于乙醇、乙醚、氯仿等有机溶剂中。低级的饱和二元羧酸也可溶于水,并随碳链的增长而溶解度降低。芳酸的水溶性极微。 饱和一元脂肪酸,除甲酸、乙酸的相对密度大于1外,其它羧酸的相对密度都小于1。二元羧酸和芳酸的相对密度都大于1。 饱和一元羧酸的沸点随相对分子质量的增加而增高。羧酸的沸点比相对分子质量相同或相近的醇的沸点高。例如,甲酸和乙醇的相对分子质量均为46,而甲酸的沸点为100.7℃,乙醇的沸点为78℃;又如乙酸和丙醇的相对分子质量均为60,而乙酸的沸点为118℃,正丙醇的沸点为97.2℃。这是由于羧酸分子之间能由两个氢键互相结合形成双分子缔和二聚体。在固态和液态,羧酸主要以二聚体形式存在。据物理方法测定证明,甲酸、乙酸等低级的羧酸,在气相时仍以双分子缔和状态存在。 O R C O H O O C R H 羧酸的熔点随着碳原子数的增加而呈锯齿状上升。含偶数碳原子的羧酸的熔点比相邻两个奇数碳原子的羧酸的熔点高。如图13-1。这是因为偶数碳原子的羧酸分子的对称性较高,晶体排列比较紧密的缘故。 RCOH O
第十一章 第十二章 羧酸 取代酸及羧酸衍生物作业(1)
羧酸取代酸及羧酸衍生物一、命名下列化合物 二. 1.将下列化合物按酸性从强到弱的顺序排列 2.将下列各组化合物按酸性从强到弱的顺序排列 3. 将下列化合物,按α-H 酸性从强到弱顺序排列 4. 将下列化合物,按酸性从强到弱顺序排列 5. 将下列化合物,按酸性从强到弱顺序排列:
6、将下列化合物按酸性大小排列 7. 按酸性由强到弱排列的顺序是: 8. 下列化合物中烯醇式含量最多的是 9.下列化合物酸性由强至弱顺序是 10. 下列化合物的亚甲基活性(或酸性)最强的是 11.将下列化合物,按α-H 酸性从强到弱顺序排列 12. 将下列化合物按烯醇化由易到难排列成序: 13. 下列反应应用何种试剂完成? A、LiAlH 4B、NaBH 4 C、Fe + CH 3 COOH D、Pt + H 2 14. 下面哪些化合物能用NaBH4还原:
15.按α-氢的活性由大到小排列成序: 16、将下列化合物按酸性大小排列 17. 将下列化合物,按α-H 酸性从强到弱顺序排列 三、鉴别 1、用简单化学方法鉴别下列化合物. 2. 用简单化学方法鉴别下列化合物 3. 用简单化学方法鉴别下列化合物. 四、完成下列反应
五、推断结构 1.
3. 可由下列步骤合成止痛药Miltown,写出A,B,C,D的结构式 六、写出下列反应机理(附加题) 七、合成 2. 由苯及其它必要的试剂合成 5. 以丙二酸及C4有机原料合成化合物 6. 由乙酰乙酸乙酯、乙炔和必要的有机、无机试剂合成:
7. 由己二酸及苯甲腈合成 10. 由丙二酸二乙酯和不超过三个碳的原料及必要试剂合成 11. 由苯,丙二酸二乙酯合成5-苯基-1,3-环己二酮。 作业-2 一、将下列化合物,按酸性从强到弱顺序排列。 二.合成 1. 由苯及环己酮合成6-苯基己酸 4. 由不超过两个碳原子的化合物合成N-正丁基异戊酰胺。
第十三章羧酸及其衍生物课后答案
第十三章 羧酸及其衍生物 一、 用系统命名法命名下列化合物: 1.CH 3(CH 2)4COOH 2.CH 3CH(CH 3)C(CH 3)2COOH 3.CH 3CHClCOOH 4. COOH 5. CH 2=CHCH 2COOH 6. COOH 7. CH 3 COOCH 3 8. HOOC COOH 9. CH 2COOH 10(CH 3CO)2O 11O CO CH 3 12. HCON(CH 3)2 13. COOH O 2N O 2N 14. CO NH 3,5-二硝基苯甲酸 邻苯二甲酰亚胺 15. CH 3CHCHCOOH CH 3 OH 16. OH COOH 2-甲基-3-羟基丁酸 1-羟基-环己基甲酸 二、 写出下列化合物的构造式: 1.草酸 2,马来酸 3,肉硅酸 4,硬脂酸 HOOCCOOH C C H H COOH COOH CH=CHCOOH CH 3(CH 2)16COOH 5.α-甲基丙烯酸甲酯 6,邻苯二甲酸酐 7,乙酰苯胺 8。过氧化苯甲酰胺 己酸 2,2,3-三甲基丁酸 2-氯丙酸 2-萘甲酸 3-丁烯酸 环己烷甲酸 对甲基甲酸甲酯 对苯二甲酸 1-萘乙酸 乙酸酐 2-甲基顺丁烯二酸酐 N,N-2-甲基甲酰胺
CH 2=C CH 3 COOCH 3 CO O NHCOCH 3 O O OO NH C O H 2NCOOC 2H 5 C C NH O O O H 2N C NH 2 NH CO O CO n CH 2 CH O C O CH 3 []n 三、写出分子式为C 5H 6O 4的不饱和二元酸的所有异构体(包括顺反异构)的结构式,并指出那些容易生成酸酐: 解:有三种异构体:2-戊烯-1,5-二酸;2-甲基-顺丁烯二酸;2-甲基-反丁烯二酸。其中2-甲基-顺丁烯二酸易于生成酸酐。 C C H COOH COOH C C H COOH CH 3 HOOC CH 3 HOOC CH=CHCH 2COOH 2-戊烯-1,5-二酸;2-甲基-顺丁烯二酸;2-甲基-反丁烯二酸 四、比较下列各组化合物的酸性强度: 1,醋酸, 丙二酸, 草酸, 苯酚, 甲酸 CH 3COOH , HOOCCOOH HOOCCH 2COOH , , OH , HCOOH HOOCCOOH HOOCCH 2COOH HCOOH OH CH 3COOH > > > > 9.ε-己内酰胺 10,氨基甲酸乙酯11,丙二酰脲 12,胍 13,聚马来酸酐 14,聚乙酸乙烯酯 酸性强度顺序:
羧酸和衍生物_习题
酸及其衍生物 习题 1. 用系统命名法命名(如有俗名请注出)或写出结构式 (CH 3)2CHCOOH OH COOH CH 3CH=CHCOOH CH 3CHCH 2COOH CH 3CH 2CH 2COCl (CH 3CH 2CH 2CO)2O CH 3 CH 2COOC 2H 5CH 3CH 2CH 2OCOCH 3 CONH 2 HOOCC=CCOOH N-U.DMF a. b. c. d.e. f.g.h.i.j. k. 邻苯二甲酸二甲酯 l. 甲酸异丙酯 m. 甲基丙酰胺 s.苯甲酰基 n---r.略 t. 乙酰基
答案: a. 2-甲基丙酸 2-Methylpropanoic acid (异丁酸 Isobutanoic acid ) b. 邻羟基苯甲酸(水酸)o -Hydroxybenzoic acid c. 2-丁烯酸 2-Butenoic acid d 3-溴丁酸 3-Bromobutanoic acid e. 丁酰氯 Butanoyl Chloride f. 丁酸酐 Butanoic anhydride g. 丙酸乙酯 Ethyl propanoate h. 乙酸丙酯 Propyl acetate i. 苯甲酰胺 Benzamide j. 顺丁烯二酸 Maleic acid s. C O t. H 3C C O k. COOCH 3 COOCH 3l. HCOOCH(CH 3)2 m. CH 3CH 2CONHCH 3 2 将下列化合物按酸性增强的顺序排列: a. CH 3CH 2CHBrCO 2H b. CH 3CHBrCH 2CO 2H c. CH 3CH 2CH 2CO 2H d. CH 3CH 2CH 2CH 2OH e. C 6H 5OH f. H 2CO 3 g. Br 3CCO 2H h. H 2O
有机化学第二版 高占先著 第十一章课后答案
第11章 羧酸及其衍生物 11-1 将下列各组化合物按酸性由强至弱排列成序。 CH 3COOH ClCH 2COOH Cl 3CCOOH OH A. B. C. D.A. B. C. D. COOH Br COOH NO 2COOH OCH 3 COOH NO 2NO 2 COOH OH COOH COOH OH A. B. C. (1) (2) (3) (1)D >B >A >C; (2)C >B >A >D; (3)B >A >C 。 知识点:羧酸的酸性。 11-2 将下列各组化合物按水解反应速率由大至小排列成序。 CH 3COCl (CH 3CO)2O CH 3CONHCH 3 A. B. C. D.COOCH 3 NO 2 COOCH 3 CH 3 COOCH 3 A. B. C. (1) (2)CH 3COOC 2H 5 (1)A >B >D >C; (2)A >C >B 。 知识点:羧酸衍生物水解反应活性。水解反应就是亲核加成-消除反应,连有吸电子基有利于反应进行。 11-3 比较下列酸在H +催化下进行酯化反应的速率。 HCOOH CH 3COOH CH 3CH 2COOH (1)(2)(3)(CH 3)2CHCOOH (4) (1)>(2)>(3)>(4) 知识点:酸酯化反应活性。 11-4 完成下列反应。 (1) COOH OH OH O O O + (1) LiAlH 4(2)H 2C COOH 2H 2C CH 2OH
SOCl 2 (3)H 3C CH 2CH 23C CH 2CH 2COCl H 3C O AlCl 3 (分子内酰基化) (1) Zn, CH 3CH(Cl)COOEt (Reformasky 反应) (4) (2) H 2O O OH CHCOOC 2H 5CH 3 (5)Br 2/红磷 CH 2 COOH CHCOOH Br (酰胺还原) (6) N H O (Hofmann 降解) (7) 2 2 C 6H 5 H 32 C 6H 5 H 3 (8) H 3O (Claisen 酯缩合反应, Wittig 反应, Mannich 反应) (CH 3CO)2O (9) △ O (10) 3 (酯与格氏试剂反应,羟醛缩合反应) HCOOC 2H 5 NaOC 2H 5(11) + C H OH CHO (12)O O 333
