纳米银组装结构上罗丹明B的表面增强荧光效应

第26卷,第4期
光 谱 实 验 室Vol .26,No .42009年7月Chinese J ournal of Spectroscopy Labor atory July ,2009
纳米银组装结构上罗丹明B 的
表面增强荧光效应11国家自然科学基金资助项目(No.20473056)
o联系人,电话:(0512)65880362;E-mail:jwzh eng@https://www.360docs.net/doc/b312695493.html,
作者简介:冒薇(1984—),女,江苏省苏州市人,硕士研究生,主要从事表面增强荧光光谱研究工作。
收稿日期:2009-03-11;接受日期:2009-03-19
冒薇 李艳 周克勤 周群 郑军伟o
(苏州大学化学化工学院 江苏省苏州市十梓街1号 215006)
摘 要 采用表面自组装技术,在玻璃表面构筑银纳米粒子的二维组装结构。银纳米粒子组装结构的
表面等离子共振光谱中偶极子表面等离子体共振对组装结构更为敏感而表现出较大位移。组装银纳米粒子可极大增强罗丹明B 的荧光。荧光的表面增强效应主要来自银纳米粒子对荧光分子所处区域的局部电磁场增强,银纳米粒子的表面分子修饰对其表面增强效应有较大的影响。
关键词 银纳米粒子;表面等离子共振;表面增强荧光光谱;罗丹明B
中图分类号:O657.32 文献标识码:A 文章编号:1004-8138(2009)04-0885-03
1 前言
荧光检测在生物科学,生物工艺学,以及诊断学等领域是常用的分析测试技术,但对微量目标分子或弱荧光分子体系,荧光检测技术仍然存在一定的局限,因而多年来人们一直致力于探寻各种物理和化学的途径来增强被检测分子的荧光强度。众所周知,金属纳米粒子内部电子在特征频率的光作用下进行协同振荡可激发金属的表面等离子体共振,并由此产生了许多重要的光学现象,其中因金属纳米粒子的表面等离子体共振而导致的周围电磁场的增强是多年来人们研究的热点[1—4]。金属纳米粒子的局部电磁场与荧光分子的耦合可导致分子荧光的增强。但金属纳米粒子与分子的直接接触也可因分子与金属间的非辐射能量转移而导致分子荧光淬灭[5]。因而,荧光分子与金属纳米粒子之间的距离是影响其荧光强度的关键。本文利用表面自组装技术,在玻璃固体基底上构筑了银纳米粒子的二维组装结构,探索了金属纳米粒子对荧光分子罗丹明B 的表面增强效应,同时考察了金属粒子表面修饰对其荧光增强效应的影响。
2 实验部分
2.1 化学试剂
罗丹明B 和聚乙烯吡啶(PVP)(比利时Acros 公司);十二硫醇(东京化纯);其他试剂均为分析纯;实验中溶液均采用三次去离子水配制。
2.2 银纳米粒子组装及其表面修饰
银纳米粒子溶胶采用氢气还原法制备,银纳米粒子的粒径约为200nm 。纳米银粒子在玻璃表面进行组装:将清洗后的载玻片置于2%PVP 的乙醇溶液中浸泡约2h ,然后用无水乙醇反复冲洗再放入银溶胶中静置约9h ,既得单层银纳米粒子组装玻片。再把已组装单层银纳米粒子的组装玻片放入十二硫醇静置约3h ,即在单层银纳米粒子表面吸附了硫醇分子。
2.3 仪器测试
紫外光谱采用T U -1800紫外光谱仪(北京普析通用仪器有限公司)测定,银纳米粒子的形貌在日本日立公司H-570型扫描电子显微镜上测定。荧光光谱测试在日本日立公司F-2500型荧光光谱仪上进行,表面增强荧光测试采用薄层法,基底表面溶液厚度约为1L m 。
3
结果与讨论
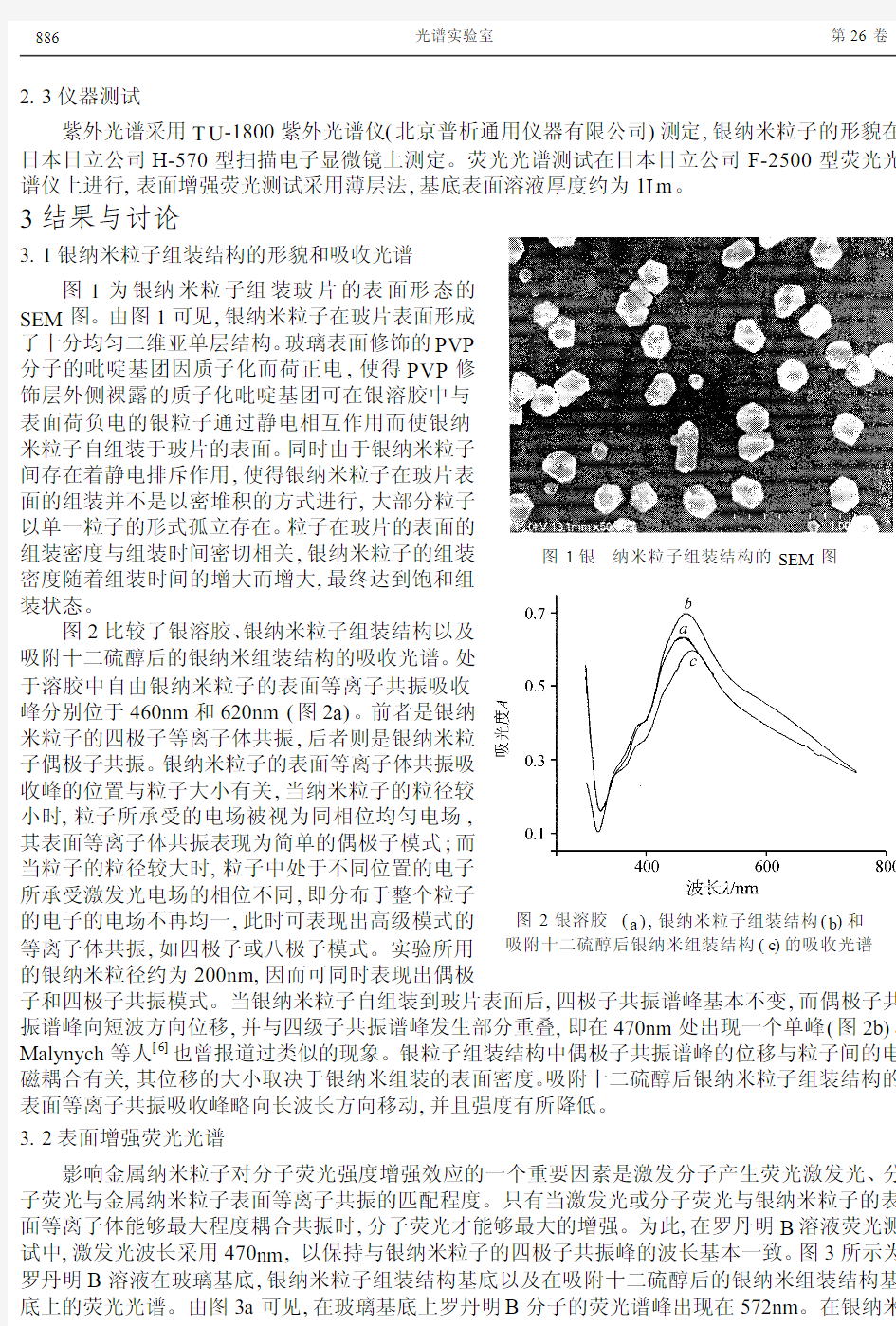
图1 银纳米粒子组装结构的SEM 图3.1 银纳米粒子组装结构的形貌和吸收光谱
图1为银纳米粒子组装玻片的表面形态的
SEM 图。由图1可见,银纳米粒子在玻片表面形成
了十分均匀二维亚单层结构。玻璃表面修饰的PVP
分子的吡啶基团因质子化而荷正电,使得PVP 修
饰层外侧裸露的质子化吡啶基团可在银溶胶中与
表面荷负电的银粒子通过静电相互作用而使银纳
米粒子自组装于玻片的表面。同时由于银纳米粒子
间存在着静电排斥作用,使得银纳米粒子在玻片表
面的组装并不是以密堆积的方式进行,大部分粒子
以单一粒子的形式孤立存在。粒子在玻片的表面的
组装密度与组装时间密切相关,银纳米粒子的组装密度随着组装时间的增大而增大,
最终达到饱和组
图2 银溶胶(a ),银纳米粒子组装结构(b )和吸附十二硫醇后银纳米组装结构(c )的吸收光谱装状态。
图2比较了银溶胶、银纳米粒子组装结构以及
吸附十二硫醇后的银纳米组装结构的吸收光谱。处
于溶胶中自由银纳米粒子的表面等离子共振吸收
峰分别位于460nm 和620nm (图2a )。前者是银纳
米粒子的四极子等离子体共振,后者则是银纳米粒
子偶极子共振。银纳米粒子的表面等离子体共振吸
收峰的位置与粒子大小有关,当纳米粒子的粒径较
小时,粒子所承受的电场被视为同相位均匀电场,
其表面等离子体共振表现为简单的偶极子模式;而
当粒子的粒径较大时,粒子中处于不同位置的电子
所承受激发光电场的相位不同,即分布于整个粒子
的电子的电场不再均一,此时可表现出高级模式的
等离子体共振,如四极子或八极子模式。实验所用的银纳米粒径约为200nm,因而可同时表现出偶极
子和四极子共振模式。当银纳米粒子自组装到玻片表面后,四极子共振谱峰基本不变,而偶极子共振谱峰向短波方向位移,并与四级子共振谱峰发生部分重叠,即在470nm 处出现一个单峰(图2b )。Malynych 等人[6]也曾报道过类似的现象。银粒子组装结构中偶极子共振谱峰的位移与粒子间的电磁耦合有关,其位移的大小取决于银纳米组装的表面密度。吸附十二硫醇后银纳米粒子组装结构的表面等离子共振吸收峰略向长波长方向移动,并且强度有所降低。
3.2 表面增强荧光光谱
影响金属纳米粒子对分子荧光强度增强效应的一个重要因素是激发分子产生荧光激发光、分子荧光与金属纳米粒子表面等离子共振的匹配程度。只有当激发光或分子荧光与银纳米粒子的表面等离子体能够最大程度耦合共振时,分子荧光才能够最大的增强。为此,在罗丹明B 溶液荧光测试中,激发光波长采用470nm ,以保持与银纳米粒子的四极子共振峰的波长基本一致。图3所示为罗丹明B 溶液在玻璃基底,银纳米粒子组装结构基底以及在吸附十二硫醇后的银纳米组装结构基底上的荧光光谱。由图3a 可见,在玻璃基底上罗丹明B 分子的荧光谱峰出现在572nm 。在银纳米
886光谱实验室第26卷
图3 罗丹明B 在玻片(a ),银纳米粒子组装结构上(b ),以及在吸附硫醇后的银纳米组装
结构上(c )的荧光吸收光谱
粒子组装结构基底上,罗丹明B 的荧光强度明显得
到增强,其荧光增强因子约为2(图3b );当组装银纳
米吸附硫醇后,罗丹明B 分子的荧光强度进一步增
加,增强因子可提高到4(图3c )。由此可清楚地看到,
银纳米粒子对罗丹明B 荧光的增强效应与银纳米粒
子的表面等离子体共振密切相关。实验中激发波长
(470nm)与表面等离子体共振谱峰重叠,使得银纳米
粒子周围激发光电磁场得到很大增强,进而使处于银
纳米粒子附近的罗丹明B 分子的荧光得到增强。罗
丹明B 的荧光增强效果还依赖于分子与银纳米粒子
之间的距离,与银粒子表面直接接触的罗丹明B 分
子因非辐射能量转移可导致这部分分子荧光淬灭。银
纳米粒子表面吸附硫醇后,消除了荧光分子与金属纳
米粒子直接接触或键合,从而使得罗丹明B 分子的
荧光得到更大程度的增强。参考文献
[1]Fauth K,Kreibig U ,Schmid G.Optical Plasmon Losses in Stabilized
Au55Clusters [J].Z .Phys .D -Atom ,Molecules and Clusters .,1991,20(1—4):297—300.
[2]Ash lee N F,Dimitrios V,Papavassiliou.Flow Around Surface-Attached Carbon Nan otubes[J].I nd .E ng .Chem .Res .,2006,45(5):
1797—1804.
[3]Rao N R,Kulkarni G U,T hom as P J et al .Size-Dependent Ch emistry:Properties of Naocrystal s [J].Chem .Eur .J .,2002,8(1):
28—35.
[4]Kelly K L ,Coronado E,Zhao L L et al .T he Optical Properties of Metal Naoparticles :The Influence of Size,Shape,and Di electric
E nvironment[J ].J .P hy .Chem .B .,2003,107(3):668—677.
[5]Kerker M,Blatchford ,C.G.Elastic Scattering,Absorpti on,and Surfac-E nhanced Raman Scattering by Concentri c Spheres
Comprised of A Metallic and A Dielectr Ic Region[J].Phys .ReV .B .,1982,26(8):4052—4063.
[6]Malynych S ,Chum anov G .Li gh t Induced Coherent Interactions between Silver Nanoparti cles in Two -Dimension al Arrays [J ].J .
Am .Chem .Soc .,2003,125(10):2896—2898.
Surface -Enhanced Fluorescence of Rhodamine B on Assembled
Structure of Silver Nanoparticles
M AO Wei L I Yan Z HOU Ke -Qin Z HOU Qun Z HENG Jun -Wei
(School of Chemistry ,Suzhou Universi ty ,Suzhou ,J iang su 215006,P .R .Chi na )
Abstract Two -dimensional structure of silver nanoparticles was constructed on glass slides by self-assembly technique.T he absorption spectra of the silver nanoparticles indicate that the dipolar surface plasmon resonance (SPR)of the silver nanoparticles is more sensitive to the assembled structure,a larger shift of this band was observed.T he assembled structure of the silver nanoparticles can greatly enhance the fluorescence of Rhodamine B molecules .The surface enhancement is ascribed to the enhancement of the local electric field near the metal particles.Surface modification of the silver nanoparticles have large effect on the enhancement of the Rhodamine B fluorescence.
Key wor ds Silver Nanoparticle ;Surface Plasmon Resonance ;Surface Enhancement Fluorescence
Spectroscopy;Rhodamine B 887第4期冒薇等:纳米银组装结构上罗丹明B 的表面增强荧光效应
实验四 血涂片的制备与染色
实验四血涂片的制备与染色 【目的】掌握血涂片的制备和染色方法(preparation and staining of thin blood films)。 【原理】将一小滴血液均匀涂在玻片上,呈单层紧密分布,制成薄血片。用含天青B和伊红的Romannowsky类染料进行染色。细胞中的碱性物质如RBC中的血红蛋白及嗜酸性粒细胞胞质中的嗜酸性颗粒等与酸性染料伊红结合染成红色;细胞中的酸性物质如淋巴细胞胞质及嗜碱性粒细胞质中的嗜碱性颗粒等与碱性染料亚甲蓝结合染成蓝色;中性粒细胞的中性颗粒呈等电状态与伊红和美蓝均可结合,染成淡紫红色。 【器材】 1.载玻片使用前,必须仔细清洗,并用乙醇或软布清洁。 2.推片选择边缘光滑的载玻片,在两角分别作斜线标记,然后用玻璃切割刀裁去两角,制成约15mm 宽度的推片。 3.吸耳球。 4.显微镜。 5.酒精灯或Bunsen灯。 6.采血针。 7.注射器和针头。 【试剂】 1.瑞氏(Wright)染液 (1)Ⅰ液:包含瑞氏染料1.0g、纯甲醇(AR级以上)600ml、甘油15ml。将全部染料放入清洁干燥的乳钵中,先加少量甲醇慢慢地研磨(至少30min),以使染料充分溶解,再加一些甲醇混匀,然后将溶解的部分倒入洁净的棕色瓶内,乳钵内剩余的未溶解的染料,再加入少许甲醇细研,如此多次研磨,直至染料全部溶解,甲醇用完为止。再加15ml甘油密闭保存。 (2)Ⅱ液:磷酸盐缓冲液(pH6.4~6.8),包含磷酸二氢钾(KH2PO4)0.3g、磷酸氢二钠(Na2HPO4)0.2g、蒸馏水加至1000ml。配好后用磷酸盐溶液校正pH,塞紧瓶口贮存。如无缓冲液可用新鲜蒸馏水代替。 2.吉姆萨染液包含吉姆萨染料0.75g、甘油35ml、甲醇65ml。将吉姆萨染料、甘油和甲醇放入含玻璃珠的容器内,每天混匀3次,连续4天,最后过滤备用。 3.瑞-吉复合染液 (1)I液:包含瑞氏染料1g、吉姆萨染料0.3g、甲醇500ml、中性甘油10ml。将瑞氏染料和吉姆萨染料置洁净研钵中,加少量甲醇,研磨片刻,再吸出上液。如此连续几次,共用甲醇500ml。收集于棕色玻璃瓶中,每天早、晚各摇3min,共5d,以后存放1周即能使用。 (2)Ⅱ液:即磷酸盐缓冲液(pH6.4~6.8)。包含无水磷酸二氢钾6.64g、无水磷酸氢二钠2.56g,加少量蒸馏水溶解,用磷酸盐调整pH,加水至1000ml。 【标本】 EDTA抗凝静脉血或末梢血。 【操作】 1.采血 (1)静脉采血法:用EDTA·K2抗凝1~2h内的标本,使用玻棒、毛细管、注射针头等在距载玻片一端1cm处加1滴抗凝血,直径约4mm。 (2)皮肤采血法:选择第三、四手指,并先采红细胞、白细胞计数,再采血1滴置洁净玻片上用于血涂片制备。 2.制作涂片左手平执载玻片,或放在类似桌子等平坦地方,右手持推片从后方移动接近血滴,使血
吉姆萨染色液
吉姆萨染色液 【产品名称】 吉姆萨染色液 【包装规格】 货号:DM0002 单瓶包装规格分别为: A液吉姆萨染液:20ml、100ml、250ml、500ml;B液磷酸盐缓冲液:250ml、500ml、5000ml; 每套/盒包装规格分别为: A液20ml+B液250ml/盒、A液100ml+B液4×250ml/盒、 A液250ml+B液5×500ml/盒、A液500ml+B液5000ml/盒。 【预期用途】 用于组织细胞学染色从而鉴别骨髓和其他造血组织(淋巴结)中的白细胞,还可用于鉴定某些微生物。 【检验原理】 吉姆萨染色原理及结果与瑞氏染色基本相同,吉姆萨染色液(Giemsa stain,又称姬姆萨染色液)对胞浆着色力较强,能较好的显示胞浆的嗜碱性程度,特别是对血液和骨髓细胞中的嗜天青、嗜酸性、嗜碱性颗粒,着色清晰,但是对胞核着色偏深,核结构显色不佳,故吉姆萨染色常与瑞氏染色联合使用。嗜酸性颗粒为碱性蛋白质,与酸性染料伊红结合,染粉红色,称为嗜酸性物质;细胞核蛋白和淋巴细胞胞浆为酸性,与碱性染料美蓝或天青结合,染紫蓝色,称为嗜碱性物质;中性颗粒呈等电状态与伊红和美蓝均可结合,染淡紫色,称为中性物质。血细胞染色:吉姆萨染料中含有美蓝和伊红两种染料,前者为碱性,后者为酸性,它们与细胞内的各种物质具有不同的亲和力,从而使其呈现出不同的色调,以便于辨认。染色体染色:也称G显带,染色体上富舍A-T碱基对的DNA和组蛋白结合紧密,胰酶处理时不易高度抽提,和染料亲和力较强,呈深带;而富含G-C碱基对的区段结合的蛋白质被胰酶抽提,和染料亲和力降低,呈浅带。 【主要组成成分】 试剂组成主要成分 1、A液吉姆萨染液吉姆萨染料 2、B液磷酸盐缓冲液磷酸盐 【储存条件及有效期】 5℃~35℃环境保存,原包装未开封染色液的有效期为24个月,在有效期内的已开封染色液应在开封后6个月内使用完,每次用后应及时拧紧瓶盖,以免挥发或变质。 【样本要求】 血细胞:要求新鲜全血或EDTA.2K抗凝血。 染色体:中期染色体。 疟原虫:耳垂或指尖采血作薄血膜或厚血膜涂片。 【检验方法】 (一)疟原虫、血细咆染色: 1、血涂片晾干后用甲醇固定; 2、配制吉姆萨染色液:取适量的A1吉姆萨染液和A2磷酸盐缓冲液,按一定比例混合,即为吉姆萨染色液,即配即用; 3、将固定的血涂片置于吉姆萨染色液浸染;
吉姆萨染色液Giemsa stain
吉姆萨/姬姆萨染色液(Giemsa stain,1:9) 产品简介: 吉姆萨染液由天青2与伊红混合而成。染色原理和结果与瑞氏染色法基本相同,姬姆萨染色液对胞浆着色力较强,能较好的显示胞浆的嗜碱性程度,特别是对血液和骨髓细胞中的嗜天青、嗜酸性、嗜碱性颗粒,着色清晰,但是对胞核着色偏深,核结构显色不佳,常与故姬姆萨染液常与瑞氏染液联合使用。 嗜酸性颗粒为碱性蛋白质,与酸性染料伊红结果,染粉红色,称为嗜酸性物质;细胞核蛋白和淋巴细胞胞浆为酸性,与碱性染料美蓝或天青结合,染紫蓝色,称为嗜碱性物质;中性颗粒呈等电状态与伊红和美蓝均可结合,染淡紫色,称为中性物质。 Leagene Giemsa stain以进口的吉姆萨/姬姆萨色素为主要原料,通过研磨配制而成,能呈现出清晰的细胞染色效果。经常用于组织切片、血液和细胞涂片、细菌、染色体显带、原生动物寄生虫等染色。 Giemsa stain(1:9)的特点在于,由Giemsa stain储存液(10×)和磷酸盐缓冲液组成,1:9混合成工作液后使用;亦可以分开使用,即先用Giemsa stain染色液染色,再经磷酸盐缓冲液处理,亦可以得到满意的染色效果。 产品组成: 主要成分: 试剂(A): 主要由吉姆萨色素、甲醇等组成。 试剂(B): 主要由磷酸盐等组成。 自备材料: 1、载玻片 2、蒸馏水或去离子水 3、甲醇 4、染色架 5、显微镜 6、0.1~0.5%的乙酸
操作步骤(仅供参考): (一)一步法涂片染色 1、Giemsa stain工作液的配制: 按试剂(A):试剂(B)=1:9混合,即取1份的Giemsa stain储存液(10×)加入到9份的磷酸盐缓冲液中充分混匀,即为Giemsa stain工作液。配制后Giemsastain的工作液为即用型试剂,不易保存,即用即配。 2、常规方法制备血液涂片或骨髓涂片,待涂片自然干燥后,用甲醇固定1~3min。 3、将血液涂片或骨髓涂片放置染色架上,滴加Giemsa stain工作液覆盖涂片,室温滴染 15~30min。 4、用自来水或蒸馏水缓慢从玻片一端冲洗。 5、干燥、镜检。 染色结果: 嗜酸性颗粒粉红色 嗜碱性颗粒紫蓝色 中性颗粒淡紫色 (二)两步法涂片染色 1、Giemsa stain工作液的配制: 按试剂(A):蒸馏水或去离子水=1:4配制Giemsa stain工作液,即取1份的Giemsa stain储存液(10×)加入到4份的蒸馏水或去离子水中充分混匀,即为Giemsa stain工作液。配制后Giemsa stain的工作液为即用型试剂,不易保存,即用即配。 2、常规方法制备血液涂片或骨髓涂片,待涂片自然干燥后,用甲醇固定1~3min。 3、将血液涂片或骨髓涂片放置染色架上,滴加Giemsa stain工作液覆盖涂片,室温滴染 10~15min。 4、加入等量磷酸盐缓冲液,轻轻晃动载玻片,室温静置5~10min。 5、用自来水或蒸馏水缓慢从玻片一端冲洗。 6、干燥、镜检。 染色结果: 嗜酸性颗粒粉红色 嗜碱性颗粒紫蓝色 中性颗粒淡紫色 (三)组织切片染色
瑞氏-吉姆萨染液是什么
瑞氏-吉姆萨染色液说明书 【产品名称】 瑞氏-吉姆萨染色液 【包装规格】 货号:DM0007 单瓶包装规格分别为:100ml、250ml、500ml、5000ml; 每套/盒包装规格分别为:2×20ml/盒、 2×100ml/盒、2×250ml/盒、2×500ml/盒、2×5000ml/盒。【预期用途】 主要用于对血细胞进行染色 【检验原理】 瑞氏染料是酸性染料伊红(Eosin)和碱性染料亚甲蓝(Methylene Blue)组成的复合染料, 对原生质的染色有很好的区别作用;吉姆萨染料由天青Ⅱ与伊红混合而成,染色原理和结果与瑞氏染色基本相同,吉姆萨染色对胞浆着色力较强,能较好的显示胞浆的嗜碱性程度,特别对血液和骨髓细胞中的嗜天青、嗜酸性、嗜碱性颗粒,着色清晰,但是对胞核着色偏深,核结构显色不佳,常与瑞氏染色联合使用。 瑞氏-吉姆萨染色液是利用Romanowsky Stain技术原理改良而成的,细胞的着色过程是染料透入被染物并存留其内部的一种过程,此过程既有物理吸附作用,又有化学亲和作用,各种细胞及相关成分由于其化学性质不同,对瑞氏-吉姆萨染色液中的酸性染料(伊红)和碱性染料(亚甲蓝)的亲和力也不一样,标本涂片经瑞氏-吉姆萨染色后,相应各类细胞呈现不同的着色,从而达到辨别其形态特征的目的。 【主要组成成分】 试剂组成主要成分 1、瑞氏-吉姆萨染液瑞氏染料、吉姆萨染料、甲醇 2、磷酸盐缓冲液磷酸盐 【储存条件及有效期】 5℃~35℃环境保存,原包装未开封染色液的有效期为24个月,在有效期内的已开封染色液应在开封后6个月内使用完,每次用后应及时拧紧瓶盖,以免挥发或变质。 【样本要求】 1、血细胞涂片染色:要求新鲜全血或EDTA.2K抗凝血。 2、阴道分泌物(妇科白带)涂片染色:新鲜标本离开人体涂片后,需尽快以火焰或酒精固定,以避免细胞变形。 3、骨髓涂片染色:涂片制成后,应在空气中快速摇动或扇干,防止细胞皱缩变形或固空气潮湿而溶血,不能用高温或火烤干燥。 4、脱落细胞涂片:取样本并涂片,待检涂片固定可采用自然干燥法或湿片固定法(具体操作可根据不同检体及所采用的固定液所对应的规范操作要求进行);若采用湿片固定法,标本浸泡时间稍长些,效果会更佳;若采用湿片固定液固定标本,固定液用后需经常过滤,更换,防止细胞交叉污染。 【检验方法】 1、滴加瑞氏-吉姆萨染液于涂片上,并让染液覆盖整个标本涂片,染色; 2、将等量的磷酸盐缓冲液滴加于瑞氏-吉姆萨染液上面,以嘴或洗耳球使两液充分混合,染色; 3、水洗,冲洗时不能先倒掉染色液,可缓慢从玻片一端冲洗,以防有沉渣沉淀在标本上; 4、干燥、镜检。 【检验方法的局限性】 仅供形态学初检观察染色使用。 【注意事项】 1、血液涂片或骨髓涂片应厚薄均匀,必须充分干燥,否则在染色过程中容易脱落,以免影响染色效果。
罗丹明类荧光探针研究进展_吴豪
罗丹明类荧光探针研究进展 吴豪,袁文兵* (海南大学材料与化工学院,海南海口 570228) [摘要]文章主要介绍近年来罗丹明衍生物在分子探针方面研究的一些新进展,系统阐述了该类探针分子在离子和小分子检测方面的应用。 [关键词]罗丹明;荧光探针;离子检测 [中图分类号]TQ [文献标识码]A [文章编号]1007-1865(2011)06-0265-01 Recent Progress in Rhodamine-Based Fluorescence Chemosensor Wu Hao, Yuan Wenbing* (College of Materials and Chemical Engineering, Hainan University, Haikou 570228, China) Abstract: The recent progress in the studies on rhodamines-based fluorescent probes was reviewed. The application of Rhodamine chemosensors in ions and small molecules sense were discussed in detail. Keywords: rhodamine;fluorescent sensor;ions sense 罗丹明B是重要的荧光探针材料,属于呫吨类染料。罗丹明B具有高的消光系数,较好的荧光量子产率,水溶性好,无毒,制备成本低等优点。因此,它是一类较好的荧光探针母体,极具广泛的应用价值。在中性或碱性条件下,罗丹明B内酰胺化合物以螺环状结构存在,体现紫外区吸收,无色,荧光减弱至消失。在酸性条件下以醌式结构存在,内酰胺结构开环,有荧光,体现长波吸收,成紫红色。 罗丹明基荧光染料由于其具有特殊的结构及相应的结构特性,使其广泛应用于化学分析和生命科学领域。目前的研究焦点多集中于通过不断修饰、优化罗丹明荧光分子探针的结构片段,以实现对小分子及离子的特异性识别,并进一步应用于生物活体及自然环境监测领域。 1 铜离子探针 铜是人体重要的微量元素,机体内铜缺失会导致代谢紊乱和诸多疾病,如胆固醇升高,动脉弹性降低,血压升高。一直以来,铜离子生物荧光探针的研究是一个热门课题。 1997年,Czarinik等[1]合成了罗丹明B酰肼,其可以选择性识别铜离子,该荧光探针是基于铜离子催化罗丹明B酰肼水解生成强荧光的罗丹明B分子的。 2006年,AijunTong等[2]合成水杨醛罗丹明B酰腙,可以可逆性的荧光增强识别铜离子。也就是说,在缓冲溶液中,当加入铜离子时,内酰胺螺环状结构被打开,吸收和荧光增强,当加入络合剂EDTA时,化合物表现出没有吸收和荧光,而在此时再加入铜离子,荧光恢复。 Yang等[3]通过在酸性条件下罗丹明B-酰肼与硫氰酸甲间的一步反应合成了一种Cu2+荧光探针。向该探针的乙腈/水溶液中添加Cu2+后,会造成荧光分子内酰胺键断裂,从而引起体系的荧光和紫外吸收明显增强。利用该探针实现了水相中Cu2+荧光和紫外检测,方法的线性范围分别为0.2~0.4和0.5~10 μmol/L。他们将该方法应用于自来水中Cu2+含量的测定,测定结果与原子吸收光谱方法测定结果一致。 Zhao等[4]在2009年设计合成了一种新型罗丹明内酰胺衍生物5,并将其应用于水溶液和活体细胞中Cu2+的检测。这种比色探针对铜离子的反应是瞬时可逆的,并且在其它金属离子浓度很高的情况下也不会对铜离子的比色和荧光信号产生干扰,这一特征使其很好地满足了生物医学和环境监测方面的特殊要求。目前,该类探针已广泛应用于环境体系中铜离子浓度的检测和生物活细胞铜离子分布成像实验,其优异的综合性能预示了极好的应用前景。 2 铁离子探针 铁是人体中所必须的微量元素,它在人体中主要以络离子的形式存在,与血红素、蛋白质等形成血红蛋白和肌红蛋白,在机体中起到运输和贮存氧的作用。由于Fe3+的顺磁性,一般的Fe3+荧光探针都是荧光熄灭型,不利于在牛物体内Fe3+的荧光成像及原位检测。因此利用罗丹明分子的闭环一开环间转换机理设计荧光增强型Fe3+荧光探针逐步受到重视。 2006年,Tong等[5]利用二乙基三胺将两个罗丹明B连接起来,从而形成无色,没有荧光的罗丹明B的衍生物,三价铁离子的加入,导致其内酰胺结构的开环,荧光增强,从而实现了对三价铁离子的检测。 2007年,Tae和Bae[6]利用肟酸作为Fe3+识别点的功能团,将氧肟酸引入罗丹明内酰胺和开环结构的平衡中。得到了一种新型的Fe3+探针。这种具有氧肟酸结构片段的罗丹明基荧光探针,在甲醇一乙腈(V∶V=1∶1)溶液中能很好的识别Fe3+,产生明显的荧光增强和颜色变化。 Peng等[7]通过乙二胺将2-羟基苯甲醛与罗丹明6G相连接,合成了一种Fe3+荧光探针。内酰胺的羰基氧原子、2-羟基苯甲醛上的羟基氧原子以及乙二胺上的氮原子同时参与了 Fe3+的螯合作用,导致了内酰胺键断裂,体系的荧光性增强。其他重金属和过渡金属离子无类似现象发生。 3 汞离子探针 汞是具有很高毒性的金属。汞单质及汞离子可通过各种途径进入环境,人体长期接触并摄入后会产生严重的恶心、呕吐、腹痛以及肾功能损伤等病症,危害极大。由于人们对汞毒性的高度重视,近年来对Hg2+荧光探针的研究日益增多。 Saresh等[8]以罗丹明6G为母体合成的Hg2+的荧光探针L1在水和甲醇(1∶1,φ)混合溶液中与Hg2+形成Hg (L1)2型复合物,荧光强度提高了90倍,利用L1测定Hg2+的检测线打到1 μg/L。25倍Hg2+浓度的Co2+,Fe2+,Ni2+,Zn2+,Pb2+,Cd2+,Mg2+,Ca2+,Ba2+,Li+,K+和Na+等离子对荧光信号基本无干扰。因而L1是一种高选择性、高灵敏度的Hg2+荧光探针。 Xu等[9]设计合成了一种罗丹明硫酰肼用于紫外和荧光检测水相中Hg2+,探针与Hg2+结合的化学计量比为2∶1.Qian等[10]设计合成的高选择性的罗丹明类Hg2+荧光探针不仅可以实现对Hg2+的荧光检测,而且利用显色反应可以对Hg2+的存在进行初步判断。该探针具有可逆性,当向显色的平衡体系中加入EDTA后,体系的紫红色变为无色。另外,荧光响应速度快是该探针的另一特点,Hg2+加入后立即产生稳定的强烈荧光,与同类的探针需要一定的平衡时间相比,该探针更适合于环境或者生物样品的实时分析。 2005年,Tae等[11]报道了一种十分精妙的罗丹明6G衍生物12,它可用于水溶液中Hg2+高灵敏度和高选择性的检测,即可以检测水溶液中低于2 μmol/L的Hg2+。 重金属与过渡金属离子的检测一般在水相中进行,尤其是生物体内的该类离子的原位检测对探针的水溶性提出了更高的要求。因此,在设计时要考虑探针的实用性,尽量引入具有一定水溶性的辅助基团。Huang等[16]将葡萄糖与罗丹明6G酰肼共价连接,合成了一种水溶性好、高选择性、高灵敏度的Hg2+荧光探针RGl。在纯水中,Hg2+的检测限达到1 μg/L,满足美国EPA规定。该探针可以在pH在5.5~10范围内使用,而且不受环境和生物样品中常见的其他金属离子的影响。因此,RGl可以应用在环境和生物体系,如细胞膜中汞离子的检测。另外,RGl与汞离子的结合是可逆的。向RGl和Hg2+共存的稳定体系中加入Na2S后,可以降低该体系的荧光强度,而再添加Hg2+时,体系的荧光则恢复。 (下转第243页) 新工艺新技术 [收稿日期] 2011-05-05 [作者简介] 吴豪(1988-),男,河南人,本科,主要研究方向为罗丹明类荧光探针。*为通讯作者。
吉姆萨染色鉴定细胞凋亡实验方法
吉姆萨检测细胞凋亡实验方案 1 材料及器具 吉姆萨染料(粉剂)、甘油、甲醇、KH2 PO4、Na2 HPO4、蒸馏水、封闭型棕色瓶 2 试剂配制 吉姆萨母液:吉姆萨染料粉剂0.75g 甘油50ml 甲醇50ml 将粉剂放于甘油内搅匀,放入60℃温箱24h,经常摇匀,取出待冷再加甲醇混匀,配成母液,封闭棕色瓶保存。 吉姆萨工作液:使用时以原液10ml加入pH为6.4-6.8的磷酸盐缓冲液100ml稀释成工作液。 磷酸盐缓冲液:A液Na2HPO4 0.946g,蒸馏水100ml B液KH2PO4 0.907g,蒸馏水100ml 临用时取A液40ml,B液60ml混合,pH值约为6.64。 3 染色步骤 (1)常规脱蜡至水; (2)蒸馏水洗; (3)在37℃温箱中吉姆萨染色30min; (4)蒸馏水洗2min; (5)PBS分色适度; (6)将切片从PBS中拿出,甩掉切片上的水分,放在空气中略干燥,以肉眼观察组织上的水分消失为度; (7)入100%酒精中30s至1min; (8)二甲苯透明5min; (9)中性树胶封片。 4 预期结果 背景淡蓝色,核为深蓝色,凋亡细胞为深蓝色。 5 体会
在染色中第6步是关键,不经过此步骤直接入100%酒精脱水,脱色会很严重,无法控制,使染色失败;在第6步后入95%的酒精中脱水,脱色也非常快;若将切片从PBS中拿出,甩掉切片上的水分,放在空气中略干燥,以肉眼观察组织上的水分消失后再入100%酒精脱水,效果良好。因此,用吉姆萨染料染料检测细胞凋亡操作简便、色彩鲜艳、对比度好、细胞核和凋亡细胞着色清晰,能够长期保存、不褪色,为一种值得推广的方法。 参考文献:《吉姆萨染色法对大脑组织凋亡细胞的染色》-徐广有,2005年
吉姆萨染色的原理
吉姆萨染色的原理 吉姆萨(Giemsa)染色法:吉姆萨染液由天青,伊红组成。染色原理和结果与瑞特染色法基本相同。 嗜酸性颗粒为碱性蛋白质,与酸性染料伊红结果,染粉红色,称为嗜酸性物质;细胞核蛋白和淋巴细胞胞浆为酸性,与碱性染料美蓝或天青结合,染紫蓝色,称为嗜碱性物质;中性颗粒呈等电状态与伊红和美蓝均可结合,染淡紫色,称为中性物质。 PH对细胞染色有影响。细胞各种成分均不蛋白质,由于蛋白质系两性电解质,所带电荷随溶液PH而定,在偏酸性环境中下在电荷增多,易与伊红结合,染色偏红;在偏三性环境中负电荷增多,易与美蓝或天青结合,染色偏蓝。因此细胞染色对氢离子浓度十分敏感,染色用正经片必须清洁,无酸碱污染。配制顼特液必须用优质甲醇,稀释染色必须用缓冲液,冲洗用水应近中性,否则可导致各种细胞染色反应异常,以致识别困难,甚至造成错误。 一般性操作技术血涂片制备;细胞染色;显微检查;血液病诊断;染色不良;瑞特(Wright)染色法;酸性染料;伊红;碱性染料;亚甲蓝;吸附作用;PH对细胞染色的影响;甲醇;吉姆(Giemsa)染色法春天要常用润肤剂,它含有松香油脂酸和丰富维生素a,常用可加快皮肤血液循环,剌激面部细胞分泌,有效改善皮肤生理环境,减少气候对皮肤的危害。 第二节血涂片的制备和细胞染色 血涂片的显微检查是血液细胞学检查的基本方法,临床上应用极为广泛,特别是对于各种血液病的诊断具有重要的价值,近年来血细胞分析仪的广泛应用,血涂片的观察也可作为判断仪器结果的简易方法。比台观察10个高倍视野血涂片中白细胞和血小板数大致估计血内这些细胞的数量,借以作为仪器结果分析后质控的参考。 但积压涂片制备和染色不良,常使细胞鉴别发生困难,甚至导致错误结论。例如,血膜过厚细胞重叠缩小,血膜太薄白细胞多集中于边缘,细胞分布不匀;染色偏酸或偏碱均可使细胞染色反应异常。因皮制备厚薄适宜,分布均匀,染色良好的血涂片是血液学检查的重要革本技术之一。 血涂片制备方法及注意事项将在实习指导中详细介绍。 1.瑞特(Wright)染色法:为发观察细胞内部结构,识别各种细胞及其异常变化,血涂片必须嘲行染色。血涂片的各种染色方法大多是罗氏染色法衍变来的。目前常用瑞特染色法。
基于罗丹明B的阳离子荧光探针的研究
基于罗丹明B的阳离子荧光探针的研究 .1分子荧光产生的原理 当用紫外或可见光照射某些物质时,这些物质吸收某种波长的光后会发射出波长和 强度各不相同的光线,当停止照射后,这种红光也随之消失,这种光被称为荧光汇1.2〕。对 荧光产生原理和条件直到十世纪中期才弄清楚。GorgeGStokes在1852年详细考察了奎 宁和叶绿素的荧光后,首先确定和报告了他们的荧光波长总比激发波长要长。他还研究 了荧光强度和荧光物质浓度的关系,发现在高浓度时荧光会淬灭,他也发现荧光可以被 外部物质淬灭,从而建议利用荧光达到检测的目的。由AlexanderJabfonski在1935年提 出的荧光产生的过程图,常被称为Jabfonski图131(见图 1.1)。通常情况下,荧光试剂 分子处于基态,吸收光后,试剂分子的电子被激发而处于激发态,基态和激发态都有单 重态和三重态两种类型。S为电子自旋量子数的代数和,其数值为O或1。S为O时, Fig.1.1JalllonskidiagramforaPhotolu刀。刃。eseentsystem 分子内轨道中的所有电子自旋配对,自旋方向相反,此时分子处于单线态,大多数有机 物分子的基态是处于单线态。分子吸收光能后,电子越迁到高能级,电子自旋方向不变, 此时分子处于激发单重态。S。,51,52,.…,表示分子的基态和第一,第二,…,激发 单重态,能量由低到高。如果处于基态单重态的有机物分子的电子在跃迁过程中伴随有
电子自旋方向的变化,在激发态分子轨道中就有两个自旋不配对的电子,此时S=l,表 明分子处于激发态的三重态,用T表示,Tl,T:分别表示三重态的第一第二激发态,分 子中的电子从基态S0跃迁到激发态51,52,比较容易发生,进行很快(10飞),而从基 态单重态到激发三重态不易发生。高能量的单重态激发态分子(如S:)可以与其它同类分子或溶剂分子碰撞通过内转换回到激发态的最低能级51,这一过程为10一,25,处于激发态最低能级的分子寿命一般为10礴一10一ss,它们会放出光子返回基态,这时产生的光就是 荧光。从51到Tl能量转化是系间跨越。从Tl到S。有两种过程:一个事物能量释放; 另一个是放出光子,即磷光,在104一105间完成。 1.2荧光分子探针的定义 荧光探针定义为能和个别组织特异结合而又不干扰其他组织成分自身荧光的那些 荧光化合物,为了和细胞中的自发荧光物质相区别,人们也曾称荧光染料为次级荧光体, 相应地把这种染色过程称为次级染色,把像叶琳这样的自然荧光物质称为初级荧光体。 而现在把所有的荧光探针,不管其染色性能和对天然荧光的影响如何,都统称为荧光探 针〔‘〕。 荧光探针大多是含有共扼双键体系的有机化合物,共辆双键使其容易吸收激发光, 其激发波长多处于近紫外区或可见光区,发射波长多处于可见光区。 作为荧光探针应该具有以下特点〔4]:第一,荧光探针的荧光必须与生物样品的背景 荧光易于区别;第二,荧光探针必须不干扰研究的主体;第三,荧光探针主要用于
吉姆萨配方
吉姆萨染色方法显示X染色质结构 吉姆萨粉1 g ,甘油 (AR) 66 mL ,甲醇(AR) 66 mL 。先将吉姆萨粉溶于少 量甘油中,用研钵研磨成匀浆,再将全部甘油倒入。 放入56 ℃温箱中2 h ,取出将甲醇加入混匀,即配成 原液,于棕色瓶中密封保存备用。临用时加入pH 为6. 8 的磷酸缓冲液( V∶V = 9∶1) 配成吉姆萨染色剂。 (二)吉姆萨染色法 此法可将细胞核与胞质同时染色,故便捷快速;但染液配制技术不易准确掌握,效果常不如HE染色稳定。 1.吉姆萨(Giemsa)染液的配制 (1)取1.5g吉姆萨粉末放入50ml甘油,置于60℃温箱,约3h后溶解。 (2)取出后倒入50ml中性甲醇,即为母液。于棕色瓶可长久保存。需要注意的是,有的甲醇内含醋酸,会使染液中的伊红沉淀出来,不利染色。 (3)将母液与0.1 mol/LPBS(Ph6.9~7.2)按1:9混合即成工作液。吉姆萨染 液对pH极敏感,偏酸时染色过红,偏碱时则过蓝。所以,工作液宜现用现配,保存时间不超过48h以免被CO2酸化。 瑞氏-姬姆萨染色方法 1、试剂配制: 原料:A:瑞氏染粉0.8--1克;吉姆萨染粉0.5克 B:甘油33ml C:甲醇500ml 配法:将A放入研钵中,加入少量B研磨,再加入少量B磨,再加入少量B磨……倒出,将未溶部分,继续加入B磨……>全溶,加入C,或中间加入C 亦可。 2、染色步骤: 滴数滴入玻片盖满标本,30秒,再加入双蒸水或PBS2-3倍染1-3分中,倾去染液,水洗……封片。 吉姆萨染色液贮备液配制:吉姆萨粉1g,加甘油60ml,加热并搅拌,待溶解冷却至室温,再加甲醇33ml 吉姆萨(Giemsa)氏母液 将吉姆萨粉末1g先溶于少量甘油,在研钵内研磨30min以上,至看不见颗粒为止,再将全部(66mL)剩余甘油倒入,于56℃温箱内保温2h。然后再加入甲醇(66mL),搅匀后保存于棕色瓶中。母液配制后放入冰箱可长期保存,一般刚配制的母液染色效果欠佳,保存时间越长越好。临用时用pH 6.8的磷酸盐缓冲液稀释10倍。 二、吉姆萨(Giemsa)氏母液 将吉姆萨粉末1g先溶于少量甘油,在研钵内研磨30min以上,至看不见颗粒为止,再将全部(66mL)剩余甘油倒入,于56℃温箱内保温2h。然后再加入甲醇(66mL),搅匀后保存于棕色瓶中。母液配制后放入冰箱可长期保存,一般刚配制的母液染色效果欠佳,保存时间越长越好。 临用时用pH 6.8的磷酸盐缓冲液稀释10倍。 Giemsa染液的配制: 吉姆萨粉(Giemsa stain) l.0g
吉姆萨染色的原理之欧阳光明创编
吉姆萨染色的原理 欧阳光明(2021.03.07) 吉姆萨(Giemsa)染色法:吉姆萨染液由天青,伊红组成。染色原理和结果与瑞特染色法基本相同。 嗜酸性颗粒为碱性蛋白质,与酸性染料伊红结果,染粉红色,称为嗜酸性物质;细胞核蛋白和淋巴细胞胞浆为酸性,与碱性染料美蓝或天青结合,染紫蓝色,称为嗜碱性物质;中性颗粒呈等电状态与伊红和美蓝均可结合,染淡紫色,称为中性物质。 PH对细胞染色有影响。细胞各种成分均不蛋白质,由于蛋白质系两性电解质,所带电荷随溶液PH而定,在偏酸性环境中下在电荷增多,易与伊红结合,染色偏红;在偏三性环境中负电荷增多,易与美蓝或天青结合,染色偏蓝。因此细胞染色对氢离子浓度十分敏感,染色用正经片必须清洁,无酸碱污染。配制顼特液必须用优质甲醇,稀释染色必须用缓冲液,冲洗用水应近中性,否则可导致各种细胞染色反应异常,以致识别困难,甚至造成错误。 一般性操作技术血涂片制备;细胞染色;显微检查;血液病诊断;染色不良;瑞特(Wright)染色法;酸性染料;伊红;碱性染料;亚甲蓝;吸附作用;PH对细胞染色的影响;甲醇;吉姆
(Giemsa)染色法春天要常用润肤剂,它含有松香油脂酸和丰富维生素a,常用可加快皮肤血液循环,剌激面部细胞分泌,有效改善皮肤生理环境,减少气候对皮肤的危害。 第二节血涂片的制备和细胞染色 血涂片的显微检查是血液细胞学检查的基本方法,临床上应用极为广泛,特别是对于各种血液病的诊断具有重要的价值,近年来血细胞分析仪的广泛应用,血涂片的观察也可作为判断仪器结果的简易方法。比台观察10个高倍视野血涂片中白细胞和血小板数大致估计血内这些细胞的数量,借以作为仪器结果分析后质控的参考。但积压涂片制备和染色不良,常使细胞鉴别发生困难,甚至导致错误结论。例如,血膜过厚细胞重叠缩小,血膜太薄白细胞多集中于边缘,细胞分布不匀;染色偏酸或偏碱均可使细胞染色反应异常。因皮制备厚薄适宜,分布均匀,染色良好的血涂片是血液学检查的重要革本技术之一。 血涂片制备方法及注意事项将在实习指导中详细介绍。 1.瑞特(Wright)染色法:为发观察细胞内部结构,识别各种细胞及其异常变化,血涂片必须嘲行染色。血涂片的各种染色方法大多是罗氏染色法衍变来的。目前常用瑞特染色法。 (1)瑞特染料是由酸性染料伊红和碱性染料亚甲蓝组成有复合染料。亚甲蓝为四甲基硫堇染料,有对醌型和邻醌型两种结构。通常
瑞氏吉姆萨复合染色液
瑞氏-吉姆萨复合染色液(Wright-Giemsa stain ) 产品简介: 瑞氏色素是酸性染料伊红(Eosin)和碱性染料亚甲蓝(Methylene Blue)组成的复合染料, 对原生质的染色有很好的区别作用。吉姆萨染液由天青2与伊红混合而成,染色原理和结果与瑞氏染色法基本相同,姬姆萨染色液对胞浆着色力较强,能较好的显示胞浆的嗜碱性程度,特别是对血液和骨髓细胞中的嗜天青、嗜酸性、嗜碱性颗粒,着色清晰,但是对胞核着色偏深,核结构显色不佳,常与故姬姆萨染液常与瑞氏染液联合使用。 Leagene Wright-Giemsa stain以进口的瑞氏色素和吉姆萨色素为主要原料,通过研磨配制而成,能呈现出清晰的细胞染色效果。经常用于血液和细胞涂片、骨髓细胞涂片、细菌染色。细胞质呈红色,细胞核及细菌呈蓝色,嗜酸性颗粒呈橘红色。染液中加中性甘油,防止甲醇挥发或氧化,同时也可使血细胞染色较清晰。 Leagene Wright-Giemsa stain的特点: 由瑞氏-吉姆萨复合染色液和磷酸盐缓冲液组成,等量混合使用或分别处理标本使用。 产品组成: 主要成分: 试剂(A): 主要由瑞氏色素、吉姆萨色素、甲醇等组成。 试剂(B): 主要由磷酸盐等组成。 自备材料: 1、载玻片 2、蒸馏水或去离子水 3、染色架 4、显微镜 操作步骤(仅供参考): 1、常规方法制备血液涂片或骨髓涂片或细菌涂片,待涂片自然干燥。
2、将血液涂片或骨髓涂片置于染色架上。 3、滴加Leagene Wright-Giemsa stain覆盖涂片,室温染色1~2min。 4、涂片滴加等量磷酸盐缓冲液,轻轻晃动玻片或采用其他方式混合,使磷酸盐缓冲液与 Wright-Giemsa stain混匀,室温静置3~10min。 5、步骤3、4亦可以采用如下方法:取Leagene Wright-Giemsa stain和磷酸盐缓冲液 等量混合后,即为Wright-Giemsa stain工作液,滴加工作液于血液涂片或骨髓涂片上,室温静置3~10min。 6、用自来水或蒸馏水从玻片一端轻轻冲洗。(注:也可用磷酸盐缓冲液等量稀释后,冲洗 玻片,时间控制在30s左右。) 7、干燥、镜检: 先用低倍镜观察血涂片,再用油镜。 染色结果: 细菌、细胞核蓝色 组织细胞的细胞质、血红蛋白、嗜酸性颗粒粉红或橘红色 注意事项: 1、血液涂片或骨髓涂片应厚薄均匀,以免影响染色结果。 2、涂片染色中,请勿先去除染液或直接对涂片用力冲洗。不能先倒掉染液,以免染料沉着 于涂片上。 3、染色液可重复使用,但不能多次重复,若有沉淀物应过滤后使用。 4、染色过深可用甲醇或酒精适当脱色,最好不复染。 5、如果染色过深或过浅,应调整染色时间或工作液的浓度。 6、为了您的安全和健康,请穿实验服并戴一次性手套操作。 有效期:12个月有效。 相关产品: 产品编号 产品名称 DM0002吉姆萨/姬姆萨染色液(Giemsa stain,1:9) DM0005瑞氏染色液(Wright Stain ) DM0015标准革兰氏染色试剂盒(Gram Stain) DM0035抗酸染色试剂盒(Kinyoun冷染法) DM0080乳酸酚棉蓝染色液
罗丹明荧光探针的设计、合成及光谱研究
罗丹明荧光探针的设计、合成及光谱研究 【摘要】:罗丹明类荧光染料具有独特的结构特性和突出的光物理性质,即在螺环状态下表现为非颜色和非荧光性质,而与客体分子作用生成其开环结构后表现为明显的颜色变化和荧光释放特性。将反应位点与罗丹明生色团相结合,设计出大量的基于罗丹明衍生物的荧光探针,不仅能够运用于识别传感阳离子,而且能用于阴离子、活性氧物质和中性分子的传感识别。本论文在总结前人工作的基础上,设计开发了四个基于罗丹明衍生物的荧光探针:罗丹明—吡啶甲酰肼衍生物、罗丹明—水杨甲酰肼衍生物、罗丹明—萘酰亚胺衍生物和罗丹明—吡啶腙衍生物。通过客体与探针分子作用后产生的独特光谱变化,采用荧光发射和紫外—可见光谱详细地研究了其传感性能,主要研究内容如下:将罗丹明和吡啶甲酰肼相结合得到了探针分子2-1,不仅能够通过与Cu2+的配位作用实现了在水溶液中对Cu2+的高选择性和高灵敏性的检测,而且利用C1O能定向氧化甲酰肼基团实现了对ClO的识别传感。实验结果表明,在乙腈/Tris-HC1(pH=7.0)缓冲溶液中,探针2-1与Cu2+形成了1:1的络合物并且结合常数为1.79×106M-1(R2=0.994),具有非常高的检测限(1nM)。在甲醇/Na2B407-NaOH(pH=12.0)缓冲溶液中对C1O-也显示出了很好的识别性能,其检测限可以达到1nM。相比于其它已经报道的Cu2+或C1O-荧光探针,这是第一个能在一个小分子中同时检测这两种离子的化学传感器。采用荧光”turn-on”策略来设计罗丹明铜离子配合物的CN-荧光传感器是非常困难的。因为氰离
子会将配合物中的Cu2+取代,生成没有颜色也没有荧光的罗丹明关环结构。将做为发色团的罗丹明B与水杨甲酰肼相连,我们设计合成了一个能够通过配位模式,导致荧光释放来传感识别氰离子的荧光探针3-1。化合物先与Cu2+发生配位作用并导致了明显的紫外吸收光谱变化,其与Cu2+的结合常数为1.7×107M-1。第一次培养出了罗丹明衍生物和铜离子络合产物的单晶,通过分析可以看出,两个水杨甲酰肼基团与两个Cu2+所形成的双铜中心近乎处于一个平面上,两个罗丹明基团处于垂直位置。由于化合物与Cu2+之间的强的配位作用和铜离子的强的荧光猝灭效应,我们将该配合物成功应用于CN-的识别。配合物3-1+Cu2+与氰离子的结合比为1:2,并且得到了高分辨质谱的证实。其对氰离子的检测限可以达到 1.4×10-7M,远远低于世界卫生组织(WHO)对饮用水中氰离子含量不得超过1.9μM的规定。基于FRET 机理,我们设计合成了一个基于罗丹明—萘酰亚胺的Hg2+比率荧光探针4-4。在甲醇/水=2/1(V/VpH=7.0,Tris-HCl,10mM)溶剂体系中探针能够和汞离子进行定量的1:1加汞脱硫反应,并进一步发生分子内成环反应而导致罗丹明开环结构,并释放出光信号。探针能够对Hg2+实现高效且具有高选择性的特异性识别,当主体浓度为0.1μM时,Hg2+浓度在0.030.08μM之间,汞离子浓度和荧光比值之间产生了良好的线性,说明探针对Hg2+浓度的检测可以在一个非常低的范围内进行。在单一分子中,同样条件下探针能够实现对不同物种的选择性识别,具有重要的实际应用价值。我们采用罗丹明肼毗啶腙化合物5-3,实现了在同一溶液中利用紫外可见光谱识别Cu2+,而通过明显的荧光增强来选
瑞氏吉姆萨复合染色液
外周血涂片的制作方法 1、采血:胶头滴管吸取血液,血液直接滴加到洗净烘干并且硅化过的载玻片的一头。 2、推片:将推片的平齐端置载玻片上血滴的稍前方,将推片略向后移使与血液相接触,血液遂于推片与载玻片的夹角间散开。以约30度的夹角向前均匀地推动推片即可制成血涂片。其薄厚度要适中,分布均匀而无空泡,边缘整齐。 3、固定:推片做好后,涂片后潮干固定,以免细胞漂落太多,影响制片质量, 甲醇固定液固定:涂片直接浸入固定液内,因固定液充足,固定效果较好。但细胞易脱落而发生交叉污染,因此应该分瓶固定,固定液回收时应过滤。多数标本用此法固定,固定时间15-30分钟。 4、染色:瑞氏-基姆萨双染 1)从固定缸里取出载片后,在室温下通风晾干。将载片平放在玻璃板上准备染色。 2)所用的两种染料事先过滤好(染料中有颗粒物,会沉淀在载玻片上影响载片的质量) 3)将染料滴加到载玻片上以后,让其均匀覆盖住载片上的血细胞,染色时间约为2到3分钟。等瑞氏染液有变红的趋势时,迅速滴加与瑞氏染液等量的PBS 溶液。继续染色2到3分钟。 4)染色时间到后,用PBS溶液冲片,小股水流,防止将大量的细胞从载片上冲落下来从而影响以后的观察。冲片结束后将载片放到阴凉处风干。 5)在玻璃板上放好牙签,将风干的载片倒扣在一根牙签上,从背面滴加基姆萨染液进行扣染。染色时间约为10分钟。时间到后用蒸馏水冲片,洗净染液后常温下风干。 5、封片:中性树胶封片,制作成永久涂片。 6、显微观察:将干燥后的血涂片置显微镜下观察。用低倍镜观察血涂片体、尾交界处的血细胞。在显微镜下,成熟红细胞染成粉红色;血小板染成紫色;中性粒细胞胞质染成粉红色,含紫红色颗粒;嗜酸性粒细胞含大的桔黄色颗粒;嗜碱性粒细胞胞质含有大量深紫蓝色颗粒;单核细胞胞质染成灰蓝色;淋巴细胞胞质染成淡蓝色。 所需材料:硅化过的载玻片,推片,甲醇瑞氏-基姆萨双染,过滤,PBS,牙签,蒸馏水,中性树胶,显微镜,吸耳球 1.载玻片使用前,必须仔细清洗,并用乙醇或软布清洁。 2.推片选择边缘光滑的载玻片,在两角分别作斜线标记,然后用玻璃切割刀裁去两角,制成约15mm宽度的推片。 目的:制备厚薄适宜,分布均匀,染色良好的血涂片
HE染色和吉姆萨染液
HE染色和吉姆萨染液 试剂和方法如下。 一、HE染色试剂:苏木素染液:苏木精1g;无水乙醇25mL;硫酸铝钾10g;蒸馏水350mL;碘酸钾0.1g;冰醋酸10mL。A 液:用25mL 无水乙醇溶解1g苏木精,摇动即可溶解。B 液:用350mL 蒸馏水溶解10g硫酸铝钾,摇动或振荡即可溶解。把A 液和B 液混合,加入碘酸钾摇动至颜色加深。最后加入10mL冰醋酸,摇动颜色变为深葡萄酒红色。染液配制当日即可应用于染色。酸化液:醋酸20-35mL加蒸馏水至700mL。伊红染液:储液:取1g伊红,溶于100mL 95%的乙醇,待溶解完全后加几滴冰醋酸至染液呈半透明状,避光保存备用。工作液:取一定量的伊红储液,加入等量70%乙醇,此液即为伊红染液的工作液。染色步骤:(1)细胞爬片放用PBS漂洗3次,每次5min,无水乙醇固定5min,风干。(2)95%乙醇1min,75%乙醇1min,三蒸水1min。( 3 ) 浸洗5 % 的醋酸液( 酸化液) 数秒。( 4 ) 苏木精染液3 - 5 m i n,胞核呈橙红色。( 5 ) 自来水冲洗至颜色变蓝。( 6) 盐酸乙醇液分化数秒,颜色再次返红。(7) 自来水再次冲洗,返蓝。( 8) 伊红染液5min,流水漂洗15min左右。二、吉姆萨染色试剂:吉姆萨染液配制:取吉姆萨粉末1g溶于66ml甘油中研磨混匀,然后放置55-60℃水浴2h,冷却后加入66ml甲醇中混匀,过滤后棕瓶分装保存。PBS甲醇液:PBS与甲醇一比一混合。染色步骤:(1)细胞爬片使用PBS漂洗3次,每次5min。(2)加PBS甲醇液静置2min,去掉PBS甲醇液。 (3)加甲醇固定10min,去掉甲醇,加入新无水甲醇漂洗去掉。(4)加吉姆萨染液2ml/25cm2,2min后加入8ml水稀释并晃动染液2min,去掉染液。(5)流水冲洗10~20s,湿润时观察。
Giemsa染色
Sorensen磷酸缓冲液配制 A液:0.067mol.L-1磷酸二氢钾溶液,称取KH2PO4 9.118g,用少许鲜蒸馏水60℃下溶后,定溶至1000ml。 B液:0.067mol.L-1磷酸氢二钠溶液,称取Na2HPO.12H2O,23.995g,用少许鲜蒸馏水60℃下溶后,定溶至1000ml;根据使用时pH值的要求按下例比例混合。 pH值:6.5 6.6 6.7 6.8 6.9 7.0 7.1 7.2 7.3 7.4 A液:68.7 62.8 57.0 51.0 44.8 38.8 33.0 27.6 22.3 18.2 B液:31.3 37.2 43.0 49.0 55.2 61.2 67.0 72.5 77.7 81.8 Sorensen缓冲液的配制: pH6.81:Na2HPO4(1/15M) 50mL + KH2PO4(1/15M) 50mL; pH6.98:Na2HPO4(1/15M) 60mL + KH2PO4(1/15M) 40mL pH7.17:Na2HPO4(1/15M) 70mL+ KH2PO4(1/15M) 30mL; pH7.38:Na2HPO4(1/15M) 80mL + KH2PO4(1/15M) 20mL。 pH的影响(pH6.4~pH6.8) 细胞各种成分均属蛋白质,因蛋白质系两性电解质,所带电荷随溶液pH而定,在偏酸性环境中正电荷增多,易与伊红结合,红细胞和嗜酸性粒细胞染色偏红,细胞核呈淡蓝色或不染色;在偏碱性环境中负电荷增多,易与美蓝结合,所有细胞呈灰蓝色,颗粒呈深暗,嗜酸性颗粒呈暗褐,甚至棕黑色,中性颗粒偏粗,呈紫黑色。稀释染液必须用缓冲液,冲洗用水应近中性,否则可导致细胞染色呈色异常,形态难以识别,甚至错误。 大型真菌Giemsa染色: 1.准备染液。吉姆萨浓缩液:吉姆萨稀释液(1:9),现配现用,2-8℃可保存一个月。 2.固定。用卡诺氏固定液或乙酸:乙醇(1:3)固定(1.5mlEP管内加500μl固定液)5h,5℃。固定的作用是杀死细胞,保持它生活时的真实状态。移至35%乙醇中15min。 3.冲洗。去离子水冲洗15min。流水冲洗——很难实现 4.置于1N HCl溶液中水解6-8min,60℃。冷去离子水冲洗15min。 5.移至磷酸缓冲液(pH7.0±0.2)浸泡10min。计算好缓冲液的量以确定加入的染色液量。 6.染色。用吉姆萨工作液染色2h, 5℃。(2滴约为0.2ml吉姆萨工作液/毫升缓冲液)染色过深可用流水冲洗或浸泡,也可用甲醇脱色。 7.加盖玻片打薄,显微观察。 对于新鲜菌褶,可先用卡诺氏固定液:乙酸:乙醇(1:3)固定后保存于35%乙醇中
