利用Gauss和Molden查看分子的轨道和电子密度等势图

利用Gauss和Molden查看分子的轨道和电子密度等势图
A——Molden的安装:
由于Molden的操作环境是Unix,因此需要在windows环境下安装X-Win32Pro这个虚拟环境,称为X-Server,然后才可以在windows下运行molden。
B——高斯文件:
要查看轨道需要输入文件把分子的轨道全部求出并写在out文件里,利用pop=full和gfinput 关键字(run a single point calculation at the desired level of theory including the pop=full and gfinput keywords. Only then will MOLDEN find all required information in the output file. 参考网址)以
#P HF/STO-3G scf=tight pop=full gfinput
HF/STO-3G//HF/STO-3G sp formaldehyde
0 1
C1
O2 1 r2
H3 1 r3 2 a3
H4 1 r3 2 a3 3 180.0
r2=1.21672286
r3=1.10137241
a3=122.73666566
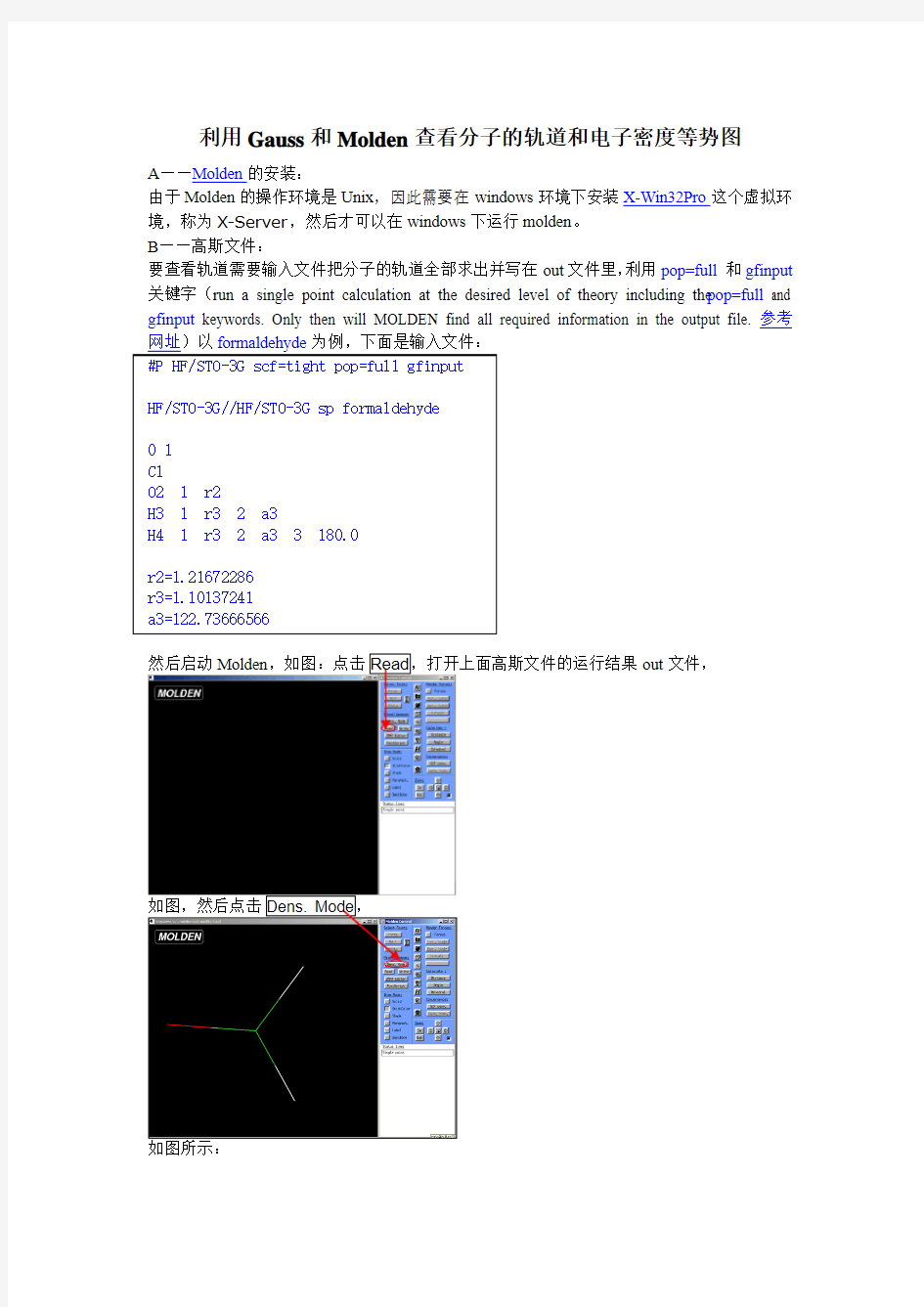
然后启动Molden,如图:点击Read,打开上面高斯文件的运行结果out文件,
如图,然后点击Dens. Mode,
这个contour HOMO的电子密度图
要查看各个轨道点击
上面的contour图是HOMO的电子密度图。
(When using Molden with GAUSSIAN 94/98/03 the following keywords are required on the GAUSSIAN 94/98/03 inputfile:
#P GFINPUT IOP(6/7=3)
#P switches on printing of SCF convergence, GFINPUT switches on printing of Basis Set info, and IOP(6/7=3) switches on printing of all MO's. GAUSSIAN 94/98 per default uses the redundant coordinate’s optim ization procedure resulting in only cartesian coordinates being available on the output file. Molden will covert these into a z-matrix which in general will have lost the dummys and therefore symmetry at the z-matrix level. Use the gaussian
keyword opt=z-matrix to get z-matrices on the output. 参考网址)
3 休克尔分子轨道法
休克尔分子轨道法 1 目的要求 (1) 运用HMO 程序计算若干平面共轭分子的电子结构。 (2) 通过HMO 程序的具体运算,加强对这一基本原理的理解,培养学生运用分子轨道概念解决实际问题的能力。 (3) 熟悉微型计算机和磁盘操作系统。 2 基本原理 (1) HMO 方法的基本原理:休克尔分子轨道法是量子化学近似计算方法之一,它以简便迅速著称,适宜于计算平面共轭分子中的π电子结构。在分析有机共轭分子的稳定性、化学反应活性和电子光谱,及研究有机化合物结构与性能的关系等方面有着广泛应用。 该方法主要运用了下列基本假定: ①σ-π分离近似。对于共轭分子,构成分子骨架的σ电子与构成共轭体系的π电子由于对称性的不同,可以近似地看成互相独立的。 ②独立π电子近似。分子中的电子由于存在相互作用,运动不是独立的,但若将其它电子对某电子的作用加以平均,近似地看成是在核和其它电子形成的固定力场上运动,则该电子的运动就与其它电子的位置无关,是独立的。 ③LCAO-MO 近似。对于π体系,可将每个π分子轨道Ψk 看成是由各原子提供的垂直于共轭体系平面的p 原子轨道i ?线性组合构成的,即 ∑= i i ki k C ?ψ (1) 在上述假定下,可列出π体系单电子Schrodinger 方程 k k E H ψ ψκπ=? (2)
将(1)式代入(2)式,利用变分原理,可得久期方程式: ()()()0112121211111=-++-+-n n n C ES H C ES H C ES H ()()()0222222212121 =-++-+-n n n C ES H C ES H C ES H ……………………………………………………………… ()()()0 222111 =-++-+-n nn nn n n n n C ES H C ES H C ES H 此方程组有非零解的充分条件 1 1 21 21 11 11n n ES H ES H ES H --- 02 2 2222 22 11112=------nn nn n n n n n n n ES H ES H ES H ES H ES H ES H 此行列式亦称为久期行列式。式中.,?ττ????d S d H H j i ij j n i ij ??= = 在H ückle 分子轨道理论中所做的近似为: 库仑积分α??τ ==?d H H j n i ij ? ?? ?+==-对杂原子对碳原子 l c x c x c βδααα0 (3) 共振积分β ??τ== ?d H H j n i ij ? 10±=? ?? ???-=-=---j i c c x x c c c 杂键碳碳键碳βηββ (4) 0 i ≠ j ±1 重叠积分 ?? ?== ?0 1τ??d S j i ij j i j i ≠= 其中c c c -βα,分别为碳原子库仑积分和C-C 键的共振积分,x x δα,分别为杂原子库仑积分与库仑积分参数,x x c ηβ,-分别为碳原子与杂原子间的共振积分和共振积分参数(β积分为负值)。代入简化行列式方程(4),解此方程可得n 个分子轨道的能量值k E (本程序中当反键前沿轨道与它后一轨道的能级差的绝对值小于或等于0.1时,实行轨道简并),将其分别代入(3)式,得出相应的{}ki C 值,再按(1)式得出分子轨道。 由系数{}ki C 可求得一系列量子化学指数如下:
拉盖尔高斯光束经透镜传输光场计算
成绩评定表 学生姓名吴宪班级学号1109020117 专业光信息科学 与技术课程设计题目拉盖尔高斯光束经 透镜传输光场计算 评 语 组长签字: 成绩 日期20 13 年12 月 27 日
学院理学院专业光信息科学与技术 学生姓名吴宪班级学号1109020117 课程设计题目拉盖尔高斯光束经透镜传输光场计算 实践教学要求与任务: 要求: 1)角向节线0,径向节线2的拉盖尔高斯光束(共焦参数=12000倍波长)通过薄透镜; 2)薄透镜(前置圆形光阑)焦距=1500倍波长,光腰在透镜处; 3)光阑半径=120倍波长。 任务: 1)计算该拉盖尔高斯光束经过薄透镜后时的轴上光强变化,分析焦点变化; 2)计算该拉盖尔高斯光束经过薄透镜前时的径向光强变化,计算截断参数; 3)计算该拉盖尔高斯光束经过薄透镜后的径向–轴向光强变化; 4)撰写设计论文。 工作计划与进度安排: 1. 第一周教师讲解题目内容、任务和论文要求,学生查阅资料,星期四提出设计方案; 2. 第一周星期四到第二周星期三(包括星期六星期日)完成设计; 3. 第二周星期四上交论文; 4. 星期四教师审查论文,合格者星期五论文答辩。 指导教师: 2013年月日专业负责人: 2013年月日 学院教学副院长: 2013年月日
目录 摘要 (4) 设计原理 (5) 一.普通球面波的传播规律 (5) 二.高斯光束的基本性质及特征参数 (6) 三.柯林斯(Collins)公式 (7) 四.基模高级光束的特征参数 (6) 计算结果10 一. 计算该拉盖尔高斯光束经过薄透镜前时的轴上光强变化,分析焦点变化 (10) 二. 计算该拉盖尔高斯光束经过薄透镜前时的径向光强变化,计算截断参数 (11) 三.计算该拉盖尔高斯光束经过薄透镜后的径向–轴向光强变化 (12)
(整理)休克尔轨道法的分子图.
休克尔轨道法的分子图 一、化学家休克尔 E.Erich Armand Arthur Josephckel (1896~) 联邦德国物理化学家。1896年8月9日生于柏林夏洛 腾堡。1914年入格丁根大学攻读物理。曾中断学习, 在格丁根大学应用力学研究所研究空气动力学。1918 年重新攻读数学和物理,1921年在P.德拜的指导下获 博士学位。他在格丁根大学工作两年,曾任物理学家 M.玻恩的助手。1922年在苏黎世工业大学再度与德拜 合作,任讲师。1930年在斯图加特工业大学任教。1937 年任马尔堡大学理论物理学教授。 休克尔主要从事结构化学和电化学方面的研究。 他1923年和德拜一起提出强电解质溶液理论,推导出强电解质当量电导的数学表达式。1931年提出了一种分子轨道的近似计算法即休克尔分子轨道法(HMO 法),主要用于π电子体系。他在30年代还对芳香烃的电子特性在理论上作出了解释,并总结出:环状共轭多烯化合物中π电子数符合4n+2(n为1,2或3)者,具有芳香性。 二、休克尔分子轨道法(HMO法)的来源 分子轨道理论在处理分子时,并不引进明显的价键结构的概念。它强调分子的整体性,认为分子中的原子是按一定的空间配置排列起来的,然后电子逐个加到由原子实和其余电子组成的“有效”势场中,构成了分子。并将分子中单个电子的状态函数称为分子轨道,用波函数ψ(x,y,z)来描述。每个分子轨道ψ i 都有一个确定的能值E i 与之相对应,E i 近似地等于处在这轨道上的电子的电离能 的负值,当有一个电子进占ψ i 分子轨道时,分子就获得E i 的能量。分子轨道是 按能量高低依次排列的。参与组合的原子轨道上的电子则将按能量最低原理、鲍里不相容原理和洪特规则进占分子轨道。根据电子在分子轨道上的分布情况,可以计算分子的总能量。π键实际上是持有电子的围绕参与组合的原子实的π分子
高斯投影正反算公式 新
高斯投影坐标正反算 一、相关概念 大地坐标系由大地基准面和地图投影确定,由地图投影到特定椭圆柱面后在南北两极剪开展开而成,是对地球表面的逼近,各国或地区有各自的大地基准面,我国目前主要采用的基准面为:基准面,为GPS基准面,17届国际大地测量协会上推荐,椭圆柱长半轴a=6378137m,短半轴b=; 2.西安80坐标系,1975年国际大地测量协会上推荐,椭圆柱长半轴a=6378140m,短半轴b=; 3.北京54坐标系,参照前苏联克拉索夫斯基椭球体建立,椭圆柱长半轴a=6378245m, 短半轴b=; 通常所说的高斯投影有三种,即投影后: a)角度不变(正角投影),投影后经线和纬线仍然垂直; b)长度不变; c)面积不变; 大地坐标一般采用高斯正角投影,即在地球球心放一点光源,地图投影到过与中央经线相切的椭圆柱面上而成;可分带投影,按中央经线经度值分带,有每6度一带或每3度一带两种(起始带中央经线经度为均为3度,即:6度带1带位置0-6度,3度带1带位置度),即所谓的高斯-克吕格投影。
图表11高斯投影和分带 地球某点经度(L)为过该点和地球自转轴的半圆与子午线所在半圆夹角,东半球为东经,西半球为西经;地球某点纬度(B)为所在水平面法线与赤道圆面的线面角。 正算是已知大地坐标(L,B),求解高斯平面坐标(X,Y),为确保Y值为正,Y增加500公里;反算则是由高斯平面坐标(X,Y)求解大地坐标(L,B)。 二、计算模型: 地球椭球面由椭圆绕地球自转轴旋转180度而成。 图表 1 椭圆 椭圆长半轴a,椭圆短半轴b, 椭圆方程:
(1) 图表2椭球面 椭球面方程: y2 a2+ x2 b2 + z2 a2 =1 /*************************************** 与网上充斥的将函数关系先展开为泰勒级数,再依据投影规则确定各参数不同,本文直接依据空间立体三角函数关系得出结果。 *****/ (一)正算 由图表1,
分子轨道理论汇总
第三节分子轨道理论(MOT) 一、概述 要点: A、配体原子轨道通过线性组合,构筑与中心原子轨道对称性匹配的配体群轨道。 B、中心原子轨道与配体群轨道组成分子轨道。 C、电子按照能量由低到高的顺序,依次排在分子轨道中。 形成LCAO-MO的三原则: 二、ABn型分子构筑分子轨道的方法
1、步骤 1)列出中心原子A及配位原子B中参与形成分子轨道的原子轨道; 2)将B原子轨道按等价轨道集合分类(由对称操作可彼此交换的轨道称为等价轨道); 3)将每一等价轨道集合作为表示的基,给出表示;再将其分解为不可约表示; 4)用每一组等价轨道集合构筑出对应于上一步所求出的不可约表示的配体群轨道;
5)将对称性相同的配体群轨道与中心原子轨道组合得分子轨道。 三、金属与配体间σ分子轨道(d轨道能级分裂) 1)A原子用ns、np、(n-1)d 9个轨道,每个B原子用3个p(p x、p y、p z)轨道,共27个轨道形成分子轨道。 * 坐标系选择及配体编号
x y z 1 2 3 5 4 6 p x p y p z A 、中心原子取右手坐标系,配体取左手坐标系; B 、每个B 原子上三个p 轨道各用一个向量表示,方向指向波函数正值方向; C 、规定p z 向量指向中心原子,则p x 、p y 向量应存在于垂直于p z 向量的平
面内; D、规定第一个B原子的p x向量与y 轴平行(* 方向相同),则该B原子的p y向量应与z轴平行(* 方向相同); E、其余(6-1)个B原子的p x和p y 向量的方向由O h群对称性决定。 2)O h群将B原子的18个轨道分为如下等价轨道的集合: I、6个p z轨道(可用于形成σ分子轨道) II、12个p x或p y轨道(可用于形成π分子轨道)
高斯投影坐标正反算VB程序
高斯投影坐标正反算 学院: 班级: 学号: 姓名: 课程名称: 指导老师:
实验目的: 1.了解高斯投影坐标正反算的基本思想; 2.学会编写高斯正反算程序,加深了解。 实验原理: 高斯投影正算公式中应满足的三个条件: 1. 中央子午线投影后为直线; 2. 中央子午线投影后长度不变; 3. 投影具有正形性质,即正形投影条件。 高斯投影反算公式中应满足的三个条件: 1. x坐标轴投影成中央子午线,是投影的对称轴; 2. x轴上的长度投影保持不变; 3. 正形投影条件,即高斯面上的角度投影到椭球面上后角度没 有变形,仍然相等。 操作工具: 计算机中的VB6.0 代码: Dim a As Double, b As Double, x As Double, y As Double, y_# Dim l_ As Double, b_ As Double, a0#, a2#, a4#, a6#, a8#, m2#,
m4#, m6#, m8#, m0#, l0#, e#, e1# Dim deg1 As Double, min1 As Double, sec1 As Double, deg2 As Double, min2 As Double, sec2 As Double Private Sub Command1_Click() Dim x_ As Double, t#, eta#, N#, W#, k1#, k2#, ik1%, ik2%, dh% deg1 = Val(Text1.Text) min1 = Val(Text2.Text) sec1 = Val(Text3.Text) deg2 = Val(Text4.Text) min2 = Val(Text5.Text) sec2 = Val(Text6.Text) l_ = (deg1 * 3600 + min1 * 60 + sec1) / 206265 b_ = (deg2 * 3600 + min2 * 60 + sec2) / 206265 dh = Val(Text9.Text) k1 = ((l_ * 180 / 3.14159 + 3) / 6) k2 = (l_ * 180 / 3.14159 / 3) ik1 = Round(k1, 0) ik2 = Round(k2, 0) If dh = 6 Then l0 = 6 * ik1 - 3 Else If dh = 3 Then
高斯投影坐标正算公式
高斯投影坐标正算公式 高斯投影坐标正反算公式 2.2.2. 1高斯投影坐标正算公式: B, x,y 高斯投影必须满足以下三个条件: ⑴中央子午线投影后为直线;⑵中央子午线投影后长度不变;⑶投影具有正形性质,即正形投影条件。 由第一条件知中央子午线东西两侧的投影必然对称于中央子午线,即 式中,x为的偶函数,y为的奇函数;,即, 如展开为的级数,收敛。 (2-10) 式中是待定系数,它们都是纬度B的函数。 由第三个条件知: 分别对和q求偏导数并代入上式 (2-11) 上两式两边相等,其必要充分条件是同次幂前的系数应相等,即
(2-12) (2-12)是一种递推公式,只要确定了就可依次确定其余各系数。 由第二条件知:位于中央子午线上的点,投影后的纵坐标x应等于投影前从赤道量至该点的子午线弧长X,即(2-10)式第一式中,当时有: (2-13) 顾及(对于中央子午线) 得: (2-14,15) (2-16) 依次求得并代入(2-10)式,得到高斯投影正算公式
(2-17) 2.2.2. 2高斯投影坐标反算公式 x,y B, 投影方程: (2-18) 高斯投影坐标反算公式推导要复杂些。 ⑴由x求底点纬度(垂足纬度),对应的有底点处的等量纬度,求x,y与 的关系式,仿照式有, 由于y和椭球半径相比较小(1/16.37),可将展开为y的幂级数;又由于是对称投影,q必是y的偶函数,必是y的奇函数。 (2-19) 是待定系数,它们都是x的函数. 由第三条件知: ,
, (2-20) (2-19)式分别对x和y求偏导数并代入上式 上式相等必要充分条件,是同次幂y前的系数相等, 第二条件,当y=0时,点在中央子午线上,即x=X,对应的点称为底点,其纬度为底点纬度,也就是x=X时的子午线弧长所对应的纬度,设所对应的等量纬度为。也就是在底点展开为y的幂级数。 由(2-19)1式 依次求得其它各系数 (2-21) (2-21)1 ………… 将代入(2-19)1式得
(完整word版)分子轨道理论
第三节分子轨道理论(MOT ) 、概述 要点: A、配体原子轨道通过线性组合,构 筑与中心原子轨道对称性匹配的体群轨道。 B、中心原子轨道与配体群轨道组成 分子轨道。 C、电子按照能量由低到高的顺序, 依次排在分子轨道中。 形成LCAO-MO 的三原则: 、ABn 型分子构筑分子轨道的方法
1、步骤 1)列出中心原子A 及配位原子B 中参与形成分子轨道的原子轨道; 2)将B 原子轨道按等价轨道集合分类(由对称操作可彼此交换的轨道称为等价轨道); 3)将每一等价轨道集合作为表示的基,给出表示;再将其分解为不可约表示; 4)用每一组等价轨道集合构筑出对应于上一步所求出的不可约表示的配体群轨道;
5)将对称性相同的 配体群轨道 与中 心原子轨道组合得分子轨道。 道能级分裂) 1)A 原子用 ns 、 每个 B 原子用 3 个 p (p x 、p y 、p z ) 轨道, 共 27 个轨道形成分子轨道。 * 坐标系选择及配体编号 、金属与配体间 σ 道( d 轨 np 、(n-1)d 9 个轨道,
5z 左手坐标系; B、每个B 原子上三个p 轨道各用 个向量表示,方向指向波函数正值方向; C、规定p z 向量指向中心原子,则 p x、p y 向量应存在于垂直于p z 向量的
面内; D、规定第一个B 原子的p x 向量与y 轴平行(* 方向相同),则该B 原子 的p y 向量应与z 轴平行(* 同); E、其余(6-1)个B 原子的p x 和p y 向量的方向由O h 群对称性决定。 2)O h 群将B 原子的18 个轨道分为如下等价轨道的集合: I 、 6 个p z 轨道(可用于形成σ 分子轨道) II 、12 个p x 或p y 轨道(可用于形成π 分子轨道)
高斯投影正算
高斯投影正、反算代码 //高斯投影正、反算 //////6度带宽 54年北京坐标系 //高斯投影由经纬度(Unit:DD)反算大地坐标(含带号,Unit:Metres) void GaussProjCal(double longitude, double latitude, double *X, double *Y) { int ProjNo=0; int ZoneWide; ////带宽 double longitude1,latitude1, longitude0,latitude0, X0,Y0, xval,yval; double a,f, e2,ee, NN, T,C,A, M, iPI; iPI = 0.0174532925199433; ////3.1415926535898/180.0; ZoneWide = 6; ////6度带宽 a=6378245.0; f=1.0/298.3; //54年北京坐标系参数 ////a=6378140.0; f=1/298.257; //80年西安坐标系参数 ProjNo = (int)(longitude / ZoneWide) ; longitude0 = ProjNo * ZoneWide + ZoneWide / 2; longitude0 = longitude0 * iPI ; latitude0=0; longitude1 = longitude * iPI ; //经度转换为弧度 latitude1 = latitude * iPI ; //纬度转换为弧度 e2=2*f-f*f; ee=e2*(1.0-e2); NN=a/sqrt(1.0-e2*sin(latitude1)*sin(latitude1)); T=tan(latitude1)*tan(latitude1); C=ee*cos(latitude1)*cos(latitude1); A=(longitude1-longitude0)*cos(latitude1); M=a*((1-e2/4-3*e2*e2/64-5*e2*e2*e2/256)*latitude1-(3*e2/8+3*e2*e2 /32+45*e2*e2 *e2/1024)*sin(2*latitude1)
高斯投影坐标正反算VB程序
高斯投影坐标正反算V B 程序 Jenny was compiled in January 2021
高斯投影坐标正反算 学院: 班级: 学号: 姓名: 课程名称: 指导老师:
实验目的: 1.了解高斯投影坐标正反算的基本思想; 2.学会编写高斯正反算程序,加深了解。 实验原理: 高斯投影正算公式中应满足的三个条件: 1. 中央子午线投影后为直线; 2. 中央子午线投影后长度不变; 3. 投影具有正形性质,即正形投影条件。 高斯投影反算公式中应满足的三个条件: 1. x坐标轴投影成中央子午线,是投影的对称轴; 2. x轴上的长度投影保持不变; 3. 正形投影条件,即高斯面上的角度投影到椭球面上后角度没有 变形,仍然相等。 操作工具: 计算机中的 代码: Dim a As Double, b As Double, x As Double, y As Double, y_#
Dim l_ As Double, b_ As Double, a0#, a2#, a4#, a6#, a8#, m2#, m4#, m6#, m8#, m0#, l0#, e#, e1# Dim deg1 As Double, min1 As Double, sec1 As Double, deg2 As Double, min2 As Double, sec2 As Double Private Sub Command1_Click() Dim x_ As Double, t#, eta#, N#, W#, k1#, k2#, ik1%, ik2%, dh% deg1 = Val min1 = Val sec1 = Val deg2 = Val min2 = Val sec2 = Val l_ = (deg1 * 3600 + min1 * 60 + sec1) / 206265 b_ = (deg2 * 3600 + min2 * 60 + sec2) / 206265 dh = Val k1 = ((l_ * 180 / + 3) / 6) k2 = (l_ * 180 / / 3) ik1 = Round(k1, 0) ik2 = Round(k2, 0) If dh = 6 Then l0 = 6 * ik1 - 3 Else
常见的分子轨道图
第11卷 第6期大 学 化 学1996年12月 常见的分子轨道图 李 平 赵桂兰 郭承育 (青海师范大学化学系 西宁810008) 摘要 用严格的计算机程序,绘出了常见的严格意义上的各类分子轨道图,包括Ρ、Π、?键等 的轨道图。并从周期律出发,讨论了它们与物质性质间的有趣联系。 分子轨道理论是当代化学键理论中最重要的部分,分子轨道的求解和讨论是量子化学的重要内容,分子轨道图形的绘制和解释则是理解化学键和分子的物理化学性质的重要手段。国外早有专著[1]介绍,国内也早有学者从事这方面工作[2,3]。现有的量子化学、结构化学方面的专著和教材,已注意到这方面的应用,但一般限于定性示意图,或者是平面等值图。常见的各种典型的化学键图常不一致,使教学和科研第一线的师生深感困惑。 作者利用自编的分子波函数等值面投影图绘制程序[4,5],完成了氢原子和多电子原子的原子轨道图及简单反应过程的分子轨道图的绘制[6-9],近期又在周期律指导下,系统地绘制了各类典型分子轨道图和化学键图。应当说明的是,各类分子轨道图形中,只有界面图的形状和大小是唯一的,得到多数人公认,称其为轨道图。界面是等值面中的一种,该面内电子出现几率较大,在90%以上。为了统一,我们取90±1%。 绘制分子轨道图,必须知道分子几何及分子轨道的具体形式。 一、 各种杂化原子轨道图 当由原子轨道组成分子轨道时,同一原子往往有两个以上的原子轨道参加,或者说是由杂化原子轨道参与形成化学键。常见的杂化轨道有sp、sp2、sp3、d sp2、d sp3、d2sp3等。 作者绘制了sp、sp2、sp3杂化轨道平面等值图,发现它们形状都相似,例如,图1(a)、(b)、(c)为C原子sp、sp2、sp3杂化轨道的平面等值图,它们的形状都相似,只是随着p轨道成分的增加,左边虚线部分逐渐增加,更趋向于p轨道的形状。图上数值为波函数?值,实线?为正,虚线?为负(下面各图皆如此)。图1(d)为C的sp2轨道的立体界面图(轨道图),界面上各点波函数绝对值为0155。 常见的由s、p、d轨道形成的杂化轨道有d sp2、d2sp3等。作者绘制了它们的平面等值图、空间等值图、空间界面图,发现它们的情况非常相似。举钴原子的d2sp3杂化轨道为例,选取其中一个轨道。 ?x=1 6<4s+1 2 <4p x + 1 3 <3d x2-y2 图1(e)为平面等值图,图1(f)为立体界面图,界面上?x的绝对值为01017,极大值在x方向,对应于图1(e)的曲线2。由轨道图1(f)可见,电子云分布除主要集中于x正向外,在x负方向也有相当分布,这反应了p原子轨道的特性。当?绝对值增大时,例如大于图1(e)中曲线2的
高斯投影正反算公式83
§8.3高斯投影坐标正反算公式 任何一种投影①坐标对应关系是最主要的;②如果是正形投影,除了满足正形投影的条件外(C-R 偏微分方程),还有它本身的特殊条件。 8.3.1高斯投影坐标正算公式: B,l ? x,y 高斯投影必须满足以下三个条件: ①中央子午线投影后为直线;②中央子午线投影后长度不变;③投影具有正形性质,即正形投影条件。 由第一条件知中央子午线东西两侧的投影必然对称于中央子午线,即(8-10)式中,x 为l 的偶函数,y 为l 的奇函数;0330'≤l ,即20/1/≈''''ρl ,如展开为l 的级数,收敛。 +++=++++=553316644220l m l m l m y l m l m l m m x (8-33) 式中 ,,10m m 是待定系数,它们都是纬度B 的函数。 由第三个条件知: q y l x l y q x ??-=????=??, (8-33)式分别对l 和q 求偏导数并代入上式 ----=++++++=+++553315 63424 42204 52 3164253l dq dm l dq dm l dq dm l m l m l m l dq dm l dq dm dq dm l m l m m (8-34) 上两式两边相等,其必要充分条件是同次幂l 前的系数应相等,即
dq dm m dq dm m dq dm m 231 20 13121? =? -== (8-35) (8-35)是一种递推公式,只要确定了 0m 就可依次确定其余各系数。 由第二条件知:位于中央子午线上的点,投影后的纵坐标x 应等于投影前从赤道量至该点的子午线弧长X ,即(8-33)式第一式中,当0=l 时有: 0m X x == (8-36) 顾及(对于中央子午线) B V M r M B N dq dB M dB dX cos cos 2 ==== 得: B V c B N r dq dB dB dX dq dX dq dm m cos cos 01===?===(8-37,38) B B N dq dB dB dm dq dm m cos sin 2 2121112=?-=?-= (8-39) 依次求得6543,,,m m m m 并代入(8-33)式,得到高斯投影正算公式
高斯光束
?基本定律/概念 o几何光学基本理论o概念与完善成像 o光路计算/近轴系统o球面光学成像系统?理想光学系统 o共线成像理论 o基点与基面 o物像关系 o放大率 o系统的组合 o透镜 ?平面系统 o平面镜成像 o平行平板 o反射棱镜 o折射棱镜与光楔 o光学材料 ?OS的光束限制 o照相系统和光阑 o望远镜的光束的选择o显微镜的光束限制o光学系统的景深 ?光度学/色度学 o辐射量/光学量 o传播中光学量的变化o系统像面的光照度o颜色分类/表现特征o颜色混合定律 o颜色匹配 o色度学中的几个概念o颜色相加原理 o CIE标准色度学系统o均匀颜色空间 ?光路计算/像差 o概述 o光线的光路计算 o轴上点球差 ?典型光学系统 o眼睛系统 o放大镜 o显微镜系统 o望远镜系统 o目镜 o摄影系统 o显外形尺寸计算 ?现代光学系统 o激光光学系统 o傅里叶变换光学
§8.1 激光光学系统 激光自60年代初问世以来,由于其亮度高、单色性好、方向性强等优点,在许多领域得到了广泛应用。例如激光加工、激光精密测量与定位、光学信息处理和全息术、模式识别和光计算、光通信等。但无论激光在哪方面的应用,都离不开激光束的传输,因此研究激光束在各种不同介质中的传输形式和传输规律,并设计出实用的激光光学系统,是激光技术应用的一个重要问题。 一、高斯光束的特性 在研究普通光学系统的成像时,我们都假定点光源发出的球面波在各个方向上的光强度是相同的,即光束波面上各点的振幅是相等的。而激光作为一种光源,其光束截面内的光强分布是不均匀的,即光束波面上各点的振幅是不相等的,其振幅A与光束截面半径r的函数关系为 其中A0为光束截面中心的振幅,w为一个与光束截面半径有关的参数,r为光束截面半径。光束波面的振幅A呈高斯(Guass)型函数分布所以激光光束又称为高斯光束。高斯光束的光斑延伸到无限远,其光束截面的中心处振幅最大,随着r的增大,振幅越来越小,因此我们常以r=w时的光束截面半径作为激光束的名义截面半径,并以w来表示,即当r=w时 说明高斯光束的名义截面半径w是当振幅A下降到中心振幅A0的1/e时所对应的光束截面半径。 二、高斯光束的传播 由激光谐振腔衍射理论可知,在均匀的透明介质中,高斯光束沿Z轴方向传播的光场分布为 式中, C为常数因子,,为波数,、和分别为高斯光束的截面半径、波面曲率半径和位相因子,它们是高斯光束传播中的三个重要参数. 1、高斯光束的截面半径高斯光束截面半径的表达式为
高斯投影坐标正反算公式
高斯投影坐标正反算公式 未知2010-04-03 10:47:15 本站 §高斯投影坐标正反算公式 任何一种投影①坐标对应关系是最主要的;②如果是正形投影,除了满足正形投影的条件外( C-R 偏微分方程),还有它本身的特殊条件。 1.1 高斯投影坐标正算公式: B, x,y 高斯投影必须满足以下三个条件: ①中央子午线投影后为直线;②中央子午线投影后长度不变;③投影具有正形性质,即正形投影条件。 由第一条件知中央子午线东西两侧的投影必然对称于中央子午线,即 (8-10) 式中, x 为 的偶函数, y 为的奇函数;,即,如展开为的级数,收敛。 ( 8-33 ) 式中是待定系数,它们都是纬度 B 的函数。 由第三个条件知: (8-33) 式分别对和 q 求偏导数并代入上式
(8-34) 上两式两边相等,其必要充分条件是同次幂前的系数应相等,即 (8-35) (8-35) 是一种递推公式,只要确定了就可依次确定其余各系数。 由第二条件知 : 位于中央子午线上的点,投影后的纵坐标 x 应等于投影前从赤道量至该点的子午线弧长 X ,即 (8-33) 式第一式中,当时有: (8-36) 顾及 ( 对于中央子午线 )
得: (8-37,38) (8-39) 依次求得并代入 (8-33) 式,得到高斯投影正算公式 (8-42) 1.2 高斯投影坐标反算公式 x,y B, 投影方程: (8-43)
满足以下三个条件:
①x 坐标轴投影后为中央子午线是投影的对称轴;② x 坐标轴投影后长度不变;③投影具有正形性质,即正形投影条件。 高斯投影坐标反算公式推导要复杂些。 ①由 x 求底点纬度 ( 垂足纬度 ), 对应的有底点处的等量纬度,求 x,y 与 的关系式,仿照 (8-10) 式有, 由于 y 和椭球半径相比较小 (1/16.37) ,可将展开为 y 的幂级数;又由于是对称投影, q 必是 y 的偶函数,必是 y 的奇函数。 (8-45) 是待定系数,它们都是 x 的函数 . 由第三条件知: , , (8-21)
对高斯光束传输理论的一些学习笔记
高斯光束传输理论 研究光与光纤耦合的时候,必须清楚的知道高斯光束在自由空间中是如何传输的,还有光束经过光学元件后高斯光束如何变化。 高斯光束的传输规律 激光光束具有方向性好的特点,光束的能量在空间的分布高度的集中在光的传播方向上,其光束具有一定的发散角,光束分布有着特殊的结构。由球面波构成谐振腔产生的激光束,在它的横截面上,光强是以高斯函数型分布的,称为高斯光束。高斯光束在光学设计中有着广泛的应用。 沿z 轴方向传播的基模高斯光束可以表示为如下的一般形式: ??? ???-+--=])2([exp ))(exp()(),,(222200f z arctg R r z k i z r z E z y x E ωωω (1) 其中E 0为常数因子,z f z z f f z f z f z z R R 2 2)(])(1[)(+=+=+== 20)(1)(f z z +=ωω; 222y x r +=; λ π 2= k ; λ πω20=f ; π λωf = 0;(2) ω0为基模高斯光束的腰斑半径;f 为高斯光束的共焦参数;R(z)为与传播轴相较于z 点的高斯光束等相位面的曲率半径; 由上式我们可以看出,高斯光束具有下述基本性质: (1)基模高斯光束在横截面内的场振幅分布按高斯函数)) (exp(22 z r ω-所描述的规律从中 心(即传输轴线)向外平滑地降落。由振幅降落到中心值的1/e 的点所定义的光斑半径为 2 2 020)( 1)(1)(πωλωωωz f z z +=+= 可见,光斑半径随坐标z 按照双曲线规律增大 1)(22 2 2=-f z z ωω
高斯投影坐标反算c语言代码
高斯投影坐标反算c语言代码 #include
高斯光束的能量耦合
高斯光束的能量耦合 在尾纤为单模光纤的光无源器件中,光束可用高斯近似处理,器件的耦合损耗可用高斯光束之间的耦合效率进行分析。两束高斯光束之间的能量耦合效率,取决于二者的光场叠加比率,可用下式计算。 两束高斯光束之间的耦合,可能存在三种失配模式:径向失配 X、轴向失配 Z 和角向失配θ,如图1所示。耦合失配造成光场重叠误差,从而影响耦合效率,根据(1)式计算得到耦合损耗与各种失配量之间的关系如图 2 所示,其中取光束束腰半径分别为 200um 和 5um 作对比,分别对应一般准直器和光纤的模场半径。束腰半径为 200um的高斯光束,对角向失配比较敏感,对径向失配次之,对轴向失配则有较大容差;束腰半径为 5um的高斯光束,对轴向失配比较敏感,对径向失配次之,对角向失配则有较大容差。
为了避免光器件中的反射光对通信系统造成影响,一般将光纤头的端面研磨成一定斜角以减少反射光。此端面斜角的选择依据是在保证回波损耗满足要求的情况下,尽量取小角度以减少对插入损耗的影响。光纤端面研磨成一定斜角之后,回波损耗可视为反射光束与正向传输光束之间的耦合损耗,从图 2(f)可以看到,不同波长的光其回波损耗不同,但并非如图 2(f)所示差异那么大。这是因为,在角向失配量相同情况下,波长越短则耦合损耗越大,光束束腰半径越大则耦合损耗越大,而在光纤中波长越长则模场半径越大,因此两种因素稍微抵消。 以下图光纤作分析,其 1310nm 和 1550nm 的模场直径分别为 9.2um 和10.4um,根据公式(1)计算得到两波长的回波损耗与端面角度关系如图 3 所示。当端面角度为 8 度时,1310nm和 1550nm光的回波损耗分别为 40dB和 36dB,前者约比后者大 4dB;在端面未镀增透膜情况下,只有约 4%的光反射回去,
经纬度BL换算到高斯平面直角坐标XY(高斯投影正算)的源码及.
经纬度BL换算到高斯平面直角坐标xy(高斯投影正算) private function bl2xy(byref a2 as double, byref f2 as double, byref e2 as double, _ byref s2 as double, byref t2 as double as boolean 'a2 输入中央子午线,以度.分形式输入,如115度30分则输入115.30; 起算数据l0 'f2 以度小数形式输入经度值, l 'e2 以度小数形式输入纬度值,b 's2 计算结果,横坐标y 't2 计算结果,纵坐标x '投影带号计算n=[l/6]+1 如:测得经度103.xxxx,故n=[103.x/6]+1=17+1=18 '中央经线经度l0 = n*6-3 = [l/6]*6+3 dim b2 as double 'dim g2 as double dim h2 as double dim i2 as double dim j2 as double dim k2 as double dim l2 as double dim m2 as double dim n2 as double dim o2 as double dim p2 as double dim q2 as double
dim r2 as double b2 = int(a2 + (int(a2 * 100 - int(a2 * 100 / 60 + (a2 * 10000 - int(a2 * 100 * 100 / 3600 '把l0化成度(a2 'g2 = f2 - b2 ' l -l0 'h2 = g2 / 57.2957795130823 '化作弧度 h2 = (f2 - b2 / 57.2957795130823 '将经差的单位化为弧度 i2 = tan(e2 / 57.2957795130823 'tan (b j2 = cos(e2 / 57.2957795130823 ' cos (b k2 = 0.006738525415 * j2 * j2 l2 = i2 * i2 m2 = 1 + k2 n2 = 6399698.9018 / sqr(m2 o2 = h2 * h2 * j2 * j2 p2 = i2 * j2 q2 = p2 * p2 r2 = (32005.78006 + q2 * (133.92133 + q2 * 0.7031 s2 = ((((l2 - 18 * l2 - (58 * l2 - 14 * k2 + 5 * o2 / 20 + m2 - l2 * o2 / 6 + 1 * n2 * (h2 * j2 s2 = s2 + 18500000 '在计算的基础上加上了“带号”(18)和“东移”(500km) '计算结果,横坐标y t2 = 6367558.49686 * e2 / 57.29577951308 - p2 * j2 * r2 + ((((l2 - 58 * l2 + 61 * _ o2 / 30 + (4 * k2 + 5 * m2 - l2 * o2 / 12 + 1 * n2 * i2 * o2 / 2 '计算结果,纵坐标x
讨论休克尔分子轨道法
讨论休克尔分子轨道法(HMO ) 1.基本假设和基本原理 休克尔分子轨道法的基本原理是变分法。其主要应用于π电子体系,基本假设有如下三点: 1.σ-π分离近似。 对于共轭分子,构成分子骨架的σ电子与构成共轭体系的π电子由于对称性的不同,可以近似地看成互相独立的。 ∑==π πn k k H 1?H ? πn 为π电子数 2.独立π电子近似。子中的电子由于存在相互作用,运动不是独立的,但若将其它电子对某电子的作用加以平均,近似地看成是在核和其它电子形成的固定力场上运动,则该电子的运动就与其它电子的位置无关,是独立的。 ∑='-?-=N n kn n k r 12k Z 21H ? n Z '是考虑了所有电子及其它p 电子的屏蔽之后的有效核电荷。 k k E ψψ=k H ? 由于电子的不可区分性,k 可省略,故单电子方程为 ψψE H ?= 3.LCAO-MO 近似。对于π体系,可将每个π分子轨道Ψk 看成是由各原子提供的垂直于共轭体系平面的p 原子轨道线性组合构成: ∑=i i ki C ?ψk 此外,还作出如下的假定: 1.库伦积分近似。即各碳原子的库伦积分都相同,其值为α。 ?==ατφφd H i i i i ?H ?*,
2.交换积分近似。分子中直接键连碳原子间的交换积分都相同,其值为β。而非键连碳原子间的交换积分都是零。 ???±><±==1 1H ?j ,i j i j i β 3.重叠积分近似。各原子轨道间的重叠积分都取为零。 ?? ?≠==i j i j j i 01S , 2.基本处理方法、步骤;可从中获得哪些信息 (1) 设共轭分子有n 个 C 原子组成共轭体系,每个C 原子提供一个 p 轨道 ,按 LCAO ,得: ∑=+++=i i n n c c c c ????ψ 2211 (2) 根据线性变分法,由 0E 1=??c ,0E 2=??c , 0 =??n c 可得久期方程: 0H H H H H H H H H 2122112 2222212121121211111=? ???? ? ????????????? ?????---------n nn nn n n n n n n n n c c c ES ES ES ES ES ES ES ES ES E 的一元n 次代数方程,有n 个解。 (3) 引入基本假设,即库伦积分,交换积分与重叠积分近似,化简久期行列式,求出n 个k E ,将每个k E 代入久期方程,得ki c 和i ?。 (4) 画出分子轨道i ψ相应的能级 i E 图,排布π电子;画出i ψ的图形。 从休克尔分子轨道处理的结果中,我们可以获得以下信息: 1.通过计算共轭分子的离域π键的键能,离域能来定性的说明分子的稳定性、芳香性等。 2.定量的计算出电荷密度、键级、原子成键度、自由价。并利用这些定量
