元素周期表打印版
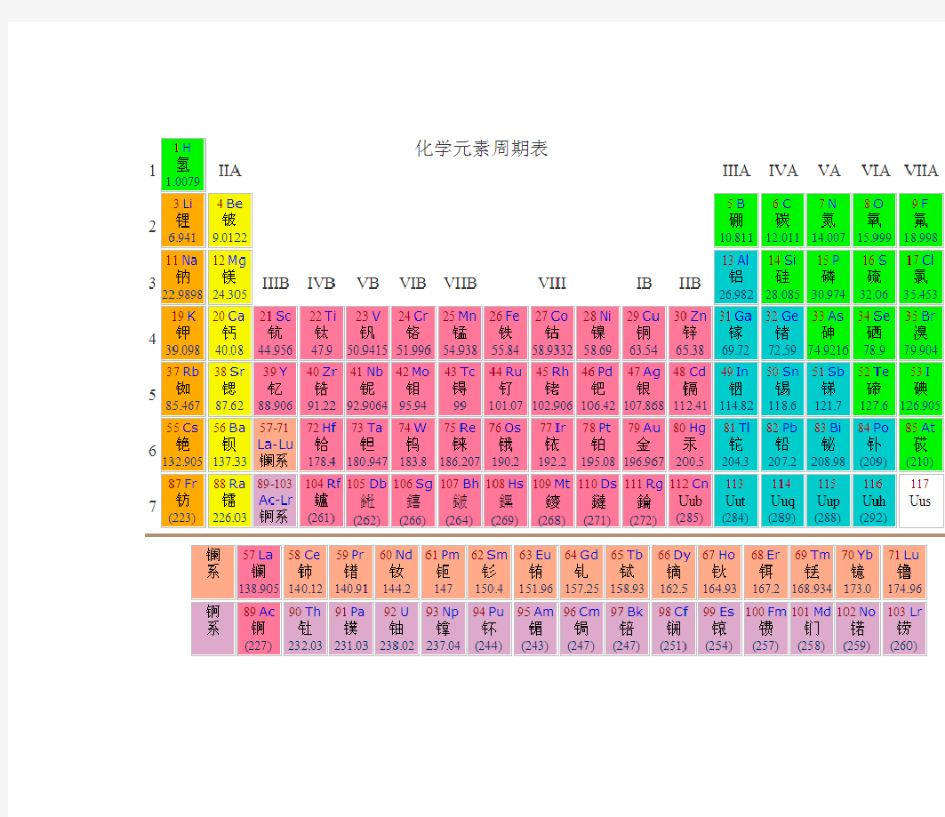
元素周期率与元素周期表
专题六元素周期率与元素周期表 【考点分析】 1.掌握元素周期率的实质,了解元素周期表(长式)的结构(周期、族)。 2.以第3周期为例,掌握同一周期内元素性质(如:原子半径、化合价、单质及化合物性质)的递变规律与原子结构的关系;以ⅠA和ⅦA族为例,掌握同一主族内元素性质递变规律与原子结构的关系。 3.以上知识是高考必考内容,常以选择题、简答题和推断填空题的形式出现。 【典型例题】 【例1】例1(2003上海理综)在人体所需的16种微量元素中有一种被称为生命元素的R 元素,对延长人类寿命起着重要的作用。已知R元素的原子有四个电子层,其最高价氧化物分子式为RO3,则R元素的名称 A.硫B.砷C.硒D.硅 【备选1】:周期表前20号元素中,某两种元素的原子序数相差1,它们形成化合物时,原子数之比为1﹕2,写出这些化合物的化学式______________ 【备选2】:X、Y、Z为短周期元素,这些元素原子的最外层电子数分别为1、4、6,则由这三种元素组成的化学式不可能是 A. XYZ B.X2YZ C.X2YZ2 D.X3YZ3 【例2】下列有关物质的性质比较正确的是 (1)同主族元素的单质从上到下,非金属性减弱,熔点增高 (2)元素的最高正化合价在数值上等于它所在的族序数 (3)同周期主族元素的原子半径越小,越难失去电子 (4)元素的非金属性越强,它的气态氢化物水溶液的酸性越强 (5)还原性:S2->Se2->Br->Cl- (6)酸性:HClO4>H2SO4>H3PO4>H2SiO3 A.(1)(3) B.(2)(4) C.(3)(6) D.(5)(6) 【备选1】下表是X、Y、Z三种元素的氢化物的某些性质: 元素熔点/℃沸点/℃与水的反应导电性(纯液体) X -283 -162 不反应不导电 Y -102 19 放热反应,形成酸性溶液不导电 Z 680 / 剧烈反应,生成H2,并形成碱性溶液导电 若X、Y、Z这三种元素属于周期表中的同一周期,则它们的原子序数递增的顺序是
化学《元素及元素周期表》优质教案、教学设计
【教学设计】第二单元第四节 元素及元素周期表(第二课时) 一、学习目标: 1. 知道元素的简单分类;元素符号所表示的意义;会正确书写元素符号并记住常见的元素符号。 2. 知道元素周期表的结构;能根据原子序数在元素周期表中找到指定元素和有关该元素的一些其它的信息。 二、学习过程: (一)、知识链接: 1、构成物质的基本粒子有、、。 如水是构成的,汞是由构成的,氯化钠是由构成的。 2、决定元素种类的是原子的数,钠原子和钠离子是否属于同种元素?。为什么?。元素:具有相同(即)的一类原子总称。 (二)、温故知新: 1、下列说法有没有错误?将错误的说法加以改正 ⑴水是由一个氧元素和两个氢元素组成的。 ⑵二氧化硫中有硫和氧两个元素。 ⑶水是由氢原子和氧原子构成的. ⑷水分子是由氢元素和氧元素组成的 ⑸一个水分子是由2 个氢原子和1 个氧原子构成的 2、填上合适的元素:
⑴地壳中含量最多的元素是: ⑵地壳中含量最多的非金属元素 ⑶地壳中含量最多的金属元素 ⑷生物细胞中含量最多的元素 3、联系生活:小华用凉开水养鱼,不久鱼全死了,下列哪个是合理的解释 A、凉开水中几乎不含氧元素 B、凉开水中几乎不含氧原子 C、凉开水中几乎不含水分子 D、凉开水中几乎不含氧气 4、5 题见课件。 (三)、自主学习与探究: 阅读课本46-47 页,完成自主学习知识点一、二。 知识点一:元素的种类 1. 稀有气体: 2. 金属元素: 3. 非金属元素:. 知识点二:元素的表示---国际通用(元素符号) 1. 为什么要使用元素符号? 2. 元素符号的读法: 3 .元素符号的书写: (1)由一个字母表示的元素: (2)由两个字母表示的元素: 4.元素符号的意义
(完整版)元素周期表练习题
【随堂练习】 1.医生建议甲状腺肿大的病人多食海带,这是由于海带中含有较丰富的( ) A .钾元素 B .铁元素 C .碘元素 D .锌元素 2.随着卤素原子半径的增大,下列递变规律正确的是----------------------------------------------( ) A .单质的熔、沸点逐渐降低 B .卤素离子的还原性逐渐增强 C .单质的氧性逐渐增强 D .气态氢化物的稳定性逐渐增强 3.砹(At )原子序数85,与F 、Cl 、Br 、I 同族,推测砹或砹的化合物不可能具有的性质是( ) A .砹是有色固体 B .非金属性:At <I C .HAt 非常稳定 D .I 2 可以从At 的可溶性的盐溶液置换出来。 4.元素X 的原子有3个电子层,最外层有4个电子。这种元素位于周期表的 -----------------( ) A.第4周期ⅢA 族 B.第4周期ⅦA 族 C.第3周期ⅣB 族 D.第3周期ⅣA 族 5.A 、B 两元素可形成AB 型离子化合物,如果A 、B 两种离子的核外电子数之和为20,则A 、B 两元素所处的 周期为-------------------------------------------------------------------------------( ) A.在同一周期 B.一种在第一周期,一种在第二周期 C.一种在第二周期,一种在第三周期 D.一种在第三周期,一种在第四周期 6.某元素原子的最外电子层上只有2个电子,该元素是 -----------------------------------------( ) A.一定是IIA 元素 B.一定是金属元素 C.一定是正二价元素 D.可能是金属元素,也可能是非金属元素 7.国际无机化学命名委员会在1989年做出决定,把长式元素周期表原先的主副族及族号取消,由左至右改为18列。如碱金属为第1列,稀有气体元素为第18列。按此规定,下列说法中错误的是() A .第9列元素中没有非金属元素 B .第17列为卤族元素 C .只有第2列元素原子的最外层有2个电子 D .在整个18列元素中,第3列元素种类最多 8.下列叙述正确的是------------------------------------------------------------------------------------( ) A. 卤素离子(X -)只有还原性而无氧化性 B. 某元素由化合态变成游离态,该元素一定被氧化 C. 失电子难的原子获得电子的能力一定强 D. 负一价卤素离子的还原性在同一族中从上至下逐渐减弱 9.下列叙述中,不正确的是----------------------------------------------------------------------------( ) A .工业上HCl 由H 2和Cl 2在点燃的条件下制得 B .氢氟酸比盐酸的酸性强 C .碘难溶于水,易溶于有机溶剂 D .碘单质能使湿润的碘化钾淀粉试纸变蓝 10.足量的氯气或盐酸分别跟下列金属反应,均有MCl 2型化合物生成的是-----------------( ) A.Al B.Mg C.Fe D.Na 11.以下各组表示卤素及其化合物的性质变化规律中,错误的是 -------------------------( ) A .得电子能力 F 2>Cl 2>Br 2>I 2 B .还原能力 F -
元素周期表中各元素名称及性质
— / [ *
、
…
氢(H) [ 主要性质和用途 熔点为℃,沸点为℃,密度为0. 089 88 g/L(10 ℃)。无色无臭气体,不溶于水,能在空气中燃烧,与空气形成爆炸混合物。工业上用于制造氨、环已烷、甲醇等。 发现 1766年由卡文迪许()在英国判明。 氦(He) ; 主要性质和用途 熔点为℃(加压),沸点为-℃,密度为 5 g/L(0 ℃)。无色无臭气体。化学性质不活泼。用于深海潜水、气象气球和低温研究仪器。 发现 1895年由拉姆塞(Sir )在英国、克利夫等(和在瑞典各自独立分离出。 锂(Li)
。 主要性质和用途 熔点为℃,沸点为1 347 ℃,密度为g/cm3(20 ℃)。软的银白色金属,跟氧气和水缓慢反应。用于合金、润滑油、电池、玻璃、医药和核弹。发现 1817年由阿尔费德森(. Arfvedson)在瑞典发现。 铍(Be) 主要性质和用途 ~ 熔点为1 278±5 ℃,沸点为2 970 ℃(加压下),密度为g/cm3(20 ℃)。较软的银白色金属,在空气和水中稳定,即使在红热时也不反应。用于与铜和镍制合金,其导电性和导热性极好。 发现 1798年由沃克兰()发现 硼(B) 主要性质和用途 * 熔点为2 300 ℃,沸点为3 658 ℃,密度为g/cm3(β-菱形)(20 ℃)。具有几种同素异形体,无定形的硼为暗色粉末,跟氧气、水、酸和碱都不起反应,跟大多数金属形成金属硼化物。用于制硼硅酸盐玻璃、漂白和防火。 发现 1808年由戴维(Sir Humphrey Davy)在英国、盖-吕萨克()和泰纳)在法国发现。 碳(C)
元素及元素周期表练习题
元素及元素周期表 一.选择题: 1.地壳中含量最多的金属元素是 ( ) A .氧 B .硅 C .铝 D .铁 2.决定元素种类的是 ( ) A .质子数 B .电子数 C .中子数 D .核外电子数 3.下列化学符号中数字表示的意义正确的是 ( ) A .CO 2:“2”表示一个二氧化碳分子含有两个氧原子 B .2Na :“2”表示两个钠元素 C . :“+2”表示镁离子带有两个单位正电荷 D .S 2- :“2–”表示硫元素的化合价为负二价 4.某粒子的结构示意图如图所示,对该粒子的说法错误的是( ) A .核电荷数为12 B .核外有3个电子层 C .带12个单位正电荷 D .在化学反应中,易失去最外层上的2个电子 5.根据右图提供的信息,下列说法正确的是( ) A .钠原子最外层有11个电子 B .钠的相对原子质量是22.99g C .钠属于非金属元素 D .钠的原子序数为11 6.生活中常接触到“加碘食盐”、“高钙牛奶”,其中的“碘”和“”应理解为( ) A.单质 B.分子 C.元素 D.原子 7.最近,“镉大米”成为公众关注的热点问题之一。据了解,含镉的大米对人的肝肾损害比较大。镉(Cd)的原子序数为48,中子数为64,下列说法错误的是( ) A 、镉原子的质子数为48 B 、镉原子的相对原子质量为112g C 、镉是金属元素 D 、镉原子的核外电子数为48 8.正确读写化学符号是学好化学的基础。铝元素符号书写正确的是( ) A.AL B.al C.aL D.Al 9.硒被誉为“抗癌大王”。根据右图提供的硒的有关信息,下列说法中,正确的是 ( ) A .硒属于金属元素 B .硒的原子序数是34 C .硒的原子结构示意图中x=4 D .硒的相对原子质量是78.96 g Mg +2
中考化学考点全解考点九元素符及元素周期表
中考化学考点全解考点九元素符及元素周期表 文档编制序号:[KK8UY-LL9IO69-TTO6M3-MTOL89-FTT688]
元素符号及元素周期表元素符号的写法: ①由一个字母表示的元素符号要大写,如 :H、C、 S、P,K。 ②由两个字母表示的元素符号,第一个字母要大写,第二个字母要小写(即“一大二小”)。如:Na、Mg、 Ca、Zn、Si。 元素周期表的结构: ①每一横行(周期):元素周期表每一横行叫做一个周期.共有7个横行,即7个周期。每个周期开头是金属元素(第一周期除外),靠近尾部是非金属元素,结尾的是稀有气体元素。同一周期元素的原子具有相同的电子层数。 ②每一纵行(族):元素周期表共有18个纵行,每一个纵行叫做一个族(第8,9,10三个纵行共同组成一个族),共有16个族。 ③每一格:在元素周期表中,每一种元素均占据一格。对于每一格,均包含元素的原子序数、元素符号、元素名称、相对原了质量等内容,如下图所示: 元素符号和化学式的关系: 化学用语元素符号化学式 易错考点
例题解析 例题1:近阶段多家媒体报道:云南铬污染和问题胶囊铬超标影响甚广.有关铬元素在元素周期表中的位置如图所示.从图中获取的信息正确的是()A.该元素为非金属元素 B.该元素在地壳中的含量为52.00% C.该元素的原子序数为52
D.该元素的原子核外有24个电子 答案:D 解析:A、根据化学元素汉字名称的偏旁可辨别元素的种类,金属元素名称一般有“金”字旁;因此该元素属于金属元素,故A正确; B、根据元素周期表中的信息,52.00是该元素的相对原子质量,而不是该元素在地壳中含量.故B错误; C、根据元素周期表中的信息可知,该元素原子的原子序数为24,故C错误; D、根据元素周期表中的信息可知,铬元素的原子序数=质子数=核外电子数,铬元素的原子核外有24个电子,故D正确. 例题2:下列符号中,既能表示一种元素,又能表示该元素的一个原子,还能表示由该元素组成的单质的是() A、H 2 B.N C.Fe D.CO 2 答案:C 解析:由原子构成的物质,元素既能表示一种元素,又能表示该元素的一个原子,还能表示由该元素组成的单质 课后练习 1、如图为元素周期表的一部分.下列说法不正确的是() A.钠、镁、铝三种原子的电子层都有3个层 B.氢、锂、钠三种原子的最外层都有1个电子
高中化学元素周期表和元素题型归纳
元素周期律和元素周期表习题 知识网络 中子N 原子核 质子Z 原子结构 : 电子数(Z 个)核外电子 排布规律 → 电子层数 周期序数及原子半径 表示方法 → 原子(离子)的电子式、原子结构示意图 随着原子序数(核电荷数)的递增:元素的性质呈现周期性变化 ①、原子最外层电子的周期性变化(元素周期律的本质) 元素周期律 ②、原子半径的周期性变化 ③、元素主要化合价的周期性变化 ④、元素的金属性与非金属性的周期性变化 ①、按原子序数递增的顺序从左到右排列; 元素周期律和 排列原则 ②、将电子层数相同的元素排成一个横行; 元素周期表 ③、把最外层电子数相同的元素(个别除外)排成一个纵行。 ①、短周期(一、二、三周期) 周期(7个横行) ②、长周期(四、五、六周期) 周期表结构 ①、主族(ⅠA ~ⅦA 共7个) 族(18个纵行) ②、副族(ⅠB ~ⅦB 共7个) ③、Ⅷ族(8、9、10纵行) ④、零族(稀有气体) 同周期同主族元素性质的递变规律 ①、核外电子排布 ②、原子半径 性质递变 ③、主要化合价 ④、金属性与非金属性 ⑤、气态氢化物的稳定性 ⑥、最高价氧化物的水化物酸碱性 电子层数 相同条件下,电子层越多,半径越大。 判断的依据 核电荷数 相同条件下,核电荷数越多,半径越小。 最外层电子数 相同条件下,最外层电子数越多,半径越大。 微粒半径的比较 1、同周期元素的原子半径随核电荷数的增大而减小(稀有气体除外) 如:Na>Mg>Al>Si>P>S>Cl. 2、同主族元素的原子半径随核电荷数的增大而增大。如:Li
物质结构及元素周期表
物质结构及元素周期表 为您服务的教育网络 主题一材料结构和元素周期表 一、审查考试地点 1.考试网站网络建设 (1)元素“位-结构-单位”之间的关系 (2)。推断元素的名称或位置是本节中常见的问题之一。其方法可以大致概括如下: 2.检查现场解释: 测试地点1:同一时期、同一主体群体性质变化的逻辑衍生关系1。相同周期和相同主族元素性质变化规律性质原子半径电子层结构电子损失能力获得电子能力金属非金属主价最高价氧化物酸相应水合物碱性非金属气态氢化物形成困难稳定性相同周期(从左到右)具有相同数量电子层的最外层电子的数量逐渐减少,最外层电子的数量逐渐减少,最外层电子的数量逐渐增加,最外层电子的数量逐渐减少,最外层电子的数量逐渐减少,最外层电子的数量逐渐增加,最外层电子的数量逐渐增加,最大正价(+1→+7)非金属负价=-(8族序数)酸度逐渐增加,最外层电子的数量XK碱度 随着主族(自上而下)电子层数的逐渐增加,最外层电子的数量也在逐渐增加,逐渐减少,逐渐增加,逐渐减少,逐渐减少,逐渐减少,最高正价=族序数(除O,F外)非金属负价=-(8-族序数)酸度逐渐减少,碱度逐渐增加,形成从难到易的稳定性逐渐增加,形成从易到难的稳
定性逐渐减少2。元素周期表中的“三角形”变化规律 如果元素a、b和c位于元素周期表中图5-1所示的位置,所有相关的性质都可以顺利释放。 1 为您服务的教育网络 订单(但D不能参与安排)。(1)原子半径:碳>氮>硼;(2)金属度:碳>碳>硼;(3)非金属:硼>碳>碳3。元素周期表(1)中的相似性规则与主族元素的性质相似(因为最外面的电子是相同的);⑵元素周期表中对角线位置(如2中的A、D位置)的元素具有相似的性质,如锂和镁、铍和铝、硼和硅等。 (3)相邻元素的性质差别不大。 测试点2元素周期定律的普通次定律 1.最外层电子数大于或等于3且小于8的元素必须是主族元素;最外层电子数为1或2的元素可以是主族、次族或0族(he)元素;最外层电子数为8的元素是稀有气体元素(氦除外)。 2.在元素周期表中,IIA族和IIA族元素的原子数有三种不同:①1-3周期(短周期)1元素的原子数不同;(2)第4和第5周期之间的差异为11;③第6和第7周期的差异为25。 3.在每个周期中排列的元素类型满足以下规则:如果n是周期序数,那么在奇数周期中它是(n?1)222(n?2)物种,物种处于偶数周期。2 4.在元素周期表中,除了第八族元素外,具有奇数(或偶数)原子序数的元素,元素所在的族的序数和主价也是奇数(或偶数)。
元素周期律和元素周期表知识总结
元素周期律和元素周期表知识总结 考试大纲要求 1.理解原子的组成及同位素的概念。掌握原子序数、核电荷数、质子数、中子数、核外电子数,以及质量数与质子数、中子数之间的相互关系。 2.以第1、2、3周期的元素为例,掌握核外电子排布规律。 3.掌握元素周期律的实质及元素周期表(长式)的结构(周期、族)。 4.以第3周期为例,掌握同一周期内元素性质(如:原子半径、化合价、单质及化合物性质)的递变规律与原子结构的关系;以ⅠA族和ⅦA族为例,掌握同一主族内元素性质递变规律与原子结构的关系。 知识规律总结 一、原子结构 1.几个量的关系() 质量数(A)=质子数(Z)+中子数(N) 质子数=核电荷数=原子序数=原子的核外电子数 离子电荷数=质子数-核外电子数 2.同位素 (1)要点:同——质子数相同,异——中子数不同,微粒——原子。 (2)特点:同位素的化学性质几乎完全相同;自然界中稳定同位素的原子个数百分数不变。 注意:同种元素的同位素可组成不同的单质或化合物,如H2O和D2O是两种不同的物质。 3.相对原子质量 (1)原子的相对原子质量:以一个12C原子质量的1/12作为标准,其它原子的质量跟它相比较所得的数值。它是相对质量,单位为1,可忽略不写。 (2)元素的相对原子质量:是按该元素的各种同位素的原子百分比与其相对原子质量的乘积所得的平均值。元素周期表中的相对原子质量就是指元素的相对原子质量。 4.核外电子排布规律 (1)核外电子是由里向外,分层排布的。 (2)各电子层最多容纳的电子数为2n2个;最外层电子数不得超过8个,次外层电子数不得超过18个,倒数第三层电子数不得超过32个。 (3)以上几点互相联系。 核外电子排布规律是书写结构示意图的主要依据。 5.原子和离子结构示意图 注意:①要熟练地书写1~20号元素的原子和离子结构示意图。 ②要正确区分原子结构示意图和离子结构示意图(通过比较核内质子数和核外电子数)。 6.微粒半径大小比较规律 (1)同周期元素(稀有气体除外)的原子半径随原子核电荷数的递增逐渐减小。 (2)同主族元素的原子半径和离子半径随着原子核电荷数的递增逐渐增大。 (3)电子层结构相同的离子,核电荷数越大,则离子半径越小。 (4)同种元素的微粒半径:阳离子<原子<阴离子。 (5)稀有气体元素的原子半径大于同周期元素原子半径。 (6)电子层数多的阴离子半径一定大于电子层数少的阳离子半径,但电子层数多的阳离子半径不一定大于电子层数少的阴离子半径。 二、元素周期律和周期表 1.位、构、性三者关系
顺序版元素周期表之歌歌词(中英文带音标)
The New Periodic Table Song 新元素周期表之歌 And now Asap SCIENCE presents: 现在,由ASAP科学推出的:The Elements of the Periodic Table. 元素周期表之歌 There is Hydrogen and Helium. 首先是氢和氦, 1 H 氢H ydrogen ['haidrid??n]美音:['ha?dr?d??n] 2 He 氦H elium ['hi:li?m]美音:['hil??m] Then Lithium, Beryllium. 然后是锂,铍, 3 Li 锂Lithium ['liθi?m]美音:['l?θ??m] 4 Be 铍Beryllium [be'rili?m]美音:[b?'r?l??m] Boron, Carbon everywhere. 硼,碳无处不在, 5 B 硼Boron ['b?:r?n]美音:['borɑn] 6 C 碳Carbon Nitrogen all through the air. 氮遍布于空气中, 7 N 氮N itrogen ['naitr?d??n]美音:['na?tr?d??n] With Oxygen so you can breath. 有氧你就能呼吸。 8 O 氧Oxygen ['?ksid??n]美音:['ɑks?d??n] And Fluorine for your pretty teeth. 并且氟效劳于你漂亮的牙齿, 9 F 氟 Fluorine ['flu?ri:n]美音:['flu?,r?n] Neon to light up the signs, 氖点亮霓虹灯。
元素和元素周期表参考答案
第三章元素和元素周期表 第一节元素的排列 阅读指南 1.元素周期表是如何发展起来的? 为每个元素制作包括熔点、密度和颜色,以及原子量和成键能力的卡片→将元素按照原子量递增顺序排列,元素呈现出了某种规律性→按照成键能力将元素分组→最早的元素周期表出现→按原子序数重新排序(现在的元素周期表) 2.元素周期表给了我们什么信息? 周期表中的每个方格内都含有某种元素的相关信息,这些信息一般包括该元素的原子序数、元素符号、元素名称以及相对原子质量。 元素周期表是由族和周期组成的,整个周期表共有18个族和7个周期。 元素的性质可以通过其在周期表中所处的位置进行预测。 3.元素的价电子与元素在周期表中的位置存在什么样的关系? 同一周期中的元素,它们的原子的价电子数从左至右是逐渐增加的。同族元素的原子具有相同的价电子数和相同的价电子排列。 技能训练 4.分类:铜暴露在空气中会慢慢失去光泽,变得暗淡。失去光泽而变色的过程属于物理变化还是化学变化? 在潮湿的含氧环境中,铜被腐蚀的主要反应就是生成碱式碳酸铜,反应过程中还有氧气参与了,2Cu +O2 +H2O +CO2 =Cu(OH)2*CuCO3 一般来说铜器如果暴露在潮湿空气中,都会生成铜绿而逐渐被腐蚀。该过程有新的物质生成,属于化学变化。 5.应用概念:氦、铍、氖的原子核内都含有质子和中子,但它们却属于完全不同的元素。为什么说它们属于不同的元素? 属于同一元素的所有原子,它们所含的质子数是完全相同的。元素原子核内的质子数定义为元素的原子序数,是识别该元素特有的性质。氦有2个,铍有4个,氖有10个,因而它们属于不同的元素。6.推论:在镍-镉电池中,可以找到什么金属? 镍和镉 7.对比:元素A与元素B是同族元素,它们与元素C属于同周期元素,上述三种元素中,哪两个元素可能具有相似的性质?说明原因。 元素A和B是同族元素,同族元素具有类似的特性。 想一想 8.周期的含义是什么? 指具有相同的电子层数并按照原子序数递增的顺序排列的一系列元素。周期表中共有七个横行,也就是七个周期。第一、二、三周期称短周期;第四、五、六周期称长周期;第七周期尚未填满,称不完全周期。一般每周期以活泼金属元素开始,逐步过渡到活泼非金属元素,最后以稀有气体元素结尾。 9.周期表中的“列”称为什么?。 族,在元素周期表中,同族的元素具有相同的价电子数和相同的价电子排列。 我的困惑和疑问 第二节金属元素 阅读指南 1.金属有哪些性质? 金属的物理性质:硬度、光泽、延展性,大多数金属都是热和电的良好导体。金属的化学活性也不尽相同。 2.你如何区分日常用的各类金属制品? 过渡金属比较稳定,与空气和水反应缓慢或者根本不能反应,所以这些金属常用来制作日常生活中的器皿。还可将两种或两种以上的而金属相互混合,生成的合金,则具有组成该合金的各金属的优良性质,如青铜(铜锡混合)、黄铜(铜锌混合),不锈钢(铁、碳、铬、钒等混合)等。
高中化学元素周期表和元素题型归纳
元素周期律和元素周期表习题 知识网络 中子N 原子核 质子Z 原子结构 : 电子数(Z 个)核外电子 排布规律 → 电子层数 周期序数及原子半径 表示方法 → 原子(离子)的电子式、原子结构示意图 随着原子序数(核电荷数)的递增:元素的性质呈现周期性变化 ①、原子最外层电子的周期性变化(元素周期律的本质) 元素周期律 ②、原子半径的周期性变化 ③、元素主要化合价的周期性变化 ④、元素的金属性与非金属性的周期性变化 ①、按原子序数递增的顺序从左到右排列; 元素周期律和 排列原则 ②、将电子层数相同的元素排成一个横行; 元素周期表 ③、把最外层电子数相同的元素(个别除外)排成一个纵行。 ①、短周期(一、二、三周期) 周期(7个横行) ②、长周期(四、五、六周期) 周期表结构 ③、不完全周期(第七周期) ①、主族(ⅠA ~ⅦA 共7个) 族(18个纵行) ②、副族(ⅠB ~ⅦB 共7个) ③、Ⅷ族(8、9、10纵行) ④、零族(稀有气体) 同周期同主族元素性质的递变规律 ①、核外电子排布 ②、原子半径 性质递变 ③、主要化合价 ④、金属性与非金属性 ⑤、气态氢化物的稳定性 ⑥、最高价氧化物的水化物酸碱性 电子层数 相同条件下,电子层越多,半径越大。 判断的依据 核电荷数 相同条件下,核电荷数越多,半径越小。 最外层电子数 相同条件下,最外层电子数越多,半径越大。 微粒半径的比较 1、同周期元素的原子半径随核电荷数的增大而减小(稀有气体除外) 如:Na>Mg>Al>Si>P>S>Cl. 2、同主族元素的原子半径随核电荷数的增大而增大。如:Li
元素周期表及各元素英文
元素周期表及各元素英文 第01 号元素: 氢[化学符号]H, 读“轻”, [英文名称]Hydrogen 第02 号元素: 氦[化学符号]He, 读“亥”, [英文名称]Helium 第03 号元素: 锂[化学符号]Li, 读“里”, [英文名称]Lithium 第04 号元素: 铍[化学符号]Be, 读“皮”, [英文名称]Beryllium 第05 号元素: 硼[化学符号]B, 读“朋”, [英文名称]Boron 第06 号元素: 碳[化学符号]C, 读“炭”, [英文名称]Carbon 第07 号元素: 氮[化学符号]N, 读“淡”, [英文名称]Nitrogen 第08 号元素: 氧[化学符号]O, 读“养”, [英文名称]Oxygen 第09 号元素: 氟[化学符号]F, 读“弗”, [英文名称]Fluorine 第10 号元素: 氖[化学符号]Ne, 读“乃”, [英文名称]Neon 第11 号元素: 钠[化学符号]Na, 读“纳”, [英文名称]Sodium 第12 号元素: 镁[化学符号]Mg, 读“美”, [英文名称]Magnesium
第13 号元素: 铝[化学符号]Al, 读“吕”, [英文名称]Aluminum 第14 号元素: 硅[化学符号]Si, 读“归”, [英文名称]Silicon 第15 号元素: 磷[化学符号]P, 读“邻”, [英文名称]Phosphorus 第16 号元素: 硫[化学符号]S, 读“流”, [英文名称]Sulfur 第17 号元素: 氯[化学符号]Cl, 读“绿”, [英文名称]Chlorine 第18 号元素: 氩[化学符号]Ar,A, 读“亚”, [英文名称]Argon 第19 号元素: 钾[化学符号]K, 读“甲”, [英文名称]Potassium 第20 号元素: 钙[化学符号]Ca, 读“丐”, [英文名称]Calcium 第21 号元素: 钪[化学符号]Sc, 读“亢”, [英文名称]Scandium 第22 号元素: 钛[化学符号]Ti, 读“太”, [英文名称]Titanium 第23 号元素: 钒[化学符号]V, 读“凡”, [英文名称]Vanadium 第24 号元素: 铬[化学符号]Cr, 读“各”, [英文名称]Chromium 第25 号元素: 锰[化学符号]Mn, 读“猛”, [英文名称]Manganese
元素周期表与元素周期律最全版
原子结构与元素性质的周期性 [考试目标] (1)掌握元素周期律的实质,了解元素周期表(长式)的结构(周期、族)及其应用。 (2)以第3周期为例,掌握同一周期内元素性质的递变规律与原子结构的关系。 (3)以ⅠA和ⅦA族为例,掌握同一主族内元素性质的递变规律与原子结构的关系。 (4)了解金属、非金属在元素周期表中的位置及其性质递变的规律。 (5)了解元素电离能的含义,并能用以说明元素的某些性质。(选考内容) [要点精析] 元素的性质随着原子序数的递增呈现周期性的变化规律,这个规律叫做元素周期律一、电子排布的周期性: 周期、族与电子层构型 — S区元素价电子特征排布为nS1~2 价电子数=主族序数 p区元素特征电子排布为ns2np1~6 d区元素价电子排布特征为(n-1)d1~10ns1~2;最高能级组中的电子总数=族数 ds区元素特征电子排布为(n-1)d10ns1~2;最外层电子数=族数 二、元素性质的周期性
电子层数:相同条件下,电子层越多,半径越大。 判断的依据核电荷数:相同条件下,核电荷数越多,半径越小。 最外层电子数:相同条件下,最外层电子数越多,半径越大。 1、同周期元素的原子半径随核电荷数的增大而减小(稀有气体除外) 如:Na>Mg>Al>Si>P>S>Cl. 2、同主族元素的原子半径随核电荷数的增大而增大。如:Li
英文版元素周期表之歌【歌词】
There’s Hydrogen and Helium Then Lithium, Beryllium Boron, Carbon everywhere Nitrogen all through the air With Oxygen so you can breathe And Fluorine for your pretty teeth Neon to light up the signs Sodium for salty times Magnesium, Aluminium, Silicon Phosphorus, then Sulfur, Chlorine and Argon Potassium, and Calcium so you’ll grow strong Scandium, Titanium, Vanadium and Chromium and Manganese This is the Periodic T able Noble gas is stable Halogens and Alkali react agressively Each period we’ll see new outer shells While electrons are added moving to the right Iron is the 26th
Then Cobalt, Nickel coins you get Copper, Zinc and Gallium Germanium and Arsenic Selenium and Bromine film While Krypton helps light up your room Rubidium and Strontium then Yttrium, Zirconium Niobium, Molybdenum, Technetium Ruthenium, Rhodium, Palladium Silver-ware then Cadmium and Indium Tin-cans, Antimony then Tellurium and Iodine and Xenon and then Caesium and... Barium is 56 and this is where the table splits Where Lanthanides have just begun Lanthanum, Cerium and Praseodymium Neodymium’s next too Promethium, then 62’s Samarium, Europium, Gadolinium and Terbium Dysprosium, Holmium, Erbium, Thulium Ytterbium, Lutetium
高中化学 元素周期表及其应用
元素周期表及其应用 知识与技术 1、知道元素周期表是元素周期律的具体表现形式,能描述元素周期表的结构,初步学会 运用元素周期表。 2、知道同周期、同主族元素性质的递变规律。 3、理解元素在周期表中的位置与它的原子结构、元素化学性质三者之间关系。 过程与方法 1、运用直接观察法学习元素周期表的结构。 2、运用逻辑推理方法研究学习同主族元素性质的递变规律。 3、采用研究性学习学方式学习有关周期表的史料。 情感、态度与价值观 1、了解周期表的编制过程,了解科学发现和发展的历程。 2、认识周期表的理论对实践的指导作用。 教学重点 元素周期表的结构及其应用 教学难点 元素在周期表中的位置与原子结构、元素化学性质三者之间的关系。 教具准备 多媒体, 元素周期表及其应用(第一课时) 导入新课: 我们已经学习过了元素周期律的有关内容,现在请大家来完成一个任务:将1—18号元素排列在一张表格中,这张表格必须体现出周期律内容。 学生活动,交流: 评价: 展示:元素周期表 投影: [问题与探究] 1、元素周期表有几行几列? 2、什么叫周期?什么叫族? 3、有几种不同的族?族是如何排列的? 4、如何确定周期和主族序数? 学生交流、讨论: 板书:一、元素周期表结构 1周期 短周期:第1、2、3行分别有2、8、8种元素 长周期:第4、5、6行分别有18、18、32种元素 不完全周期:第7行有26种元素 2族 主族:(A)有7个 副族:(B)有7个 Ⅷ族:1个有3纵横 0族:1个 提问:请写出氮、铝、氖元素周期中的位置?
学生活动: 提问:通过以上练习你能看出这些元素原子的核外电子数,最外层电子数,主要化合价与周期数及族的序数是什么关系? 学生思考、交流: 板书:周期序数=电子层数 主族序数=最外层电子数 投影:指出下列主族元素在周期表中的位置,并推测其主要化合价 学生回答: 投影:锂、钠、钾、铷、铯的性质具有哪些相似性? 学生活动 演示实验:钾与水反应 学生观察: 视频:锂、钠、钾、铷、铯与水反应 结论:性质相似,但金属性逐渐增强。 投影:氟、氯、溴、碘元素 讲述:(性质的递变) [练习] 依据碳、氮元素在周期表中的位置,在下列空格中填上必要的内容。 [板书] (1)、核电荷数:碳氮 (2)、原子半径:碳氮 (3)、非金属性:碳氮 (4)、氧化性:碳氮气 (5)、热稳定性:甲烷氨气 (6)、酸性:碳酸硝酸 [结论] 同周期元素由左向右,随着核电荷递增,最外层电子逐渐增多,原子半径逐渐减小,原子得电子能力逐渐增强,失电子能力逐渐减弱;金属性逐渐减弱,非金属性逐渐增强。[思考与探究] 根据氟、氯、溴、碘在周期表中的位置及原子结构,对下列事实给出合理解释 (1)、它们的单质与氢气反应越来越难。 (2)、它们的单质与水反应越来越难。 (3)、氯、溴、碘的置换顺序为:氯>溴>碘。 (4)、它们气态氢化物的热稳定性顺序为:氟>氯>溴>碘。 (5)、它们最高价氧化物的水化物的酸性强弱顺序为:氯>溴>碘。 [结论]
化学元素周期表中文及英文读音
PET) ['haidr?ud??n] ?m, -li?m] m] ?m,b?'r-] ?:r?n] ɑ:b?n] ?d??n] ?ksid??n] ?ri:n] ?n] ?udj?m, -di?m] [m?g'ni:zj?m] ?m] ?n] ?sf(?)r?s] ?lf?] ?:ri:n] ɑ:g?n] ?'t?sj?m] ['k?lsi?m] [s'k?ndi?m] ?m, ti-] ?'neidi?m, -dj?m] ?umj?m] ?g?'ni:z] ?n] ?'b?:lt, 'k?ub?:lt] ?p?]
?k] ['g?li?m] ??:'meini?m] ɑ:s?nik] ?m, -nj?m] ?umi:n] ?n] ?m] ?n t i?m] ?tr??m] ?:'k?uni?m] ?ubi?m] ?'libdin?m] ?i?m] θi:ni?m] ?udi?m, -dj?m] ?'leidi?m] ?] ['k?dmi?m] ?m] ?m] ??ri?m] ?di:n; (US) 'ai?dain] ?n] ?m] ??ri?m] ['l?nθ?n?m] ?ri?m] ?u'dimi?m]
?'dimi?m] ?'mi:θi?m] ?'m??ri?m] ?'r?upi?m] ?'lini?m] ?:bi?m] ?usi?m] ?lmi?m] ?:bi?m] θju:li?m] ?:bi?m] ?i?m, -si?m] ?m] ['t?nt?l?m] ??st?n] ?m] ?zmi?m, -mj?m] ?m] ?m] ?uld] ?:kjuri] θ?li?m] ?θ] ?'l?uni?m] ?ti:n] 第86 号元素: 氡 Rn, 读“冬”, [英文名称]Radon ['reid?n] ['fr?nsi?m] ?m] ?m]
元素周期表及各元素英文
元素周期表及各元素英文 精品
第 01 号元素: 氢 [化学符号]H, 读“轻”, [英文名称]Hydrogen 第 02 号元素: 氦 [化学符号]He, 读“亥”, [英文名称]Helium 第 03 号元素: 锂 [化学符号]Li, 读“里”, [英文名称]Lithium 第 04 号元素: 铍 [化学符号]Be, 读“皮”, [英文名称]Beryllium 第 05 号元素: 硼 [化学符号]B, 读“朋”, [英文名称]Boron 第 06 号元素: 碳 [化学符号]C, 读“炭”, [英文名称]Carbon 第 07 号元素: 氮 [化学符号]N, 读“淡”, [英文名称]Nitrogen 第 08 号元素: 氧 [化学符号]O, 读“养”, [英文名称]Oxygen 第 09 号元素: 氟 [化学符号]F, 读“弗”, [英文名称]Fluorine 第 10 号元素: 氖 [化学符号]Ne, 读“乃”, [英文名称]Neon 第 11 号元素: 钠 [化学符号]Na, 读“纳”, [英文名称]Sodium 第 12 号元素: 镁 [化学符号]Mg, 读“美”, [英文名称]Magnesium 第 13 号元素: 铝 [化学符号]Al, 读“吕”, [英文名称]Aluminum 精品
第 14 号元素: 硅 [化学符号]Si, 读“归”, [英文名称]Silicon 第 15 号元素: 磷 [化学符号]P, 读“邻”, [英文名称]Phosphorus 第 16 号元素: 硫 [化学符号]S, 读“流”, [英文名称]Sulfur 第 17 号元素: 氯 [化学符号]Cl, 读“绿”, [英文名称]Chlorine 第 18 号元素: 氩 [化学符号]Ar,A, 读“亚”, [英文名称]Argon 第 19 号元素: 钾 [化学符号]K, 读“甲”, [英文名称]Potassium 第 20 号元素: 钙 [化学符号]Ca, 读“丐”, [英文名称]Calcium 第 21 号元素: 钪 [化学符号]Sc, 读“亢”, [英文名称]Scandium 第 22 号元素: 钛 [化学符号]Ti, 读“太”, [英文名称]Titanium 第 23 号元素: 钒 [化学符号]V, 读“凡”, [英文名称]Vanadium 第 24 号元素: 铬 [化学符号]Cr, 读“各”, [英文名称]Chromium 第 25 号元素: 锰 [化学符号]Mn, 读“猛”, [英文名称]Manganese 第 26 号元素: 铁 [化学符号]Fe, 读“铁”, [英文名称]Iron 精品
