2010年版中国药典品种盐酸多西环素及其制剂含量和有关物质测定用HPLC法的建立
比浊法测定多西环素效价含量

比浊法测定多西环素效价含量应茵;楼娉婷【摘要】目的本文建立了比浊法测定多西环素效价的方法,为比浊法的进一步应用提供了依据.方法以金黄色葡萄球菌为试验菌,采用比浊法测定多西环素的含量,并对微生物比浊法、管碟法测定多西环素制剂的结果进行比较.结果多西环素的线性范围为1.0 ~3.3 u/ml(r =0.997 9),片剂平均回收率为99.84%,方法重复性良好(RSD为0.42%).同时,多西环素制剂的比浊法和管碟法测定结果无显著性差异,可信限率均小于5%.结论比浊法具有简便、精确、快捷的特点,可以应用于该产品的质量控制.【期刊名称】《药学实践杂志》【年(卷),期】2013(031)005【总页数】3页(P368-370)【关键词】多西环素;效价含量;比浊法【作者】应茵;楼娉婷【作者单位】浙江省立同德医院药剂科,浙江杭州310012;浙江省中山医院药剂科,浙江杭州310005【正文语种】中文【中图分类】R978.1+4多西环素(doxycycline)是以土霉素为原料制得的半合成广谱四环素类抗生素,体内、外试验均表明它对革兰氏阳性、阴性菌有良好的抗菌作用;对支原体、衣原体和立克次体均高度敏感[1]。
临床上应用于立克次体、支原体、衣原体及回归热螺旋体等非细菌性感染和布氏杆菌病,以及敏感菌所致的呼吸道、胆道、尿路及皮肤软组织等部位的感染。
中国药典对多西环素的效价测定只收载了管碟法[2]。
实际上,比浊法具有耗时短、灵敏度高、操作简单、人为影响因素少、测定结果准确度与精密度高的优点,被各国药典广泛采用[3,4]。
因此,笔者对用比浊法进行多西环素的效价测定方法进行了可行性考察。
1.1 实验材料多西环素标准品(中国药品生物制品检定所,批号K013-0614,效价836 μ/mg),多西环素胶囊(永信药品工业有限公司,批号V002、V017)、多西环素片(江苏联环药业有限公司,批号110213、110308)。
金黄色葡萄球菌[CMCC(B)26003](中国药品生物制品检定所);抗生素检定培养基Ⅲ(北京三药科技开发有限公司,批号:060403),蛋白胨、牛肉浸出粉、酵母浸出粉、氯化钠、磷酸氢二钾、磷酸二氢钾、葡萄糖。
药物分析习题含答案

药物分析复习题(红色是答案或提示)第一章一、最佳选择题1. ICH有关药品质量的技术要求文件的标识代码是A. EB. MC. PD. QE. S2. 药品标准中鉴别试验的意义在于A. 检查已知药物的纯度B. 验证已知药物与名称的一致性C. 确定已知药物的含量D. 考察已知药物的稳定性E. 确证未知药物的结构3. 盐酸溶液(9→1000)系指A. 盐酸1.0 ml加水使成1000 ml的溶液B. 盐酸1.0 ml加甲醇使成1000 ml的溶液C. 盐酸1.0 g加水使成1000 ml的溶液D. 盐酸1.0 g加水1000 ml制成的溶液E. 盐酸1.0 ml加水1000 ml制成的溶液4. 中国药典凡例规定:称取“2.0 g”,系指称取重量可为A. 1.5-2.5 gB. 1.6-2.4 gC. 1.45-2.45 gD. 1.95-2.05 gE. 1.96-2.04 g5. 中国药典规定:恒重,除另有规定外,系指供试品连续两次干燥或炽灼后的重量差异在A. 0.01 mgB. 0.03 mgC. 0.1 mgD. 0.3 mgE.0.5 mg6. 原料药稳定性试验的影响因素试验,疏松原料药在开口容器中摊成薄层的厚度应A.>20 cmB.≤20 cmC.≤10 cmD. ≤5 cmE. ≤10 mm7. 下列内容中,收载于中国药典附录的是A. 术语与符号B. 计量单位C. 标准品与对照品D. 准确度与精密度要求E. 通用检测方法8. 下列关于欧洲药典(EP)的说法中,不正确的是A. EP在欧盟范围内具有法律效力B. EP不收载制剂标准C. EP的制剂通则中各制剂项下包含:定义、生产、和检查D. EP制剂通则项下的规定为指导性原则E. EP由WHO起草和出版二、配伍题[1-2] A. SFDA B. ChP C. GCP D. GLP E. GMP下列管理规范的英文缩写是D 1.药品非临床研究质量管理规范E 2. 药品生产质量管理规范[3-5] A. 溶质1 g (ml)能在溶剂不到1 ml中溶解B. 溶质1 g (ml)能在溶剂1-不到10 ml中溶解C. 溶质1 g (ml)能在溶剂10-不到30 ml中溶解D. 溶质1 g (ml)能在溶剂30-不到100 ml中溶解E. 溶质1 g (ml)能在溶剂100-不到1000 ml中溶解B 3. 易溶C 4. 溶解E 5. 微溶[6-9] A. 2-10℃ B. 10-30℃ C. 40-50℃ D. 70-80℃ E. 98-100 ℃D 6. 热水C 7. 温水A 8. 冷水B 9. 常温[10-11] A. BP B. ChP C. EP D. Ph. Int. E. USPA 10. 英国药典C 11. 欧洲药典三、多项选择题1. 下列方面中,ICH达成共识,并已制定出相关技术要求的有A. 质量B. 安全性C. 有效性D. 综合要求E. 均一性2. 《中国药典》内容包括A. 前言B. 凡例C. 正文D. 附录E. 索引3. 下列关于《中国药典》凡例的说法中,正确的有A. 《中国药典》的凡例是《中国药典》的内容之一B. 《中国药典》的凡例是为正确使用《中国药典》进行药品质量检定的基本原则C. 《中国药典》的凡例是对其正文、附录及与质量检定有关的共性问题的统一规定D. 《中国药典》的凡例收载有制剂通则E. 《中国药典》的凡例收载有通用检测方法4. 药品标准中,“性状”项下记载有A. 外观B. 臭C. 味D. 溶解度E. 物理常数5. 药品标准中,“检查”项系检查药物的A. 安全性B. 有效性C. 均一性D. 纯度E. 稳定性6. 单一对映体的绝对构型确证常用的方法A. 比旋度测定B. 手性柱色谱C. 单晶X-衍射D. 旋光色散E. 圆二色谱7. 原料药稳定性试验的内容一般包括A. 影响因素试验B. 加速试验C. 长期试验D. 干法破坏试验E. 湿法破坏试验8. 国家药品标准的构成包括A. 前言B. 凡例C. 正文D. 附录E. 索引四、简答题1. 简述《中国药典》附录收载的内容2. 简述药品标准中药品名称的命名原则3. 简述药品标准的制定原则4. 简述中国药典凡例的性质、地位与内容5. 简述药品检验工作的机构和基本程序。
中国药典(2010版)

4附录XIX C 原料药与药物制剂稳定性试验指导原则稳定性试验的目的是考察原料药或药物制剂在温度、湿度、光线的影响下随时间变化的规律,为药品的生产、包装、贮存、运输条件提供科学依据,同时通过试验建立药品的有效期。
稳定性试验的基本要求是:(1)稳定性试验包括影响因素试验、加速试验与长期试验。
影响因素试验用1批原料药或1批制剂进行。
加速试验与长期试验要求用3批供试品进行。
(2)原料药供试品应是一定规模生产的,供试品量相当于制剂稳定性试验所要求的批量,原料合成工艺路线、方法、步骤应与大生产一致。
药物制剂供试品应是放大试验的产品,其处方与工艺应与大生产一致。
药物制剂如片剂、胶囊剂,每批放大试验的规模,片剂至少应为10000片,胶囊剂至少应为10000粒。
大体积包装的制剂如静脉输液等,每批放大规模的数量至少应为各项试验所需总量的10倍。
特殊品种、特殊剂型所需数量,根据情况另定。
(3)供试品的质量标准应与临床前研究及临床试验和规模生产所使用的供试品质量标准一致。
(4)加速试验与长期试验所用供试品的包装应与上市产品一致。
(5)研究药物稳定性,要采用专属性强、准确、精密、灵敏的药物分析方法与有关物质(含降解产物及其他变化所生成的产物)的检查方法,并对方法进行验证,以保证药物稳定性试验结果的可靠性。
在稳定性试验中,应重视降解产物的检查。
(6)由于放大试验比规模生产的数量要小,故申报者应承诺在获得批准后,从放大试验转入规模生产时,对最初通过生产验证的3批规模生产的产品仍需进行加速试验与长期稳定性试验。
本指导原则分两部分,第一部分为原料药,第二部分为药物制剂。
4.1一、原料药原料药要进行以下试验。
4.1.1(一)影响因素试验此项试验是在比加速试验更激烈的条件下进行。
其目的是探讨药物的固有稳定性、了解影响其稳定性的因素及可能的降解途径与降解产物,为制剂生产工艺、包装、贮存条件和建立降解产物分析方法提供科学依据。
供试品可以用1批原料药进行,将供试品置适宜的开口容器中(如称量瓶或培养皿),摊成≤5mm厚的薄层,疏松原料药摊成≤1 0mm厚的薄层,进行以下试验。
中国药典 2010 年版一部附录

中国药典2010 年版一部附录附录Ⅰ A 丸剂丸剂系指饮片细粉或提取物加适宜的黏合剂或其他辅料制成的球形或类球形制剂,分为蜜丸、水蜜丸、水丸、糊丸、蜡丸和浓缩丸等类型。
蜜丸系指饮片细粉以蜂蜜为黏合剂制成的丸剂。
其中每丸重量在0.5g(含0.5g)以上的称大蜜丸,每丸重量在0.5g 以下的称小蜜丸。
水蜜丸系指饮片细粉以蜂蜜和水为黏合剂制成的丸剂。
水丸系指饮片细粉以水(或根据制法用黄酒、醋、稀药汁、糖液等)为黏合剂制成的丸剂。
糊丸系指饮片细粉以米粉、米糊或面糊等为黏合剂制成的丸剂。
蜡丸系指饮片细粉以蜂蜡为黏合剂制成的丸剂。
浓缩丸系指饮片或部分饮片提取浓缩后,与适宜的辅料或其余饮片细粉,以水、蜂蜜或蜂蜜和水为勤合剂制成的丸剂。
根据所用黏合剂的不同,分为浓缩水丸、浓缩蜜丸和浓缩水蜜丸。
丸剂在生产与贮藏期间应符合下列有关规定。
一、除另有规定外,供制丸剂用的药粉应为细粉或最细粉。
二、蜜丸所用蜂蜜须经炼制后使用,按炼蜜程度分为嫩蜜、中蜜和老蜜,制备蜜丸时可根据品种、气像等具体情况选用。
除另有规定外,用塑制法制备蜜丸时,炼蜜应雄热加入药粉中,混合均匀;处方中有树脂类、胶类及含挥发性成分的药味时,炼蜜应在60℃左右加入;用泛制法制备水蜜丸时,炼蜜应用沸水稀释后使用。
三、浓缩丸所用提取物应按制法规定,采用一定的方法提取浓缩制成。
四、除另有规定外,水蜜丸、水丸、浓缩水蜜丸和浓缩水丸均应在80℃以下干燥;含挥发性成分或淀粉较多的丸剂(包括糊丸)应在60℃以下干燥;不宜加热干燥的应采用其他适宜的方法干燥。
五、制备蜡丸所用的蜂蜡应符合本版药典该饮片项下的规定。
制备时,将蜂蜡加热熔化,待冷却至60℃左右按比例加入药粉,棍合均匀,趁热按塑制法制丸,并注意保温。
六、凡需包衣和打光的丸剂,应使用各品种制法项下规定的包衣材料进行包衣和打光。
七、丸剂外观应圆整均匀、色泽一致。
蜜丸应细腻滋润,软硬适中。
蜡丸表面应光滑无裂纹,丸内不得有蜡点和颗粒。
第七届中国药学会施维雅青年药物化学奖评选有关情况和获奖名单

Induction of Cu Zn Superoxide Dismutase by CCL5CCR5 Activation Causes TNFα and ROS Production in Macrophages
第二军医大学药学院
肖莹
Lithospermicacid B is more responsive to silver ion (Ag+) thanrosmarinicacid in Salviamiltiorrhizahairy root cultures
北京大学临床药理研究所
王欣
抗肿瘤生物治疗药物AAV2-TRAIL在荷瘤小鼠体内生物分布研究
中国药品生物制品检定所国家药物安全评价监测中心
都丽萍
CYP2C9及VKORC1基因多态性对华法林剂量和抗凝效果的影响
北京协和医院
三等奖:
2009年中国药学大会暨第九届中国药师周优秀论文获奖名单
一等奖:
作者
论文题目
作者单位
毛根祥
抗肿瘤抗生素C3509B的研究
中国医学科学院医药生物技术研究所
阿基业
基于代谢组学技术探索药效学和药物安全性评价的新方法
中国药科大学
焦正
NONMEM法考察MDR1和CYP3A基因型和CYP3A表型对他克莫司药动学的影响
北京大学药学院
尹莉芳
左氧氟沙星缓释胶囊体内外评价
中国药科大学
朱赛杰
聚乙二醇化的聚酰胺-胺树枝状聚合物作为阿霉素肿瘤靶向递释载体的研究
复旦大学药学院药剂系
侯静文
酶催化合成两亲嵌段共聚物聚乙二醇-b-聚酯及其在药剂学中的应用
上海交通大学药学院
张洪斌
肠膜状明串珠菌右旋糖酐蔗糖酶基因的克隆、表达及其酶学性质研究
HPLC法测定盐酸多西环素软胶囊中盐酸多西环素及有关物质

北方药学 2 0 1 3素软胶囊 中盐酸 多西环素及有关物质
蔡正 东 ( 上 海信 谊万象药 业股份有限 公司 上海 2 0 1 7 0 3 )
摘要 : 目的: 建 立盐酸 多西环素软胶囊 中盐酸多西环 素的含量测定和有 关物质的控制 。方法: 采用 H P L C法, C s 色谱柱( 4 . 6 mi n x 2 5 0 m m, 5 m, p H值适用 范围大于 9 ) ; 以醋 酸 盐 缓 冲 液 [ 0 . 2 5 m o 1 / L醋 酸 铵 一 0 . i n  ̄ o l / L 乙二 胺 四 醋 酸 二 钠 一 三 乙胺 ( 1 0 0 : 1 0 : 1 ) , 用冰 醋酸或氨水调节 p H值 至 8 . 8 卜乙腈 ( 8 5 : 1 5 )  ̄流动相 ; 检测波长为 2 8 0 n m, 流速 1 . 0 ml d m i n , 进样量 2 0 1 x L 。结果: 盐酸多西环素检 测限为 0 . 0 0 3 I n L , 定量限 为 O . 0 1 I x g / mL , 在 浓度 1 - 2 0 0  ̄ m L范围 内与峰面积呈 良好 的线性 关 系, r = 0 . 9 9 9 9 9 ( n = 5 ) ; 各种 降解 产物 能 与 主戍 分峰 达 到 完全 分 离 。平 均 回 收 率 为 1 0 0 . 2 8 %( n = 9 , R S D = 0 . 8 %) 。结 论 : 此 方 法 简便 、 准确、 专 属性 强 , 可 用 于测 定 盐 酸 多西环素软胶 囊的含 量和有 关物 质。 关键词 : 高效 液 相 色谱 法 盐酸 多西 环 素 软 胶 囊 含 量测 定 有 关物 质
2 . 1 色谱条件 : 色谱柱 : C 。 色谱柱 ( 4 . 6 m mx 2 5 0 m m, 5 n l , p H 值 适 用范 围大 于 9 ) , 流动相 : 醋酸 盐缓 冲液【 0 . 2 5 m o l / L醋酸铵一 0 . 1 mo l / L乙二胺 四醋酸二钠一 三乙胺( 1 0 0 : 1 0 : 1 ) , 用冰醋酸或氨 H值至 8 . 8 卜乙腈 ( 8 5 : 1 5 ) 嘲 ; 流速 : 1 . O m Umi n ; 检测 波 织等部位的感染f l 1 。许多立克次体属 、 支原体属 、 衣原体属 、 非 水 调节 p 典型分枝杆菌属 、 螺旋体也对本 品敏感 。本品对革兰 阳性菌作 长 为 2 8 0 i r m; 进样量 2 0 , l z L 。 用优于革 兰阴性菌 , 但 肠球菌 属对其耐药 。其他如放线菌属 、 2 . 2对照品溶液的制备 : 称取多西环索对照品适量 , 加0 , 0 1 m o l / L 炭疽杆菌 、 单核细胞增 多性李斯 特菌 、 梭状 芽孢杆菌 、 奴卡菌 盐 酸 溶 液 溶 解 并 制 成 每 mL中 含 多 西环 素 0 . 1 mg的溶 液 属、 弧菌布鲁菌属 、 弯曲杆菌 、 耶尔森菌对 本品敏感 。多年来由 ( 1 0 0 1 x g / mL ) , 作为对照品溶液。 于四环素类 的广泛应用 ,临床常见病 原菌对本 品耐药现象严 2 . 3供试品溶 液的制备 : 取本 品 2 0粒 ( 上海信谊 万象药业 股份 重, 包括葡萄球菌等革兰 阳性菌及多数革兰阴性杆 菌 3 1 。本品 有 限公 司, 批号 0 9 0 3 0 2 ) , 用剪刀剪开将 内容物挤入烧杯 A, 混 与 四环素类抗 生素不同品种之间存在交叉耐药 。本品作 用机 匀 , 用玻璃棒 蘸取内容物 于烧 杯 B中 , 精 密称 定( 约相 当于多 . 1 g ) , 用2 0 m L 三氯 甲烷将内容物转移人分液漏斗。 用 制为药物 能特异性 与细菌核糖 体 3 0 S 亚基 的 A位 置结合 , 抑 西环素 0 制肽链的增长 和影响细菌蛋 白质的合成。 约2 0 m L的 0 . O l m o Y L盐酸溶液淋洗烧杯 , 洗液并入分液漏斗 , 软胶囊是指把一定量的原料 、原料 提取物加上适宜 的辅 强烈振摇 1 分钟 , 静置分层 。 下层的三氯甲烷层 回收入烧杯 B, 料密封于球形 、 椭圆形或其 他形状 的软质囊 中制成 的剂型。软 上层的水层过 滤入 2 0 0 m E容量瓶 ,烧杯 B中液体重新转移人 胶囊的特 点 : ①软胶囊的可塑性强 、 弹性大 。这是 由软胶囊囊 分液漏 斗 , 白“ 用约 2 0 m L的 0 . m o l / L 盐酸溶液 淋洗烧 杯” 开 材组成的性质所决 定的 , 取决于 明胶 、 增塑剂和水 三者之间的 始同法操作 , 萃取 5 遍 的滤液收集 之后 , 用0 . 0 1 m o Y L 盐 酸溶 比例 。 ②软胶囊可弥补其他 固体剂 型的不足 , 如含油量高或液 液稀释至刻度 ,摇匀。精密量取! - 5 mL ,置 2 5 n i L容量瓶中 , 加 态药物不易制成丸剂、 片剂时 , 可制成软胶曩 。盐酸多西环素 0 . 0 1 m o l / L 盐 酸 溶 液稀 释 至 刻 度 ,摇 匀 ,即得 供 试 品溶 液 的软胶囊剂型是信谊万象的 国内独家剂型 , 在 国 内外药典均 ( 1 0 0 1 x g / mL ) 。 未发现收载本 剂型 的质量标准 , 也未见有相关 的文献报道。国 2 . 4系统适用性实验 阁 : 称取 土霉素对 照品 、 美他环素对照 品、 家药 品标 准 WS 一 1 0 0 0 1 ~ ( H D 一 1 5 7 0 ) 一 2 0 0 5收载 了本品的含量 B 一 多四环素对照 品及 多西环素对照 品适量 , 加0 . 0 1 m o Y L盐酸 测定方法 , 为微生物效价法Ⅲ 。但 已无 法满足现在 日趋高效准 溶液溶解并制成每 m L中分别约含土 霉素 、 美 他环素 、 一 多 确灵敏 的分析要求 , 而且在有关 物质检测方 面还是空 白。为了 环素 O . 1 i n g 与多西 环素 0 . 2 a r g的混合溶液 。 理论板数按多西环 寻求更合 理高效 的分析方法 ,本 文拟采用现行方法 中的前处 素峰计为 3 3 1 7 , 多西 环素主峰与 p ~ 多西 环素峰 的分离度大于 理方法 , 再对其稍作 改进 , 与2 0 1 0版 中国药 典 中盐 酸多 环 4 . 0 , 与其他相邻 峰的分离度符合要求( 见图 1 ) 。 素原料含量测定方法 ( H P L C法 ) 相结合 , 来测定本剂型 的含量 与有关物质。 1仪器与试药 1 . 1实 验 仪 器 : W a t e r s 1 5 2 5高 效 液 相 色 谱 仪 ; C 色 谱 柱 ( 4 . 6 m m x 2 5 0 m m, 5 m, p H值 适 用 范 围 大 于 9 ) ; A p o l l o C l 8 ( 5 0 2 3 1 9 4 5 , 0 7 0 3 0 0 0 6 5 4 ) 、 A g i l e n t E x t e n d — C ( 7 7 0 4 5 0— 9 0 2 ) ;
2010版中国药典

2010版中国药典凡例总则一、《中华人民共和国药典》简称《中国药典》,依据《中华人民共和国药品管理法》组织制定和颁布实施。
《中国药典》一经颁布实施,其同品种的上版标准或其原国家标准即同时停止使用。
《中国药典》由一部、二部、三部及其增补本组成,内容分别包括凡例、正文和附录。
除特别注明版次外,《中国药典》均指现行版《中国药典》。
本部为《中国药典》二部。
二、国家药品标准由凡例与正文及其引用的附录共同构成。
本部药典收载的凡例、附录对药典以外的其他中药国家标准具同等效力。
三、凡例是为正确使用《中国药典》进行药品质量检定的基本原则,是对《中国药典》正文、附录及与质量检定有关的共性问题的统一规定。
四、凡例和附录中采用的“除另有规定外”这一用语,表示存在与凡例或附录有关规定不一致的情况时,则在正文中另作规定,并按此规定执行。
五、正文中引用的药品系指本版药典收载的品种,其质量应符合相应的规定。
六、正文所设各项规定是针对符合《药品生产质量管理规范》(Good Manufacturing Practices, GMP)的产品而言。
任何违反GMP 或有未经批准添加物质所生产的药品,即使符合《中国药典》或按照《中国药典》没有检出其添加物质或相关杂质,亦不能认为其符合规定。
七、《中国药典》的英文名称为Pharmacopoeia of The People’s Republic of China, 英文简称Chinese Pharmacopoeia;英文缩写为Ch.P.。
正文八、正文系根据药物自身的理化与生物学特性,按照批准的处方来源、生产工艺、贮藏运输条件等所制定的、用以检测药品质量是否达到用药要求并衡量其质量是否稳定均一的技术规定。
九、正文项下根据品种和剂型不同,按顺序可分别列有:(1)品名(包括中文名称、汉语拼音与英文名);(2)有机药物的结构式;(3)分子式与分子量;(4)来源或有机药物的化学名称;(5)含量或效价规定;(6)处方;(7)制法;(8)性状;(9)鉴别;(10)检查;(11)含量或效价测定;(12)类别;(13)规格;(14)贮藏;(15)制剂等。
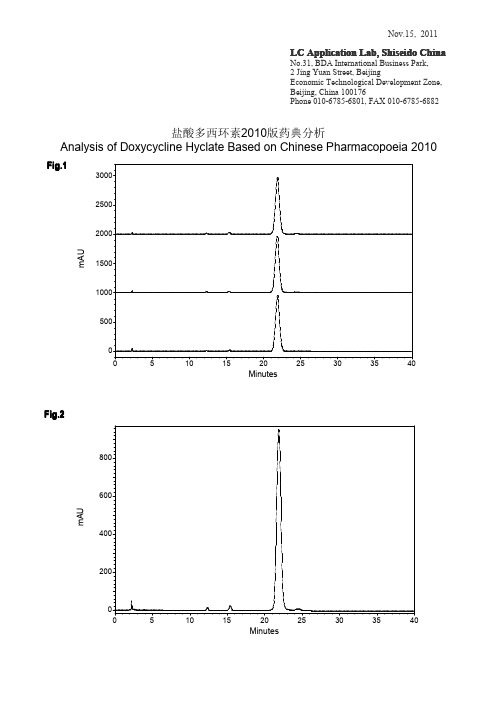
盐酸多西环素 2010版中国药典分析
盐酸多西环素 Doxycycline Hyclate
盐酸多西环素容易和填料表面重金属离子螯合, 导致色谱峰拖尾及分离度变差。 通过采用了聚合物包被处理 的资生堂 CAPCELL PAK MGII 色谱柱,按照 2010 版药典方法成功保留了盐酸多西环素,并且色谱峰形良好, 重现性好,主峰与其后杂质峰得到良好分离(分离度 2.31,见 Fig.1-3)。
800
600
mAU
400 200
0 0 5 10 15 20 25 30 35 40
Minutes
Fig.3
70 60 50 40
m10
15
20
25
30
35
40
Minutes
HPLC Conditions Column: CAPCELL PAK MGII 5μm, 4.6 mm i.d.×250mm (Col. No. A4AD03965) Oven temp.: 35 °C M. phase: A) 0.25mol/L CH3COONH4:0.1mol/L EDTA:TEA=100:10:1, B) CH3CN, A:B=85:15 Flow rate: 1000μL /min Inj. vol.: 20μL Sample: 0.2mg/mL, dissolved in 0.01mol/L HCl Detector: PDA 280nm
郭彦丽
城田修
Nov.15, 2011
LC Application Lab, Shiseido China
No.31, BDA International Business Park, 2 Jing Yuan Street, Beijing Economic Technological Development Zone, Beijing, China 100176 Phone 010-6785-6801, FAX 010-6785-6882
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
2010年版中国药典品种盐酸多西环素及其制剂含量和有关物质测定用HPLC法的建立袁耀佐1*;张玫1;钱文1;杨志明2;赵恂1(1 江苏省食品药品检验所,南京 210008 ;2 常州制药厂有限公司,常州 213018)摘要目的:建立先进的盐酸多西环素及其制剂含量和有关物质测定方法,用于2010年版中国药典。
方法:用十八烷基硅烷键合硅胶为填充剂(pH值适用范围应大于9);以醋酸盐缓冲液[0.25mol/L醋酸铵-0.1mol/L乙二胺四醋酸二钠-三乙胺(100:10:1),用冰醋酸或氨水调节pH值至8.8]-乙腈(85:15)为流动相;柱温35℃;检测波长为280nm,流速:1.0ml/min;进样体积:20µl。
结果:新色谱条件中用醋酸铵代替草酸铵,解决了《中国药典》2005年版流动相中容易结晶析出堵塞系统管路的问题;通过调整流动相pH值提高了柱效,通过添加EDTA钠和三乙胺改善色谱峰的对称性,使部分原来色谱条件无法有效分离杂质C和杂质F在新系统中能与相邻峰完全分离。
代表性样品色谱图中检出6个主要杂质峰,用杂质对照品对杂质A(ß-多西环素)、B(美他环素)、E(土霉素)进行了定位;用文献方法制备含已知杂质的溶液对杂质C(4-表多西环素)、D(4-表-6-表多西环素)进行了定位;用制备薄层色谱制得杂质F(2-乙酰-2-脱碳酰胺多西环素)溶液(纯度大于99%),用LC-ESI-IP-MS2对主成分的结构进行了鉴定,用该溶液对杂质F 进行了定位,土霉素、美他环素、ß-多西环素相对于多西环素的相对响应因子(relative response factor,RRF)分别为0.95、1.29、0.77。
建立的方法在0.07~122.556µg/ml范围内线性良好(r=1.0),检测限和定量限分别约为0.016、0.063µg/ml,多西环素及已知杂质的检测精密度良好,片剂和胶囊的回收率分别为99.2%(n=9)、99.4%(n=9)(RSD%均为0.2%),主成分在0.01mol/L的溶剂中可以稳定24小时。
微调该色谱条件,可用于土霉素、四环素、金霉素、米诺环素和美他环素的含量和有关物质的测定。
结论:建立的方法优于CP2005、USP31/NF26、BP2008、Ph.Eur 6.0、JPⅩⅤ中同品种方法,被2010年版中国药典采用。
关键词盐酸多西环素;高效液相色谱法;含量测定;有关物质;中国药典2010版The Establishment of Chromatographic Analysis Method of Doxycycline Hyclate and Its Preparations for Pharmacopoeia of the People’s Republic of China 2010Yuan Yao-zuo1, Zhang Mei1,Qian Wen1,Yang Zhi-ming2 and Zhao Xun1(1.Jiangsu Institute for drug control, Nanjing 210008; 2.Changzhou Pharmaceutical factory Changzhou 213018) Abstract Objectives To establish a better chromatographic analysis method of doxycycline hyclate and its preparations for Pharmacopoeia of the People’s Republic of China 2010 . Methods Carry out the method for high performance liquid chromatogram, using a column packed with octadecysilane bonded silica gel and a mixture of a buffer solution which consistof 100 volumes of 0.25 mol/L ammonium acetate solution, 10 volumes of 0.1 mol/L ethyldiaminetetraacetic acid disodiumsalt solution and 1 volume of triethyamine adjusting pH to 8.8 with glacial acetic acid –acetonitrile (85:15) as the mobile phase, maintain the column temerature at 35℃, detection wavelength is 280nm, flow rate is 1 mL·min-1, injection volume is20µl.Results The chromaotograhic mobile phase of doxycycline hyclate and its preparations used in CP2005 was changed completely, substituting ammonium acetate for ammonium oxalate as buffer salt to avoid the tunnel block of chromatographic system, substituting acetonitrile for dimethylformamide and tetrahydrofuran, the adjustment of pH value of mobile phase improves the separation ability, the addition of triethyamine and ethyldiaminetetraacetic acid disodium improves the symmetry of peaks. Impurity C and impurity F which can’t be separated effectively with their neighboring components inCP2005 chromatographic system can be separated completely under the new chromatographic system. Impurity A(6-epidoxycycline), B(metacycline), E(oxytetracycline) were located in the chromatogram by impurity standards. Impurity C (4-epidoxycycline), D(4-epi-6-epi-doxycycline) were located in the chromatogram by impurity solutions prepared according as literature methods, impurity F was located by the solution of impurity F which prepared by a preparative TLC method, and identified by LC-ESI-IP-MS2, the relative response factors of oxytetracycline, metacycline and 6-epidoxycycline were 0.95, 1.29 and 0.77 respectively. The linear range was 0.07~122.556µg/ml (r=1.0). The precision of method is good.The average recovery of the tablet method was 99.2%(n=9) and RSD% 0.2%, the average recovery of the capsule method was 99.4%(n=9) and RSD% 0.2%. Doxycycline can be stable in a 0.01 mol/L hydrochloric acid solution for 24hours. This chromatographic system can be applied to the determination of oxytetracycline, tetracycline, chlorotetracycline, minocycline and metacyclineby adjusting the mobile phase ratio of acetate buffer and acetonitrile. Conclusions the established method was better than the corresponding methods of CP2005,USP31/NF26,BP2008,Ph.Eur 6.0 and JPⅩⅤ and was used in CP2010.Key words Doxycycline hyclate High performance liquid chromatography Assay Related substances Pharmacopoeia of the People’s Republic of China 2010*袁耀佐,男,1968.03.10,博士,副主任药师,主要从事抗生素药物质量分析。
引言盐酸多西环素(Doxycycline Hyclate)是以土霉素为原料制得的半合成广谱四环类抗生素[1],其含半分子乙醇和半分子结晶水的盐酸盐在临床上有着广泛的应用,盐酸多西环素及其片剂、胶囊剂在USP31/NF26、BP2008、Ph.Eur 6.0、JPⅩⅤ和中国药典2005年版等标准中均有收载[2~7],Ph.Eur 6.0提供了其6个潜在杂质的化学结构,分别命名为杂质A、B、C、D、E、F,多西环素及其潜在杂质的化学结构如图1所示[4]。
