江苏省高三化学二轮复习 专题12《物质的组成、性质、分类、变化、化学用语》课时作业
高三二轮专题复习学案(全套)

专题一物质的组成、性质和分类【考纲展示】1.了解分子、原子、离子等概念的定义。
了解原子团的定义。
2.理解物理变化和化学变化的区别和联系。
3.了解化学的主要特点是在原子、分子水平上认识物质。
了解化学可以识别、改变和创造分子。
4.了解物质的组成、结构和性质的关系。
5.理解混合物与纯净物、单质与化合物、金属与非金属的概念。
6.理解酸、碱、盐、氧化物的概念及其相互联系。
7.了解电解质的概念。
了解强电解质和弱电解质的概念。
8.了解浊液、溶液和胶体都是常见的分散系。
(1)溶液的含义,了解溶解度、饱和溶液的概念。
(2)了解溶液的组成。
理解溶液中溶质的质量分数的概念,并能进行相关计算。
(3)了解胶体的性质(如丁达尔效应、聚沉及电泳等),并能利用胶体的性质解释一些与胶体有关的简单计算。
(不要求识记胶体粒子的带电情况)。
【知识回扣】知识网络金属非金属(包括稀有气体)单质氧化物酸性氧化物碱性氧化物两性氧化物不成盐氧化物根据酸根分为含氧酸、无氧酸根据电离出H +数目分为一元酸、二元酸、多元酸根据电离程度分为强酸、弱酸根据溶解性可分为可溶性碱、微溶性碱和难溶性碱根据电离程度可分为强碱、弱碱根据电离出OH —数目可分为一元碱、二元碱等酸碱根据阳离子可分为钠盐、钾盐等根据酸根分为硫酸盐、硝酸盐等根据组成可分为正盐、酸式盐、复盐等根据成盐的酸碱性可分为强酸弱碱盐、弱酸强碱盐等盐化合物无机物有机物烷烃烯烃炔烃芳香烃醇、酚醛、酮羧酸、酯卤代烃烃烃的衍生 物物质纯净物混合物要点扫描一、电解质和非电解质概念理解的易错点1.电解质和非电解质都是化合物,单质既不是电解质也不是非电解质。
2.有些电解质只能在水溶液里导电,如共价型电解质HCl 、H 2SO 4等,因为液态HCl 、H 2SO 4不导电;离子型电解质,如NaHCO 3、CaCO 3、BaCO 3等,因为这些物质不存在熔融态。
3.判断一种化合物是电解质还是非电解质,要看起导电作用的离子是否是由该物质自身电离出来的。
江苏高考化学二轮最新讲义:专题一 物质的组成、性质、分类和化学用语

专题一物质的组成、性质、分类和化学用语近三年的江苏高考题中的第2小题都考查有关化学用语,涉及电子式、结构示意图、结构简式、电离方程式、模型等正误判断,有机检测题中都涉及键线式的辨认等,都考查了有关元素化合物的性质;2011年还考查了胶体的相关作用。
作为常规考题,复习时关注表达式的差异,多加练习即可。
预测2013年江苏高考将重现该题型。
一物质的性质1(2012·淮安四模)下列有关物质的性质或应用的说法,正确的是()A. 钠属于活泼金属,可用电解NaCl溶液的方法获得金属钠B. FeCl3具有氧化性,可用于工业铜电路板的刻蚀C. Cl2和SO2都具有漂白性,故可以使NaOH、酚酞混合液褪色D. 浓硫酸具有脱水性,因此实验室可用浓硫酸与浓盐酸制取少量HCl气体1. 物质的变化(1) 物理变化:没有生成其他物质的变化。
例如:水的三态变化、蓝色的胆矾固体在研钵中研碎、酒精的挥发等。
这些变化通常是形状或者状态(气态、液体、固体)的改变。
(2) 化学变化:生成其他物质的变化,又叫做化学反应。
例如:木柴的燃烧、铁生锈、石灰石和盐酸反应等。
化学变化的基本特征是有新物质生成。
常常表现为颜色改变、生成气体或者沉淀等,也伴随有发光、放热或者吸热等能量的变化。
这些现象常常可以帮助我们判断有没有化学变化发生。
(3) 变化中的三色五解十八化三色:焰色反应(物理变化)、颜色反应、显色反应;五解:潮解(物理变化)、分解、裂解、水解、电解;[来源:学#科#网]十八化:熔化、汽化、液化、酸化(四化都是物理变化)、氧化、氢化、水化、风化、钝化、皂化、炭化、催化、硫化、酯化、硝化、裂化、卤化、油脂硬化。
2. 物质的性质(1) 化学性质:物质在化学变化中表现出来的性质。
胆矾溶液和氢氧化钠溶液反应有蓝色沉淀氢氧化铜生成,石灰石与盐酸反应有二氧化碳气体生成。
这里物质表现出的性质都是化学性质。
(2) 物理性质:物质不需要发生化学变化就表现出来的性质。
高考化学二轮复习--物质的组成性质分类及化学用语热点要点探究PPT课件
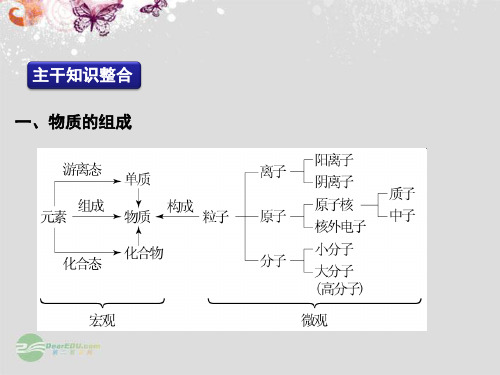
均一,透 不均一, 均一,透
明
不透明 明
稳定 不稳定 介稳定
能
不能 能能不能 不能无 Nhomakorabea无
有
考情分析:物质的组成、性质和分类,化学用语是中学 化学最基础的概念,是历年高考的必考内容,也是新 课标所要求的重点内容,属于热点问题,但试题一般 难度都不大,主要以生活中的化学知识或重大科技成 果为背景,以相关的基础化学知识为考点。重点侧重 概念的类比和辨析,突出对概念的准确理解和化学用 语的书写规范。预计今后的高考中对本专题内容的考 查不会有太大的变化,但考查的方式会因试题的变化 而变化。
(2)物质的分类依据不同,可以有多种分类方法, 特别是氧化物的分类是物质分类的难点,要 掌握此类知识,关键是明确其分类方法:
氧化物的分类比较复杂,判断氧化物所属类别时,应注意以下
几个问题:
①酸性氧化物不一定是非金属氧化物,如CrO3是酸性氧化物; 非金属氧化物不一定是酸性氧化物,如CO、NO和NO2等。
质方面来分类的;它是金属氧化物、最高价氧化物,
是从组成方面分类的。
[点拨] 1.分类的标准及原则 必须按同一标准进行,分类的子项应当互不相容,各子项必须是全异关系,
各子项之和必须等于母项。 2.物质类别的判断 判断物质的类别,主要看物质的组成元素和该物质中粒子的相互作用。 (1)根据有无固定的组成可判断是纯净物还是混合物,再根据是由几种元
题型一 物质的组成和分类
【例1】 物质分类的依据通常有组成和性质,下列物 质分类中,只考虑组成的是( )
A.Na2SO4是钠盐、硫酸盐、正盐 B.HNO3是一元酸、强酸、挥发性酸 C.Mg(OH)2是二元碱、难溶性碱、中强碱 D.Al2O3是两性氧化物、金属氧化物、最高价氧化物 [答案] A
苏教版高考化学二轮复习精品PPT系列:第 1 讲 物质的组成、性质和分类.

高考专题辅导与测试·化学
2.(2014·烟台模拟)下列物质的分类依据正确的是( )
物质类别
分类依据
A
酸
电离时能否产生氢离子
B 碱性氧化物 是否属于金属氧化物
C
胶体
能否发生丁达尔现象
D 强电解质 水溶液中能否完全电离
高考专题辅导与测试·化学
解析:(1)从“铜绿”的化学式 Cu2(OH)2CO3 可以看出它属于铜盐、碳 酸盐、碱式盐。(2)Cu2(OH)2CO3 与盐酸反应生成 CuCl2、H2O 和 CO2,反应的 化学方程式为 Cu2(OH)2CO3+4HCl===2CuCl2+3H2O+CO2↑。(3)题目中的转 化关系为 Cu→Cu2(OH)2CO3→CuCl2→Cu(OH)2→CuO→Cu,故 B 为 CuO。(4)由 Cu 转化为 Cu2(OH)2CO3 属于化合反应;④属于分解反应。(5)能聚沉的是胶 体。
(8)(2012· 重 庆 高 考 改 编 ) 向 沸 水 中 滴 加 过 量 饱 和 FeCl3 溶液,形成带电的胶粒,导电能力增强。( )
高考专题辅导与测试·化学
解析:(1)甲烷水合物也称“可燃冰”,是甲烷气体和水分子 形成的晶体。(2)浓氨水与 FeCl3 溶液反应得到的是 Fe(OH)3 沉淀。 (3)SO2、SiO2 是酸性氧化物,而 CO 为不成盐氧化物。(4)AlCl3 是共 价化合物,熔融态不导电,不能用于电解法制铝,工业上常用电解 熔融 Al2O3 的方法冶炼铝。(5)NaClO 是盐,属于强电解质。(6)炼油 厂对石油这种混合物控制不同的温度范围得到各沸点范围内的馏 分,是一种混合物的分离过程,是物理变化。(7)HCl 是共价化合物。 (8)形成胶体后,Fe3+的浓度下降,溶液的导电能力降低。
高三化学 第1单元第1讲_物质的组成、性质和分类复习课件 苏教版

物:碱性氧化物一定是金属氧化物,但金属氧化物不一 定是碱性氧化物。非金属氧化物不一定是酸性氧化物, 酸性氧化物也不一定是非金属氧化物。
【迁移训练4】下列过程中,不涉及化学变化的是 () A.甘油加水作护肤剂 B.用明矾净化水 C.烹鱼时加入少量的料酒和食醋可减少腥味,增 加香味
【点拨】以下是电子式表示时的常见错误,看清楚, 不要犯类似错误。 (1)漏写未参与成键的电子对。如
(2)离子错误归并。如MgCl2:
(3)错写分子中原子的结合方式。如HClO: HClO中H应与O相连,应写成 (4)漏写或多加“[ ]”及错写电荷数等。
【迁移训练1】下列物质的化学用语正确的是( ) A.NH4H的电子式:
第1讲 物质的组成、性质和分类
一、化学用语
化学用语是化学考查的重要内容。为避免由 于化学用语书写不规范而造成不应有的失分,应 注意三点:一要切实提高对规范书写的认识;二 要熟悉各种化学用语的内涵、书写特点和要求, 做到正确书写;三要从各次考试中发现书写错误, 寻找错写原因,不断纠正,逐渐杜绝不规范书写。
【参考答案】D
【点拨】胶体和溶液的本质区别是分散质粒子的大小, 区分的方法是丁达尔现象,这是胶体部分要识记的知 识点。
【迁移训练3】下列关于胶体和溶液的说法中正确的 是( )
A.胶体区别于其他分散系的本质特征是丁达尔效应
B.胶体不均一、不稳定,静置后易产生沉淀;溶液 均一、稳定,静置后不产生沉淀
C.光线通过时,胶体产生丁达尔效应,溶液则无丁 达尔效应
纯净物 有固定的组成和结构
有固定的熔沸点 保持一种物质的性质
混合物
无固定的组成和结构 无固定的熔沸点
保持原有物质各自性质
高中化学江苏版知识点总结

高中化学江苏版知识点总结一、基本概念与原理1. 物质的组成与分类- 物质由元素组成,分为纯净物和混合物。
- 纯净物包括单质和化合物,单质是由同种元素组成的纯净物,化合物是由不同元素组成的纯净物。
2. 原子结构- 原子由原子核和核外电子组成。
- 原子核包含质子和中子,核外电子围绕原子核运动。
3. 元素周期律- 元素的性质随着原子序数的增加而呈现周期性变化。
- 元素周期表是按照原子序数排列元素的表格,显示元素的周期律。
4. 化学键- 化学键是原子之间的相互作用,包括离子键、共价键和金属键。
- 离子键是由电荷相反的离子间的静电吸引力形成。
- 共价键是由原子间共享电子对形成的。
- 金属键是金属原子间的电子共享形成的。
5. 化学反应- 化学反应是原子重新排列形成新物质的过程。
- 化学反应遵循质量守恒定律,即反应前后物质的总质量不变。
二、无机化学1. 氧化还原反应- 氧化还原反应是电子转移的反应,包括氧化和还原两个过程。
- 氧化是失去电子的过程,还原是获得电子的过程。
2. 酸碱中和反应- 酸是能够提供质子的物质,碱是能够接受质子的物质。
- 酸碱中和反应是酸和碱反应生成水和盐的过程。
3. 盐类水解- 盐在水中溶解后,离子与水分子发生反应,导致溶液的pH值发生变化。
4. 常见无机物的性质与反应- 金属元素的化学性质,如活泼金属与酸的反应。
- 非金属元素的化学性质,如氯、硫、氮等元素的化合物。
三、有机化学1. 有机化合物的分类- 根据官能团的不同,有机化合物可以分为烷、烯、炔、醇、醛、酮、酸、酯等。
2. 有机反应类型- 取代反应:原子或原子团被其他原子或原子团所替代。
- 消除反应:分子中两个原子或原子团脱离,形成双键。
- 加成反应:分子中的双键或三键断裂,加入新的原子或原子团。
3. 有机化合物的性质- 有机化合物的物理性质,如沸点、熔点、溶解性等。
- 有机化合物的化学性质,如燃烧反应、氧化反应等。
四、化学实验1. 实验基本操作- 常见化学仪器的使用,如试管、烧杯、滴定管等。
江苏省高三化学二轮复习 专题12《物质的组成、性质、分类、变化、化学用语》课时作业

专题十二 物质的组成、性质、分类、变化、化学用语作业纸1.下列物质按纯净物、混合物、强弱电解质和非电解质顺序排列的是 A. 单甘油酯、混甘油酯、苛性钾、氢硫酸、三氧化硫B. 胆矾、漂白粉、硫酸钠、次氯酸、氯气C. 明矾、水煤气、盐酸、醋酸、铜D. 冰醋酸、福尔马林、硫酸钡、氢硫酸、乙醇2.化学科学需要借助化学专用语言描述,下列有关化学用语正确的是 A .CO 2的电子式B . Cl -的结构示意图C .氢有三种同位素:11H 、21H、31H,故可形成三种分子D .氧气和臭氧、红磷和白磷、普通水和重水互称为同素异形体 3.下列选项中正确的是A .氢氧化纳的结构式:Na-O-HB .乙烯的最简式:CH 2C .甲酸甲酯的结构简式:CH 3OCHOD .N 2的电子式:4.下列表达式正确的是 ( ) A. 羟基的电子式:[:O :H]-B.Na 2CO 3的水解方程式为:-23CO +H 2O -3HCO +-OHC.甲酸甲酯的结构简式:HCOOC 2H 5D.用Cu 做阳极电解饱和食盐水的阳极反应式为:2-Cl -2e-=Cl 2↑ 5.下列黄色不属于因化学反应而产生的现象的是A 无色试剂瓶中的浓硝酸呈黄色B 久置的碘化钾溶液呈黄色C 鸡蛋白遇浓硝酸呈黄色D 在普通玻璃导管中点燃纯净氢气时火焰呈黄色 6.下列变化肯定不可逆的组是 ①晶体的溶解; ②盐溶液的电解; ③盐的水解; ④电解质的电离; ⑤乙酸乙酯的生成; ⑥Fe(OH)3溶液与硅酸溶胶混合;⑦蛋白质溶液中加入饱和的硫酸铵溶液; ⑧蛋白质溶液中加入福尔马林;⑨合成氨. A .①②③④⑦⑨ B .②⑤⑥⑧ C .⑤⑥⑦⑧ D .②⑥⑧ 7.下列变化的实质相似的是①浓硫酸和浓盐酸在空气中敞口放置时浓度均减小②二氧化硫和氯气均能使品红溶液褪色③二氧化硫能使品红溶液、溴水褪色 ④氨气和碘化氢气体均不能用浓硫酸干燥⑤常温下浓硫酸用铁的容器存放、加热条件下浓硫酸能与木炭反应⑥浓硫酸能在白纸上写字,氢氟酸能在玻璃上刻字A .只有②③④ B.只有⑤ C.只有③④⑥ D.全部8.下列物质的电子式书写正确的是A.次氯酸 B.过氧化氢C.氨基 D.二氧化碳9.以下表示氦原子结构的化学用语中,对电子运动状态描述最详尽的是A.:He B. C.1s2 D.10.类比是研究物质性质的常用方法之一,可预测许多物质的性质。
物质的组成性质分类化学用语

1.概念辨析:混合物、纯净物、单质、化合物
混合物与纯净物的本质区别是组成的物质是一种分子 还是多种分子,而不是一种元素还是多种元素。因此, ①由同种分子构成的物质是纯净物,但由分子式相同的物 质组成的物质不一定是纯净物,也就是说,同种分子和分 子式相同并不是一回事,如分子式同为C5H12的正戊烷和 异戊烷,它们组成混合物; ②由同种元素组成的物质不一定是纯净物;如O2、O3 由同种原子构成的物质不一定是纯净物;如16O2和16O3, 组成混合物。
HCl、H2SO4
NaOH、Ba(OH)2
Na2CO3、NaHSO4、FeS
★ ★ ★氧化物的分类
还有酸、碱、盐的不同分类等
3.知识回顾
⑴电解质、强电解质、弱电解质的概念 ⑵属于强电解质的物质有: 强酸、强碱、大多数的 盐、活泼金属氧化物 ⑶离子化合物、共价化合物的概念 ⑷属于离子化合物的物质有: 强碱、大多数的盐、活 泼金属氧化物
强调:强、弱电解质与溶液的导电能力 的强弱、与溶解度的大小无关。
注意:氨水、盐酸是混合物,而NH3· H2O、HCl 是电解质。
注意: 1、四个关系:一定是吗?
酸性氧化物
× ×
(Mn2O7) (NO2 NO)
非金属氧化物
碱性氧化物
∨ × (Na2O2)
金属氧化物
2、易错的物质概念
冰醋酸、纯碱、干冰、 碱石灰、水玻璃、盐酸、氨水、福尔马林、 淀粉溶液 练习2:
课前背诵:
1.碱性氧化物一定是金属氧化物,但金属氧化物不一定是碱性 氧化物;酸性氧化物不一定是非金属氧化物,非金属氧化物也 不一定是酸性氧化物, 2.酸性氧化物、碱性氧化物不一定都能与水反应生成相应的酸、 碱,如SiO2、CuO等;能与水反应生成酸的氧化物不一定是酸 性氧化物,如NO2;能与水反应生成碱的氧化物不一定是碱性 氧化物,如Na2O2。 3.由同种元素组成的物质不一定是单质,也可能属于混合物, 如O2和O3的混合气体是混合物,只有由同一种元素组成的纯 净物才属于单质。 4.能电离出H+的物质不一定是酸,如NaHSO4,能电离出OH -的物质不一定是碱,如Cu (OH) CO ;盐的构成并不一定都 2 2 3 有金属阳离子和酸根阴离子,如铵盐。 5.电解质与非电解质指的一定是化合物;一种物质是否为电解 质与其能否导电无必然联系,如盐酸、醋酸,虽然能导电,因 它们是溶液,属于混合物,故它们不是电解质也不是非电解质。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
专题十二 物质的组成、性质、分类、变化、化学用语作业纸
1.下列物质按纯净物、混合物、强弱电解质和非电解质顺序排列的是 A. 单甘油酯、混甘油酯、苛性钾、氢硫酸、三氧化硫
B. 胆矾、漂白粉、硫酸钠、次氯酸、氯气
C. 明矾、水煤气、盐酸、醋酸、铜
D. 冰醋酸、福尔马林、硫酸钡、氢硫酸、乙醇
2.化学科学需要借助化学专用语言描述,下列有关化学用语正确的是
A .CO 2的电子式
B . Cl -
的结构示意图
C .氢有三种同位素:1
1H 、2
1H、3
1H,故可形成三种分子
D .氧气和臭氧、红磷和白磷、普通水和重水互称为同素异形体 3.下列选项中正确的是
A .氢氧化纳的结构式:Na-O-H
B .乙烯的最简式:CH 2
C .甲酸甲酯的结构简式:CH 3OCHO
D .N 2的电子式:
4.下列表达式正确的是 ( ) A. 羟基的电子式:[:O :H]-
B.Na 2CO 3的水解方程式为:-
23CO +H 2O
-3HCO +-OH
C.甲酸甲酯的结构简式:HCOOC 2H 5
D.用Cu 做阳极电解饱和食盐水的阳极反应式为:2-Cl -2e-=Cl 2↑ 5.下列黄色不属于因化学反应而产生的现象的是
A 无色试剂瓶中的浓硝酸呈黄色
B 久置的碘化钾溶液呈黄色
C 鸡蛋白遇浓硝酸呈黄色
D 在普通玻璃导管中点燃纯净氢气时火焰呈黄色 6.下列变化肯定不可逆的组是 ①晶体的溶解; ②盐溶液的电解; ③盐的水解; ④电解质的电离; ⑤乙酸乙酯的生成; ⑥Fe(OH)3溶液与硅酸溶胶混合;
⑦蛋白质溶液中加入饱和的硫酸铵溶液; ⑧蛋白质溶液中加入福尔马林;⑨合成氨. A .①②③④⑦⑨ B .②⑤⑥⑧ C .⑤⑥⑦⑧ D .②⑥⑧ 7.下列变化的实质相似的是
①浓硫酸和浓盐酸在空气中敞口放置时浓度均减小
②二氧化硫和氯气均能使品红溶液褪色③二氧化硫能使品红溶液、溴水褪色 ④氨气和碘化氢气体均不能用浓硫酸干燥
⑤常温下浓硫酸用铁的容器存放、加热条件下浓硫酸能与木炭反应
⑥浓硫酸能在白纸上写字,氢氟酸能在玻璃上刻字
A .只有②③④ B.只有⑤ C.只有③④⑥ D.全部 8.下列物质的电子式书写正确的是
A . 次氯酸
B . 过氧化氢
C . 氨基
D . 二氧化碳
9.以下表示氦原子结构的化学用语中,对电子运动状态描述最详尽的是
A .:He
B .
C .1s 2
D .
10.类比是研究物质性质的常用方法之一,可预测许多物质的性质。
但类比是相对的,不能违背客观事实。
下列各种类比推测的说法中正确的是
①已知Fe 与S 能直接化合生成FeS ,推测Cu 与S 可直接化合生成CuS ②已知CaCO 3与稀硝酸反应生成CO 2,推测CaSO 3与稀硝酸反应生成SO 2 ③已知CO 2分子是直线型结构,推测CS 2分子也是直线型结构 ④已知Fe 与CuSO 4溶液反应,推测Fe 与AgNO 3溶液也能反应
⑤已知NaOH 是强电解质,其饱和溶液导电能力很强,Ca(OH)2也是强电解质,推测其饱和溶液导电能力也很强
A .①③④
B .①②⑤
C .③④
D .③④⑤
11. 化学用语是学习化学的工具和基础。
下列有关化学语的使用正确的是 A .用食醋除去水壶内的水垢:CaCO 3+2H +
= Ca 2+
+CO 2↑+H 2O B .纯碱溶液呈碱性的原因是:CO 32—
+2H 2
O H 2CO 3+2OH
—
C. 钢铁发生吸氧腐蚀的正极反应式:O 2+ 4e - +2H 2O
=4OH —
D .表示氢气燃烧热的热化学方程式为:2H 2(g )+O 2(g )= 2H 2O (1);△H = -571.6 KJ·mol -1
12.选择下列某种答案的序号, 填入下表的空格
①同位素 ②同素异形体 ③同分异构体 ④同系物 ⑤同种物质
13.短周期元素Q、R、T、W在元素周期表中的位置如右图所示,其中T
所处的周期序数与主族序数相等,请回答下列问题:
(1)T的原子结构示意图为_______.
(2)元素的非金属性为(原子的得电子能力):Q______W(填“强于”或“弱于”)。
(3)W的单质与其最高价氧化物的水化物浓溶液共热能发生反应,生成两种物质,其中一种是气体,反应的化学方程式为_____
(4)原子序数比R多1的元素是一种氢化物能分解为它的另一种氢化物,此分解反应的化学方程式是__________.
(5)R有多种氧化物,其中甲的相对分子质量最小。
在一定条件下,2L的甲气体与0.5L的氯气相混合,若该混合气体被足量的NaOH溶液完全吸收后没有气体残留,所生成的R的含氧酸盐的化学式是__________.
(6)在298K下,Q、T的单质各1mol完全燃烧,分别放出热量aKJ和bKJ。
又知一定条件下,T的单质能将Q从它的最高价氧化物中置换出来,若此置换反应生成3molQ的单质,则该 =________(注:题中所设单质均为最稳定单质)
反应在298K下的H
专题十二:
典例:1.A 2.D 3.B 4.D 5.A 6.BD 7.B 8.D
考题在线:1.A 2.D 3.C 4.B 5.D
作业纸:
13、
(1)(2)弱于
(3)S + 2H2SO4(浓) △3SO2↑+ 2H2O
(4)2H2O2 MnO22H2O + O2↑(或其他合理答案)
(5)NaNO2
(6)(3a – 4b)KJ/mol。
