2015朝阳高考一模

北京市朝阳区高三年级第一次综合练习
理科综合化学试卷2015.4
可能用到的相对原子质量:H 1 C12 N 14 O 16 Na 23 Al 27 Cl 35.5 6.塑料的合理回收是再利用的关键,焚烧会产生大量HCl气体的是
7.下列物质的用途利用了其还原性的是
A.用葡萄糖制镜或保温瓶胆 B.用Na2S除去废水中的Hg2+
C.用NaHCO3治疗胃酸过多 D.用Na2SiO3溶液制备木材防火剂
8.下列解释事实的方程式不正确的是
A.铝热法炼铁:
B.工业进行“氮的固定”:
C.铅蓄电池充电时阴极反应:
D.用铜和稀硝酸制备硝酸铜:
9.用灼烧法证明海带中含有碘元素,各步骤选用的实验用品不必都用到
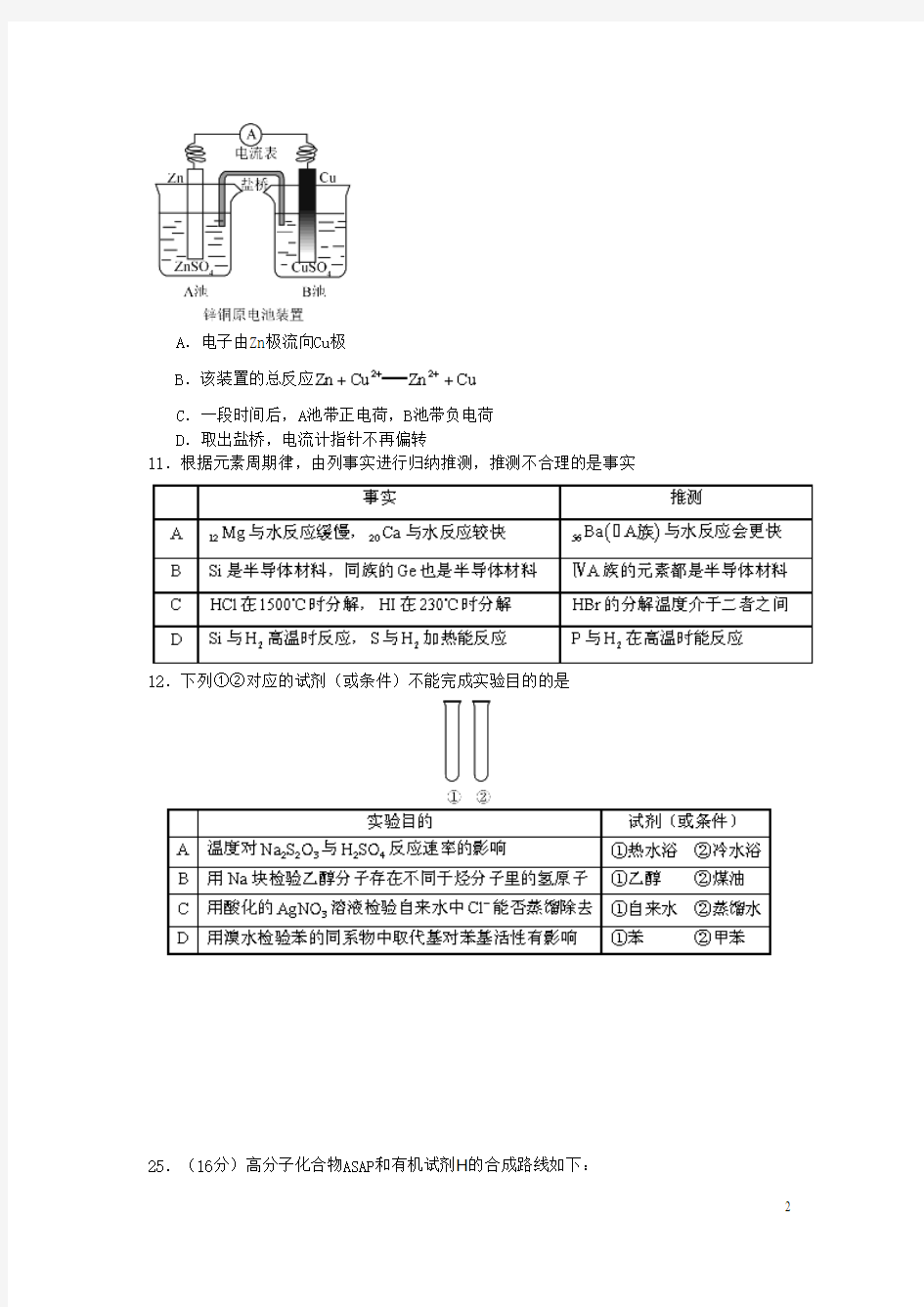
10.如图为锌铜显示原电池装置图,下列说法不正确
A.电子由Zn极流向Cu极
B.该装置的总反应
C.一段时间后,A池带正电荷,B池带负电荷
D.取出盐桥,电流计指针不再偏转
11.根据元素周期律,由列事实进行归纳推测,推测不合理的是事实
12.下列①②对应的试剂(或条件)不能完成实验目的的是
25.(16分)高分子化合物ASAP和有机试剂H的合成路线如下:
⑴AA中含有一个氯原子,生成A的反应类型是
⑵B中含有的官能团是
⑶D与Ag(NH3)2OH与反应的化学方程式是
⑷ASAP是制作尿不湿的材料,其结构简式是
⑸N→X的化学方程式是
⑹E有多种同分异构体,其中一种在相同条件下也能合成F,该同分异构体结构简式是
⑺下列说法正确的是.
a.1—丙醇的沸点比丙烯的高1
b.有机物M、X均存在顺反异构体
c.相同温度下,A的溶解度比B的小
⑻F的相对分子质量为182,H的结构简式是
26.(14分)
Cl2、漂白液(有效成分为NaClO)在生产、生活中广泛用于杀菌、消毒.
⑴电解NaCl溶液生成Cl2的化学方程式是
⑵Cl 2溶于H2O、NaOH溶液即获得氯水、漂白液.
①干燥的氯气不能漂白物质,但氯水却有漂白作用,说明起漂白作用的物质是
②25℃,Cl 2与H2O、NaOH的反应如下:
不直接使用氯水而使用漂白液做消毒剂的原因是
⑶家庭使用漂白液时,不宜直接接触铁制品,漂白液腐蚀铁的电极反应为:
;发生的电极反应式是
⑷研究漂白液的稳定性对其生产和保存有实际意义.30℃时,pH=11的漂白液中NaClO的质量百分含量随时间变化如下:
①分解速v(Ⅰ)、v(Ⅱ)的大小关系是,原因是
②NaClO分解的化学方程式是
③(常温下漂白液的密度约为1g / cm3,且变化忽略不计)
27.(13分)
氮化铝(AlN)广泛应用于集成电路,其制备原理是将氧化铝与碳粉混合均匀,在持续流动的氮气流中加热至1750℃,发生如下反应:
(1)断开N2分子内的共价键要热量(填“吸收”或“放出”)
(2)分析反应②对①、③平衡移动的影响。
(3)Al2O3、C、N2合成AlN的平衡常数表达式K=。
(4)用蒸馏法测定产品中AlN的含量,装置如下(加热及夹持装置略):
①AlN与NaOH溶液反应产生NH3的化学方程式是
②锥形瓶内吸收NH3的离子方程式是
③检验NH3是否完全蒸出的方法是:另取少量蒸馏出的溶液,(将检验过程补充完整)。
④NH3完全吸收后,向锥形瓶中加入指示剂,用浓度为c((N aOH)mol/L的NaOH标准溶液滴定过量的H2SO4,终点时用去标准溶液的体积为。下面有关计算正确的是。
A.样品中AlN的质量:
B.AlN的质量分数:
C.锥形瓶吸收NH3的物质的量:
28.(15分)某学生对Na2SO3与AgNO3在不同PH下的反应进行探究。
(1)测得Na2SO3溶液PH=11,AgNO3溶液PH=5,二者水解的离子分别是
(2)调节PH,实验记录如下:
查阅资料得知:
i.Ag2SO3:白色,难溶于水,溶于过量Na2SO3的溶液
ii.Ag2O:棕黑色,不溶于水,能和酸反应
①推测a中白色沉淀为Ag2SO3,离子方程式是
②推测a中白色沉淀为Ag2SO4,推测的依据是
(3)取b、c中白色沉淀,置于Na2SO3溶液中,沉淀溶解。该同学设计实验确认了白色沉淀不是Ag2SO4,实验方法是:另取Ag2SO4固体置于溶液中,未溶解。
(4)将中滤出、洗净,为确认其组成,实验如下:
Ⅰ.向X中滴加稀盐酸,无明显变化
Ⅱ.向X中加入过量浓HNO3,产生红棕色气体
Ⅲ.用Ba(NO3)2溶液、BaCl2溶液检验Ⅱ中反应后的溶液,前者无变化,后者产生白色沉淀
①实验Ⅰ的目的是。
②根据上述现象,分析X的性质和元素组成是
③Ⅱ中反应的化学方程式是
(5)该同学综合以上实验,分析产生X的原因,认为随着酸性的增强,还原性增强。通过进一步实验确认了这种可能性,实验如下:
①气体Y是。
②白色沉淀转化为X的化学方程式是
2015年朝阳一模化学试卷答案及解析
6. 选B
【解析】本题考查化学与生活,常见塑料的成分和垃圾的回收与处理。聚氯乙烯中含有氯元素,焚烧时会产生HCl气体,其他塑料中都不含有氯元素,焚烧时不会产生HCl气体。
7. 选A
【解析】本题考查物质的常见用途。葡萄糖制镜利用葡萄糖的还原性,与银氨溶液发生氧化还原反应,生成银单质;用Na2S除去废水中的Hg2+,利用S2-和Hg2+反应生成难溶物HgS,为复分解反应;NaHCO3治疗胃酸过多利用NaHCO3与酸反应生成CO2和H2O,为复分解反应。
8. 选D
【解析】本题考查重要反应的方程式书写。铝热法是铝单质和某些金属氧化法在高温条件下发生置换反应,生成活泼性弱于铝的金属单质;工业固氮的第一步是以氮气和氢气为原料直接化合生成氨气,再通过氨气合成其他含氮化合物;铅蓄电池充电时,阴极上是PbSO4得电子发生还原反应生成Pb单质;铜与稀硝酸反应生成NO。
9. 选C
【解析】本题考查检验海带中碘元素的重要实验。灼烧海带时使用三角架、泥三角、坩埚、坩埚钳、酒精灯;海带灰溶解、过滤时使用烧杯、普通漏斗、玻璃棒、铁架台;氧化碘离子时不需要使用容量瓶。
10. 选C
【解析】本题考查原电池基本原理。铜锌原电池中锌为负极,铜为正极,电子由Zn极移向Cu 极;原电池总反应为:Zn+Cu2+=Zn2++Cu;取出盐桥,原电池中闭合回路断开,不再存在电流,电流表指针不偏转;盐桥中阳离子移向B池,阴离子移向A池,A池和B池中溶液仍然保持电中性。
11. 选B
【解析】本题考查元素周期律的应用。同主族金属元素由上至下金属性增强,与水反应剧烈程度增强,A正确;半导体材料通常位于元素周期表中金属元素和非金属元素的分界处,第IVA族元素并不都是半导体材料;同主族非金属元素由上至下非金属性减弱,气态氢化物的热稳定性减弱,C正确;同周期非金属元素从左到右非金属性增强,与氢气化合难度减小,D 正确。
12. 选D
【解析】本题考查实验方案的设计和评价。热水浴和冷水浴是反应温度不同,体现了温度对反应速率的影响;乙醇与钠反应生成氢气,煤油(主要成分是烃)和钠不反应,可以用钠块检验乙醇分子中存在不同于烃分子里的氢原子;酸化的AgNO3溶液和含Cl-的自来水反应生成白色沉淀AgCl,若蒸馏水中Cl-被除去,则不产生白色沉淀;苯和甲苯都不与溴水反应,都能萃取溴水中的溴,因此不能验证苯的同系物中取代基对苯基活性的影响。
25.【答案】
(1) 取代反应
(2) 碳碳双键、羟基
