铜锌原电池电动势的测定及应用-推荐下载
电池电动势的测定及应用实验报告

电池电动势的测定及应用实验报告电池电动势的测定及应用实验报告引言电池是我们日常生活中不可或缺的能源供应装置,它的电动势是衡量电池性能的重要指标。
本实验旨在通过测定电池的电动势,了解电池的工作原理,并探索电池在实际应用中的一些可能性。
实验方法1. 实验仪器与材料本实验使用的仪器有:直流电压表、电流表、可变电阻箱、导线等。
材料包括:干电池、铜片、锌片等。
2. 实验步骤(1)将干电池的正极与铜片连接,负极与锌片连接,形成一个闭合电路。
(2)将直流电压表的正极与铜片连接,负极与锌片连接,测量电池的电动势。
(3)通过调节可变电阻箱的电阻,改变电路中的电流强度,记录电压和电流的变化。
(4)根据测得的数据,绘制电压与电流的关系曲线。
实验结果通过实验,我们得到了以下数据:电流(A) 0.1 0.2 0.3 0.4 0.5电压(V) 1.5 1.3 1.1 0.9 0.7根据实验数据,我们可以绘制出电压与电流的关系曲线。
从图中可以看出,电压随着电流的增大而逐渐降低,呈现出线性的负相关关系。
讨论与分析1. 电池的内阻根据欧姆定律,我们可以通过实验数据计算出电池的内阻。
内阻的大小会影响电池的电动势稳定性和输出能力。
通过实验计算,我们得到电池的内阻为0.8欧姆。
2. 电池的工作原理电池是通过化学反应将化学能转化为电能的装置。
在干电池中,锌片发生氧化反应,释放出电子,形成负极;铜片则接受电子,发生还原反应,形成正极。
这种化学反应产生的电子流动就是电池的电流。
3. 电池的应用电池作为一种便携式能源装置,广泛应用于日常生活和工业领域。
它可以为各种电子设备提供电力,如手机、手提电脑、闹钟等。
此外,电池还可以用于储能系统,如太阳能电池板储存太阳能,以备不时之需。
结论通过本次实验,我们成功测定了电池的电动势,并了解了电池的工作原理。
通过分析实验数据,我们得出了电压与电流之间的关系,并计算出了电池的内阻。
电池作为一种重要的能源装置,具有广泛的应用前景。
《物理化学基础实验》原电池电动势的测定及应用实验

《物理化学基础实验》原电池电动势的测定及应用实验一、实验目的1.测定Cu-Zn原电池的电动势及Cu、Zn电极的电极电势;2.学会几种电极和盐桥的制备方法;3.掌握可逆电池电动势的测量原理和UJ-25型电位差计的操作技术。
二、实验原理凡把化学能转变为电能的装置称为化学电源(或电池、原电池)。
电池是由两个电极和连通两个电极的电解质溶液组成的。
如图13-1所示。
图13-1 Zn-Cu电池示意图Figure 13-1 Zinc - Cu battery diagram把Zn片插入ZnSO4溶液中构成Zn电极,把Cu片插在CuSO4溶液中构成Cu电极。
用盐桥(其中充满电解质)把这两个电极连接起来就成为Cu-Zn电池。
可逆电池应满足如下条件:(1) 电池反应可逆,亦即电池电极反应可逆。
(2) 电池中不允许存在任何不可逆的液接界。
(3) 电池必须在可逆的情况下工作,即充放电过程必须在平衡态下进行,亦即允许通过电池的电流为无限小。
因此在制备可逆电池、测定可逆电池的电动势时应符合上述条件,在精确度不高的测量中,常用正负离子迁移数比较接近的盐类构成“盐桥”来消除液接电位。
用电位差计测量电动势也可满足通过电池电流为无限小的条件。
在电池中,每个电极都具有一定的电极电势。
当电池处于平衡态时,两个电极的电极电势之差就等于该可逆电池的电动势,按照我们常采用的习惯,规定电池的电动势等于正、负电极的电极电势之差。
即:-+-=ϕϕE (1)式中:E 是原电池的电动势。
+ϕ、-ϕ分别代表正、负极的电极电势。
其中:氧化还原a a zF RT ln-=++θϕϕ (2) 氧化还原a a zF RT ln-=--θϕϕ (3) 在式(2)、(3)中:θϕ+、θϕ-分别代表正、负电极的标准电极电势,R =8.314 J •mol -1•K -1。
T是绝对温度。
z 是反应中得失电子的数量。
F =96500 C ,称法拉第常数。
还原a 、氧化a 分别为参与电极反应的物质的还原态、氧化态的活度。
原电池电动势的测定及应用实验报告

原电池电动势的测定及应用实验报告实验目的1、学会Cu、Zn电极的制备和简单处理方法。
2、测定Cu-Zn原电池的电动势和Cu、Zn电极的电极电势。
3、掌握电位差计(包括数字式电子电位差计)的测量原理和正确使用方法。
实验原理电池电动势E的测定必须是在热力学可逆的条件下进行。
因此在测定时,首先要求被测电池反应本身是可逆的,即要求电池的电极反应是可逆的,并且不存在不可逆的液体接界,同时要求电池在放电或充电过程都必须在平衡态或无限接近平衡态下进行,即要求通过电池的电流无限小。
当一个可逆的化学反应是在无限缓慢的情况下进行时,就可以认为该电池的反应是在接近热力学可逆的条件下进行的。
而一个电池反应的快慢是以通过该电池电流的大小反映的,当通过电池的电流无限小时,则该可逆电池的反应就是在接近热力学可逆的情况下进行的。
为了使可逆电池在接近热力学可逆条件下进行,通常采用根据补偿法或称对消法(在外电路上加一个方向相反而电动势几乎相等的电池)设计的电位差计来测量电池的电动势。
液体接界电势的存在会破坏电池的可逆性,所设计的电池要尽量避免出现液接界,在精确度要求不高的测量中,常用“盐桥”来减小液接界电势。
电位差计(示意图如下),是利用补偿法测量直流电动势(或电压)的精密仪器,其工作原理如图所示:工作电源E,限流电阻R p,滑线电阻R AB构成辅助回路,待测电源E x(或标准电池E n),检流计G和R AC构成补偿回路。
按图中规定电源极性接入E、E x,双向开关K打向2,调节C点,使流过G中的电流为零。
(称达到平衡。
若E<E x或E、E x极性接反,则无法达到平衡),则E x=V AC=I R AC 即E x被电位差I R AC所补偿。
I为流过滑线电阻R AB的电流,称辅助回路的工作电流。
若已知I和R AC就可求出E x。
实际的电位差计,滑线电阻由一系列标准电阻串联而成,工作电流总是标定为一固定数值I0,使电位差计总是在统一的I0下达到平衡,从而将待测电动势的数值直接标度在各段电阻上(即标在仪器面板上),直接读取电压值,这称为电位差计的校准。
原电池电动势的测定及应用实验报告

原电池电动势的测定及应用实验报告实验报告:原电池电动势的测定及应用一、实验目的:1.学习如何测定原电池的电动势。
2.了解原电池的构造和工作原理。
3.研究原电池的应用。
二、实验仪器和材料:1.原电池(例如锌银电池、铜锌电池等)2.电流表3.电位计4.导线5.开关6.电阻箱7.连接板8.电源三、实验原理:原电池是一种将化学能转化为电能的装置,由两个不同的金属或合金及其周围的电解质溶液组成。
在原电池中,金属条与电解质之间的化学反应产生电流。
电动势是原电池提供给外部电路单位正电荷所需的能量。
电动势的实际值与原电池的化学反应和电化学平衡有关。
四、实验步骤及数据处理:1.将原电池、电流表、电位计以及电阻箱按照电路图连接好。
2.打开开关,通过调节电阻箱中的电阻,使电流表示数保持在一个恒定的值。
3.根据电位计的示数和电流表的示数,计算出原电池的电动势。
五、实验结果与分析:根据电位计的示数和电流表的示数,我们进行了多组实验,并计算出了不同条件下原电池的电动势。
在分析实验结果时,我们可以发现,原电池的电动势与电流的大小无关,主要取决于原电池中的化学反应和电化学平衡。
不同种类的原电池,其电动势可能会有所不同。
六、实验应用:1.用于供电:原电池可以直接为电器设备或电路提供稳定的直流电源。
2.计算电动势:通过测量原电池的电动势,我们可以了解原电池的性能与工作状态,判断其是否需要更换或维修。
3.进行电解实验:原电池可以为电解实验提供所需的电流。
4.进行电池组装:原电池可以通过串联或并联的方式组装成电池组,提供更大的电动势和容量。
七、实验总结:通过本次实验,我们学习了如何测定原电池的电动势,并了解了原电池的构造、工作原理和应用。
电动势是一个重要的物理概念,对于理解电路的工作原理和实际应用具有重要意义。
铜锌电池的标准电动势

铜锌电池的标准电动势铜锌电池是一种常见的原电池,它由铜阳极、锌阴极和硫酸溶液组成。
在电池中,铜阳极失去电子形成Cu2+,而锌阴极接受电子形成Zn2+,同时硫酸溶液中的H+也参与了电池的反应过程。
这些化学反应产生了电流,从而实现了电池的电能转化。
铜锌电池的标准电动势是指在标准状态下,即溶液中的活度为1M时,电池的电动势。
标准状态下,铜锌电池的标准电动势可以通过以下半反应得到:Cu2+ + 2e→ Cu (标准电动势为+0.34V)。
Zn2+ + 2e→ Zn (标准电动势为-0.76V)。
根据电化学原理,铜锌电池的标准电动势可以通过上述半反应的标准电动势差来计算,即:E°cell = E°cathode E°anode。
E°cell = (-0.76V) (+0.34V)。
E°cell = -1.10V。
由此可见,铜锌电池的标准电动势为-1.10V。
这意味着在标准状态下,铜锌电池可以提供1.10V的电动势,可以用来驱动电子流动,从而实现电能转化。
铜锌电池的标准电动势对于电池的性能具有重要意义。
首先,标准电动势可以反映出电池的电化学活性,即电池中的化学物质参与反应的倾向性。
标准电动势越高,电池的电化学活性越强,电池产生电流的能力也越强。
其次,标准电动势还可以反映出电池的电压稳定性,即电池在不同工作条件下产生的电动势变化情况。
标准电动势越稳定,电池的输出电压波动越小,电池的使用寿命和稳定性也越高。
在实际应用中,铜锌电池的标准电动势可以通过改变电池中的活性物质、溶液浓度、温度等因素来调控,从而实现对电池性能的优化。
例如,可以通过合理选择阳极和阴极材料,调节溶液浓度,控制温度等手段来提高电池的标准电动势,从而提高电池的输出电压和稳定性。
总之,铜锌电池的标准电动势是电池性能的重要指标,它反映了电池的电化学活性和电压稳定性。
通过对标准电动势的深入研究和优化,可以实现对铜锌电池性能的提升,推动电池技术的发展和应用。
原电池电动势的测定及其应用

(7)使用饱和甘汞电极,要防止溶液倒流入甘汞电极中。甘 汞电极和盐桥中应保留少量氯化钾晶体,使溶液处于饱和状 态。 (8)标准电池在搬动和使用时,不要使其倾斜和倒置,要放 置平稳。接线时正接正、负接负,两极不允许短路。
正极——电势高的电极,电流从正极流向负极。 负极——电势低的电极,电子从负极流向正极。
阳极——发生氧化作用的电极,阴(负)离子向阳极迁移。 阴极——发生还原作用的电极,阳(正)离子向阴极迁移。
原电池 电解池
阳极 负极 正极
阴极 正极 负极
在电解池中正极为 阳极,负极为阴极; 在原电池中则相反
2、原电池如何把化学反应转变成电能?
Cu | Cu 2+(0.0100mol·L-1)||Cu2+(0.1000mol·L-1)|Cu
四、实验步骤
3、电动势测定
1)根据Nernst公式计算实验温度下电池1、2、3、4的电 动势理论值。
2)正确接好测量电池1的线路。用SDC数字电位差计测 量电池1的电动势。每隔2分钟测一次,共测三次,偏差小于 ±0.5mV,可认为已达平衡,其平均值就为该电池的电动势。
如图所示,电位差计有工作、标准、测量三条回路。
2)测量未知电池电 动势EW
开关K打向2, 调节测量回路的电
阻RX至检流计无电 流通过,此时I RX与 被测电池电动势对
消。
EX IW RX En IW Rn
IW
En Rn
EX
EN
RX RN
原电池电动势和电极电势的测定
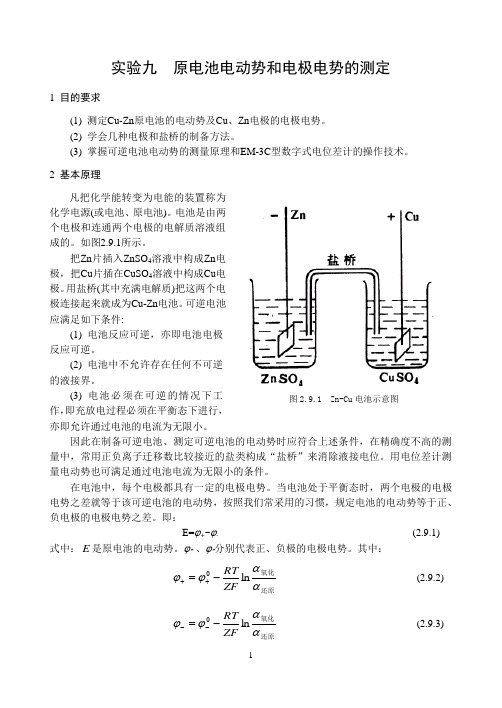
实验九 原电池电动势和电极电势的测定1 目的要求(1) 测定Cu-Zn 原电池的电动势及Cu 、Zn 电极的电极电势。
(2) 学会几种电极和盐桥的制备方法。
(3) 掌握可逆电池电动势的测量原理和EM-3C 型数字式电位差计的操作技术。
2 基本原理凡把化学能转变为电能的装置称为化学电源(或电池、原电池)。
电池是由两个电极和连通两个电极的电解质溶液组成的。
如图2.9.1所示。
把Zn 片插入ZnSO 4溶液中构成Zn 电极,把Cu 片插在CuSO 4溶液中构成Cu 电极。
用盐桥(其中充满电解质)把这两个电极连接起来就成为Cu-Zn 电池。
可逆电池应满足如下条件:(1) 电池反应可逆,亦即电池电极反应可逆。
(2) 电池中不允许存在任何不可逆的液接界。
(3) 电池必须在可逆的情况下工作,即充放电过程必须在平衡态下进行,亦即允许通过电池的电流为无限小。
因此在制备可逆电池、测定可逆电池的电动势时应符合上述条件,在精确度不高的测量中,常用正负离子迁移数比较接近的盐类构成“盐桥”来消除液接电位。
用电位差计测量电动势也可满足通过电池电流为无限小的条件。
在电池中,每个电极都具有一定的电极电势。
当电池处于平衡态时,两个电极的电极电势之差就等于该可逆电池的电动势,按照我们常采用的习惯,规定电池的电动势等于正、负电极的电极电势之差。
即:E=ϕ+-ϕ- (2.9.1) 式中:E 是原电池的电动势。
ϕ+ 、ϕ-分别代表正、负极的电极电势。
其中:还原氧化ααϕϕln0ZF RT -=++ (2.9.2) 还原氧化ααϕϕlnZF RT -=--(2.9.3)在式(2.9.2)、(2.9.3)中:ϕ+、ϕ-分别代表正、负电极的标准电极电势。
R=8.134J.mol -1.K -1。
T 是绝对温度。
Z 是反应中得失电子的数量。
F=96500C ,称法拉第常数。
α氧化为参与电极反应的物质的还原态的活度。
对于Cu-Zn 电池,其电池表示式为:Zn|ZnSO 4(m 1)||CnSO 4(m 2)|Cu其电极反应为:⎩⎨⎧+→→+++++e Zn Zn Cu e Zn Cu 2)(2)(Cu 2222αα负极反应:正极反应:其电池反应为:)()(2222+++++→+Zn Cu Zn Cu Cu Zn αα其电动势为: Zn Zn Cu Cu E ,,22++-=ϕϕ (2.9.4)+++-=2221ln20,,Cu CuCu CuCu F RT αϕϕ (2.9.5) +++-=2221ln20,,Zn ZnZn ZnZnF RT αϕϕ (2.9.6) 在式2.9.5和2.9.6中,Cu 2+, Zn 2+的活度可由其浓度m i 和相应电解质溶液的平均活度系数γ±计算出来。
原电池电动势的测定及其应用

原电池电动势的测定及其应用
实验项目:中级化学实验(物理化学)编号:2014_jcsy2_007
一.实验名称:原电池电动势的测定及其应用
二.实验目的:
1.测定Cu-Zn电池电动势和Cu、Zn电极的电动势。
2.学会一些电极的制备和处理方法。
3.了解电位差计的基本原理和正确使用。
三.实验仪器: 数字式电位差、饱和甘汞电极、电极管、电极架
四.实验技能:抽气、电极反应
五.注意事项
1.电池电动势不能用伏特计直接测量,因为伏特计接通后就有电流通过电极,使电极发生极化而偏离平衡状态,此外电池本身有内阻,所以伏特计所测量的仅是两极的电位降。
2.通常将标准电池封在电木盒子里。
在放置或移动标准电池时,只能正放、平移,绝不可斜放、斜拿,更不允许倒置。
3.在测量电动势过程中,应经常注意校正工作电流,在校正工作电流时,测量转换开关K1应指向“标准”位置。
六.实验技能列表。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
铜锌原电池电动势的测定及应用
实验目的
1. 掌握对消法测定电池电动势的原理及电位差计的使用方法。
2. 通过电池电动势的测量,加深理解可逆电池、盐桥等基本概念。
3. 学会金属电极的制备和处理方法。
4. 通过原电池电动势的测定掌握有关热力学函数的计算。
实验原理
铜锌原电池是由两个“半电池”所组成,而每一个半电池中有一个电极和相应的电解质溶液。
在铜锌原电池放电反应中,正极起还原反应,负极起氧化反应,电池反应是两个电极反应的总和,其电动势为组成该电池的两个半电池的电极电势的代数和。
在恒温恒压、可逆条件下,各热力学函数与电池电动势有如下关系:
(1)
(2)
(3)
式中:F是法拉第常数(96485.34C),z是电池输出元电荷的物质的量,E 是可逆电池的电动势。
故只要在恒温恒压下测出铜锌电池的电动势E和电动势的温度系数,便可求出各热力学函数。
书写电池的电动势和电极电势的表达式:
根据能斯特方程,可得电池的电动势与活度的关系式:
(4)
由于Cu 、Zn 为纯固体,它们的活度为1,则式(4)可书写为:
(5) 式中 为溶液中锌离子的活度和铜离子的活度均等于1时的电池的电动势(即原电池的标准电动势)。
的数值可由下法得到。
=E 0+-E 0- (6)E 0以标准氢电极作为标准(标准氢电极是氢气压力为100kPa ,溶液中为1,其电极电势规定为零)测得。
将标准氢电极作为负极铜电极作为正极组成电池测定E(Zn|Zn2+),标准氢电极作为负极锌电极作为正极组成电池测定E(Cu|Cu2+)。
E(Zn|Zn2+)= E 0(Zn|Zn2+)- 2RT F ()ln (2+a Zn a Zn ) (7)E(Cu|Cu2+)= E 0(Cu|Cu2+)- 2RT F ()ln (2+a Cu a Cu ) (8)得出E 0(Zn|Zn2+),E 0(Cu|Cu2+)。
由(6)得 。
由E 0 还可以计算出ΔrGmθ,可由下式求出:ΔrGmθ=-zFE 0 (9)计算原电池反应电动势的温度系数(E T ∂∂)P 。
测定不同温度下铜锌原电池的电动势,作E-T 图求斜率,斜率即为(E T ∂∂)P 。
实验仪器及试剂 仪器:SDC-ⅡB 数字电位差综合测试仪1台(南京桑力电子设备厂) ,铜电极 1
支,锌电极 1 支,50ml 烧杯2只,恒温装置一套,U型管。
试剂:0.100×103 mol.m-3 ZnSO4 ,0.100×103 mol m-3CuSO4,1∶3的稀硝酸,稀硫酸溶液,饱和KNO3溶液,琼脂,CuSO4.5H2O ,乙醇。
湖南工学院
实验步骤
1. 电极制备
(1)铜电极的制备:将铜电极在1∶3的稀硝酸中浸泡片刻,除去氧化物,用水冲洗干净。
以此电极作为负极,另一铜板作正极在镀铜液中电镀(镀铜液组成为:每升中含125gCuSO4.5H2O,25gH2SO4,50mL乙醇),控制电镀的电流为20mA,电镀20min得表面呈红色的Cu电极,洗净后放入0.10 mol.dm-3的CuSO4溶液中备用。
(2)锌电极的制备:将锌电极在稀硫酸溶液中浸泡片刻,除掉锌电极上的氧化层。
取出后用自来水洗涤,再用蒸馏水淋洗,然后浸入饱和硝酸亚汞溶液中
6~10s,取出后用滤纸擦拭锌电极,使锌电极表面上有一层均匀的汞齐,再用蒸馏水洗净(汞有剧毒,用过的滤纸不能乱丢,应放入指定的地方),将洗净后的锌电极插入0.10 mol.dm-3 的ZnSO4溶液中待用。
2.盐桥制备
⑴简易法
用滴管将饱和KNO3(或NH4NO3)溶液注入U型管中,加满后用捻紧的滤纸塞紧U型管两端即可,管中不能存有气泡。
⑵凝胶法
称取琼脂1g放入50mL饱和KNO3溶液中,浸泡片刻,再缓慢加热至沸腾,待琼脂全部溶解后稍冷,将洗净之盐桥管插入琼脂溶液中,从管的上口将溶液吸满(管中不能有气泡),保持此充满状态冷却到室温,即凝固成冻胶固定在管内。
取出擦净备用。
3.电动势测定:
(1).开机5分种后,如果使用"内标"做基准(不用外配的标准电池),就将功能档旋至"内标"位,将最大档"X100V"调至1处,其余各档都调至0处,"补偿"档调至最小。
这等于是给出了1.0000V 的标准,此时按"采零"键,使"检零指示"显示为"-00.00")。
然后将功能档旋到"测量"位,将红线夹接铜电极,黑线夹接锌
湖南工学院
电极(切勿接错了),稳定一段时间后开始测电池:-Pt|H2(g,100kPa)|H+{a(H+) =1}||Cu2+{a(Cu2+)}|Cu+的电动势。
办法是由大档位到小档位依次逼近电动势值(刚开始测量时,"检零指示"档会显示 "QU.L" 或 "**.**", 随着测量值的逼近,绝对值越来越小,但不能为正值),直至"检零指示"档为"00.00"(如最后不为"00.00",则缓缓旋"补偿"档,使"检零指示"刚好显示"00.00"),记录这个时候的读数。
注意,只有原电池真正处于平衡状态,测出的值才会稳定不变。
因此要尽可能使被测电池平稳、不受振动、不含气泡、室内气温恒定。
(2).同样的操作侧电池:-Pt|H2(g,100kPa)|H+{a(H+)=1}||Zn2+{a(Zn2+)}|Zn+的电动势。
(3.控制恒温浴温度为25℃,将电池:
置于恒温浴中恒温 15~20 分钟。
根据要求正确连接好电位差计,重复(1)操作测量250C下的电动势。
同理测定30℃,35℃,40℃,45℃下该电池的电动势。
4.整理仪器。
数据处理
1.计算ΔrGmθ
E/V平均E/V E0/V铜锌电池
ΔrGmθ
E0/V 铜电极
锌电极
湖南工学院
2.计算原电池反应电动势的温度系数(
E
T
∂
∂)P。
温度T/0C2530354045电动势E/V
作图求斜率。
3.用公式(1),(2),(3)计算250C 的rHm
∆,rSm
∆,rGm
∆。
思考题
测定电池反应电动势时,为什么按电位差计的电键应间断而短促?。
