(完整word版)高中化学必修二练习题.doc
(完整word版)高中化学必修二第一章知识点和习题(含答案),推荐文档

第一章物质结构元素周期律一、原子结构质子(Z个)原子核注意:中子(N个)质量数(A)=质子数(Z)+中子数(N)1.原子)原子序数=核电荷数=质子数=原子的核外电子数核外电子(Z个)★熟背前20号元素,熟悉1~20号元素原子核外电子的排布:H He Li Be B C N O F Ne Na Mg Al Si P S Cl Ar K Ca2.原子核外电子的排布规律:①电子总是尽先排布在能量最低的电子层里;②各电子层最多容纳的电子数是2n2;③最外层电子数不超过8个(K层为最外层不超过2个),次外层不超过18个,倒数第三层电子数不超过32个。
电子层:一(能量最低)二三四五六七对应表示符号: K L M N O P Q3.元素、核素、同位素元素:具有相同核电荷数的同一类原子的总称。
核素:具有一定数目的质子和一定数目的中子的一种原子。
同位素:质子数相同而中子数不同的同一元素的不同原子互称为同位素。
(对于原子来说)二、元素周期表1.编排原则:①按原子序数递增的顺序从左到右排列②将电子层数相同......的各元素从左到右排成一横行..。
(周期序数=原子的电子层数)③把最外层电子数相同........的元素按电子层数递增的顺序从上到下排成一纵行..。
主族序数=原子最外层电子数2.结构特点:核外电子层数元素种类第一周期 1 2种元素短周期第二周期 2 8种元素周期第三周期 3 8种元素元(7个横行)第四周期 4 18种元素素(7个周期)第五周期 5 18种元素周长周期第六周期 6 32种元素期第七周期 7 未填满(已有26种元素)表主族:ⅠA~ⅦA共7个主族族副族:ⅢB~ⅦB、ⅠB~ⅡB,共7个副族(18个纵行)第Ⅷ族:三个纵行,位于ⅦB和ⅠB之间(16个族)零族:稀有气体三、元素周期律1.元素周期律:元素的性质(核外电子排布、原子半径、主要化合价、金属性、非金属性)随着核电荷数的递增而呈周期性变化的规律。
元素性质的周期性变化实质是元素原子核外电..........子排布的周期性变化.........的必然结果。
化学必修二测试题及答案

化学必修二测试题及答案一、选择题(每题3分,共30分)1. 下列关于化学反应速率的描述,哪一项是错误的?A. 反应速率与反应物浓度成正比B. 升高温度可以加快反应速率C. 催化剂可以改变反应速率D. 反应速率与反应物的表面积有关2. 在一个封闭的容器中,下列哪种情况不会影响气体的压强?A. 增加气体的量B. 减少容器的体积C. 升高温度D. 降低温度3. 下列关于化学平衡的描述,哪一项是正确的?A. 化学平衡是一个动态平衡B. 化学平衡只受温度的影响C. 在平衡状态下,正逆反应速率相等D. 所有化学反应都会达到平衡状态4. 在下列物质中,哪一种不是电解质?A. 硫酸B. 食盐水C. 铜D. 氢氧化钠5. 下列关于溶液的描述,哪一项是错误的?A. 溶液是均一的混合物B. 溶液的浓度可以用质量分数来表示C. 溶液中的溶质可以是气体、液体或固体D. 饱和溶液比不饱和溶液的浓度一定更高6. 下列关于氧化还原反应的描述,哪一项是错误的?A. 氧化剂在反应中被氧化B. 还原剂在反应中被还原C. 氧化还原反应中一定有电子的转移D. 氧化剂的氧化性比还原剂强7. 下列关于有机化合物的描述,哪一项是正确的?A. 有机化合物只含有碳和氢两种元素B. 有机化合物的熔点通常比无机化合物低C. 所有的有机化合物都能燃烧D. 有机化合物的分子结构通常比无机化合物简单8. 下列关于酸碱性的描述,哪一项是错误的?A. 酸是能够提供氢离子的物质B. 碱是能够提供氢氧根离子的物质C. 酸碱中和反应生成盐和水D. 所有的酸都有腐蚀性9. 下列关于化学键的描述,哪一项是错误的?A. 离子键是由正负离子之间的静电吸引力形成的B. 共价键是通过电子的共享形成的C. 金属键是金属原子之间通过电子云的重叠形成的D. 所有的化学键都是不可断裂的10. 下列关于化学反应中能量变化的描述,哪一项是错误的?A. 放热反应在反应过程中会释放能量B. 吸热反应在反应过程中需要吸收能量C. 反应物的总能量高于产物的总能量时,反应是放热的D. 任何化学反应都伴随着能量的变化二、填空题(每空2分,共20分)11. 化学反应的四种基本类型包括____、____、____和____。
(完整)高中化学必修二第二章习题(含答案),推荐文档
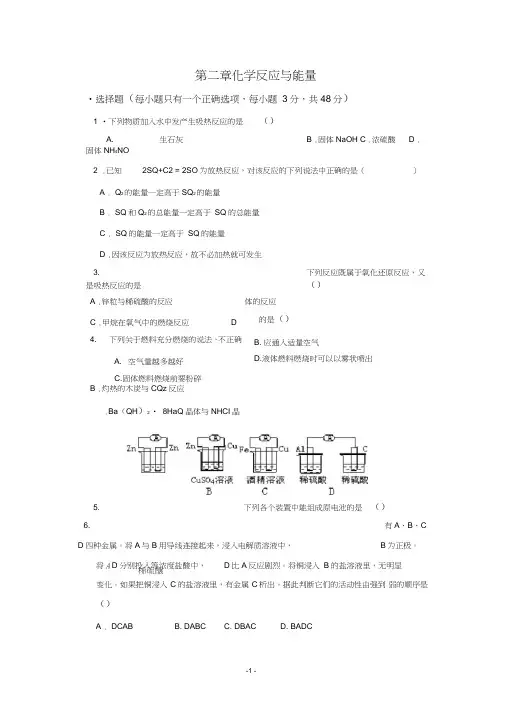
第二章化学反应与能量•选择题(每小题只有一个正确选项,每小题3分,共48分)1 •下列物质加入水中发产生吸热反应的是()A. 生石灰 B .固体NaOH C .浓硫酸 D .固体NH4NO2 .已知2SQ+C2 = 2SO为放热反应,对该反应的下列说法中正确的是()A . Q2的能量一定高于SQ2的能量B . SQ和Q2的总能量一定高于SQ的总能量C . SQ的能量一定高于SQ的能量D .因该反应为放热反应,故不必加热就可发生3. 下列反应既属于氧化还原反应,又是吸热反应的是()A .锌粒与稀硫酸的反应C .甲烷在氧气中的燃烧反应D4. 下列关于燃料充分燃烧的说法,不正确A. 空气量越多越好C.固体燃料燃烧前要粉碎B .灼热的木炭与CQz反应.Ba(QH)2 • 8HaQ晶体与NHCI晶体的反应的是()B. 应通入适量空气D.液体燃料燃烧时可以以雾状喷出5. 下列各个装置中能组成原电池的是()6. 有A、B、C D四种金属。
将A与B用导线连接起来,浸入电解质溶液中,B为正极。
将A D分别投入等浓度盐酸中,D比A反应剧烈。
将铜浸入B的盐溶液里,无明显变化。
如果把铜浸入C的盐溶液里,有金属C析出。
据此判断它们的活动性由强到弱的顺序是()A . DCAB B. DABC C. DBAC D. BADC稀硫醸7. 下列化学电池不易造成环境污染的是()A .氢氧燃料电池B .锌锰电池C .镍镉电池D .铅蓄电池&对于锌一铜一稀酸组成的原电池装置中,当导线中有1 mol电子通过时,理论上的两极变化是()。
①锌片溶解了 32. 5g ②锌片增重32. 5g ③铜片上析出lg H 2④铜片上析出1mol H 2A.①和③B .①和④C .②和③D .②和④9•过量的锌粉与一定量的稀盐酸反应,为了减慢反应速率,但是又不影响生成的氢气 总量,可以采取的措施是 ()A•升高温度B•加入适量的水C .加入少量CuSO 溶液D .加入浓度较大的盐酸10•下列四种盐酸溶液,均能跟锌片反应,其中最初反应速率最快的是 A . 10C 20mL 3mol/L的盐酸溶液B. 20C 30mL 2mol/LC . 20C 20mL 2mol/L 的盐酸溶液D. 20C 10mL 4mol/L11. 一定温度下,可逆反应3X(g)+Y(g) — 2Z(g)达到限度的标志是13. 下列叙述正确的是()A .化学反应除了生成新的物质外,还伴随着能量的变化B .物质燃烧不一定是放热反应C .放热的化学反应不需要加热就能发生D .吸热反应不加热就不会发生 14. 把镁条投入到盛有盐酸的敞口容器中,产生H 2的速率可由 右图表示。
(完整版)高中化学必修2有机化合物试题

《有机化合物》测试题本试卷分第一部分(选择题)和第二部分(非选择题),满分100分。
一、选择题(每小题3分)1.只用水不.能鉴别的一组物质是 A .乙醇和乙酸 B .乙酸乙酯和乙醇C .苯和四氯化碳D .溴水和溴苯2.下列关于有机化合物的说法正确的是A . 和 是两种不同的物质B .由乙烯之间的相互加成可以得到聚乙烯C .丁烷有3种同分异构体D .1mol 乙酸与足量乙醇在浓硫酸催化下加热,可生成1 mol 乙酸乙酯3.下列有机物的命名中,正确的是( )。
A .2,4-二甲基丁烷B .2,3,3-三甲基丁烷C .2-乙基戊烷D .2,3-二甲基戊烷4.下列实验方案不合理的是( )A .鉴定蔗糖水解产物中有葡萄糖:直接在水解液中加入新制Cu(OH)2B .鉴别织物成分是真丝还是人造丝:用灼烧的方法C .鉴定苯中无碳碳双键:加入高锰酸钾酸性溶液D .鉴别己烯和苯:将溴的四氯化碳溶液分别滴加到少量己烯和苯中5.下列各组物质一定互为同系物的是( )①CH 3CH 2OH 和CH 3CH 2CHO②HCOOCH 3和CH 3COOCH 2CH 3③CH 3CH 2OH 和HOCH 2CH 2OH④CH 4和C 18H 38⑤C 2H 4和C 6H 12⑥CH 3OH 和CH 3OCH 3⑦葡萄糖和麦芽糖⑧淀粉(C 6H 10O 5)n 和纤维素(C 6H 10O 5)mA .②③④⑤⑥⑧B .③⑤⑧C .②④D .②④⑤6.下列除去杂质的方法正确的是( )①除去乙烷中少量的乙烯:光照条件下通入Cl 2,气液分离;②除去乙酸乙酯中少量的乙酸:用饱和碳酸氢钠溶液洗涤,分液、干燥、蒸馏; ③除去CO 2中少量的SO 2:气体通过盛饱和碳酸钠溶液的洗气瓶;④除去乙醇中少量的乙酸:加足量生石灰,蒸馏。
A .①②B .②④C .③④D .②③7.只用一种试剂就可以鉴别乙酸溶液、葡萄糖溶液、乙醇,这种试剂是( )A .NaOH 溶液B .新制的Cu(OH)2悬浊液C .石蕊试液D .Na 2CO 3溶液8.下列反应中属于加成反应的是( )A .乙烯使酸性KMnO 4溶液褪色Cl —C —Cl H HCl —C —H Cl HB.将苯滴入溴水中,振荡后水层接近无色C.乙烯使溴水褪色D.甲烷与氯气混合,黄绿色消失9.巴豆酸的结构简式为CH3—CH==CH—COOH。
高中化学必修二试题及答案

高中化学必修二试题及答案一、选择题(每题2分,共20分)1. 下列物质属于纯净物的是:A. 空气B. 矿泉水C. 蒸馏水D. 果汁2. 化学反应中,能量变化的类型不包括:A. 放热反应B. 吸热反应C. 光能反应D. 电能反应3. 根据化学方程式2H2 + O2 → 2H2O,若生成3mol水,需要消耗氢气的物质的量是:A. 1molB. 2molC. 3molD. 6mol4. 原子核外电子排布遵循的规则是:A. 能量最低原理B. 洪特规则C. 泡利不相容原理D. 所有上述规则5. 下列物质中,不属于电解质的是:A. 氯化钠B. 硫酸C. 酒精D. 氢氧化钠二、填空题(每空1分,共10分)1. 化学平衡常数K的表达式为 _________。
2. 氧化还原反应中,氧化剂被还原,其氧化态 _________。
3. 根据阿伏伽德罗定律,1摩尔任何气体在标准状况下的体积是_________。
4. 金属晶体中,金属原子通过 _________ 键连接。
5. 酸碱中和反应的实质是 _________。
三、简答题(每题10分,共20分)1. 简述什么是化学平衡以及影响化学平衡的因素。
2. 描述原子结构中的电子排布规律。
四、计算题(每题15分,共30分)1. 某工厂排放的废气中含有0.5%的SO2,若排放量为1000立方米/小时,求每小时排放的SO2的质量。
2. 将一定量的NaOH溶液与盐酸反应,已知NaOH的浓度为0.1mol/L,体积为50mL,求反应后溶液的pH值。
五、实验题(共20分)1. 描述如何使用滴定法测定溶液中HCl的浓度,并说明实验中应注意的事项。
答案:一、选择题1. C2. D3. B4. D5. C二、填空题1. K = [C]^c[D]^d/[A]^a[B]^b2. 降低3. 22.4L4. 金属5. 氢离子与氢氧根离子结合生成水三、简答题1. 化学平衡是指在一个封闭系统中,正反应和逆反应同时进行,且速率相等,系统宏观性质不发生变化的状态。
高中化学必修二习题附答案

高中化学必修二习题附答案第一章化学反应和能量选择题1. 燃烧甲烷的反应式为(CH_4+2O_2→CO_2+2H_2O),该反应的氧化数变化是:A. 炭和氧的氧化数都是0B. 炭的氧化数从-4变为+4,氧的氧化数从0变为-2C. 炭的氧化数从+4变为-4,氧的氧化数从0变为+2D. 炭和氧的氧化数都是-2答案:B2. 下列物质中能够与氧气反应的是:A. 氢气B. 二氧化碳C. 氨水D. 乙醇答案:D3. 化学反应放热时能量的变化是:A. 化学能转化为热能,温度升高B. 热能转化为化学能,温度降低C. 化学能转化为电能,电流流过D. 化学能转化为机械能,物体运动答案:A4. 已知化学反应的物质量,求该反应所放出的热量需要知道的是:A. 晶格能B. 成键能C. 热容量D. 反应热答案:D5. 同一量的物质参与不同化学反应时,这些反应所释放的能量:A. 相同B. 不同C. 可能相同也可能不同,要根据反应类型及物质性质而定D. 不确定答案:C6. 摩尔反应热的单位是:A. J/gB. J/LC. kJ/molD. kJ/L答案:C7. 摩尔反应热的符号正负表示反应放热或吸热,以下符号代表放热的反应是:A. ΔH>0B. ΔH<0C. ΔH=0D. ΔH没有符号答案:B8. 化学反应的焓变可以根据:A. 物质的量B. 参与反应的化学物质C. 组成物质的元素种类和数量D. 以上三种方法的组合答案:A9. 实验测量可燃气体燃烧的焓变时,其测量原则为:A. 直接燃烧法B. 间接计算法C. 直接计算法D. 间接燃烧法答案:D10. 一些物质在燃烧时所放出的总能量,不能完全被转化为功,部分能量被转化为:A. 电能B. 化学能C. 热能D. 动能答案:C填空题1. 化学反应类型中,按符号表示元素和离子的能力从右至左依次增强的顺序是_____________。
答案:共价→极性共价→离子型2. 某化学反应的热效应为-150kJ,说明该反应为________。
高中化学必修2试题及答案
高中化学必修2试题及答案一、选择题(每题2分,共20分)1. 下列物质中,属于纯净物的是:A. 空气B. 矿泉水C. 蒸馏水D. 果汁2. 化学反应中,能量变化通常表现为:A. 电能B. 热能C. 光能D. 机械能3. 根据元素周期表,下列元素中原子半径最大的是:A. 氢B. 氧C. 钠D. 氯4. 一个化学反应的平衡常数表达式为K,当温度升高时,如果K值增大,该反应是:A. 吸热反应B. 放热反应C. 不变反应D. 无法判断5. 根据化学键理论,下列物质中属于离子化合物的是:A. 氧气B. 氢气C. 氯化钠D. 二氧化碳二、填空题(每空2分,共20分)6. 化学方程式2H2 + O2 → 2H2O 中,反应物和生成物的摩尔比是__________。
7. 原子序数为11的元素是 __________。
8. 根据酸碱中和反应原理,盐酸与氢氧化钠反应生成 __________ 和__________。
9. 元素周期表中,第IA族元素的特点是 __________。
10. 根据氧化还原反应的原理,氧化剂在反应中 __________。
三、简答题(每题10分,共20分)11. 请简述什么是氧化还原反应,并给出一个例子。
12. 请解释什么是化学平衡,并说明影响化学平衡的因素。
四、计算题(每题15分,共30分)13. 某化学反应的初始浓度为A=0.1M,B=0.2M,反应速率常数k=0.05s^-1。
如果反应进行10秒后,求A的浓度。
14. 给定一个酸碱中和反应,已知酸的浓度为0.01M,碱的浓度为0.02M,反应后溶液的pH值为9。
求酸和碱的摩尔比。
五、实验题(10分)15. 设计一个实验来验证质量守恒定律。
答案:一、选择题1. C2. B3. C4. A5. C二、填空题6. 1:1:27. 钠(Na)8. 氯化钠(NaCl)和水(H2O)9. 最外层电子数为110. 被还原三、简答题11. 氧化还原反应是指在化学反应中,物质之间发生电子转移的过程。
高中同步测试卷·人教化学必修2:高中同步测试卷(二) Word版含答案
高中同步测试卷(二)集训2元素周期律(时间:90分钟,满分:100分)一、选择题(本题包括16小题,每小题只有一个选项符合题意,共48分)1.某元素原子的最外层电子数为次外层电子数的3倍,则该元素原子核内质子数为() A.3 B.7C.8 D.102.核电荷数为16的元素和核电荷数为4的元素的原子相比较,前者的下列数据是后者的4倍的是()①电子数②最外层电子数③电子层数④次外层电子数A.①④B.①③④C.①②④D.①②③④3.某元素原子的最外层电子数是次外层的a倍(a>1),则该原子的核内质子数是() A.2a+2 B.2a+10C.a+2 D.2a4.如图是一块非常独特的手表,用H~Mg 12种元素分别表示1:00~12:00,关于此表的下列说法中不正确的是()A.2:00时的时针和12:00时的分针所指元素极难形成化合物B.7:00时,时针和分针所指元素可能形成相对分子质量为100的化合物C.8:00时,时针和分针所指元素形成的氧化物属于碱性氧化物D.3:00时,时针所指元素的金属性比11:00时时针所指元素的金属性强5.下列选项与Li<Na<K<Rb<Cs的变化规律不相符的是()A.与水或酸作用置换出氢气的反应程度越来越剧烈B.对应元素的金属性由弱到强C.对应金属阳离子的氧化性由弱到强D.原子半径由小到大6.某主族元素R的最高正化合价与最低负化合价的代数和为4,由此可以判断() A.R一定是第四周期元素B.R一定是第ⅣA族元素C.R的气态氢化物比同周期其他元素气态氢化物稳定D.R气态氢化物化学式为H2R7.如图是M、N两种主族元素的原子结构示意图,下列说法正确的是()A.M位于第五周期Ⅶ族B.N位于IA族,该主族中的元素又称为碱金属元素C.N在空气中燃烧,生成化学式为N2O的氧化物D.M所在的主族中各元素是同周期元素中非金属性最强的元素8.下列事实不能作为实验判断依据的是()A.钠和镁分别与冷水反应,判断金属活动性强弱B.铁投入CuSO4溶液中,能置换出铜,钠投入CuSO4溶液中不能置换出铜,判断钠与铁的金属活动性强弱C.酸性H2CO3<H2SO4,判断硫与碳的非金属性强弱D.F2、Cl2分别与H2反应,判断氟与氯的非金属性强弱9.W、X、Y、Z四种元素是原子序数依次增大的短周期元素,已知:(1)四种元素的电子层数之和等于10,且它们分属于连续的四个主族;(2)四种元素的原子中半径最大的是X原子。
化学必修2试题及答案
化学必修2试题及答案一、选择题(每题3分,共30分)1. 下列物质中,属于混合物的是:A. 氧气B. 蒸馏水C. 空气D. 纯碱答案:C2. 元素周期表中,第IA族元素的原子最外层电子数为:A. 1B. 2C. 3D. 4答案:A3. 根据质量守恒定律,化学反应前后不变的是:A. 元素种类B. 物质种类C. 分子种类D. 分子个数答案:A4. 下列化合物中,属于共价化合物的是:A. NaClB. CaOC. HClD. MgO答案:C5. 金属活动性顺序中,位于氢前面的金属能与酸反应生成氢气,这是因为:A. 金属的还原性B. 金属的氧化性C. 金属的导电性D. 金属的延展性答案:A6. 在化学反应中,氧化剂和还原剂的关系是:A. 氧化剂被还原,还原剂被氧化B. 氧化剂被氧化,还原剂被还原C. 氧化剂和还原剂都被氧化D. 氧化剂和还原剂都被还原答案:A7. 根据酸碱中和反应的实质,下列说法正确的是:A. 酸的氢离子和碱的氢氧根离子结合生成水B. 酸的氢离子和碱的氢氧根离子结合生成盐C. 酸的氢离子和碱的氢氧根离子结合生成水和盐D. 酸的氢离子和碱的氢氧根离子结合生成氢气答案:C8. 下列物质中,属于电解质的是:A. 酒精B. 蔗糖C. 硫酸D. 石墨答案:C9. 根据化学反应速率的定义,下列说法错误的是:A. 反应速率与反应物浓度有关B. 反应速率与反应物表面积有关C. 反应速率与反应物的量无关D. 反应速率与反应物的接触面积有关答案:C10. 根据原子结构,下列说法正确的是:A. 原子核中的质子数等于核外电子数B. 原子核中的质子数等于核外中子数C. 原子核中的质子数小于核外电子数D. 原子核中的质子数大于核外电子数答案:A二、填空题(每题2分,共20分)1. 元素周期表中,第VIIA族元素的原子最外层电子数是______。
答案:72. 根据元素周期律,原子序数越大,原子半径越______。
答案:小3. 金属钠与水反应生成氢气和______。
必修2化学测试题及答案
必修2化学测试题及答案一、选择题(每题2分,共20分)1. 下列物质中,属于混合物的是()A. 氧气B. 蒸馏水C. 空气D. 酒精答案:C2. 根据质量守恒定律,化学反应前后不变的是()A. 元素种类B. 分子种类C. 原子种类D. 分子数目答案:A3. 下列物质中,属于化合物的是()A. 氧气B. 蒸馏水C. 氢气D. 酒精答案:B4. 根据化学方程式2H2 + O2 → 2H2O,下列说法正确的是()A. 氢气和氧气反应生成水B. 氢气和氧气反应生成氧气C. 氢气和氧气反应生成氢气D. 氢气和氧气反应生成二氧化碳答案:A5. 下列物质中,属于单质的是()A. 氧气B. 蒸馏水C. 空气D. 酒精答案:A6. 根据化学方程式Fe + CuSO4 → FeSO4 + Cu,下列说法正确的是()A. 铁和硫酸铜反应生成硫酸亚铁和铜B. 铁和硫酸铜反应生成硫酸亚铁和银C. 铁和硫酸铜反应生成硫酸亚铁和金D. 铁和硫酸铜反应生成硫酸亚铁和锌答案:A7. 下列物质中,属于氧化物的是()A. 氧气B. 蒸馏水C. 氢气D. 酒精答案:B8. 根据化学方程式2H2O → 2H2 + O2,下列说法正确的是()A. 水分解生成氢气和氧气B. 水分解生成氢气和二氧化碳C. 水分解生成氧气和二氧化碳D. 水分解生成氢气和氮气答案:A9. 下列物质中,属于酸的是()A. 盐酸B. 氢氧化钠C. 硫酸钠D. 碳酸钠答案:A10. 下列物质中,属于碱的是()A. 盐酸B. 氢氧化钠C. 硫酸钠D. 碳酸钠答案:B二、填空题(每题2分,共20分)1. 根据原子的构成,原子核由____和____组成。
答案:质子;中子2. 元素周期表中,元素的排列顺序是按照原子的____排列的。
答案:原子序数3. 化学方程式2H2 + O2 → 2H2O表示的意义是____。
答案:氢气和氧气反应生成水4. 根据化学方程式Fe + CuSO4 → FeSO4 + Cu,铁在反应中表现出____性。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
1.根据元素在周期表中的位置判断,下列元素中原子半径最小的是A .氧B .氟C .碳D . 氮2. X 元素最高氧化物对应的水化物为 H 3XO 4,则它对应的气态氢化物为A . HXB . H 2XC . XH 4D . XH 33.医学研究证明,用放射性135135 53 I治疗肿瘤可收到一定疗效,下列有关53 I叙述正确的是 135 I 是碘的一种同素异形体B . 135I 是一种新发现的元素A . 53 53 135I 位于元素周期表中第135I 核内的中子数与核外电子数之差为29C . 53 4 周期Ⅶ A 族D . 5334.下列关于 2 He 的说法正确的是3He 原子核内含有 2 个中子3He 原子核内含有 3 个质子A . 2B .2 3He 原子核外有 3 个电子34C . 2D . 2 He 和 2 He 是两种不同的核素5.下列有关元素周期律的叙述中,正确的是A .氧化性强弱: F 2< Cl 2B .金属性强弱: K < NaC .酸性强弱: H 3PO 4< H 2SO 4D .碱性强弱: NaOH < Mg(OH) 26. X 、 Y 、 Z 为短周期元素,这些元素原子的最外层电子数分别为 1、 4、 6,则由这三种元素组成的化合物的化学式可能是A . XYZB . X 3YZC . XYZ 2D . X 2YZ 37.下列关于元素周期表的说法正确的是A .能生成碱的金属元素都在Ⅰ A 族B .原子序数为 14 的元素位于元素周期表的第 3 周期Ⅳ A 族C .稀有气体元素原子的最外层电子数均为8D .第二周期Ⅳ A 族元素的原子核电荷数和中子数一定为68.已知同周期 X 、 Y 、 Z 三种元素的最高价氧化物对应水化物酸性由强到弱的顺序为HXO 4>2YO 434H > H ZO ,则下列判断中正确的是A .元素非金属性按 X 、Y 、Z 的顺序减弱B .阴离子的还原性按 X 、Y 、Z 的顺序减弱C .气态氢化物的稳定性按X 、Y 、 Z 的顺序增强 D .单质的氧化性按 X 、 Y 、 Z 的顺序增强9.下列关于Ⅶ A 族元素的叙述正确的是A .Ⅶ A 族元素是同周期中原子半径最大的元素B .Ⅶ A 族元素是同周期中非金属性最弱的元素C .Ⅶ A 族元素的最高正价都是+7 价D .Ⅶ A 族元素其简单阴离子的核外电子层数等于该元素所在的周期数10.元素性质呈周期性变化的决定因素是A .元素原子半径大小呈周期性变化B .元素相对原子质量依次递增C .元素原子最外层电子排布呈周期性变化D .元素的最高正化合价呈周期性变化11.下列各组元素性质递变情况错误..的是A . Li 、 Be 、B 原子最外层电子数逐渐增多 B . N 、 O 、 F 原子半径依次增大C . P 、 S 、 Cl 最高正价依次升高D . Li 、 Na 、 K 、 Rb 的金属性依次增强12.雷雨天闪电时空气中有臭氧(O 3 )生成,下列说法正确的是 A . O 2 和 O 3 互为同位素B . O 2 和 O 3 的相互转化是化学变化C . O 3 是由 3 个氧原子构成的化合物D .等物质的量 O 2 和 O 3 含有相同的质子数13.含硒( Se )的保健品已开始进入市场。
已知硒与氧、硫同主族,与溴同周期,则下列关于硒的叙述中,正确的是A .非金属性比硫强B .氢化物比 HBr 稳定C .原子序数为 34D .最高价氧化物的水化物显碱性14.已知质量为数为n+A 的某阳离子 R , 核外有 X 个电子,则核内中子数为 A . A-x B. A-x-n C . A-x+n D .A+x-n 15. 对于 Z AX 和A+1ZX + 两种粒子,下列叙述正确的是 A .质子数一定相同,质量数和中子数一定不同 B .化学性质几乎相同C .一定都由质子、中子、电子构成D .核电荷数,核外电子数一定相同16、某粒子含有 6个质子, 7个中子,电荷为 0,则它的化学符号是 CA . 13AlB .13C . 13 CD . 13 CAl 17、对于AA+1 +ZX 和 Z X 两种粒子,下列叙述正确的是A .质子数一定相同,质量数和中子数一定不同B .化学性质及乎相同C .一定都由质子、中子、电子构成D.核电荷数,核外电子数一定相同18、下列叙述中错误的是AA .原子半径: Cl>S>OB .还原性: Na>Mg>AlC .稳定性: HF>HCl>HBrD.酸性: HClO>H SO>H PO4243419、下列各组元素性质递变情况错误的是BA . Li 、 Be 、B 原子最外层电子 数逐渐增多 B . N 、 O 、 F 原子半径依次增大C . P 、 S 、Cl 最高正价依次升高D. Li 、 Za 、 K 、 Rb 的金属性依次增强1820、 H 2 O 和D 2 O 分子中的中子数,前者和后者的关系是A .大于B.小于C .等于D.无法确定21、 X 元素的阳离子与 Y 元素的阴离子具有相同的电子层结构,下列叙述正确的是A .原子序数 X<YB .原子半径 X<YC .离子半径 X>YD.原子最外层电子数X 〈 Y22、某元素 X 气态氢化物与该元素最高价氧化物的水化物反应生成盐,则该元素:A .在周期表中处于第三周期Ⅶ A 族, B.在周期表中处于第2 周期Ⅴ A 族C .氢化物比 PH 3 稳定D.常见化合价只有 -3 、 +2、 +3、 +5 价23、一些科学家预言,存在稳定的超重元素,如: Z=114, N=184 的原子,它位于元素周期表的第7周期,第Ⅳ A 族,下列说法正确的是A .第七周期有 50种元素B.该原子的质量数为 184C .该元素的相对原子质量为 292D .该原子核外有 114个电子24、某元素 X 气态氢化物与该元素最高价氧化物的水化物反应生成盐,则该元素:A .在周期表中处于第三周期ⅦA 族,B .在周期表中处于第 2 周期Ⅴ A 族C .氢化物比 3D.常见化合价只有 -3 、+2、 +3、 +5 价PH 稳定25. 元素的下列性质,随原子序数的递增不是周期性变化的是( )A. 相对原子质量B.化合价C. 原子半径D. 元素的化学性质26. 元素性质呈周期性变化的决定因素是 ( )A. 元素原子半径大小呈周期性变化B.元素原子量依次递增C. 元素原子最外层电子排布呈周期性变化D. 元素的最高正化合价呈周期性变化27. 下列各组中的性质比较中,不正确的是()44 422> Mg ( OH )2A 酸性 HClO > HBrO > HIOB 碱性 Ba ( OH ) > Ca (OH )- --C 还原性 F > Cl >BrD2 3稳定性 HCl > H S > PH28. 可用来判断金属性强弱的依据是( )A 、原子电子层数的多少B、最外层电子数的多少C 、最高价氧化物的水化物的碱性强弱D 、等物质的量的金属置换氢气的多少29. 同一周期 X 、 Y 、 Z 三种元素,已知最高价氧化物对应水化物的酸性是42434HXO>H YO>HZO ,则下列判断错误的是 ( )A 、原子半径 X>Y>ZB、气态氢化物的稳定性23HX>HY>ZHC 、非金属性 X>Y>Z D、阴离子的还原性 3-2--Z >Y >X 30. 按 C 、 N 、 O 、F 顺序下列性质递增的是( )A 、最高化合价B 、非金属性C 、电子层数D 、原子半径 31.( 14 分)下表是元素周期表的一部分,针对表中的①~⑩中元素,用元素符号或化学式 填空回答以........下问题:主族IAIIAIIIAIVA VAVIAVIIA0 周期二①②三 ③ ④⑤⑥⑦ ⑧四⑨⑩( 1)在这些元素中,金属性最强的元素是,最活泼的非金属元素是; ( 2)化学性质最不活泼的元素是,其原子的原子结构示意图为;( 3)元素的最高价氧化物对应的水化物中酸性最强的是 ,碱性最强的是,呈两性的氢氧化物是;( 4)在③~⑦元素中,原子半径最大的是,原子半径最小的是;( 5)在⑦与⑩的单质中,化学性质较活泼的是,可用什么化学反应说明该事实(写出反应的化学方程式) :。
32.( 14 分) A 、B 、 C 、 D 、E 为原子序数依次增大的短周期元素,已知 A 、B 、 E 3 种原子最外层共有 11 个电子,且这 3 种元素的最高价氧化物的水化物两两皆能发生反应生成盐和水,C 元素的最外层电子数比次外层电子数少4, D 元素原子次外层电子数比最外层电子数多 3。
( 1)写出下列元素符号:A ,B ,C ,D ,E ( 2)写出 A 、 B 两元素相互反应的化学方程式:。
( 3)比较 C 、 D 的最高价氧化物的水化物的酸性:(用化学式表示)。
33.(12 分) A 、 B 、 C 、 D 四种元素,原子序数依次增大,A 原子的最外层上有 4 个电子;B 的阴离子和 C 的阳离子具有相同的电子层结构,两元素的单质反应, 生成一种淡黄色的固体E ,D 的 L层电子数等于 K 、 M 两个电子层上的电子数之和。
( 1)A 为,B 为 , C 为 。
D 的最高价氧化物的水化物是 。
( 2)写出 A 、 B 的化合物与 E 反应的化学方程式:。
( 3) A 、 B 两元素形成化合物属( “离子 ”或 “共价 ”)化合物。
( 4)写出 D 的最高价氧化物的水化物和A 反应的化学方程式:。
34、(9分)在第 3周期中,置换酸中氢的能力最强的元素的元素符号为,化学性质最稳定的元素符号是,最高价氧化物的水化物的酸性最强的化合物的化学式是,碱性最强的化合物的化学式是,显两性的氢氧化物的化学式是,该两性氢氧化物与盐酸、氢氧钠溶液分别反应的离子方程式为、,原子半径最大的金属元素的名称是 ,离子半径最小的离子结构示意图是( 2) Ar ,(各1分)( 3) HClO 4, KOH , Al(OH) 3 (各 1 分)( 4) Na, Cl (各 1 分)( 5) Cl 2( 2 分), 2NaBr +Cl 2= 2NaCl + Br 2(3 分)17.( 14 分)( 1) A : Na, B: Al , C: Si, D: P, E : Cl (各 2 分,共 10 分)( 2) Al(OH) 3+ NaOH === NaAlO 2+2H 2O ( 2 分)( 3) H 3PO 4> H 2SiO3 ( 2 分)18.( 12 分)( 1) C(碳), O(氧), Na(钠)(各 1 分)( 2) 2Na2O 2+ CO2= 2Na2CO 3+ O 2 ( 3 分)( 3)共价( 2 分)( 4) C+ 2H 2SO4 (浓 ) △(4 分)CO2↑+ 2SO2↑+ 2H 2O鲁科版必修 2 第一章《原子结构与元素周期律》测试题参考答案一、选择题(每小题 4 分,每小题只有 1 个选项符合题意,15 题,共60 分。
