高中化学中的有色物质和有色离子
高中化学有色物质大全

物质的颜色一、红色1、Li 的焰色:紫红色(用于元素锂元素存在的检验)2、Ca 的焰色:砖红色(用于元素钙元素存在的检验)3、Sr 的焰色:洋红色(用于元素锶元素存在的检验)4、固体铜:红色(有金属光泽)5、红磷:暗红色6、液溴:深红棕色(水溶液为橙色,蒸汽为红棕色)7、氧化铁粉末:红棕色(通常用作颜料,俗称铁红)8、氢氧化铁胶体或沉淀:红褐色(通常用来检验Fe2、Fe3的存在)9、氧化亚铜沉淀:砖红色(用于检验有机物中醛基的存在)10、二氧化氮气体:红棕色11、Fe3+溶液中加入SCN-:棕色溶液变成血红色(用来检验Fe3的存在)12、碱性溶液中滴入酚酞溶液:溶液变红色13、酸性溶液中滴入石蕊试液:溶液变红色二、黄色1、Au:金黄色(有金属光泽)2、Na 的焰色:黄色(用于检验Na 元素的存在)3、白磷:黄色或白色4、硫固体:淡黄色晶体5、AgBr:淡黄色(不溶于稀硝酸,用于检验溴离子的存在)6、AgI:黄色(不溶于稀硝酸,用于检验碘离子的存在)7、Ag3PO4:黄色(溶于稀硝酸)8、Na2O2:淡黄色固体(用于潜水艇中的制氧气)9、Fe3的溶液:棕黄色10、工业盐酸:因含有Fe3而显黄色11、浓硝酸:因长久放置分解出NO2 而显黄色12、鸡蛋白溶液:遇浓硝酸而变黄色三、绿色1、Cu 的焰色:绿色(用于检验铜元素的存在)2、Ba 的焰色:黄绿色(用于检验钡元素的存在)3、白磷自燃:绿色(俗称鬼火)4、FeSO47H2O:绿色(俗称绿矾)5、CuOH2CO3:绿色(铜锈)6、氯气:黄绿色气体7、氯水:黄绿色8、氟气:淡黄绿色气体9、Fe 溶液:浅绿色四、蓝色:淡蓝色1、O2(液态或固态)2、CuSO45H2O 晶体:蓝色(俗称蓝矾,又叫胆矾)3、Cu(OH)2 沉淀:蓝色4、CuSO4 溶液:蓝色5、CuCl2 溶液:蓝绿色(与溶液浓度有关)6、CO 在空气中燃烧:蓝色火焰7、H2、H2S、CH4、C2H5OH、S 在空气中燃烧:淡蓝色火焰8、淀粉遇上I2:变蓝色9、葡萄糖溶液中加入氢氧化铜悬浊液:变成绛蓝色溶液(若加热煮沸则生成砖红色沉淀Cu2O)10、碱性溶液中加入石蕊试液:变蓝色11、湿润的红色石蕊试纸遇氨气变蓝色12、白色的碘化钾淀粉试纸:遇氧化性物质变蓝色(如H2O2、Cl2、NO2 等)五、紫色1、I2 固体:紫黑色(有金属光泽)2、I2 蒸汽:紫色3、I2 的CCl4 溶液或苯溶液:紫红色(I2 水呈褐色)4、KMnO4 溶液:紫色或紫红色5、石蕊试液:紫色6、苯酚溶液中滴加FeCl3 溶液:变紫色7、K 的焰色:紫色(透过蓝色钴玻璃,用于检验钾元素的存在)8、Rb(铷)的焰色:紫色(用于检验铷元素的存在)六、白色1、大多数金属固体都是银白色(铯略带金色光泽)2、AgCl:白色沉淀(不溶于稀硝酸,用于检验氯离子的存在)3、BaSO4:白色沉淀(不溶于稀硝酸,用于检验钡离子或硫酸根离子的存在)4、Fe(OH)2:白色絮状沉淀(接触空气后迅速变为灰绿色,最后变为红褐色氢氧化铁,可用于检验Fe2的存在)5、澄清石灰水中通入过量的CO2 或SO2:先出现白色浑浊,后又澄清。
高中化学的知识点口诀

高中化学的知识点口诀高中化学必备的知识点口诀其实学习高中的化学知识也是有技巧的,特别是在记忆知识点时候,我们可以利用口诀来记忆,非常方便有效。
下面是店铺为大家整理的高中化学必备的知识,希望对大家有用!高中化学知识口诀(1)常见元素的主要化合价:氟氯溴碘负一价;正一氢银与钾钠。
氧的负二先记清;正二镁钙钡和锌。
正三是铝正四硅;下面再把变价归。
全部金属是正价;一二铜来二三铁。
锰正二四与六七;碳的二四要牢记。
非金属负主正不齐;氯的负一正一五七。
氮磷负三与正五;不同磷三氮二四。
有负二正四六;边记边用就会熟。
一价氢氯钾钠银;二价氧钙钡镁锌,三铝四硅五氮磷;二三铁二四碳,二四六硫都齐;全铜以二价最常见。
(2)常见根价的化合价一价铵根硝酸根;氢卤酸根氢氧根。
高锰酸根氯酸根;高氯酸根醋酸根。
二价硫酸碳酸根;氢硫酸根锰酸根。
暂记铵根为正价;负三有个磷酸根。
高中化学重点知识颜色铁:铁粉是黑色的;一整块的固体铁是银白色的。
Fe2+——浅绿色 Fe3O4——黑色晶体 Fe(OH)2——白色沉淀Fe3+——黄色 Fe (OH)3——红褐色沉淀 Fe (SCN)3——血红色溶液FeO——黑色的粉末 Fe (NH4)2(SO4)2——淡蓝绿色Fe2O3——红棕色粉末铜:单质是紫红色Cu2+——蓝色 CuO——黑色 Cu2O——红色 CuSO4(无水)—白色CuSO4·5H2O——蓝色 Cu2(OH)2CO3 —绿色Cu (OH)2——蓝色 [Cu(NH3)4]SO4——深蓝色溶液FeS——黑色固体BaSO4 、BaCO3 、Ag2CO3 、CaCO3 、AgCl 、 Mg (OH)2 、三溴苯酚均是白色沉淀Al(OH)3 白色絮状沉淀 H4SiO4(原硅酸)白色胶状沉淀Cl2、氯水——黄绿色F2——淡黄绿色气体Br2——深红棕色液体I2——紫黑色固体HF、HCl、HBr、HI均为无色气体,在空气中均形成白雾CCl4——无色的液体,密度大于水,与水不互溶Na2O2—淡黄色固体 Ag3PO4—黄色沉淀 S—黄色固体 AgBr—浅黄色沉淀AgI—黄色沉淀 O3—淡蓝色气体 SO2—无色,有剌激性气味、有毒的气体SO3—无色固体(沸点44.8度) 品红溶液——红色氢氟酸:HF——腐蚀玻璃N2O4、NO——无色气体 NO2——红棕色气体NH3——无色、有剌激性气味气体高中化学易错知识常错点1 错误地认为酸性氧化物一定是非金属氧化物,非金属氧化物一定是酸性氧化物,金属氧化物一定是碱性氧化物。
高中化学常见物质颜色和状态

高中化学常见物质的颜色和状态1、黑色固体:石墨、炭粉、铁粉、FeS、CuS、CuO、MnO2、Fe3O42、红色固体:Cu、Cu2O、Fe2O3、HgO、红磷3、淡黄色固体:S、 Na2O2、 AgBr4.紫黑色固体:KMnO4、5、黄色固体: AgI 、Ag3PO46、绿色固体: Cu2(OH)2CO37、蓝色晶体:CuSO4·5H2O8 、蓝色沉淀 Cu(OH)29、红褐色沉淀: Fe(OH)310、白色固体:MgO、P2O5、CaO、 NaOH、Ca(OH)2、KClO3、KCl、Na2CO3、NaCl、无水CuSO4;铁、镁为银白色(汞为银白色液态)11、溶液的颜色:凡含Cu2+的溶液呈蓝色;凡含Fe2+的溶液呈浅绿色;凡含Fe3+的溶液呈棕黄色,MnO4-溶液为紫红色,其余溶液一般无色。
12、不溶于酸的白色沉淀: BaSO4 、AgCl13、不溶于水的白色沉淀 CaCO3 (溶于酸)、BaCO3(溶于酸)、Al(OH)3、 Mg(OH)2 等14、(1)具有刺激性气体的气体:NH3、SO2、HCl(皆为无色(2)无色无味的气体:O2、H2、N2、CO2、CH4、CO(剧毒)(3) 红棕色气体: Br2(气体) NO2(4)黄绿色气体:Cl2(5)臭鸡蛋气味气体:H2S15、具有刺激性气味的液体:盐酸、硝酸、醋酸、酒精16、有毒的: 气体:CO SO2 H2S 液体:CH3OH 固体:NaNO2 CuSO4(可作杀菌剂 ,与熟石灰混合配成天蓝色的粘稠状物质——波尔多液)中学常见物质颜色归纳2、单质化学式颜色化学式颜色化学式颜色Cu 紫红 Au 黄 S 黄B 黄或黑 F2 淡黄绿 C(石墨)黑Cl2 黄 Br2 红棕 C(金刚石)无Si 灰黑 I2紫黑 P 白、黄、红棕3、氧化物化学式颜色化学式颜色化学式颜色NO2 棕红 ClO2 黄 Na2O2 浅黄K2O 黄 Pb3O4 红 MnO 绿化学式颜色化学式颜色化学式颜色CuO 黑 MnO2 黑 Ag2O 棕黑FeO 黑 ZnO 白 Fe3O4 黑Hg2O 黑 Fe2O3 红棕 HgO 红或黄Cu2O 红4、氧化物的水化物化学式颜色化学式颜色化学式颜色Fe(OH)3 红褐 HNO2 亮蓝 Cu(OH)2 蓝5、盐化学式颜色化学式颜色化学式颜色CuFeS2 黄 ZnS 白 Ag2S 黑FeS 黑棕 FeS2 黄 Sb2S3 黑或橙红HgS 红 PbS 黑 CuS 黑Cu2S 黑 FeCl3·6H2O 棕黄 FeSO4 9H20 蓝绿Fe2(SO4)3.9H2O 棕黄 Fe3C 灰 FeCO3 灰Ag2CO3 黄 Ag3PO4 黄 CuCl2 棕黄AgF 黄 CuCl2 7H2O 蓝绿 AgCl 白CuSO4 白 AgBr 浅黄 CuSO4 5H2O 蓝AgI 黄 Cu2(OH2)CO3 暗绿6、盐溶液中离子特色:化学式颜色化学式颜色化学式颜色Cu2+ 蓝 MnO4-紫红 [CuCl4]2- 黄Cr2O72- 橙红 Fe2+ 浅绿 Fe3+ 棕黄7、非金属互化物物质颜色物质颜色物质颜色氯水黄绿溴水黄-橙碘水黄褐溴的有机溶液橙红-红棕 I2的有机溶液紫红8、其它:蛋白质遇浓变黄、遇淀粉变蓝、 TNT 淡黄、遇酚酞溶液变紫黄色:AgI、Ag3PO4、P4(黄磷)、溴水(黄--橙)、FeS2、Al2S3、甲基橙在弱酸性、中性或碱性环境中、某些蛋白质加硝酸。
高中化学有色物质大全

高中化学有色物质大全高中化学中,有色物质是一个重要的研究对象。
有色物质广泛存在于我们的生活和实验室中,对于理解物质的性质和应用具有重要意义。
本文将为大家介绍一些常见的有色物质及其相关知识。
1. 金属离子溶液金属离子溶液是实验中常见的有色物质。
当某些金属离子溶解在水中时,其溶液会呈现出特定的颜色。
例如,铁离子溶液呈现出淡黄色,铜离子溶液呈现出蓝色,铬离子溶液呈现出绿色等。
这些颜色是由金属离子的电子跃迁引起的,不同金属离子的电子跃迁能级不同,因而呈现出不同的颜色。
2. 过渡金属络合物过渡金属络合物是一类常见的有色物质。
过渡金属离子在与配体形成络合物后,其电子转移发生变化,从而导致溶液呈现出不同的颜色。
例如,铜离子与氨水(NH3)形成四氨合铜离子(Cu(NH3)4²⁺)的络合物,呈现出深蓝色。
这是由于络合物的形成改变了铜离子的电子跃迁过程。
3. 配位化合物配位化合物是一类由中心金属原子或离子与多个配体形成配位键的化合物。
这类化合物通常呈现出明亮的颜色。
例如,紫色的[Co(H2O)6]²⁺,粉红色的[KMnO4]等。
这些有色配位化合物的颜色主要是由于配位原子或离子的变化以及电子的吸收和发射引起的。
4. 有机化合物在有机化学中,一些有机物分子结构上的共轭体系也能引起物质呈现出有色。
共轭体系中的π电子有较低的跃迁能级,可以吸收较长波长的可见光,因而呈现出有色。
例如,苯(C6H6)呈现无色,而具有共轭结构的苯类化合物(如芳香族化合物)多呈现出黄色至红色。
5. 部分过渡金属氧化物部分过渡金属氧化物在不同的氧化态下呈现出不同的颜色。
这是由于氧化物的电子结构发生改变,从而引起能带结构的变化。
例如,二氧化钛(TiO2)在纯净状态下是白色的,但掺杂不同的氧化态(如二价钛或三价钛)后,颜色会发生变化。
总结:高中化学中,有色物质的研究对于了解物质的性质和应用具有重要意义。
金属离子溶液、过渡金属络合物、配位化合物、有机化合物以及部分过渡金属氧化物都是常见的有色物质。
化学中的有色离子-定义说明解析

化学中的有色离子-概述说明以及解释1.引言1.1 概述概述部分:有色离子是指在溶液中具有颜色的离子,它们在化学反应和分析中具有重要的意义。
有色离子的颜色来源于其分子或离子结构中的电子跃迁,通常是d电子或f电子的跃迁。
有色离子在化学实验中具有广泛的应用,包括分析化学、荧光材料、催化剂和生物标记等领域。
本文将对有色离子的定义、特点、化学应用、反应性质等进行详细介绍,旨在深入探讨有色离子在化学中的重要性和潜在的应用价值。
1.2 文章结构文章结构部分:本文共分为引言、正文和结论三个部分。
在引言部分,对有色离子进行了简要的概述,并介绍了本文的结构和目的。
在正文部分,将详细介绍有色离子的定义和特点,有色离子在化学中的应用以及有色离子的反应和性质。
最后,在结论部分对本文进行总结,强调了有色离子在化学领域中的重要性,并展望了未来有色离子研究的发展方向。
通过以上结构,本文将全面、系统地介绍了有色离子在化学中的重要作用和相关知识。
目的部分的内容可以如下编写:1.3 目的本文旨在深入探讨化学中有色离子的相关知识,包括其定义、特点、应用、反应和性质等方面。
通过对有色离子的研究和分析,我们可以更好地理解化学反应中的颜色变化原理,以及有色离子在催化剂、染料、金属与非金属离子识别等方面的重要应用。
同时,也可以进一步探讨有色离子在环境清洁、能源材料、医药和食品领域的潜在应用。
通过本文的阐述,旨在增进读者对有色离子的认识,促进相关领域的研究和应用,为化学领域的发展做出贡献。
2.正文2.1 有色离子的定义和特点有色离子是指在水溶液或固体中存在的带有颜色的离子,通常是由于其d或f电子能级发生跃迁导致的。
有色离子的特点包括:1. 吸收和发射特定波长的光线:有色离子能够吸收特定波长的光线,使得其呈现出特定的颜色。
通过吸收光线的波长,我们能够推断出离子的电子结构和能级分布。
2. 电子能级跃迁:有色离子的颜色是由于其电子在不同能级之间跃迁所致,这种跃迁导致了特定波长的光线的吸收和发射。
高中化学有色物质大全
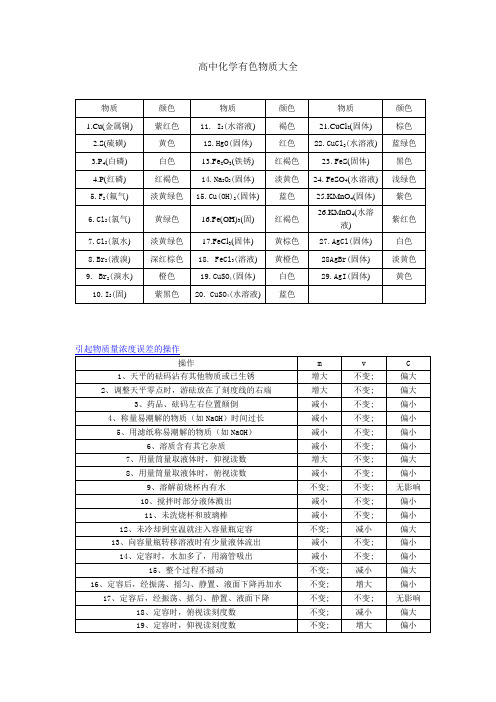
高中化学有色物质大全硝酸固碘硝酸银,低温避光棕色瓶。
液溴氨水易挥发,阴凉保存要密封。
白磷存放需冷水,钾钠钙钡煤油中,碱瓶需用橡皮塞,塑铅存放氟化氢。
易变质药放时短,易燃易爆避火源。
实验室中干燥剂,蜡封保存心坦然。
1、硝酸固碘硝酸银,低温避光棕色瓶:意思是说硝酸、固体碘和硝酸银都属于受热见光易分解的物质,所以必须存放在棕色瓶里,并放在阴凉处。
2、碱瓶需用橡皮塞:意思是说盛放碱液的试剂瓶要用橡皮塞或木塞。
3、塑铅存放氟化氢:意思是说氟化氢(氢氟酸)易腐蚀玻璃,因而必须存放在塑料或铅制器皿中。
4、易变质药放时短:意思是说易变质的药品存放时间较短,即不能长久贮存,最好现用现配制常见易变质的药品有:①氢硫酸放久了,则大部分将挥发,部分被空气氧化;②氯水长期存放将因慢慢分解而失效;③亚铁盐长期存放,则易被氧化为铁盐;④酸化的高锰酸钾溶液长期存放则慢慢退色]。
5、易燃易爆避火源:意思是说易燃物质(如:二硫化碳、酒精、丙酮、苯、硫、磷、镁粉等)和易爆炸的物质(如:氯酸钾、硝酸铵等)存放时要远离火源。
6、实验室中干燥剂,蜡封保存心坦然:意思是说实验室中用的干燥剂极易吸水,因而要用蜡封保存。
燃烧及火焰的颜色(一)燃烧的一般条件1.温度达到该可燃物的着火点2.有强氧化剂如氧气、氯气、高锰酸钾等存在3.(爆炸物一般自身具备氧化性条件,如硝化甘油、三硝基甲苯、火药等,只要达到温度条件,可以在封闭状态下急速燃烧而爆炸)(二)镁在哪些气体中可以燃烧?1镁在空气或氧气中燃烧2.镁在氯气中燃烧3.镁在氮气中燃烧4.镁在二氧化碳中燃烧(三)火焰的颜色及生成物表现的现象氢气在空气中燃烧—-淡蓝色火焰氢气在氯气中燃烧---苍白色火焰,瓶口有白雾。
甲烷在空气中燃烧---淡蓝色火焰酒精在空气中燃烧---淡蓝色火焰硫在空气中燃烧---微弱的淡蓝色火焰,生成强烈剌激性气味的气体。
硫在纯氧中燃烧---明亮的蓝紫色火焰,生成强烈剌激性气味的气体硫化氢在空气中燃烧---淡蓝色火焰,生成强烈剌激性气味的气体。
化合价及有色离子和物质

4.紫黑色固体:KMnO4、I2 5、黄色固体: AgI 、Ag3PO4
6、绿色固体: Cu2(OH)2CO3 7、蓝色晶体:CuSO4·5H2O
8 、蓝色沉淀 Cu(OH)2 9、红褐色沉淀: Fe(OH)3
带颜色的离子:
高锰酸根:紫色
锰酸根:墨绿色
重铬酸根:橙红色
铬酸根:柠檬黄色 Cu2+:蓝色/绿色 Fe3+:黄褐色 Fe2+:淡绿色 Ni2+:绿色 Cr3+:绿色/蓝色 Mn2+:淡粉色 Co2+:粉红色
[Fe(SCN)6]3-:血红色 苯酚合铁络离子:紫堇色
以下是一些物质的颜色: 黄色: AgI、Ag3PO4、P4(黄磷)、溴水(黄--橙)、FeS2、Al2S3、甲基 橙在弱酸性、中性或碱性环境中、某些蛋白质加硝酸。 淡黄色: S、Na2O2、T N T、PCl5、AgBr、浓 HNO3(混有 NO2)、浓 HCl (混有 Fe3+)、硝基苯(溶有 NO2)。 灰黄色:Mg3N2 棕黄色: FeCL3 溶液、碘水(深黄--褐) 黑色: CuS、Ag2S、Cu2S、PbS、HgS(黑色或红色)、FeS、FeO、Fe3O4、 MnO2、CuO、Ag2O、I2(紫黑)、Si(灰黑)、C、Ag、KMnO4(紫 黑)、石油 绿色: CuCl2 溶液、Cu2(OH)2CO3、FeSO4/7H2O(浅绿)、F2(浅黄 绿)、Cl2(黄绿)、氯水(浅黄绿) 红色:
CuO、Cu、Fe(SCN)2+、甲基橙在酸性环境中、紫色石蕊试液 在酸性环境中、酚酞在碱性环境中、品红试液、红磷(暗红)、 Br2(深红棕)、Br2 在 CCl4 溶液中(紫红)、苯酚被空气氧化(粉 红)
新人教高中化学必修1讲义06 第一章第二节第3讲 离子共存

第一章物质及其变化第二节离子反应第3讲离子共存【讲】知识点1离子共存1.离子共存的判断几种离子在同一溶液中能大量共存,就是指离子之间不发生任何反应,若离子之间能发生反应,则不能大量共存。
2.离子不能大量共存的情况(1)生成难溶物质的离子不能大量共存:①Ag+与Cl—、Br—、I—、CO32—①Ba2+与SO42—、CO32—、SO32—①Ca2+与CO32-、SO32—、①Mg2+、Al3+、Cu2+、Fe2+、Fe3+与OH—①SiO32—与H+①Cu2+、Fe2+与S2—(2)离子间反应生成微溶物,则不能大量共存①Ag+、Ca2+与SO42—①Mg2+与CO32—①Ca2+与OH—(3)生成气体的离子不能大量共存:①CO32—、HCO3—、S2—、HS—、SO32—、HSO3—与H+不能大量共存①NH4+与OH—(加热)(4)难电离物质(弱酸、弱碱、水)的离子不能大量共存:H+与OH-、H+与CH3COO-、OH-与NH+4等3.注意事项——“隐含条件”(1)“无色”溶液不存在有色离子,如:Cu2+(蓝色)Fe3+(黄色)Fe2+(浅绿色)MnO-4(紫红色)(2)在酸性(H+)溶液中(pH=1、pH<7、紫色石蕊试液变红的溶液中)不能共存的离子有①氢氧根离子:OH—①弱酸根离子:CO32—、S2—、SO32—、ClO—、F—、CH3COO—、PO43—①弱酸酸式酸根离子:HCO3—、HS—、HSO3—、HPO42—、H2PO4—(3)在碱性(OH—)溶液中(pH=13、pH>7、紫色石蕊试液变蓝、酚酞变红的溶液中)不能共存的离子有①氢离子:H+①弱碱阳离子:NH4+、Mg2+、Al3+、Cu2+、Fe2+、Fe3+①弱酸酸式酸根离子:HCO3—、HS—、HSO3—、HPO42—、H2PO4—(4)弱酸的酸式根离子既不能与H+离子大量共存,又不能与OH—大量共存如:HCO3— 、HS—、HSO3—、HPO42—、H2PO4—与H+、OH—不共存HCO3— + H+===CO2↑+ H2O HCO3— + OH—===CO32— + H2OHSO3— + H+===SO2↑+ H2O HSO3— + OH—===SO32— + H2OHS— + H+===H2S↑HS— + OH—===S2— + H2O3方法规律解答离子共存问题的方法(1)、一是判断离子共存,还是判断不共存,注意题目要求是“一定大量共存”、“可能大量共存”还是“不能大量共存” 等要求(2)二是看是否有隐含限制条件,如:碱性、酸性、无色等。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
高中化学中的有色物质和
有色离子
Final approval draft on November 22, 2020
色离子(C o l o r e d i o n)在水溶液中,有些离子是有色的。
常见的有色离子有:
有色离子的颜色
Cu2+铜离子-----------蓝色
Fe2+亚铁离子-----------浅绿色
Fe3+铁离子 -----------几近无色的淡紫色(黄色是在一般溶液中的颜色。
)
Mn2+锰离子-----------浅粉色
Co2+钴离子-----------粉色
Ni2+镍离子---------绿色
Cr2+亚铬离子 -----------蓝绿色
Cr3+铬离子 -----------绿色
Cd2+镉离子 -----------蓝绿色
Au3+金离子--------金黄色
MnO4-高锰酸根离子 ----------紫红色
MnO42-锰酸根离子 ---------墨绿色
CrO42-铬酸根离子 ---------黄色
Cr2O72-重铬酸根离子 --------橙色
[Fe(SCN)]2+硫氰合铁络离子------血红色
[CuCl4]2-四氯合铜络离子--------黄色
血红色:Fe3+遇到SCN-时的颜色
有色物质
1. 有色气体:Cl2(黄绿色)、NO2、Br2(气)红棕色
2. 液体:Br2(红棕色)
3. 有色固体:红色Cu、Cu2O、Fe2O3
红褐色:Fe(OH)3,Fe3O4
绿色:Cu2(OH)2CO3,FeSO4*7H2O
蓝色:Cu(OH)2,CuSO4*5H2O
黑色:CuO,FeS,CuS,MnO2,C,FeO,Ag2S
浅黄色:S,AgBr 黄色:AgI,Ag3PO4
4. 有色溶液:Cu2+(蓝色)、Fe2+(浅绿色)、Fe3+(黄色)、MnO4-(紫红色)、溴
水(橙色)。
5. 焰色反应:Na+(黄色)、K+(紫色)
6. 使品红褪色的气体:SO2(加热后又恢复到红色)、Cl2(加热后不恢复红色)
颜色变化的反应:1.蛋白质遇变黄(如做实验时,被某液体溅到皮肤上,皮肤变黄)
2.酚类遇Fe3+显紫色
3.Fe3+遇SCN-呈现血红色
4.Fe2+(浅绿色或灰绿色)遇比较强的氧化剂变成Fe3+(黄色)
5.Fe(OH)2(白色),在空气或溶液中会迅速变为灰绿色沉淀,最后变为Fe(OH)3红褐色沉
淀.
6.白色溶于水会变蓝
7.淀粉遇碘变蓝
8.氧化漂白:HClO(氯气通到湿润的有色布条,使有色布条褪色,其实是氯气与水生成次氯酸HClO,而次氯酸HClO具有强氧化性使布条褪色),臭氧O3,双氧水H2O2等都可使高锰酸钾溶液褪色
9.二氧化硫通入品红溶液,品红溶液褪色,但非氧化漂白,再加热品红溶液,颜色恢复.
10.不饱和烃(如烯烃,炔烃等)会使溴水或高锰酸钾溶液褪色(与溴发生加成反应,还原高锰酸钾)
11.苯酚(固体)在空气中露置被氧气氧化变为粉红色
12.2NO(无色)+O2=2NO2(红棕色)
13. NO2(红棕色)=N2O4(无色) (由于技术有限,这里的等号应为可逆号)(正反应条件好像是加压,逆反应条件反之)
14.黑色氧化铜CuO会与还原性物质(如氢气H2,一氧化碳CO,碳C等)反应生成红
色的铜Cu。
15.醛基与银氨溶液反应生成光亮的银镜 (反应要在水浴中进行)
16.醛基与新制氢氧化铜悬浊液反应,反应现象是蓝色絮状沉淀(Cu(OH)2)到砖红色沉淀(Cu2O)
17.无机反应(沉淀或有色离子) CH3COO-与 Pb2+Ba2+与SO42-Ba2+与SO32-Sn2+与SO42-Ag+与Cl-Hg+(Hg2Cl2) 与Cl-等等都是生成白色沉淀
18. Cu2+与碱生成Cu(OH)2蓝色沉淀.
19.Fe2+与碱生成Fe(OH)2,但它易被氧化,所以实验现象中没有我们期望的白色沉淀,而是灰绿色沉淀,过一段时间最终形成Fe(OH)3红褐色沉淀.
20.Fe3+与碱生成Fe(OH)3红褐色絮状沉淀。
