《化学反应工程》第六章
化学反应工程练习题解答

第一章习题1有一反响在间歇反响器中进行,经过8min 后,反响物转化掉80%,经过18min 后,转化掉90%,求表达此反响的动力学方程式。
解2A A min 18A0min 8A0AA A0d d 219.019.0181)(218.018.081)(11kc tc kc kc x x c kt =-=-⋅==-⋅=-⋅=为假设正确,动力学方程 2在间歇搅拌槽式反响器中,用醋酸与丁醇生产醋酸丁酯,反响式为:()()()()S R B A O H H COOC CH OH H C COOH CH 2943SO H 94342+−−→−+反响物配比为:A(mol):B(mol)=1:4.97,反响在100℃下进行。
A 转化率达50%需要时间为24.6min ,辅助生产时间为30min ,每天生产2400kg 醋酸丁酯〔忽略别离损失〕,计算反响器体积。
混合物密度为750kg·m -3,反响器装填系数为0.75。
解3313111111i 1.2m 0.750.8949总体积反应0.8949m 0.910.9834有效体积反应0.91hr6054.6折合54.6min 3024.6总生产时间hr 0.9834m 750737.5换算成体积流量hr 737.5kg 634.1103.4总投料量hr 634.1kg 744.97724.1B 4.97:1B :A hr 103.4kg 601.724折算成质hr 1.724kmol 0.50.862的投料量A ,则50%转化率hr 0.862kmol 116100hr 100kg 2400/24R 116 74 60 M S R B A ==⨯==+=⋅=+⋅=⨯⨯=⋅=⨯⋅=⋅=⋅=+→+-------器器投料量则量流量产量3反响(CH 3CO)2O+H 2O →2CH 3COOH 在间歇反响器中15℃下进行。
一次参加反响物料50kg ,其中(CH 3CO)2O 的浓度为216mol·m -3,物料密度为1050kg·m -3。
化学反应工程1_7章部分答案

第一章绪论习题1.1 解题思路:(1)可直接由式(1.7)求得其反应的选择性(2)设进入反应器的原料量为100 ,并利用进入原料气比例,求出反应器的进料组成(甲醇、空气、水),如下表:组分摩尔分率摩尔数根据式(1.3)和式(1.5)可得反应器出口甲醇、甲醛和二氧化碳的摩尔数、和。
并根据反应的化学计量式求出水、氧及氮的摩尔数,即可计算出反应器出口气体的组成。
习题答案:(1) 反应选择性(2) 反应器出口气体组成:第二章反应动力学基础习题2.1 解题思路:利用反应时间与组分的浓度变化数据,先作出的关系曲线,用镜面法求得反应时间下的切线,即为水解速率,切线的斜率α。
再由求得水解速率。
习题答案:水解速率习题2.3 解题思路利用式(2.10)及式(2.27)可求得问题的解。
注意题中所给比表面的单位应换算成。
利用下列各式即可求得反应速率常数值。
习题答案:(1)反应体积为基准(2)反应相界面积为基准(3)分压表示物系组成(4)摩尔浓度表示物系组成习题2.9 解题思路:是个平行反应,反应物A的消耗速率为两反应速率之和,即利用式(2.6)积分就可求出反应时间。
习题答案:反应时间习题2.11 解题思路:(1)恒容过程,将反应式简化为:用下式描述其反应速率方程:设为理想气体,首先求出反应物A的初始浓度,然后再计算反应物A的消耗速率亚硝酸乙酯的分解速率即是反应物A的消耗速率,利用化学计量式即可求得乙醇的生成速率。
(2)恒压过程,由于反应前后摩尔数有变化,是个变容过程,由式(2.49)可求得总摩尔数的变化。
这里反应物是纯A,故有:由式(2.52)可求得反应物A的瞬时浓度,进一步可求得反应物的消耗速率由化学计量关系求出乙醇的生成速率。
习题答案:(1)亚硝酸乙酯的分解速率乙醇的生成速率(2)乙醇的生成速率第三章釜式反应器习题3.1 解题思路:(1)首先要确定1级反应的速率方程式,然后利用式(3.8)即可求得反应时间。
(2)理解间歇反应器的反应时间取决于反应状态,即反应物初始浓度、反应温度和转化率,与反应器的体积大小无关习题答案:(1)反应时间t=169.6min.(2)因间歇反应器的反应时间与反应器的体积无关,故反应时间仍为169.6min.习题3.5 解题思路:(1)因为B过量,与速率常数k 合并成,故速率式变为对于恒容过程,反应物A和产物C的速率式可用式(2.6)的形式表示。
化学反应工程Chapter 6

Conversion Relationship
1 C A1 / C A0 X A1 1 AC A1 / C A0
FA1
R X A1 X Af R 1
1 R RX Af FA0 FA3 FA0 RFA0 1 X Af CA1 C A0 1 R R X 1 0 R f 0 R0 1 A X Af A Af
2
A=xy
dA 0 ydx xdy
dy y dx x
Figure 6.11
P6.7
Optimum Reactor Sequence
First-order reaction
n>1 n<1
Equal size
Smaller Larger Larger Smaller
1 C0 P ln k C
N reactors
C 1/ N N N i 0 1 K C N
P6.5
P6.4
Second-Order Reaction
2 A products A B products, C A0 CB 0
Factors in Design
级间的 There are many ways of processing a fluid: in a single batch or flow reactor, in a chain of reactors possibly with interstage feed injection or heating, in a reactor with recycle of the product stream using various feed ratios and conditions, and so on. Which scheme should we use? Unfortunately, numerous factors may have to be considered in answering this question; for example, the reaction type, planned scale of production, cost of equipment and operations, safety, stability and flexibility of operation, equipment life expectancy, length of time that the product is expected to be manufactured, ease of convertibility of the equipment to modified operation conditions or to new and different processes.
陈甘棠主编化学反应工程第六章

转化的多段绝
热反应器,段间引入冷空气
进行冷激。
对于这类可逆放热反应过
程,通过段间换热形成先高 后低的温度变化,提高转化 率和反应速率。
总之,不论是吸热或放热的反应,绝热 床的应用是相当广泛的,特别对于大型 的,高温或高压的反应器,希望结构简 单,同样大小的装置内能容纳尽可能多 的催化剂以增加生产能力(少加换热空 间),而绝热床正好能符合这种要求。 但绝热床的温度变化总是较大的,由于 温度对反应的影响同样不可忽视,故要 综合分析并根据实际情况来决定。
体积:(非球形颗粒折合成同体积的球形颗粒应当 具有的直径)
球形体积: VP
6
d3
6VP
1
3
dV
外表面积: (非球形颗粒折合成相同外表面积的 球形颗粒应当具有的直径)
球形外表面积: p d 2 a
ap
1
2
da
d 6 球形比表面积: V S 3 VS d d
6.2.2床层压降
气体流动通过催化剂床层的空隙形成的通道时, 与孔道皱襞摩擦将产生压降。 厄根(Ergun)方程:
2 um 1 B dP 150 R 1.75 3 d dL em B s
式中:Rem : 修正的雷诺数,Rem u m:平均流速空塔气速 d s : 颗粒当量直径
ap 6 VS 6 dS 6 SV ap
比表面积: (非球形颗粒折合成相同比表面积 的球形颗粒应当具有的直径) 2
混合粒子的平均直径:(各不同粒径的粒子直 径的加权平均)
1 dm xi d i
xi - 直径等于d i的颗粒占的分数
化学反应工程原理(华东理工大学版)第六章答案
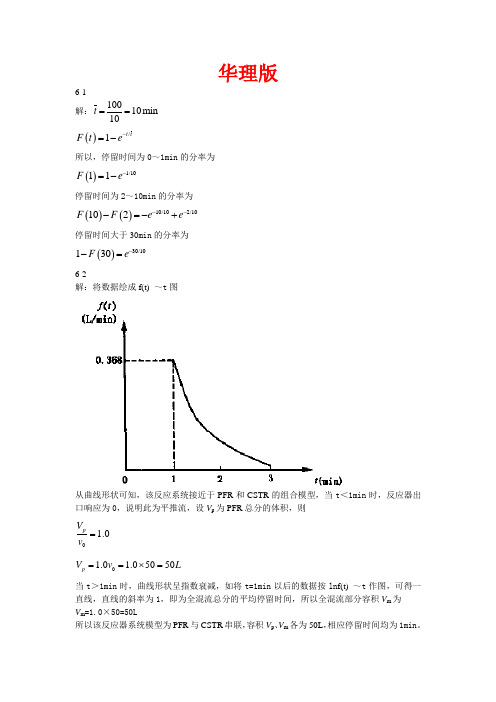
华理版6-1 解:10010min 10t == ()/1t t F t e -=-所以,停留时间为0~1min 的分率为()1/1011F e -=-停留时间为2~10min 的分率为()()10/102/10102F F e e ---=-+停留时间大于30min 的分率为()30/10130F e --=6-2解:将数据绘成f(t) ~t 图从曲线形状可知,该反应系统接近于PFR 和CSTR 的组合模型,当t <1min 时,反应器出口响应为0,说明此为平推流,设V p 为PFR 总分的体积,则0 1.0pV v =01.0 1.05050p V v L ==⨯=当t >1min 时,曲线形状呈指数衰减,如将t=1min 以后的数据按ln f(t) ~t 作图,可得一直线,直线的斜率为1,即为全混流总分的平均停留时间,所以全混流部分容积V m 为 V m =1.0×50=50L所以该反应器系统模型为PFR 与CSTR 串联,容积V p 、V m 各为50L ,相应停留时间均为1min 。
6-3解:CSTR中均相二级反应00c c ====0.435 即转化率为0.565CSTR 中固相二级反应:0100011i c k c e e c c k c k τττ⎛⎫=∙ ⎪⎝⎭6-4 解:()()000c t c f t dt c c ∞=⎰ 根据动力学方程可知,()21/200022c t c kt c c ⎛⎫-= ⎪⎝⎭,f(t)=0.5 代入已知条件,()21/200022c t c kt c c ⎛⎫-= ⎪⎝⎭= ()21t - ()()000c t c f t dt c c ∞=⎰=()2201t dt -⎰=0.667 所以转化率为A x =1-0.667=0.3336-5解:(1)由图知,反应器为通过一PFR 反应器和一全混釜反应器,0.4P ks τ=,求()dF t dt ,再取对数,用ln f(t) ~t 作图,可得一直线,斜率为1.25,所以0.8m ks τ=,平均停留时间为1.2ks 。
《化学反应工程》全册配套完整教学课件

Copyright 2011 by Southeast University
Chemical Reaction Engineering
物质在反应装置中的流动、传质和传热与化学反应之间相互关系的 概念,称为物理概念模型。 数学模型 表达物理概念模型的数学式称为数学模型。 数学模拟方法 用基于物理概念模型的数学模型来模拟反应过程的 方法称为数学模拟方法。
Copyright 2011 by Southeast University
固体颗粒细小,气流流动情况 复杂。
催化剂带出少,要求气液分布 均匀,温度调节较难。
固相在液相中悬浮,气相连续 流入及流出反应器。
固相在液相中悬浮,液相和气 相连续进入及流出反应器。
粒子返混小,相接触面小,传 热效能低。
Copyright 2011 by Southeast University
Chemical Reaction Engineering
一、化学反应工程学的研究范畴
过程工业
从事物质的化学转化,生成新的物质产品; 各个生产环节具有一定的不可分性,形成生产流程,并多数连续生
产。
过程工业包括两个过程:
Copyright 2011 by Southeast University
Chemical Reaction Engineering
气流床 滴流床 鼓泡淤浆床 三相流化床 回转筒式 螺旋挤压机式
气-固相 气-液-固三相 气-液-固(催化及非催化) 气-液-固(催化及非催化) 气-固相,固-固相 高黏度液相
《化学反应工程》第三版(陈甘堂著)课后习题答案

《化学反应工程》第三版(陈甘堂著)课后习题答案第二章均相反应动力学基础2-4三级气相反应2NO+O22NO2,在30℃及1kgf/cm2下反应,已知反应速率常数2kC=2.65×104L2/(mol2 s),若以rA=kppApB表示,反应速率常数kp应为何值?解:原速率方程rA=dcA2cB=2.65×104cAdt由气体状态方程有cA=代入式(1)2-5考虑反应A课所以kp=2.65×104×(0.08477×303) 3=1.564后当压力单位为kgf/cm2时,R=0.08477,T=303K。
答p p 2rA=2.65×10 A B =2.65×104(RT) 3pApBRT RTp表示的动力学方程。
解:.因,wwnAp=A,微分得RTVdaw案24网pAp,cB=BRTRT3P,其动力学方程为( rA)=dnAn=kA。
试推导:在恒容下以总压VdtVδA=3 1=21dnA1dpA=VdtRTdt代入原动力学方程整理得wdpA=kpAdt设初始原料为纯A,yA0=1,总量为n0=nA0。
反应过程中总摩尔数根据膨胀因子定义δA=n n0nA0 nA若侵犯了您的版权利益,敬请来信通知我们!Y http://.cn.co(1)mol/[L s (kgf/cm2) 3]m(1)则nA=nA01(n n0)δA1(P P0)δA(2)恒容下上式可转换为pA=P0所以将式(2)和式(3)代入式(1)整理得2-6在700℃及3kgf/cm2恒压下发生下列反应:C4H10发生变化,试求下列各项的变化速率。
(1)乙烯分压;(2)H2的物质的量,mol;(3)丁烷的摩尔分数。
解:P=3kgf/cm2,(1)课MC4H10=58,(2)w.krC2H4=2( rC4H10)=2×2.4=4.8kgf/(cm2 s)PC4H10=PyC4H101 dpC4H10= P dt2.4-1==0.8 s 3w(3)nC4H10=nyC4H10=n0(1+δC4H10yC4H10,0xC4H10)yC4H10dnH2dtdnH2dt=hdaw后n0=nC4H10,0=δC4H10rC4H10=反应开始时,系统中含C4H*****kg,当反应完成50%时,丁烷分压以2.4kgf/(cm2 s)的速率dyC4H10dt答1rCH=2.4224wdnC4H10dt案116×1000=2000mol582+1 1==21网dyC4H10=n0(1+δC4H10yC4H10,0xC4H10) dt=2000×(1+2×1×0.5)×0.8=3200 mol/s若侵犯了您的版权利益,敬请来信通知我们!Y http://.cno2C2H4+H2,dP=k[(δA+1)P0 P]=k(3P0 P)dtm(3)dpA1dP= dtδAdt2-9反应APS,( r1)=k1cA , ( r2)=k2cp,已知t=0时,cA=cA0 ,cp0=cS0=0, k1/k2=0.2。
反应工程复习题摘要

反应工程复习题摘要第一章绪论.1 .化学反应工程是一门研究__ _ _ _ _的科学。
2 .化学反应工程是一门研究化学反应的工程问题的科学,既以__ _作为研究对象,又以_ _ _ _为研究对象的学科体系。
3 . _ _ _是化学反应工程的基础。
4 .化学反应困呈按操作方法分为__ _、__ _、__ _操作。
5 .化学反应工程中的“三传一反”中的三传是指、、。
6 .不论是设计、放大或控制,都需要对研究对象作出定量的描述,也就要用数学式来表达个参数间的关系,简称。
第二章均相反应动力学一、填空1 .均相反应是指。
5 .活化能的大小直接反映了对温度的敏感程度。
P (主)6 .平行反应A S (副)均为一级不可逆反应,若E E >副主,选择性P S 与无关,仅是的函数。
8 . 一级连串反应 12K K A P S ??→??→在全混流釜式反应器中,则目的产物P 的最大浓度max pC =___apv t =____9 . 一级连串反应 12K K A P S ??→??→在平推流反应器中,则目的产物P 的最大浓度max p C =___apv t =____二、选择题1 .化学反应222222NO H N H O +?+,其中化学反应计量系数为+2的是哪种物质_。
A.NOB.H2C.N2D.H2O 2 .对于一非恒容均相化学反应B A B A αα?,反应组分A的化学反应速率A r -=_。
A .Vdt dn r A A -=- B. Vdt dn r A A =- C. dt dC r A A =- D.dt dC rB A =-3 .对于反应aA + bB 一pP +sS ,则P r ____()A r - A.a pB.a pC. p aD. p a4 .气相反应43A B R S +→+进料时无惰性气体,A 与B 以3:1的摩尔比进,则膨胀因子A δ= ____A.1/4B.2/3C.-1/4D.-2/35 . 气相反应2423CO H CH H O ++?进料时无惰性气体,CO 与2H 以1:2摩尔比进料,则膨胀因子CO δ=___A.-2B.-1C.1D.2 7 . 反应4102422C H C H H →+,12.0k s -=,则反应级数n=____。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
列 管 是 固 定 床 反 应 器
出料
处料
⑷自热式固定床反应器——适于放热反应(合成氨)。
主进气 床层温度 tb
t
双套管 催化剂
坐标位置 I
600 平衡线 换热器
t/℃
500 床层实际 400 操作线 0 最佳 温度线 0.3
出气
旁路进气
0.1 0.2 氮含量y
双套管并流式反应器及床层温度分布
2 u dp 150 m g (1 B ) ( 1.75) 3 dl Re m dS B
⑵物料恒算方程 dVR At dl d t2 dl , 4
输入A量 = FA
FA
dVS (1 B )dVR
dl At FA+dFA 体积单元物料示意图
输出A量 = FA+d FA 反应消耗A量 = (-RA)(1-εB)d VA = (-RA)(1-εB)Atdl 积累A量 = 0 因为
SO
2
1 1.5 0.5, 1
0 SO2
0 SO ySO SO 0.08 (0.5) 0.04
2 2 2
pSO2 p
(1 xSO2 ) 1 SO2 xSO2
p
0 SO2
(1 xSO2 ) 1 0.04xSO2
1-空管内层流;2-空管内湍流;3-充填层内液体流动; 4-充填层内气体流动(Um为平均流速)
6.1.1.2颗粒的定型尺寸
体积当量直径(dV):与颗粒具有相同体积(VS)的球体的直径
6V dV S
1/ 3
面积当量直径(da):与颗粒具有相同外表面积(SS)的球体的 1/ 2 直径 S S
第六章 气固相催化反应固定床反应器
6.1流体在固定床内的传递性质
6.1.1流体在固定床内的流动特性
6.1.1.1床层孔隙率与流体的流动
蒸气
床层孔隙率εB
B
1.0
进气
空隙体积 颗粒体积 V 1 1 P 1 B 床层体积 床层体积 VB P
调 节 阀
补充水
0.8 0.6
催化剂
床层高度
um0c A0 x A dxA L dl 0 (1 B ) 0 ( RA )
L
方程组的解
p
TW T
(H )( RA )(1 B )d t B )d t dxA T 4h0 dl
xA
L 等温床层分布图
2 pSO 3 1 2 km ol/[ skg (cat.)] 2 2 pSO2 pO2 K p / pSO3 )
5 1 . 339 10 2 式中 k 9.86910 exp RT 1.138105 8 K M 2.3 10 exp RT
2
2
厄根方程
um g (1 B ) dp 150 ( 1.75) 3 dl Re m dS B or um g (1 B ) p 150 ( 1.75) , (T , p都较小) 3 L Re m dS B
2
解:⑴ ⑵
dm
( x / d )
7.1.2.2:径向传质 可造成反混,用Per=dpum/Er 描述。
6.2固定床催化反应器的设计
6.2.1固定床催化反应器的特点及特征
6.2.1.1固定床催化反应器的特点
优点:催化剂不易磨损,使用时间长; 生产能力大; 转化率、选择性高。 缺点:传热差,对温度敏感; 更换催化剂需停产,粉尘大。 另一流化床反应器特点: ①等温操作;②传热强度高; ③催化剂用量少;④压降稳定; ⑤反混严重;⑥设备精度高。
or
dp u 2 g dl de 2
dp/dl流体通过单位床高引起的压强变化, u 气体实际流速。 若 um 为气体通过床层的空塔流速, um = u×εB。 de 为床层 的当量直径.
de 4 截面积 B 2 B 6 4 ,(SV ) 浸润周边 (1 B ) SV 3 (1 B )d S dS
进气
出气
流 化 床 催 化 反 应 器
6.2.1.2固定床催化反应器的类型
⑴绝热固定床反应器——适于反应热不大的过程。 ⑵多断绝热式反应器——温度适宜,转化率高。
⑶列管式固定床反应器——反应速度快,转化率、选择性高。
进料
进料
冷激气
进料
进料
cat.
绝 热 固 定 床 反 应 器
冷剂 冷剂 冷剂
多 段 绝 热 床 反 应 器
i i
1
3.96 mm 3.96 10 3 m
Re m
dSG 1901 g (1 B )
⑶
150 G 2 (1 B ) 5 p ( 1.75) L 1 . 898 10 Pa 3 Re m dS g B
7.1.2固定床内径向传递
1.339105 式中 k 9.86910 exp RT 1.138105 8 K M 2.3 10 exp RT lg K p 4905 .5 5.6484 T
③将动力学方程变化为转化率[x(SO2)]的函数。该反应
da
比表面当量直径(dS):与颗粒具有相同比表面积(SV)的球体 6 Va 的直径 d 6
S
SV
Sa
不同粒径的混合粒子其平均直径:
dm 1 ( xi / di )
xi是直径为di的粒子所占质量分率。
6.1.1.3:流体通过床层的压降
dp
g
dl u 2 de 2
xA D G A B E c F C b D
平衡曲线
xA
C
a
B
最佳温度曲线
A Tmax T Tmin 吸热反应T-x图 T 可逆放热反应的T-x图
对可逆放热反应,应使反应速率保持最大,于是随转化率 升高,按最佳温度曲线相应的降低温度。见上图示。
进
1
对第i段反应床,所需催化剂体积为 At um0c A0 x dxA V0c A0 x dxA VRi At L x (1 B ) ( RA ) (1 B ) x ( RA )
满足条件Ⅱ
寻优步骤: ①有xA0、T0,在图上定出A点。
②根据绝热操作线方程做出AB线,B点在最佳温度线上。 ③由B作xA轴垂线到C,满足条件Ⅰ。
④从C作AB平行线到D,满足条件Ⅱ。
⑤进行下去,直到转化率达到要求为止。
⑥由优化条件计算VR、L。
( RSO2 ) kpO2
1
K M ( pSO2 / pSO3 ) K M ( pSO2
6.2.2.3单层绝热床的计算
绝热反应器的数学模型 2 u dp 150 m g (1 B ) ( 1.75) 3 dl Re m dS B dxA ( RA )(1 B )
dl um 0 c A0
Q=0
边值条件: L=0时,p=p0,xA=0,T=T0. 解
Re
deu g
g
2 d S um g , 3 g (1 B )
um g (1 B ) dp 3 ' , ' 3 dl dS B 4 d S um g 150 ' 1.75 Re m g (1 B ) Re m
边值条件: L=0时,p=p0,xA=0,T=T0. 解
p
T xA L
6.2.2.2等温反应的计算
dT/dl=0 2 u 150 m g (1 B ) 动量恒算式 p p0 L( 1.75) 3 Re m dS B
dxA ( RA )(1 B ) 物料恒算式 dl um 0 c A0
um g (1 B ) 150 p p0 L( 1.75) 3 Re m dS B
联解即得床层内温度、压力、转化率的分布曲线,求得达 到一定转化率所需的床层高度(催化剂用量)。
p T~L xA~L
T xA
p~L
L
7.2.2.4多段绝热反应器的计算
Q=0
对吸热反应,随xA↑→T↓,到达B点反应停止,这时需升温 到C,再继续反应。这就是多段绝热反应器。
ε
0.4
0.2
0
2
4
6
空隙率与床层径向位置的关系
δ /d
出气
固定床反应器的 基本单元组合
2 1
沿壁效应:影响流速、 传热、传质、停留时间、 化学反应。 减少沿壁效应:床层直 径(Dt)不小于粒径dP的 八倍,即 Dt>8dP
U/Um
2 3 4
1
1 管壁
r/R
0 中心
r/R
1 管壁
床层径向流速分布示意图
T T0 ( xA xA0 )
um0c A0 x A dxA L (1 B ) 0 ( RA )
根据
( RA ) k0e
E RT
f (cA0 , xA )
2
um0c A0 x A dxA L (1 B ) 0 ( RA )
T T0 ( xA xA0 )
dFA FA0dxA At um0cA0dxA
dxA ( RA )(1 B ) dl um 0 c A0
⑶热量恒算方程 输入热量-输出热量+反应热量 = 向外界供热+积累热 输出热量=Gcp(T+dT) 输入热量=GcpT 反应放热= (-△H)(-RA)(1-εB)Atdl 积累热=0 向外界供热=h0(T-TW)πdtdl h0 dT 1 [(H )( RA )(1 B ) 4 (T TW )] dl um0 g c p dt
