初中化学溶液的酸碱性知识点与习题(含答案)
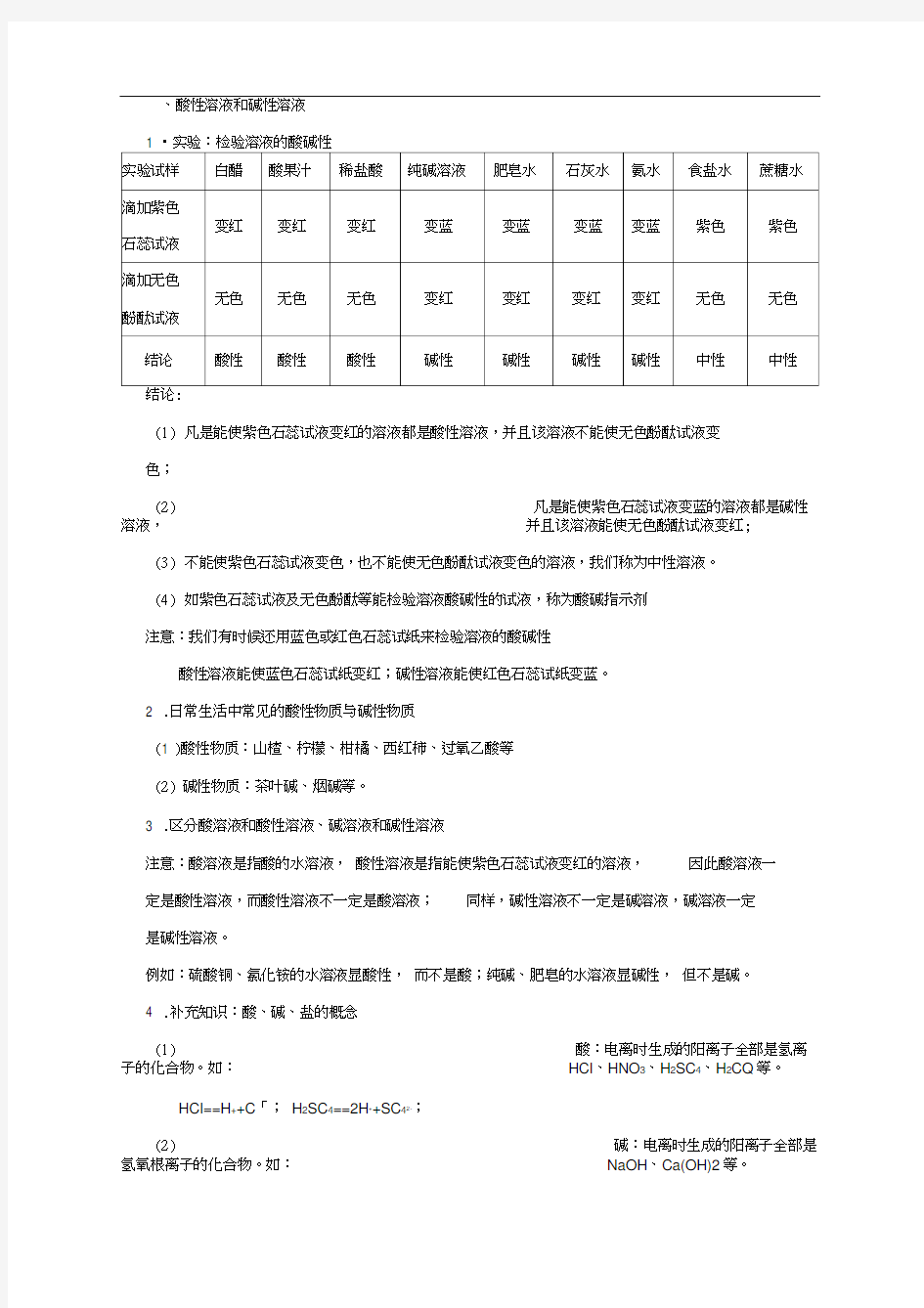

、酸性溶液和碱性溶液
(1)凡是能使紫色石蕊试液变红的溶液都是酸性溶液,并且该溶液不能使无色酚酞试液变
色;
(2)凡是能使紫色石蕊试液变蓝的溶液都是碱性溶液,并且该溶液能使无色酚酞试液变红;
(3)不能使紫色石蕊试液变色,也不能使无色酚酞试液变色的溶液,我们称为中性溶液。
(4)如紫色石蕊试液及无色酚酞等能检验溶液酸碱性的试液,称为酸碱指示剂
注意:我们有时候还用蓝色或红色石蕊试纸来检验溶液的酸碱性
酸性溶液能使蓝色石蕊试纸变红;碱性溶液能使红色石蕊试纸变蓝。
2 .日常生活中常见的酸性物质与碱性物质
(1 )酸性物质:山楂、柠檬、柑橘、西红柿、过氧乙酸等
(2)碱性物质:茶叶碱、烟碱等。
3 .区分酸溶液和酸性溶液、碱溶液和碱性溶液
注意:酸溶液是指酸的水溶液,酸性溶液是指能使紫色石蕊试液变红的溶液,因此酸溶液一
定是酸性溶液,而酸性溶液不一定是酸溶液;同样,碱性溶液不一定是碱溶液,碱溶液一定
是碱性溶液。
例如:硫酸铜、氯化铵的水溶液显酸性,而不是酸;纯碱、肥皂的水溶液显碱性,但不是碱。
4 .补充知识:酸、碱、盐的概念
(1)酸:电离时生成的阳离子全部是氢离子的化合物。如:HCI、HNO3、H2SC4、H2CQ等。
HCI==H++C「;H2SC4==2H++SC42-;
(2)碱:电离时生成的阳离子全部是氢氧根离子的化合物。如:NaOH、Ca(OH)2等。
NaOH==Na++OH T;Ca(OH)>==Ca2++2OH-;
NaCI、NH4NO3 (3)盐:电离时生成金属离子(或铵根离子)和酸根离子的化合物。如:
等。
NaCI==Na++CI;NH4NO3==NH4++NO3-;
、溶液的酸碱性的强弱程度
1 ?酸碱度:用来表示溶液的酸性或碱性的强弱程度。
2 ? pH试纸用来定量的测定溶液的酸碱度。
pH 值123456789 10 11 12 13 14
-------------------------------------------------------------------------------------------------------------------------- ?
I
酸性增强中性碱性增强
溶液的pH值与酸碱性关系
pH=7,溶液呈中性;pH<7,溶液呈酸性,pH越小,酸性越强;pH>7,溶液呈碱性,pH越大,碱性越强3 ? pH试纸的使用方法;
用胶头滴管(或玻璃棒)把待测试液滴(或涂)在pH试纸上,然后把试纸显示的颜色(半
分钟内)与标准比色卡对照,标准比色卡上相同颜色的pH即为该溶液的pH。
(1)不能直接把pH试纸浸入待测溶液中,以免带入杂质,同时这种操作可能泡掉pH试纸上一部分指示剂,以致比色发生较大的误差;
(2)不能先用水将pH试纸润湿,再进行测试,因为水润湿后的pH试纸将测定的是稀释后溶液的pH。
(3)我们实验室一样使用的pH试纸是广泛pH试纸,测出的pH值是1-14的整数
(4)为了比较精确的测定溶液的pH,我们可以用精密pH试纸和酸度计(pH计)来测量。三、溶液酸碱性与生命活动的关系
1 ?人的体液有一定的酸碱度。血液、组织间液和细胞内液的酸碱度都接近于中性,而且变
化极小;
2. 胃液的pH在0.9~1.5之间,在这样的环境中铁屑都可被溶解,但胃本身却能安然无恙。因为胃里有一层“粘液屏障”,它是由粘液细胞和上皮细胞分泌出的一种胶冻状粘液,在胃粘膜表面构成一个保护膜,用来保护胃,防止胃酸对其本身的腐蚀及胃蛋白酶对胃本身的消
化,还能防止粗糙的食物对胃的机械性损伤。
3 .大多数的农作物适宜在接近中性(pH在6.5~7.5之间)的土壤中生长
A.纯碱溶液 B .食醋 C .食盐水 D .自来水
在改良酸性土壤时,我们一般是使用熟石灰来调节其酸碱度。 4?雨水一般呈略酸性(由于空气中的二氧化碳溶解在雨水中) 雨水称为酸雨。
1.实验室用于测定溶液酸碱度的 pH 试纸(适用的变色范围在 1-14之间)常见的颜色为
()
A. 黄色 B .白色 C .蓝色 D .红色
2.
则下列说法中,不正确的是 ()
A.鸡蛋清显碱性
B. 胃酸过多的人应少吃四川泡菜
3. 下列物质的p H 大于7的是(
6.以下是一些食物的近似 pH 值:①苹果3.3?4.5②鸡蛋清 4.0?4.4④玉米粥6.8?8.0⑤柑橘汁3.4?4.2,胃酸过多的人宜经常食用的是 ) C.④⑤
D.③⑤
如果先将试纸用蒸馏水润湿, 再把食醋滴到试纸上,
() D. 无法比较
其pH 约为6,且难溶于水。则在沾有胆汁的地方涂上下列物质可消除苦味的是
(
,人们一般把pH 小于5.6的
C.橘子汁能使石蕊试液变红
D.
牛奶比鸡蛋清的碱性强
A .食盐水
B .食醋
C .石灰水
D .汽水
4. 在Ca(OH) 2的饱和溶液中加入下列物质,冷却至室温,溶液
的 ) pH 没有改变的是
7.6 A.CQ
B.CaO
C.C
5. 一些食物的近似 pH 如下:葡萄 -8.0。其中显碱性的一种食物是
A.鸡蛋清 B .牛奶 C
u( NO s ) 2
3.5?
4.5 ;苹果 (
D.HCl
2.9 ?
3.3 ; )
牛奶6.3?6.6 ;鸡蛋清
.苹果 D .葡萄
A.①④
B .②④
7.用pH 试纸测定食醋的酸碱度时, 测得的结果与食醋实际的
pH 比较
A.偏低
B. 偏高
C. 相等
8.鱼味道鲜美,但剖鱼时弄破鱼胆, 胆汁沾在鱼肉上,便有苦味,产生苦味的是胆汁酸,
7.6?8.0 ③番茄
9.
某环保部门取下降的雨水测定(正常雨水的 pH 约为5.6,酸雨的pH 则不于5.6 ),其
中含有亚硫酸(H 2SO ),该酸不稳定,易发生如下反应: 2H2SO+Q=2HSQ (已知同等条件下亚 硫酸比硫酸酸性弱)。每隔一段时间测定收集的雨水的
pH 如下:
测定时间/分钟
0 1 2 4 5
pH
4.73
4.62 4.56 4.55 4.55
F 列说法不正确的是 ()
A. 主要是因为雨水中的成份发生变化,溶液
pH 发生变化
B. 雨水酸性逐渐减弱
C. 酸雨可腐蚀某些金属制品
D. 酸雨是空气受污染造成的
10. 测定生活中一些物质的 pH,结果如下:
A.肥皂水是中性物质
B. 草木灰可改良碱性土壤
C.吃松花蛋一般添加食醋去除涩味
D.
橘子汁能使酚酞试液变红
11.
某种消化药片的有效成分氢氧化镁,能减缓因胃酸过多引起的疼痛。在氢
氧化镁与 胃酸作用的过程中,胃液
pH 变化的情况是 ()
J --------------------- - ——?
J --------------------- -- ■
-- -------------------- -- ■
- ---------------------- =?
A B C D
12. 一些食物的近似 pH 如下表:
食物
苹果 葡萄 牛奶 玉米
草木灰
肥皂—
牙膏
pH 2 3 4 5 6 7 8 9 10 11
(1)___________________________________________________ 苹果汁和葡萄汁相比较,酸性较强的是________________________________________________ ;
(2)_____________________________________________________________________ 人的胃液中含有盐酸,对于胃酸过多的人,空腹时最宜食用的食物是_________________________ ;
(3)鸡蛋壳中含有CaCO,以前因胃酸过多导致胃痛时,有人吃鸡蛋壳粉,其原因是(用
化学方程式表示) ____________________________________________________ 。现今,许多治疗胃酸过多的药品的有效成分是氢氧化铝,而不是CaCQ请提出一种理由说明为什么氢氧化铝
优越于碳酸钙___________________________________________________________ 。
答案
ADCCA BBAACB 苹果玉米CaCO+HCL=HP+C& CaCL 氢氧化铝显碱性,同样会对胃有刺激作用
