高中化学 2.2 钠、镁及其化合物知识点总结 苏教版必修1

专题二从海水中获得的化学物质
第二单元钠、镁及其化合物
钠的物理性质:
银白色固体、有金属光泽、密度比煤油大比水小、质软、熔点低、能导电导热。
钠的化学性质:
1.钠与水反应
盖玻璃片。
观察到的现象及由现象得出的结论有:
(1)钠浮在水面上(钠的密度比水小)
(2)钠熔成一个闪亮的小球(钠与水反应放出热量,钠的熔点低)
(3)钠在水面上四处游动(有
(4)发出嘶嘶的响声(生成了气体,反应剧烈)
(5)事先滴有酚酞试液的水变红(有碱生成)
反应方程式:
2Na+2H2O=2NaOH+H2↑
2.钠与氧气反应
在常温时:4Na+O2=2Na2O (白色粉末)
在点燃时:2Na+O2=△=Na2O2 (淡黄色粉末)
3.钠与钛、锆、铌等金属氯化物反应
4Na+TiCl4==熔融==4NaCl+Ti(条件为高温且需要氩气做保护气)
补充
4.与酸溶液反应
钠与水反应本质是和水中氢离子的反应,所以钠与盐酸反应,不是先和水反应,钠与酸溶液的反应涉及到钠的量,如果钠少量,只能与酸反应,如钠与盐酸的反应:2Na+2HCl=2NaCl+H2↑ 如果钠过量,则优先与酸反应,然后再与酸溶液中的水反应。
5.与盐溶液反应
将钠投入盐溶液中,钠先会和溶液中的水反应,生成的氢氧化钠如果能与盐反应则继续反应。如将钠投入硫酸铜溶液中:
2Na+2H2O=2NaOH+H2↑ 2NaOH+CuSO4=Na2SO4+Cu(OH)2↓
钠的制取:
电解熔融氯化钠
2NaCl(熔融)=电解=2Na+Cl2↑
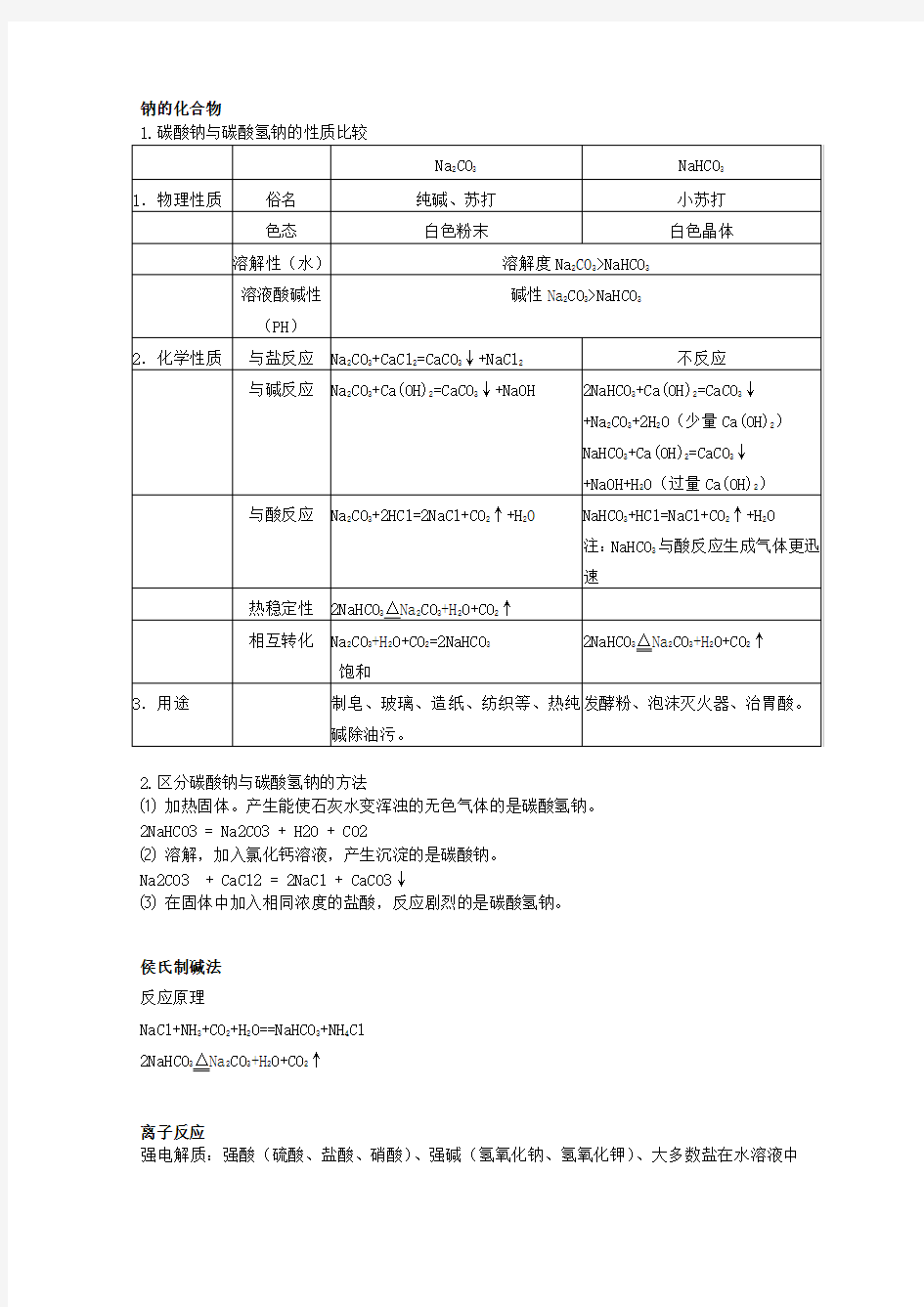
钠的化合物
2.区分碳酸钠与碳酸氢钠的方法
⑴加热固体。产生能使石灰水变浑浊的无色气体的是碳酸氢钠。
2NaHCO3 = Na2CO3 + H2O + CO2
⑵溶解,加入氯化钙溶液,产生沉淀的是碳酸钠。
Na2CO3 + CaCl2 = 2NaCl + CaCO3↓
⑶在固体中加入相同浓度的盐酸,反应剧烈的是碳酸氢钠。
侯氏制碱法
反应原理
NaCl+NH3+CO2+H2O==NaHCO3+NH4Cl
2NaHCO3△Na2CO3+H2O+CO2↑
离子反应
强电解质:强酸(硫酸、盐酸、硝酸)、强碱(氢氧化钠、氢氧化钾)、大多数盐在水溶液中
完全电离的一类电解质。
弱电解质:弱酸(碳酸、醋酸)、弱碱(一水和铵)在水溶液中不能完全电离的一类电解质。
离子方程式书写
用实际参加反应的离子符号来表示反应的式子。它不仅表示一个具体的化学反应,而且表示同一类型的离子反应。
复分解反应这类离子反应发生的条件是:生成沉淀、气体或水。书写方法: 写:写出反应的化学方程式
拆:把易溶于水、易电离的物质拆写成离子形式 删:将不参加反应的离子从方程式两端删去 查:查方程式两端原子个数和电荷数是否相等
海水中提取镁的方法
化学反应方程式:
镁的化学性质:
1、与空气的反应
2Mg + O 2 === 2MgO
3Mg + N 2 ===2Mg 2N 3
2Mg + CO 2 === 2MgO + C
2、与水的反应
Mg+2H 2O === Mg(OH)2+H 2↑
3、与酸的反应
Mg + H 2SO 4 === MgSO 4 + H 2↑
镁的用途:
1)镁合金的密度较小,但硬度和强度都较大,因此被用于制造火箭.导弹和飞机的部件 2)镁燃烧发出耀眼的白光,因此常用来制造通信导弹和焰火; 3)氧化镁的熔点很高,是优质的耐高温材料
点燃
点燃
点燃
写出下列物质之间的转化的化学方程式:
