初中化学酸碱盐推断题

样品
A
溶 ^ 液
B
滤
液
甲
沉
淀
乙 沉 淀
] C 滤 液
①
水 溶解
③ 过量
BaCl 2溶液 过滤 ;
②
过量 NaOH 溶液 过滤
④ 过量 Na 2CO 3溶液
过滤
丙 沉 ` 淀
D
滤
液 ⑤ 过量 盐酸
加热蒸发
固体丁
1.A 、B 、C 、D 、E 、F 、G 为常见的物质,其中B 、E 、G 属于单质,反应②是炼铁工业中的主要反应,下
图是它们之间的相互转化关系。请回答:
#
(1)A 物质的化学式 。
(2)写出反应②的化学方程式 ,
C 物质固态时的名称 ,该固体物质在实际生活中的一种用途是 。 (3)写出反应③中生成红色固体的化学方程式 。 (4)上图转化中产生无色气体G 的原因是 ,
写出物质G 和A 在加热条件下反应的化学方程式
2.现有初中化学中常见的易溶于水的三种钠盐组成的混合物,将其溶于水后得无色溶液A ,进行如下实验并得到相应结果:
~
试回答下列问题: (1)无色气体D 的化学式为 ,白色沉淀E 的化学式为 ,钡盐B 的化学式为 。 (2)原混合物中含有的三种易溶于水的钠盐的化学式分别为 、 、 。
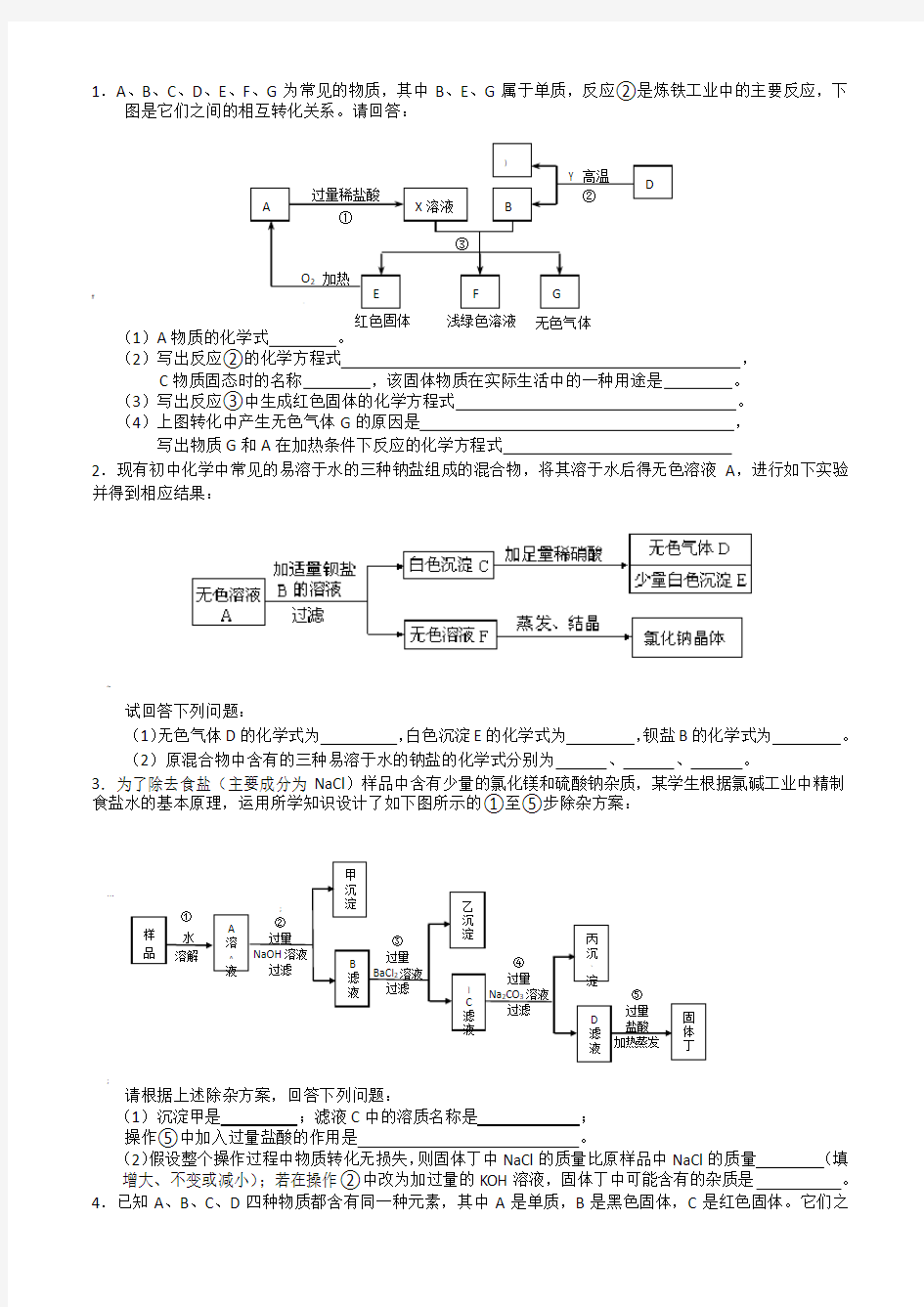
3.为了除去食盐(主要成分为NaCl )样品中含有少量的氯化镁和硫酸钠杂质,某学生根据氯碱工业中精制食盐水的基本原理,运用所学知识设计了如下图所示的①至⑤步除杂方案:
…
;
请根据上述除杂方案,回答下列问题:
(1)沉淀甲是 ;滤液C 中的溶质名称是 ; 操作⑤中加入过量盐酸的作用是 。 (2)假设整个操作过程中物质转化无损失,则固体丁中NaCl 的质量比原样品中NaCl 的质量 (填增大、不变或减小);若在操作②中改为加过量的KOH 溶液,固体丁中可能含有的杂质是 。 4.已知A 、B 、C 、D 四种物质都含有同一种元素,其中A 是单质,B 是黑色固体,C 是红色固体。它们之
红色固体 ③ A B D E F )
G
Y 高温
②
X 溶液 过量稀盐酸 ①
O 2 加热 -
无色气体
浅绿色溶液
间存在着如下转化关系:(1)A 在不同条件下能够转化成B 或C ;(2)A 和稀硫酸反应有D 生成;(3)在高温条件下,B 、C 分别和无色气体E 反应,都能生成A 和另一种无色气体。根据上述信息,写出下列物质的化学式:
A ;
B ;
C ;
D ;
E 。
5.有一种白色固体可能含有:BaCl 2、NaCl 、Na 2CO 3、Na 2SO 4和CuSO 4中的一种或几种。对该固体进行如下
实验。
①取样,加足量的水,充分搅拌,过滤。得到白色沉淀A 和无色溶液B 。
②在白色沉淀A 中加入稀盐酸,沉淀全部溶解,放出能使石灰水变浑浊的无色气体。
③在无色溶液B 中加入AgNO 3溶液,得到白色沉淀,再加入稀盐酸,白色沉淀不溶解。请回答下列问
题。 、
(1)原白色固体中一定不含有..._________________;一定含有______________。
(2)实验①得到的无色溶液B 中一定含有....的溶质是_______________________。 (3)原白色固体中可能含有________________________________________
6.某固体可能由Na 2SO 4、NaCl 、Na 2CO 3、KNO 3中的一种或几种组成,现实验如下:
试回答:
(1)白色沉淀A 的化学式为 ,无色气体D 的化学式为 。 (2)原固体中一定含有 ,一定不含有 ,可能含有 。
(3)为检验上述可能含有的物质是否一定存在,某同学又设计了如下实验方案:
① 取少量固体溶于水,加入足量的Ba(NO 3)2溶液,充分反应后,过滤; (
② 取滤液加入AgNO 3溶液,观察有无白色沉淀生成,由此得出结论。
在上述某同学的实验方案①中,加入足量的Ba(NO 3)2溶液的目的是 。
7.某化学试剂厂A 、B 、C 、D 四个车间排放的废水中,分别含有氢氧化钠、氯化铁、碳酸钠、盐酸中的一种。在不加试剂的情况下,若控制流量,将它们排放到反应池中,使其恰好完全反应,最后可形成不污染环境的废液排入河流。已知B 车间排放的污水显碱性,C 车间排放的污水有颜色,反应池1中有气泡产生,则A 车间排放的废水中含有____________,D 车间排放的废水中含有_____________。反应池2中可观察到的现象是_________________________________________,反应的化学方程式为________________,最后排入河流的废液中含有的主要物质是______________。
A
B C
D
反应池1
反应池2
河 流
8.有一包白色固体A ,可能含有FeCl 3、CaCO 3、NaOH 、Ba OH ()2、BaCl 2、Na SO 24中的几种,取少量A 做如下实验,主要现象如图所示。试用化学式填空:
全部溶解
白色沉淀D
(1)白色沉淀B 是________________,D 是________________________;
(2)白色固体A 中一定不存在的物质是_________________________________; (3)若白色固体A 中只含两种物质,它们是_________________________________; (4)白色固体A 还有哪些可能的组成: 《 ①______________________________ ②______________________________ ③______________________________
④______________________________
9.某化工厂排出的废液中含有AgNO Cu NO 332、()和Zn NO ()32。为了减少废液对环境的污染,并回收银和铜,某化学小组同学设计了如下方案进行实验:
根据实验推断:
(1)固体甲是______________________;
(2)滤液2中的溶质是________________(写化学式);
(3)滤液2跟固体a 反应的化学方程式是_____________________。
10.研究小组为了解北京西山的地质情况,从实地选取两块样品D 和J ,进行如下所示的实验(其中部分反应产物被略去):
(1)样品D 和J 的主要成分分别是(用化学式表示)_________、_________。 :
(2)实验室用固体J 制取气体G 的化学方程式为___________________________。 (3)上述实验中部分反应的化学方程式
J→H :______________________________________________________; F+X→:______________________________________________________; D+E→:______________________________________________________; B+C→:______________________________________________________。
11.有一包固体物质,可能是由H 2SO 4、CaCO 3、Fe(NO 3)3、Ba(OH)2、NaCl 、MgCl 2中的一种或几种组成。为确定其成分,进行如下实验:
①取样品放入小烧杯中,加水充分溶解,静置,有白色沉淀。
②再向小烧杯中逐滴加入稀硝酸,开始无现象,后沉淀逐渐溶解,最后沉淀不再减少。试推断: (1)这包固体中一定不存在的物质是___________,可能存在的物质是___________。 【
(2)写出①中发生的反应方程式:
_______________________________________________________ _______________________________________________________ 12.有四家相邻的小化工厂排放的废水中溶质的主要成分如下表:
厂名
A 厂
B 厂
C 厂
D 厂
废水中溶质的主要成分
H 2SO 4 Na 2CO 3 Ba(OH)2 CuCl 2
为保持环境、防止污染,四厂决定联合处理废水,其处理方案如下:
(1)排气池中发生反应的化学方程式为:____________________________ (2)沉淀池中出现的现象是______________,化学方程式为_______________
(3)若进入混合池中的物质恰好完全反应,经检测合格后排入江河的溶液中的溶质是____________________(填化学式); 。
(4)若排气池中B 厂废水过量,则混合池中发生反应的化学方程式为: _____________________________________________________________
13.“三酸两碱”是几种重要的无机化工原料,下图是它们与其他物质间相互转化的关系。已知:
①A A A 、、12是工业上常见的三大强酸,B B B 、、12是正盐,C C C 、、12是碱。②B 2是食盐的主
要成分,且B B B C 、、、121中含有相同的金属离子。③A B CO B C +→↑+→2,白色沉淀+?→?
A
2
沉淀完全溶解并放出二氧化碳,A C +→白色沉淀+?→?
A
2
沉淀不溶解。
请回答:
(1)有关物质的化学式:B2____________,C1____________。
(2)有关反应的化学方程式:
A B
+:____________________________________________________________,
B C
+:____________________________________________________________。
$
(3)C2可能的化学式(写三个):____________________________________。
14.有A、B、C、D四种化合物,A是硝酸盐,B是酸,C是碱,D是含+3价元素的氯化物。以上物质间发生下列反应:
①A、B的溶液相混,产生不溶于稀硝酸的白色沉淀。
②B、C的溶液完全反应后,得到食盐溶液。
③C、D的溶液相混,出现红褐色沉淀。
试推断写出A、B、C、D的化学式:
A:______________;B:______________;
C:____________ _;D:______________。
15.A、B、C、D四个试剂瓶中分别盛碳酸钠、硝酸银、烧碱、稀硫酸四种稀溶液中的一种,取四种溶液各
;
A
B C D
X白色沉淀白色沉淀白色沉淀无现象
稀硝酸\
沉淀不消失
沉淀消失
有气体产生
沉淀不消失无现象
(1)物质X的化学式是_________。
(2)物质B是_______________,加入X后反应的化学方程式是__________________,加稀硝酸后,沉淀消失的反应化学方程式是___________________________。
(3)为进一步区别A和C,可根据置换反应的原理进行实验,写出其中一个反应的化学方程式___________________________。
参考答案
1.(1)CuO (2)3CO+Fe2O3 2Fe+3CO2↑干冰人工降雨(3)Fe+CuCl2==FeCl2+Cu —
(4)①反应中稀盐酸过量与铁反应放出氢气H2+CuO Cu+H2O
2.(1)CO2;BaSO4;BaCl2
(2)Na2CO3;Na2SO4;NaCl
3.(1)氢氧化镁[或Mg(OH)2] 氯化钠、氢氧化钠、氯化钡(或NaCl、NaOH、BaCl2)除去滤液D中的NaOH和Na2CO3
(2)增大氯化钾(或KCl)
4.Fe;Fe2O3;FeSO4;CO
5.(1)CuSO4、Na2SO4;BaC12、Na2CO3(2)NaCl (3)NaCl
6.(1)BaCO3;CO2
(2)Na2CO3;Na2SO4、KNO3;NaCl
~
(3)除去Na2CO3
7.盐酸氢氧化钠产生红褐色沉淀
3333NaOH FeCl Fe OH NaCl +=↓+() 氯化钠 8.(1)CaCO BaCO 3
3 (2)FeCl Na SO 324、 (3)Ba OH CaCO ()23、
(4)Ba OH CaCO NaOH ()23、、(写对两个给1分,全写对给2分)
Ba OH CaCO BaCl Ba OH CaCO BaCl NaOH BaCl CaCO NaOH
()()232
23223、、、、、、、
9.(1)Ag 、Cu 、Fe
(2)FeSO H SO 424、(或FeSO CuSO 44、)
(3)Fe H SO FeSO H +=+↑2442(或Fe CuSO FeSO Cu +=+44 10.(1)Fe O 23 CaCO 3
…
(2)CaCO HCl CaCl H O CO 32222+=++↑ (3)CaCO CaO CO 3
2高温
+↑
Fe H SO FeSO H +=+↑2442 (或)Fe HCl FeCl H +=+↑222 Fe O CO
Fe CO 232323++高温
Fe SO Ca OH Fe OH CaSO 243234323()()()+=↓+ (写出“”不扣分)CaSO 4↓
]3)(2)(32[2323CaCl OH Fe OH Ca FeCl +↓=+或 11.(1)CaCO 3、Fe(NO 3)3 NaCl
(2)H SO Ba OH H O BaSO 242242+=+↓()
MgCl Ba OH Mg OH BaCl 2222+=↓+()()
12.(1)H SO Na CO Na SO H O CO 24232422+→++↑
(2)蓝色沉淀;Ba OH CuCl BaCl Cu OH ()()2222+→+↓ (3)NaCl
(4)Ba OH Na SO BaSO NaOH ()22442+→↓+ Ba OH Na CO BaCO NaOH ()22332+→↓+
13.(1)NaCl NaOH
(2)H SO Na CO Na SO H O CO 24232422+=++↑ Na CO Ba OH BaCO NaOH 23232+=↓+()
(3)Cu OH ()2;Fe OH ()3;Mg OH ()2;Al OH ()3等(写出三个全对的化学式给1分,若不写、少写、错写化学式则不给分,不出现分) 14.A :AgNO 3 B :HCl C :NaOH
D :FeCl 3
15.(1)2BaCl
(2)碳酸钠(或32CO Na 或纯碱)
↑
++=++↓=+2223333232)(22CO O H NO Ba HNO BaCO NaCl BaCO BaCl CO Na
(3)Ag NO Fe AgNO Fe 2)(2233+=+(或↑+=+2442H FeSO SO H Fe
