有机化学第二版(高占先)(全14章答案完整版)_第8-14章(1)

有机化学第二版(高占先)(全14章答案完整版)_第8-14章史上最全的《有机化学第二版(高占先)》全14章答案完整版!!其中包括各种判断题、推断题、思考题以及合成题的答案!!
Ps:亲!给好评,有送财富值哦! #^_^!!
第8章卤代烃
8-2 完成下列各反应式。
(CH3)3CBr C2H5OH(CH3)2C=CH2
+
CH3CH=CH2HBr
+O O
CH3CH2CH2CH3CH2CH2CN
NaCN
(1)
(2)
(CH3)2CHCH=CH2Br
+500℃(CH
3
)2CCH=CH2
Br H2O
(CH3)2C=CHCH2Br +
(CH3)2CCH=CH2
OH
(CH3)2C=CHCH2OH +
(3)
NaCN
KOH
25
(4)
(5)
(6)ClCH=CHCH2Cl CH3
+ClCH=CHCH23
O
Br
Br
Br
CN
CH2CHCH3
Br
CH=CHCH3
CH3 Br
2
NH3(l)
CH3
NH2
CH3
2
+
Cl
Cl NO2
NaOH-H2O
OH
Cl
NO
2
ZnCl2
(HCHO + HCl)
+
CH2Cl
Mg
CH2MgCl CH2COOH ClCH2CHCH2CH2CH3
PhCH2MgCl
CH3
+PhCH2CH2CHCH2CH2CH3
CH3
(7)
(8)
(9)
(10)
3
RC CLi
(11)
RC CR'
RC CCOOH
RC CCH2CH2OH
CHBr3
Br
Br
(12)
8-3写出下列反应主要产物的构型式。
C2H5
CH 3NaI
+C
C2
H5
CH3
NaSCH3
+
(S N2)
(S N2)
(S N2)
CH3
I
2
(CH2)4CH3
H
H2O
CH3
H
CH2(CH2)4CH3
HO
C
Br
CH2CH2CH3CCH2CH3
H2
Lindar催化剂
C
H
C
CH2CH2CH3
H
(1)
(2)
(3)
(4)
3
KOH
25
3
H3t-BuOK
t-BuOH, △
H3C
Ph Ph
H
C6H5
H3C H
6
H5
H Br
C6H5
H C6H5
CH3
2525
Br
(H3C)2HC
CH3
(H3C)2HC
CH3
CH3
H Br
CH2CH3
H Br
C2H5CH3
25
Zn
t-BuOK
(E2反式消除)
(E2反式消除)
(E2反式消除)
(顺式消除)
(E2反式消除,但很慢)
(5)
(6)
(7)
(8)
(9)
8-4比较下列每对亲核取代反应,哪一个更快,为什么
(1)B>A (亲核性C2H5O->C2H5OH)
(2)A>B (烯丙型卤代烃活泼)
(3)B>A (极性非质子溶剂有利于S N2反应)
(4)A>B (亲核性-SH>-OH)
(5)A>B (亲核性硫比氮强)
(6)B>A (离去能力I->Cl-)
8-5卤代烷与NaOH在H2O-C2H5OH溶液中进行反应,指出哪些是S N2机理的特点,哪些是S N1机理的特点
(1)产物发生Walden转化; S N2
(2)增加溶剂的含水量反应明显加快; S N1
(3)有重排反应产物; S N1
(4)反应速率明显地与试剂的亲核性有关; S N2
(5)反应速率与离去基的性质有关; S N2和S N1
(6)叔卤代烷反应速度大于仲卤代烷。 S N 1 8-6 把下列各组化合物按发生S N 1反应的活性排列成序。
(1)A. 正溴丁烷 B. 2-溴丁烷 C. 2-甲基-2-溴丙烷
(CH 3)3Br Br
CH 2CH 2Br
A. B.
C.
(2)
(3)A. CH 3CH 2Cl B. CH 3CH 2Br C. CH 3CH 2I (1)C >B >A ; (2)A >C >B ; (3) C >B >A 。 8-7把下列各组化合物按发生S N 2反应的活性排列成序。
A. B. C.CH 3CH 2Br C CH 3
H 3C
CH 3
CH 2Br
H
CH 3
H 3C
CH 2Br
B.
B. C.
CH 2=CHBr BrCH 2CH=CH 2CH 3CHBrCH 3Br
Br
Br
C.
A.A.
(1)(2)(3)
(1)A >C >B ; (2)B >C >A ; (3)B >A >C 。 8-8把下列各组化合物按发生E2反应速率由快至慢排列成序。
B.
B. C.C.
A.A.(1)(2)CH 3CH CH CH Cl H 3
3
H 33
H 33
H 3C
CH 3
H 3C
CH 3
CH 3
Br
CH 2=CH CH CH Cl
(1)B >A >D >C ; (2)A >B >C 。
8-9 把下列各组组化合物按E1反应速率由快至慢排列成序。
A. D.
(2)C CH 3
H 3C
Br
CH 2CH 3
H C
CH 3H 3C
H C
B.
B. C.
C.
A.
(1)CH 3
Br
BrCH 2CH 2CHCH 3
3
CHBrCH 3
CHBrCH 3
CHBrCH 3
CHBrCH 3
NO 2
OCH 3
CH 3
(1)C >D >A >B (E1反应中间体为碳正离子,连给电子基有利于中间体稳定); (2)A >B >C (从碳正离子稳定性考虑)。
8-10 将下列各组化合物按照对指定试剂的反应活性由大到小排列成序。 (1)在2%AgNO 3乙醇溶液中反应。
A.
H
C Cl
H 3C
CH 3
B. C.
(CH 3)3CCl
CH 3CH 2Cl
(2)在碘化钠的丙酮溶液中反应。
A. D.
B.
C.CH 3CH 2CH 2CH 2Br CH 3CHCH 2CH 3
Br
CH 2=CHBr
BrCH 2CH=CH 2
(1)C >B >A (S N 1反应); (2)A >C >D >B (S N 2反应)。 8-11 把下列各组中的基团按亲核性从强至弱排列成序。
(1)A. C 2H 5O - B. HO - C. C 6H 5O - D. CH 3COO -
(2)A. R 3C - B. R 2N - C. RO - D. F - (3)A. CH 3O - B. CH 3CH 2O - C. (CH 3)2CHO - D. (CH 3)3CO -
(1)A >B >C >D ; (2)A >B >C >D ; (3)A >B >C >D 。 8-12 用化学方法区别下列各组化合物。
CH 2=CHCl CH 3C CH CH 3CH 2CH 2Br
A. B. C.n -C 4H 9Cl
n -C 4H 9I
n -C 6H
14
A. B. C.
D.
(1)(2)
(1)Na
-+-H 3CC
CNa
A B
C
A
C
AgNO 3/C 2H 5OH
-
+
(2)+A
C D
Br 2/CCl 4
试剂
(褪色)
--
-
8-13 给出下列反应的机理。
CH 3CH=CHCH 2Br
H 2O
CH 3CH=CHCH 2OH CH 32OH
(1)( ± )+
CH 3CH=CHCH 2Br
CH 3CH=CHCH 2
2O
2O
CH 3
2OH
2
CH 3CHCH=CH 2
OH -H +
+
CH 3CH=CHCH 2OH
CH 32
OH
Br
(1)CH 32
N CH 3
CH 2CH 2NHCH 乙醚
N N CH 3
3(2)
N CH 3
CH 2CH 2NHCH 乙醚
(2)
3
CH 33
N
N CH 33
Br
OH
O
+
+
+
50%C 2H 5OH-H 2O
(3)
2
OH
O
OH 2
OHC 2H 5
-H +
+
8-14 从丙烯开始制备下列下列化合物。
CH 3CHDCH 3CH 3CH 2CH 2C CCH 3
CH 2=C
Br
CH 3
H C C CH 3
Br Br
(1)(2)(3)(4)
(1)CH 3CH=CH 2
CH 3CHCH 3
Br
CH 3CHCH 3
MgBr
2CH 3CHCH 3
CH 2=C
Br
CH 3
(2)CH 3CH=CH 2
2
CH 3CHCH 2
CH 3C
KOH/n -C 4H 9OH
CH
1mol HBr
2CH 3CH 2CH 2Br
CH 3CH 2CH 2C
CCH
3
(3)CH 3CH=CH 2HBr CH 3C
利用(2)中制备的NH 3(l)CH 3C
CNa
2
H C C CH 3
Br Br Br Br (4)CH 3C
利用(2)中制备的
8-15 由指定原料合成下列化合物。
(1)(2)CH 3CHCH 3CH 3CH CH 3CH 2Cl CH 2CH 3CHCH 2Cl 3
CH 2=CHCH 2CH 2CH(CH 3)2
由和合成由和合成CH 3CH=CH CH=CH 2
KOH/醇,△(1)Cl 2
乙醚
CH 3CHCH 3CH 3CHCH 2Cl
CH 3
CH 2=CHCH 2CH 2CH(CH 3)2
CH 3CH=CH 2
ClCH 2CH=CH Mg 2=CHCH 2MgCl
KOH/醇,△
Cl 2乙醚
利用(1)中制备的CH 2=CHCH 2CH 2CH 3
ClCH 2CH=CH CH 3CH 2Cl
Mg 3CH 2MgCl
CH 2=CHCHCH 2CH 3
(2)CH 3CH=CH CH=CH 2
8-16 列出以碳正离子为中间体的5类反应,并各举一例加以说明。 (1)亲电加成反应,如烯烃与HX 加成;
(2)亲电取代反应,如芳烃的Friedel-Crafts 烷基化反应; (3)S N 1反应,如叔卤代烃的取代反应; (4)E1反应,叔卤代烃的消除反应; (5)重排反应
(CH 3)2C 2H 5
(CH 3)2C=CHCH 3
AgNO 3-C 2H 5OH
(CH 3)3CCH 2Cl
CH 2CH 3+
8-17 推测化合物构造式。(利用1
H NMR 谱推测结构)
CH 2=C(CH 2Cl)2CH 3C=CHCH 2Cl
A. B.
8-18 试写出A~H 的构造式及各步反应式。(涉及到烯烃、二烯烃和卤代烃的化学性质)
(CH 3)2C=CH 2
3)2C=CH 高温
(CH 3)22CH 2C(CH 3)2
(CH 3)2CClCH 2Cl
22CH 2C=CH 2
ClCH 2C=CH 2
CH 3
CH 3
3
Na
A B
C
D
E
CH=C(CH 3)2
F
HOOCCCH 2CH 2CCOOH
CH 33
CH 3
3
8-19 推测A 、B 、C 的构造式(标明立体构型)。
(烯丙位卤代烃的亲取代 ,取代化合物旋光
性判断)
2A
B
C
CH 3
Cl
3
CH 3
HO
(R, S
)
S N 1
(无旋光性)
33H 2O N 3333
+H 3CH 2
8-20 略
8-21 解释下列结果。
(
1)在极性溶剂中,3°RX 的S N 1与E1反应速率相同。
S N 1与E1反应的控速步骤是相同的(生成碳正离子的一步为控速步),因而,反应速率也是相同的。 HI (CH 3)3CI H 2O OH -+(CH 3)3CI (CH 3)3COH +++(CH 3)2C=CH 2H 2O I -
+(2)
在亲核性溶剂中,如果不存在强碱,3°RX 发生溶剂解反应;如果存在强碱(OH -、RO -
等)时,3°RX 主要发生E1消除反应。
HCl
CH 3CH 2SCH 2CH 2Cl H 2O +n -C 6H 13Cl +(3)
CH 3CH 2SCH 2CH 2OH 2
n -C 6H 13OH H 2O
+HCl
+k 1 / k 2 = 3×103
S
OH
-Cl-
硫原子的邻位参与作用有利于氯原子的解离。
H O, OH-
CH3
H Br
3
HO H
CH3
H OH
3
HO H
( dl )
(4)
+
CH3
H Br
3
HO H
CH3
H OH
3
HO H
H
HO
3
CH3
Br H
OH
H3C
H
CH3
Br
3H
=
=-
CH3
HO H
3
H OH
HOBr
(5)H
2
C C
H
C CH3
CH3
H3C C C CH2Br
CH3
O
CH3
H
C
H3C
CH3
H3C
C C CH2Br
CH3
O
CH3
2
H32
H
C
C
3
C
CH3
O
H
Br
-H+
8-22比较下列化合物的结构和性质。
(1)苯与六氟代苯的结构及物理性质。
(
2
)已烷与全氟已烷的稳定构象及溶解性。
苯的结构六氟苯的结构
(1)
物理性质相似。苯的熔点℃,沸点80℃;六氟代苯的熔点℃,沸点℃。
(2)已烷是平面锯齿状结构,全氟已烷非平面锯齿状,而是扭转成棒状。已烷沸点69℃,溶于有机溶剂中,不溶于水;而全氟已烷不溶于有机溶剂也不溶于水,形成氟相。
第9章醇、酚、醚
9-1 命名下列化合物。
CH 3CH
OH
C
CH
O O
O O
O OH
H 3C
OCH 3
OH
CH 2OH
Ph
CHCH 2CH 2CH 3OH
PhOCH 2CH=CH 2O
OCH 3
H 3CO
O
CH 2CH 3
CH 3(CH 2)10CH 2SH
CH 3SCH 2CH 3
O 2S
(1)(2)
(3)
(4)
(5)
(6)
(7)(8)(9)
(10)(11)(12)
(1)3-丁炔-2-醇; (2)15-冠-5; (3)(1R )-5-甲基-2-异丙基环已醇; (4)3-甲基-5-甲氧基苯酚; (5)3-羟甲基苯酚; (6)1-苯基-1-丁醇; (7)苯基烯丙基醚; (8)4,4’-二甲氧基二苯醚; (9)1,2-环氧丁烷; (10)正十二硫醇; (11)甲乙硫醚; (12)二苯砜。 9-2 完成下列反应
(1)
25
H 3C 6H
5
25
H 3C 6H 5
2H 5
3
(S N i 反应,构型保持)
(S N 2反应,构型翻转)
H
OH CH 3
H PBr 3
H
H CH 3Br
(S N 2反应,构型翻转)
(CH 3)3CCH 2OH
24
CrO 3,
(CH 3)2C=CHCH 3(E1反应,碳架发生重排)
HO
OH CH 3
N
O
OH
CH 3
(弱氧化剂不能氧化叔醇和双键)
O
3OH
(S N 2反应,进攻位阻较小的碳原子)
(2)
(3)(4)
(5)
OH HCO 3H H 2O / H
(6)
OH
H OH
OH
H +
(中间产物为环氧化物,亲核试剂进攻两碳原子的几率相等)
CH 3AlCl 3(8)OH
+O CH 3O
OH
C
O CH 3
(Fries 重排,热力学控制产物)
(7)
OH OH
O
O
O (频哪醇重排)
(邻二醇氧化)
222(10)
O CH 2CH=CHCH 2CH 3OH
(1) NaOH (9)
OH
OH
O
O (亲核取代反应)
H 3C
CH 3
*
OH
H 3C
3
2CH=CHCH 2CH 3
*(发生两次Claisen 重排)
OH OHC +
(Reimer-Tiemann 反应)
(11)
C 2H 5SH
(13)
CH 3CH 2CHCH 2CH 3
(15)
CH 3Br +
(12)OCH 3
+
CH 3CH 2CHCH 2CH 3
OH
+(S N 2反应)
O
HO
Br
HBr
(S N 1反应)
(CH 3)2CHCH 2CH 2CH 2Br
+OH
(CH 3)2CHCH 2CH 2CH 2SVH 2CH 3(S N 2反应)
OH H
Cl
H H OH H OH
OH
H
OH
H (1) OH (2) H 2O
(14)
9-3 将下列各组组化合物按酸性由强至弱排列成序。
OH
OH
OH
OH
OH
NO 2NO 2
NO 2
NO 2
CH 3
A.
B.
C.
D.
E.
OH
OH
OH
OH
OCH 3
OCH 3
3
A.
B.
C.
D.
(1)(2)
(1)D >B >C >A >E ; (2)B >A >D >C 。 9-4 将下列化合物按分子内脱水反应的相对活性排列成序。
OH
OH
A. B.
C.
A.
B. C.(1)(2)CHCH 3OH
CH 3CH 2CH 2OH
CH 2=CHCHCH 3
(CH 3)2CHOH
(1)B >A >C ; (2)B >A >C 。
9-5 将下列各组化合物按与氢溴酸反应的相对活性排列成序。
CH 2OH A. B. C.(1)(2)CH 2OH CH 2OH
H 3C O 2N CH 2OH
A.
B.
C.
CHOH CH 2CH 2OH
CH 3
(1)B >A >C ; (2))B >A >C (从中间体碳正离子稳定性考虑)。 9-6 试写出除去下列化合物中少量杂质的方法和原理。
(1)C 2H 5OH 中含有少量H 2O ;(2)(C 2H 5)2O 中含有少量H 2O 和C 2H 5OH ; (3)C 2H 5Br 中含有少量C 2H 5OH ;(4)n -C 6H 14中含有少量(C 2H 5)2O 。 (1)加Mg ,加热回流,蒸出乙醇;
(2)先加CaCl 2除大部分水和乙醇,再加入钠,蒸出乙醚;
(3)用H 2SO 4洗涤,分液,蒸出C 2H 5Br 。醇可H 2SO 4与形成烊盐并溶于H 2SO 4中。 (4)用H 2SO 4洗涤,分液,蒸出n -C 6H 14。 9-7用化学方法鉴别下列各组化合物。
OH
E. D.C.B. C.(1)(2)CH 3CH 2CH 2CH 2OH
CH 3CH 2CHCH 3
OH
(CH 3)3COH
A.
B.CH 2=CHCH 2Br
CH 3CHCH 2OH
OH
(CH 3)3CBr
CH 3CH 2OCH 2CH 3
n -C 4H 10
F.A.
(1)
A
B C 试剂片刻混浊
浓HCl/ZnCl 2
片刻混浊
(2)
FeCl 3A B
C
试剂
D
E F
(蓝紫色)(褪色)
溶
浓H 2SO 4
Br 2/CCl 4
(1)HIO 4,(2)AgNO 3AgNO 3/C 2H 5OH
+
++
+
9-8 完成下列转化。
(1)
CH 2Br CH 2CH
CH 2
O
CH 2CH
CH 2O
Mg
3CH 3CO 3H
H +
CH 2
Br
CH 2MgBr
CH 2CH 2CH 2OH CH 2CH=CH 2
方法之二
CH 2Br
3CH 2C
CH
CH 2CH
CH 2
O CH 3CO 3H
2CH=CH 2
(2)
OH 3
OH
3
CHCH=CH 2
CH 3
NaOH
CH 3CH=CHCH 2Cl
OH
CH
3
OH
CH 3
CHCH=CH 2
CH 3
ONa
CH 3
OCH 2CH=CHCH 3
CH 3
(3)
卤代烃与NaCN 反应,虽然能制备目标产物,但不是理想的合成路线,因为NaCN 是剧毒物。
(4)
OH OH
Cl
OH
H 3O
OH
浓H 2SO 4
3OH
SO 3H
(5)
O
O
O
O
O
O Cl NaCl
ONa
+
+
9-9 用适当的原料合成下列化合物。
(4)
(1)
(3)CH 3CH 2CH 2OCH(CH 3)2
(2)CH 3CH 2OCH=CH 2O
H 3CH 2C
CH 2CH 2OH
(CH 3)3CCHOCH(CH 3)2
3
(1)O
3CH 2CH 2OCH(CH 3)2
△(2)
3CH 2OCH=CH 2
(1)
324+
(CH 3)2CHONa
CH 3CH 2CH 2CH 3CH 2OH
3CH 2OCH 2CH 2OH
+
O CH 2CH 3
CH 2CH 2
OH
OC 2H 5
MgBr
O
+(CH 3)3CCH=CH 2(1) Hg(OOCCF 3)2
4
(4)(CH 3)2(CH 3)3CCHOCH(CH 3)2
CH 3
该反应生成醚可避免消除重排等副反应,但所用试剂毒性较大。
9-10 化合物A 是一种性引诱剂,请给出它的系统命名法的名称,并选择适当原料合成化合
物A 。
A 的名称:(7R ,8S )-2-甲基-7,8-环氧十八烷。
(1) B 2H 6
2-252
A Br
OH
CH 3CO 3H
(±)
9-11 推测下列反应的机理,并用弯箭头表示出电子转移方向。
HO
3(1)
HO
3
3 (2)
H
CH 2OH
△
+
H +
重排
+
CH 3OH (3)
+
3Ph
H 3CO (±)(±)
CH3OH
+
3
Ph
H3CO
(±)(±)
Ph
HO CH3
Ph
H3CHO
(±)+(±)
(4)
H2
O
(5)
H
+
O
OH
H+
OH
OH
H
重排
(6)(CH3)2C C(CH3)2
I
OH
(CH3)3C C CH3
O
Ag+
H
AgI
重排
(CH3)2C C
I
OH
(CH3)3C C CH3
O
Ag+
CH3
CH3(CH
3
)2C
OH
3
CH3(CH3)2
CH3
CH3 (CH3)2C C
CH3
OH
CH3
9-12推断A、B、C的构造式。(利用酚的性质,烯烃的氧化,Claisen重排)
各化合物之间的关系如下:
HCHO
A (C 10H 12O)
10H 12O)
200℃
(1)NaOH,(2)CH 3Br
(1)O 3, (2)Zn, H 2O 3
NaOH
3, (2)Zn, H 2O 3(1) KMnO 4, OH -(2) H 3O
COOH
OCH 3
化合物B 的信息较多,是解题的关键。
OH
CH 2CH=CHCH 3
O
H C
CH=CH 2
CH 3
OCH 3
CH 2CH=CHCH 3
A
B C
9-13 推断A 的构造式,并标明质子的化学位移及红外吸收的归属。(利用酚的性质、IR 谱
和1
H NMR 谱)
化合物A 的不饱和度为4,可能含有苯环;A 能溶于NaOH 溶液,但不溶于NaHCO3溶液,可能为酚;结合IR 谱数据可知,A 为对位二取代(830cm -1
有吸收峰)酚类。再结合1
H NMR 数据可推测A 可能的构造式为:
OH
(H 3C)3C
1.3
7.0
4.9
(9H,s)
(4H,m)
(1H,s)δ:
IR :3 250cm -1
为νO —H 伸缩振动吸收峰;830cm -1
为νAr —H (面外)弯曲振动吸收峰。 9-14 推测化合物构造式。(醇的亲核取代反应,消去反应,烯烃的氧化反应、水解反应)
CH 3
CH 3
OH
OH
CH 3
CH 3
CH 3
CH 3
HO
HO
A.
B.
C.
9-15 为什么RX 、ROH 、R —O —R 都能发生亲核取代反应试说明它们发生亲核取代反应的异同
点。
自己归纳总结。(抓住结构与性质的关系,亲核取代反应) 9-16 说明烯丙基卤与烯丙基醇,苄卤与苄醇的取代反应有何异同。
自己归纳总结。(抓住结构与性质的关系)
9-17试说明HI分解醚的反应是如何按S N2或S N1机理进行的,为什么HI比HBr更好醚有弱碱性,与HX生成烊盐,加大了C—O键的极性,C上正电荷更高,X-对其进行亲核进攻,醚键断裂,发生了S N2反应;如果是叔丁基醚,由于叔丁基碳正离子较稳定,反应以S N1机理进行。
HI比HBr更好,因为前者酸性较强,有利于生成烊盐,且亲核性I->Br-
9-18为什么醚蒸馏前必须检验是否有过氧化物存在(RCH2)2O和(R2CH)2O哪个更容易生成过氧化物
久置的醚中可含有过氧化物。在蒸馏乙醚时,其中含有的过氧化物因乙醚的蒸出而浓度逐渐增大,受热时会发生爆炸。因此,蒸馏醚前必须检验是否有过氧化物存在。可用KI淀粉试纸进行检验,如果试纸变蓝,则表示有过氧化物,则可以向醚中加入5%FeSO4溶液,经充分搅拌,可以破坏其过氧化物。醚的过氧化物的形成是自由反应,(R2CH)2O比(RCH2)2O更容易形成过氧化物。
9-19说明实验现象。(反应介质对S N2、S N1机理的影响)
(CH3)3COCH
3
I(CH3)3COH
CH3OH(CH
3
)3CI +
+
在乙醚中,反应介质的极性较低,有利于S N2机理,亲核试剂I-进攻空间位阻小的甲基碳原子;在水溶液中,反应介质的极性很强,有利于S N1机理,生成较稳定的叔碳正离子中间体。
9-20试说明实验现象。(环醚在不同介质中开环反应机理及开环规律)
在酸性介质中,H+催化反应按S N1机理进行,生成较稳定的碳正离子。在碱性介质中,反应按S N2机理进行,亲核试剂进攻空间位阻小的碳原子。
第10章醛、酮、醌
10-1 命名下列化合物。
(1)3-甲基-1-苯基-1-戊酮;(2)2,4,4-三甲基戊醛;(3)1-(1-环已烯基)
丁酮;
(4)(E )-苯基丙基酮肟; (5)3-丁酮缩乙二醇; (6)2-环已烯酮; (7)三氯乙醛缩二甲醇; (8)2-戊酮苯腙; (9)2,6-萘醌; (10)2,4-已二酮; (11)((E )-间甲基苯甲醛肟。 10-2 写出下列反应的主要产物。
PhCHO
HCOONa +浓NaOH
HCHO
2OH
+
(Cannizzaro 反应)
O
Zn-Hg / HCl
HCN
H 3O
OH COOH
O
(Clemmensen 还原)
H 3C
C CH 3
O Mg
66
H 3O
H 2SO 4
△
(CH 3)2C C(CH 3)2OH OH
(H 3C)3C
C CH 3
O
(pinacol 重排)(1)(2)
(3)
(4)
+
HCHO
(Mannich 反应)
+
HCl
(5)
(6)
O
N H
CH 2CH 2N
O
CH 3
O
CH
3
CH 3
OH
(黄鸣龙还原)
CO 3Cl
+
CO 2H
Cl
+
(Baeyer-Villiger reaction)
O
NH 2+
PCl 5
H N
O
(Beckmann 重排)
O
(1) HSCH 2CH 2SH
2O
(1) Cl 2 / NaOH 3OH
O
(卤仿反应)(7)
(8)(9)
(10)
CHCl 3
+
(Wittig reaction)
CH 3MgBr +
Ph 3(1) CuCl 3(13)
(12)
(11)O
+O
(1,4-加成产物
)
O
CHCH 2CH 3
O O
OH
HO
NC
O
(双烯合成反应)
10-3 比较下列化合物的亲核加成反应活性。
(2)
(1)C O
CH 3
H 3C C CH 3
O
H 3C
C H
O
C
O
CH 3
H 3C
(3)(4)
(3)>(1)>(2)>(4)
10-4 将下列化合物按烯醇式的含量多少排列成序。 CH 3COCHCOCH 3
CH 3COCH 2CH 3
(2)(1)Ph
C H 2
C O
(3)(4)3
CH 3COCH 2COCH 3
C CH 3
O
(1)>(4)>(3)>(2)
10-5 指出下列化合物中,哪些能发生碘仿反应哪些能与饱和NaHSO 3反应
(2)(1)O
(3)(4)(5)ICH 2CHO
CH 3CH 2CHO
C 6H 5COCH 3
CH 3CHO
CH 3CH 2CH 2OH
CH 3CH 2CCH 2CH 3
CH 3CH 23
OH
(7)(6)(8)
O
能与饱和NaHSO 3反应的有(1)、(2)、(5)、(8)[脂肪族甲基酮、大多数醛和8个碳以下的脂肪酮能进行此反应]。
能发生碘仿反应的是(1)、(3)、(4)、(5)。 10-6 用简单的化学方法区别下列化合物。
(1)2-已醇 (2)2-已酮 (3)3-已酮 (4)已醛
有机化学第二版高占先全章答案完整版第章精编版
有机化学第二版高占先全章答案完整版第章精 编版 MQS system office room 【MQS16H-TTMS2A-MQSS8Q8-MQSH16898】
有机化学第二版(高占先)(全14章答案完整版)_第1-7章史上最全的《有机化学第二版(高占先)》全14章答案完整版!!其中包括各种判断题、推断题、思考题以及合成题的答案!! Ps:亲!给好评,有送财富值哦! #^_^!! 1-3 写出下列化合物短线构造式。如有孤对电子对,请用黑点标明。 1-5 判断下列画线原子的杂货状态 (1)sp2,(2)sp,(3)sp,(4)sp3,(5)sp,(6)sp。 1-6哪些分子中含有极性键?哪些是极性分子?试以“”标明极性分子中偶极 矩方向。 答:除(2)外分子中都含有极性键。(2)和(3)是非极性分子,其余都是极性分子。分子中偶极矩方向见下图所示,其中绿色箭头所示的为各分子偶极矩方向。1-7 解释下列现象。 (1)CO 2 分子中C为sp杂化,该分子为直线型分子,两个C=O键矩相互抵消,分子偶极矩为零,是非极性分子;而SO2分子中S为sp2杂化,分子为折线型,两个S —O键矩不能抵消,是极性分子。 (2)在NH 3中,三个N—H键的偶极朝向N,与电子对的作用相加;而NF 3 中三个N —F键的偶极朝向F,与N上的未成对电子的作用相反并有抵消的趋势。 (3)Cl和F为一同主族元素,原子共价半径是Cl比F大,而电负性是F比Cl 大。键的偶极矩等于μ=qd,q为正电荷中心或负电荷中心上的电荷量,d为正负电荷中心的距离。 HCl键长虽比HF的长,但F-中心上的电荷量大大于Cl-上的电荷量,总的结果导致HF的偶极矩大于HCl。所以键长是H—Cl较长,偶极矩是H—F 较大。 1-8 将下列各组化合物中指定键的键长由长到短排列并说明理由。 答:(1)从乙烷,乙烯到乙炔,碳原子杂化态由sp3到sp2至sp,s成份提高,拉电子能力增强,虽同属于碳氢键但键长缩短。 (2)键长顺序为C—I>C—Br>C—Cl>C—F。因为卤素原子核外电子层数为I>Br>Cl>F,即其范德华半径为I>Br>Cl>F,则其原子共价半径I>Br>Cl>F。(3)碳碳键键长为乙烷>乙烯>乙炔。因为碳原子杂化态由sp3到sp2至sp,其共价键分别为单键、双键和叁键,碳碳原子间的作用力是乙烷<乙烯<乙炔,作用力越强,则两原子被拉得越紧,键长越短。 1-9 将下列各组化合物按酸性由强到弱排列。 (1)D>A>C>B;(2)A>B>D>C 1-10 下列物种哪些是:(1)亲核试剂,(2)亲电试剂,(3)既是亲核试剂又是亲电试剂? 答;(1)亲核试剂:Cl-,H 2O,CH 3 OH,CH 2 =CH 2 ,HCHO,CH 3 CN,-CH 3 ; (2)亲电试剂:H+, AlCl 3,Br+,Fe3+,+NO 2 ,HCHO,CH 3 CN,+CH 3 ,ZnCl 2 ,Ag+, BF 3 ; (3)既是亲核试剂又是亲电试剂: HCHO,CH 3 CN; (4)两者都不是的:CH 4 。 1-11 按质子酸碱理论,下列化合物哪些是酸?哪些是碱?哪些既是酸又是碱? 答:酸:NH 3,HS-,HBr,H 2 O,NH 4 +,HCO 3 -;
有机化学课后习题参考答案完整版
目录lin 湛
第一章绪论 扼要归纳典型的以离子键形成的化合物与以共价键形成的化合物的物理性质。 答案: NaCl与KBr各1mol溶于水中所得的溶液与NaBr及KCl各1mol溶于水中所得溶液是否相同?如将CH4及CCl4各1mol混在一起,与CHCl3及CH3Cl各1mol的混合物是否相同?为什么? 答案: NaCl与KBr各1mol与NaBr及KCl各1mol溶于水中所得溶液相同。因为两者溶液中均为Na+,K+,Br-, Cl-离子各1mol。由于CH4与CCl4及CHCl3与CH3Cl在水中是以分子状态存在,所以是两组不同的混合物。碳原子核外及氢原子核外各有几个电子?它们是怎样分布的?画出它们的轨道形状。当四个氢原子与一个碳原子结合成甲烷(CH4)时,碳原子核外有几个电子是用来与氢成键的?画出它们的轨道形状及甲烷分子的形状。 答案: 写出下列化合物的Lewis电子式。 答案: 下列各化合物哪个有偶极矩?画出其方向。 答案: 根据S与O的电负性差别,H2O与H2S相比,哪个有较强的偶极-偶极作用力或氢键? 答案: 电负性O>S,H2O与H2S相比,H2O有较强的偶极作用及氢键。 下列分子中那些可以形成氢键? b. CH3CH3 c. SiH4 d. CH3NH2 e. CH3CH2OH f. CH3OCH3 答案: d. CH3NH2 e. CH3CH2OH 醋酸分子式为CH3COOH,它是否能溶于水?为什么? 答案:能溶于水,因为含有C=O和OH两种极性基团,根据相似相容原理,可以溶于极性水。 第二章饱和烃 卷心菜叶表面的蜡质中含有29个碳的直链烷烃,写出其分子式。 答案:C29H60 用系统命名法(如果可能的话,同时用普通命名法)命名下列化合物,并指出(c)和(d)中各碳原子的级数。答案: a. 2,4,4-三甲基-5-正丁基壬烷5-butyl-2,4,4-trimethylnonane b. 正己烷 hexane ,3-二乙基戊烷 3,3-diethylpentane -甲基-5-异丙基辛烷5-isopropyl-3-methyloctane e.2-甲基丙烷(异丁烷)2-methylpropane(iso-butane) ,2-二甲基丙烷(新戊烷) 2,2-dimethylpropane(neopentane)
有机化学-第12章 习题解答
第12章 杂环化合物 1.解: (1) α-呋喃甲醛 (2) N -甲基-2-乙基吡咯 (3) 2-噻吩磺酸 (4) 3-吡啶甲酸 (5) 2-氨基嘧啶 (6) N -甲基-2-羟基咪唑 (7) 3-硝基-5-羟基吲哚 (8) 8-羟基-5-喹啉磺酸 (9) 4-乙基吡啶-N -氧化物 (10) 咪唑并[4,5-d]噁唑 (11) 咪唑并[2,1-b]噻唑 (12) 6-巯基嘌呤 N N NH 2 CH 3N S O 2N (13) N N H 2N (14) (15)(16) H S (20) (19) H (18) (17)N Br N H 3C CH 3 Br N SO 3 N 2.解: O NO 2 (1) (2) (3) (4) H N SO 3H S Br H N COCH 3 (5) (6) (7) (8) NH 2 N N COOH N Cl OCH 3 N CH 3 H (9)(11) (10) N N C 2H 5 NH 2 3 3 3N N N H 3C CH 3 H 3.解: (2)、(5)和(7)有芳香性。 4.解: (1) 4-甲基吡啶 > 吡啶 > 吡咯 (2) 四氢吡咯 > 氨 > 苯胺 > 吡咯 5.解: (1) 吡啶的未共用电子对在sp 2杂化轨道上,s 成分多,受到核的束缚强,不易给出电子,所以碱性弱。六氢吡啶是仲胺,未共用电子对在sp 3杂化轨道上,s 成分少,离原子核远,受核束缚力小,易给出电子,因而碱性强。 (2) 吡啶氮原子上处于sp 2杂化轨道的未共用电子对不参与形成大π键,能结合氢质子而显碱性。吡咯氮上的孤对电子参与了环的共轭体系,使氮上的电子云密度降低,因而难以与质子结合,碱性极弱,不能与酸形成稳定的盐。相反,由于这种共轭作用,吡咯的N-H 键极
有机化学第8章课后习题答案
第八章 立体化学 一、下列化合物有多少中立体异构体? 1. CH 3CH CH CH 3 Cl Cl CH 3CH 3 CH 3 CH 3 Cl H H H H H H 3CH 3 Cl Cl Cl Cl Cl 2. CH 3CH CH CH 3 Cl OH CH 3Cl CH 3 CH 3 CH 3 CH 3 CH 3 CH 3 CH 3 Cl Cl Cl OH OH OH OH H H H H H H H H 3. CH 3CH 3 CH CH CH 3 OH CH 3CH 3 H OH HO H CH(CH 3)2 CH(CH 3)24. CH 3CH CH CH CH 2CH 3 Cl Cl CH 3 CH 3 CH 3 CH 3CH 3 CH 3CH 3CH 3CH 2CH 3 CH 2CH 3 CH 2CH 3 CH 2CH 3CH 2CH 3CH 2CH 3CH 2CH 3CH 2CH 3Cl Cl Cl Cl Cl Cl Cl Cl Cl Cl Cl Cl Cl Cl Cl Cl Cl Cl Cl Cl Cl Cl Cl H H H H H H H H H H H H H H H H H H H H H H H H Cl 5. CH 3CH CH Cl Cl CH 3 6. CH 3CH(OH)CH(OH)COOH CH 3 CH 3COOH COOH CH 3 CH 3COOH COOH OH OH OH OH OH OH OH OH H H H H H H H H 7. BrCH 2CH 2CH O
3CH 2C=C=C H CH 2CH 3 H CH 3CH 2 C=C=C H CH 2CH 3H 9.1,3-二甲基环戊烷,三种 3CH 3CH 3 3 H H 二、写出下列化合物所有立体异构。指出其中那些是对映体,那些是非对映体。 解:颜色相同的是对映体,不同的为非对映体。 1. CH 3CH=CH CH CH 3 OH CH 3 C=C H H CH 3 H OH CH 3 H OH H C=C H CH 3H C=C CH 3 H OH H CH 3 CH 3 C=C OH H H CH 3 H 2. CH 3 CH 3 CH 3 3 3 3 H H 四种立体异构,两对对映体
有机化学 高占先(第二版)课后答案
有机化学(第二版)课后习题参考答案 第一章绪论 1-1 扼要解释下列术语. (1)有机化合物(2) 键能、键的离解能(3) 键长(4) 极性键(5) σ键 (6)π键(7) 活性中间体(8) 亲电试剂(9) 亲核试剂(10)Lewis碱 (11)溶剂化作用(12) 诱导效应(13)动力学控制反应(14) 热力学控制反应 答:(1)有机化合物-碳氢化合物及其衍生物 (2) 键能:由原子形成共价键所放出的能量,或共价键断裂成两个原子所吸收的能量称为键能。 键的离解能:共价键断裂成两个原子所吸收的能量称为键能。以双原子分子AB为例,将1mol气态的AB 拆开成气态的A和B原子所需的能量,叫做A—B键的离解能。 应注意的是,对于多原子分子,键能与键的离解能是不同的。分子中多个同类型的键的离解能之平均值为键能E(kJ.mol-1)。 (3) 键长:形成共价键的两个原子核之间距离称为键长。 (4) 极性键: 两个不同原子组成的共价键,由于两原子的电负性不同, 成键电子云非对称地分布在两原子核周围,在电负性大的原子一端电子云密度较大,具有部分负电荷性质,另一端电子云密度较小具有部分正电荷性质,这种键具有极性,称为极性共价键。 (5) σ键:原子轨道沿着轨道的对称轴的方向互相交叠时产生σ分子轨道, 所形成的键叫σ键。 (6) π键:由原子轨道侧面交叠时而产生π分子轨道,所形成的键叫π键。 (7) 活性中间体:通常是指高活泼性的物质,在反应中只以一种”短寿命”的中间物种存在,很难分离出来,,如碳正离子, 碳负离子等。 (8) 亲电试剂:在反应过程中,如果试剂从有机化合物中与它反应的那个原子获得电子对并与之共有形成化学键,这种试剂叫亲电试剂。 (9) 亲核试剂:在反应过程中,如果试剂把电子对给予有机化合物与它反应的那个原子并与之共有形成化学键,这种试剂叫亲核试剂。 (10) Lewis碱:能提供电子对的物种称为Lewis碱。 (11)溶剂化作用:在溶液中,溶质被溶剂分子所包围的现象称为溶剂化作用。 (12)诱导效应:由极性键的诱导作用而产生的沿其价键链传递的电子对偏移(非极性键变成极性键)效应称为诱导效应。它可分为静态诱导效应和动态诱导效应。 (13)动力学控制反应:在有机反应中,一种反应物可以向多种产物方向转变时,在反应未达到平衡前,利用反应快速的特点来控制产物组成比例的,称为动力学控制或速率控制。 (14) 热力学控制反应:在有机反应中,一种反应物可以向多种产物方向转变时,在反应未达到平衡前,用平衡到达来控制产物组成比例的,称为热力学控制或平衡控制。 1-2 简述处理化学键的价键法、分子轨道法和共振论。 答:价键法要点:价键的形成可看作是原子轨道的重叠或电子配对的结果。两个原子如果都有未成键的电子,并且自旋方向相反,则可以配对,也就是原子轨道可重叠形成共价键;重叠部分越大,所形成的共价键越牢固,因此要尽可能地使原子轨道让某一方向互相接近,以达到最大的重叠(共价键的方向性);一个原子的未成到电子如果已经配对,它就不能再与其他原子的未成对电子配对(共价键的饱和性);能量相近的原子轨道可以进行杂化,组成能量相等的杂化轨道,这样可使成键能力更强,体系能量降低,成键后可达到最稳定的分子状态。 分子轨道法要点:分子中的原子以一定的方式连接形成分子轨道,分子中的电子分布在分子轨道中,分子轨道可以由组成分子的原子轨道线性组合得到;分子轨道的数目与组成分子轨道的原子轨道数目相等;每个分子轨道有一定的能量,每个分子轨道只能容纳两个自旋方向相反的电子,即同样遵循能量最低原理、泡利不相容原理和洪特规则。
课件有机化学第14章 含氮化合物
第十四章
含氮化合物
Nitrogen Compounds
1
CONTENT
1 2 3 4 5 6
硝基化合物 胺的结构和物理性质 胺的制备 胺的化学性质 季铵盐化合物 重氮与偶氮化合物
2
14.1 硝基化合物
硝基化合物的结构(了解)
O R N O R N
O O
3
α-H 的反应
CH3(CH2)7CHO + CH3NO2 NaOH CH3CH2OH OH CH3(CH2)7CHCH2NO2
O CH3NO2 NaOH CH2NO2 RCH
ORCHCH2NO2 CH3CH2OH OH RCHCH2NO2
4
硝基化合物的还原反应
CH 3 NO 2 CH 3 H 2/ Ni 87 ~ 90% NH 2
CH(CH 3)2 CH 3 NO 2
CH(CH 3)2 CH 3 NH 2
Fe / HCl EtOH,
常用 常用 Fe // HCl HCl Fe Zn // HCl HCl Zn
NO 2 NO 2 SnCl2 浓 HCl CHO
74% NH 3
NH 2 NH 2 NaOH
5
CHO
CHO
Na2S, NaSH, (NH4)2S, NH4SH
NO2 NaSH EtOH, NO2 79 ~ 85% NH2 NO2 H2S, NH4OH EtOH, NO2 52 ~ 58% NO2
6
NH2
NO2 NH2 NH2
有机化学下册课后答案李景宁
第十二章羧酸(P32-33) 1.命名下列化合物或写出结构式: (1) 3-甲基丁酸 (2) 3-对氯苯基丁酸 (3) 间苯二甲酸 (4) 9,12-十八碳二烯酸 (5) 4-甲基己酸 CH 3CH 2 CH(CH 3 )CH 2 CH 2 COOH (6) 2-羟基丁二酸 HOOCCH(OH)CH 2 COOH (7) 2-氯-4-甲基苯甲酸 (8) 3,3,5-三甲基辛酸 2.试以反应式表示乙酸与下列试剂的反应 3.区别下列各组化合物:
4.指出下列反应的主要产物:(第四版保留) (1)C6H5CH2Cl 干醚 Mg C6H5CH2MgCl (1) CO2 (2) H2O C6H5CH2COOH SOCl2C6H5CH2COCl 4.完成下列转变: 5、怎样由丁酸制备下列化合物?
6、解: 7、指出下列反应中的酸和碱。 按lewis酸碱理论:凡可接受电子对的分子、离子或基团称为酸,凡可给予电子对的分子、离子或基团成为碱。 8.(1)按酸性降低的次序排列下列化合物: ①酸性: 水>乙炔>氨; ②酸性: 乙酸>环戊二烯>乙醇>乙炔 (2)按碱性降低的次序排列下列离子: ①碱性:CH3HC C CH3O >> ②碱性:(CH3)3CO>(CH3)2CHO>CH3O 9. 解:化合物A有一个不饱和度,而其氧化产物B含有两个不饱和度。产物 DC 5H 10 有一个不饱和度。从题意可知:D的结构式可能为环戊烷;C的结构为环戊 酮;B的结构为己二酸;A的结构式为环己醇。10.解:
(1)由题意:该烃氧化成酸后,碳原子数不变,故为环烯烃,通式为CnH2n-2。(2)该烃有旋光性,氧化后成二元酸,所以分子量=66*2=132。故二元酸为 CH3CH(CH2COOH)COOH 11.由题意:m/e=179,所以马尿酸的分子量为179,它易水解得化合物D和E,D 的IR谱图:3200-2300cm-1为羟基中O-H键的伸缩振动。1680为共扼羧酸的>C=O的伸缩振动;1600-1500cm-1是由二聚体的O-H键的面内弯曲振动和C-O 键的伸缩振动之间偶合产生的两个吸收带;750cm -1和700cm-1是一取代苯的 C-H 键的面外弯曲振动。再由化学性质知D为羟酸,其中和当量为121±1,故D的分 子量为122,因此,又由题意:E为氨基酸,分子量为75, 所以E的结构为H 2NCH 2 COOH。 第十三章羧酸衍生物(P77-78) 1.说明下列名词: 酯、油脂、皂化值、干性油、碘值、非离子型洗涤剂。 酯:是羧酸分子和醇分子间脱水形成的产物。 油脂:是高级脂肪酸的甘油醇酯。 皂化值:是指完全皂化1克油脂所需的KOH的质量(以mg为单位)。 干性油:是指那些在空气中放置后能逐渐变成有韧性的固态薄膜的油。 碘值:是指100克油脂完全加成时所能吸收的碘的质量(以克为单位)。 非离子型洗涤剂:此处实指非离子型表面活性剂,即在水溶液中不离解出正负离子的表面活性剂(此处的非离子型表面活性剂起主要的洗涤去污作用)。 2.试用方程式表示下列化合物的合成路线: (1)由氯丙烷合成丁酰胺;
(完整word)高职高专《有机化学》课后习题答案第八章
174 第八章 羧酸及其衍生物 思考与练习 8-1 命名下列化合物。 ⑴ 3-甲基-2-丁烯酸 ⑵ 2-甲基-2-乙基丙二酸 ⑶ 3-羧基-3-羟基戊二酸(柠檬酸) ⑷ 2-溴环戊基甲酸 8-2写出下列化合物的结构式。 ⑴ ⑵ ⑶ ⑷ 8-3将下列各组化合物按酸性由强到弱的顺序排列。 ⑴ > > > ⑵ > > > ⑶ > > 8-4写出丙酸与下列试剂作用的主要产物。 ⑴ CH 3CH 2COCl ⑵ CH 3CH 2COBr ⑶ (CH 3CH 2CO)2O ⑷ CH 3CH 2CONHCH 2CH 3 ⑸ CH 3CH 2COOCH 2CH 2CH(CH 3)2 ⑹ CH 3CH 2COONa 8-5完成下列化学反应。 8-6命名下列化合物。 ⑴ 异戊酰溴(3-甲基丁酰溴)⑵ 醋酸乙烯酯 ⑶ 苯甲酐 ⑷ N ,N -二甲基苯甲酰胺 ⑸ 2-甲基丁烯二酸酐 ⑹ 对氯苯甲酰溴 8-7写出下列化合物的构造式。 ⑴ ⑵ ⑶ COOH O 2N O 2N COOH CH 3COOH CH 3CH 3CH 2CHCOOH CH 3CH 3CH 2C CH 3COOH CH 3CH 2CHCOOH Cl CH 3COOH CH CH Cl Cl COOH O 2N CH 3CHCH 2CHCOOH 3 3 CH 3C CH 3COOH CH 3CHCH 2COOH CH 2COOH F COOH CH 3O CO OH COOH H 3C ( )1CH 3CH 2COOH 2CH 3CHCOOH Br +HBr CH 3 CH 3 ( )2 25 Δ C C O O O CH 3CH 2COOH + H Δ( )3CH 3CH 2COO +H 2O ( )4CH 3 CH CH 3 CH 3CH CH 3 COBr CH 3 CH CH 3 COCl SO 2HCl H 3PO 3+++C C O O O C C OCH 2 2 O O CH 3CON(CH 3)2
有机化学第二版(高占先)(全14章答案完整版)_第8-14章(1)
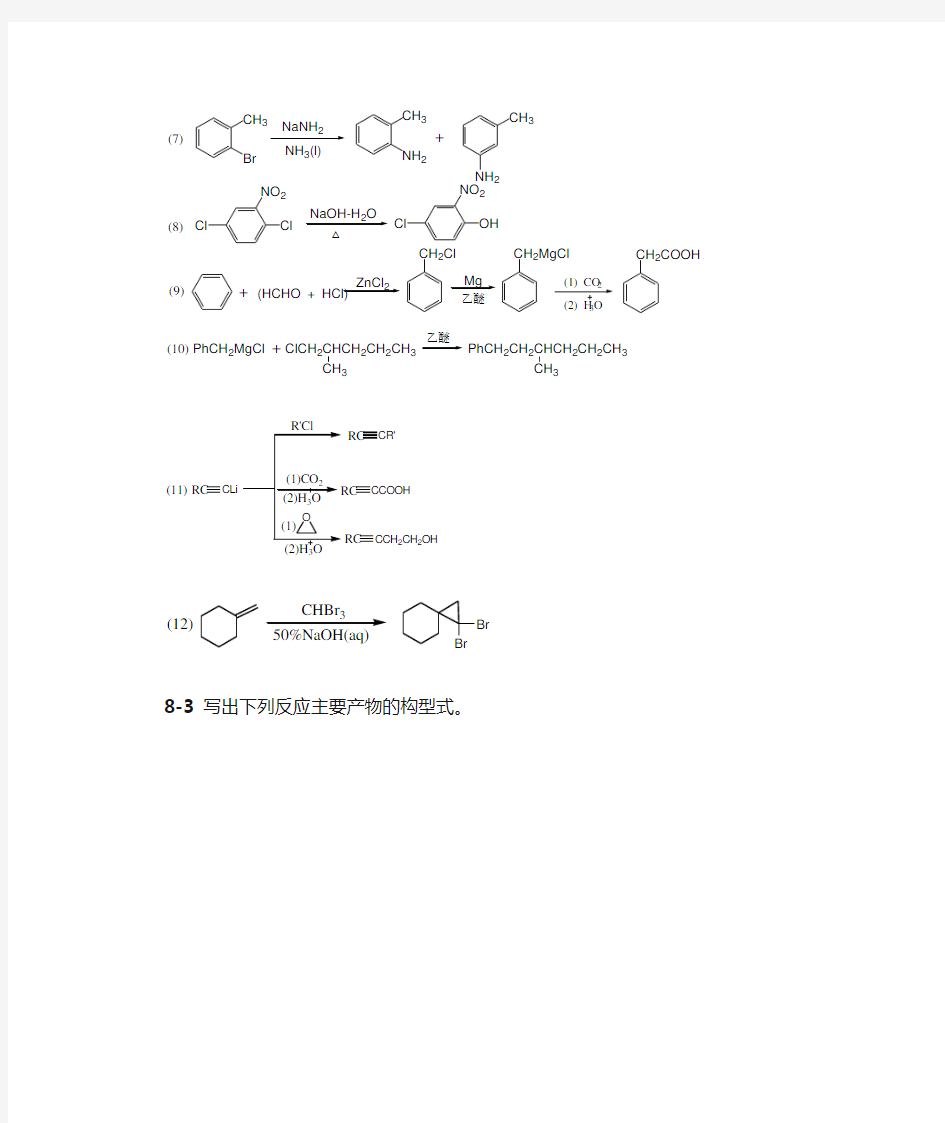
有机化学第二版(高占先)(全14章答案完整版)_第8-14章史上最全的《有机化学第二版(高占先)》全14章答案完整版!!其中包括各种判断题、推断题、思考题以及合成题的答案!! Ps:亲!给好评,有送财富值哦! #^_^!! 第8章卤代烃 8-2 完成下列各反应式。 (CH3)3CBr C2H5OH(CH3)2C=CH2 + CH3CH=CH2HBr +O O CH3CH2CH2CH3CH2CH2CN NaCN (1) (2) (CH3)2CHCH=CH2Br +500℃(CH 3 )2CCH=CH2 Br H2O (CH3)2C=CHCH2Br + (CH3)2CCH=CH2 OH (CH3)2C=CHCH2OH + (3) NaCN KOH 25 (4) (5) (6)ClCH=CHCH2Cl CH3 +ClCH=CHCH23 O Br Br Br CN CH2CHCH3 Br CH=CHCH3
CH3 Br 2 NH3(l) CH3 NH2 CH3 2 + Cl Cl NO2 NaOH-H2O OH Cl NO 2 ZnCl2 (HCHO + HCl) + CH2Cl Mg CH2MgCl CH2COOH ClCH2CHCH2CH2CH3 PhCH2MgCl CH3 +PhCH2CH2CHCH2CH2CH3 CH3 (7) (8) (9) (10) 3 RC CLi (11) RC CR' RC CCOOH RC CCH2CH2OH CHBr3 Br Br (12) 8-3写出下列反应主要产物的构型式。 C2H5 CH 3NaI +C C2 H5 CH3 NaSCH3 + (S N2) (S N2) (S N2) CH3 I 2 (CH2)4CH3 H H2O CH3 H CH2(CH2)4CH3 HO C Br CH2CH2CH3CCH2CH3 H2 Lindar催化剂 C H C CH2CH2CH3 H (1) (2) (3) (4)
2020高考化学大一轮复习第十二章有机化学基础第3节检测(含解析)
有机化学基础 一、选择题 1.下列化合物中,能发生酯化、还原、加成、消去四种反应的是( ) A.CHCH3CHCHO B. C.HOCH2—CH2—CH===CH—CHO D. 【答案】C 2.(2019·湖南长郡中学月考)羟甲香豆素是一种治疗胆结石的药物,其结构简式如图所示。下列说法不正确的是( ) A.羟甲香豆素的分子式为C10H8O3 B.1 mol羟甲香豆素最多可以与5 mol H2发生加成反应 C.1 mol羟甲香豆素溶于足量NaOH溶液,最多可消耗3 mol NaOH D.羟甲香豆素分子中含有酯基、酚羟基、碳碳双键,属于芳香族化合物 【答案】B 【解析】1 mol羟甲香豆素最多可以与4 mol H2发生加成反应,酯基不能与H2发生加成反应,B项错误。 3.(2018·安徽六校联考)某有机物是农药生产中的一种中间体,其结构简式如右图所示。下列叙述正确的是( ) A.该有机物属于芳香烃 B.该有机物可以和Br2的CCl4溶液发生加成反应 C.该有机物和浓硫酸混合加热,可能发生消去反应 D.1 mol该有机物和足量的NaOH溶液反应,最多可与3 mol NaOH反应 【答案】D 4.分子式为C4H8O2的有机物跟NaOH溶液混合加热,将蒸出的气态有机物冷凝后得到相对分子质量为32的液体。则原有机物的结构简式为( ) A.CH3COOC2H5B.CH3CH2COOCH3
C.HCOOC3H7D.(CH3)2CHCOOH 【答案】B 【解析】酯在碱性条件下水解产生羧酸盐和醇。分子式为C4H8O2的有机物跟NaOH溶液混合加热,将蒸出的气态有机物冷凝后得到相对分子质量为32的液体,则该物质是甲醇,则原有机物是丙酸甲酯,其结构简式为CH3CH2COOCH3。 5.有机羧酸酯A的分子式为C22H34O5,n mol A完全水解可得到n mol羧酸和2n mol乙醇,该羧酸的分子式为( ) A.C18H18O5B.C18H24O4 C.C18H26O5D.C18H28O5 【答案】C 【解析】某羧酸酯的分子式为C22H34O5,n mol A完全水解可得到n mol羧酸和2n mol 乙醇,这说明分子中含有2个酯基,因此有2分子水参加反应,即C22H34O5+2H2O―→羧酸+2C2H6O,则根据原子守恒可知该羧酸的分子式中碳原子个数是22-2×2=18,氢原子个数是34+4-2×6=26,氧原子个数是5+2-2×1=5,即分子式为C18H26O5。 6. (2018·江西南昌质检)某种作为添加剂的酯M在一定条件下水解,得到CH3COOH和化学式为C4H9OH的物质。下列有关说法正确的是( ) A.M的化学式可表示为C6H13O3 B.一定条件下C4H9OH可与H2加成 C.碱性条件下M的水解比酸性条件彻底 D.化学式为C4H9OH的醇可能有三种 【答案】C 【解析】A项,酯水解生成羧酸和醇,所以M的化学式为C6H12O2,错误;B项,C4H9OH 属于饱和一元醇,不能与H2加成,错误;C项,酯在碱性条件下的水解为不可逆反应,在酸性条件下的水解为可逆反应,酯M在碱性条件下水解比酸性条件彻底,正确;D项,化学式为C4H9OH的醇有四种,错误。 7.(2017·广东深圳三模)有机物甲、乙的结构如下图所示,下列说法错误的是( ) A.甲、乙互为同分异构体 B.一定条件下,甲、乙均能发生取代反应 C.甲、乙都能与金属钠反应生成氢气 D.甲、乙都能使酸性KMnO4溶液褪色 【答案】C
大学有机化学练习题—第八章 醛酮
第八章:醛酮 学习指导 1、醛酮构造和命名 2、酮的化学性质:羰基的加成反应(加氰化氢,加亚硫酸氢钠,加醇,加Grignard试剂, 与氨衍生物的缩合)及亲核加成反应历程, —氢原子的反应(羟醛缩合及反应历程,卤代反应,卤仿反应) 氧化和还原反应(银镜反应,Fehling试剂反应,还原反应,Cannizzaro反应) 一.命名下列各物种或写出结构式 1、写出的系统名称。 2、用Fischer投影式表示(S)-3-甲基-4-庚酮。 3、写出的系统名称。 4、写出的系统名称。 5、写出的名称。 二.完成下列各反应式 1、 2、 3、 4、
5、 6、 三.理化性质比较题 1、比较下列化合物与ROH加成反应活性的大小: (A) CH3CHO (B) CH3COCH3(C) C2H5COC2H5(D) ClCH2CHO 2、比较下列化合物与HCN加成速率的快慢: (A) CH2O (B) CH3CHO (C) (CH3)2CO (D)Cl3CCHO 3、可发生碘仿反应的化合物有: (A) CH3COCH2CH3(B) (C2H5)2CO 4、将下列化合物按烯醇式含量的多少排列成序: (A) CH3COCH3(B) CH3COCH2COCH3(C) CH3COCH2CH2COCH3 5、比较下列化合物羰基上亲核加成的活性大小: (A) CH3CHO (C) CH3COCH2CH3(D) CCl3CHO 6、将下列化合物按亲核加成反应活性排列成序: (C) CH3CHO 7、比较下列化合物与NaHSO3加成速率的快慢: 四.基本概念题
1、下列相对分子质量均为72的化合物中,沸点最高的是: 1. CH 3CH 2CH 2CH 2CH 3 4.CH 3CH =CHCH 2OH 2、指出下列化合物哪些能发生碘仿反应,哪些可发生银镜反应,哪些可发生自身羟醛缩合反应。 3、下列化合物中哪些分子内能形成氢键 ? 4、下列化合物中,可进行Cannizzaro 反应的有: 1.乙醛 2.苯甲醛 3.丙醛 4.丙烯醛 五. 用简便的化学方法鉴别下列各组化合物 1、用简便的化学方法鉴别以下化合物的水溶液: (A) 甲醛 (B) 乙醛 (C) 丙醛 (D) 丙酮 2、用简便的化学方法鉴别以下化合物: (A)1-戊醇 (B)2-戊醇 (C)3-戊醇 (D)2-甲基-2-丁醇 六. 有机合成题 1、用C 4以下的烃为原料(无机试剂任选)合成: 2、以乙酰乙酸乙酯为原料(其它试剂任选)合成: 3、用苯和C 3以下的有机物为原料(无机试剂任选)合成: 七、分离 1、用化学方法分离3-戊醇、3-戊酮和戊醛的混合物。 2、用化学方法分离2, 4-二甲基-3-戊酮、庚醛和2-己醇的混合物。 3、用化学方法除去环己酮中的少量苯酚。 八、推导结构题
有机化学高占先第二版课后习题答案
第六章 不饱和烃 6-1 命名下列各化合物。 (CH 3)2CHCH 2 CH 2 CH 3 CH 2CH(CH 3)2 C C H 3C H C CH 2 H H 3CH 2CH 3 H CH 3 1 2 3 4 5 6 7 8 9 12 34 5 6 78 C C C 25 H 3C C 3)3 C C 2H 5 2,4-二甲基-1-戊烯 3-异丁基环已烯(E )-1,3-戊二烯(S )-6-甲基-1,3-环辛二烯(3R ,4Z )-3,6-二甲基-5-丙基-4-壬烯 (E )-3-甲基-4-叔丁基-3-辛烯-5-炔 1 2 3 4 5 (1)(2) (3) (4)(5)(6) (2)也可命名为:3-(2-甲基丙基)环已烯 6-2 按要求比较反应活性。 (1)B >C >A ; (2)A >B >C >D >E ; (3)A >C >B >D ; (4)B >A >C >D . 6-3 将下列各组碳正离子按稳定性由大到小排列成序。 (1)B →A →C →D ; (2)A →C →B 。 (3)C →D → B →A 6-4 指出下列分子中各存在哪些类型的共轭体系? (1)、(3)和(4)都是p-π共轭体系;(2)π-π和p-π共轭体系。 (1)和(4)还有π-σ和p-σ超共轭。 6-5下列各对结构式是构造异构体系还是共振结构关系? (1)构造异构体; (2)、(3)和(4)共振结构。 6-6 下列各组极限结构式,哪一个极限结构对共振杂化体的贡献较大? (1) B 式(负电荷处在电负性较大的O 上比处在C 上稳定) ; (2) B 式(B 式中所有原子均有完整的价电子层,而在A 式中+C 上没有完整的价电子层); (3)A 式(A 式的正离子为三级碳正离子,正电荷较分散)。 6-7 将下列烯烃按稳定性由大至小排列。 稳定性由大至小顺序为:(2)→(4)→(1)→(3) 反式烯烃比顺式烯烃稳定,内烯烃比端烯烃稳定,双键上取代基多的烯烃比取代基少的烯烃稳定。 6-8查阅并比较(Z )-2-丁烯与(E )-2-丁烯;(Z )-1,2-二氯乙烯与(E )-1,2-二氯乙烯的熔沸点、偶极矩,说明结 构与熔沸点的关系。 经查阅(见下表),题中所给的二组顺反异构体中,Z 型的皆有一定偶极矩,是极性分子,分子间作用较大,因而沸点比E 型的高;而E 型的偶极矩为0,是非极性分子,但对称性较好,有对称中心。熔点比Z 型的高。
有机化学-第五版-第十二章答案
有机化学-第五版-第十二章答案
第十二章 羧酸 1. 命名下列化合物或写 出结构式。 H C CH 2COOH 3 H 3C (1) Cl 2COOH CH 3 (2) COOH COOH (3) (4) CH 3(CH 2)4CH=CHCH 2CH=CH(CH 2)7COOH (5) 4-methylhexanoic acid (6) 2-hydroxybutanedioic acid (7) 2-chloro-4-methylbenzoic acid (8) 3,3,5-trimethyloctanoic acid 1. 解:(1)3-甲基丁酸 (2)3-对氯苯基丁酸
(3)间苯二甲酸 (4)9,12-十八二烯酸 (5) CH3CH2CHCH2CH2COOH 3 CHCOOH HO 2 COOH (6) COOH H3C (7) (8) CH3CH2CH2CHCH2CCH2COOH 33 CH3 2.试以方程式表示乙酸与下列试剂的反应。 (1)乙醇(2)三氯化磷(3)五氯化磷(4)氨 (5)碱石灰热熔 2.解:(1) CH3COOH + C2H5OH H+ CH3COOC2H5 + H2O (2)
CH 3COOH + PCl 3CH 3COCl + H 3PO 3 (3) CH 3COOH + PCl 5 CH 3COCl + POCl 3 + HCl (4) (5) △ CH 3COOH 碱石灰4 3.区别下列各组化合物。 (1) 甲酸、乙酸和乙醛; (2) 乙醇、乙醚和乙酸; (3) 乙酸、草酸、丙二酸; (4) 丙二酸、丁二酸、己二酸 3 解: CH 3COOH + NH 3 CH 3COONH 4 CH 3CONH 2 + H 2O Δ
有机化学第二版(高占先)第五章习题答案
第五章饱和烃 5-1 写出符合下列条件的C7H16的构造式,并各以系统命名法命名。 (1)庚烷(3)3-甲基已烷 (4)2,2-二甲基戊烷(5)2,3-二甲基戊烷(6)2,4-二甲基戊烷 (7)3,3-二甲基戊烷(8)3-乙基戊烷(9)2,2,3-三甲基丁烷 5-2 写出下列烷基的名称及常用缩写符号。 (1)甲基(Me—);(2)乙基(Et—);(3)正丙基(n-Pr—);(4)异丙基(i-Pr—);(5)正丁基(n-Bu—);(6)异丁基(i-Bu—);(7)仲丁基(s-Bu—); (8)叔丁基(t-Bu—)。 5-3 比较下列化合物沸点的高低,并说明原因。 (1) CH3(CH2)4CH3(2) (CH3)2CH(CH2)2CH3 (3)CH3CH2C(CH3)3(4) CH3CH2CH(CH3)CH2CH3 (1)>(4) >(2)>(3)同碳数的烷烃异构体,含支链越多,分子间作用力越弱,沸点越低。 5-4 完成下列反应式: OSO3 H Br Br Br (1) HO2C(CH2)4CO2H HNO3 + (2)
Br Br -60℃ Br 2 +(3) CH(CH 3) 2 CO 2H 2O Cl +Cl Cl Cl 碳正离子重排导致的产物 ++ CH(CH 3)2Br C(CH 3)2Br + (4)Br HBr (5) 5-5 比较下列化合物构象的稳定性大小。 1,4-二甲基环已烷的构象稳定性(1)<(2)。原因是(1)中的二个甲基均处于a 键上,而(2)中的二个甲基则皆处于e 键上,后者构象能量较低,较稳定。 3 H 3 3 CH 3 CH 3 H 3C CH 3 (1) (2) 5-6 下列异构体中哪个最稳定? 题目所示二甲基环已酮三个异构体对应的构象式如下,从中可看出(3)最稳定,因为其两个甲基均处于e 键上,体系能量较低。 O O O (1) (2)(3) 5-7 环丙烷内能高是由哪些因素造成的? 环丙烷分子中碳原子为不等性sp 3杂化,轨道重叠比开链烷烃的小,形成的碳碳共价键键能小(即有角张力),容易断裂,不如开链烷烃牢固;其次是环丙烷的三个碳原子共平面,
有机化学(第二版)_ 课后答案
第二章 烷烃作业参考答案 1、 共有九种: CH 3-CH 2-CH 2-CH 2-CH 2-CH 2-CH 3 CH 3-CH-CH 2-CH 2-CH 2-CH 3 2CH 3-CH 2-CH-CH 2-CH 2-CH 3 3CH 3-CH-CH-CH 2-CH 3 CH 3CH 3CH 3-CH-CH 2-CH-CH 3 3 CH 3 CH 3-C-CH 2-CH 2-CH 3 CH 3 CH 3 CH 3-CH 2-C-CH 2-CH 3 CH 3 CH 3-CH 2-CH-CH 2-CH 2 CH 2-CH 3 CH 3-C 3 CH 3CH-CH 3 CH 3 2、(1)3-甲基戊烷 (2)2,5-二甲基-3,4-二乙基己烷 (3)2,2,3,4-四甲基戊烷 (4)2-甲基-5-乙基庚烷 (5)2-甲基-3-环丁基丁烷 (6)顺-1-甲基-3-乙基环戊烷(7)反-1-甲基-4-乙基环己烷 (8)1-甲基-4-乙基-3-叔丁基环己烷 3、(1) (2) CH 3-CH-CH 2-CH 2-CH 3 3 CH 3-C-CH 2CH 3CH 3CH 3 (3) (4) CH 3-CH-CH-CH-CH-CH 3 CH 33CH 2CH 3 2CH 3 3)3 4、(1) (2) CH 3CH 2-C CH 3 CH-CH 3 CH 3 CH 3-C-CH-CH-CH 3CH 3CH 3 CH 3 CH 3-CH-C-CH 2-CH 3CH 3CH 3CH 3 CH 3-C-CH 2-CH-CH 3CH 3CH 3 CH 3 5、(1)错。改为:2,2-二甲基丁烷 (2)错。改为:2,2,5-三甲基-4-乙基己烷 (3)正确 (4)错。改为:2,2-二甲基丁烷
有机化学答案第二章
第二章 脂烃 思考与练习 2-1同系列和同系物有什么不同?丁烷的两种构造异构体是同系物吗? 同系列和同系物含义不同。同系列是指通式相同,结构相似,在组成上相差一个或多个CH 2基团的一系列化合物的总称,同系物则是指同一系列中的具体化合物。如:烷烃是同系列,烷烃中的甲烷和乙烷互称为同系物。丁烷的两种构造异构体不是同系物。 2-2推导烷烃的构造异构体应采用什么方法和步骤?试写出C 6H 14的所有构造异构体。 推导烷烃的构造异构体时,应抓住“碳链异构”这一关键。首先写出符合分子式的最长碳链式,然后依次缩减最长碳链(将此作为主链),将少写的碳原子作为支链依次连在主链碳原子上。如:C 6H 14存在以下5种构造异构体。 2-3脂烃的涵义是什么?它包括哪些烃类?分别写出它们的通式。 脂烃涵盖脂肪烃和脂环烃。 2-4指出下列化合物中哪些是同系物?哪些是同分异构体?哪些是同一化合物? 同系物:⑴和⑻;⑵、⑶和⑸ 同分异构体:⑴和⑷;⑹和⑺ 同一化合物:⑵和⑶ 2-5 写出下列烃或烃基的构造式。 ⑴ (CH 3)3C — ⑵ ⑶ CH 3CH=CH — ⑷ CH 2=CHCH 2— ⑸ ⑹ ⑺ CH 3 CH 2 CH 2 CH 2 CH 2 CH 3 CH 3CH CH 2CH 2CH 3 CH 3 CH 3 CH 2 CH CH 2 CH 33 CH 3 CH CH CH 33CH 3 CH 3C CH CH 3 CH 3 3 (环烯烃、环炔烃、环二烯烃等) (环烷烃) 不饱和脂环烃饱和脂环烃 二烯烃炔烃烯烃 (烷烃)不饱和烃饱和烃 脂环烃 脂肪烃 脂烃 C n H 2n+2C n H 2n C n H 2n-2C n H 2n-2C n H 2n CH 3CHCH 2CH 3CH 3CHCH 2CH 33 CH 3CCH 2CH 3CH 3 3 CH 2CCH 3 3
高职高专《有机化学》课后习题答案 第十二章
259 第十二章 萜类和甾族化合物 思考与练习 12-1简述萜类化合物的结构特征?它是如何分类的? 萜类化合物具有异戊二烯的基本单位,其分子结构可以看作是异戊二烯分子结构头尾相连接而成的低聚合体或其衍生物。根据分子中所含异戊二烯单位的数目,萜类化合物可以分为单萜、倍半萜、二萜、二倍半萜、三萜、四萜和多萜等。其中单萜又根据其碳架分为开链单萜(如香叶烯)、单环单萜(如苧烯)和二环单萜3类。 12-2维生素A 与胡萝卜素有什么关系?它们各属于哪一类? 在动物体中胡萝卜素可以转化为维生素A ,所以胡萝卜素又称为维生素A 原。维生素A 属于二萜,胡萝卜素属于四萜。 12-3象形字“甾”的含义是什么?什么是角甲基?什么是甾核?什么是正系、别系?什么是α-、β-构型? 甾族化合物又称为类固醇,指环戊烷并全氢化菲的衍生物。这类化合物含有4个环和3个侧链,所以用象形文字“甾” 表示。“田”代表4个环,“<<<”代表3个侧链。 一般将C 1~C 19部分称为甾核,18、19为角甲基。若C 5上的氢原子与C 10上的角甲基在环的同侧,称为5β-系(也叫正系),属于β-型;若C 5上的氢原子与C 10上的角甲基在环的异侧,称为5α-系(也叫别系),属于α-型。 12-4简述甾族化合物的结构特征?它是如何分类的? 甾族化合物按其基本碳架结构可分为甾烷、雌甾烷、雄甾烷、孕甾烷、胆烷、胆甾烷、麦角甾烷、豆甾烷。也可以根据其天然来源和生理作用并结合结构分为甾醇类、胆甾酸类、甾族激素类、甾族皂素类、强心苷类与蟾毒等。 12-5 胆甾酸与胆汁酸的含义有什么不同?胆汁酸盐的生理作用是什么? 在大部分脊椎动物的胆汁中含有几种结构相似的酸,叫做胆甾酸。其中最重要的是胆酸,其结构式如下: 在胆汁中,胆酸多与甘氨酸或牛磺酸(H 2NCH 2CH 2SO 3H )通过酰胺键结合成甘氨胆酸或牛磺胆酸。这种结合胆酸称为胆汁酸。 甘氨胆酸 牛磺胆酸 23 4 5 6 7 89 101112 1314 15 1617 1A B C D 18 192021222324 25 2627 2829 HO COOH OH OH HO CONHCH 2COOH OH OH H HO CONHCH 2CH 2SO 3H OH OH H
有机化学-第五版-第十二章答案
第十二章羧酸 1.命名下列化合物或写出结构 式。 (4) CH3(CH2)4CH=CHCH2CH=CH(CH2)7COOH (5) 4-methylhexanoic acid (6) 2-hydroxybutanedioic acid (7) 2-chloro-4-methylbenzoic acid (8) 3,3,5-trimethyloctanoic acid 1. 解:(1)3-甲基丁酸(2)3-对氯苯基丁酸(3)间苯二甲酸 ( 4)9,12-十八二烯酸
2.试以方程式表示乙酸与下列试剂的反应。 (1)乙醇 (2)三氯化磷 (3)五氯化磷(4)氨 (5)碱石灰热熔 2.解:(1) CH 3COOH + C 2H 5OH H + CH 3COOC 2H 5 + H 2O (2) CH 3COOH + PCl CH 3COCl + H 3PO 3 (3) CH 3COOH + PCl 5CH 3COCl + POCl 3 + HCl (4) (5) CH 3COOH + NH 3CH 3COONH 4CH 3CONH 2 + H 2O Δ
3.区别下列各组化合物。 (1) 甲酸、乙酸和乙醛; (2) 乙醇、乙醚和乙酸; (3) 乙酸、草酸、丙二酸; (4) 丙二酸、丁二酸、 己二酸 3 解: (1) 甲 (+)(+)(-) 有气体放出Tollens 试剂(+)银镜 (2) (-)(-)(+) 有气体放出I 2 + NaOH (+)△(-)
(3) 草酸 乙酸 丙二酸 KMnO 4/H + (+)(-)(-)紫色褪去(-)有气体放出(CO 2)△(+) (4) 丁二酸 丙二酸 己二酸(-)(+)(+)(-)△(+) 有气体放出(CO 2) 4.完成下列转变。 (1) CH 2=CH 2 CH 3CH 2COOH (2) 正丙醇 2-甲基丙酸 (3) 丙酸 乳酸 (4) 丙酸 丙酐 (5) 溴苯 苯甲酸乙酯 4. 解: (1) H 2C CH HBr 3CH 21) Mg , Et 2O 2) CO 2 ; 3) H 3+O 3CH 2COOH or H 2C CH HBr 3CH 2Br 3CH 2COOH NaCN CH 3CH 2CN H 3+O
