压力蒸汽灭菌效果的监测方法文档

压力蒸汽灭菌效果的监测方法
(一)物理监测方法
【目的】
是通过仪表和记录的曲线图等显示,判定物品灭菌处理中机械运行状况是否达到灭菌标准规定的条件。
【频次频次】
每次灭菌应连续监测并记录灭菌时的温度、压力和时间等灭菌参数。温度波动范围+3℃以内,时间满足最低灭菌时间的要求,同时应记录所有临界点的时间、温度与压力值,结果应符合灭菌的要求。记录资料留存时间≥3年。
【结果判定】
1.预真空压力蒸汽灭菌器的灭菌压力为205、8KPa ,温度为132-134℃,灭菌时间最低4分钟,真空度8.oKPa 。脉动预真空循环3次以上。硬质容器、超重、外来器械灭菌时间应参考使用器械厂商的说明适当延长;
2.下排气压力蒸汽灭菌器的灭菌压力为102、9KPa ,温度为121℃,灭菌时间20—30分钟。【注意事项】
1.物理监测有一定的局限性,只能证实灭菌循环参数是否符合要求,只能监测腔体中的一点温度(灭菌器排水口),无法监测包装内部情况。同时不能直接反应微生物死亡,也无法直接和精确考核蒸汽质量、不可压缩气体、冷空气等;
2.新购置的设备或维修后的灭菌器,对各项灭菌参数必须进行物理校正;
3.物理监测不合格时,所有物品不能灭菌发放。应分析原因改进,直至监测结果符合要求;
4.整个灭菌过程中,灭菌人员不得离开,时刻观察仪器仪表运行的情况;
5.物理监测各项内容均详实、客观记录,归档备查。
(二)化学监测方法
【目的】
通过化学反应原理,利用各种化学指示物与灭菌介质的相互作用,在特定的灭菌条件下产生化学反应而产生颜色变化。通过观察测试品颜色变化情况,来达到对灭菌过程的监测。【特点】
可监测每个灭菌包内部的灭菌状况,具有快速、简单和费用低廉等,能及时反应每个灭菌物品包内外的灭菌效果,但不能直接反应微生物死亡。
【种类】包内化学指示物、包外化学指示物、BD测试纸。
1、B-D试验(适用于预排气压力蒸汽灭菌器)
【目的】
对预真空和脉动真空压力蒸汽灭菌器进行真空系统性能测试,通过检测灭菌器冷空气排除和热蒸汽穿透的效果。灭菌完毕取出测试图,通过观察其颜色变化情况,以判断试验包中有无残留空气存在。
【监测频次】
每台灭菌器每天灭菌前空锅进行B-D试验。资料留存时间3年以上。
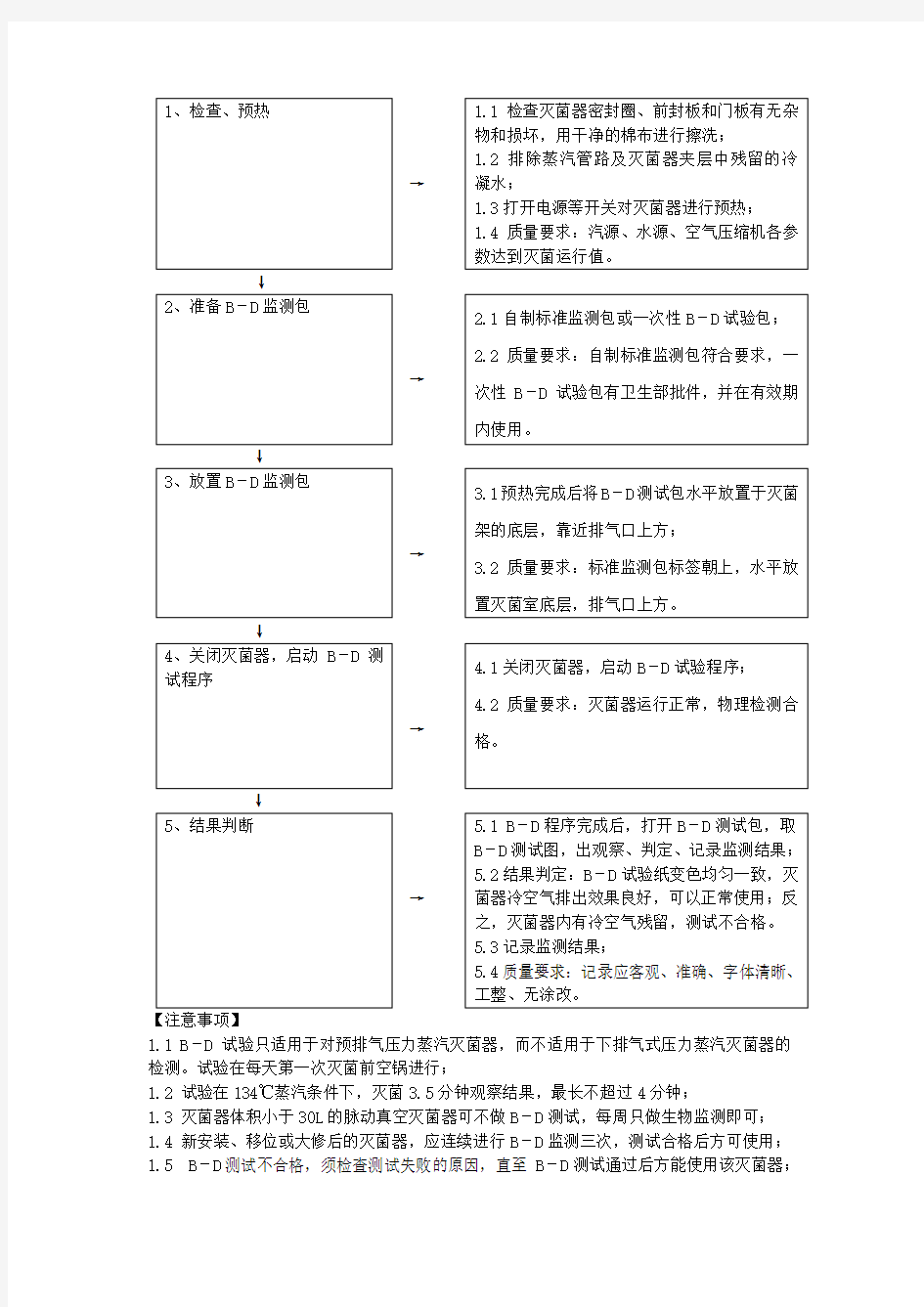
【操作流程】【方法步骤】
1、检查、预热
→1.1检查灭菌器密封圈、前封板和门板有无杂物和损坏,用干净的棉布进行擦洗;
1.2 排除蒸汽管路及灭菌器夹层中残留的冷凝水;
1.3打开电源等开关对灭菌器进行预热;
1.4质量要求:汽源、水源、空气压缩机各参数达到灭菌运行值。
↓
2、准备B-D监测包
→2.1自制标准监测包或一次性B-D试验包;
2.2质量要求:自制标准监测包符合要求,一次性B-D试验包有卫生部批件,并在有效期内使用。
↓
3、放置B-D监测包
→3.1预热完成后将B-D测试包水平放置于灭菌架的底层,靠近排气口上方;
3.2质量要求:标准监测包标签朝上,水平放置灭菌室底层,排气口上方。
↓
4、关闭灭菌器,启动B-D测
试程序
→4.1关闭灭菌器,启动B-D试验程序;
4.2质量要求:灭菌器运行正常,物理检测合格。
↓
5、结果判断
→5.1 B-D程序完成后,打开B-D测试包,取B-D测试图,出观察、判定、记录监测结果;
5.2结果判定:B-D试验纸变色均匀一致,灭菌器冷空气排出效果良好,可以正常使用;反之,灭菌器内有冷空气残留,测试不合格。5.3记录监测结果;
5.4质量要求:记录应客观、准确、字体清晰、工整、无涂改。
【注意事项】
1.1 B-D试验只适用于对预排气压力蒸汽灭菌器,而不适用于下排气式压力蒸汽灭菌器的检测。试验在每天第一次灭菌前空锅进行;
1.2 试验在134℃蒸汽条件下,灭菌3.5分钟观察结果,最长不超过4分钟;
1.3 灭菌器体积小于30L的脉动真空灭菌器可不做B-D测试,每周只做生物监测即可;1.4 新安装、移位或大修后的灭菌器,应连续进行B-D监测三次,测试合格后方可使用;
1.5 B-D测试不合格,须检查测试失败的原因,直至B-D测试通过后方能使用该灭菌器;
1.6一次性监测指示物须经卫生部批准,并在有效期内使用,测试图存放应避免受潮,同时禁与酸、碱性物质接触;自制标准监测包应宽松一些,不可过分干燥或潮湿。
1.7在记录中应有操作人员、质检员或护士长的签字。
B-D图测试包
100%纯棉布;长为30㎝±20㎝,宽为25㎝±20㎝,高为25至㎝28㎝;包的重量为4㎏±0.2㎏大小的布包裹;B-D测试纸放入布测试包的中间包裹后用化学指示胶带封扎
BD测试包是标准的做法,《医院供应室的管理与技术》一书79页依据:约由46-50条80-90cm 的纯棉巾组成,布巾先横折为三层,再纵折形成6层。将折好的布巾一条摞一条至25——28CM 厚,摞放时各层布巾按折叠侧左右交替摆放,务使两侧厚度相等。布巾摆好后,将BD测试纸水平放于中央层布巾之间,然后用布将所有布巾包成一试验包-一层布即可,外面用化学指示胶带定。BD包的要求是:1,应打得略宽松一些,太紧的包,蒸汽不易进入。2,可用手术室治疗巾用前洗涤一次,重复使用的包,布巾必须洗净,布巾可连续使用30次。
包的大小为高25-28CM、宽23-25CM 、长27-30CM,重4kg加减百分之十。
2、包外化学指示物监测方法
包外化学指示物包括化学指示胶带、化学指示块。主要作用是提示物品经过灭菌过程,同时还具有封口、标识作用。
【目的】
指示和说明物品包是否经过灭菌处理。但不能判定物品灭菌质量和处理效果。
【监测频次】
应对每个灭菌包包外化学指示物标记(化学指示胶带或化学指示块)进行监测。
【监测方法】
2.1灭菌包冷却后,取出灭菌包。
2.2观察、比对灭菌包外化学指示物灭菌前、后变色情况。
【结果判定】
2.1标识齐全、清晰;
2.2包外化学指示物灭菌后变色均匀一致;
2.3包外化学指示物灭菌后,无发灰、水渍等现象。
【注意事项】
2.1变色不合格的灭菌包不能发放和使用;
2.2如发现包外化学指示物不合格的灭菌包,应查找原因重新更换包外指示物,再次进行灭菌处理;
2.3如变色不合格是由于物品码放过紧原因造成的个别问题。可只对变色不合格的物品包重新处理。
3、灭菌包内化学指示物的监测方法
【目的】
指示和说明物品包在灭菌处理中接触灭菌温度、时间、持续时间和条件,为使用无菌包人员提供快速判定灭菌效果的方法。
【监测频次】
各类无菌穿刺包、手术器械包、手术敷料包等高度危险性物品包内均应放置化学指示物。放置位置:在灭菌包难以灭菌的部位或灭菌包的中央。
【监测方法】
3.1经过一个灭菌周期后,灭菌人员或使用人员,打开灭菌包,取出包内化学指示物。
3.2观察、比对变色区包内化学指示物灭菌后的变色情况。
【结果判定】
包内化学指示物灭菌后指示区显示均匀一致的颜色,与对照区颜色一致,视为合格。
【注意事项】
3.1打开灭菌包检查包内化学指示物变色未达到要求时,该物品视为灭菌不合格,不能使用;
3.2包内化学指示物有134℃、121℃等,须根据灭菌设备和设定程序的温度条件选择使用;
3.3放置时不要与金属器械直接接触,避免冷凝水影响其结果。
4、化学PCD的监测方法
【目的】
指示和说明物品包在灭菌处理中接触灭菌温度、时间、持续时间和条件。为灭菌人员和质检人员提供快速判定灭菌效果的方法。
【监测频次】
每台灭菌器每批次应进行化学PCD试验。资料留存时间3年以上。
【操作流程】【方法步骤】
1、检查、预热
→1.1检查灭菌器密封圈、前封板和门板有无杂物和损坏,用干净的棉布进行擦洗;
1.2排除蒸汽管路及灭菌器夹层中残留的冷凝水;
1.3打开电源等开关对灭菌器进行预热;
1.4质量要求:汽源、水源、空气压缩机达各参数到灭菌运行值。
↓
2、准备标准监测包
→2.1自制标准监测包或一次性标准试验包;2.2质量要求:自制标准监测包符合要求,一次性标准试验包有卫生部批件,并在有效期内使用。
↓
3、放置标准监测包
→3.1预热完成后将标准监测包水平放置于灭菌架的底层,靠近排气口上方;
3.2质量要求:标准监测包标签朝上,水平放置灭菌室底层,排气口上方。
↓
4、装载
→4.1按要求转载各类灭菌包;
4.2质量要求:
↓
5、灭菌
→5.1关闭灭菌器,启动器械或织物程序
5.2质量要求:灭菌器运行正常,物理检测合格。
↓
6、结果判断
→6.1灭菌周期完成后打开测试包,取出包内化学指示物,观察、判定、记录监测结果;
6.2结果判定:包内化学指示物灭菌后指示区显示均匀一致的颜色,与对照区颜色一致,视为合格。
6.3记录监测结果;
6.4质量要求:记录应客观、准确、字体清晰、工整、无涂改。
【注意事项】
3.1质检人员打开标准监测包,检查包内化学指示物变色未达到要求时,该批次灭菌包视为灭菌不合格,不能发放;
3.2灭菌人员发现变色不合格的灭菌包,则该批次灭菌的所有物品均视为灭菌不合格,查找原因重新再次灭菌处理;
3.3采用快速压力蒸汽灭菌程序灭菌时,应直接将一片包内化学指示物置于待灭菌物品旁边进行化学监测;
3.4包内化学指示物有134℃、121℃等,须根据灭菌设备和设定程序的温度条件选择使用。
(三)生物监测方法
【目的】
生物监测是用抗力较强的生物指示物进行灭活试验的监测方法,以判断和裁决灭菌质量是否合格。通常用于灭菌程序监测过程和终末质量的监测。生物指示物设计依据是根据细菌芽孢的死亡曲线。是最有效、最可靠地灭菌效果监测方法。
【监测频次】
每台灭菌器每周监测一次,有植入物或外来器械的灭菌包应每批次进行监测一次。灭菌质量监测资料和记录的保留期应大于或等于3年。
【操作流程】【方法步骤】
1、检查、预热
→1.1检查灭菌器密封圈、前封板和门板有无杂物和损坏,用干净的棉布进行擦洗;
1.2排除蒸汽管路及灭菌器夹层中残留的冷凝水;
1.3打开电源等开关对灭菌器进行预热;
1.4质量要求:汽源、水源、空气压缩机各参数达到灭菌运行值。
↓
2、准备生物测试包
→2.1将生物指示剂置于生物测试包的中心部位,制作成生物测试包或一次性生物测试包;
2.2质量要求:自制生物测试包符合要求,一次性生物测试包有卫生部批件,并在有效期内使用。
↓
3、放置生物测试包
→3.1预热完成后将生物测试包水平放置于灭菌架的底层,靠近排气口上方;
3.2质量要求:标准监测包标签朝上,水平放置灭菌室底层,排气口上方。
↓
4、装载
→4.1按要求转载各类灭菌包;
4.2质量要求:
↓
5、灭菌
→5.1关闭灭菌器,启动器械或织物程序
5.2质量要求:灭菌器运行正常,物理检测合格。
↓
6、结果判断
→6.1灭菌周期完成后打开测试包,取出生物指示剂,根据指示剂与设备说明进行生物培养;
6.2结果判定:阳性对照组培养阳性阴性对照组培养阴性,试验组培养阴性,判定为灭菌合格。阳性对照组培养阳性,阴性对照组培养阴性,试验组培养阳性,则灭菌不合格;
6.3记录监测结果;
6.4质量要求:记录应客观、准确、字体清晰、工整、无涂改。
【注意事项】
1.生物监测不合格时,必须停止使用灭菌器。应查找原因,并追回已发放的物品,待生物监测合格后,灭菌器方能使用。
2.监测所用菌片需经卫生部批准,并在有效期内使用。对照菌片与监测菌片必须是同一批号,否则不能作为阳性对照。如果一天内进行多次生物监测,且生物指示剂为同一批号,则只设
一次阳性对照即可。
3.新安装的设备、移位或大修后的灭菌器,应进行生物测试合格后方可使用。应连续进行3次生物测试合格后方可使用。
4.采用新的包装材料和方法时必须进行生物监测,以确定方法的安全性。
5.紧急情况灭菌植入物器械时,可在生物PCD中加用5类化学指示物。5类化学指示物可作为提前放行的标志,生物监测的结果应及时通报使用部门。
6.小型压力蒸汽灭菌器因一般无标准生物监测包,应选择灭菌器常用的、有代表性的灭菌包制作生物测试包或生物PCD,置于灭菌器最难灭菌的部位,且灭菌器应处于满载状态。生物测试包或生物PCD应侧放,体积大时应平放。
7.采用快速压力蒸汽灭菌程序灭菌时,应直接将一支生物指示物,置于空载的灭菌器内,经一个灭菌周期后取出,规定条件下培养,观察结果。生物监测结果记录归档并保留大于或等于3年。
8.在记录中应有操作人员、质检员或护士长的签字。
附件:标准试验包的制作方法
1、准备16条全棉布手术斤,规格:41cm×66cm。
2、将每条手术斤的长边先折成3层,短边折成2层。
3、将折好的的手术斤交替叠放,制成23cm×23cm×15cm大小的测试包。
4、把生物指示剂或包内化学指示物放入测试包的中心部位,包装备用。
参考文献
1.中华人民共和国卫生行业标准.WS310.3—2009医院消毒供应中心第三部分:清洗消毒及灭菌技术监测标准〖S〗.2009.
2.任伍爱.消毒供应中心管理指南.北京:科学技术文献出版社,2006:145-170.
3、通过活动,使学生养成博览群书的好习惯。
B比率分析法和比较分析法不能测算出各因素的影响程度。√
C采用约当产量比例法,分配原材料费用与分配加工费用所用的完工率都是一致的。X
C采用直接分配法分配辅助生产费用时,应考虑各辅助生产车间之间相互提供产品或劳务的情况。错
C产品的实际生产成本包括废品损失和停工损失。√
C成本报表是对外报告的会计报表。×
C成本分析的首要程序是发现问题、分析原因。×
C成本会计的对象是指成本核算。×
C成本计算的辅助方法一般应与基本方法结合使用而不单独使用。√
C成本计算方法中的最基本的方法是分步法。X
D当车间生产多种产品时,“废品损失”、“停工损失”的借方余额,月末均直接记入该产品的产品成本中。×
D定额法是为了简化成本计算而采用的一种成本计算方法。×
F“废品损失”账户月末没有余额。√
F废品损失是指在生产过程中发现和入库后发现的不可修复废品的生产成本和可修复废品的修复费用。X
F分步法的一个重要特点是各步骤之间要进行成本结转。(√)
G各月末在产品数量变化不大的产品,可不计算月末在产品成本。错
G工资费用就是成本项目。(×)
G归集在基本生产车间的制造费用最后均应分配计入产品成本中。对
J计算计时工资费用,应以考勤记录中的工作时间记录为依据。(√)
J简化的分批法就是不计算在产品成本的分批法。(×)
J简化分批法是不分批计算在产品成本的方法。对
J加班加点工资既可能是直接计人费用,又可能是间接计人费用。√
J接生产工艺过程的特点,工业企业的生产可分为大量生产、成批生产和单件生产三种,X
K可修复废品是指技术上可以修复使用的废品。错
K可修复废品是指经过修理可以使用,而不管修复费用在经济上是否合算的废品。X
P品种法只适用于大量大批的单步骤生产的企业。×
Q企业的制造费用一定要通过“制造费用”科目核算。X
Q企业职工的医药费、医务部门、职工浴室等部门职工的工资,均应通过“应付工资”科目核算。X
S生产车间耗用的材料,全部计入“直接材料”成本项目。X
S适应生产特点和管理要求,采用适当的成本计算方法,是成本核算的基础工作。(×)
W完工产品费用等于月初在产品费用加本月生产费用减月末在产品费用。对
Y“预提费用”可能出现借方余额,其性质属于资产,实际上是待摊费用。对
Y引起资产和负债同时减少的支出是费用性支出。X
Y以应付票据去偿付购买材料的费用,是成本性支出。X
Y原材料分工序一次投入与原材料在每道工序陆续投入,其完工率的计算方法是完全一致的。X
Y运用连环替代法进行分析,即使随意改变各构成因素的替换顺序,各因素的影响结果加总后仍等于指标的总差异,因此更换各因索替换顺序,不会影响分析的结果。(×)
Z在产品品种规格繁多的情况下,应该采用分类法计算产品成本。对
Z直接生产费用就是直接计人费用。X
Z逐步结转分步法也称为计列半成品分步法。√
A按年度计划分配率分配制造费用,“制造费用”账户月末(可能有月末余额/可能有借方余额/可能有贷方余额/可能无月末余额)。
A按年度计划分配率分配制造费用的方法适用于(季节性生产企业)
2016年消毒灭菌效果监测方案
2016年消毒灭菌效果监测方案 为进一步规范我院的环境卫生学监测工作,有效预防医院感染,根据《医疗机构消毒技术规范(WST 367-2012)》、《医院消毒卫生标准(GB 15982-2012)》、《医疗机构空气净化规范(WST 368-2012)》、《医院洁净手术部建筑技术规范(GB 50333-2013)》《医务人员手卫生规范》和《血液透析相关治疗用水》等规范的要求,结合我院实际,特制定本方案。本方案自2016年1月1日起实施。 一、监测标准 (一)采样和检查原则 1.采样后应尽快对样品进行相应指标的检测,送检时间不得超过4 h;若样品保存于O℃~4℃时,送检时间不得超过24 h。 2.常规监督检查可不进行致病性微生物检测,涉及疑似医院感染暴发、医院感染暴发调查或工作中怀疑微生物污染时,应进行目标微生物的检测。 3. I类环境为采用空气洁净技术的诊疗场所,分洁净手术部和其他洁净场所。Ⅱ类环境为非洁净手术部(室);产房;导管室;血液病病区、烧伤病区等保护性隔离病区;重症监护病区;新生儿室等。Ⅲ类环境为母婴同室;消毒供应中心的检查包装灭菌区和无菌物品存放区;血液透析中心(室);其他普通住院病区等。Ⅳ类环境为普通门(急)诊及其检查、治疗室;感染性疾病科门诊和病区。 (二)诊疗器械、器具和物品清洗的效果监测 1.手术器械:每月随机抽取消毒供应中心机械清洗、手工清洗的手术器械;将器械分为平面类、关节类、管腔类、结构复杂类四种类型,每类器械随机抽取5个清洗后样本进行ATP检测。 1.1采样时间:手术器械清洗后。 1.2采样部位:手术器械全表面。 1.3手术器械检测方法: 1.3.1采样:对器械的全部表面进行采样。 1.3.2激活/震荡:将采样棒蓝色末端彻底按压进入管腔内液体中,激活反应水平窄幅震荡5秒钟。 1.3.3测量:将采样棒放入荧光检测仪中读取数值。 2.内镜:将内镜分为灭菌内镜、高水平消毒内镜两种类型分别抽样检测;每季度抽取科室25%内镜数量进行ATP监测。 2.1采样时间:内镜清洗后。 2.2采样部位:内镜外表面及内腔面。 2.3软式内镜检测方法:
压力蒸汽灭菌生物指示剂
压力蒸汽灭菌生物指示剂 是由嗜热指肪杆菌( ATCC 7953)芽孢菌片、恢复培养基和外管组成。菌片 含菌量为5.0 X?5.0 x cfU片。生物指示剂的抗力符合国际标准和国家标准的规定:既在121C饱和蒸汽作用下,存活时间 >3.9min杀灭时间< 19min D10值 1.3? 1.9min。 【适用范围】 适用于121 C下排气式压力蒸汽灭菌器、132C?134C预真空或脉动真空压力蒸汽灭菌器、134C?136C台式或卡式压力蒸汽灭菌器灭菌效果的监测和制药工业、医院制剂生产等各行业使用的压力蒸汽灭菌器灭菌效果的监测。 【使用方法】,,, 1使用时,将生物指示剂放入标准检测包的中心或待灭菌物品包的中心,置于灭菌器的难消毒的位置按规定的灭菌温度和时间进行灭菌处理。 2灭菌完毕,即刻将生物指示剂取出,盖朝上垂直握于手中,用专门工具夹碎管内安瓶,让培养液流出浸没菌片,置于56C恒温培养箱内或配套的微型培养器内培养24小时观察初步结果,48小时观察最终结果,按规定每月至少用生物指示剂进行一次灭菌效果监测。 【结果判定】 培养后生物指示剂中的溴甲酚紫培养液由紫色澄清液体变为黄色澄清液体即表示有菌生长,判定为灭菌不合格;培养液仍为紫色澄清液体为无菌生长,同时阳性对照管中的嗜热脂肪杆菌生长正常即培养液由紫色澄清液体变为黄色澄清液体,判定为灭菌合格。 【注意事项】 1 将生物指示剂管从灭菌器内取出或从冰箱内取出后,需在室温下放10min 左右,再夹碎安瓿,以免过热或过冷夹碎外管。
2液体培养基的pH值低于7.0或高于7.5,均可使嗜热脂肪杆菌不能生长; 3培养温度须在56C?65C之间,否则可导致嗜热脂肪杆菌生长不良,或不能生长。 4 灭菌处理后,生物指示剂中的液体培养基颜色与压力蒸汽灭菌前比较会变浅,呈显浅紫色,这种变化属正常现象。 5用恢复培养液在56C培养时间过长(72小时以上),阳性对照管中培养液的黄色容易消退,培养液逐渐干燥,应注意每天观察,随时记录培养结果。 6本生物指示剂于4C条件下保存。 【包装规格】20 支/ 盒, 10 盒/ 箱。 【有效期】12个月。
压力蒸汽灭菌效果的监测方法
压力蒸汽灭菌效果的监测方法(一)物理监测方法 【目的】 是通过仪表和记录的曲线图等显示,判定物品灭菌处理中机械运行状况是否达到灭菌标准规定的条件。 【频次频次】 每次灭菌应连续监测并记录灭菌时的温度、压力和时间等灭菌参数。温度波动范围+3℃以内,时间满足最低灭菌时间的要求,同时应记录所有临界点的时间、温度与压力值,结果应符合灭菌的要求。记录资料留存时间≥3年。 【结果判定】 1.预真空压力蒸汽灭菌器的灭菌压力为205、8KPa ,温度为132-134℃,灭菌时间最低4分钟,真空度8.oKPa 。脉动预真空循环3次以上。硬质容器、超重、外来器械灭菌时间应参考使用器械厂商的说明适当延长; 2.下排气压力蒸汽灭菌器的灭菌压力为102、9KPa ,温度为121℃,灭菌时间20—30分钟。【注意事项】 1.物理监测有一定的局限性,只能证实灭菌循环参数是否符合要求,只能监测腔体 中的一点温 度(灭菌器排水口),无法监测包装内部情况。同时不能直接反应微生物死亡,也无法直接 和精确考核蒸汽质量、不可压缩气体、冷空气等; 2.新购置的设备或维修后的灭菌器,对各项灭菌参数必须进行物理校正; 3.物理监测不合格时,所有物品不能灭菌发放。应分析原因改进,直至监测结果
符合要求; 4.整个灭菌过程中,灭菌人员不得离开,时刻观察仪器仪表运行的情况; 5.物理监测各项内容均详实、客观记录,归档备查。 (二)化学监测方法 【目的】 通过化学反应原理,利用各种化学指示物与灭菌介质的相互作用,在特定的灭菌条件下产生化学反应而产生颜色变化。通过观察测试品颜色变化情况,来达到对灭菌过程的监测。 【特点】 可监测每个灭菌包内部的灭菌状况,具有快速、简单和费用低廉等,能及时反应每个灭菌物品包内外的灭菌效果,但不能直接反应微生物死亡。 【种类】包内化学指示物、包外化学指示物、BD测试纸。 1、B-D试验(适用于预排气压力蒸汽灭菌器) 【目的】 对预真空和脉动真空压力蒸汽灭菌器进行真空系统性能测试,通过检测灭菌器冷空气排除和热蒸汽穿透的效果。灭菌完毕取出测试图,通过观察其颜色变化情况,以判断试验包中有无残留空气存在。 【监测频次】 每台灭菌器每天灭菌前空锅进行B-D试验。资料留存时间3年以上。 【操作流程】【方法步骤】 →
环境及消毒灭菌效果监测制度
环境及消毒灭菌效果监测制度 一、监测目的 为有效评价医院消毒设备是否正常,消毒药剂是否有效,消毒方法是否合理,消毒效果是否达标,定期对医院环境及消毒灭菌效果等进行监测,以有效预防医院感染,保证医疗安全。 二、监测范围 对医疗环境、医务人员手、使用中的消毒液、紫外线灯、压力蒸汽灭菌、消毒灭菌后物品等进行监测,并做好监测记录,对不符合要求的立即整改。 三、监测要求 (一) 压力蒸汽灭菌 1.物理监测:每锅登记温度、压力、时间、锅次、物品、消毒员等。 2.化学监测:常规进行包外、包内化学指示物监测。采用快速压力蒸汽灭菌程序灭菌时,应直接将一片包内化学指示物置于待灭菌物品旁边进行化学监测。 3.生物监测:每周一次,有植入物时每锅进行生物监测。 (二) 紫外线灯 1.日常监测:登记照射时间、累计使用时间、使用人签名,每周一次擦拭记录。 2.强度监测:每半年一次,有监测记录。 (三) 消毒剂 1.化学指示卡监测:含氯消毒剂每日监测,戊二醛每周监测,有记录。 2.生物监测:消毒剂每季进行生物学监测。使用中的灭菌用消毒液要求:无细菌生长;使用中皮肤黏膜消毒液染菌量:≤10cfu/ml;其他使用中消毒液染菌量≤100cfu/ml。 (四)医疗环境、医务人员手的清洁消毒效果监测 每季度对感染高风险部门(病房手术室、外科门诊手术室、妇科门诊手术室、口腔科、检验科、供应室、急诊室)、普通科室的治疗室、注射室、换药室等部门进行空气、医务人员手、物体表面、使用中的消毒剂、消毒灭菌后物品的微生物监测一次;当怀疑与医院感染暴发有关时,及时进行监测,并进行相应致病性微生物的检测。 1.灭菌后的物品不得检出任何微生物。消毒后的医疗用品不得检出致病微生物(乙型溶血性链球菌、金黄色葡萄球菌及其他治病微生物)。 2.各治疗室空气中细菌数≤4cfu/(5min·直径9cm平皿),物体表面的细菌菌落总数≤10cfu/ cm2。 3.手术室空气中细菌总数≤4cfu/(15min·直径9cm平皿);物体表面的细菌菌落总数≤5cfu/ cm2。 4.卫生手消毒,监测的细菌菌落总数应≤10cfu/cm2。外科手消毒,监测的细菌菌落总数应≤5cfu/cm2。
压力蒸汽灭菌效果的监测
压力蒸汽灭菌效果的监测 一、通用要求: 1. 对灭菌质量采用物理监测法、化学监测法和生物监测法进行。 2. 物理监测不合格的灭菌物品不得发放;并应分析原因进行改进,直至监测结果符合要求。 3. 包外化学监测不合格的灭菌物品不得发放,包内化学监测不合格的灭菌物品不得使用。并应分析原因进行改进,直至监测结果符合要求。 4. 生物监测不合格时,应尽快召回上次生物监测合格以来所有尚未使用的灭菌物品,重新处理;并应分析不合格的原因,改进后,生物监测连续三次合格后方可使用。 5. 灭菌植入性器械应每批次进行生物监测。生物监测合格后,方可发放。 6. 按照灭菌装载物品的种类,可选择具有代表性的PCD(PCD都不应该是产品名称,而是验证装置的一种工具.欧洲EN867-5标准中分为敷料PCD和管腔PCD。敷料PCD就是目前3M推广的那种试纸或生物菌片、管腔型PCD的标准是长1500mm,内径2mm,而目前来讲,只有环氧乙烷和低温甲醛能达到。生物PCD:生物体内,细胞的程序性死亡。5类化学指示物——酸碱指示剂,氧化还原指示剂,络合滴定指示剂,荧光指示剂,吸附指示剂。)进行灭菌效果的监测。 二、监测方法: (一)压力蒸汽灭菌效果的监测 1. 物理监测法: 每次灭菌应连续监测并记录灭菌时的温度、压力和时间等灭菌参数。温度波动范围在+3°C以内,时间满足最低灭菌时间的要求,同时应记录所有临界点的时间、温度与压力值,结果应符合灭菌的要求。 2. 化学监测法: (1)应进行包外、包内化学指示物监测。具体要求为灭菌包包外应有化学指示物,高度危险性物品包内应放置包内化学指示物,置于最难灭菌的部位。如果透过包装材料可直接观察包内化学指示物的颜色变化,则不必放臵包外化学指示物。通过观察化学指示物颜色的变化,判定是否达到灭菌合格要求。
2016年消毒灭菌效果监测方案
2016年消毒灭菌效果监测方案
2016年消毒灭菌效果监测方案 为进一步规范我院的环境卫生学监测工作,有效预防医院感染,根据《医疗机构消毒技术规范(WST 367-2012)》、《医院消毒卫生标准(GB 15982-2012)》、《医疗机构空气净化规范(WST 368-2012)》、《医院洁净手术部建筑技术规范(GB 50333-2013)》《医务人员手卫生规范》和《血液透析相关治疗用水》等规范的要求,结合我院实际,特制定本方案。本方案自2016年1月1日起实施。 一、监测标准 (一)采样和检查原则 1.采样后应尽快对样品进行相应指标的检测,送检时间不得超过4 h;若样品保存于O℃~4℃时,送检时间不得超过24 h。 2.常规监督检查可不进行致病性微生物检测,涉及疑似医院感染暴发、医院感染暴发调查或工作中怀疑微生物污染时,应进行目标微生物的检测。 3. I类环境为采用空气洁净技术的诊疗场所,分洁净手术部和其他洁净场所。Ⅱ类环境为非洁净手术部(室);产房;导管室;血液病病区、烧伤病区等保护性隔离病区;重症监护病区;新生儿室等。Ⅲ类环境为母婴同室;消毒供应中心的检查包装灭菌区和无菌物品存放区;血液透析中心(室);其他普通住院病区等。Ⅳ类环境为普通门(急)诊及其检查、治疗室;感染性疾病科门诊和病区。 (二)诊疗器械、器具和物品清洗的效果监测 1.手术器械:每月随机抽取消毒供应中心机械清洗、手工清洗的手术器械;将器械分为平面类、关节类、管腔类、结构复杂类四种类型,每类器械随机抽取5个清洗后样本进行ATP检测。 1.1采样时间:手术器械清洗后。 1.2采样部位:手术器械全表面。 1.3手术器械检测方法: 1.3.1采样:对器械的全部表面进行采样。 1.3.2激活/震荡:将采样棒蓝色末端彻底按压进入管腔内液体中,激活反应水平窄幅震荡5秒钟。 1.3.3测量:将采样棒放入荧光检测仪中读取数值。 2.内镜:将内镜分为灭菌内镜、高水平消毒内镜两种类型分别抽样检测;每季度抽取
消毒灭菌效果监测制度
消毒灭菌效果监测制度 (一)对使用中的消毒剂、灭菌剂进行染菌量和浓度检测 1.染菌量监测 消毒剂每季度1次,其细菌含量必须<100,不得检出致病性微生物。灭菌剂每月检测1次,不得检出任何微生物。 2.浓度检测 应根据消毒、灭菌剂的性能定期检测、如含氯消毒剂、过氧乙酸等应现用现配,每次配制后都应测试浓度,对戊二醛的监测应每周不少于2次,腔镜中心要每日监测。 (二)消毒灭菌物品进行消毒灭菌效果监测 1.消毒物品每季度监测1次,不得检出致病性微生物。 2.灭菌物品每月检测1次,不得检出任何微生物。 3.消毒后的内镜(如胃镜、肠镜、喉镜、气管镜),细菌总数≤20件,并未检出致病菌为合格。 4.灭菌后内镜(如腹腔镜、关节镜、胆道镜、膀胱镜、胸腔镜)未检出任何微生物为合格。 (三)紫外线消毒:应进行照射强度检测和生物检测。 1.照射强度检测 各科室应做好每支灯管应用时间、累计时间和使用人、监督人签名的登记。检测灯管照射强度,新灯管的照射强度50≧?2,使用中的灯管照射强度≧70?2。 2.生物检测 必要时进行 (四)环境卫生学检测 1.各科室按照要求每季度对本科重点区域的空气、物体表面及医护人员的手进行消毒灭菌效果监测。 2.医院感染管理科应每季度对重点科室及病房等进行环境卫生学检测,并做好检测统计分析。
3.判定标准:医院内感染检测监控目标 ①医院感染发病率(现患率)≤10%。 ②医院感染现患率实查率≧96%。 ③医院感染漏报率≤20%。 ④抗菌药物使用率≤60%。 ⑤清洁手术切口感染率≤0.5%。 ⑥医疗器械消毒灭菌合格率100%。 ⑦卫生手消毒后医务人员手表面菌落数应≤102;外科手消毒后医务人员手表面菌落数应≤52 ⑧Ⅰ、Ⅱ类环境科室物体表面细菌总数≤52;Ⅲ、Ⅳ类环境科室物体表面细菌总数≤102。 ⑨Ⅰ类环境科室空气细菌总数≤4.0/皿(30),Ⅱ类环境科室空气细菌总数≤4.0/皿(15),Ⅲ、Ⅳ类环境科室空气细菌总数≤4.0/皿(5)。 ⑩消毒后内镜细菌总数20件,并未检出致病菌。 ?使用中的灭菌用消毒液为无菌生长;使用中的皮肤粘膜消毒液染菌量≤10 ,其他使用中消毒液染菌量≤100吗,不得检出致病性微生物。 母婴同室、婴儿室、新生儿室及儿科病房的工作人员手上不得检出沙门氏菌、大肠埃希菌、溶血性链球菌、金黄色葡萄球菌。母婴同室、婴儿室、新生儿室及儿科病房的物体表面不得检出沙门菌。
供应室清洗消毒及灭菌效果监测制度
供应室清洗消毒及灭菌效果监测制度 一、应专人负责质量监测工作。 二、器械、器具和物品清洗质量的监测 1、日常监测在检查包装时进行,应目测和/或借助带光源放大镜检查。清洗后的器械表面及其关节、齿牙应光洁,无血渍、污渍、水垢等残留物质和锈斑。 2、定期抽查每月应至少随机抽查3个~5个待灭菌包内全部物品的清洗质量,检查的内容同日常监测,并记录监测结果。 三、灭菌质量的监测 4.4.1 通用要求 4.4.1.1 对灭菌质量采用物理监测法、化学监测法和生物监测法进行,监测结果应符合本标准的要求。 4.4.1.2 物理监测不合格的灭菌物品不得发放,并应分析原因进行改进,直至监测结果符合要求。 4.4.1.3 包外化学监测不合格的灭菌物品不得发放,包内化学监测不合格的灭菌物品不得使用。并应分析原因进行改进,直至监测结果符合要求。 4.4.1.4 生物监测不合格时,应尽快召回上次生物监测合格以来所有尚未使用的灭菌物品,重新处理;并应分析不合格的原因,改进后,生物监测连续三次合格后方可使用。 4.4.1.5 灭菌植入型器械应每批次进行生物监测。生物监测合格后,方可发放。 4.4.1.6 按照灭菌装载物品的种类,可选择具有代表性的PCD进行灭菌效果的监测。 4.4.2 压力蒸汽灭菌的监测 4.4.2.1 物理监测法:每次灭菌应连续监测并记录灭菌时的温度、压力和时间等灭菌参数。温度波动范围在+3℃内,时间满足最低灭菌时间的要求,同时应记录所有临界点的时间、温度与压力值,结果应符合灭菌的要求。 4.4.2.2 化学监测法 4.4.2.2.1 应进行包外、包内化学指示物监测。具体要求为灭菌包包外应有化学指示物,高度危险性物品包内应放置包内化学指示物,置于最难灭菌的部位。如果透过包装材料可直接观察包内化学指示物的颜色变化,则不必放置包外化学指示物。通过观察化学指示物颜色的变化,判定是否达到灭菌合格要求。 4.4.2.2.2 采用快速压力蒸汽灭菌程序灭菌时,应直接将一片包内化学指示物置于待灭菌物品旁边进行化学监测。 4.4.2.3 生物监测法 4.4.2.3.1 应每周监测一次,监测方法见附录A。 4.4.2.3.2 紧急情况灭菌植入型器械时,可在生物PCD中加入5类化学指示物。5类化学指示物合格可作为提前放行的标志,生物监测的结果应及时通报使用部门。 4.4.2.3.3 采用新的包装材料和方法进行灭菌时应进行生物监测。 4.4.2.3.4 小型压力蒸汽灭菌器因一般无标准生物监测包,应选择灭菌器常用的、有代表性的灭菌制作生物测试包或生物PCD,置于灭菌器最难灭菌的部位,且灭菌
消毒灭菌效果监测制度
消毒灭菌效果监测制度 This model paper was revised by the Standardization Office on December 10, 2020
消毒灭菌效果监测制度 (一)对使用中的消毒剂、灭菌剂进行染菌量和浓度检测 1.染菌量监测 消毒剂每季度1次,其细菌含量必须<100cfu/ml,不得检出致病性微生物。灭菌剂每月检测1次,不得检出任何微生物。 2.浓度检测 应根据消毒、灭菌剂的性能定期检测、如含氯消毒剂、过氧乙酸等应现用现配,每次配制后都应测试浓度,对戊二醛的监测应每周不少于2次,腔镜中心要每日监测。 (二)消毒灭菌物品进行消毒灭菌效果监测 1.消毒物品每季度监测1次,不得检出致病性微生物。 2.灭菌物品每月检测1次,不得检出任何微生物。 3.消毒后的内镜(如胃镜、肠镜、喉镜、气管镜),细菌总数≤20cfu/件,并未检出致病菌为合格。 4.灭菌后内镜(如腹腔镜、关节镜、胆道镜、膀胱镜、胸腔镜)未检出任何微生物为合格。 (三)紫外线消毒:应进行照射强度检测和生物检测。 1.照射强度检测 各科室应做好每支灯管应用时间、累计时间和使用人、监督人签名的登记。检测灯管照射强度,新灯管的照射强度50≧W/cm2,使用中的灯管照射强度≧70W/cm2。 2.生物检测 必要时进行
(四)环境卫生学检测 1.各科室按照要求每季度对本科重点区域的空气、物体表面及医护人员的手进行消毒灭菌效果监测。 2.医院感染管理科应每季度对重点科室及病房等进行环境卫生学检测,并做好检测统计分析。 3.判定标准:医院内感染检测监控目标 医院感染发病率(现患率)≤10%。 医院感染现患率实查率≧96%。 ③医院感染漏报率≤20%。 ④抗菌药物使用率≤60%。 ⑤清洁手术切口感染率≤%。 ⑥医疗器械消毒灭菌合格率100%。 ⑦卫生手消毒后医务人员手表面菌落数应≤10cfu/cm2;外科手消毒后医务人员手表面菌落数应≤5cfu/cm2 ⑧Ⅰ、Ⅱ类环境科室物体表面细菌总数≤5cfu/cm2;Ⅲ、Ⅳ类环境科室物体表面细菌总数≤10cfu/cm2。 ⑨Ⅰ类环境科室空气细菌总数≤皿(30min),Ⅱ类环境科室空气细菌总数≤皿(15min),Ⅲ、Ⅳ类环境科室空气细菌总数≤皿(5min)。 ⑩消毒后内镜细菌总数20cfu/件,并未检出致病菌。 使用中的灭菌用消毒液为无菌生长;使用中的皮肤粘膜消毒液染菌量≤10cfu/ ml,其他使用中消毒液染菌量≤100cfu/ml吗,不得检出致病性微生物。
消毒灭菌效果监测
消毒灭菌效果监测 This model paper was revised by the Standardization Office on December 10, 2020
消毒灭菌效果监测 医院必须对消毒、灭菌效果定期进行监测,灭菌合格率必须达到100%;不合格物品不得进入临床使用部门 1.1、使用中的消毒剂、灭菌剂:应进行生物和化学监测。生物监测:消毒剂每季度一次,其细菌含量必须<100cfu/m1,不得检出致病性微生物;灭菌剂每月监测一次,不得检出任何微生物。化学监测:应根据消毒、灭菌剂的性能定期监测,如含氯消毒剂、过氧乙酸等应每日监测,对戊二醛的监测应每周不少于一次,应同时对消毒、灭菌物品进行消毒、灭菌效果监测,消毒物品不得检出致病性微生物,灭菌物品不得检出任何微生物。 1.2、紫外线消毒:应进行日常监测、紫外灯管照射强度监测和生物监测。日常监测包括灯管应用时间、累计照射时间和使用人签名。对新的和使用中的紫外灯管内进行照射强度监测,新灯管的照射强度不得低于100uW/cm2。使用中灯管不得低于70uw/cm2照射强度监测应每半年一次、生物监测必要时进行,经消毒后的物品或空气中的自然菌应减少90.00%以上,人工染菌杀灭率应达到99.90%。 1.3、各种消毒后的内窥镜(如胃镜,肠镜,喉镜,气管等)及其它消毒物品:应每季度进行监测,不得检出致病微生物。 1.4、各种灭菌后的内窥镜(如腹腔镜、关节镜、胆道镜、膀镜、胸腔镜等)、活检钳和灭菌物品:必须每月进行监测,不得检出任何微生物。 1.5、血液净化系统;必须每月对入、出透析器的透析液进行监测。当疑有透析液污染或有严重感染病例时,应增加采样点,如原水口、软化水出口、反渗水出口、透析液配液口等,并及时进行监测。当检查结果超过规定标准值时,须再复查。标准值为:透析器入口液的细菌菌落总数必须≤200cfu/ml,出口液的细菌的落总数必须≤2000cfu/m1,并不得检出致病微生物。
压力蒸汽灭菌效果的监测方法文档
压力蒸汽灭菌效果的监测方法 (一)物理监测方法 【目的】 是通过仪表和记录的曲线图等显示,判定物品灭菌处理中机械运行状况是否达到灭菌标准规定的条件。 【频次频次】 每次灭菌应连续监测并记录灭菌时的温度、压力和时间等灭菌参数。温度波动范围+3℃以内,时间满足最低灭菌时间的要求,同时应记录所有临界点的时间、温度与压力值,结果应符合灭菌的要求。记录资料留存时间≥3年。 【结果判定】 1.预真空压力蒸汽灭菌器的灭菌压力为205、8KPa ,温度为132-134℃,灭菌时间最低4分钟,真空度8.oKPa 。脉动预真空循环3次以上。硬质容器、超重、外来器械灭菌时间应参考使用器械厂商的说明适当延长; 2.下排气压力蒸汽灭菌器的灭菌压力为102、9KPa ,温度为121℃,灭菌时间20—30分钟。【注意事项】 1.物理监测有一定的局限性,只能证实灭菌循环参数是否符合要求,只能监测腔体中的一点温度(灭菌器排水口),无法监测包装内部情况。同时不能直接反应微生物死亡,也无法直接和精确考核蒸汽质量、不可压缩气体、冷空气等; 2.新购置的设备或维修后的灭菌器,对各项灭菌参数必须进行物理校正; 3.物理监测不合格时,所有物品不能灭菌发放。应分析原因改进,直至监测结果符合要求; 4.整个灭菌过程中,灭菌人员不得离开,时刻观察仪器仪表运行的情况; 5.物理监测各项内容均详实、客观记录,归档备查。 (二)化学监测方法 【目的】 通过化学反应原理,利用各种化学指示物与灭菌介质的相互作用,在特定的灭菌条件下产生化学反应而产生颜色变化。通过观察测试品颜色变化情况,来达到对灭菌过程的监测。【特点】 可监测每个灭菌包内部的灭菌状况,具有快速、简单和费用低廉等,能及时反应每个灭菌物品包内外的灭菌效果,但不能直接反应微生物死亡。 【种类】包内化学指示物、包外化学指示物、BD测试纸。 1、B-D试验(适用于预排气压力蒸汽灭菌器) 【目的】 对预真空和脉动真空压力蒸汽灭菌器进行真空系统性能测试,通过检测灭菌器冷空气排除和热蒸汽穿透的效果。灭菌完毕取出测试图,通过观察其颜色变化情况,以判断试验包中有无残留空气存在。 【监测频次】 每台灭菌器每天灭菌前空锅进行B-D试验。资料留存时间3年以上。 【操作流程】【方法步骤】
消毒与灭菌效果监测制度
消毒灭菌效果监测制度 医院必须对消毒、灭菌效果定期进行监测并做好记录备查。灭菌合格率必须达到100%, 不合格物品不得进入临床使用。监测方法见中华人民共和国卫生部《消毒技术规范》(2002 年版) 。 1、对使用中消毒剂、灭菌剂进行生物和化学监测。 (1)生物监测: 消毒剂每季度一次, 其含菌量必须〈100 时, 不得检出致病原性微生物; 灭菌剂每月监测一次, 不得检出任何微生物 (2)化学监测: 根据消毒、灭菌剂的性能定期监测, 如含氯消毒剂、过氧乙酸等应每日监测,戍二醒的监测, 每周不少于一次 (3)对消毒、灭菌物品进行效果监测, 消毒物品不得检出致病性微生物, 灭菌物品不得检出任何微生物。 (4)必须对压力蒸汽灭菌器进行工艺监测、化学监测、和生物监测。 (5)工艺监测应每锅进行, 并详细记录。 (6)化学监测应每包进行, 手术包尚需进行中心部位的化学监测。预真空压力蒸汽灭菌器每天灭菌前第一锅需进行试验。 (7)生物监测应每月进行, 新灭菌器使用前必须先进行
生物监测, 合格后才能使用; 对拟采用的新包装容器、摆放方式、排气方式及特殊灭菌工艺, 也必须进行生物监测, 合格后才能采用。 (8)环氧乙: 院气体灭菌: 必须每锅进行工艺监测、每包进行化学监测, 每月进行生物监测。 (9)紫外线消毒: 应进行日常照射强度和生物监测。日常监测包括灯管应用时间、累积照射时间、使用人签名和新灯管照射强度监测, 新灯管的照射强度不低于100 μ2, 使用中灯管不得低于70 μ2 。照射强度监测应每半年一次, 生物监测必要时进行。 (10)各种消毒后的内镜( 如胃镜、肠镜、喉镜等) 及其它消毒物品应每季度进行监测, 不得检出致病性微生物。 (11)各种灭菌后内镜( 如腹腔镜、关节镜、胆道镜、膀脱镜、胸腔镜等) 、活检钳和灭菌物品,必须每月进行监测, 不得检出任何微生物。 2、进入人体无菌组织、器官或接触破损皮肤、粘膜的医疗用品和接触皮肤、粘膜的医疗用品卫生标准: 应符合《医院消毒卫生标准》(15982-1995)( 附录三) 中4.2 规定。监测方法见《医院消毒卫生标准》( 15982-1995) 。
消毒灭菌效果监测实施方案
消毒灭菌效果监测实施方 案 This manuscript was revised by the office on December 10, 2020.
吐哈石油医院2015年消毒灭菌效果监测 实施方案 医院消毒是预防医院内感染的重要措施之一,消毒效果的监测是评价其消毒设备运转是否正常、消毒药剂是否有效、消毒方法是否合理、消毒效果是否达标的唯一手段。为规范消毒效果监测,依据卫计委《医院感染管理办法》、《医院感染监测规范》、《医院消毒技术规范规范(2012版)》特制定哈密地区中心医院消毒灭菌效果监测实施方案。 一、监测项目: 1. 空气消毒效果的监测; 2. 手和物体表面的消毒效果监测; 3. 牙科用水的监测; 4. 内镜消毒及灭菌效果的监测; 5. 使用中消毒剂及灭菌剂的监测; 6. 压力蒸汽灭菌效果监测; 7. 血液透析用水和透析液的监测 8. 灭菌物品监测 二、监测单的填写: 1.空气监测:采样地点、样品名称(空气)、采样时间、采样人,检验项目:细菌总数、致病菌(如金黄色葡萄球菌、溶血性链球菌等)。 2.物表监测:采样地点、物表名称(注明所采物品的名称和部位)、采样人、采样时间、检验项目、细菌总数、致病菌(如金黄色葡萄球菌等)。 3.手监测:采样地点、被监测人姓名、采样人、采样时间、检验项目:细菌总数、致病菌(如金黄色葡萄球菌等)。 4.其他物品的监测:采样地点、样品名称、检验项目、采样人、采样时间等。 (一)空气消毒效果的监测 1.监测科室:非洁净手术室、产房、血透室、消毒供应室等。 2.监测频次:重点科室每季度一次,如有疑似感染发生随时采样。 3.采样(沉降法) ⑴采样时间:空气消毒后4小时内、操作前。 ⑵平板暴露法:(非洁净手术室)暴露前先检查平板是否污染,是否有气泡及霉点。将普通营养琼脂平板(直径为 9cm)放在室内各采样点处,采样高度为距地面0.8m-- 1.5m,采样时将平板盖打开,斜扣放于平板旁,暴露 15min,在放置、收取平皿时,手不能在暴露平皿的正上方移动。
清洗消毒及其灭菌效果监测规范标准
清洗消毒及灭菌效果监测标准 基本信息 中文名称清洗消毒及灭菌效果监测标准 外文名称surveillance standardfor cleaning, disinfection and steriliztion 引用文件GB15982 医院消毒卫生标准 前言 根据《中华人民共和国传染病防治法》和《医院感染管理办法》制定本标准。 本标准第4.2.2.2.1、4.4.1.6、4.4.2.3.2为推荐性,其余为强制性条款。 附录A、附录B、附录C为规范性附录。 本标准由卫生部医院感染控制标准专业委员会提出。 本标准主要起草单位:北京大学第一医院、卫生部医院管理研究所、北京协和医院、中国疾病预防控制中心、上海瑞金医院、广州市第一人民医院、江苏省南京市卫生局、煤炭总医院、北京大学人民医院。 本标准主要起草人:李六亿、巩玉秀、么莉、任伍爱、张青、张流波、李新武、钱黎明、冯秀兰、王易非、钟秀玲、武迎宏、张宇、黄靖雄。 1 范围
本标准规定了医院消毒供应中心(central sterile supply department ,CSSD)消毒与灭菌效果监测的要求与方法和质量控制过程的记录与可追溯要求。 本标准适用于医院CSSD和为医院提供消毒灭菌服务的社会化消毒灭菌机构。暂未实行消毒供应工作集中管理的医院,其手术部(室)的消毒供应工作应执行本标准。 已采取污水集中处理的其他医疗机构可参照使用。 2 规范性引用文件 下列文件中的条款通过本标准的引用而成为本标准的条款。凡是标注日期的引用文件,其随后所有的修改(不包括勘误内容)或修订版均不适用于本标准,然而,鼓励根据本标准达成协议的各方研究是否可使用这些文件的最新版本。凡是不注明日期的引用文件,其最新版本适用于本标准。 GB15982 医院消毒卫生标准 GB 18278 医疗保健产品灭菌确认和常规控制要求(工业湿热灭菌第1篇压力蒸汽灭菌效果评价方法与标准) WS310.1 医院消毒供应中心第1部分:管理规范 WS 310.2 医院消毒供应中心第2部分:清洗消毒及灭菌技术操作规范 消毒技术规范卫生部 3 术语和定义 WS310.1和WS 310.2的术语和定义以及下列术语和定义适用于本标准。 3.1可追溯traceability 对影响灭菌过程和结果的关键要素进行记录,保存备查,实现可追踪。 3.2灭菌过程验证装置process challenge device,PCD
消毒灭菌效果检测方法.
一、手和皮肤黏膜消毒效果监测 1、采样时间:在消毒后立即采样。 2、采样方法 (1) 手的采样:被检人五指并拢,用浸有含相应中和剂的无菌洗脱液的棉拭子在双手指屈面从指根到指端往返涂擦 2 次(一只手涂擦面积约 30cm2),并随之转动采样棉拭子,剪去操作者手接触部位,将棉拭子投入 10ml 含相应中和剂的无菌洗脱液试管内,立即送检。 (2) 皮肤粘膜采样:用 5cm×5cm 的标准灭菌规格板,放在被检皮肤处,用浸有含相应中和剂的无菌洗脱液的棉拭子 1 支,在规格板内横竖往返均匀涂擦各 5 次,并随之转动棉拭子,剪去手接触部位后,将棉拭子投入 10ml 含相应中和剂的无菌洗脱液的试管内,立即送检。不规则的粘膜皮肤处可用棉拭子直接涂擦采样。3、检测方法 (1) 细菌总数检测:将采样管在混匀器上振荡20s或用力振打 80 次,用无菌吸管吸取 1.0ml 待检样品接种于灭菌平皿,每一样本接种2个平皿,内加入已溶化的45℃~48℃的营养琼脂 15ml~18ml,边倾注边摇匀,待琼脂凝固,置 36℃±1℃温箱培养 48h,计数菌落数。 采样结果计算方法: 平板上菌落数 ×稀释倍数 细菌总数(cfu/cm2)=──────────────── 采样面积(cm2) (2) 致病菌检测:致病菌的检测依据污染情况进行相应指标检测的原则执行。 4、结果判定 (1) 消毒洗手 Ⅰ、Ⅱ类区域工作人员:细菌总数≤5cfu/cm2,并未检出金黄色葡萄球菌、大肠杆菌、铜绿假单孢菌为消毒合格。 Ⅲ类区域工作人员:细菌总数≤10cfu/cm2,并未检出金黄色葡萄球菌、大肠杆菌为消毒合格。 Ⅳ类区域工作人员:细菌总数≤15cfu/cm2,并未检出金黄色葡萄球菌、大肠杆菌为消毒合格。 母婴同室、婴儿室、新生儿室及儿科病房的工作人员手上,不得检出沙门菌、大肠杆菌、溶血性链球菌、金黄色葡萄球菌为消毒合格。 (2)皮肤黏膜:参照手的卫生学标准执行。 5、注意事项 皮肤粘膜采样处,若表面不足 5cm×5cm 可用相应面积的规格板采样。 二、物品和环境表面消毒效果的监测
消毒灭菌效果监测制度
消毒灭菌效果监测制度-标准化文件发布号:(9456-EUATWK-MWUB-WUNN-INNUL-DDQTY-KII
消毒灭菌效果监测制度医院消毒灭菌及管理部门必须对消毒、灭菌效果定期进行监测并做好记录备查。灭菌合格率必须达到100%,不合格物品不得进入临床使用。监测方法见卫生部《消毒技术规范》(2002年版)。 1、对使用中的消毒剂、灭菌剂应进行化学和生物监测。 1)化学监测:根据消毒、灭菌剂的性能定期进行有效浓度监测,如含氯消毒剂、过氧乙酸等应每日监测,戊二醛的监测,每周不少于一次。用于内镜消毒或灭菌的戊二醛必须每日或使用前进行监测。 2)生物监测:消毒剂每季度一次,其细菌含量必须﹤100cfu/ml,不得检出致病性微生物;灭菌剂每月一次,不得检出任何微生物。 2、对消毒、灭菌物品进行效果监测。 消毒后直接使用的物品(包括各种消毒后的内镜及其他物品)应每季度进行生物监测,细菌总数<20cfu/件,不得检出致病性微生物;灭菌物品(包括各种灭菌后内镜如腹腔镜、关节镜、胆道镜、膀胱镜、活检钳和其他灭菌物品)每月进行生物监测,不得检出任何微生物。 3、压力蒸汽灭菌的监测。 必须对压力蒸汽灭菌器进行物理、化学、生物监测(遵循《医院消毒供应中心:清洗消毒及灭菌效果监测标准》)。 1)物理监测:每次灭菌应连续监测并记录灭菌时的温度、压力和时间等灭菌参数。温度波动范围+3℃以内,时间满足最低灭菌时间的要
求,同时应记录所有临界点的时间、温度与压力值,结果应符合灭菌的要求。 2)化学监测:应进行包内、包外化学指示物监测。具体要求为灭菌包包外应有化学指示物,高度危险性物品包内应放置化学指示物,置于最难灭菌的部位。如果透过包装材料可直接观察包内化学指示物的颜色变化,则不必放置包外化学指示物。通过观察化学指示物颜色的变化,判断是否达到灭菌合格要求。采用快速压力蒸汽灭菌程序灭菌时,应直接将一片包内化学指示物置于待灭菌物品旁边进行化学监测。 3)生物监测:应每周监测一次 4)B-D试验:预真空(包括脉动真空)压力蒸汽灭菌器应每日开始灭菌前进行,B-D测试合格后,灭菌器方可使用。 5)灭菌器新安装、移位或大修后均应进行物理、化学、生物监测。生物监测、B-D试验应连续进行三次,三次均监测合格后方可使用。 4、过氧化氢低温等离子灭菌的监测 1)物理监测:每次灭菌应连续监测并记录每个灭菌周期的临界参数如舱内压、温度、过氧化氢的浓度、电源输入和灭菌时间等。灭菌参数要符合灭菌器的使用说明或操作手册的要求。 2)化学监测:每个灭菌物品包外应使用包外化学指示物,作为灭菌过程的标志;每包内最难灭菌位置放置包内化学指示物,通过观察其颜色变化,判断其是否达到灭菌合格要求。 3)生物监测:应每天至少进行一次灭菌循环的生物监测。
供应室压力蒸汽灭菌锅生物监测报告.doc
供应室压力蒸汽灭菌锅生物监测报告 。LS压力蒸汽灭菌锅生物监测报告生物监测灭菌器类型灭菌温度(℃)灭菌时间(分钟)生物指示剂(管)生物监测结果监测人结果报告日期监测方法名称有效期标准包装指示剂(管)标签控制指示剂(管) 标签灭菌后56℃恒温器48 hxg1-DM3M-证明灭菌后56℃恒温器48 hxg1-DM3M-证明灭菌后48 hxg1-DM3M-证明在56℃恒温器中灭菌后48 hxg1-DM3M-证明在56℃恒温器中灭菌后48 hxg1-DM3M-证明在56℃恒温器中灭菌后48 hxg1-DM3M-证明在56℃恒温器中灭菌后48 hxg1-DM3M-证明在56℃恒温器中灭菌后48 hxg1-DM3M-证明在生物监测结果监测人员结果报告日期2012年监测方法名称有效期标准包装指示器(试管)标签控制点指示器(试管)标签灭菌,然后放入56℃培养箱48hSTE-16L3M-A-a中。试验灭菌后,将其放入56℃培养箱48hSTE-16L3M-A中灭菌,然后放入56℃培养箱48HSte-16L 3M-A中灭菌,放入56℃培养箱48HSte-16L 3M-A中灭菌,放入56℃培养箱中灭菌并置于56℃的培养箱中进行48hSTE-16L灭菌。灭菌后,将3M-Endex置于56℃的培养箱中进行48hSte-16LM-Endex灭菌,然后置于56℃的培养箱中进行48hSte-16LM-Endex灭菌时间: 134℃4分钟无包装,6分钟无包装,134℃18分钟无包装,121℃16分钟无包装,20分钟无包装。 毛毛雨还在下。当月亮照耀时,照亮你的民歌依然如故。 闪闪发光的星星升了起来,杨树的绿色影子还在旋转。好风就像水。你可以无惧地安睡。
消毒灭菌效果监测方案
消毒灭菌效果监测 方案
消毒灭菌效果监测方案 为进一步规范我院的环境卫生学监测工作,有效预防医院感染,根据《医疗机构消毒技术规范(WST 367- )》、《医院消毒卫生标准(GB 15982- )》、《医疗机构空气净化规范(WST 368- )》、《医院洁净手术部建筑技术规范(GB 50333- )》《医务人员手卫生规范》和《血液透析相关治疗用水》等规范的要求,结合我院实际,特制定本方案。本方案自 1月1日起实施。 一、监测标准 (一)采样和检查原则 1.采样后应尽快对样品进行相应指标的检测,送检时间不得超过4 h;若样品保存于O℃~4℃时,送检时间不得超过24 h。 2.常规监督检查可不进行致病性微生物检测,涉及疑似医院感染暴发、医院感染暴发调查或工作中怀疑微生物污染时,应进行目标微生物的检测。 3.I类环境为采用空气洁净技术的诊疗场所,分洁净手术部和其它洁净场所。Ⅱ类环境为非洁净手术部(室);产房;导管室;血液病病区、烧伤病区等保护性隔离病区;重症监护病区;新生儿室等。Ⅲ类环境为母婴同室;消毒供应中心的检查包装灭菌区和无菌物品存放区;血液透析中心(室);其它普通住院病区等。Ⅳ类环境为普通门(急)诊及其检查、治疗室;感染性疾病科门诊和病区。 (二)诊疗器械、器具和物品清洗的效果监测 1.手术器械:每月随机抽取消毒供应中心机械清洗、手工清洗的手术
器械;将器械分为平面类、关节类、管腔类、结构复杂类四种类型,每类器械随机抽取5个清洗后样本进行ATP检测。 1.1采样时间:手术器械清洗后。 1.2采样部位:手术器械全表面。 1.3手术器械检测方法: 1.3.1采样:对器械的全部表面进行采样。 1.3.2激活/震荡:将采样棒蓝色末端彻底按压进入管腔内液体中,激活反应水平窄幅震荡5秒钟。 1.3.3测量:将采样棒放入荧光检测仪中读取数值。 2.内镜:将内镜分为灭菌内镜、高水平消毒内镜两种类型分别抽样检测;每季度抽取科室25%内镜数量进行ATP监测。 2.1采样时间:内镜清洗后。 2.2采样部位:内镜外表面及内腔面。 2.3软式内镜检测方法: 2.3.1内镜外表面的检测方法: 2.3.1.1取样:取末端10cm长的外表面进行采样,对采样棒施加适当压力,旋转采样棒,以“Z”形取样。 2.3.1.2激活/震荡:将采样棒蓝色末端彻底按压进入管腔内液体中,激活反应水平窄幅震荡5秒钟。 2.3.1.3测量:将采样棒放入荧光检测仪中读取数值。 2.3.2内腔:吸引/活检管道的检测方法 2.3.2.1准备:把检测工具包中的连接管,塞子连接到位。
消毒灭菌效果监测
消毒灭菌效果监测 医院必须对消毒、灭菌效果定期进行监测,灭菌合格率必须达到100%;不合格物品不得进入临床使用部门 1.1、使用中的消毒剂、灭菌剂:应进行生物和化学监测。生物监测:消毒剂每季度一次,其细菌含量必须<100cfu/m1,不得检出致病性微生物;灭菌剂每月监测一次,不得检出任何微生物。化学监测:应根据消毒、灭菌剂的性能定期监测,如含氯消毒剂、过氧乙酸等应每日监测,对戊二醛的监测应每周不少于一次,应同时对消毒、灭菌物品进行消毒、灭菌效果监测,消毒物品不得检出致病性微生物,灭菌物品不得检出任何微生物。 1.2、紫外线消毒:应进行日常监测、紫外灯管照射强度监测和生物监测。日常监测包括灯管应用时间、累计照射时间和使用人签名。对新的和使用中的紫外灯管内进行照射强度监测,新灯管的照射强度不得低于100uW/cm2。使用中灯管不得低于70uw/cm2照射强度监测应每半年一次、生物监测必要时进行,经消毒后的物品或空气中的自然菌应减少90.00%以上,人工染菌杀灭率应达到99.90%。 1.3、各种消毒后的内窥镜(如胃镜,肠镜,喉镜,气管等)及其它消毒物品:应每季度进行监测,不得检出致病微生物。 1.4、各种灭菌后的内窥镜(如腹腔镜、关节镜、胆道镜、膀镜、胸腔镜等)、活检钳和灭菌物品:必须每月进行监测,不得检出任何微生物。 1.5、血液净化系统;必须每月对入、出透析器的透析液进行监测。当疑有透析液污染或有严重感染病例时,应增加采样点,如原水口、软化水出口、反渗水出口、透析液配液口等,并及时进行监测。当检查结果超过规定标准值时,须再复查。标准值为:透析器入口液的细菌菌落总数必须≤200cfu/ml,出口液的细菌的落总数必须≤2000cfu/m1,并不得检出致病微生物。
压力蒸汽灭菌效果监测方法完整版
压力蒸汽灭菌效果监测 方法 HEN system office room 【HEN16H-HENS2AHENS8Q8-HENH1688】
压力蒸汽灭菌效果监测方法 一、目的物理监测方法 :是通过仪表和记录的曲线图等显示,判定物品灭菌处理中机械运行状况是否达到灭菌标准规定的条件。 内容:监测灭菌器灭菌时的温度、压力、时间等灭菌参数。 判定结果:灭菌压力为,温度132—134°C 时间4min,脉动循环3次,真空在80kpa-﹣80kpa之间。 注意事项:物理监测只能证实灭菌参数是否符合要求;新购的设备或维修后,要对各项灭菌参数进行校正处理;监测不合格时,所有物品不能灭菌发放。 二、化学监测方法 1、B—D试验 目的:监测灭菌器内冷凝水的排除,通过其颜色变化情况判断。方法:将B—D试验包放于灭菌架底层,近排气口处上方,经过一个灭菌周期后,取出观察结果。 判定结果:颜色均匀为合格,不均匀有残留空气测试为不合格。注意事项:B—D只适用与预排气的灭菌器,每天第一次灭菌前进行;灭菌温度134°C 时间,观察结果;新安装或维修后要连续B—D监测3次,合格后才能使用。 2、包外化学指示胶贴 目的:说明物品包是否经过灭菌处理,但不能判定质量和效果。
注意事项:变色不合格的包,不能发放和使用。如果发现不合格应查找原因,重新更换在进行灭菌。 3包内化学指示物 目的:灭菌包在灭菌过程中的温度、时间、压力达到饱和,为使用无菌包的人员提供快速判定的灭菌效果的方法。 监测方法:经过一个灭菌周期后,打开灭菌包取出指示物,观察指示物的变色情况。 判定结果:变色均匀与对照区一致为合格。变色未达到要求为不合格。 注意事项:不合格的灭菌包不能使用。 三、生物监测方法 目的:用抗力较强的生物指示物进行灭活试验的监测方法,以判定灭菌质量是否合格,是最可靠的灭菌效果监测方法。 方法:近测试包放入灭菌架底层,近排气口处,经过一个灭菌周期,取出指示剂根据说明进行培养。 判定结果:阴性为合格,阳性为不合格。 注意事项:生物监测不合格必须停止使用灭菌器:植入物与外来器械必须有生物监测。 以上各种监测方法均要有详细记录,有操作员和质检员签名,记录保存3年以上。 主将:李永伶
