探究酶促反应速率

揭秘酶促反应速率
班级:高一(7)
组长:陈铭皓
组员:林钦泽、谢浩天、戴嘉文
指导老师:戈云、实验室黄老师
摘要:酶促反应是细胞代谢的基本反应。细胞中几乎所有的代谢反应都在
酶的作用下有条不紊地进行着。那么,酶促反应速率与底物浓度又有什么关系呢?
关键词:酶促反应、速率、底物浓度
一、背景
物质代谢是生命活动的基本特征,也是一切生命活动的基础。酶是由活细胞合成的生物催化剂,生物体内几乎所有的代谢反应都是在酶的作用下有条不紊地完成。酶最重要的特征是具有高效的催化能力,因而酶促反应的速率就代表了酶的活性。
酶的活性与很多因素有关,例如底物浓度、酶的浓度、温度、PH值、抑制剂和激活剂等。在本课题中,我们只研究酶促反应速率与底物浓度的数量关系。
二、实验探究
为了探究酶促反应速率与底物浓度的数量关系,我们在化学实验室进行了一次实验。实验药剂和器材如下:
1.普通漏斗一只;
2.500ml容量瓶一只;
3.5ml、50ml、100ml量筒各一只;
4.水槽一只;
5.胶头滴管一只;
6.分液漏斗与锥形瓶各一只;
7.导管、橡皮塞及秒表;
8.质量分数30%的过氧化氢溶液一瓶;
9.新鲜猪肝100克。
实验过程如下:
1.用新鲜猪肝加水研磨,制成猪肝研磨液;
2.定容,配置500毫升的溶液。
3.取50毫升研磨溶液置于锥形瓶,在分液漏斗中加入0.5毫升过氧化
氢溶液,5秒后将气体通入倒置量筒,排水收集,两秒后读出体积,
重复两次,计算平均值,为15毫升;
4.重取50毫升研磨液,分别加入1毫升、2毫升、3毫升、4毫升、6
毫升、8毫升、12毫升、16毫升、150毫升的过氧化氢,重复步骤
3,得到数据25毫升、40毫升、50毫升、57毫升、68毫升、75
毫升、82毫升、90毫升、112毫升;
5.收拾器具。
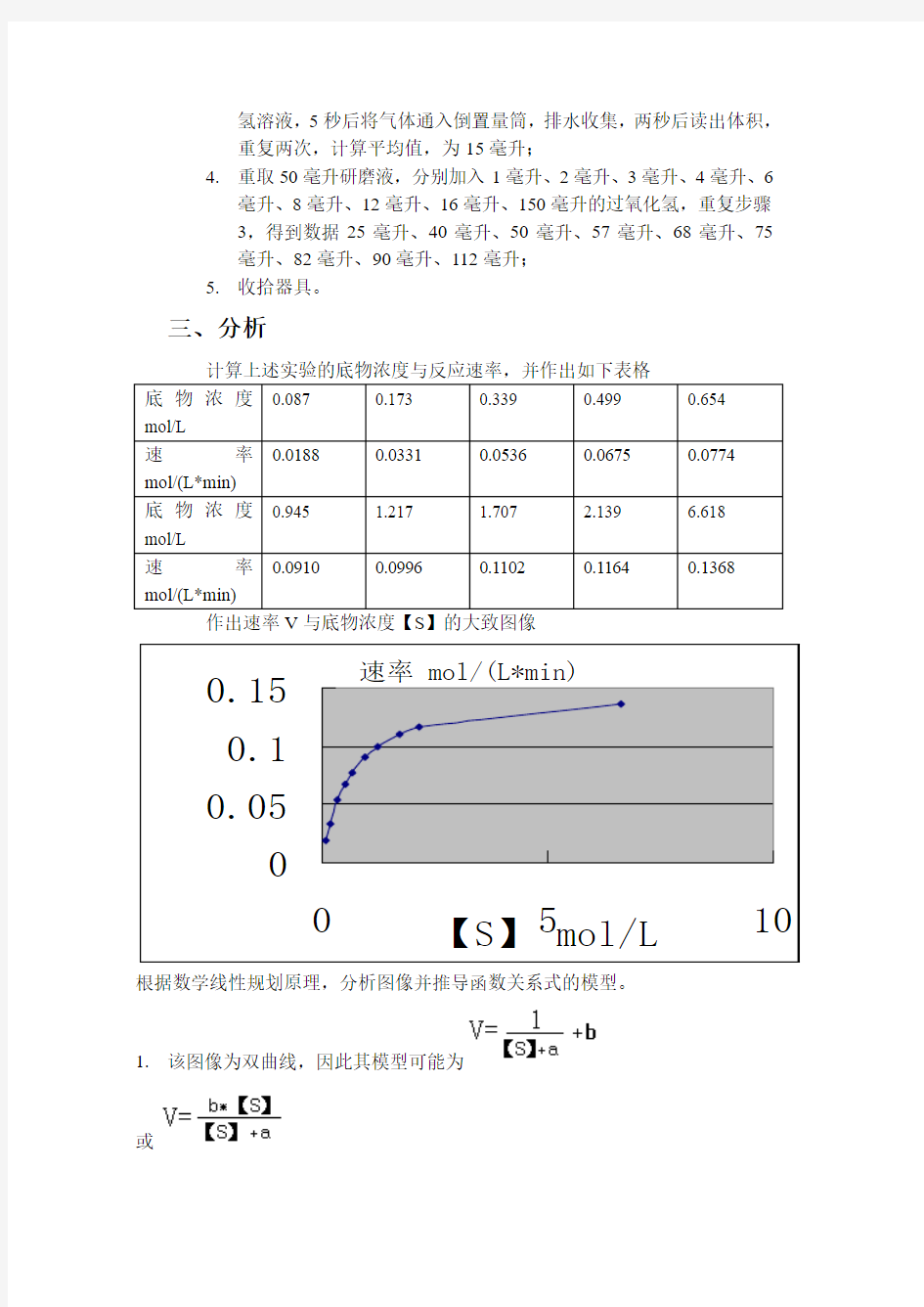
三、分析
根据数学线性规划原理,分析图像并推导函数关系式的模型。
1.该图像为双曲线,因此其模型可能为
或
2.将代入三组数值进行运算,发现不符合
图像,而将代入三组数值进行运算,发现符合图像,并算出b≈0.14,a≈0.62,其中b的单位为mol/(L*min),a的单位为mol/L.
3.观察a与b的值与单位,发现b几乎是该酶促反应的最大反应速率,而a似
乎是0.07 mol/(L*min)即最大反应速率一半时的底物浓度。
4.代入其他几组数据,计算,发现基本符合。
四、结论
在过氧化氢酶的酶促反应中,反应速率V等于最大反应速率与底物浓度的积处以底物浓度与最大反应速率的一半时底物浓度K的和,方程式为:
五、致谢
我们能够完成这项艰巨的课题,许多人的帮助是不可或缺的。首先,当然要感谢进行理论指导的化学老师戈云老师,以及亲自帮助我们进行实验的黄老师,是她们使得我们的研究得以逐步深入。其次,当然还要感谢支持我们的研究的班主任老师、生物老师和关注我们的各位同学,是你们给了我们克服困难的信心!
六、参考文献
1.《生物化学(第二版)》(科学出版社)
2.《生物化学精要》(东南大大学出版社)
化学反应速率及活化能测定实验报告
实验名称:化学反应速度与活化能的测定 一、实验目的 1、测定Na2SO3与KIO3反应的速率、反应级数,速率系数和反应的 活化能; 2、了解浓度、温度、催化剂对化学反应速率的影响。 二、实验原理 (NH4)2S2O8+3KI=(NH4)2SO4+K2SO4+KI3 S2O3^2-+3I^-=2SO4^2-+I3^- 五、数据结果 1、表3-1 2、表3-2 浓度对化学反应速率的影响 实验编号 1 2 3 4 5 试液的体积V/mL 0.2mol/L(NH4)2S2O8 20 10 5 20 20 0.2mol/LKI 20 20 20 10 5 0.01mol/LNa2S203 8 8 8 8 8 0.2%淀粉 4 4 4 4 4 0.2mol/LKNO3 0 0 0 10 15 0.2mol/L(NH4)2SO4 0 10 15 0 0 反应物的起始浓度c/mol/L (NH4)2S2O8 0.2 0.2 0.2 0.2 0.2 KI 0.2 0.2 0.2 0.2 0.2 Na2S2O3 0.01 0.01 0.01 0.01 0.01 反应开始至溶液显蓝色时所需时间 △t/s 76 172 324 178 300 反应的平均速率v/mol/L*S 0.000066 0.000029 0.000015 0.000028 0.000017 反应的速率常数k k=10140 反应级数 m=1 n=1 m+n=2 温度对化学反应速率的影 响 实验编号 反应温度T/℃ 反应时间△t/s 反应速率v/mol/L*S 反应速率常数 k Lgk 1/T 4 18.9 178 0.000028 10140 4.01 0.05 6 29 74 0.000068 22984 4.36 0.03
化学反应速率和限度教材分析报告文书
教材分析报告:“化学反应速率与反应限度” 化学111班11240119 灵君 必修二教版 专题2 化学反应与能量转化 第一单元化学反应速率与反应限度 一,单元与课标关系 (1)课标里的容标准:通过实验认识化学反应的速率和化学反应的限度,了解控制反应条件在生产和科学研究中的作用。 (2)对本单元的容分析(明线+暗线) 本单元的主要知识线是由化学反应速率与化学反应限度构成的。 化学反应速率主要容:定量描述化学反应进行的快慢,反应速率的计算,影响反应速率的因素,应用化学反应速率的知识,解释生活中的相关现象。 化学反应的限度主要容:认识可逆反应,与化学反应限度的含义,通过反应速率判断化学反应所能达到的限度,初步了解什么是化学平衡。 从课标来看,要学习的容是相对宏观的。根据对化学课程标准及教材的分析,可以确定本单元教学在知识技能的重点是化学反应速率的原理理解和化学反应限度的涵义,在过程与方法方面的重点是通过实验来认识这两方面的容在化学研究中的作用,学会在实验当中的观察,归纳总结这两块容的知识。情感态度价值观的重点是感受控制反应条件在科学研究中的作用。 二,教材单元知识分层建构及衔接 化学反应速率及限度涉及初中,高中必修,选修三个学习阶段的容:
初中反应的快慢(冷热),反应条件(燃烧是否完全),量的多少会 对生成物造车一些影响等基础的化学反应 高中必修化学反应速率描述化学反应的快慢,反应限度(可逆反应), 化学平衡的初步了解 高中选修《化学反应原理》化学平衡的移动,各种因素对化学平衡的 影响,化学反应速率与化学平衡的关系 图1 “化学反应速率及限度”涉及的主要容 这三个学习阶段是呈现螺旋上升的组织特点,三个阶段都是符合中学生的心理发展特点所制定的,所以本单元的知识处于中间地位,起着承上启下的作用,不仅在本书中是学科知识的关键,也是整个化学学习的重要组成部分。 三,教材单元知识结构 本单元在学生接触过大量的化学反应,并且对化学反应有了快与慢的经验的基础上,继续深入对于化学反应快慢的探究,告诉学生可以用定量的方式来描述化学反应的快慢,通过实验探究,引导学生总结出不同因素对反应速率的影响
酶促反应的影响因素影响
酶促反应的影响因素影响 实验八酶促反应的影响因素 一、目的要求 1(了解温度、pH、激活剂、抑制剂对酶促反应速度的影响。 2(学习检定温度、pH、激活剂、抑制剂影响酶促反应速度的方法。 二、实验原理 在酶促反应中,酶的催化活性与环境温度、 pH有密切关系,通常各种酶只有在一定的温度、pH范围内才表现它的活性,一种酶表现其活性最高时的温度、 pH 值称为该酶的最适温度、最适pH。 在酶促反应中,酶的激活剂和抑制剂可加速或抑制酶的活性,如氯化钠在低浓度时为唾液淀粉酶的激活剂,而硫酸铜则是它的抑制剂。 本实验利用淀粉水解过程中不同阶段的产物与碘有不同的颜色反应,定性观察唾液淀粉酶在酶促反应中各种因素对其活性的影响。 淀粉(遇碘呈蓝色)?紫色糊精(遇碘呈紫色)?红色糊精(遇碘呈红色)?无色糊精(遇碘不呈色)?麦芽糖(遇碘不呈色)?葡萄糖(遇碘不呈色)。 所以淀粉被唾液淀粉酶水解的程度,可由水解混合物遇碘呈现的颜色来判断,以此反映淀粉酶的活性,由此检定温度、pH、激活剂、抑制剂对酶促反应的影响。 三、实验器材 试管和试管架、恒温水浴、冰浴、吸量管(1 mL6支、2 mL4支、5 mL4支)、滴管、量筒、玻棒、白瓷板、秒表、烧杯、棕色瓶。 四、实验试剂
1(新鲜唾液稀释液(唾液淀粉酶液):每位同学进实验室自己制备,先用蒸馏水漱口,以清除食物残渣,再含一口蒸馏水,0.5 min后使其流入量筒并稀释至200倍(稀释倍数可因人而异)混匀备用。 2(1%淀粉溶液A(含0.3%NaCl):将1 g可溶性淀粉及0.3 g氯化钠混悬于5 mL 蒸馏水中,搅动后,缓慢倒入沸腾的60 mL蒸馏水中,搅动煮沸1 min,冷却至室温,加水至100 mL,置冰箱中保存。 3(1%淀粉溶液B(不含NaCl) 4(碘液:称取2 g碘化钾溶于5 mL蒸馏水中,再加入1 g碘,待碘完全溶解后,加蒸馏水295 mL,混匀贮于棕色瓶中。 5(1%NaCl溶液 6(1%CuSO溶液 4 7(缓冲溶液系统按下表混合配制。 0.2 mol/L磷酸氢二钠溶液 0.1 mol/L柠檬酸溶液 pH 体积/ mL 体积/ mL 5.0 5.15 4.85 5.8 6.05 3.95 6.8 7.72 2.28 8.0 9.72 0.28 五、操作步骤 1(温度对酶促反应的影响 取3支试管编号,按下表进行操作: 反应温淀粉酶酶液处理温1%淀粉溶试管pH6.8缓冲溶度/ 液体积度/ 液A体积/ 观察结果号液体积/ mL ?,10 / mL ?,5 min mL min 1 1 0 2 1 0
化学反应速率实验步骤
实验十化学反应速率实验(参考报告) 一、实验目的: 略 二、实验原理: 略 三、实验用品: 1.实验仪器: 10mL量筒、5mL注射器、50mL烧杯、恒温水浴锅、秒表、滴管、玻棒 2.实验试剂: 0.20mol/L (NH4)2S2O3、0.20mol/L KI、0.010 mol/L Na2S2O3、0.20mol/L KNO3、0.20mol/L (NH4)2SO4、0.20mol/L Cu(NO3)2、0.2%淀粉溶液 四、实验内容: 1.浓度对化学反应速率的影响: ①根据表1中的试剂用量分别将试剂同时迅速倒入50mL烧杯中,同时用秒表记时,当溶液开始变色时记下反应的时间,根据公式v=C(Na2S2O3)/2△t,计算反应速率v,数据记录及处理见表1: ②数据分析与讨论: 根据数据处理结果我们可知: a.当(NH4)2S2O8和KI的初始浓度最大时,反应的时间最短,反应速率最大; b.(NH4)2S2O8的初始浓度反应的时间与成反比,与反应速率成正比; c.KI的初始浓度反应的时间与成反比,与反应速率成正比; 根据以上规律我们得出结论:反应物的浓度对化学反应速率有影响,当反应物的初始浓度越高,反应的时间越短,化学反应速率越快。
2. 温度对化学反应速率的影响: ① 根据表1中第Ⅳ组的试剂用量分别进行三组实验,三组实验分别在温度比室温高10°C 、 15°C 、20°C 的条件下进行。将反应物先在恒温水浴锅中加热至条件所需温度,再进行反应,当溶液开始变色时记下反应的时间,根据公式v=C(Na 2S 2O 3)/2△t ,计算反应速率v ,数据记录及处理见表2: 室温:25°C ② 数据分析与讨论: 根据数据处理的结果我们可知:在反应初始浓度不变的情况下,随着温度升高,反应的时间减少,反应速率越快。 由此我们得出结论:温度越高,反应速率越快。 3. 催化剂对化学反应速率的影响: ① 根据表1中第Ⅳ组的试剂用量进行一组实验,在反应的开始,滴加2滴0.20mol/L Cu(NO 3)2溶液,记录反应时间,并且跟第Ⅳ组的数据作对比。根据公式v=C(Na 2S 2O 3)/2△t ,计算反应速率v ,数据记录及处理见表3: ② 数据分析与讨论: 将两组实验数据对比我们可知:在反应物初始浓度不变的情况下,加入催化物使反应的时间大幅缩短,反应速率提高了数十倍。根据有关的理论知识,我们已知,催化剂可以降低反应的活化能,使反应物迅速达到反应进行所需的能量,从而促进反应进行。 由以上结果我们可以得出结论:催化剂可以提高反应速率。 五、 思考题: 1. 反应液中为什么加入KNO 3、(NH 4)2SO 4? 答:当减少了实验中(NH 4)2S 2O 8或KI 的用量时,溶液中的NH 4+或K +物质的量减少,分别用(NH 4)2SO 4、KNO 3补足,目的是维持反应液中NH 4+或K +的离子强度不变,降低对实验结果的干扰。 2. 取(NH 4)2S 2O 8试剂量筒没有专用,对实验有何影响? 答:如果取(NH 4)2S 2O 8试剂量筒没有专用,有可能在所用的量筒中残留有KI 试剂或Na 2S 2O 3试剂,会在量筒中发生反应,改变了(NH 4)2S 2O 8的初始浓度,使实验结果不准确。 3. (NH 4)2S 2O 8缓慢加入KI 等混合溶液中,对实验有何影响? 答:如果将(NH 4)2S 2O 8缓慢加KI 等混合液中,那么(NH 4)2 S 2O 8的起始浓度,就处在不断变化中,使反应速率不断变化,不能得到准确数据。 4. 催化剂Cu(NO 3)2为何能够加快该化学反应的速率? 答:催化剂Cu(NO 3)2降低了反应所需达到的活化能,降低了发生反应的条件,使反应更容
【典型题】酶促反应速率问题的研究
[2003年上海高考生物第11题]下图纵轴为酶反应速度,横轴为底物浓度,其中正确表示酶量增加1倍时,底物浓度和反应速度关系的是 命题者提供的参考答案是B。但在K12生物论坛的讨论中,很多老师认为应该选A。也有老师说虽然知道应该选B,但总觉得理由不充分。笔者认为,要正确理解这道题目,首先是必须弄懂酶促反应速度(题目中如此,其实正确的说法,应该称为“酶促反应速率”)的含义,其次要有酶促反应的动力学的有关知识作为基础。下面,笔者先把那些认为应该选A 的老师提出的理由整理出来,然后介绍酶促反应速率的含义以及酶促反应的动力学的有关知识,并在此基础上阐述该题正确答案是B的理由。 1 许多老师错误地选A的理由 先观察A、B选项中任何一条曲线,曲线的前半段,随横坐标底物浓度的增加,纵坐标酶促反应速度也增加,说明底物浓度是此时反应速度增加的限制因素。此时,即使增加酶量也不会使反应速度也增加。而曲线的后半段反应速度不再随底物浓度变化而变化,说明底物足够,此时底物浓度已不是反应速度增加的限制因素了;此时,酶的数量则相对不足,此时增加酶量会使反应速度加快。综上所述,正确的曲线应该是最初两条曲线重合,底物浓度足够多时才能体现出酶的数量对反应速度的影响。 2 酶促反应速率的概念 酶促反应的速率(v),一般是以单位时间内底物被分解的量来表示的。假设x克蔗糖在t时间内被一定的蔗糖酶水解为葡萄糖和果糖,则x/t即为蔗糖酶反应的速率。 酶促反应在开始的初期速率较大,一定时间后,由于反应产物浓度逐渐增加,反应速率渐渐下降,最后完全停止。如果底物浓度相当大,而pH及温度又保持恒定,则在反应初期的一定短时限内,酶的反应速率尚不受反应产物的影响,可以保持不变。故测酶的反应速率一般只测反应开始后的初速,而不是测反应达到平衡时所需要的时间。 3 酶促反应的动力学(影响酶反应的因素)的相应知识 酶促反应的速率是受酶浓度、底物浓度、pH、温度、反应产物、变构效应、活化剂和抑制剂等因素的影响的。下面仅讨论与此题有关的酶浓度和底物浓度的影响。 3.1 酶浓度的影响 在有足够底物的情况下,而又不受其他因素的影响,则酶的反应速率(v)与酶浓度成正比。即 v=k[E] (1) k为反应速率常数,[E]为酶浓度。 因为有底物足够的条件,因此,对任一酶浓度[E],由(1)式求出的酶的反应速率v应当就是在该酶浓度下的最大反应速率Vmax。 3.2 底物浓度的影响(米氏方程) 实验证明:当酶浓度、温度和pH恒定时,在底物浓度很低的范围内,反应初速与底物浓度成正比;此后,随着底物浓度的增加,反应速率的增加量逐渐减少;最后,当底物浓度增加到一定量时,反应速率达到一最大值Vmax,此时再增加底物浓度也不能使反应速率再增加。1931年,Michaelis与Menten根据中间产物理论提出了能表示整个反应中底物浓度与反应速率关系的公式,称Michaelis-Menten方程或简称米氏方程:
《实验活动7 化学反应速率的影响因素》教案、导学案
《实验活动7 化学反应速率的影响因素》教案 【教学目标】 知识与技能: 1.进一步理解化学反应速率的概念及表示方法。 2.进一步掌握影响化学反应速率的因素。 过程与方法: 1.初步探究温度、浓度和催化剂对化学反应速率的影响结果。 2.认识实验方法的选择及反应条件的控制在实验探究中的重要性。 3.尝试用比较法来寻找实验的最佳方案。 情感态度与价值观: 1.通过实验,提高处理实验数据和分析实验结果的能力。 2.了解实验的反应原理,初步认识和把握实验成功的关键。 【教学重难点】 重点:影响化学反应速率的外界因素。 难点:实验方法的选择及反应条件的控制在实验探究中的重要性。 【教学方法】 策略方法:实验探究、学生讨论、教师分析 教学媒体选择:多媒体、烧杯、试管、量筒、试管架、胶头滴管、温度计、药匙、秒表 【教学过程】 [引入] 1.由现象到本质(带着问题走出课本): 利用蓝瓶子实验引入课题:实验比较法研究影响化学反应速率的外界因素。同样的试剂,用不同的力度振荡,显示蓝色的程度不一样。说明外因对反应的快慢有影响。 [对旧知识的回顾] 2.由定性到定量 (1)化学反应速率的表示方法:V = ?C / ? t
(2)化学反应速率的测定方法:测定的数据:时间变化? t,浓度变化?C 还可以测定其它哪些物理量也可以获得反应速率?(学生讨论) ①单位时间内产生气体体积:如 H 2O 2 分解制O 2 或CO 2 的制取 ②单位时间内体系颜色变化:如有关NO 2、I 2 (淀粉)的反应 ③单位时间内产物质量变化 ④单位时间内体系压强变化 视频演示H 2O 2 分解制O 2 反应速率的测定方法,了解描点法作图的方法。 3.由理论到实际(学会探究) 本堂课的主要任务是利用实验探究浓度和温度对S 2O 3 2- + 2H+ = SO 2 + S + H 2 O 反应速率的影响;利用实验探究催化剂对H 2O 2 分解速率的影响。 (1)如何测该反应的速率?测单位时间内SO 2 的体积产量,还是S单质的固体产量?浑浊度 如何测该反应的速率?气泡出现的快慢 (2)讨论下列哪些外界因素对该反应有影响? ①浓度②温度③催化剂 (3)如何通过实验来研究浓度、温度和催化剂对该反应速率的影响?实验比较法 探究浓度对反应速率的影响(室温为20℃) 探究温度对反应速率的影响
实验化学反应速率与活化能
实验 化学反应速率与活化能 一、实验目的 1.了解浓度、温度和催化剂对反应速率的影响。 2.测定过二硫酸铵与碘化钾反应的速率,并计算反应级数、反应速率常数和反应的活化能。 二、实验原理: 在水溶液中过二硫酸铵与碘化钾反应为: (NH 4)2S 2O 8 + 3KI === (NH 4)2SO 4 + K 2SO 4 + KI 3 其离子反应为: S 2O 82- + 3I - === SO 42- + I 3- (1) 反应速率方程为: n I m O S c kc r - - ?=28 2 式中r 是瞬时速率。若-28 2O S c 、- I c 是起始浓度,则r 表示初速率(v 0)。在实验中 只能测定出在一段时间内反应的平均速率。 t c r O S ??-= - 28 2 在此实验中近似地用平均速率代替初速率: t c c kc r O S n I m O S ??-= =- - -28 2 28 20 为了能测出反应在△t 时间内S 2O 82-浓度的改变量,需要在混合(NH 4)2S 2O 8 和KI 溶液的同时,加入一定体积已知浓度的Na 2S 2O 3溶液和淀粉溶液,这样在(1)进行的同时还进行着另一反应: 2S 2O 32- + I 3- === S 4O 62- + 3I - (2) 此反应几乎是瞬间完成,(1)反应比(2)反应慢得多。因此,反应(1)生成的I 3-立即与S 2O 32-反应,生成无色S 4O 62-和I -,而观察不到碘与淀粉呈现的特征蓝
色。当S 2O 32-消耗尽,(2)反应不进行,(1)反应还在进行,则生成的I 3- 遇淀粉呈蓝色。 从反应开始到溶液出现蓝色这一段时间△t 里,S 2O 32- 浓度的改变值为: )O S )O S )O S O S c c c c 始始终(((23 223 223 223 2][----=--=? 再从(1)和(2)反应对比,则得: 2 (23 2 28 2 ) O S O S c c 始--= ? 通过改变S 2O 82- 和I -的初始浓度,测定消耗等量的S 2O 82- 的物质的量浓度- ?28 2O S c 所需的不同时间间隔,即计算出反应物不同初始浓度的初速率,确定出速率方程和反应速率常数。 三、实验步骤 1.浓度对化学反应速率的影响 在室温条件下进行编号Ⅰ的实验。用量筒分别量取 L KI 溶液, LNa2S2O3溶液和 %淀粉溶液,全部注入烧杯中,混合均匀。 然后用另一量筒取 L(NH4)2S2O8溶液,迅速倒入上述混合溶液中,同时开动秒表,并不断搅拌,仔细观察。 当溶液刚出现兰色时,立即按停秒表,记录反应时间和室温。 按下表各溶液用量进行实验。 室温 ℃
化学反应速率的探究实验
《关于化学反应速率的探究实验》 姓名:班级: 【知识准备】 化学反应速率与分子间的有效碰撞频率有关,因此所有能够改变内能、运动速率,以及有效碰撞几率的方法,都可以用来改变、控制反应的速率。影响化学反应速率的外界因素有________________________________ 。 1)压强影响反应速率对反应本身有什么要求? 2)增加接触机会的具体措施有哪些? 【活动探究】 (08广东改)某探究小组用HNO3与大理石反应过程中质量减小的方法,研究影响反应速率的因素。所用HNO3浓度为1.00 mol·L-1、2.00 mol·L-1,大理石有细颗粒与粗颗粒两种规格,实验温度为298 K、308 K,每次实验HNO3的用量为25.0mL、大理石用量为10.00g。请完成以下实验设计表,并在实验目的一栏中填上相应的内容: 【思维深化】 【拓展练习】 某实验小组探究MnO2对双氧水分解制取氧气的速率的影响,设计并进行了5次试验,情况如下:
根据上表,回答以下问题: (1)、实验②和③探究 对反应速率的影响;结论是: ; (2)、实验②和④探究 对反应速率的影响;结论是: ;(3)、表中的实验⑤与实验①作为对比实验,探究温度对化学反应速率的影响,请把它补齐。(温度为50℃) 【能力提升】 在25℃时,取40ml0.001 mol ·L -1的KMnO 4、38 ml 0.1 mol ·L -1 H 2C 2O 4 和 2ml3.68 mol ·L -1的H 2SO 4混合反应液的平均反应速率数据 2KMnO 4+5H 2C 2O 4+3H 2SO 4 = K 2SO 4+2MnSO 4+10CO 2 ↑+8H 2O c-t 图 v-t 图
探究酶促反应速率
揭秘酶促反应速率 班级:高一(7) 组长:陈铭皓 组员:林钦泽、谢浩天、戴嘉文 指导老师:戈云、实验室黄老师 摘要:酶促反应是细胞代谢的基本反应。细胞中几乎所有的代谢反应都在 酶的作用下有条不紊地进行着。那么,酶促反应速率与底物浓度又有什么关系呢? 关键词:酶促反应、速率、底物浓度 一、背景 物质代谢是生命活动的基本特征,也是一切生命活动的基础。酶是由活细胞合成的生物催化剂,生物体内几乎所有的代谢反应都是在酶的作用下有条不紊地完成。酶最重要的特征是具有高效的催化能力,因而酶促反应的速率就代表了酶的活性。 酶的活性与很多因素有关,例如底物浓度、酶的浓度、温度、PH值、抑制剂和激活剂等。在本课题中,我们只研究酶促反应速率与底物浓度的数量关系。 二、实验探究 为了探究酶促反应速率与底物浓度的数量关系,我们在化学实验室进行了一次实验。实验药剂和器材如下: 1.普通漏斗一只; 2.500ml容量瓶一只; 3.5ml、50ml、100ml量筒各一只; 4.水槽一只; 5.胶头滴管一只; 6.分液漏斗与锥形瓶各一只; 7.导管、橡皮塞及秒表; 8.质量分数30%的过氧化氢溶液一瓶; 9.新鲜猪肝100克。 实验过程如下: 1.用新鲜猪肝加水研磨,制成猪肝研磨液; 2.定容,配置500毫升的溶液。 3.取50毫升研磨溶液置于锥形瓶,在分液漏斗中加入0.5毫升过氧化
氢溶液,5秒后将气体通入倒置量筒,排水收集,两秒后读出体积, 重复两次,计算平均值,为15毫升; 4.重取50毫升研磨液,分别加入1毫升、2毫升、3毫升、4毫升、6 毫升、8毫升、12毫升、16毫升、150毫升的过氧化氢,重复步骤 3,得到数据25毫升、40毫升、50毫升、57毫升、68毫升、75 毫升、82毫升、90毫升、112毫升; 5.收拾器具。 三、分析 根据数学线性规划原理,分析图像并推导函数关系式的模型。 1.该图像为双曲线,因此其模型可能为 或
高一:实验 化学反应速率和化学平衡
高中化学新课程标准教材 化学教案( 2019 — 2020学年度第二学期 ) 学校: 年级: 任课教师: 化学教案 / 高中化学 / 高一化学教案 编订:XX文讯教育机构
实验化学反应速率和化学平衡 教材简介:本教材主要用途为通过学习化学知识和做实验,可以让学生培养自己的严谨精神、提高动手能力、合作沟通能力,本教学设计资料适用于高中高一化学科目, 学习后学生能得到全面的发展和提高。本内容是按照教材的内容进行的编写,可以放心修改调整或直接进行教学使用。 [教学目标] 1.知识目标 (1)巩固浓度、温度和催化剂对化学反应速率的影响等基本知识,加深浓度、温度对化学平衡影响等基础知识的理解。 (2)通过实验,体会用定量方法研究化学反应速率、化学平衡规律基本程序,掌握相关的实验操作规范。 (3)掌握“na2s2o3+h2so4=na2so4+s+h2o、fecl3+3kscn fe(scn)3+3kcl”等反应,体会用化学实验研究某个化学反应的一般程序。 2.能力和方法目标 (1)定量实验中数据采集、记录和处理方法。 (2)通过从实验现象、实验数据推测理论规律,提高推理分析能力。 3.情感和价值观目标
本实验中的实验现象生动有趣、实验操作简便、推理和分析过程引人入胜,所以可以通过本实验来提高学生学习化学的兴趣,引发学生探究规律、研究自然现象的乐趣。 [实验内容和实验要点] 本学生实验共包含浓度对化学反应速率的影响、温度对化学反应速率的影响、催化剂对化学反应速率的影响、浓度对化学平衡的影响、温度对化学平衡的影响等5个内容,实验过程中既有定性研究要求、又有定量研究要求,要求学生用定性和定量两方面的综合思维来分析和研究。实验中应要求带着研究的观点、在探究的层面上去思考。本实验的各个内容中所涉及的实验技能、实验注意事项等列表如下: 实验 内容 应巩固的知识 涉及的实验技能 注意事项 浓度对化学反应速率的影响 硫代硫酸钠跟稀硫酸溶液的反应原理、单质硫的颜色、溶解性等。 (1)量筒、烧杯的使用
化学反应速率及其测定
化学反应速率及其测定 一.化学反应速率、 1.表示方法:通常用反应物浓度的或生成物浓度的来表示 2.计算式: 3.单位:一般为或或 4.注意 ①化学反应速率只能用单位时间内的变化来表示 ②化学反应速率指的是一段时间内的,无值 ③同一个化学反应,用不同物质表示化学反应速率时,数值可能不同,但其意义相同。如aA+bB=cC+dD,有如下关系 ④比较同一反应在不同反应条件下的反应速率的大小,要 ⑤不能用或表示化学反应速率,但可以换算 【例】将化合物A的蒸气2mol充入0.5L容器中加热,发生分解反应2A(g)==B(g)+nC(g),反应到3min时,将化合物A的蒸气2mol充入0.5L容器中加热,发生分解反应2A(g)==B(g)+nC(g),反应到3min时容器中S的浓度为1.6mol/L,并测得这段时间内用C的浓度变化表示的平均反应速率为v(C)=1.2mol/(L.min). (1)求化学方程式中的计量数n的值 (2)以B的浓度变化表示该反应的平均速率 二.测量化学反应速率的常见实验方法 1.气体法 见教材P18第二段 2.颜色法 已知YYYY 现利用该反应设计实验,探究“浓度对化学反应速率的影响” #实验操作# ①取两支试管,各加入4mL0.01mol/L的高锰酸钾溶液 ②向其中一支试管加入2mL0.1mol/L的草酸溶液,记录溶液褪色的时间 ③向另外一支试管加入2mL0.2mol/L的草酸溶液,记录溶液褪色的时间 3.沉淀法 #实验操作# ①向两支试管各加入5mL0.1mol/L硫代硫酸钠溶液 ②另取两支试管,各加入5mL0.1mol/L硫酸溶液 ③将四支试管分为两组(各有一支硫酸溶液和硫代硫酸钠溶液),将其中一组试管加入冷水中,另一组试管加入热水中 ④一段时间后,分别混合搅拌。记录出现浑浊时间
化学反应的速率和限度教学设计
《化学反应的速率和限度)教学设计 第一课时 三维目标: 知识与技能: 1.通过实例和实验初步认识化学反应的速率及其影响因素。 2会比较化学反应速率的快慢。 过程与方法: 1.通过实验探究总结化学反应速率的影响因素。 2.增进学生对化学科学的兴趣与情感,体会化学学习的价值。 情感态度与价值观: 1.从学生日常生活中的化学现象和实验中抽象出有关的概念和原理。形成-个由宏观到微观、由感性到理性、由简单到复杂的科学探究过程。 2.培养学生良好的实验习惯,认真的观察能力。 教学重点:化学反应速率概念;了解影响化学反应速率的因素。 教学难点:影响化学反应速率的因素。 教学用具:实验用品 教学方法:图片展示一-实验探究-一小组讨论--归纳总结--习题巩固 教学过程: 新课引入: [投影:图2-17快慢差别很大的化学反应 [思考与交流]:通过投影观察到在我们的生活中,有的反应很快,
有的反应很慢,但许多反应我们希望快,有些反应希望慢,人们希望能控制反应速率的快慢为人类造福。根据投影同学们交流一下在炸药爆炸、金属腐蚀、食物腐败、塑料老化、溶洞形成、石油及煤生成等方面,那一些人们希望快?那一些人们希望慢? [学生活动]: [讲述]:咱们这一节就要讨论人们最关心的化学反应速率的快慢问题。 [板书]:第三节化学反应的速率和极限 一、化学反应的速率 [讲述]:不同的化学反应速率快慢千差万别,快与慢是相对而言,在科学研究中需要一个统一的定量标准来衡量或比较。与物理学中物体的运动快慢用“速度”表示想类似,化学反应的过程进行的快慢用“反应速率”来表示。 [学生活动]:学生认真阅读教材,结合运动速率的理解,自学化学反应速率的知识内容。 [提问]:请-位同学回答一下化学反应速率的定义是什么?葛 [回答]:通常用单位时间里反应物浓度的减少或生成物浓度的增加来表示,用来衡量化学反应进行快慢程度的。 [板书]:1化学反应速率的概念:用单位时间里反应物浓度的减少或生成物浓度的增加来表示。 [提问]:化学反应速率的常用单位有哪些呢? [回答]:由于浓度(物质的量浓度)的单位是mol·L-1,而时间的单位
化学反应速率限度教材分析
《化学反应速率与限度》教材分析 一、单元与课标关系 1.课标里的内容标准:通过实验认识化学反应的速率和化学反应的限度,了解控制反应条件在生产和科学研究中的作用。 2.对本单元的内容分析(明线+暗线) 本单元的主要知识线是由化学反应速率与化学反应限度构成的。 化学反应速率主要内容:定量描述化学反应进行的快慢,反应速率的计算,影响反应速率的因素,应用化学反应速率的知识,解释生活中的相关现象。 化学反应的限度主要内容:认识可逆反应,与化学反应限度的含义,通过反应速率判断化学反应所能达到的限度,初步了解什么是化学平衡。 从课标来看,要学习的内容是相对宏观的。根据对化学课程标准及教材的分析,可以确定本单元教学在知识技能的重点是化学反应速率的原理理解和化学反应限度的涵义,在过程与方法方面的重点是通过实验来认识这两方面的内容在化学研究中的作用,学会在实验当中的观察,归纳总结这两块内容的知识。情感态度价值观的重点是感受控制反应条件在科学研究中的作用。 二、教材单元知识分层建构及衔接 化学反应速率及限度涉及初中,高中必修,选修三个学习阶段的内容: 初中:反应的快慢(冷热),反应条件(燃烧是否完全),量的多少会 对生成物产生一些影响等基础的化学反应。 高中必修:化学反应速率描述化学反应的快慢,反应限度(可逆反应), 化学平衡的初步了解。 高中选修:《化学反应原理》化学平衡的移动,各种因素对化学平衡的 影响,化学反应速率与化学平衡的关系。 这三个学习阶段是呈现螺旋上升的组织特点,三个阶段都是符合中学生的心理发展特点所制定的,所以本单元的知识处于中间地位,起着承上启下的作用,不仅在本书中是学科知识的关键,也是整个化学学习的重要组成部分。 三、教材单元知识结构 本单元在学生接触过大量的化学反应,并且对化学反应有了快与慢的经验的基础上,继续深入对于化学反应快慢的探究,告诉学生可以用定量的方式来描述
化学反应速率及活化能的测定实验报告.
化学反应速率及活化能的测定实验报告 1.概述 化学反应速率用符号J或ξ表示,其定义为: J=dξ/dt(3-1) ξ为反应进度,单位是mol,t为时间,单位是s。所以单位时间的反应进度即为反应速率。 dξ=v-1B dn B(3-2) 将式(3-2)代入式(3-1)得: J=v-1B dn B/dt 式中n B为物质B的物质的量,dn B/dt是物质B的物质的量对时间的变化率,v B为物质B的化学计量数(对反应物v B取负值,产物v B取正值)。 反应速率J总为正值。J的单位是mol·s-1。 根据质量作用定律,若A与B按下式反应: aA+bB→cC+dD 其反应速率方程为: J=kc a(A)c b(B) k为反应速率常数。
a+b=n n为反应级数。n=1称为一级反应,n=2为二级反应,三级反应较少。反应级数有时不能从方程式判定,如: 2HI→I2+H2 看起来是二级反应。实际上是一级反应,因为 HI→H+I(慢) HI+H→H2+I(快) I+I→I2(快) 反应决定于第一步慢反应,是一级反应。从上述可知,反应级数应由实验测定。 反应速率的测定 测定反应速率的方法很多,可直接分析反应物或产物浓度的变化,也可利用反应前后颜色的改变、导电性的变化等来测定,如: 可通过分析溶液中Cl-离子浓度的增加,确定反应速率,也可利用反应物和产物颜色不同,所导致的光学性质的差异进行测定。从上式还可以看到,反应前后离子个数和离子电荷数都有所改变,溶液的导电性有变化,所以也可用导电性的改变测定反应速率。概括地说,任何性质只要它与反应物(或产物)的浓度有函数关系,便可用来测定反应速率。但对于反应速率很快的 本实验测定(NH4)2S2O8(过二硫酸铵)和KI反应的速率是利用一个 在水溶液中,(NH4)2S2O8和KI发生以下反应:
化学反应速率与活化能的测定实验报告
化学反应速率与活化能的测定实验报告 姓名 班级 试验时间 第 室 号位 指导教师 实验目的 1. 了解浓度、温度及催化剂对化学反应速率的影响。 2. 测定(NH 4)2S 2O 8与KI 反应的速率、反应级数、速率系数和反应的活化能。 实验原理 (NH 4)2S 2O 8和KI 在水溶液中发生如下反应: S 2O 82-(aq)+ 3I -(aq) = 2SO 42- (aq)+ I 3-(aq) (1) 这个反应的平均反应速率为 v = - 228(S O ) c t - = 228(S O )(I )kc c αβ-- 式中:v ── 反应的平均反应速率; 228(S O )c - ── t 时间内228S O -的浓度变化; 228(S O )c -,(I )c - ── 228S O -,I -的起始浓度; k ── 该反应的速率系数; ,αβ ──反应物228S O -,I -的反应级数,()αβ+为该反应的总级数。 为了测出在一定时间(t )内S 2O 82-的浓度变化,在混合(NH 4)2S 2O 8和KI 溶液的同时,加入一定体积的已知浓度的Na 2S 2O 3溶液和淀粉,这样在反应(1)进行的同时,还有以下反应发生: 2S 2O 32- (aq) + I 3-(aq) ══ S 4O 62-(aq) + 3I -(aq) (2) 由于反应(2)的速率比反应(1)的大得多,由反应(1)生成的I 3-会立即与S 2O 32-反应生成无色的S 4O 62-和I -。这就是说,在反应开始的一段时间内,溶液呈无色,但当Na 2S 2O 3一旦耗尽,由反应(1)生成的微量I 3-就会立即与淀粉作用,使溶液呈蓝色。 由反应(1)和(2)的关系可以看出,每消耗1mol S 2O 82- 就要消耗2 mol 的S 2O 32-,即 c (S 2O 82-)= 12 c (S 2O 32-) 由于在t 时间内,S 2O 32-已全部耗尽,所以c (S 2O 32-)实际上就是反应开始时Na 2S 2O 3的浓度,即 -c (S 2O 32-)= 0c (S 2O 32-) 这里的0c (S 2O 32-)为Na 2S 2O 3的起始浓度。在本实验中,由于每份混合液中Na 2S 2O 3的起始浓度都相同,因而c (S 2O 32-)也是相同的,这样,只要记下从反应开始到出现蓝色所需要的时间(t ),就可以算出一定温度下该反应的平均反应速率: v =228() c S O t - - =()2232c S O t -- = ()02232c S O t - 按照初始速率法,从不同浓度下测得的反应速率,即可求出该反应的反应级数α和β,进而求得
大学实验化学 化学反应速率
大学实验化学 化学反应速率 难题解析 例7-1 HNO 2分解反应机理如下,求总反应的速率方程表示式。 分析 复合反应的每一步都是元反应,反应的速率方程由速率控制步骤决定。 解 )2 (HNO O)2(H )2(NO (NO)21c c c c k = , )2(NO )4O 2(N 22c c k = =)O 2 H ()NO ()2HNO ()NO ()2HNO (212123c c c k c c k k k ? v =)O 2 H ()NO ()2HNO (222123c c c k k k 例 7-2 证明一级反应完成99.9%所需要的时间近似为半衰期的10倍。 解 t 1/2 = 0.693/ k 例 7-3 根据如下的气相反应相关数据 T (K) 600 645 k (L 2·mol -2m·in -1) 6.62? 105 6.81? 105 k’ (L·mol -1·min -1) 8.40 40.8 求:(1)两个温度下的平衡常数。 (2)正向反应和逆向反应的活化能。 解 (1)600K 时,45 1088.740.81062.6'?=?==k k K 640K 时,45 1067.18 .401081.6'?=?==k k K (2)正反应的活化 1 21221ln )(k k T T T RT E a -= = 5 1062.65 1081.6ln K )600645(K 645K 600K mol J 314.811??-????-- =2.02 kJ ·mol -1 逆反应的活化能 1 22112'''ln )(k k T T T T R E a -= =40 .88.40ln K )600645(K 645K 600K mol J 314.811-????--=113.0 kJ ·mol -1
《化学反应速率影响因素的探究》教学设计
化学反应速率影响因素的探究 陈波芜湖市第十二中学 【教学设计构架】 在开始本课题教学设计之初,首先对教学设计的各环节予以统筹考虑,初步搭建与整合教学设计架构,使之保证后续教学设计各环节的合理性、针对性和有效性。如图所示本课题的教学设计将按照以下关系展开。 本课题教学设计架构的突出点在于:在研读课标和教材的基础上,对教科书中关于影响化学反应速率因素的定性探究实验进行重构,在探究验证知识结论的同时渗透科学研究方法的教育。本课题着眼于探究过程中“方案设计”能力的培养,着重以“方案设计”中“控制变量”和“寻找标记”两个要点为突破口,力图在学习知识的同时形成科学探究方案的设计能力,让学生多角度、深层次地体验科学研究的过程与方法,从而达成课标的有关要求。 一、课标与教材分析 《普通高中化学课程标准》(简称“课标”)在课程目标中提出:“理解基本的化学概念和原理,认识化学现象的本质,学习实验研究的方法,学习科学探究的基本方法,提高科学探究能力”。联系本课题的内容,课标具体指出的内容标准有:“体会定量研究的方法对研究和学习化学的重要作用;初步认识实验方案的
设计、实验条件控制、数据处理等方法在化学学习和科学研究中的应用;通过实验认识化学反应的速率,了解控制反应条件在生产和科学研究中的作用”。 本课题位于人教版必修2第二章第三节,其知识属于化学反应原理范畴,是化学学科的重要的原理性知识之一,也是深入认识和理解化学反应特点和进程的入门性知识。同时,本课题的知识在生活生产与科学研究中有广泛的应用,对人类文明进步和现代化发展有重大价值。因此,教学中不但要注意进行概念和原理的教学,还应注重本课题知识与生产生活的联系,从学科中心回归到学生的生活经验,从社会实际问题出发组织教学。 二、学情分析 从本学科纵向维度上看,学生学习本课题时,已经经过必修1的学习,掌握了各种化学反应(尤其是氧化还原反应)的原理,也学习了各种金属与非金属元素的化合物知识。同时,在必修2第一章已经从元素周期律和化学键的角度系统学习了有关化学反应和元素性质的知识。可以这样说,此时的学生已经掌握了较多的化学反应,对于化学反应的本质有了较深刻地理解,并初步系统地建立起了对各元素性质的基本认知。这一方面为本课题学习的内容提供了丰富的教学分析案例,为探究实验的顺利进行提供了知识基础的保证,另一方面也便于教学中从元素性质的角度帮助学生分析内因是影响化学反应速率的主要因素。 从新课程理念角度考虑,怎样在掌握学习内容的同时培养学生的学习兴趣,发展科学探究能力与解决问题的能力是关键点。因此,采用“碘钟实验的探究”一方面将提升学生化学学习的兴趣,另一方面培养科学探究能力和方法。 三、确定教学目标 综上分析所述,结合课标的三维目标要求,确定本课题的教学目标如下。知识与技能: 1. 知道温度是影响化学反应速率的外界因素及其影响效果。 2. 知道浓度是影响化学反应速率的外界因素及其影响效果。 过程与方法: 1. 渗透观察和描述实验现象能力、实验现象分析、推理和判断的能力培养。 2. 体验科学探究过程,学习科学探究方法。 3. 以“探究方案的设计”为突破点培养科学探究能力。 情感态度与价值观: 1. 关注社会生产生活中有关化学反应速率的实例,在此基础上说出化学反应速率对人类的利弊。
酶促反应动力学实验
酶促反应动力学实验
————————————————————————————————作者: ————————————————————————————————日期:
酶动力学综合实验 实验(一)——碱性磷酸酶Km值的测定 【目的要求】 1.了解底物浓度对酶促反应速度的影响 2.了解米氏方程、Km值的物理意义及双倒数作图求Km值的方法。 【实验原理】 1、碱性磷酸酶: 碱性磷酸酶是广泛分布于人体各脏器器官中,其中以肝脏为最多。其次为肾脏、骨骼、肠和胎盘等组织。但它不是单一的酶,而是一组同功酶。本实验用的碱性磷酸酶是从大肠杆菌中提取的。 2、米氏方程: Michaelis-Menten在研究底物浓度与酶促反应速度的定量关系时,导出了酶促反应动力学的基本公式,即: (1) 式中:v表示酶促反应速度, 表示酶促反应最大速度, [S]表示底物浓度, 表示米氏常数。 3、值的测定主要采用图解法,有以下四种: ①双曲线作图法(图1-1,a) 根据公式(1),以v对[s]作图,此时1/2时的底物浓度[s]值即为Km值,以克分子浓度(M)表示。这种方法实际上很少采用,因为在实验条件下的底物浓度很难使酶达到饱和。实测一个近似值,因而1/2不精确。此外由于v对[S]的关系呈双曲线,实验数据要求较多,且不易绘制。 ②Lineweaver- Burk作图法双倒数作图法(图1-1,b) 实际工作中,常将米氏方程(式(1))作数学变换,使之成为直线形式,测定要方便、精确得多。其中之一即取(1)式的倒数,变换为Lineweaver- Burk方程式: (2)
以对作图,即为y=ax+b形式。此时斜率为,纵截距为。把直线外推与横轴相交,其截距相交,其截距即为—。 ③Hofstee作图法(略) 把(2)式等号两边乘以,得: (3) 以v对作图,这时斜率为,纵截距为,横截距为。 ④Hanas作图法(略) 把(2)式等号两边乘以[S],得: (4) 以对[s]作图,这时斜率为,纵截距为。 (a)(b) 本实验主要以双倒数法,即Lineweaver-Burk作图法来测定碱性磷酸酶Km值。具体原理如下: 本实验以碱性磷酸酶为例,用磷酸苯二钠为其作用物,碱性磷酸酶能分解磷酸苯二钠产生酚和磷酸,在适宜条件下(PH10.0,和60℃),准确反应13分钟。在碱性条件下酚可与酚试剂生成蓝色化合物,以波长620nm比色。在一定条件下色泽深浅与光密度成正比。反应式如下:
化学反应速率探究题专项练习
“化学反应速率”探究题专项练习 1.(2013安徽题)“五一”假期,小兵对“锌与硫酸反应快慢的影响因素”进行了探究。 【提出问题】锌与硫酸反应的快慢受哪些因素的影响呢? 【猜想与假设】a.可能与硫酸的质量分数有关;b.可能与锌的形状有关。 【设计并实验】小兵用不同质量分数的硫酸和不同形状的锌进行如下实验。 硫酸的质量分数(均 (1)写出稀硫酸与锌反应的化学方程式______________________________________。 (2)小兵用右图装置收集并测量氢气的体积,其中量筒的作 用是____________________,氢气应从________(填e或f 或g)管通入。 【收集证据】(3)要比较不同质量分数的硫酸对反应快慢的影 响,应选择的实验编号是____________。 【得出结论】(4)结论是________________________________ _____________________________________________________。 【评价与反思】(注意:若答对(5)(6)两小题奖励4分,化学试卷总分不超过60分) (5)下表是小兵第①组实验的详细数据。 _______________________________________________________。 (6)锌与硫酸反应的快慢可能还受哪些因素影响?设计实验验证。___________________ _________________________________________________________________ 2.(2012安徽题)实验室常用加热氯酸钾与二氧化锰混合物的方法制取氧气,写出反应的化学方程式:______________________________________ 小芳发现,氯酸钾与氧化铜混合加热,也能较快产生氧气,于是进行如下探究: 【提出猜想】除Mn02、CuO外,Fe203也可以作KCl03分解的催化剂。 【完成实验】按下表进行实验:并测定分解温度(分解温度越低,催化效果越好)。 (2)实验所用的三种金属氧化物,催化效果最好的是_____________________。 【反思】(1)若要证明Fe203是该反应的催化剂,还要验证它在化学反应前的质量和______ ____不变; (2)同种催化剂,颗粒大小可能影响催化效果,请设计实验方案进行验证_____ (3)同种催化剂,还有哪些因素可能影响催化效果,请你再探究 (探究一种因素即可)。.
