精馏1传质过程概述1传质过程的定义传质过程的定义

第六章 精馏
§1 传质过程概述 6-1 传质过程的定义
传质过程的定义——物质以扩散的方式,从一相转移到另一相的相界面的转移过程,称为物质的传递过程,简称传质过程。
日常生活中的冰糖溶解于水,樟脑丸挥发到空气中,都有相界面上物质的转移过程。
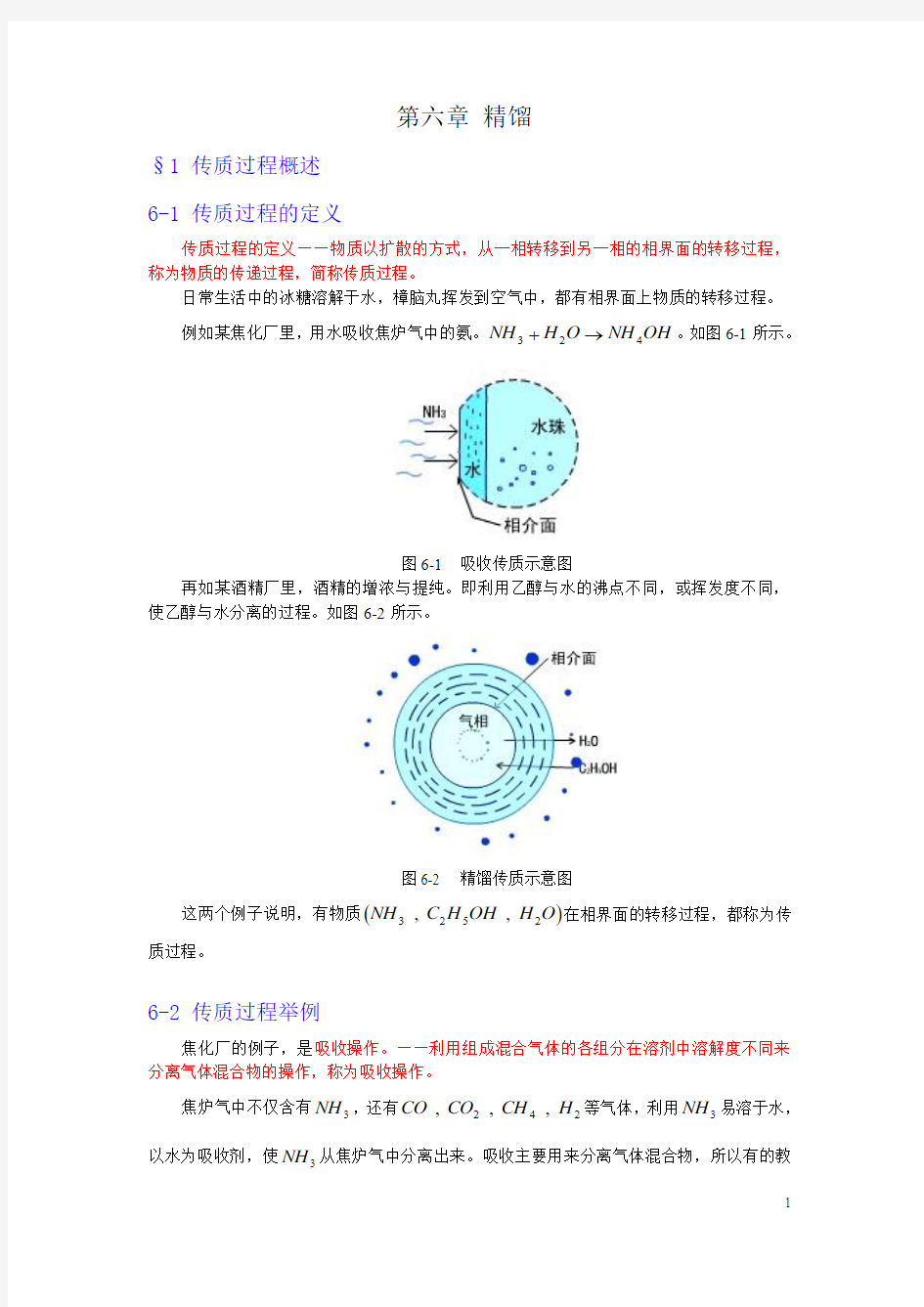
例如某焦化厂里,用水吸收焦炉气中的氨。OH NH O H NH 423→+。如图6-1所示。
图6-1 吸收传质示意图
再如某酒精厂里,酒精的增浓与提纯。即利用乙醇与水的沸点不同,或挥发度不同,使乙醇与水分离的过程。如图6-2所示。
图6-2 精馏传质示意图
这两个例子说明,有物质()O H OH H C NH 2523 , , 在相界面的转移过程,都称为传质过程。
6-2 传质过程举例
焦化厂的例子,是吸收操作。——利用组成混合气体的各组分在溶剂中溶解度不同来分离气体混合物的操作,称为吸收操作。
焦炉气中不仅含有3NH ,还有242 , , , H CH CO CO 等气体,利用3NH 易溶于水,以水为吸收剂,使3NH 从焦炉气中分离出来。吸收主要用来分离气体混合物,所以有的教
材称吸收为气体吸收。如图6-3所示。
图6-3 吸收局部示意图
水称为溶剂,3NH 称为溶质,炉气中其他气体称为惰性组分。 用水吸收氯化氢气体)(HCl ,制备盐酸,也是一种吸收操作。
酒精厂的例子,是精馏操作。——利用液体混合物各组分沸点(或挥发度)的不同,将物质多次部分汽化与部分冷凝,从而使液体混合物分离与提纯的过程,称为精馏操作。
精馏主要用来分离液体混合物,所以有的教材称精馏为液体精馏。 传质过程还有,
萃取——利用混合物各组分对某溶剂具有不同的溶解度,从而使混合物各组分得到分离与提纯的操作过程。
例如用醋酸乙酯萃取醋酸水溶液中的醋酸。如图6-4所示。
图6-4 萃取示意图
此例中醋酸乙酯称为萃取剂)(S ,醋酸称为溶质)(A ,水称为稀释剂)(B 。萃取操作能够进行的必要条件是:溶质在萃取剂中有较大的溶解度,萃取剂与稀释剂要有密度差。
干燥操作——利用热能使湿物料的湿分汽化,水汽或蒸汽经气流带走,从而获得固体产品的操作。如图6-5所示。
图6-5 干燥传质示意图
还有固—液萃取,结晶,吸附等操作。
要研究传质过程,主要从三个方面进行研究。相平衡关系(气-液溶解度,液-液溶解度,干燥中的水蒸气分压),物料衡算关系和传质速率关系。
浓度表示法及其换算:重量百分率(质量分率)
的摩尔数
的摩尔数
摩尔比分率的摩尔数
的摩尔数的摩尔数
摩尔分率
)质量百分率(质量分率B A X B A A x kg
m m kg m W A A B A A A =
+=
+=
()()A
A A A
A A B
A A A
A
A A
B A A A A
A A X X x x x X M W M W M W x M x M x M x W +=
-=-+=
-+=1111
§2 理想溶液的汽-液平衡 6-3 由制酒作坊引出相平衡
大庆油田开采出来的是原油,如何将原油加工成汽油、煤油、柴油、重油呢?酿酒厂酿制出了原酒,如何将粗酒加工成?60的白酒呢?
先介绍以下古老的烧酒作坊吧!目前江浙一带仍有这种家庭小作坊,主要分三步: (1) 粬的制作——发酵过程(获得菌种)
(2) 粗酒的制作——将酒粬与蒸熟的米饭,按一定比例混合发酵,制成酒、水、酒
糟的糊状混和物(生物降解)。
(3) 酒的提纯——蒸馏操作过程。
图6-6 制酒作坊装置图
锅为汽化器,顶盖为冷凝器。如图6-6所示。
这就是一种简单蒸馏的操作过程。我还不知道“对酒当歌”源于哪个朝代的帝王将相,但可以肯定,从“对酒当歌”那个时候起,劳动人民已经掌握了简单精馏这种操作过程。
为什么能使乙醇增浓呢?主要因为乙醇比水的沸点低(或说乙醇比水的挥发度高)。这样蒸汽中乙醇的含量()A y 高于粗酒中乙醇的含量()A x ,即A A x y >。蒸汽冷凝之后,就得到乙醇含量高的酒。
()A y ——蒸汽中乙醇所占的摩尔分率
=
A y 水的摩尔数
乙醇的摩尔数乙醇的摩尔数
+
()A x ——液相中乙醇所占的摩尔分率
本章中,y 均代表蒸汽的组成(摩尔分率),x 均代表液体的组成(摩尔分率)
我们要问,()A y 与()A x 服从什么规律呢?即()A x f y =的函数关系如何呢?本节就要回答这个问题。
6-4 理想溶液及拉乌尔定律
图6-7 拉乌尔定律示意图
()
A B
B B
B A
A A x p x p p x p p -===100
如图6-7所示,在一定的温度下,溶液上方任意组分的蒸汽分压,等于该纯组分在同温度下的蒸汽压与该组分在溶液中的摩尔分率之乘积。——拉乌尔定律。
()
o
B
o A p p 的意思是()11==B A x x 时的蒸汽分压。 道尔顿分压定律的表达式为:
P y p P y p B B A A ?=?= ,
6-5 y x t --图
在一定外压条件下()P ,沸点t 与汽液相组成),(y x 的关系,绘在图上即是y x t --图。
图6-8 温度-组成图
如图6-8所示,对于一定组成的溶液)(1x 加热到与x t -相交的点,即出现第一个气泡,所以x t -线亦称泡点线。
对于组成为1y 的蒸汽,冷却至与y t -线相交,出现第一个露珠,所以称y t -线为露点线。
若x t -线与y t -线重合,则表示该溶液不能分离。若两线相距愈远,则表示愈易分离。 y x t --图可通过实验测定。
若为二元理想溶液,t-x-y 图可利用计算方法求得:
A o A A x p p = ()A o
B B o B B x p x p p -==1 ()A o
B A o A B A x p x p P p p -+==+1 ?
?
?
?
???==--=∴P x p P p y p p p P x A o
A A A o
B
o
A o
B
A …………)(I 式)(I 说明,只要知道某温度下的o
B o A p p 和(饱和蒸汽压数据)
,就可以计算得到x 与y ,
就可以作出在指定外压()P 下的y x t --图。式)(I 还说明,总压P 对y x t --图是有影响的。
6-6 x-y 图
取y x t --图中的y x ,数据,以x 为横坐标,y 为纵坐标,绘成的图为y x -图。 如图6-9所示,用一条曲线表达汽-液相平衡,图面清晰,数据易查。
图6-9 x-y 图
对于易挥发组分,因为A A x y >,所以y x -线均在对角线上方。
y x -线与对角线偏离越远,表示越易分离。若y x -线与对角线重合,则不能用精馏
方法分离。
对于二元理想溶液,y x -图可由式)(I 计算得到。
6-7 汽-液平衡解析表达式
用图表达汽-液相平衡关系,利用计算机计算就十分不便,能不能用一解析式来表达呢? 挥发度——达到相平衡时,某组分在蒸汽中的分压()A p 和它在平衡液相中的摩尔分率
()A x 之比,叫做该组分的“挥发度”。
B
B
B A
A
A x p v x p v =
=
,
相对挥发度——各组分的挥发度之比,称为组分间的“相对挥发度”。
o
B
o A
B B o B A A o A B B A A AB B A AB
p p x x p x x p x p x p v v =??===αα , 在本课程中,通常定义易挥发组分挥发度与难挥发组分挥发度之比为相对挥发度。这样
定义的α,则1>α。
对于二元理想溶液
()()A A o B
o
A
A o B
o A
A o
B A o A A
o
A B A A A x x p p x p p x p x p x p p p p y -+=-+=+=11 ()
A A A
x x x -+=
1αα
∴() 11A
A
A x x y -+=
αα ……………)(II
式)(II 为汽-液平衡的解析表达式。
由式)(II 得知,当1=α时,A A x y =,则表示该二元溶液不能用精馏的方法分离。 注意:以后所见的y x ,均为易挥发组分浓度,就是表示A A y x , 的意思。
6-8 相平衡计算举例
【例6-1】正庚烷和正辛烷的饱和蒸汽压和温度的关系数据如下表所示。试求出该体系
157.26
949.126
===∑α
§3 简单蒸馏及其计算
传质分离过程
传质分离过程 1.分离过程可以定义为借助于物理、化学、电学推动力实现从混合物中选择性的分离某 些成分的过程。 2.分离过程可分为机械分离和传质分离两大类。机械分离的对象是两相以上的混合物。 传质分离过程用于各种均相混合物的分离。特点是有能量传递现象发生。 3.传质分离过程分为平衡分离过程和速率分离过程。 4.相平衡的准则为各相的温度、压力相同,各组分的逸度也相等。 5.相平衡的表示方法有相图、相平衡常数、分离因子。 6.维里方程用来计算气相逸度系数。 7.闪蒸是连续单级蒸馏过程。 8.指定浓度的组分成为关键组分,其中易挥发的成为轻关键组分,难挥发的成为重关键 组分。 9.若溜出液中除了重关键组分外没有其他重组分,而釜液重除了轻关键组分外没有其他 轻组分,这种情况称为清晰分割。 10.多组分精馏与二组分精馏在浓度分布上的区别可以归纳为:在多组分精馏中,关键组 分的浓度分布有极大值;非关键组分通常是非分配的,即重组分通常仅出现在釜液中,轻组分仅出现在溜出液中;重、轻非关键组分分别在进料板下、上形成接近恒浓的区域;全部组分均存在于进料板上,但进料板浓度不等于进料浓度。塔内各组分的浓度分布曲线在进料板处是不连续的。 11.最小回流比是在无穷多塔板数的条件下达到关键组分预期分离所需要的回流比。 12.特殊精馏分为萃取精馏(加入的组分称为溶剂)、共沸精馏、加盐精馏。 13.气体吸收是气体混合物一种或多种溶质组分从气相转移到液相的过程。解吸为吸收的 逆过程,即溶质从液相中分离出来转移到气相的过程。 14.吸收过程按溶质数可以分为单组分吸收和多组分吸收;按溶质与液体之间的作用性质 可以分为物理吸收和化学吸收;按吸收温度状况可以分为等温吸收和非等温吸收。 15.吸收的推动力是气相中溶质的实际分压与溶液中溶质的平衡蒸气压力之差。 16.难溶组分即轻组分一般只在靠近塔顶的几级被吸收,而在其余级上变化很小。易溶组 分即重组分主要在塔底附近的若干级上被吸收,而关键组分才在全塔范围内被吸收。 17.吸收塔的操作压力、操作温度和液气比是影响吸收过程的主要参数。操作压力越大吸 收率越大,操作温度越低吸收率越大。液气比越大吸收率越大。 18.超临界流体萃取是一种以超临界流体作为萃取剂,从固体或液体中提取出待分离的高 沸点或热敏性物质的新型萃取技术。超临界流体是状态处于高于临界温度、压力条件下的流体,它具有低粘度、高密度、扩散系数大、超强的溶解能力等特性。与传统的溶液萃取的优势:超临界流体具有极强的溶解能力,能实现从固体中提取有效成分; 可通过温度、压力的调节改变超临界流体的溶解能力的大小,因而超临界流体萃取具有较好的选择性;超临界流体传质系数大,可大大缩短分离时间;萃取剂的分离回收容易。 19.二氧化碳是最理想的超临界流体。 20.超临界流体的典型萃取流程:等温法、等压法、吸附法。 21.反胶团萃取有效的解决了溶剂萃取过程中蛋白质不溶于有机溶剂和易变性、失活的问 题。 22.吸附是指流体与固体多孔物质接触时,流体中的一种或多种组分传递并附着在固体 内、外表面形成单分子层或多分子层的过程。
过程控制作业答案
第一章 概述 1.1 过程控制系统由哪些基本单元构成?画出其基本框图。 控制器、执行机构、被控过程、检测与传动装置、报警,保护,连锁等部件 1.2 按设定值的不同情况,自动控制系统有哪三类? 定值控制系统、随机控制系统、程序控制系统 1.3 简述控制系统的过渡过程单项品质指标,它们分别表征过程控制系统的什么性能? a.衰减比和衰减率:稳定性指标; b.最大动态偏差和超调量:动态准确性指标; c.余差:稳态准确性指标; d.调节时间和振荡频率:反应控制快速性指标。 第二章 过程控制系统建模方法 习题2.10 某水槽如图所示。其中F 为槽的截面积,R1,R2和R3均为线性水阻,Q1为流入量,Q2和Q3为流出量。要求: (1) 写出以水位H 为输出量,Q1为输入量的对象动态方程; (2) 写出对象的传递函数G(s),并指出其增益K 和时间常数T 的数值。 (1)物料平衡方程为123d ()d H Q Q Q F t -+= 增量关系式为 123d d H Q Q Q F t ??-?-?= 而22h Q R ??= , 33 h Q R ??=, 代入增量关系式,则有23123 ()d d R R h h F Q t R R +??+=? (2)两边拉氏变换有: 23 123 ()()()R R FsH s H s Q s R R ++ =
故传函为: 23232 3123 ()()()11R R R R H s K G s R R Q s Ts F s R R +=== +++ K=2323 R R R R +, T=23 23R R F R R + 第三章 过程控制系统设计 1. 有一蒸汽加热设备利用蒸汽将物料加热,并用搅拌器不停地搅拌物料,到物料达到所需温度后排出。试问: (1) 影响物料出口温度的主要因素有哪些? (2) 如果要设计一温度控制系统,你认为被控变量与操纵变量应选谁?为什么? (3) 如果物料在温度过低时会凝结,据此情况应如何选择控制阀的开、闭形式及控制器 的正反作用? 解:(1)物料进料量,搅拌器的搅拌速度,蒸汽流量 (2)被控变量:物料出口温度。因为其直观易控制,是加热系统的控制目标。 操作变量:蒸汽流量。因为其容易通过控制阀开闭进行调整,变化范围较大且对被 控变量有主要影响。 (3)由于温度低物料凝结所以要保持控制阀的常开状态,所以控制阀选择气关式。控制 器选择正作用。 2. 如下图所示为一锅炉锅筒液位控制系统,要求锅炉不能烧干。试画出该系统的框图,判断控制阀的气开、气关型式,确定控制器的正、反作用,并简述当加热室温度升高导致蒸汽蒸发量增加时,该控制系统是如何克服干扰的? 解:系统框图如下:
07传质与分离工程期末考试题(含答案)
,考试作弊将带来严重后果! 华南理工大学期末考试 2007《传质与分离工程英文》试卷A (含答案) 1. 考前请将密封线内填写清楚; 所有答案请直接答在试卷上(或答题纸上); .考试形式:开(闭)卷; S in the air is absorbed by NaOH solution is ( A ). 2 B. liquid film “controls”; C. two film “controls”. AB=1. When C ). >x A; B. y A
传质过程
长沙学院教案(课时备课) 授课日期2007年10月10日第15次课 2 学时
第四章传质过程 §1传质分离过程概述 传质过程 在含有两个或两个以上组分的混合体系中,由于存在浓度差,某一或某些组分由高浓度区向低浓度区的传递过程,称为传质过程。 传质过程可以在一相中进行,也可以在两相间进行,两相间的传质是分离过程的基础。 1-1分离操作在化工生产中的作用 1.作用:分离设备费用和分离操作费用占总生产费的比例很大。 2.分类: ①机械分离:过滤、沉降 ②传质分离: 两相间:利用混合物中各组分在两相中的溶解度或挥发性等物理性质的差异,使某一或某些组分在相间转移(如吸收、精馏、萃取)。 一相中:热扩散、膜分离。 1-2化工生产中常见的传质操作 1.蒸馏:分离液体混合物,利用各组分挥发性的差异 2.吸收与解吸:分离气体混合物,利用气体溶解度的差异 3.液-液萃取:分离液体混合物,利用各组分溶解度的差异 4.吸附:分离气体或液体混合物,利用各组分在固体上吸附程度的差异5.干燥:固、气分离 6.膜分离:分离气体或液体混合物 7.热扩散:由于温度梯度而引起的物质扩散。
§2 传 质 过 程 机 理 传质过程: ①扩散物质从一相主体向界面传递 ②扩散物质在界面上从一相进入另一相 ③扩散物质从界面向另一相传递 2-1单相中的传质 一.分子扩散与菲克定律 1.分子扩散 在一相内有浓度差异存在时,由于分子的热运动,而造成的物质传递现象。 分子扩散速率(通量)A,0N :单位时间内通过单位截面积而扩散的物质量。 2.费克(Fick )定律(只适用于双组分混合物) =-A A,0AB dc N D dl (因A dc dl 为负值,加“-”使A,0N 为正) A,0N ——组分A 的分子扩散速率,)/(2s m kmol ?; A dc dl ——组分A 在扩散方向的浓度梯度,4/m kmol ; AB D ——组分A 在组分B 中的分子扩散系数,s m /2。 AB D 的值由试验测定,可通过手册查取,见教材P183表5-2,5-3。 对理想气体混合物,由于RT p c A A =,故有=-AB A A,0D dp N RT dl 。
传质过程
第八章 传质过程导论 1.含有4CCl 蒸汽的空气,由101.3kPa(绝)、293K 压缩到l013kPa(绝)后,进行冷却冷凝,测出313K 下开始有4CCl 冷凝,混合气出冷凝器时的温度为300K 求: (l)压缩前、压缩后开始冷凝前与出冷凝器时,4CCl 蒸汽的质量分率、质量比和摩尔浓度。 (2)出冷凝器时4CCl 蒸汽冷凝的百分率。 注:a 解:(1)l013kPa(绝),313K 下开始有4CCl 冷凝,则 0276.01013 3 .101760210 =?=y 压缩前: 131.029)0276.01(1540276.0154 0276.0=?-+??= a 15.029)0276.01(1540276.0=?-?=a 33/1015.1293314.83.1010276.0m kmol RT yp C -?=??== 压缩后开始冷凝前 131.0=a 15.0=a 32/1007.1313 314.810130276.0m kmol RT yp C -?=??== 出冷凝器时 0162.01013 3 .101760123 '=?=y
080.029)0162.01(1540162.0154 0162.0'=?-+??= a 087.029)0162.01(1540162.0'=?-?=a 33/1058.6300314.810130162.0m kmol RT yp C -?=??== (2)%42%10015.0087.015.0%100'=?-=?-a a a 解:由公式 10064+=a a x 和总 p p y i =可算得x 、y 数据入下表所示: 3.试用Fuller 等人的方法分别估算20℃、101.3kPa 下氨和二氯化硫在空气中的扩散系数D ,并将结果和表8-2中能查到的数据进行核对。 解:∑∑++?= -2 3/13 /12 /175.17] )()[()11( 1000.13B A B A NH p M M T D υυ
贾绍义《化工传质与分离过程》(第2版)配套题库-模拟试题【圣才出品】
第三部分模拟试题 贾绍义《化工传质与分离过程》(第2版)配套模拟试题及详解(一) 一、选择题(每题3分,共15分) 1.利用气体混合物各组分在液体中溶解度的差异而使气体中不同组分分离的操作称为()。 A.蒸馏 B.萃取 C.吸收 D.解吸 【答案】C 2.操作中的精馏塔,若维持及进料位置不变,而减小,则有()。 A.D增大,R减小 B.D不变,R增加 C.D减小,R增加 D.D减小,R不变 【答案】C 【解析】精馏段板数不变,所以当x F减小时,为维持x D不变,必须加大回流比,以提高精馏段塔板的分离能力。 又因不变,q、F不变,故随着R增加,D必减小。
3.若萃取相和萃余相在脱除溶剂后均与原料液的组成相同,则所用萃取剂的选择性系数()。 A.小于1 B.大于1 C.不确定 D.等于1 【答案】D 4.在恒定干燥条件下,将含水20%的湿物料进行干燥,开始时干燥速率恒定,当干燥至含水量为5%时,干燥速率开始下降,再继续干燥至物料恒重,并测得此时物料含水量为0.05%,则物料的临界含水量为()。 A.5% B.20% C.0.05% D.4.55% 【答案】A 5.间歇干燥过程将某湿物料由含水量0.25kg水/kg绝干物料降至0.05kg水/kg绝于物料,测出物料的平衡含水量为0.007kg水/kg绝于物料,物料的平衡分压保持 的最小含水量X=0.2kg水/kg绝干物料,干燥过程的临界含水量为kg水/kg 绝干物料,则降速阶段除去的结合水量为()。
A.0.2kg水/kg绝干物料 B.0.15kg水/kg绝干物料 C.0.16kg水/kg绝干物料 D.0.01kg水/kg绝干物料 【答案】B 二、填空题(每题4分,共20分) 1.在吸收操作过程中,保持气、液相流量、气相进口组成不变,若液相进口浓度降低,则塔内平均传质推动力将______,气相出口浓度将______。 【答案】增大;减小 2.在低浓度难溶气体的逆流吸收塔中,若其他条件不变而入塔液体量增加,则此塔的 液相传质单元数N OL将______,而气相总传质单元数N OG将______,气体出口浓度将______。 【答案】减少;不变;降低 3.对填料塔气膜控制的逆流吸收过程,如其他操作条件不变,将气液流量同比例减小,则气体出塔组成y2将______,液体出塔组成x1将______。 【答案】不变;不变 4.设计连续精馏塔时,欲保持馏出液组成x D和易挥发组分的回收率不变,试定性判断
热工过程控制系统
热工过程控制系统 第一章 过程控制系统概述 1.1过程控制定义及认识 1.2过程控制目的 *1.3过程控制系统的组成 1.4过程控制系统的特点 *1.5过程控制系统的分类 *1.6过程控制性能指标 1.7 过程控制仪表的发展 1.8 过程控制的地位 1.9 过程控制的任务 1.1过程控制定义及认识 过程控制定义 所谓过程控制(Process Control )是指根据工业生产过程的特点,采用测量仪表、执行机构和计算机等自动化工具,应用控制理论,设计工业生产过程控制系统,实现工业生产过程自动化。 1.3 过程控制系统组成 被控过程(Process ), 指运行中的多种多样的工艺生产设备; 过程检测控制仪表(Instrumentation ), 包括: 测量变送元件(Measurement ); 控制器(Controller ); 执行机构(Control Element ); 显示记录仪表 1.5 过程控制系统的分类 按系统的结构特点来分::反馈控制系统,前馈控制系统,复合控制系统(前馈-反馈控制系统) 按给定值信号的特点来分: 定值控制系统,随动控制系统,程序控制系统 性能指标: 对自动控制系统性能指标的要求主要是稳、快、准。 最大超调量σ%反映系统的相对稳定性,稳态误差ess 反映系统的准确性,调整时间ts 反映系统的快速性。 第三章 过程执行器 主要内容 执行器 电动执行器 气动执行器 调节阀及其流量特性 变频器原理及应用 本节内容在本课程中的地位 执行器用于控制流入 或流出被控过程的物 料或能量,从而实现 对过程参数的自动控 制。 3.1 调节阀(调节机构)结构 调节阀是一个局部阻力可以改变的节流元件。由于阀芯在阀体内移动,改变了阀芯与阀座之 间的流通面积,即改变了阀的阻力系数,被调介质的流量也就相应地改变,从而达到调节工艺参数的目的。 3.1 调节阀 功能:接受控制器输出的控制信号,转换成直线位移或角位移,来改变调节阀的流通截面积。 3.1.1 调节阀的组成 要求观察 思考调节变换 显示记录调节给定值执行机构检测 仪表记录仪显示器调节器控制器测量变送被控过程 执行器r(t)e(t)u(t)q(t)f(t)y(t)z(t)-控制器 测量变送 被控过程 执行器 r ( t ) e ( t ) u ( t ) q ( t ) f ( t ) y ( t ) z ( t ) -
传质分离过程习题答案
第二章习题 1. 计算在和下苯(1)-甲苯(2)-对二甲苯(3)三元系,当x 1 = 、x 2 =、x 3 =时的K 值。汽相为理想气体,液相为非理想溶液。并与完全理想系的 K 值比较。已知三个二元系的wilson 方程参数(单位: J/mol ): λ12-λ11=-; λ12-λ22= λ23-λ22=; λ23-λ33=- λ13-λ11=; λ13-λ33=- 在T = K 时液相摩尔体积(m 3 /kmol )为: =×10 -3 ; =×10 -3 ; =×10 -3 安托尼公式为(p s :Pa ; T :K ): 苯:1n =(); 甲苯:1n =(); 对 -二甲苯:1n = (); 解: 由Wilson 方程得: Λ12=l l V V 12exp[-(λ12-λ11)/RT] =3 3 1091.1001055.177??×exp[-/×]= Λ21= Λ13= Λ31= Λ23= Λ32= ln γ1=1-ln (Λ12X 2+Λ13X 3)-[ 3 32231131323322112 2131321211X X X X X X X X X X X X +Λ+ΛΛ+Λ++ΛA +Λ+Λ+] = γ1= 同理,γ2=; γ3= lnP 1S = P 1S = lnP 2S = P 2S =
lnP 3S = P 3S = 作为理想气体实际溶液, K 1= P P S 11γ=, K 2=, K 3= 若完全为理想系, K 1=P P S 1= K 2= K 3= 2. 在361K 和下,甲烷和正丁烷二元系呈汽液平衡,汽相含甲烷%( mol ),与其平衡的液相含甲烷%。用 R -K 方程计算 和Ki 值。 解:a 11= 1 1 5 .2 242748.0c c p T R ?= ? dm 6 ? ? mol -2 a 22= 2 2 5 .2 242748.0c c p T R ?= MPa ?dm 6 ??mol -2 b 1= 1 1 208664.0c c p T R ?= dm 3mol -1 b 2= 2 2 5 .2 242748.0c c p T R ?= dm 3mol -1 其中T c1=, P c1= T c2=, P c2= 均为查表所得。 a 12=√a 11?a 22=?dm 6 ??mol -2 液相: a =a 11x 12+2a 12x 1x 2+a 22x 22 =×+2×××+× = b= b 1x 1+b 2x 2=×+×= 由R -K 方程: P=RT/(V-b)-a/[(V+b)] =0740.03610083145.0-?l m V - )0740.0(3611711 .245.0+l m l m V V
热工过程控制系统
热工过程控制系统 第一章 过程控制系统概述 1.1过程控制定义及认识 1.2过程控制目的 *1.3过程控制系统的组成 1.4过程控制系统的特点 *1.5过程控制系统的分类 *1.6过程控制性能指标 1.7 过程控制仪表的发展 1.8 过程控制的地位 1.9 过程控制的任务 1.1过程控制定义及认识 过程控制定义 所谓过程控制(Process Control )是指根据工业生产过程的特点,采用测量仪表、执行机构和计算机等自动化工具,应用控制理论,设计工业生产过程控制系统,实现工业生产过程自动化。 1.3 过程控制系统组成 被控过程(Process ), 指运行中的多种多样的工艺生产设备; 过程检测控制仪表(Instrumentation ), 包括: 测量变送元件(Measurement ); 控制器(Controller ); 执行机构(Control Element ); 显示记录仪表 1.5 过程控制系统的分类 按系统的结构特点来分::反馈控制系统,前馈控制系统,复合控制系统(前馈-反馈控制系统) 要求 观察 思考 调节变换显示记录调节给定值 执行 机构检测仪表 记录仪显示器调节器 控制器 测量变送 被控过程 执行器 r(t)e(t) u(t) q(t) f(t) y(t) z(t) -
按给定值信号的特点来分: 定值控制系统,随动控制系统,程序控制系统 性能指标: 对自动控制系统性能指标的要求主要是稳、快、准。 最大超调量σ%反映系统的相对稳定性,稳态误差ess 反映系统的准确性,调整时间ts 反映系统的快速性。 第三章 过程执行器 主要内容 执行器 电动执行器 气动执行器 调节阀及其流量特性 变频器原理及应用 本节内容在本课程中的地位 执行器用于控制流入 或流出被控过程的物 料或能量,从而实现 对过程参数的自动控 制。 3.1 调节阀(调节机构)结构 调节阀是一个局部阻力可以改变的节流元件。由于阀芯在阀体内移动,改变了阀芯与阀座之间的流通面积,即改变了阀的阻力系数,被调介质的流量也就相应地改变,从而达到调节工艺参数的目的。 3.1 调节阀 功能:接受控制器输出的控制信号,转换成直线位移或角位移,来改变调节阀的流通截面积。 3.1.1 调节阀的组成 执行机构:执行机构是指根据控制器控制信号产生推力或位移的装置; 控制器 测量变送 被控过 程 执行器 r ( t ) e ( t ) u ( t ) q ( t ) f ( t ) y ( t ) z ( t ) -
传质分离过程课后习题答案
传质分离过程课后习题答 案 Modified by JEEP on December 26th, 2020.
第一章 绪论 略 第二章习题 1. 计算在和下苯(1)-甲苯(2)-对二甲苯(3)三元系,当x 1 = 、x 2 =、x 3 =时的K 值。汽相为理想气体,液相为非理想溶液。并与完全理想系的 K 值比较。已知三个二元系的wilson 方程参数(单位: J/mol ): λ12-λ11=-; λ12-λ22= λ23-λ22=; λ23-λ33=- λ13-λ11=; λ13-λ33=- 在T = K 时液相摩尔体积(m 3/kmol )为: =×10 -3 ; =×10 -3 ; =×10 -3 安托尼公式为(p s :Pa ; T :K ): 苯:1n =(); 甲苯:1n =(); 对 -二甲苯:1n = (); 解: 由Wilson 方程得: Λ12=l l V V 12exp[-(λ12-λ11)/RT] =3 3 1091.1001055.177??×exp[-/×]= Λ21= Λ13= Λ31= Λ23= Λ32=
ln γ1=1-ln(Λ12X 2+Λ13X 3)-[ 3 32231131323322112 2131321211X X X X X X X X X X X X +Λ+ΛΛ+Λ++ΛA +Λ+Λ+] = γ1= 同理,γ2=; γ3= lnP 1S = lnP 2S = lnP 3S = 作为理想气体实际溶液, K 1=P P S 11γ=, K 2=, K 3= 若完全为理想系, K 1=P P S 1= K 2= K 3= 2. 在361K 和下,甲烷和正丁烷二元系呈汽液平衡,汽相含甲烷%( mol ),与其平衡的液相含甲烷%。用R -K 方程计算 和Ki 值。 解:a 11=1 1 5 .2 242748.0c c p T R ?= dm 6 mol -2 a 22=2 2 5 .2 242748.0c c p T R ?=MPadm 6mol -2 b 1=1 1 208664.0c c p T R ?=dm 3mol -1 b 2= 2 2 5 .2 242748.0c c p T R ?=dm 3mol -1 其中T c1=, P c1=
第八章 传质过程导论 第九章 气体吸收
第八章传质过程导论 第九章气体吸收 1-1 吸收过程概述与气液平衡关系 1-1 在25℃及总压为101.3kPa的条件下,氨水溶液的相平衡关系为p*=93.90x kPa。试求 (1) 100g水中溶解1g的氨时溶液上方氨气的平衡分压和溶解度系数H; (2) 相平衡常数m。 1-2 已知在20℃和101.3kPa下,测得氨在水中的溶解度数据为:溶液上方氨平衡分压为0.8kPa时,气体在液体中溶解度为1g (NH3)/1000g(H2O)。试求在此温度和压力下,亨利系数E、相平衡常数m及溶解度系数H。 1-3 在总压为101.3kPa,温度为30℃的条件下,含有15%(体积%)SO2的混合空气与含有0.2%(体积%)SO2的水溶液接触,试判断SO2的传递方向。已知操作条件下相平衡常数m=47.9。 1-2 传质机理 1-4 组分A通过厚度为的气膜扩散到催化剂表面时,立即发生化学反应:,生成的B离开催化剂表面向气相扩散。试推导稳态扩散条件下组分A、B的扩散通量及。 1-5 假定某一块地板上洒有一层厚度为1mm的水,水温为297K,欲将这层水在297K的静止空气中蒸干,试求所需时间为若干。已知气相总压为101.3kPa,空气湿含量为0.002kg/(kg 干空气),297K时水的饱和蒸汽压为22.38 kPa。假设水的蒸发扩散距离为5mm。 1-3 吸收速率 1-6 采用填料塔用清水逆流吸收混于空气中的CO2。已知25℃时CO2在水中的亨利系数为1.66×105kPa,现空气中CO2的体积分率为0.06。操作条件为25℃、506.6kPa,吸收液中CO2的组成为。试求塔底处吸收总推动力?p、?c、? X和? Y。 1-7 在101.3kPa及20℃的条件下,在填料塔中用清水逆流吸收混于空气中的甲醇蒸汽。若在操作条件下平衡关系符合亨利定律,甲醇在水中的溶解度系数H=1.995kmol/(m3·kPa)。塔内某截面处甲醇的气相分压为6kPa,液相组成为2.5 kmol/m3,液膜吸收系数k L=2.08×10-5m/s,气相总吸收系数K G=1.122×105 kmol/(m2·s·kPa)。求该截面处
传质导论部分题解
第八章 传质过程导论 1. 求例8-1中以摩尔比和质量浓度表示时的平衡关系。 解:例8-1表示出的平衡关系为:气相氨分压mmHg p 6=,液相氨的质量比1a =1g 氨/100g 水 (1)以摩尔比表示: 气相 ()00796.07546==-=p P p Y 液相 ()()01059.01810017 1===W AL n n X (2)以质量浓度表示: 气相300558.0000328.017m Kg C M C AG A AG =?== 液相390.9582.017m Kg C M C AL A AL =?== 式中AG C ,AL C 之值取自例8-1。 2.空气中含有4ccl 蒸气,由atm 1,K 293压缩到atm 10后通入一冷凝器,测得K 313下开始有4ccl 冷凝,混合气出冷凝器时的温度为K 300,求, (1)压缩前及冷凝前、后4ccl 蒸气的质量分率、质量比和摩尔浓度。 (2)4ccl 蒸气冷凝的百分率。 4ccl 的饱和蒸气压数据0p 如下: 提示:在过程中那一参数保持不变?应当用什么组成进行计算? 解:(1)冷凝后4ccl 在空气中的分压3p 等于K 300下的蒸气压:mmHg p 1233=;冷凝前的分压2p 等于K 313下的蒸气压mmHg p 2102=;压缩前的分压1p 为2p 的 101,即mmH g 21。4ccl 的分子量154=M 。由于混合气体的分子量尚未求得,故 以先计算质量比为便。
压缩前 质量比1a = ()空气M M p p ? -11760 =29 15473921?=1509.0 质量分率1a =1 11a a += 1509 .11509 .0=1311.0 摩尔浓度1c = 11RT p =293 36.6221?=300115.0m Kmol 冷凝前质量比和质量分率在压缩过程中保持不变,故 1509012.a a ==,1311.012==a a 而摩尔浓度取为K 313下的: 2c = 22RT p =313 36.62210?=301076.0m Kmol 冷凝后 3a = 29154760033? -p p =29 154 7477123?=0874.0 3a =0803.00874.10874.0= =3c 300657.030036.62123m Kmol =? (2)在冷凝过程中气相中的空气量不变,故应当用空气为物料衡算的基准,即用比质量分率作计算: 冷凝分率 2 3 2a a a -=- 11509 .00874 .0=421.0 即1.42﹪ 3.一园筒形容器高m 2.1,直径m 1,内盛4ccl 液体至32,器顶有一与外界平衡压力的小孔。由于昼夜温度的差异,器内的空气将因空气的膨胀、收缩而通过小孔发生“呼吸”现象(取大气压为atm 1,忽略其变化所引起的呼吸)。若某天的最高、最低温度分别为20℃及10℃,试求因呼吸而损失的4ccl 量(可作适当的简化近似,如蒸气压可取平均温度下的,作为常数)。 解:呼出的气体重:△n = ??? ? ??-=-212111T T R pV RT pV RT pV 式中 =p a t m 1, V =()()314.012.143212=?? ? ????? ? ?-π3 m
过程控制系统(1)
第一章过程控制系统概述 1.五大参量:温度、压力、流量、物位(液位)、成分 2.过程控制系统的组成:控制器,执行器,被控过程和测量变送等组成;除被控对象外都是变送单元。 过程控制系统由两大部分组成:过程仪表和被控对象 过程控制系统由三大部分组成:检测变送单元,控制器,被控对象。 系统中的名词术语: 1)被控过程:生产过程中被控制的工艺设备或装置(即从被控参数检测点至调节阀之间的管道或设备)。 2)检测变送器:检测量转换为统一标准的电信号。 3)调节器(控制器):实时地对被控系统施加控制用。 4)执行器:将控制信号进行放大以驱动调节阀。 5)被控参数:被控过程内要求保持稳定的工艺参数。 6)控制参数:使被控参数保持期望值的物料量或能量。 7)设定值:被控参数的预定值。 8)测量值:测量变送器输出的被控参数值。 9)偏差:设定值与测量值之差。 10)扰动作用:作用于被控对象并引起被控变量变化的作用。 11)控制作用:调节器的输出(控制调节阀的开度)。 控制器,执行器和检测变送环节称为过程仪表;过程控制系统由过程仪表和被控过程组成。 3.性能指标:包含了对控制系统的稳定性、准确性和快速性三方面的评价。 稳态误差ess:描述系统稳态特性的唯一指标(静态指标)。 衰减比n:n<1,表示过渡过程为发散振荡;
n=1,表示过渡过程为等幅振荡; n>1,表示过渡过程为衰减振荡。 一般为4:1-10:1,4:1为理想指标,也是用来调试的。 前馈,反馈控制特点 (1)反馈控制系统: 根据系统被控参数与给定值的偏差进行工作;是按照偏差进行调节,达到减小或消除偏差的目的;偏差值是系统调节的依据;可以有多个反馈信号;属于闭环控制系统。 (2)前馈控制系统: 根据扰动大小进行控制,扰动是控制的依据;控制及时; 属于开环控制系统; 实际生产中不采用 第二章过程检测仪表 控制器输出: 1.电动仪表:4-20mA,DC(远距离);1-5V,DC(短距离) 气动仪表:20-100Kpa(100m) 直流电流4-20mA,空气压力20-100Kpa为通用标准信号。 由通讯方式划分电流二线制、四线制。区别:二线制信号线和电源线在一个回路。 2.数字滤波:测量信号噪声(干扰)的滤波,消除低频干扰。 (1)算术平均值滤波:周期性等幅振荡的干扰; (2)程序判断滤波:滤除随机干扰; (3)中位值法滤波:去掉方波脉冲; (4)一阶惯性滤波:滤掉高频。 .热电偶冷端补偿: 补偿条件:只有当热电偶冷端温度保持不变时,热电势才是被测温度的单值函数:E(T,0)=E(T,T0)+E(T0,0) 只有将冷端温度保持为0℃,或者进行一定的修正才能得到准确的测量结果,并称之为热电偶冷端温度补偿。
第八章 传质过程导论
第八章传质过程导论 第一节概述 8-1 物质传递过程(传质过程) 传质过程 ? 相内传质过程 ? 相际传质过程 相内传质过程:物质在一个物相内部从浓度(化学位)高的地方向浓度(化学位)高的地方转移的过程。 实例:煤气、氨气在空气中的扩散,食盐在水中的溶解等等。 相际传质过程:物质由一个相向另一个相转移的过程。 相际传质过程是分离均相混合物必须经历的过程,其作为化工单元操作在工业生产中广泛应用,如蒸馏、吸收、萃取等等。 几种典型的相际传质过程 ●吸收:物质由气相向液相转移,如图8-1所示 A 图8-1 吸收传质过程 ●蒸馏:不同物质在汽液两相间的相互转移,如图8-2所示。 相界面 B 图8-2 蒸馏传质过程 ●萃取,包括液-液萃取和液-固萃取 液-液萃取:物质从一个相向另一个相转移。例如用四氯化碳从水溶液中萃取碘。 液-固萃取:物质从固相向液相转移。
●干燥:液体(通常为水)由固相向气相转移 其它相际传质过程:如结晶、吸附、气体的增湿、减湿等等。 传质过程与动量传递、热量传递过程比较有相似之处,但比后二者复杂。例如与传热过程比较,主要差别为: (1)平衡差别 传热过程的推动力为两物体(或流体)的温度差,平衡时两物体的温度相等;传质过程的推动力为两相的浓度差,平衡时两相的浓度不相等。 例如1atm,20oC 下用水吸收空气中的氨,平衡时液相的浓度为0.582 kmol/m3 ,气相的浓度为3.28×10 - 4 kmol/m3 ,两者相差5个数量级。 (2)推动力差别 传热推动力为温度差,单位为oC ,推动力的数值和单位单一;而传质过程推动力浓度有多种表示方法无(例如可用气相分压、摩尔浓度、摩尔分数等等表示),不同的表示方法推动力的数值和单位均不相同。 8-2浓度及相组成的表示方法 1. 质量分数和摩尔分数 ● 质量分数:用w 表示。以A 、B 二组分混合物为例,有 w A = (8-1) ● 质量分数:用x 或y 表示。以A 、B 二组分混合物为例,有 x A = (8-2) 2. 质量比与摩尔比 ● 质量比:混合物中一个组分的质量对另一个组分的质量之比,用w 表示。以A 、B 二组分混合物为例,有 (8-3) ● 摩尔比:混合物中一个组分的摩尔数对另一个组分的摩尔数之比,用X 表示。以A 、B 二组分混合物为例,有 (8-4) 使用质量比或摩尔比在某些计算如吸收、干燥计算中较为方便。 3. 浓度 包括质量浓度和摩尔浓度,后者较常用。 第二节 扩散原理 8-3基本概念和费克定律 分子扩散:物质依靠分子运动从浓度高的地方转移到浓度低的地方,称为分子扩散。分子扩 B A A A m m m m m +=B A A A n n n n n +=B A AB m m w =B A AB n n X =
化工传质与分离过程
化工传质与分离过程
尽量逆流流动(最大的传质推动力): 气体在压差下由下而上,液体在重力下由上而下; 错流塔板:总体上逆流流动,板上错流流动 ?:?板式塔的设计意图(理想流动状态): 气液充分接触,总体上逆流流动,板上错流流动 ?板式塔上两相接触状态: 鼓泡接触状态:U 低,清液层,气泡为传质表面,液相为连续相; 泡沫接触状态:U 增加,清液层降低,不断更新的液膜为传质表面, 喷射接 触状态:U 较大,不断更新的液滴为传质表面曲线,气相为连续相。 第三章塔设备>>3.1板式塔(1) 功能^ 气液接触(传质系数大、接触面积大) 液相为连续相;
液膜夹带 气泡夹带 A 不均匀流动 气体不均匀流动(液面落差和水力学梯度) 液体不均匀流动 随气速增大,使塔板阻力增大,上层塔板上液层增厚,塔板液 流不畅,液层迅速积累,以致充满整个空间,即液泛。由此原 因诱发的液泛为液沫夹带液泛。开始发生液泛时的气速称之为 液泛气速 当塔内气、液两相流量较大,导致降液管内阻力及塔板阻力 增大时,均会引起降液管液层升高,。当降液管内液层髙度 难以维持塔板上液相畅通时,降液管内液层迅速上升,以致 达到上一层塔板,逐渐充满塔板空间,即发生液泛 三章塔设备〉>3」板式塔(2) ?板式塔上非理想流动一降低传质推动力 ?三种不正常现象 A 夹带液泛
第三章塔设备>>3.1板式塔(3)?:?板式塔的塔板基本结构 1、降液管的受液区 2、进口安定区 3、鼓泡区 4、出口安定区(破沫区) 5、降液管的溢流区 6、无效区 液体流动方向
第三章塔设备〉>3?1板式塔(4) ?接触状态的选择 泡沫接触状态:液膜足够稳定,不易形成大气泡,有利传质 喷射接触状态:液滴不断更新,小液滴(要求液滴不稳定)
习题-(07)第七章 传质与分离过程概论天津大学化工原理
第七章 传质与分离过程概论 1.在吸收塔中用水吸收混于空气中的氨。已知入塔混合气中氨含量为5.5%(质量分数,下同),吸收后出塔气体中氨含量为0.2%,试计算进、出塔气体中氨的摩尔比1Y 、2Y 。 解:先计算进、出塔气体中氨的摩尔分数1y 和2y 。 120.055/17 0.09030.055/170.945/29 0.002/170.00340.002/170.998/29 y y ==+==+ 进、出塔气体中氨的摩尔比1Y 、2Y 为 10.09030.099310.0903Y = =- 20.0034 0.003410.0034Y ==- 由计算可知,当混合物中某组分的摩尔分数很小时,摩尔比近似等于摩尔分数。 2. 试证明由组分A 和B 组成的双组分混合物系统,下列关系式成立: (1) 2)B A A B A B A A (d d M x M x x M M w += (2)2A )(d d B B A A B A A M w M w M M w x += 解:(1) B B A A A A A M x M x x M w += B A A A )1(A A M x M x x M -+= 2)B B A )B A )B B A (A A (A (A A A d A d M x M x M M M x M x M x M x w +-+=-2)B B A )B A (B A A (M x M x x x M M +=+ 由于 1B A =+x x 故 2)B B A A B A A (d A d M x M x x M M w += (2) B B A A A A A M w M w M w x += 2)()(A d A d B B A A B A A A B B A A A 11)(1 M w M w M M M w M w M w M w x +-+=- 2)(B A 1(B B A A )B A M w M w M M w w ++= 2)(B B A A B A 1M w M w M M +=
