高三化学工艺流程图习题汇总

化学工艺流程题
1.医用氯化钙可用于补钙、抗过敏和消炎等,以工业碳酸钙(含少量Na+、Al3+、Fe3+等杂质)生产医用二水合氯化钙工艺流程为:
氢氧化物Fe(OH)3Al(OH)3
开始沉淀时的pH开始溶解:
完全沉淀时的pH完全溶解:
(1)CaCO3与盐酸反应的离子方程式。
(2)除杂操作是加入氢氧化钙,调节溶液的pH为,目的是除去溶液中少量的Al3+、Fe3+。检验Fe(OH)3是否沉淀完全的实验操作是________ ________。
(3)过滤时需用的玻璃仪器有。滤渣主要成分的化学式。
(4)酸化时加盐酸的目的为:①,②防止Ca2+ 在蒸发时发生水解。(5)为什么蒸发结晶要保持160℃:。
(6)若所测样品 CaCl2 ·2H2O的质量分数偏高(忽略其它实验误差),可能的原因之一为。
2、实验室用硫酸厂烧渣(主要成分为Fe2O3及少量FeS、SiO2等)制备聚铁(碱式硫酸铁的聚合物)和绿矾(FeSO4·7H2O),过程如下:
(1)将过程②中产生的气体通入下列溶液中,溶液不会褪色的是________(填编号);
A.品红溶液B.紫色石蕊溶液 C.酸性KMnO4溶液 D.溴水
(2)在①中已知FeS中铁元素生成Fe3+,写出FeS、O2、H2SO4反应的方程式 _____;
(3)在③中,需加入的物质是________;
(4)在④中,蒸发浓缩需要的硅酸盐仪器除酒精灯外,还有______ ____________;
(5)在⑥中,将溶液Z控制到70~80 ℃的目的是________ __________;
(6)为测量聚铁样品中铁元素的质量分数,进行下列实验(假设杂质中不含铁元素和硫元素):称取 g样品,
将样品溶于足量的盐酸后,滴加过量的BaCl2;过滤、洗涤、干燥,称量固体的质量为 g。若该聚铁主要成分为[Fe(OH)(SO4)]n,求该聚铁样品中铁元素的质量分数【Mr (BaSO4)=233 Mr (Fe)=56】。(写出计算过程,结果保留4位有效数字)
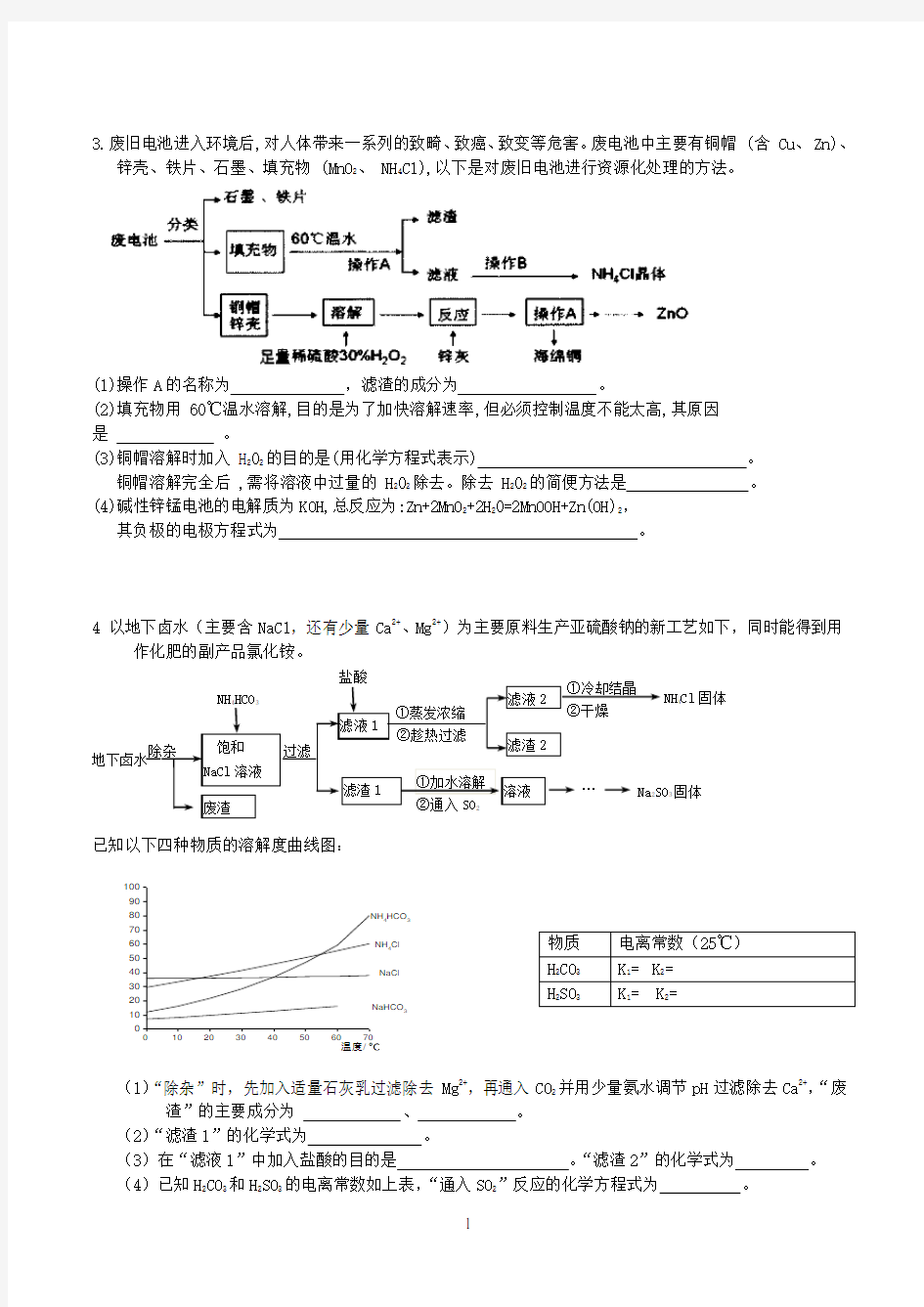
3.废旧电池进入环境后,对人体带来一系列的致畸、致癌、致变等危害。废电池中主要有铜帽 (含 Cu 、 Zn)、 锌壳、铁片、石墨、填充物 (MnO 2、 NH 4Cl),以下是对废旧电池进行资源化处理的方法。
(1)操作A 的名称为 ,滤渣的成分为 。
(2)填充物用 60℃温水溶解,目的是为了加快溶解速率,但必须控制温度不能太高,其原因是 。
(3)铜帽溶解时加入 H 202的目的是(用化学方程式表示) 。 铜帽溶解完全后 ,需将溶液中过量的 H 202除去。除去 H 202的简便方法是 。 (4)碱性锌锰电池的电解质为KOH,总反应为:Zn+2MnO 2+2H 20=2MnOOH+Zn(OH)2, 其负极的电极方程式为 。
4 以地下卤水(主要含NaCl ,还有少量Ca 2+、Mg 2+
)为主要原料生产亚硫酸钠的新工艺如下,同时能得到用
已知以下四种物质的溶解度曲线图:
10
20
30
40
50
60
70
102030405060
708090100
温度/
溶解度/g
NaHCO 3NaCl
NH 4Cl NH 4HCO 3
(1)“除杂”时,先加入适量石灰乳过滤除去Mg 2+
,再通入CO 2并用少量氨水调节pH 过滤除去Ca 2+
,“废
渣”的主要成分为 、 。 (2)“滤渣1”的化学式为 。
(3)在“滤液1”中加入盐酸的目的是 。“滤渣2”的化学式为 。 (4)已知H 2CO 3和H 2SO 3的电离常数如上表,“通入SO 2”反应的化学方程式为 。
物质 电离常数(25℃) H 2CO 3 K 1=
K 2= H 2SO 3
K 1=
K 2=
NH 4Cl 固体
②干燥
②通入SO 2
除杂
饱和 NaCl 溶液
NH 4HCO 3
过滤
滤渣1
①加水溶解 溶液
①蒸发浓缩 滤液2 滤渣2 ①冷却结晶 … Na 2SO 3固体
②趁热过滤
废渣
滤液1
盐酸
地下卤水
5电镀污泥中含有NiO CuO ZnO O Al OH Cr 、、、、323)(等物质,工业上通过“中温焙烧—钠氧化法”回收722O Cr Na 等物质。
已知:水浸后溶液中存在22242ZnO Na NaAlO CrO Na 、、等物质 (1)水浸后的溶液呈____性(“酸”、“碱”、“中”) (2)完成氧化焙烧过程中生成42CrO Na 的化学方程式
____Cr(OH)3+____Na 2CO 3+_____ = ____Na 2CrO 4+___CO 2
(3)滤渣II 的主要成分有2)(OH Zn 、___________________________________
(4)“系列操作”中为:继续加入42SO H ,________冷却结晶,过滤。继续加入42SO H 目的是________。
已知:①除去滤渣II 后,溶液中存在如下反应:O H O Cr H CrO 22722422+==+-
+-
②722CrO Na O Cr Na 、在不同温度下的溶解度如下表
温度 化学式
20℃ 60℃ 100℃ 42SO Na 722O Cr Na 183 269 415 42CrO Na
84
115
126
(5)工业上还可以在水浸过滤后的溶液42加入适量42,用石墨做电极电解生产金属铬,写出生成铬的电极反应方程式____________________________
6.(16分)为了提高资源利用率,减少环境污染,化工集团将钛厂、氯碱厂和甲醇厂组成产业链,如下图所示。
请填写下列空白:
(1)钛铁矿进入氯化炉前通常采取洗涤、粉碎、烘干、预热等物理方法处理,请从原理上解释粉碎的作用___________________;已知氯化炉中反应氯气和焦炭的理论用料物质的量比为7:6,则氯化炉中的还原剂化学式是________________________; (2)已知:①)()()(22s MgCl g Cl s Mg =
+ 1641-?-=?mol kJ H
②)()(12)(1)(224s Ti s Mgc s Tic s Mg +=+ mol kJ H /512-=?
则)()(2)(42s TiCl g Cl s Ti =+ ________;=?H
(3)Ar 气通入还原炉中并不参与反应,通入Ar 气的作用是:___________________________; (4)以甲醇、空气、氢氧化钾溶液为原料,石墨为电极可构成燃料电池。已知该燃料电池
的总反应式为:O H CO OH O OH
CH 2232362432+=++--,该电池中负极上的电极反应式是:
O H CO OH e OH CH 223312216122+=++---。则正极上发生的电极反应为:__________________________ 。
工作一段时间后,测得溶液的pH 是____(填“减小”、“增大”或“不变”)。
7、碱式硫酸铁Fe (OH )SO 4对水中的悬浮物、有机物、硫化物、重金属等都能絮凝,工业上常用硫酸亚铁法制备,工艺流程如下图所示:
FeSO
一系列操作
空气
已知: Fe 3+
沉淀完全时的pH= , Fe 2+
沉淀完全时的pH=
(1)请写出溶解过程中加快溶解速率和提高浸出率的两点措施:_______,__________。
(2)加入硫酸的作用是控制体系的pH 值,若硫酸加入量过低,则反应体系酸度太低,容易生成_____________沉淀;若硫酸加入量过高,不利于产品形成,试从平衡移动的角度分析原因是_______________________; (3)氧化过程中生成一种气体,遇空气变红棕色,写出氧化过程发生的化学方程式:___________________。 (4)流程图中的“一系列操作”包括_______________,_______________,过滤,洗涤,烘干。写出检验沉淀是否洗涤干净的操作_________________________________________。 8、锌钡白是一种白色颜料。工业上是由ZnSO 4与BaS 溶液混合而成:
BaS+ZnSO 4 = ZnS↓+BaSO 4↓。请根据以下工业生产流程回答有关问题. Ⅰ.ZnSO 4溶液的制备与提纯:
有关资料:a.菱锌矿的主要成分是ZnCO 3,含少量SiO 2、FeCO 3、Cu 2(OH)2CO 3等;(OH)2与Al(OH)3相似,能溶于过量的NaOH 溶液生成Na 2ZnO 2;
(1)滤渣1的化学式为 ;②中使用的氧化剂最好是下列的 (填序号)。 D.浓HNO 3
(2)滤渣2中主要成份的化学式为 ;为了达到综合利用、节能减排的目的,上述流程步骤④中的CO 2可以来自于步骤 (选填①、②、③、⑤)。
(3)步骤④发生的离子反应方程式为 。 Ⅱ.BaS 溶液的制备
有关数据: Ba (s )+S (s )+2O 2(g )=BaSO 4(s ) △H 1 = — kJ ?mol -1
C (s )+ 1/2O 2(g )=CO (g ) △H 2 = — kJ ?mol -1
溶解 水、铁粉 氧化 NaNO 2 催化剂 硫酸 气体
调节pH 值
固体碱式硫酸铁产品
BaS 溶液 水浸取 过滤 重晶石(BaSO 4) 矿粉、煤 粉 煅烧还原 BaS CO 1
菱锌矿
滤液1滤渣15mol .L -1H 2SO 42氧化剂溶液3
5ZnSO 46mol .L -1NaOH
(过量)滤渣2滤液24过量CO 2
滤渣3
滤液35mol .L -1H 2SO 4
溶 液
Ba(s)+ S(s)=BaS(s)△H3 = —460 kJ?mol-1
(4)若煅烧还原的产物仅为BaS和CO,则其反应的热化学方程式为:。
Ⅲ.制取锌钡白
(5)如果Ⅰ中步骤⑤使用硫酸过量,产生的后果是。
9、(13分)将磷肥生产中形成的副产物石膏(CaSO4·2H2O)转化为硫酸钾肥料和氯化钙水合物储热材料,
无论从经济效益、资源综合利用还是从环境保护角度看都具有重要意义。以下是石膏转化为硫酸钾和氯化钙的工艺流程示意图。
(1)本工艺中所用的原料除CaSO4·2H2O、CaCO3、H2O外,还需要等原料。
(2)写出石膏悬浊液中加入碳酸铵溶液后发生反应的离子方程式:
(3)过滤Ⅰ操作所得滤液是(NH4)2SO4溶液。检验滤液中含有CO32-的操作方法是:
_________________________________________________________________。
(4)若过滤I的滤液中的Ca2+浓度低于×10-5mol·L-1时可认为被沉淀完全。若要使Ca2+沉淀完全,则滤液中CO32-离子的物质的量浓度不得低于。(已知:K sp(CaCO
=×10-9)
3)
(5)写出蒸氨过程中的化学方程式。
(6)氯化钙结晶水合物(CaCl2·6H2O)是目前常用的无机储热材料,选择的依据是
a.熔点较低(29℃熔化) b.能导电 c.能制冷 d.无毒
10.(15分)工业上设计将VOSO4中的K2SO4、SiO2杂质除去并回收得到V2O5的流程如下:
请回答下列问题:
(1)步骤①所得废渣的成分是(写化学式),操作I的名称。
(2)步骤②、③的变化过程可简化为(下式R表示VO2+,HA表示有机萃取剂):
R2(SO4)n (水层)+ 2nHA(有机层)2RA n(有机层) + nH2SO4 (水层)
②中萃取时必须加入适量碱,其原因是
。
③中X试剂为。
(3)⑤的离子方程式为。
(4)25℃时,取样进行试验分析,得到钒沉淀率和溶液pH之间关系如下表:
pH
钒沉淀率%
结合上表,在实际生产中,⑤中加入氨水,调节溶液的最佳pH为;
若钒沉淀率为%时不产生Fe(OH)3沉淀,则溶液中c(Fe3+)< 。
〖已知:25℃时,Ksp[Fe(OH)3]=×10-39〗
(5)该工艺流程中,可以循环利用的物质有和。
11.(15分)信息时代产生的大量电子垃圾对环境构成了极大的威胁。某“变废为宝”学生探究小组将一批废弃的线路板简单处理后,得到含70%Cu、25%Al、4%Fe及少量Au、Pt等金属的混合物,并设计出如下制备硫酸铜和硫酸铝晶体的路线:
请回答下列问题:
(1)第①步Cu与混酸反应的离子方程式为______________________________;
得到滤渣1的主要成分为______________ _____。
(2)第②步加H2O2的作用是_____________________,使用H2O2的优点是_________;调溶液pH的目的是使_______________________________生成沉淀。
(3)简述第③步由滤液2得到CuSO4·5H2O的方法是________________________ 。
(4)由滤渣2制取Al2(SO4)3·18H2O ,探究小组设计了三种方案:
上述三种方案中,_________________方案不可行,原因是_________________________:
从原子利用率角度考虑,___________方案更合理。
(5)探究小组用滴定法测定CuSO4·5H2O (Mr=250)含量。取a g试样配成100 mL溶液,每次取 mL,消除干扰离子后,用c mol·L-1 EDTA(H2Y2-)标准溶液滴定至终点,平均消耗EDTA溶液b mL。滴定反应如下:Cu2+ + H2Y2-= CuY2- + 2H+
写出计算CuSO4·5H2O质量分数的表达式ω= _____________________________ ;
下列操作会导致CuSO4·5H2O含量的测定结果偏高的是_____________。
a.未干燥锥形瓶 b.滴定终点时滴定管尖嘴中产生气泡
c.未除净可与EDTA反应的干扰离子
高三化学工艺流程图习题汇总
化学工艺流程题 1.医用氯化钙可用于补钙、抗过敏和消炎等,以工业碳酸钙(含少量Na+、Al3+、Fe3+等杂质)生产医用二水合氯化钙工艺流程为: … Fe(OH)3Al(OH)3 氢氧化物 开始沉淀时的pH开始溶解: 完全沉淀时的pH< 完全溶解: (1)CaCO3与盐酸反应的离子方程式。 (2)除杂操作是加入氢氧化钙,调节溶液的pH为,目的是除去溶液中少量的Al3+、Fe3+。检验Fe(OH)3是否沉淀完全的实验操作是________ ________。 (3)过滤时需用的玻璃仪器有。滤渣主要成分的化学式。 (4)酸化时加盐酸的目的为:①,②防止Ca2+ 在蒸发时发生水解。(5)为什么蒸发结晶要保持160℃:。 ~ (6)若所测样品CaCl2 ·2H2O的质量分数偏高(忽略其它实验误差),可能的原因之一为。 2、实验室用硫酸厂烧渣(主要成分为Fe2O3及少量FeS、SiO2等)制备聚铁(碱式硫酸铁的聚合物)和绿矾(FeSO4·7H2O),过程如下: (1)将过程②中产生的气体通入下列溶液中,溶液不会褪色的是________(填编号); 》 A.品红溶液B.紫色石蕊溶液C.酸性KMnO4溶液D.溴水 (2)在①中已知FeS中铁元素生成Fe3+,写出FeS、O2、H2SO4反应的方程式_____; (3)在③中,需加入的物质是________; (4)在④中,蒸发浓缩需要的硅酸盐仪器除酒精灯外,还有______ ____________; (5)在⑥中,将溶液Z控制到70~80 ℃的目的是________ __________; (6)为测量聚铁样品中铁元素的质量分数,进行下列实验(假设杂质中不含铁元素和硫元素):称取g样品,将样品溶于足量的盐酸后,滴加过量的BaCl2;过滤、洗涤、干燥,称量固体的质量为g。若该聚铁主要成分为[Fe(OH)(SO4)]n,求该聚铁样品中铁元素的质量分数【Mr (BaSO4)=233 Mr (Fe)=56】。(写出计算过程,结果保留4位有效数字)
典型超纯水工艺流程设计方案
典型超纯水工艺流程设 计方案 集团标准化小组:[VVOPPT-JOPP28-JPPTL98-LOPPNN]
1纯化水工艺设计方案:(产水水质标准达到的标准:中国药典2005版纯化水标准) 自来水→预处理→一级反渗透→一级EDI→UV杀菌→超滤除热原设备→用水 自来水→预处理→一级反渗透→二级EDI→UV杀菌→超滤除热原设备→用水 2注射用水工艺设计方案:(产水水质标准达到的标准:中国药典2005版注射用水标准) 自来水→预处理→一级反渗透→一级EDI→微滤→多效蒸馏除热原设备→用水 自来水→预处理→一级反渗透→二级EDI→微滤→超滤除热源设备→用水 3电厂高压锅炉给水工艺设计方案(产水水质标准达到的标准:工业锅炉水质GB1576-2001) 自来水→预处理→一级反渗透→脱气装置→二级EDI→微滤→用水 自来水→预处理→一级反渗透→脱气装置→PH调节→二级反渗透→一级EDI→微滤→用水 4微电子/半导体级超纯水工艺设计方案(产水水质标准达到的标准:中国电子工业部高纯水水质试行标准) 自来水→预处理→一级反渗透→脱气装置→二级EDI→UV杀菌装置→超滤→用水 自来水→预处理→一级反渗透→脱气装置→PH调节→二级反渗透→一级EDI→抛光混床→UV杀菌装置→超滤→用水 5实验室用分析级纯水工艺设计方案(产水水质标准达到的标准:分析级实验室用水标准 GB6682-2000) 自来水→预处理→一级反渗透→二级EDI→UV杀菌装置→超滤→用水 自来水→预处理→二级反渗透→一级EDI→UV杀菌装置→超滤→用水 进水电导率在400~1000μs/cm的含EDI设备的典型超纯水工艺流程设计方案 1纯化水工艺设计方案:(产水水质标准达到的标准:中国药典2005版纯化水标准) 自来水→预处理→一级反渗透→二级EDI→UV杀菌→微滤→用水 自来水→预处理→一级反渗透→脱气装置→PH调节→二级反渗透→一级EDI→UV杀菌→微滤→用水 2注射用水工艺设计方案:(产水水质标准达到的标准:中国药典2005版注射用水标准) 自来水→预处理→二级反渗透→一级EDI→多效蒸馏除热源设备→用水 自来水→预处理→一级反渗透→二级EDI→UV杀菌装置→超滤除热源设备→用水 3电厂高压锅炉给水工艺设计方案(产水水质标准达到的标准:工业锅炉水质GB1576-2001) 自来水→预处理→一级反渗透→脱气装置→PH调节→二级反渗透→一级EDI→混床→微滤→用水自来水→预处理→一级反渗透→脱气装置→二级EDI→微滤→用水 4微电子/半导体级超纯水工艺设计方案(产水水质标准达到的标准:中国电子工业部高纯水水质试行标准) 自来水→预处理→一级反渗透→脱气装置→二级EDI→抛光混床→UV杀菌装置→超滤→用水
反渗透工艺方案.教程文件
3t/h 纯水设备 设 计 方 案 二0一二年六月
目录 一、设计基础资料 二、成品水制备工艺流程 三、工艺设计说明 四、自控系统说明 五、设备设计运行参数 六、公用工程条件 七、验收考核项目 八、其它说明 附件: 一、反渗透膜元件污染清洗方法 二、制备工艺流程图
一、工程设计基础资料 1.1设计概况 科润公司新建镀锌生产线工程因生产工艺需要,需配置1套3t/h自动纯水品设备一套,要求出水水质电阻率12McmΩ.cm(20℃)。制备工艺采用反渗透,双级混床,PLC自动控制。同时设备选型留有合理的设计余量。 1.2设计原则 1、优化工艺设计,使系统设备经济、合理、安全、可靠。 2、选用新颖材料和配件,单体设备结构先进、合理。 3、操作维护方便,减少劳动强度。 4、设备布局合理美观。 5、设备选型留有合理的设计余量,确保整个系统运行安全、可靠,尽可能延长设备使用寿命。 6、采用合理工艺和流程,降低运行费用。 7、控制系统可实现自动、手动的切换。 8、关键元器件采用进口件,确保使用性能稳定。 1.3设计依据 (1)原水水质: P H 8.2 计) 76mg/l 总硬度(以CaCO 3 总碱度(以CaCO 计) 850mg/l 3 水温 : 8-24℃
碳酸盐硬度(以CaCO 计) 760mg/l 3 K++Na+ : 250mg/l (2)出水水质: PH ≥7 SS 不得检出 碳酸盐硬度(以CaCO 计)≤1mg/l 3 Na+≤0.5mg/l 电导率:≧12McmΩ.cm(20℃) <0.1mg/l SiO 2 (5)出水水量:3t/h×1套 (6)设计、制造标准 JB/T2932-99《水处理设备制造技术条件》 GB5749-85 《生活饮用水卫生标准》 GBJ109-87 《工业用水软化、除盐设计技术规范》 ZBJ98003-87《水处理设备油漆、包装技术条件》 CD130A15-85《橡胶衬里设备设计技术规范》 GB11446.1-89《电子级水质量标准》 (7)制水效率:出水水量/进水水量≥65% (即进水量为:3/75%=4.6t/h) (8)控制方式:原水至成品水设备系统微电脑自动控制,全自动运行,可进行自动、手动的切换。 (9)电源:电压380V/220V,频率50HZ
高考化学工艺流程 (1)
高考化学工艺流程题 一、探究解题思路 呈现形式:流程图、表格、图像设问方式:措施、成分、物质、原因 能力考查:获取信息的能力、分解问题的能力、表达能力知识落点:基本理论、元素化合物、实验 无机工业流程图题能够以真实的工业生产过程为背景,体现能力立意的命题指导思想,能够综合考查各方面的基础知识及将已有知识灵活应用在生产实际中解决问题的能力。 【例题】某工厂生产硼砂过程中产生的固体废料, 主要含有 MgCO 3、MgSiO 3、 CaMg(CO3 2、 Al 2O 3和 Fe 2O 3等,回收其中镁的工艺流程如下: 原料:矿石(固体 预处理:酸溶解(表述:“ 浸出”
除杂:控制溶液酸碱性使金属离子形成沉淀 核心化学反应是:控制条件,调节 PH ,使 Mg 2+全部沉淀 1. 解题思路 明确整个流程及每一部分的目的→ 仔细分析每步发生的反应及得到的产物→ 结合基础理论与实际问题思考→ 注意答题的模式与要点 在解这类题目时: 首先,要粗读试题,尽量弄懂流程图,但不必将每一种物质都推出。其次,再精读试题,根据问题去精心研究某一步或某一种物质。第三,要看清所问题,不能答非所问,并注意语言表达的科学性在答题时应注意:前一问回答不了,并不一定会影响回答后面的问题。 Ⅱ分离提纯 Ⅰ预处理Ⅱ分离提纯 Ⅲ还原 分析流程图需要掌握的技巧是: ①浏览全题, 确定该流程的目的——由何原料获得何产物(副产物 , 对比原料和产物 ; ②了解流程图以外的文字描述、表格信息、后续设问中的提示性信息,并在下一步分析和解题中随 时进行联系和调用; ③解析流程图并思考: 从原料到产品依次进行了什么反应?利用了什么原理(氧化还原?溶解度?溶液中的平衡?。每一步操作进行到什么程度最佳?每一步除目标物质外还产生了什么杂质或副产物?杂质或副产物是怎样除去的?
反渗透水处理设备工艺说明讲解.doc
【奥凯反渗透设备】流程说明:Reverse osmosis equipment advantage In 1, the recovery rate of >75%RO machine design; In 2, RO inlet low pressure protection, prevent the high-pressure pump water idling; In 3, RO system boot automatic flushing, automatic flushing system to run continuously for 1hours; 4, pretreatment, backwash regeneration RO system for automatic shutdown; raw water pump auto start; In 5, the water level is low or the pure water tank water level when the RO machine automatically shut down, the pure water tank level low when RO machine automatic boot; 6, fault alarm indication; In 7, the built-in PLC lights, easy maintenance; 反渗透设备优点 1、RO 机设计回收率>75%; 2、RO 进水低压保护,防止高压泵缺水空转; 3、RO 系统开机自动冲洗,系统连续运行1小时自动冲洗; 4、预处理再生、反冲洗时RO 系统自动关机;原水泵自动启动; 5、原水箱水位低或纯水箱水位高时RO 机自动关机,纯水箱水位低时RO 机 自动开机; 6、设置故障报警指示; 7、内置PLC 有灯示,维护更容易;
反渗透设备原理,反渗透水处理系统工程工艺流程
奥凯〖反渗透设备〗概述; Okay reverse osmosis water treatment equipment(inverse)with high selectivity for reverse osmosis membrane element desalination rate can be high up to99.7%.So the choice of high salt rejection rate,low osmotic pressure,high flux membrane, can be the most salt ions removal from water. Ro(reverse osmosis)is a kind of pressure driven by a semipermeable membrane, the selection of interception function,the solution of the solute and solvent separation separation method.They are widely used in various liquid separation and concentration.Water treatment process,water,inorganic ion,bacteria,virus, organic matter and colloid and other impurities are removed,to obtain a high quality water. 奥凯反(逆)渗透水处理设备采用选择性较高的反渗透膜元件除盐率可以高达99.7%。所以选择脱盐率高,低渗透压力,高通量的膜,可以将水中的大部分的盐离子去除。 反渗透(逆渗透)是一种在压力驱动下,借助半透膜的选择截留作用,将溶液中的溶质与溶剂分开的分离方法。目前被广泛的应用于各种液体的分离与浓缩。水处理工艺中,将水中无机离子、细菌、病毒、有机物及胶质等杂质去除,以获得高质量的水。 奥凯〖反渗透设备〗原理: Ro(reverse osmosis)technology:reverse osmosis is REVERSE OSMOSIS,it is the United States of America NASA set international scientists,in support of the government,to spend billions of dollars,after many years of research into.Reverse osmosis principle is applied in water on one side than the natural osmotic pressure greater pressure,so that the water molecules from the high concentrations of a reverse osmosis to the low concentration of a party.Due to the reverse osmosis membrane pore size is much smaller than a virus and bacterial hundreds of times or even thousands of times,so a variety of viruses,bacteria,heavy metal,solid solubles,organic pollution,such as calcium and magnesium ions cannot pass reverse osmosis membrane,so as to achieve the purpose of purifying water quality softening. Reverse osmosis membrane of the epidermis is covered with many very fine pores of the membrane,the membrane surface selective adsorption of a layer of water molecules, salt solute is membrane rejection,higher valence ion exclusion of more distant, film hole surrounding water molecules in reverse osmosis pressure role,through the membrane of the capillary effect of water and salt to reach out.RO membrane pore size< 1.0nm,thus can remove at least one bacterium Pseudomonas aeruginosa (specifically10-10m3000influenza virus(800),specifically for10-10m), meningitis,virus(10-10m200specifically for various viruses,can even remove pyrogen
高考化学工艺流程图题型分类
化学工艺流程 1.Li4Ti5O12和LiFePO4都是锂离子电池的电极材料,可利用钛铁矿(主要成分为FeTiO3,还含有少量MgO、SiO2等杂质)来制备,工艺流程如下: 回答下列问题: (1)“酸浸”实验中,铁的浸出率结果如下图所示。由图可知,当铁的净出率为70%时,所采用的实验条件为 ___________________。 (2)“酸浸”后,钛主要以TiOCl42-形式存在,写出相应反应的离子方程式__________________。 (3)TiO2·xH2O沉淀与双氧水、氨水反应40 min所得实验结果如下表所示: 温度/℃30 35 40 45 50 TiO2·xH2O转化率% 92 95 97 93 88 分析40℃时TiO2·xH2O转化率最高的原因__________________。 (4)Li2Ti5O15中Ti的化合价为+4,其中过氧键的数目为__________________。 (5)若“滤液②”中c(Mg2+)= mol/L,加入双氧水和磷酸(设溶液体积增加1倍),使Fe3+恰好沉淀完全即溶液中 c(Fe3+)=1×10-5 mol/L,此时是否有Mg3(PO4)2沉淀生成___________(列式计算)。 FePO4、Mg3(PO4)2的K sp分别为×10-22、×10-24。 (6)写出“高温煅烧②”中由FePO4制备LiFePO4的化学方程式。 【答案】(1)100℃、2h,90℃,5h (2)FeTiO3+ 4H++4Cl? = Fe2++ TiOCl42? + 2H2O (3)低于40℃,TiO2·xH2O转化反应速率随温度升高而增加;超过40℃,双氧水分解与氨气逸出导致TiO2·xH2O 转化反应速率下降 (4)4 (5)Fe3+恰好沉淀完全时,c(PO43-)= 22 5 1.310 1.010 mol·L?1=×10-17mol·L?1,c3(Mg2+)×c2(PO43-)=3××10-17)2=×10-40< K sp [Mg3(PO4)2],因此不会生成Mg3(PO4)2沉淀。
[整理]二级反渗透EDI纯水处理.
广东南方营养保健品有限公司(5.0 m3/h 二级反渗透+EDI纯化水设备)方案报价书
目录 (一)公司简介 (2) (二)设计总导则 (3) (三)设计原始资料 (4) (四)系统对外界的要求 (4) (五)系统流程图 (5) (六)系统流程说明 (5) (七)系统配置及报价 (27) (八)交货期及付款方式 (29) (九)验收标准 (29) (十)设备技术服务内容 (29) (十一)安装、调试、售后服务 (31) (十二)施工现场管理 (32) 一、公司简介
二、设计总导则 2.1技术设计导则 本套水处理设备为5.0m3/h二级反渗透+EDI的纯化水系统,整套设备工艺的设计是基于充分考虑下列因素的基础上制定的: 2.1.1原水水质; 2.1.2用户对产品水的水质和产水量的要求; 2.1.3工艺设计的可靠性; 2.1.4设备对原水水质改变的适应能力; 2.1.5操作的简便性与运行的智能化; 2.1.6废液的处理与排放符合环保要求; 2.1.7投资和运行费用; 2.1.8设备的物理及化学清洗功能; 2.1.9产水质量的稳定性。 2.2 本技术总则用于本工程的水处理脱盐系统。它提出了该系统的功能设 计、结果、性能、安装和调试方面的技术要求。 2.3 需方即使未规定所有的技术要求和适用的标准,供方应提供一套满足 本技术方案和所列标准要求的高质量产品及其相应服务。对国家安全、环境保护高强制性标准,必须满足其要求。 2.4 设备采用的专利涉及到的全部费用均包含在设备报价中,供方应保证 需方不承担有关的设备专利的一切责任。 2.5 供方应提供高质量的设备。这些设备应是技术先进、经济上科学合理、 质量成熟可靠的产品,能满足需方的各项要求。所有设备的设计、制造和安装应保证工作的可靠性,并保证尽可能少的维修量。所有设备的设计结构及配置,必须保证运行中操作者的安全,防护设施及噪音,应符合国际和中国的有关标准。
反渗透设备的工艺流程
反渗透设备是将原水经过精细过滤器、颗粒活性碳过滤器、压缩活性碳过滤器等,使较高浓度的水变为低浓度水,洁净度几乎达到100%,所以人们称这种产水机器为反渗透纯水设备。 目前这种净水设备的应用非常广泛,下面跟大家介绍一下反渗透设备的工艺流程。 1.原水罐 储存原水,用于沉淀水中的大泥沙颗粒及其它可沉淀物质,同时缓冲原水管中水压不稳定对水处理系统造成的冲击,如水压过低或过高引起的压力传感的反应。 2.原水泵 恒定系统供水压力,稳定供水量。 3.多介质过滤器 采用多次过滤层的过滤器,主要目的是去除原水中含有的泥沙、铁锈、胶体物
质、悬浮物等颗粒在20um以上的物质,可选用手动阀门控制或者全自动控制器进行反冲洗、正冲洗等一系列操作。保证设备的产水质量,延长设备的使用寿命。 4.活性炭过滤器 系统采用果壳活性炭过滤器,活性炭不但可吸附电解质离子,还可进行离子交换吸附。经活性炭吸附还可使高锰酸钾耗氧量(COD)由15mg/L(O2)降至2~7mg/L(O2),此外,由于吸附作用使表面被吸附复制的浓度增加,因而还起到催化作用、去除水中的色素、异味、大量生化有机物、降低水的余氯值及农药污染物和除去水中的三卤化物(THM)以及其它的污染物。同时,设备具有自我维护系统,运行费用很低。 5.离子软化系统/加药系统 R/O装置为了溶解固体形物的浓缩排放和淡水的利用,为防止浓水端特别是RO装置最后一根膜组件浓水侧出CaCO3, MgCO3, MgSO4, CaSO4, BaSO4, SrSO4, SiSO4的浓度积大于其平衡溶解度常数而结晶析出,损坏膜原件的应有特性,在进入反渗透膜组件之前,应使用离子软化装置或投放适量的阻垢剂阻止碳酸盐,SiO2,硫酸盐的晶体析出. 6.精密过滤器 采用精密过滤器对进水中残留的悬浮物、非曲直粒物及胶体等物质去除,使RO系统等后续设备运行更安全、更可靠。滤芯为5um熔喷滤芯,目的是把上级过滤单元漏掉的大于5um的杂质除去。防止其进入反渗透装置损坏膜的表面,从而损坏膜的脱盐性能。
二级反渗透设备介绍
二级反渗透设备介绍 包括两级RO装置、清洗系统和中间水箱。 RO反渗透主要去除水中溶解盐类、有机物、二氧化硅胶体、大分子物质及预处理未去除的颗粒物等。采用两级RO工艺可有效去除水中离子,同时使出水满足后续EDI装置工艺进水要求。 反渗透系统由1台5μ过滤器、2台高压泵和压力容器及反渗透膜组成。第一级反渗透装置RO按2∶1排列,采用6支8寸膜串联排列方式,产水量为m3/h,回收率75%;第二级反渗透装置RO按1∶1排列,采用3支8寸膜串联排列方式,产水量为m3/h,回收率85%。膜元件第一级选择海德能公司低压复合膜CPA3,第二级选择海德能公司超低压复合膜ESPA2。(选用ESPA3膜) 为确保RO装置的稳定运行,在RO前设置了UV消毒器和阻垢剂加药系统。UV消毒器1台,处理量为17.6m3/h,主要作用是杀死水中的细菌,避免RO膜受到污堵。紫外灯发射波长为254nm,强度为30000μWs/cm2,杀菌率为99%。 为防止RO装置中浓水侧结垢,须在进水中投加阻垢剂,阻垢剂采用FLOCON260,设计投加量为2.4mg/L。或采用PTP0100阻垢剂,设计投加量为1mg/L。 为去除水中的CO2,在两级RO之间投加NaOH调节一级RO出水的pH值为7.83,NaOH 的设计投加量为4.5mg/L。 RO清洗系统为撬装设备,包括清洗箱、5μm过滤器和清洗泵。当RO系统发生结垢或污堵时可对RO装置进行清洗,同时也可清洗EDI。 中间水箱的功能为储存RO产水、调节水量,使系统运行可以灵活调节。 两级RO系统产水的电导率<10μs/cm,SiO2含量<500μg/L,TOC<50μg/L。[1] 工艺流程 原水加压泵-多介质过滤器-活性炭过滤器-软水器-保安过滤器-第一级反渗透机-第二级反渗透机-储水罐-纯水输送泵-用水点 反渗透装置的应用范围
反渗透水处理技术主要工艺及基本指标
反渗透水处理技术主要工艺及基本指标 一、反渗透设备基本原理 RO反渗透技术是一种高科技水处理技术,它依靠反渗透膜在压力下使溶液中的溶剂和溶质分离的特性工作。“渗透”是一种物理现象,逆渗透就是在含有盐及各种细微杂质的水中(即原水)施加比自然渗透更大的压力,使水从浓度高的一方逆渗透到浓度低的一方,而原水中绝大多数的细微杂质、有机物、重金属、细菌、病毒及其它有害物质等都经污水出口排放掉。 二、反渗透设备标准工艺流程图 三、反渗透纯水设备主要工艺流程说明 1.原水罐(可选) 储存原水,用于沉淀水中的大泥沙颗粒及其它可沉淀物质。同时缓冲原水管中水压不稳定对水处理系统造成的冲击。(如水压过低或过高引起的压力传感的反应)。 2.原水泵 恒定系统供水压力,稳定供水量。 3.多介质过滤器
采用多次过滤层的过滤器,主要目的是去除原水中含有的泥沙、铁锈、胶体物质、悬浮物等颗粒在20um以上的物质,可选 用手动阀门控制或者全自动控制器进行反冲洗、正冲洗等一系列操作。保证设备的产水质量,延长设备的使用寿命。 4.活性炭过滤器 系统采用果壳活性炭过滤器,活性炭不但可吸附电解质离子,还可进行离子交换吸附。经活性炭吸附还可使高锰酸钾耗氧量(COD)由15mg/L(O2)降至2~7mg/L(O2),此外,由于吸附作用使表面被吸附复制的浓度增加,因而还起到催化作用、去除水中的色素、异味、大量生化有机物、降低水的余氯值及农药污染物和除去水中的三卤化物(THM)以及其它的污染物。可选用手动阀门 控制或者全自动控制器进行反冲洗、正冲洗等一系列操作。保证设备的产水质量,延长设备的使用寿命。同时,设备具有自我维护系统,运行费用很低。 5.离子软化系统/加药系统 R/O装置为了溶解固体形物的浓缩排放和淡水的利用,为防止浓水端特别是RO装置最后一根膜组件浓水侧出现 CaCO3,MgCO3,MgSO4,CaSO4,BaSO4, SrSO4, SiSO4的浓度积大于其平衡溶解度常数而结晶析出,损坏膜原件的应有特性,在进入
反渗透系统工艺流程及原理..
反渗透系统工艺流程及说明 原水箱 作用:克服管网供水的不稳定性,保证整个系统的供水稳定连续;同时也给各设备长期性能可靠提供了保障。 选型:PE材质。 控制:水箱配置高水位浮球阀和低水位液位开关。其具备了可靠性高,价格低廉,结构简单,安装方便等优点。当水位处于高位时,浮球阀关闭,停止进水。水位处于低水位时,高水位浮球阀打开,开始向水箱注水。同时,低水位液位开关断开,增压泵停止工作。 增压泵 作用:给预处理各设备提供必需的工作压力。 选型:根据预处理各设备设计压力降(每台过滤设备最大压降0.05Mpa),以及高压泵前压力不能小于0.5Kg/cm2,确定增压泵的工作压力。 控制:泵后用调节阀调节压力及进水量。 机械过滤器 作用:原水首先经过机械过滤器,在过滤器中放置1-16目的精致石英砂,使原水中的絮凝体、铁锈等悬浮杂质在此过程中被截留。由于机械过滤器在工作中截留了大量的悬浮杂质,为保证过滤器的正常工作,必须对过滤器定期进行冲洗、反冲洗。 选型:选用碳钢材质容器. 控制:机械过滤器的反洗操作採用手工控制器,过滤器应每周天进行一次清洗,清洗时间为10-20分钟。 活性碳过滤器 作用:本工艺采用活性碳过滤器,作为反渗透装置的予处理,是非常重要的。反渗透系统要求进水指标SDI≤5,余氯<0.1mg/L。为满足其进水要求,需进一步纯化原水,使之达到反渗透的进水指标。在反渗透装置前设置碳滤器,主要有两
个功能:1、吸附水中部分有机物,吸附率为60%左右;2、吸附水中余氯。吸附粒度在10-20埃左右的无机胶体、有机胶体和溶解性有机高分子杂质以及在砂滤器中是难以去除的余氯。活性碳之所以能用来吸附粒度在几十埃左右的活性物,是由于其结构存在大量平均孔径在20-50埃的微孔和粒缝隙,活性碳的这个结构特点,使它的表面吸附面积能够达到500-2000m2/g,由于一般有机物的分子直径略小于20-50埃,因此活性碳对有机物具有很强的吸附作用。此外活性碳具有很强的脱氯能力,由于余氯具有很强的氧化性,余氯和碳起反应,生成二氧化碳和-1价氯离子,因此只是损失了少量的碳,所以活性碳脱氯可以使用相当长的时间。活性碳不仅仅具有以上功能,还能够去除水中的异味、色素,提高水的澄明度,活性碳使用一段时间后,其吸附能力下降,需要进行再生或更换。所以,原水通过碳滤器后,能大大提高水质,减少对反渗透膜的污染,经过处理后的水质都能达到反渗透装置进水水质要求(余氯<0.1mg/L)。 选型:选用碳钢材质容器。 控制:活性碳过滤器的控制採用手工控制器,由于活性碳过滤器在工作中吸附了大量的悬浮杂质,为保证系统正常工作,每天必须进行冲洗、反冲洗,冲洗过程由清洗时间为10-15分钟。 精密过滤器 作用:精密过滤又称为保安过滤器。它是原水进入反渗透膜装置前的一道处理工艺。PP过滤芯具有过滤流量大,纳污量大,压力损耗小的特点,可阻截不同粒径的杂质颗粒,集表面过滤与深层过滤于一体。精密过滤器使用一定时期后也有堵塞现象,因此,一定时期后PP熔喷滤芯必须更换,更换依据:精密过滤前后的压力差在0.05-0.1Mpa时更换。 选型:选用不锈钢材质容器. 高压泵 作用:高压泵是提供给反渗透系统所需产水流量及水质的工作压力。使过滤水经过泵体后达到10公斤左右的压力,以满足膜体的进水压力,保证纯水的出水量。
高考化学工艺流程题目解题方法指导
工艺流程题解题技巧专题 一、【考点分析】无机化工题实际上是考查考生运用化学反应原理及相关知识来解决工业生产中实际问题的能力。解此类型题目的基本步骤是:①从题干中获取有用信息,了解生产的产品②分析流程中的每一步骤,从几个方面了解流程:A.反应物是什么B.发生了什么反应C.该反应造成了什么后果,对制造产品有什么作用。抓住一个关键点:一切反应或操作都是为获得产品而服务。③从问题中获取信息,帮助解题。 了解流程后着手答题。对反应条件的分析可从以下几个方面着手: 对反应速率有何影响?对平衡转化率有何影响?对综合生产效益有何影响?如原料成本,原料来源是否广泛、是否可再生,能源成本,对设备的要求,环境保护(从绿色化学方面作答)。 二、【工业流程题中常用的关键词】 原材料:矿样(明矾石、孔雀石、蛇纹石、大理石、锂辉石、黄铜矿、锰矿、高岭土,烧渣),合金(含铁废铜),药片(补血剂),海水(污水) 灼烧(煅烧):原料的预处理,不易转化的物质转化为容易提取的物质:如海带中提取碘 酸:溶解、去氧化物(膜)、调节pH促进水解(沉淀) 碱:去油污,去铝片氧化膜,溶解铝、二氧化硅,调节pH促进水解(沉淀) 氧化剂:氧化某物质,转化为易于被除去(沉淀)的离子 氧化物:调节pH促进水解(沉淀) 控制pH值:促进某离子水解,使其沉淀,利于过滤分离 煮沸:促进水解,聚沉后利于过滤分离;除去溶解在溶液中的气体,如氧气 趁热过滤:减少结晶损失;提高纯度 三、【工业流程常见的操作】 (一)原料的预处理 ①溶解:通常用酸溶。如用硫酸、盐酸、浓硫酸等 ②灼烧:如从海带中提取碘 ③煅烧:如煅烧高岭土改变结构,使一些物质能溶解。并使一些杂质高温下氧化、分解 ④研磨:适用于有机物的提取如苹果中维生素C的测定等。 (二)控制反应条件的方法 ①控制溶液的酸碱性使其某些金属离子形成氢氧化物沉淀——pH值的控制。 调节pH所需的物质一般应满足两点:能与H+反应,使溶液pH值增大不引入新杂质。若要除去Cu2+溶液中混有的Fe3+,可加入CuO、Cu(OH)2、Cu2(OH)2CO3等物质来调节溶液的pH值 ②蒸发、反应时的气体氛围 ③加热的目的:加快反应速率或促进平衡向某个方向移动 ④降温反应的目的:防止某物质在高温时会溶解或为使化学平衡向着题目要求的方向移动 ⑤趁热过滤:防止某物质降温时会析出 ⑥冰水洗涤:洗去晶体表面的杂质离子,并减少晶体在洗涤过程中的溶解损耗 (三)物质的分离和提纯的方法 ①结晶——固体物质从溶液中析出的过程(蒸发溶剂、冷却热饱和溶液、浓缩蒸发) 重结晶是利用固体物质均能溶于水,且在水中溶解度差异较大的一种除杂质方法。 ②过滤——固、液分离 ③蒸馏——液、液分离 ④分液——互不相溶的液体间的分离 ⑤萃取——用一种溶剂将溶质从另一种溶剂中提取出来。 ⑥升华——将可直接气化的固体分离出来。 ⑦盐析——加无机盐使溶质的溶解度降低而析出 (四)常见名词
吨单级反渗透标准工艺方案
北京珑海水处理设备有限公司 2t/h单级反渗透设备 设计方案 项目名称:2t/h单级反渗透设备 设计单位:北京珑海水处理设备制造有限公司联系人: 设计日期:2016年07月 目录
进水状况............................................................. 错误!未定义书签。 出水情况............................................................. 错误!未定义书签。2设计依据和指思想..................................................... 错误!未定义书签。 设计依据............................................................. 错误!未定义书签。 设计指导思想......................................................... 错误!未定义书签。3工艺概述 ............................................................ 错误!未定义书签。4主要设备性能描述..................................................... 错误!未定义书签。 预处理系统........................................................... 错误!未定义书签。 原水箱............................................................. 错误!未定义书签。 原水增压泵......................................................... 错误!未定义书签。 石英砂过滤器....................................................... 错误!未定义书签。 活性炭过滤器....................................................... 错误!未定义书签。 阻垢剂投加系统..................................................... 错误!未定义书签。 反渗透系统........................................................... 错误!未定义书签。 反渗透膜概述....................................................... 错误!未定义书签。 保安过滤器......................................................... 错误!未定义书签。 高压泵............................................................. 错误!未定义书签。 反渗透膜........................................................... 错误!未定义书签。 电导率仪........................................................... 错误!未定义书签。 流量计............................................................. 错误!未定义书签。 压力表............................................................. 错误!未定义书签。 进水电磁阀......................................................... 错误!未定义书签。 冲洗电磁阀......................................................... 错误!未定义书签。 压力保护装置....................................................... 错误!未定义书签。 膜的清洗系统....................................................... 错误!未定义书签。
二级反渗透工艺流程图
二级反渗透工艺流程图 反渗透技术介绍 反渗透技术,是当今最先进和最节能有效的膜分离技术。其原理是在高于溶液渗透压的作用下,依据其他物质不能透过半透膜而将这些物质和水分离开来。由于反渗透膜的膜孔径非常小(仅为10A左右),因此能够有效地去除水中的溶解盐类、胶体、微生物、有机物等(去除率高达97%-98%)。反渗透是目前高纯水设备中应用最广泛的一种脱盐技术,它的分离对象是溶液中的离子范围和分子量几百的有机物;反渗透(RO)、超过滤(UF)、微孔膜过滤(MF)和电渗析(EDI) 技术都属于膜分离技术。 反渗透系统设计概述 1. 原水供水单位:原水可能是自来水、地下水、水库水或其它水源,但一般反渗透系统都有一个储水槽。在系统设计时要
考虑避免二次污染,防止沙土、灰尘等机械杂质和发酵、水藻 等生物污染的发生。 2. 预处理系统:针对原水得水质指标和水源特点,设置合理的预处理系统,保证经过预处理的水质能达到反渗透系统对于COD、SDI、余氯和LSI等的要求。对于一定的原水,不同的预处理工艺和污染因子去除效果会影响到反渗透膜元件类型、数量和系统残谁的选择。再目前越来越多的反渗透系统被用于地。表水和回用污水的情况下,为了保证系统性能和效率,推荐优先选用膜法预处理(超滤/微滤) 3. 高压泵系统:高压泵系统的压力(扬程)和流量的选择主要依据运行按照海德能设计软件的模拟计算结果。为了保证系统的安全可靠,再实际选型时,可以再计算结果推荐选型的基础上提高10%扬程和流量规格。在反渗透高压泵要求使用性能高度稳定的耐腐蚀泵。泵系统一般由给水泵和高压泵组成。给水泵加再保安过滤器之前,用于高压泵供水和低压冲洗。再高压泵出口一般要安装手动调压阀和慢开电动阀。手动调压阀用于调节泵的出力,电动阀可以防止高压泵启动时发生水锤现 象。 4. RO膜单元:RO膜单元由压力容器、膜元件、管道和浓水 阀门等组成,是反渗透系统的核心。 5. 仪表和控制系统:为了装置能够安全可靠的运行、便于过程监控,一般要配备温度表,PH计、压力表、流量计、电导
反渗透设备工艺流程简介讲解
反渗透设备工艺流程简介 当代反渗透纯水设备主流工艺流程已基本确定,每家公司工艺总体来说都是: 储水箱→原水加压泵→多介质过滤器→活性炭过滤器→软化水设备→中间水箱→加压泵→阻垢剂添加装置→保安过滤器→反渗透装置→离子交换器→杀菌设备→纯水箱→用水点 1.原水罐 储存原水,用于沉淀水中的大泥沙颗粒及其它可沉淀物质。同时缓冲原水管中水压不稳定对水处理系统造成的冲击。(如水压过低或过高引起的压力传感的反应)。 2.原水泵 恒定系统供水压力,稳定供水量。 3.多介质过滤器 采用多次过滤层的过滤器,主要目的是去除原水中含有的泥沙、铁锈、胶体物质、悬浮物等颗粒在20um以上的物质,可选用手动阀门控制或者全自动控制器进行反冲洗、正冲洗等一系列操作。保证设备的产水质量,延长设备的使用寿命。 4.活性炭过滤器 系统采用果壳活性炭过滤器,活性炭不但可吸附电解质离子,还可进行离子交换吸附。经活性炭吸附还可使高锰酸钾耗氧量(COD)由15mg/L(O2)降至2~7mg/L(O2),此外,由于吸附作用使表面被吸附复制的浓度增加,因而还起到催化作用、去除水中的色素、异味、大量生化有机物、降低水的余氯值及农药污染物和除去水中的三卤化物(THM)以及其它的污染物。可选用手动阀门控制或者全自动控制器进行反冲洗、正冲洗等一系列操作。保证设备的产水质量,延长设备的使用寿命。同时,设备具有自我维护系统,运行费用很低。 5.离子软化系统/加药系统 R/O装置为了溶解固体形物的浓缩排放和淡水的利用,为防止浓水端特别是RO装置最后一根膜组件浓水侧出现CaCO3,MgCO3,MgSO4,CaSO4,BaSO4, SrSO4, SiSO4的浓度积大于其平衡溶解度常数而结晶析出,损坏膜原件的应有特性 ,在进入反渗透膜组件之前,应使用离子软化装置或投放适量的阻垢剂阻止碳酸盐, SiO2,硫酸盐的晶体析出. 6.精密过滤器(也叫保安过滤器) 采用精密过滤器对进水中残留的悬浮物、非曲直粒物及胶体等物质去除,使RO系统等后续设备运行更安全、更可靠。滤芯为5um熔喷滤芯,目的是把上级过滤单元漏掉的大于5um的杂质除去。防止其进入反渗透装置损坏膜的表面,从而损坏膜的脱盐性能。 7.反渗透系统
高考化学工艺流程图题型分类
化学工艺流程 1. Li4Ti5O12和LiFePO4都是锂离子电池的电极材料,可利用钛铁矿(主要成分为FeTiO3,还含有少量MgO、SiO2等杂质)来制备,工艺流程如下: 回答下列问题: (1)“酸浸”实验中,铁的浸出率结果如下图所示。由图可知,当铁的净出率为70%时,所采用的实验条件为___________________。 (2)“酸浸”后,钛主要以TiOCl42-形式存在,写出相应反应的离子方程式__________________。 (3)TiO2·x H2O沉淀与双氧水、氨水反应40 min所得实验结果如下表所示: 分析40℃时TiO2·x H2O转化率最高的原因__________________。 (4)Li2Ti5O15中Ti的化合价为+4,其中过氧键的数目为__________________。 (5)若“滤液②”中c(Mg2+)= mol/L,加入双氧水和磷酸(设溶液体积增加1倍),使Fe3+恰好沉淀完全即溶液中c(Fe3+)=1×10-5 mol/L,此时是否有Mg3(PO4)2沉淀生成?___________(列式计算)。 FePO4、Mg3(PO4)2的K sp分别为×10-22、×10-24。 (6)写出“高温煅烧②”中由FePO4制备LiFePO4的化学方程式。 【答案】(1)100℃、2h,90℃,5h (2)FeTiO3+ 4H++4Cl? = Fe2++ TiOCl42? + 2H2O (3)低于40℃,TiO2·x H2O转化反应速率随温度升高而增加;超过40℃,双氧水分解与氨气逸出导致TiO2·x H2O 转化反应速率下降 (4)4 (5)Fe3+恰好沉淀完全时,c(PO43-)=mol·L?1=×10-17mol·L?1,c3(Mg2+)×c2(PO43-)=3××10-17)2=×10-40<K sp [Mg3(PO4)2],因此不会生成Mg3(PO4)2沉淀。 (6)2FePO4 + Li2CO3+ H2C2O42LiFePO4+ H2O↑+ 3CO2↑ 2.水泥是重要的建筑材料。水泥熟料的主要成分为CaO、SiO2,并含有一定量的铁、铝和镁等金属的氧化物。实验室测定水泥样品中钙含量的过程如图所示: 回答下列问题: (1)在分解水泥样品过程中,以盐酸为溶剂,氯化铵为助溶剂,还需加入几滴硝酸。加入硝酸的目的是__________,还可使用___________代替硝酸。 (2)沉淀A的主要成分是_________,其不溶于强酸但可与一种弱酸反应,该反应的化学方程式为____________________________________。 (3)加氨水过程中加热的目的是___________。沉淀B的主要成分为_____________、____________(填化学式)。(4)草酸钙沉淀经稀H2SO4处理后,用KMnO4标准溶液滴定,通过测定草酸的量可间接获知钙的含量,滴定反应为:+H++H2C2O4→Mn2++CO2+H2O。实验中称取 g水泥样品,滴定时消耗了mol·L-1的KMnO4溶液 mL,则该水泥样品中钙的质量分数为______________。 【答案】(1)将样品中可能存在的Fe2+氧化为Fe3+ ;双氧水(H2O2) (2) SiO2 (或H2SiO3);SiO2+4HFSiF4↑+2H2O (3)防止胶体生成,易沉淀分离;Fe(OH)3、 (OH)3 (4)% 3.重铬酸钾是一种重要的化工原料,一般由铬铁矿制备,铬铁矿的主要成分为FeO·Cr2O3,还含有硅、铝等杂质。制备流程如图所示:
