乙酸乙酯的皂化反应数据处理

1
五.数据记录及处理
25℃时к0、к
∞的测定
项目
0.01moL/L 的NaOH 溶液的电导率 平均值 к0/m ?*cm
① 3.70 ② 3.75 ③ 3.72 3.72 К∞/m ?*cm
① 0.95
② 0.95
③ 0.95
0.95
表4-3 25℃时不同反应时间的电导率 t /min 4 9 14 19 24 29 34 39 44 49 кt/m ?/cm
3.4 3 2.8 2.6 2.5 2.45 2.35 2.31 2.252 2.25 (к0-кt )/t /m ?/cm/min
0.08 0.08 0.0657 0.0589 0.0508 0.0438 0.0403 0.0362 0.0334 0.03 (к0-кt )/(кt -к∞)
0.1306
0.3512
0.4973
0.6788
0.7871
0.8467
0.9786
1.0368
1.1275
1.1308
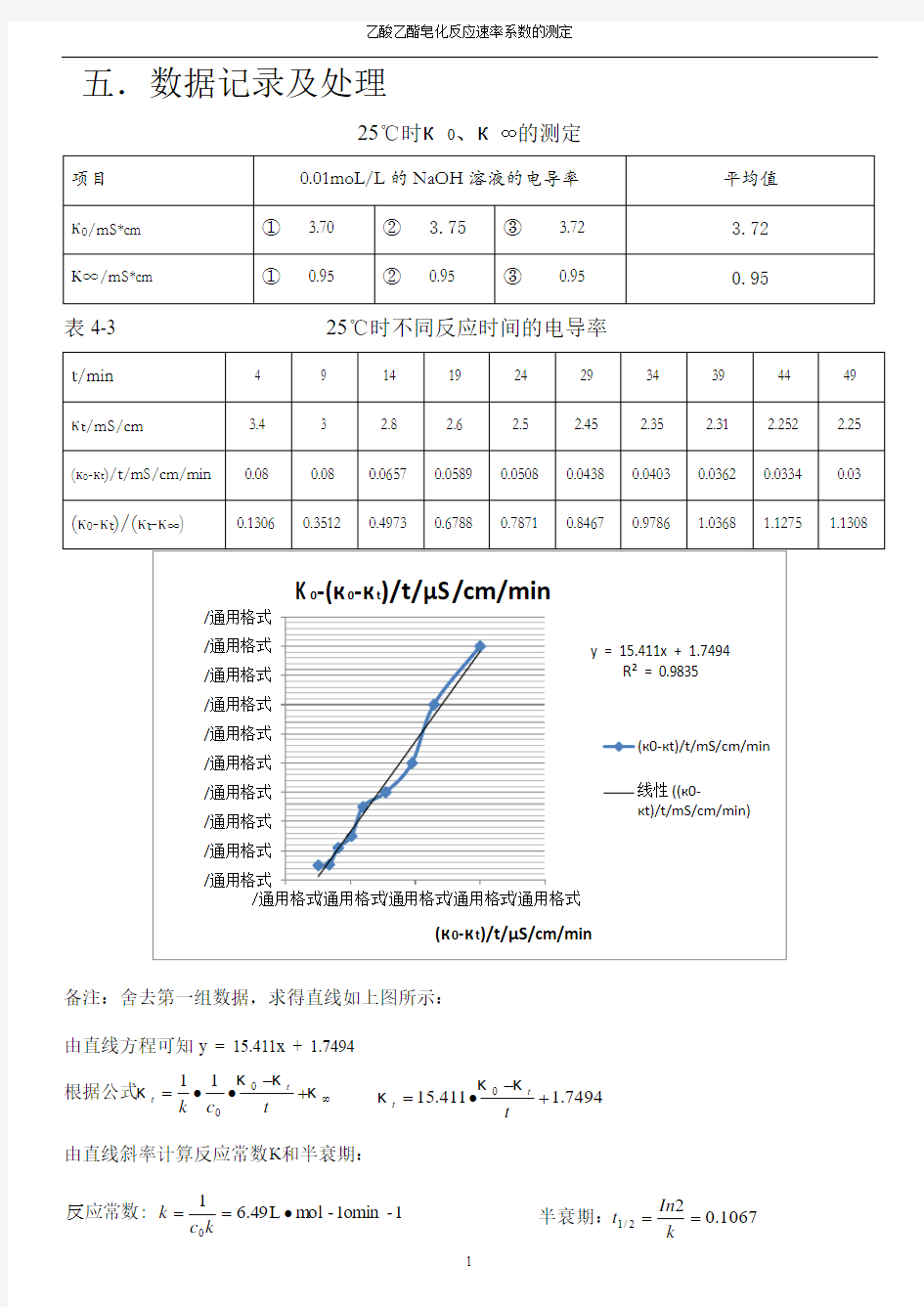
备注:舍去第一组数据,求得直线如上图所示:
由直线方程可知y = 15.411x + 1.7494 根据公式∞+-??=
κκκκt c k t t 0011 7494.1411.150+-?=t
t t κκκ
由直线斜率计算反应常数К和半衰期:
1-1omin -m ol L 49.61:反0?==
k c k 应常数 1067
.022/1==k In t 半衰期:
y = 15.411x + 1.7494
R2 = 0.9835
/通用格式
/通用格式
/通用格式 /通用格式 /通用格式 /通用格式 /通用格式 /通用格式 /通用格式 /通用格式 /通用格式 /通用格式 /通用格式 /通用格式 /通用格式
кt /m ?/c m
(к0-кt )/t/μ?/cm/min
K 0-(к0-кt )/t/μ?/cm/min
(к0-кt)/t/m?/cm/min 线性 ((к0-кt)/t/m?/cm/min)
2
35℃时к0、к
∞的测定
项目
0.01moL/L 的NaOH 溶液的电导率 平均值 к0/m ?*cm
② 1.85 ② 1.87 ③ 1.86 1.86 К∞/m ?*cm
① 0.55
② 0.54
④ 0.56
⑤ 0.55
表4-3 35℃时不同反应时间的电导率 t /min 5 10 15 20 25 30 35 40 45 50 кt/m ?/cm
1.82
1.66
1.5
1.45
1.42
1.39
1.37
1.365
1.36
1.355
(к0-кt )/t /m ?/cm/min
0.008 0.02 0.024 0.0205 0.0176 0.0157 0.014 0.0124 0.0111 0.0101
(к0-кt )/(кt -к∞)
0.0315 0.1802 0.3789 0.4556 0.5057 0.5595 0.5976 0.6074 0.6173 0.6273
由直线方程可知y = y = 10.572x + 1.2356
根据公式
∞+-??=
κκκκt
c k t t 0011 2356
.1572.100+-?=t t
t κκκ
由直线斜率计算反应常数К和半衰期:
1-1omin -mol L 458.91
:反0?==
k
c k 应常数
0733.02
2/1==
k In t 半衰期:
由25和35求出的速率常数,根据阿累尼乌斯公式计算活化能Ea
1
21
212T T T T R Ea k k In
?-?= 即
298
308298
308314..849.657.10?-?
=Ea In
解得:Ea=37.2KJ/mol
y = 10.572x + 1.2356
R2 = 0.9657
/通用格式
/通用格式
/通用格式 /通用格式 /通用格式 /通用格式 /通用格式 /通用格式 /通用格式 /通用格式 /通用格式 /通用格式 /通用格式 /通用格式 /通用格式 /通用格式 /通用格式 /通用格式
кt /m ?/c m
(к0-кt )/t/m ?/cm/min
кt /m ?/cm-(к0-кt)/t/m ?/cm/min
(к0-кt )/t/m?/cm/min 线性 ((к0-кt )
/t/m?/cm/min)
乙酸乙酯皂化反应实验报告
乙酸乙酯皂化反应速度常相数的测定 一、实验目的 1.通过电导法测定乙酸乙酯皂化反应速度常数。 2.求反应的活化能。 3.进一步理解二级反应的特点。 4.掌握电导仪的使用方法。 二、基本原理 乙酸乙酯的皂化反应是一个典型的二级反应: 325325CH COOC H OH CH COO C H OH --+??→+ 设在时间t 时生成浓度为x ,则该反应的动力学方程式为 ()()dx k a x b x dt - =-- (8-1) 式中,a ,b 分别为乙酸乙酯和碱的起始浓度,k 为反应速率常数,若a=b,则(8-1)式变为 2()dx k a x dt =- (8-2) 积分上式得: 1() x k t a a x =?- (8-3) 由实验测的不同t 时的x 值,则可根据式(8-3)计算出不同t 时的k 值。如果k 值为常数,就可证明反应是二级的。通常是作 () x a x -对t 图,如果所的是直线,也可证明反应是二级 反应,并可从直线的斜率求出k 值。 不同时间下生成物的浓度可用化学分析法测定,也可用物理化学分析法测定。本实验用电导法测定x 值,测定的根据是: (1) 溶液中OH -离子的电导率比离子(即3CH COO -)的电导率要大很多。因此,随着反应的进行,OH -离子的浓度不断降低,溶液的电导率就随着下降。 (2) 在稀溶液中,每种强电解质的电导率与其浓度成正比,而且溶液的总电导率
就等于组成溶液的电解质的电导率之和。 依据上述两点,对乙酸乙酯皂化反应来说,反映物和生成物只有NaOH 和NaAc 是 强电解质,乙酸乙酯和乙醇不具有明显的导电性,它们的浓度变化不至于影响电导率的数值。如果是在稀溶液下进行反应,则 01A a κ= 2A a κ∞= 12()t A a x A x κ=-+ 式中:1A ,2A 是与温度、溶剂、电解质NaOH 和NaAc 的性质有关的比例常数; 0κ,κ∞分别为反应开始和终了是溶液的总电导率;t κ为时间t 时溶液的总电导率。由此三 式可以得到: 00( )t x a κκκκ∞ -=- (8-4) 若乙酸乙酯与NaOH 的起始浓度相等,将(8-4)式代入(8-3)式得: 01t t k ta κκκκ∞ -= ?- (8-5) 由上式变换为: 0t t kat κκκκ∞-= + (8-6) 作0~ t t t κκκ-图,由直线的斜率可求k 值,即 1m ka = ,1k ma = 由(8-3)式可知,本反应的半衰期为: 1/21 t ka = (8-7) 可见,两反应物起始浓度相同的二级反应,其半衰期1/2t 与起始浓度成反比,由(8-7)式可知,此处1/2t 亦即作图所得直线之斜率。 若由实验求得两个不同温度下的速度常数k ,则可利用公式(8-8)计算出反应的活化能a E 。
乙酸乙酯皂化反应实验报告(详细参考)
浙江万里学院生物与环境学院 化学工程实验技术实验报告 实验名称:乙酸乙酯皂化反应 姓名成绩 班级学号 同组姓名实验日期 指导教师签字批改日期年月日
一、实验预习(30分) 1.实验装置预习(10分)_____年____月____日 指导教师______(签字)成绩 2.实验仿真预习(10分)_____年____月____日 指导教师______(签字)成绩 3.预习报告(10分) 指导教师______(签字)成绩 (1)实验目的 1.用电导率仪测定乙酸乙酯皂化反应进程中的电导率。 2.掌握用图解法求二级反应的速率常数,并计算该反应的活化能。 3.学会使用电导率仪和超级恒温水槽。 (2)实验原理 乙酸乙酯皂化反应是个二级反应,其反应方程式为 CH3COOC2H5+Na++OH-→CH3COO-+Na++C2H5OH 当乙酸乙酯与氢氧化钠溶液的起始浓度相同时,如均为a,则反应速率表示为 (1)式中,x为时间t时反应物消耗掉的浓度,k为反应速率常数。将上式积分得 (2) 起始浓度a为已知,因此只要由实验测得不同时间t时
的x值,以对t作图,应得一直线,从直线的斜率便可求出k值。 乙酸乙酯皂化反应中,参加导电的离子有OH-、Na+和CH3COO-,由于反应体系是很稀的水溶液,可认为CH3COONa是全部电离的,因此,反应前后Na+的浓度不变,随着反应的进行,仅仅是导电能力很强的OH-离子逐渐被导电能力弱的CH3COO-离子所取代,致使溶液的电导逐渐减小,因此可用电导率仪测量皂化反应进程中电导率随时间的变化,从而达到跟踪反应物浓度随时间变化的目的。 令G0为t=0时溶液的电导,G t为时间t时混合溶液的电导,G∞为t=∞(反应完毕)时溶液的电导。则稀溶液中,电导值的减少量与CH3COO-浓度成正比,设K为比例常数,则 由此可得 所以(2)式中的a-x和x可以用溶液相应的电导表示,将其代入(2)式得: 重新排列得: (3) 因此,只要测不同时间溶液的电导值G t和起始溶液的电导值G0,然后 以G t对作图应得一直线,直线的斜率为,由此便求出某温 度下的反应速率常数k值。由电导与电导率κ的关系式:G=κ代入(3)式得: (4) 通过实验测定不同时间溶液的电导率κt和起始溶液 的电导率κ0,以κt,对作图,也得一直线,从直线的斜率也可求出反应速率数k值。如果知道不同温度下的反应速率常数k(T2)和k(T1),根据Arrhenius公式,可计算出该反应的活化能E和反应半衰期。 (5)
乙酸乙酯实验报告
乙酸乙酯皂化反应速率常数测定 实验日期: 提交报告日期: 带实验的老师 一、 引言 1. 实验目的 1.学习测定化学反应动力学参数的一种物理化学分析方法——电导法。 2.了解二级反应的特点,学习反应动力学参数的求解方法,加深理解反应动力学特征。 3.进一步认识电导测定的应用,熟练掌握电导率仪的使用方法。 2. 实验原理 反应速率与反应物浓度的二次方成正比的反应为二级反应,其速率方程式可以表示为 22dc - =k c dt (1) 将(1)积分可得动力学方程: c t 22c 0dc -=k dt c ?? (2) 20 11-=k t c c (3) 式中:0c 为反应物的初始浓度;c 为t 时刻反应物的浓度;2k 为二级反应的反应速率常数。将1/c 对t 作图应得到一条直线,直线的斜率即为2k 。 对于大多数反应,反应速率与温度的关系可以用阿累尼乌斯经验方程式来表示: a E ln k=lnA-RT (4) 式中:a E 为阿累尼乌斯活化能或反应活化能;A 为指前因子;k 为速率常数。 实验中若测得两个不同温度下的速率常数,就很容易得到 21T a 21T 12k E T -T ln =k R T T ?? ??? (5) 由(5)就可以求出活化能a E 。 乙酸乙酯皂化反应是一个典型的二级反应,
325325CH COOC H +NaOH CH COONa+C H OH → t=0时, 0c 0c 0 0 t=t 时, 0c -x 0c -x x x t=∞时, 0 0 0x c → 0x c → 设在时间t 内生成物的浓度为x ,则反应的动力学方程为 220dx =k (c -x)dt (6) 2001x k =t c (c -x) (7) 本实验使用电导法测量皂化反应进程中电导率随时间的变化。设0κ、t κ和κ∞分别代表时间为0、t 和∞(反应完毕)时溶液的电导率,则在稀溶液中有: 010=A c κ 20=A c κ∞ t 102=A (c -x)+A x κ 式中A 1和A 2是与温度、溶剂和电解质的性质有关的比例常数,由上面的三式可得 0t 00-x= -c -κκκκ∞ (8) 将(8)式代入(7)式得: 0t 20t -1k = t c -κκκκ∞ (9) 整理上式得到 t 20t 0=-k c (-)t+κκκκ∞ (10) 以t κ对t (-)t κκ∞作图可得一直线,直线的斜率为20-k c ,由此可以得到反应速率系数2k 。 溶液中的电导(对应于某一电导池)与电导率成正比,因此以电导代替电导率,(10)式也成立。本实验既可采用电导率仪,也可采用电导仪。 3实验操作 3.1 实验用品
乙酸乙酯皂化反应速率常数的测定
乙酸乙酯皂化反应速率常数的测定 一、实验目的 1.学习电导法测定乙酸乙酯皂化反应速率常数的原理和方法以及活化能的测定方法; 2.了解二级反应的特点,学会用图解计算法求二级反应的速率常数; 3.熟悉电导仪的使用。 二、实验原理 (1)速率常数的测定 乙酸乙酯皂化反应时典型的二级反应,其反应式为: CH 3COOC 2H 5+NaOH = CH 3OONa +C 2H 5OH t=0 C 0 C 0 0 0 t=t Ct Ct C 0 - Ct C 0 -Ct t=∞ 0 0 C 0 C 0 速率方程式 2kc dt dc =- ,积分并整理得速率常数k 的表达式为: t 0t 0c c c c t 1k -?= 假定此反应在稀溶液中进行,且CH 3COONa 全部电离。则参加导电离子有Na + 、OH -、CH 3COO -,而Na +反应前后不变,OH -的迁移率远远大于CH 3COO -,随着反 应的进行, OH - 不断减小,CH 3COO -不断增加,所以体系的电导率不断下降,且体系电导率(κ) 的下降和产物CH 3COO -的浓度成正比。 令0κ、t κ和∞κ分别为0、t 和∞时刻的电导率,则: t=t 时,C 0 –Ct=K (0κ-t κ) K 为比例常数 t→∞时,C 0= K (0κ-∞κ) 联立以上式子,整理得:
∞+-?= κκκκt kc 1t 00t 可见,即已知起始浓度C 0,在恒温条件下,测得0κ和t κ,并以t κ对t t 0κκ-作图,可得一直线,则直线斜率0 kc 1 m = ,从而求得此温度下的反应速率常数k 。 (2)活化能的测定原理: )11(k k ln 2 1a 12T T R E -= 因此只要测出两个不同温度对应的速率常数,就可以算出反应的表观活化能。 三、仪器与试剂 电导率仪 1台 铂黑电极 1支 大试管 5支 恒温槽 1台 移液管 3支 氢氧化钠溶液(0.02mol/L ) 乙酸乙酯溶液(0.02mol/L ) 四、实验步骤 1.标定NaOH 溶液及乙酸乙酯溶液的配制 计算标定0.023/dm mol NaOH 溶液所需的草酸二份,放入锥形瓶中,用少量去离子水溶解之,标定溶液。计算出配制与NaOH 等浓度的乙酸乙酯溶液100mL 所需化学纯乙酸乙酯的质量,根据不同温度下乙酸乙酯的密度计算其体积(乙酸乙酯的取样是通过量取一定量的体积),于ml 100容量瓶中加入约3/2容积的去离子水,然后用1mL 移液管吸取所需的乙酸乙酯加入容量瓶中,加水至刻度,摇匀。 2.调节恒温水浴调节恒温水浴温度为30℃1.0±℃。 3.电导率0K 的测定 用mL 20移液管量取去离子水及标定过的NaOH 溶液各mL 20,在干燥的100mL 烧杯中混匀,用少量稀释后的NaOH 溶液淋洗电导电极及电极管3次,装入适量的此NaOH 溶液于电极管中,浸入电导电极并置于恒温水浴中恒温。将
酯化反应
第2课时乙酸和乙醇的酯化反应 课前预热 1.乙酸和乙醇在浓硫酸存在下加热,乙醇中的________键断裂,乙酸中的________键断裂,生成了________和________。这种________跟________在加热条件下生成酯和________的反应叫做________反应。 2.乙酸是重要的有机化工原料,也是一种有机________。在染料、油漆、塑料、维尼纶、醋酸纤维等生产过程中都需要大量的乙酸。用乙酸制取的铝盐、铁盐和铬盐是染色的________。 拓展延伸 1.乙酸和乙醇酯化反应的方程式为: 2.乙酸乙酯是无色透明液体,有水果香。易挥发,对空气敏感,能吸水分,水分能使其缓慢分解而呈酸性反应。乙酸乙酯微溶于水,易溶于有机溶剂,密度比水小。 3.乙酸乙酯在酸性或碱性条件下微热会发生水解: 酸性条件下:CH3COOCH2CH3 + H2O CH3COOH + CH3CH2OH 碱性条件下:CH3COOCH2CH3 + H2O CH3COONa + CH3CH2OH 4.实验室里用乙醇与乙酸在浓硫酸的吸水和催化作用下加热制取。反应器常用烧瓶或试管,并有回流装置,并用冷凝管蒸出乙酸乙酯。接受器里放有饱和碳酸钠溶液,以除去酯中杂入的乙酸并降低酯在水里的溶解度。工业上还用乙醛缩合法制取。需催化剂、助催化剂,使2分子乙醛生成1分子乙酸乙酯。 5.乙酸乙酯大量用做清漆、硝化纤维、涂料和有机合成的溶剂等,此外,还可以于人造香精、香料、人造皮革等的制造。 【典例精析】实验室制取乙酸乙酯的实验中,加入浓硫酸的作用是什么?为什么要加入过量的乙醇?为什么要加入沸石?饱和碳酸钠的作用是什么? 【分析】实验室制取乙酸乙酯的实验中,浓硫酸有催化剂和吸水的作用;该反应是可逆反应,加入过量乙醇可以是平衡正向移动,提高乙酸转化率和乙酸乙酯产率;加入沸石可以防止爆沸;饱和碳酸钠可以出去酯中杂入的乙酸,并降低酯在水中的溶解度。 【答案】作为催化剂,吸水提高乙酸乙酯产率防止爆沸除去杂质乙酸,降低乙酸乙酯在水中的溶解度 【变式训练】“酒是陈的香”,就是因为酒在贮存过程中生成了具有香味的乙酸乙酯,在实验室我们也可以用如图所示装置制取乙酸乙酯。回答下列问题: (1)写出制取乙酸乙酯的化学方程式:__________________________________________,反应类型为:_____________。 (2)B试管中饱和碳酸钠的主要作用是__________________________________________。 (3)装置中通蒸气的导管要插在饱和碳酸钠的液面上,不能插入溶液中,目的是防止
乙酸乙酯皂化反应实验报告精选doc
浙江万里学院生物与环境学院化学工程实验技术实验报告 实验名称:乙酸乙酯皂化反应
一、实验预习(30分) 1.实验装置预习(10分)_____年____月____日 指导教师______(签字)成绩 2.实验仿真预习(10分)_____年____月____日 指导教师______(签字)成绩 3.预习报告(10分) 指导教师______(签字)成绩 (1)实验目的 1.用电导率仪测定乙酸乙酯皂化反应进程中的电导率。 2.掌握用图解法求二级反应的速率常数,并计算该反应的活化能。 3.学会使用电导率仪和超级恒温水槽。 (2)实验原理 乙酸乙酯皂化反应是个二级反应,其反应方程式为 CH3COOC2H5+Na++OH-→CH3COO-+Na++C2H5OH 当乙酸乙酯与氢氧化钠溶液的起始浓度相同时,如均为a,则反应速率表示为
(1) 式中,x为时间t时反应物消耗掉的浓度,k为反应速率常数。将上式积分得 (2) 起始浓度a为已知,因此只要由实验测得不同时间t时的x值,以对t作图,应得一直线,从直线的斜率便可求出k值。
乙酸乙酯皂化反应中,参加导电的离子有OH-、Na+和CH3COO-,由于反应体系是很稀的水溶液,可认为CH3COONa是全部电离的,因此,反应前后Na+的浓度不变,随着反应的进行,仅仅是导电能力很强的OH-离子逐渐被导电能力弱的CH3COO-离子所取代,致使溶液的电导逐渐减小,因此可用电导率仪测量皂化反应进程中电导率随时间的变化,从而达到跟踪反应物浓度随时间变化的目的。 令G0为t=0时溶液的电导,G t为时间t时混合溶液的电导,G∞为t=∞(反应完毕)时溶液的电导。则稀溶液中,电导值的减少量与CH3COO-浓度成正比,设K为比例常数,则 由此可得 所以(2)式中的a-x和x可以用溶液相应的电导表示,将其代入(2)式得:
(整理)实验八十二电导法测定乙酸乙酯皂化反应的速率常数题目.
实验八十二 电导法测定乙酸乙酯皂化反应的速率常数 一、预习提问 1、简述电导法测定乙酸乙酯皂化反应的速率常数的实验原理。 答:乙酸乙酯皂化反应是一个二级反应,其反应式为: CH 3COOC 2H 5 +Na + + OH - → CH 3COO - + Na + +C 2H 5OH 随着反应的进行,OH -离子浓度减低,使得溶液的电导率逐渐减少。故用电导率法测定反应速率。 2、书上要测的是溶液的电导值,而我们测定的是溶液的电导率值,对结果有无影响? 答:没有影响,该实验是以()()0t t κκκκ∞--对t 作图 ,而电导池常数被约去,对())0t t κκκκ∞--没有影响。 3、实验中,初始浓度过大或过小,对实验有何影响? 答:初始浓度过大,离子就不能完全电离,不能以() ckt t t =--∞κκκκ0作图。 初始浓度过小,则电导率变化太小影响准确度。 4、可否将NaOH 溶液稀释一倍后测得的电导率值作为皂化反应的初始电导率?为什么? 答:可以,乙酸乙酯不具有明显的电导率。 5、如何测得乙酸乙酯皂化反应的活化能? 答:测定不同温度下的反应速率常数k 1,k 2 。根据阿仑尼乌斯(Arrhenius)公式
ln ()k k Ea R T T 212111=--来计算Ea 的值 计算得到。 二、书后思考题 1.反应分子数与反应级数是两个完全不同的概念,反应级数只能通过实验来确定。试问如何从实验结果来验证乙酸乙酯皂化反应为二级反应 ? 2.乙酸乙酯的皂化反应为吸热反应,试问在实验过程中如何处置这一影响而是使实验得到较好的结果? 答:采用稀溶液控制反应速率,并适当搅拌。 3.如果和溶液均为浓溶液,试问能否用此方法求得K 值?为什么? 答:不能。因为影响因素太多,在浓的溶液中不可认为CH 3COONa 全部电离,该反应的逆反应不能忽略,此时不可以认为体系电导率值的减少与CH 3COONa 的浓度x 的增加量成正比。 4.为什么两溶液混合一半是就开始计时? 答:因为溶液要尽快混合,而且反应速率较快,电导率也下降较快,所以加入一半时,就开始计时。
乙酸乙酯皂化反应
乙酸乙酯皂化反应 一、实验目的 1. 用电导法测定乙酸乙酯皂化反应的反应级数、速率常数和活化能 2. 通过实验掌握测量原理和电导率一的使用方法 二、实验原理 1. 乙酸乙酯皂化反应为典型的二级反应,其反应式为: CH3COOC2H5+NaOH→CH3COONa+C2H5OH A B C D 当C A,0=C B,0其速率方程为: -dC A/dt=kC A2 积分得: 由实验测得不同时间t时的C A 值,以1/C A 对t作图,得一直线,从直线斜率便可求出K的值。 2. 反应物浓度CA的分析 不同时间下反应物浓度C A可用化学分析发确定,也可用物理化学分析法确定,本实验采用电导率法测定。 对稀溶液,每种强电解质的电导率与其浓度成正比,对于乙酸乙酯皂化反应来说,溶液的电导率是反应物NaoH与产物CH3CooNa两种电解质的贡献: 式中:Gt—t时刻溶液的电导率;A1,A2—分别为两电解质的电导率与浓度关系的比例系数。反应开始时溶液电导率全由NaOH贡献,反应完毕时全由CH3COONa贡献,因此 代入动力学积分式中得: 由上式可知,以Gt对 作图可得一直线,其斜率等于 ,由此可求得反应速率常数k。
3. 变化皂化反应温度,根据阿雷尼乌斯公式: ,求出该反应的活化能Ea。 三、实验步骤 1. 恒温水浴调至20℃。 2. 反应物溶液的配置: 将盛有实验用乙酸乙酯的磨口三角瓶置入恒温水浴中,恒温10分钟。用带有刻度的移液管吸取V/ml乙酸乙酯,移入预先放有一定量蒸馏水的100毫升容量瓶中,再加蒸馏水稀释至刻度,所吸取乙酸乙酯的体积 V/ml可用下式计算: 式子:M =88.11, =0.9005, 和NaOH见所用药品标签。 3. G0的测定: (1)在一烘干洁净的大试管内,用移液管移入电导水和NaOH溶液(新配置)各15ml,摇匀并插入附有橡皮擦的260型电导电极(插入前应用蒸馏水淋洗,并用滤纸小心吸干,要特别注意切勿触及两电极的铂黑)赛还塞子,将其置入恒温槽中恒温。 (2)开启DDSJ-308A型电导仪电源开关,按下"ON/OFF"键,仪器将显示产标、仪器型号、名称。按“模式”键选择“电导率测量”状态,仪器自动进入上次关机时的测量工作状态,此时仪器采用的参数已设好,可直接进行测量,待样品恒温10分钟后,记录仪器显示的电导率值。 (3)将电导电极取出,用蒸馏水林洗干净后插入盛有蒸馏水的烧杯中,大试管中的溶液保留待用。 4. Gt的测定; (1)取烘干洁净的混合反应器一支,其粗管中用移液管移入15ml新鲜配置的乙酸乙酯溶液,插入已经用蒸馏水淋洗并用滤纸小心吸干(注意:滤纸切勿触及两级的铂黑)带有橡皮塞的电导电极,用另一只移液管于细管移入15ml已知浓度的NaOH溶液,然后将其置于20摄氏度的恒温槽中恒温。 注意:氢氧化钠和乙酸乙酯两种溶液此时不能混合。
11乙酸乙酯皂化反应试题
实验十一乙酸乙酯皂化反应 第一题、填空题 1. 乙酸乙酯溶液应在使用前现配,目的是____________________________。 2. 乙酸乙酯皂化反应中,我们将酯加入到NaOH溶液中,而不是反过来操作,目的是__________________________________________。 3. 二级反应的速度常数有K=1/t(a-b)lnb(a-x)/a(b-x)和K=X/a(a-x)·1/t二种形式,条 件分别为__________________________和______________________________。 4.乙酸乙酯皂化反应,K(G0--G t )可表示________________________________。 5.乙酸乙酯皂化反应中,给出了________________________,测定_________________,用_________________与______________________作图处理,求得反应速度常数。 6. 测定乙酸乙酯皂化反应中的实验用水应为。 7. 常时间放置的去离子水内含有。 8. 测量溶液电导值时,须对其恒温,因为____________________,若温度升高,则电导 值_____________________。 9.乙酸乙酯皂化反应中,以K t对(K0 -K t )/t作图,初期点偏离直线的原因是_________________或__________________所致。 10.电导池常数是法得到的。向电导池内加入溶液的量定量加入,因为 11. 电导测量时须使用____电源,目的是防止____________________。 12.电导法测HAc电离常数时,测量KCI溶液电导的目的是_____________________。 13.电导池常数是____________________________法得到的。 14. 若将15℃下配制的饱和硫酸钡溶液用电导法测其25℃时的Ksp,其结果必然 _________理论值。 15. 电导电极上镀有一层铂黑目的是__________________________________,防止__________________________。 16. 电导测量时,若采用直流电将_________________,若采用低频交流电,会使电极__________。 第二题、选择题 1.若将氢氧化钠加入到乙酸乙酯中一半时作为反应起点,不考虑酯的挥发,对所测结果: 有正误差;有负误差;
乙酸的酯化反应教学设计
乙酸的酯化反应教学 设计 Revised on November 25, 2020
乙酸的酯化反应教学设计 一、教材分析 乙酸是第三章第三节“生活中两种常见的有机物”其中的一种,是典型的烃的衍生物。在学生对乙酸初步认识基础上,帮助学生打好进一步学习的方法论基础,同时鼓励学生用学习到的知识解释常见有机物的性质。 酯化反应是高中有机化学中的重要知识点之一,通过对乙酸的酯化反应这一实验的完成,系统的呈现出有机物制备的基本思路、基本方法及基本技能,使学生不断对固有的思维及实验装置产生质疑,在质疑中进行探究,对化学实验的思路及装置持续进行改进,从而优化出一套理念先进的实验体系。同时,通过这一内容的学习,也有利于学生思维能力和学科素养的提高。 二、学情分析 在初中化学中,学生对乙酸已有了初步的认识与了解。学生在学习这一节课之前,已经学习了乙醇的知识以及乙酸的结构和物理性质及乙酸的酸性,初步掌握了学习有机物及其性质的方法。在以上两点的教学基础上,学生通过预习听讲基本掌握本节课的知识,并通过课后习题练习进行能力的进一步提高。而且,在乙醇的内容学习过程中,学生已接触过物质的结构、性质和用途的科学关系,在此节课上学生可继续加以应用。三、教学目标1、知识与技能目标(1)掌握乙酸的酯化反应的化学方程式,理解酯化反应的概念。 (2)从结构的角度初步认识乙酸与乙醇的酯化反应(3) 了解酯化反应在生活中的应用,能结合相关知识解释。
2、过程与方法目标(1)通过操作乙酸的酯化反应实验,提高学生实验观察、实验现象准确描述、分析的能力。(2)培养学生对知识的分析归纳、总结的思维能力与表达能力。 (3)培养学生提出问题、解决问题的能力。 3、情感态度价值观(1)通过实验的分组与探究,激发学生学习的兴趣和求知欲望。(2)通过学习乙酸在生活中的应用,培养联系生活的意识,赞赏化学对人类生活的贡献。四、教学内容(1)通过分组实验的过程与结果,讲解本节课内容,乙酸与乙醇的酯化反应,并解答疑问分析反应方程式,探究酯化反应反应机理。 (2)以科学性为原则,对实验装置进行改进。 (3)本节课的小结。五、重点难点(1)教学重点:乙酸的酯化反应。 (2)教学难点:酯化反应的实质。 六、教学方法策略 本节课总体上从生活实际入手,引导学生进行思考分析,深入学习知识点,最后再回到生活的实际应用中。具体使用了一下教学策略:情境创设法:引导学生去闻摆在面前水果的香味。 (1)问题引入法:通过“水果的香味”的问题引入到本节的学习内容。通过比较贴近生活的问题引入到比较枯燥的重难点内容,可以激发学生的学习兴趣,增加知识的可接受程度。 分组实验法:①通过分组实验可以激发学生的学习兴趣和对这个知识点的好奇心,同时亲自动手,使学生感悟实验中必须遵守的原则与细节。②从学生观察实验现象入手,引导学生分析产生现象的因果关系和本质联系,从而了解学习
乙酸乙酯皂化反应速率常数测定
乙酸乙酯皂化反应速率系数测定 :腾 学号:2012011864 班级:化21 同组人:田雨禾 实验日期:2014年10月23日 提交报告日期:2014年10月30日 指导教师: 麻英 1 引言 1.1 实验目的 (1)学习测定化学反应动力学参数的一种物理化学分析方法——电导法。 (2)了解二级反应的特点,学习反应动力学参数的求解方法,加深理解反应动力学特征。 (3)进一步认识电导测定的应用,熟练掌握电导率仪的使用方法。 1.2 实验原理 反应速率与反应物浓度的二次方成正比的反应为二级反应,其速率方程式可以表示为 22dc -=k c dt (1) 将(1)积分可得动力学方程: c t 22c 0dc - =k dt c ? ? (2) 20 11 -=k t c c (3) 式中: 为反应物的初始浓度;c 为t 时刻反应物的浓度; 为二级反应的反应速率常数。 将1/c 对t 作图应得到一条直线,直线的斜率即为 。 对于大多数反应,反应速率与温度的关系可以用阿累经验方程式来表示: a E ln k=lnA-RT (4) 式中: 乌斯活化能或反应活化能;A 指前因子;k 为速率常数。 实验中若测得两个不同温度下的速率常数,就很容易得到 21 T a 21T 12k E T -T ln = k R T T ?? ??? (5) 由(5)就可以求出活化能。
乙酸乙酯皂化反应是一个典型的二级反应, 325325CH COOC H +NaOH CH COONa+C H OH → t=0时, 0c 0c 0 0 t=t 时, 0c -x 0c -x x x t=∞时, 0 0 0x c → 0x c → 设在时间t 生成物的浓度为x ,则反应的动力学方程为 220dx =k (c -x)dt (6) 2001x k = t c (c -x) (7) 本实验使用电导法测量皂化反应进程中电导率随时间的变化。设 、 和 分别代表时间为0、t 和∞(反应完毕)时溶液的电导率,则在稀溶液中有: 010=A c κ 20=A c κ∞ t 102=A (c -x)+A x κ 式中A 1和A 2是与温度、溶剂和电解质的性质有关的比例常数,由上面的三式可得 0t 00-x= -c -κκκκ∞ (8) 将(8)式代入(7)式得:
1乙酸乙酯皂化反应试题
实验一乙酸乙酯皂化反应 简答题 1.在乙酸乙酯皂化反应中,为什么所配NaOH和乙酸乙酯必须是稀溶液? 2.为何乙酸乙酯皂化反应实验要在恒温条件下进行,且氢氧化钠和乙酸乙酯溶液在混合前 还要预先恒温? 3.电导xx常数如何校正? 4.为什么乙酸乙酯皂化反应可用电导结果测其不同时刻的浓度变化?测定时对反应液 的浓度有什么要求?为什么? 5.在乙酸乙酯皂化反应中,若反应起始时间计时不准,对反应速度常数K有何影响?为什么? 6.乙酸乙脂皂化反应中,反应起始时间必须是绝对时间吗?为什么? 7.对乙酸乙酯皂化反应,当a=b时,有x=K(G 0-G t ),c=K(G 0-G ∞)。若[NaOH]≠[酯]时应怎样计算x和c值? 8.某人使用电导率仪时,为快而保险起见老在最大量程处测定,这样做行吗?为什么?测量 水的电导率时,能否选用仪器上ms.cm-1量程来测量,为什么?
9.电导率测量中,由于恒温槽性能不佳,温度逐渐升高,由此导致不同浓度时的K c 值将发生什么变化? 10.在乙酸乙酯造化反应实验过程中,我们先校正电极常数,后测定水以及溶液的电导率,请叙述原因、操作过程以及目的? 11.在乙酸乙酯皀化实验中为什么由 0.0100mol·dm-3的NaOH溶液测得的电导率可以认为是κ 0? 12.在乙酸乙酯皀化实验中为什么由 0.0100mol·dm-3的CH 3COONa溶液测得的电导率可以认为是κ ∞? 13.在乙酸乙酯皀化实验中如果NaOH和乙酸乙酯溶液为浓溶液时,能否用此法求k值,为什么? 14.乙酸乙酯皂化反应实验中,乙酸乙酯溶液应在使用前现配,目的是什么? 15.乙酸乙酯皂化反应实验中,反应体系的电导率随温度变化情况如何? 16.在乙酸乙酯皀化实验中铂电极的电极常数是如何确定的? 17、在乙酸乙酯皀化实验中电导率仪面板上温度补偿旋钮有何用途?怎样使用? 18.乙酸乙酯皂化反应是通过利用测定反应体系在不同时刻的电导或者电导率来跟踪产物和反应物浓度的变化,试问,溶液的电导或者电导率和反应物或者产物的浓度之间是什么样的关系?
物理化学实验报告-乙酸乙酯皂化反应动力学
乙酸乙酯皂化反应动力学 一、实验目的 1)了解二级反应的特点。 2)用电导法测定乙酸乙酯皂化反应的速率常数。 3)由不同温度下的速率常数求反应的活化能。 二、实验原理 乙酸乙酯在碱性水溶液中的消解反应即皂化反应,其反应式为: +→+ 反应式是二级反应,反应速率与及的浓度成正比。用分别表示乙酸乙酯和氢氧化钠的初始浓度,表示在时间间隔内反应了的乙酸乙酯或氢 氧化钠的浓度。反应速率为: 为反应速率常数,当时,上式为: 反应开始时,反应物的浓度为,积分上式得: 在一定温度下,由实验测得不同时的值,由上式可计算出值。 改变实验温度,求得不同温度下的值,根据Arrhenius方程的不定积分式有:
以对作图,得一条直线,从直线斜率可求得。 若求得热力学温度时的反应速率常数,也可由Arrhenius方程的定积分式变化为下式求得值: 本实验通过测量溶液的电导率代替测量生成物浓度(或反应物浓度)。乙酸乙酯、乙醇是非电解质。在稀溶液中,非电解质电导率与浓度成正比,溶液的电导率是各离子电导之和。反应前后离子浓度不变,整个反应过程电导率的变化取决于与浓度的变化,溶液中的导电能力约为的五倍,随着反应的进行,浓度降低,的尝试升高,溶液导电能力明显下降。 一定温度下,在稀溶液中反应,为溶液在时的电导率,分别是与、电导率有关的比例常数,于是: ,; ,; ,; 由此得 即
即 而即 上式变形为: 以对作图为一直线,斜率为,由此可求出。三、仪器和试剂 恒温槽、电导率仪、电导电极、叉形电导池、秒表、碱式滴定管、10ml、25m移液 管、100mL,50ml容量瓶、乙酸乙酯(A.R.)、氢氧化钠溶液(0.04mol·) 四、实验步骤 1.准备溶液: 1)打开恒温槽,设置温度为25℃。将叉形电导池洗净、烘干。同时清洗两个100ml、一个50ml的容量瓶;
实验六酯化反应(乙酸乙酯)
实验六酯化反应—乙酸乙酯的制备 一、酯化反应原理、方法、注意事项 1、原理 羧酸与醇在酸的催化下作用生成酯和水的反应叫做酯化反应。 CH3COOH + CH3CH2OH CH3COOCH2CH3 + H2O H2SO4 酯化为一可逆反应,升高温度与使用催化剂可加速反应达到动态平衡。当平衡达到后,酯的生成量就不再增多。为了提高产量,可以根据质量作用定律,增加反应物的浓度,或除去生成物以破坏平衡,使平衡向右进行。 本实验以浓硫酸作催化剂,加速达到平衡,使用过量醋酸,并用分水装置,不断移去反应过程中生成的乙酸乙酯和水,使反应完全 2、实验方法 用下列装置图进行实验 图14 乙酸乙酯合成实验装置 3、注意事项 (1)酸的用量为醇的用量的3% 时即能起催化作用。当硫酸用量较多时,由于它同时又能起脱水作用而增加酯的产率。但硫酸用量过多时,由于高温时氧化作用的结果对反应反而不利。 (2)用油浴加热时,油浴的温度约在135℃左右。如果不采用油浴,也可改用在电热套上接
加热的方法,但反应液的温度必须控制在不超过120℃的范围,否则将增加副产物乙醚的量。 二、实验——乙酸乙酯的制备 (一)实验目的 了解从有机酸合成酯的一般原理及方法;熟练掌握蒸馏、分液漏斗的使用等操作。(二)实验原理 同上 (三)药品和仪器 1、仪器 125ml三颈烧瓶150℃温度计150ml分液漏斗直型冷凝管接收管50ml锥形瓶电热套。 2、药品 95%乙醇冰醋酸浓硫酸饱和碳酸钠溶液饱和食盐水饱和氯化钙溶液无水硫酸钠pH试纸 (四)实验步骤 按图14装置进行实验。在100毫升三颈瓶中放入10毫升乙醇,在用冷水冷却的同时,一边振摇一边分批加入10毫升浓硫酸,使混合均匀,加入几粒沸石,在烧瓶两侧的两口分别插入温度计和60毫升滴液漏斗(其中已经分别加入10毫升95 % 乙醇和10毫升醋酸并混合均匀),温度计的水银球必须浸入液面以下距离瓶底0.5~1厘米处,烧瓶的中间一口装一根与直型冷凝管相连接的蒸馏头,直型冷凝管通过一接引管与三角瓶相通。 将反应瓶在油浴上加热,当反应液温度升到110~120℃时,开始通过滴液漏斗滴加混合液,控制滴加速度与蒸出液体的速度尽可能等同,并始终维持反应液温度在110~120℃之间,滴加完毕后继续加热数分钟,直到反应液温度升高到130℃时不再有液体馏出为止。 在馏出液中慢慢加入饱和碳酸钠溶液,边加边摇,直至不再有二氧化碳气体产生,然后将混合液移入分液漏斗,分去下层水溶液,酯层用6毫升/次饱和食盐水洗涤2~3次,再用饱和氯化钙溶液20毫升分两次洗涤。最后分去下层液体,酯层自漏斗上口倒入一干燥的三角烧瓶中,用无水硫酸钠干燥。 将干燥后的酯层进行蒸馏,收集73~78℃的馏分,产率在60%左右。
实验六 乙酸乙酯皂化反应
实验六 乙酸乙酯皂化反应 【目的要求】 1. 用电导率仪测定乙酸乙酯皂化反应进程中的电导率。 2. 学会用图解法求二级反应的速率常数,并计算该反应的活化能。 3. 学会使用电导率仪和恒温水浴。 【实验原理】 乙酸乙酯皂化反应是个二级反应,其反应方程式为: CH 3COOC 2H 5 +Na ++ OH - → CH 3COO - + Na ++C 2H 5OH 当乙酸乙酯与氢氧化钠溶液的起始浓度相同时,如均为a ,则反应速率表示为 2)(d d x a k t x -= (1) 式中,x 为时间t 时反应物消耗掉的浓度,k 为反应速率常数。将上式积分得 kt x a a x =-) ( (2) 起始浓度a 为已知,因此只要由实验测得不同时间t 时的x 值,以x /(a -x )对t 作图,若所得为一直线,证明是二级反应,并可以从直线的斜率求出k 值。 乙酸乙酯皂化反应中,参加导电的离子有OH -、Na +和CH 3COO -,由于反应体系是很稀的水溶液,可认为CH 3COONa 是全部电离的,因此,反应前后Na +的浓度不变,随着反应的进行,仅仅是导电能力很强的OH -离子逐渐被导电能力弱的CH 3COO -离子所取代,致使溶液的电导逐渐减小,因此可用电导率仪测量皂化反应进程中电导率随时间的变化,从而达到跟踪反应物浓度随时间变化的目的。 令G 0为t =0时溶液的电导,G t 为时间t 时混合溶液的电导,G ∞为t = ∞(反应完毕)时溶液的电导。则稀溶液中,电导值的减少量与CH 3COO -浓度成正比,设K 为比例常数,则 t =t 时, x =x , x =K (G 0-G t ) t = ∞时, x →a , a =K (G 0-G ∞) 由此可得: a -x =K (G t -G ∞) 所以a -x 和x 可以用溶液相应的电导表示,将其代入(2)式得: kt G G G G a t t =--∞ 01 重新排列得: ∞+-?=G t G G ak G t t 01 (3)
实验七 乙酸乙酯皂化反应速率常数的测定
实验七乙酸乙酯皂化反应速率常数得测定 [日期:2008—06 来源:作者: [字体:大中小]-18] 乙酸乙酯皂化反应速率常数得测定 一、目得及要求 1、测定皂化反应中电导得变化,计算反应速率常数。 2、了解二级反应得特点,学会用图解法求二级反应得速率常数。 3、熟悉电导率仪得使用。 二、原理 乙酸乙酯得皂化反应为二级反应: CH3COOC2H5+NaOH=CH3COONa+C2H5OH 在这个实验中,将CH3COOC2H5与NaOH采用相同得浓度,设a为起始浓度,同时设反 应时间为t时,反应所生成得CH3COONa与C2H5OH得浓度为x,那么CH3COOC2H5与NaO H得浓度为(a—x),即 CH3COOC2H5+NaOH=CH3COONa+ C2H5OH t=0时,a a 0 0 t=t时, a-xa-x x x t→∞时,0 0 a a 其反应速度得表达式为: dx/dt=k(a-x)2 k—反应速率常数,将上式积分,可得 kt=x/[a(a—x)]* 乙酸乙酯皂化反应得全部过程就是在稀溶液中进行得,可以认为生成得CH3COONa就 是全部电离得,因此对体系电导值有影响得有Na+、OH-与CH3COO—,而Na+、在反应得过 程中浓度保持不变,因此其电导值不发生改变,可以不考虑,而OH—得减少量与CH3COO-得 增加量又恰好相等,又因为OH—得导电能力要大于CH3COO-得导电能力,所以体系得电导 值随着反应得进行就是减少得,并且减少得量与CH3COO-得浓度成正比,设L0—反应开始 时体系得电导值,L∞-反应完全结束时体系得电导值,L t-反应时间为t时体系得电导值,则有 t=t时,x=k’(L0-L t) t→∞时,a=k’(L0—L∞) k'为比例系数。 代入*式得 Lt=1/ka×[(L0-Lt)/t]+L∞
实验六酯化反应(乙酸乙酯)
实验六 酯化反应—乙酸乙酯的制备 一、酯化反应原理、方法、注意事项 1、原理 羧酸与醇在酸的催化下作用生成酯和水的反应叫做酯化反应。 CH 3COOH + CH 3CH 2OH CH 3COOCH 2CH 3 + H 2O 24 酯化为一可逆反应,升高温度与使用催化剂可加速反应达到动态平衡。当平衡达到后,酯的生成量就不再增多。为了提高产量,可以根据质量作用定律,增加反应物的浓度,或除去生成物以破坏平衡,使平衡向右进行。 本实验以浓硫酸作催化剂,加速达到平衡,使用过量醋酸,并用分水装置,不断移去反应过程中生成的乙酸乙酯和水,使反应完全 2、实验方法 用下列装置图进行实验 图14 乙酸乙酯合成实验装置 3、注意事项 (1)酸的用量为醇的用量的3% 时即能起催化作用。当硫酸用量较多时,由于它同时又能起脱水作用而增加酯的产率。但硫酸用量过多时,由于高温时氧化作用的结果对反应反而不利。 (2)用油浴加热时,油浴的温度约在135℃左右。如果不采用油浴,也可改用在电热套上接加热的方法,但反应液的温度必须控制在不超过120℃的范围,否则将增加副产物乙醚的量。
二、实验——乙酸乙酯的制备 (一)实验目的 了解从有机酸合成酯的一般原理及方法;熟练掌握蒸馏、分液漏斗的使用等操作。(二)实验原理 同上 (三)药品和仪器 1、仪器 125ml三颈烧瓶150℃温度计150ml分液漏斗直型冷凝管接收管50ml锥形瓶电热套。 2、药品 95%乙醇冰醋酸浓硫酸饱和碳酸钠溶液饱和食盐水饱和氯化钙溶液无水硫酸钠pH试纸 (四)实验步骤 按图14装置进行实验。在100毫升三颈瓶中放入10毫升乙醇,在用冷水冷却的同时,一边振摇一边分批加入10毫升浓硫酸,使混合均匀,加入几粒沸石,在烧瓶两侧的两口分别插入温度计和60毫升滴液漏斗(其中已经分别加入10毫升95 % 乙醇和10毫升醋酸并混合均匀),温度计的水银球必须浸入液面以下距离瓶底0.5~1厘米处,烧瓶的中间一口装一根与直型冷凝管相连接的蒸馏头,直型冷凝管通过一接引管与三角瓶相通。 将反应瓶在油浴上加热,当反应液温度升到110~120℃时,开始通过滴液漏斗滴加混合液,控制滴加速度与蒸出液体的速度尽可能等同,并始终维持反应液温度在110~120℃之间,滴加完毕后继续加热数分钟,直到反应液温度升高到130℃时不再有液体馏出为止。 在馏出液中慢慢加入饱和碳酸钠溶液,边加边摇,直至不再有二氧化碳气体产生,然后将混合液移入分液漏斗,分去下层水溶液,酯层用6毫升/次饱和食盐水洗涤2~3次,再用饱和氯化钙溶液20毫升分两次洗涤。最后分去下层液体,酯层自漏斗上口倒入一干燥的三角烧瓶中,用无水硫酸钠干燥。 将干燥后的酯层进行蒸馏,收集73~78℃的馏分,产率在60%左右。 纯乙酸乙酯为无色而有香味的液体,沸点为77.06℃,折光率为1.3723。 (五)注意事项 1、若滴加速度太快则乙醇和乙酸可能来不及完全反应就随着酯和水一起蒸出,从而影响酯的收率。 2、在馏出液中除了酯和水外,还含有未反应的少量乙醇和乙酸,也还有副产物乙醚。
实验十 二级反应乙酸乙酯皂化反应
实验十 二级反应乙酸乙酯皂化反应 一、实验目的 1.了解二级反应的特点。 2.掌握电导率法测定反应速率常数和活化能。 二、实验原理 乙酸乙酯与碱的反应称为皂化反应,它是一个典型的二级反应。其反应式为: 325325C H C O O C H N aO H C H C O O N a C H O H +→+ 当两种反应物初始浓度相同时 0t =, 0C 0C 0 0 t t =, 0C x - 0C x - x x t =∞ , 0 0 0C 0C 设:两种反应物的起始浓度均为C 0,在时间t 时生成物的浓度为x ,则反应速率方程为: 2 0() dx k C x dt =- (1) 式中:k 为速率常数;t 为时间。 将(1)式积分得: 00() x k tC C x = - (2) 若以00() x C C x -对t 作图,可得一直线,由直线的斜率可求速率常数k 。但由 于难以测定t 时刻的x 值,故本实验采用电导率法测定皂化反应过程中的电导率。由电导率随时间的变化规律来代替浓度的变化。这主要是因为,随着皂化反应的进行,溶液中电导能力强的OH -离子逐渐被导电能力弱的Ac -离子所取代。使溶液的电导率逐渐减小,溶液中CH 3COOC 2H 5和C 2H 5OH 的导电能力都很小,可以忽略不计。因此,溶液电导率的变化是和反应物浓度变化相对应的。 在电解质稀溶液中,可近似认为电导率κ与浓度C 有如下的正比关系,并且溶液的电导率等于各电解质离子电导之和 m C κ=Λ 上式中Λm 为摩尔电导率,Λm 在恒定温度的稀溶液中,可近似看作为一常数,于是可写成κ=fC : 设:0t =, 溶液的电导率 0κ t t =, 溶液的电导率 t κ
