化学必修一知识网络图
混合物的分离与提纯
必修一
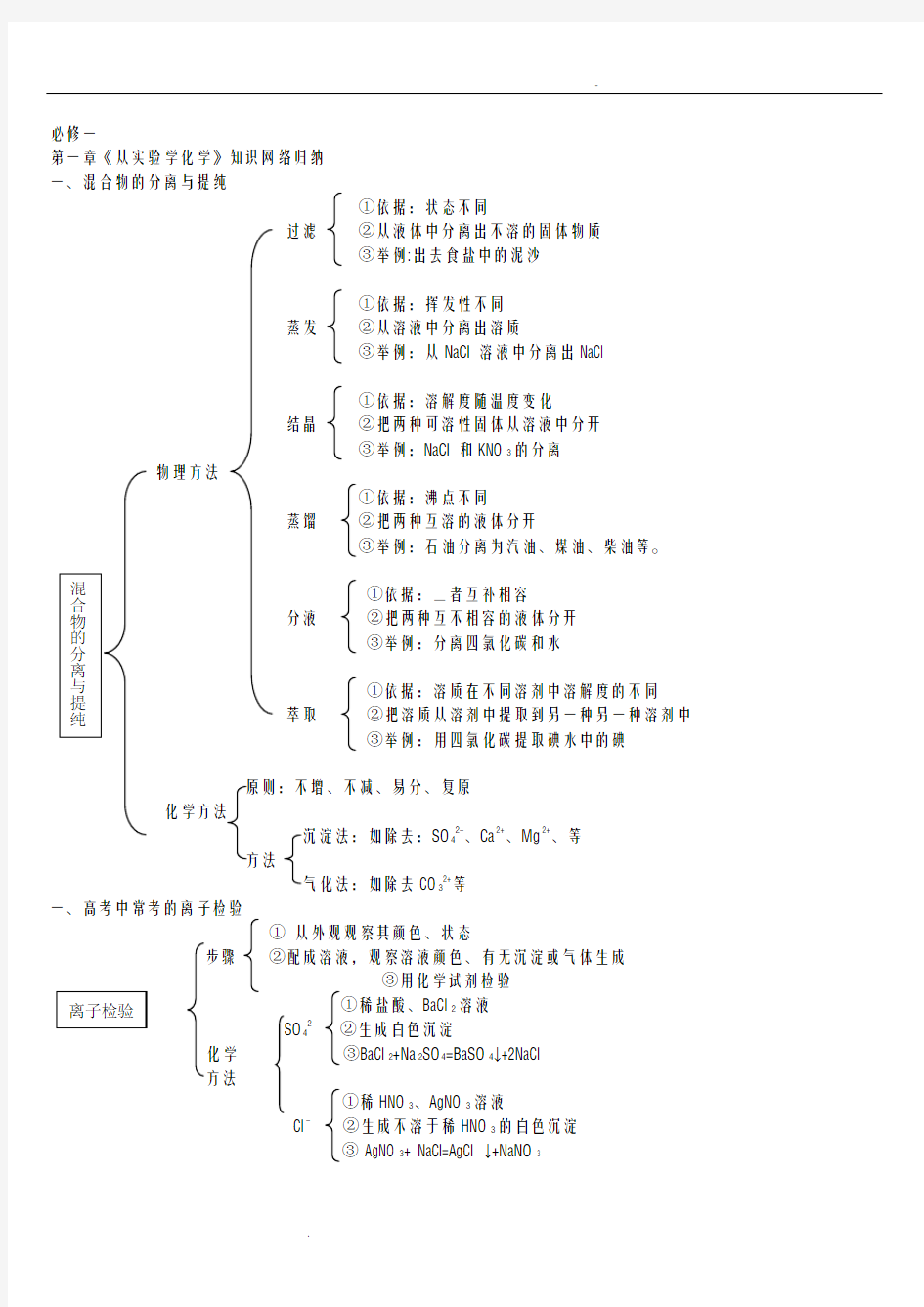
第一章《从实验学化学》知识网络归纳 一、混合物的分离与提纯
①依据:状态不同
过滤 ②从液体中分离出不溶的固体物质
③举例:出去食盐中的泥沙
①依据:挥发性不同
蒸发 ②从溶液中分离出溶质
③举例:从NaCl 溶液中分离出NaCl
①依据:溶解度随温度变化
结晶 ②把两种可溶性固体从溶液中分开
③举例:NaCl 和KNO 3的分离
物理方法
①依据:沸点不同
蒸馏 ②把两种互溶的液体分开
③举例:石油分离为汽油、煤油、柴油等。
①依据:二者互补相容
分液 ②把两种互不相容的液体分开
③举例:分离四氯化碳和水
①依据:溶质在不同溶剂中溶解度的不同
萃取 ②把溶质从溶剂中提取到另一种另一种溶剂中
③举例:用四氯化碳提取碘水中的碘
原则:不增、不减、易分、复原
化学方法
沉淀法:如除去:SO 42-、Ca 2+、Mg 2+
、等
方法
气化法:如除去CO 32+
等
一、高考中常考的离子检验
① 从外观观察其颜色、状态
步骤 ②配成溶液,观察溶液颜色、有无沉淀或气体生成
③用化学试剂检验
①稀盐酸、BaCl 2溶液 SO 42- ②生成白色沉淀
化学 ③BaCl 2+Na 2SO 4=BaSO 4↓+2NaCl 方法
①稀HNO 3、AgNO 3溶液
Cl - ②生成不溶于稀HNO 3的白色沉淀
③ AgNO 3+ NaCl=AgCl ↓+NaNO 3
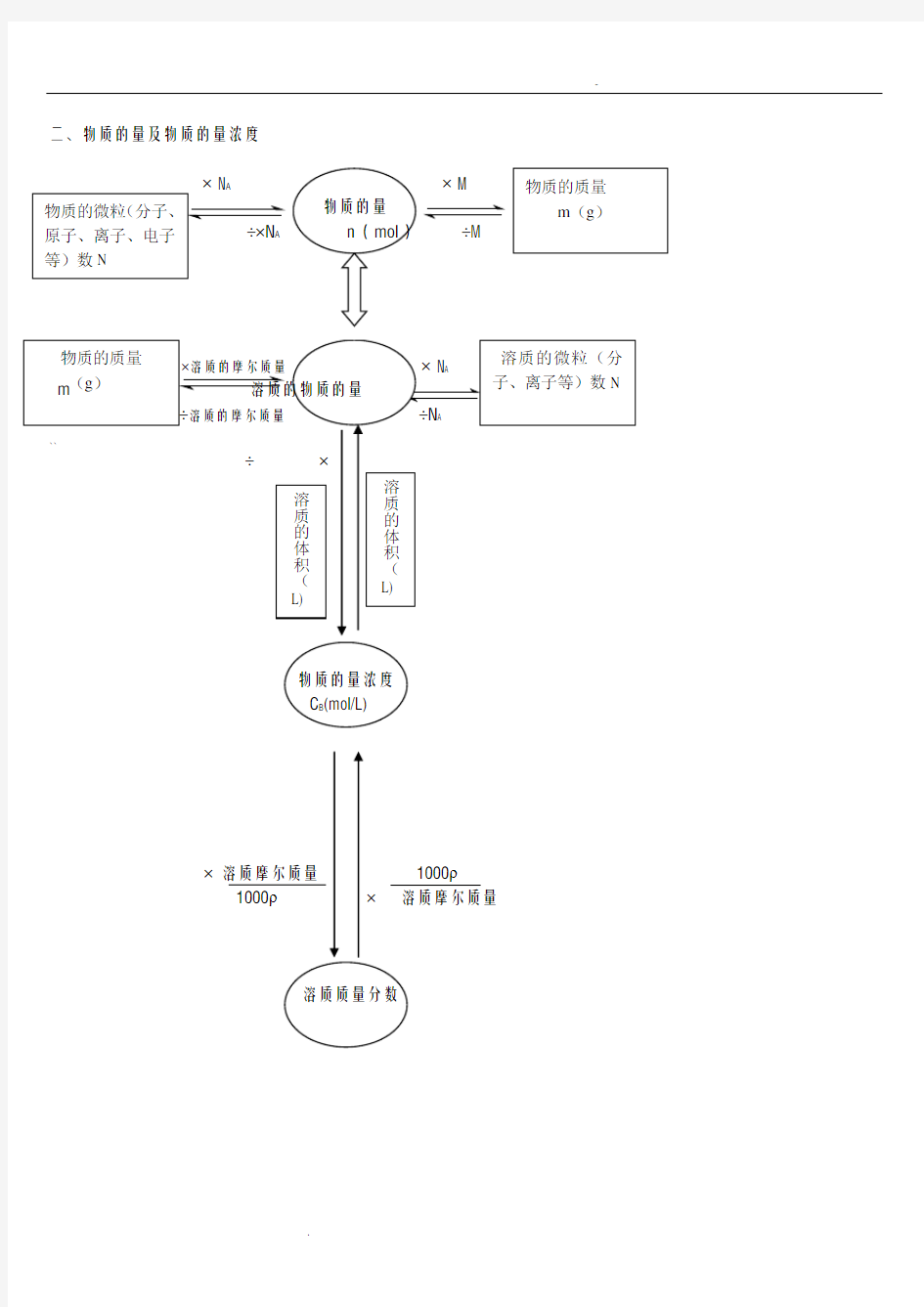
二、物质的量及物质的量浓度
× M
× 1000ρ × 溶质摩尔质量
第二章《化学物质及其分类》知识网络归纳
一、物质的分类。金属:Na、Mg、Al
单质
非金属:S、O、N
酸性氧化物:SO3、SO2、P2O5等
氧化物碱性氧化物:Na2O、CaO、Fe2O3
氧化物:Al2O3等
纯盐氧化物:CO、NO等
净含氧酸:HNO3、H2SO4等
物按酸根分
无氧酸:HCl
强酸:HNO3、H2SO4、HCl
酸按强弱分
弱酸:H2CO3、HClO、CH3COOH
化一元酸:HCl、HNO3
合按电离出的H+数分二元酸:H2SO4、H2SO3
物多元酸:H3PO4
强碱:NaOH、Ba(OH)2 物按强弱分
质弱碱:NH3·H2O、Fe(OH)3
碱
一元碱:NaOH、
按电离出的HO-数分二元碱:Ba(OH)2
多元碱:Fe(OH)3
正盐:Na2CO3
盐酸式盐:NaHCO3
碱式盐:Cu2(OH)2CO3
溶液:NaCl溶液、稀H2SO4等
混悬浊液:泥水混合物等
合乳浊液:油水混合物
物胶体:Fe(OH)3胶体、淀粉溶液、烟、雾、有色玻璃等
A+B AB
聚反应物和生成物类别分解反应:AB A+B
以及
反应前后物质种类的多少置换反应:A+BC B+AC
AB+CD AD+CB
实质:有电子转移(得失或偏移)
氧化特征:反应前后元素的化合价有变化
还原
根据反应概念氧化剂→有氧化性→得电子→化合价降低→发生还原反应→还原产物
反应及其反↓↓↓↓↓↓
中是相互应同时存在同时体现总数相等总数相等同时发生同时产生化否有关系物↓↓↓↓↓↓
学电子还原剂→有还原性→失电子→化合价升高→发生氧化反应→氧化产物反转移
应
非氧化还原反应
定义:有离子参加的一类反应反
发生条件(复分解类型):生成难容物质、难电离物质、挥发性物质
写:写出反应的化学方程式
离子反应拆:把易溶于水、易电离的物质拆成离子形式
书写
方法删:将不参加反应的离子从方程式两端删去
离子方程式查:查方程式两端原子个数和电荷数是否相等根据反应中是
否有离子参加表示一类化学反应
特点
分子反应
三、三类分散系的比较
第三章《金属及其化合物》知识网络归纳
一、部分金属与其重要化合物之间的转化关系。
1、钠及其重要化合物之间的转化关系
O2
Na2S NaOH C 2 NaCO3 NaHCO3
NaCl
熔融电解
2、铝及其化合物之间的转化关系
电解①
②
△
3
NaOH
3 3
H2O
KAl(SO4)2
3
Fe2O3 Fe 2Fe(OH)2Fe(OH)3Fe(SCN)3
O
Ca(OH)2
CO2、H2O
Ca(OH)2
S
二、金属的化学性质
常温下:Na +O 2 Na 2O 钠与氯气反应
加热时:2Na +O 2 Na 2O 2 铝与氧气反应:4Al +3O 2 2Al 2O 3 金属与氧气反应 镁与氧气反应:2Mg +O 2 2MgO
金属 铁与氧气反应:3Fe +2O 2 Fe 3O 4
的 钠与水反应:2Na +2H 2O 2NaOH +H 2↑
化学 常温下,铁与水不反应 性质 铁与水反应
金属 在高温下,铁跟水蒸气发生反应:3Fe +4H 2O(g) Fe 3O 4+4H 2 与水 与冷水反应缓慢
反应 镁与水反应
与沸水反应迅速:Mg +2H 2O Mg(OH)2↓+H 2↑
与冷水很难反应缓慢 铝与水反应
与沸水能发生反应:2Al +6H 2O(沸水) 2Al(OH)3↓+3H 2↑
三、几种重要的金属化合物
MgO 的制备、性质和用途 Al 2O 3的制备、性质和用途 氧化物 CuO 的制备、性质和用途 FeO 铁的氧化物 Fe 2O 3 Fe 3O 4
几 Fe(OH)2 的制备、性质和用途
种 铁的氢氧化物 Fe(OH)3 的制备、性质和用途 重 氢 Fe(OH)2与Fe(OH)3的相互转化 要 氧 物理性质:白色胶状物质,有吸附性
的 化 Al(OH)3 制备:Al 3++3NH 3·H 2O Al(OH)3↓+3NH 3+
金 物 化学性质:具有两性,受热分解 属 Mg(OH)2的制备和性质
化 溶解性 合 Na 2CO 3和NaHCO 3 热稳定性 物 用途
盐 硫酸铝钾(复盐):无色晶体,易溶于水,可做净水剂
亚铁盐:Fe 2+的检验,Fe 2+
的还原
铁盐和亚铁盐 铁盐: Fe 3+的检验,Fe 3+
的氧化
Fe 2+和Fe 2+
的转换
含义 焰色反应
操作方法:洗、烧、蘸、烧
点燃
点燃
点燃
点燃
高温
△
高温
第四章《非金属及其化合物》知识网络归纳 一、硅
性质:导电性介于导体和绝缘体之间 1、单质硅
用途:应用于制造晶体管、光电池、硅芯片等高科技产品的重要部件
存在:地球上存在的天然二氧化硅约占地壳质量的12%,其存在形态有结晶性和无定形两种 性质:不溶于水的固体;可跟强碱反应;易和氢氟酸反应,但不和一般的酸反应;
在高温条件下可得CaO 、CaCO 3、NaCO 3等
反应:有弱氧化性,在高温条件下可被碳还原 2、 用途 CaSiO 3
Si SiO 2 H 2SiO 3(或H 4SiO 4)
Na 2SiO 3
用途:既可用于制造玻璃、陶瓷等多种传统的无机非金属材料,又可用于制造压电材料、光导纤
维等多种个性非无机非金属材料
SiO 2+2NaOH Na 2SiO 3+H 2O
Na 2SiO 3 性质:可溶于水,水溶液呈碱性、有粘性、不燃烧 用途:用作肥皂填料、木材防火剂及胶黏剂等 3、硅酸盐
硅酸盐产品:玻璃、水泥、陶瓷、高温结构陶瓷、压电陶瓷、透明陶瓷、超导陶瓷等 二、氯
物理性质:黄绿色气体,密度大,较容易液化,有刺激性气味,有毒,能溶于水
Cl 2+H 2O HClO +HCl 与水反应
Cl 2应用于消毒和漂白 1、 氯气
2NaOH +Cl 2 NaCl +NaClO +H 2O NaOH
化 NaClO 应用于消毒剂和漂白剂
学 与碱反应
性 2Ca(OH)2+2HCl CaCl 2+Ca(ClO)2+H 2O 质 Ca(ClO)2
Ca(ClO)2应用于消毒剂和漂白剂
Na +Cl 2 2NaCl 与金属反应 Fe +Cl 2 FeCl 3
Cu +Cl2 C uCl2
离子方程式:Cl-+Ag+ AgCl ↓ 2、Cl-离子的检验
试剂:AgNO 3溶液和稀硝酸
点燃
点燃
点燃
三、硫及其化合物
物理性质:无色、有刺激性气体、有毒气体、易液化、易溶于水 ①品红 褪色恢复
②酸性氧化物
二氧化硫 化学性质
③可逆反应:SO 2+H 2O H 2O 3
④大气污染物:SO 2 SO 3 H 2SO 4,形成
硫 酸雨,酸雨Ph<5. 6 酸雨的形成及防治 稀H 2SO 4:酸的通行 脱水性
吸水性:干燥剂 硫酸 浓H 2SO 4
Cu +2H 2SO 4(浓) CuSO 4+2H 2O +SO 2↑ 强氧化性
用途 C +2H 2SO 4(浓)
CO 2↑+2H 2O +2SO 2↑ 四、氮及其化合物
存在:占空气体积的4/5
单质 N 2+O 2 2NO 无色有毒、不溶于水
性质 2NO +O 2 2NO 2红棕色、有毒、易溶于水、易液化 3NO +H 2O 2HNO 3+NO 形成酸雨 物理性质:无色、有刺激性气味、极易容易水
水:NH 3+H 2O NH 3·
H 2O NH 4++OH - 弱碱性 化学性质
酸:NH 3+HCl NH 4Cl
氨 原理:2NH 4Cl +Ca(OH)2 CaCl 2+2H 2O +2NH 3↑
氮 制法 装置:固+固 气
收集:向下排空气
检验:湿润的红色石蕊试纸
用途
物理性质:白色固体易溶于水
NH 4Cl NH 3↑+H 2O
铵盐 不稳定性
化学 NH 3HCO 3 NH 3↑+H 2O +CO 2↑
性质
与碱反应:NH 4NO 3+NaOH NaNO 3+H 2O +NH 3↑
Cu +4HNO 3(浓) Cu(ON 3)2+2NO 2↑+2H 2O 硝酸的强氧化性
3 Cu +8HNO 3(稀) 3Cu(ON 3)2+2NO ↑+4H 2O
SO 3
△
催化剂
O 2△
H 2O
△
△
△
△
△
△
△
