心房颤动抗凝治疗中国专家共识

心房颤动抗凝治疗中国专家共识
心房颤动(房颤)是最常见的心律失常之一。根据2004年所发表的数据,我国30岁至85岁居民中房颤患病率为0.77%,其中80岁以上人群中患病率达30%以上[1,2]。血栓栓塞性并发症是房颤致死致残的主要原因,而脑卒中则是最为常见的表现类型。在非瓣膜性房颤患者中,缺血性卒中的每年发生率(约5%)是非房颤患者的2~7倍[3-6]。预防卒中的新发与复发应成为房颤患者综合管理策略中的主要内容。越来越多的研究证实,对于发生卒中风险增高的患者,合理应用抗凝药物有助于显著降低缺血性卒中的发生率,然而在我国大多数房颤患者未得到抗凝治疗[1, 2]。
进一步增强对房颤及其并发症危害性的认识、加强血栓栓塞并发症(特别是卒中)的预防对于改善患者预后进而减轻与之相关的社会经济和家庭负担具有重要意义。目前已有多种口服抗凝药物应用于临床,如华法林、达比加群、利伐沙班、阿哌沙班等。为促进与规范房颤患者的抗凝治疗,降低缺血性卒中等血栓栓塞性并发症的发生率,中华医学会心血管病学分会、中华医学会心电生理和起搏分会、中国老年学学会心脑血管病专业委员会、中国生物医学工程学心律分会、中国医师协会循证医学专业委员会、与心律失常联盟(中国)组织国内专家制定了此专家共识。
1 房颤患者卒中和血栓栓塞的危险分层与抗凝治疗原则
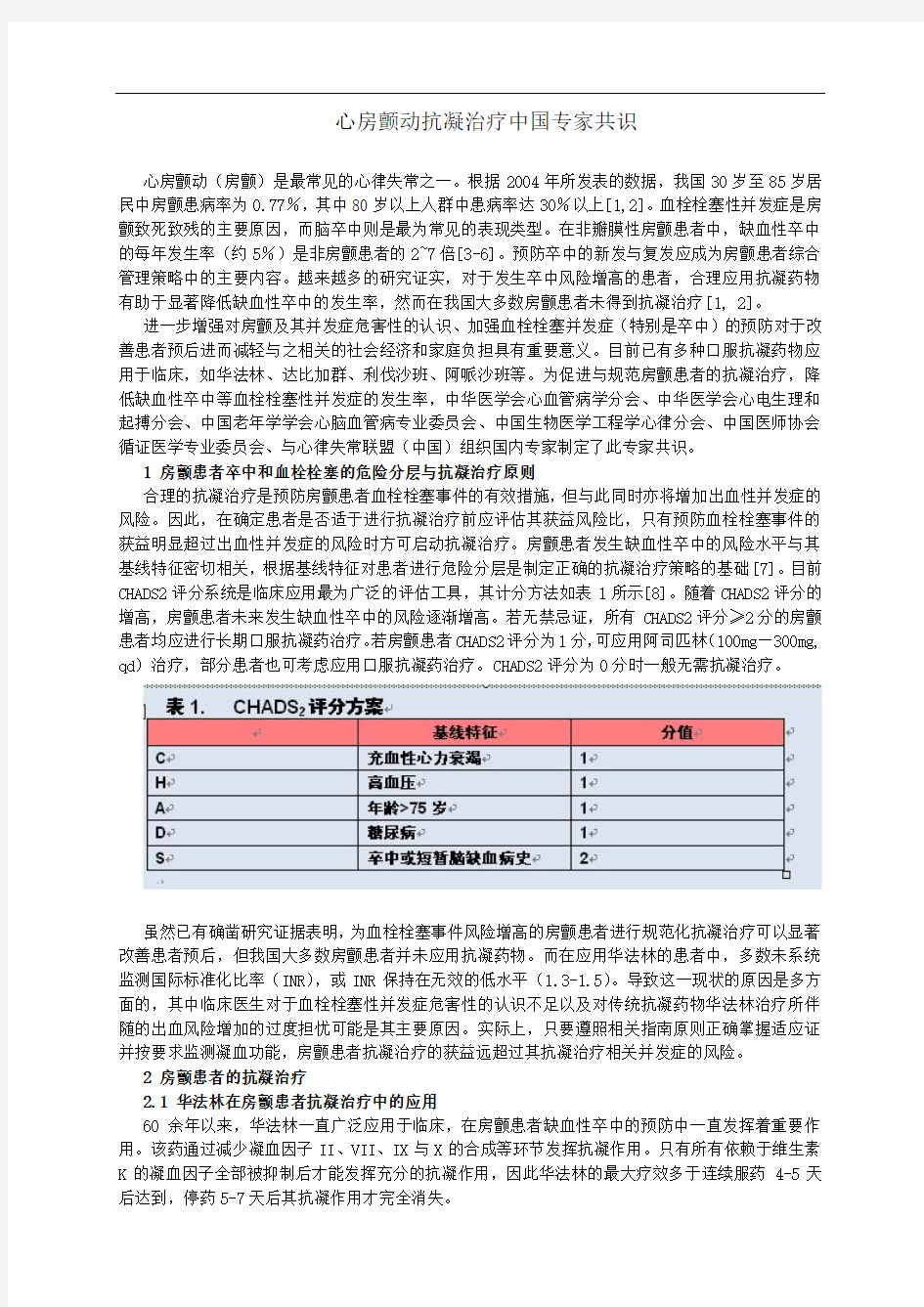
合理的抗凝治疗是预防房颤患者血栓栓塞事件的有效措施,但与此同时亦将增加出血性并发症的风险。因此,在确定患者是否适于进行抗凝治疗前应评估其获益风险比,只有预防血栓栓塞事件的获益明显超过出血性并发症的风险时方可启动抗凝治疗。房颤患者发生缺血性卒中的风险水平与其基线特征密切相关,根据基线特征对患者进行危险分层是制定正确的抗凝治疗策略的基础[7]。目前CHADS2评分系统是临床应用最为广泛的评估工具,其计分方法如表1所示[8]。随着CHADS2评分的增高,房颤患者未来发生缺血性卒中的风险逐渐增高。若无禁忌证,所有CHADS2评分≥2分的房颤患者均应进行长期口服抗凝药治疗。若房颤患者CHADS2评分为1分,可应用阿司匹林(100mg—300mg, qd)治疗,部分患者也可考虑应用口服抗凝药治疗。CHADS2评分为0分时一般无需抗凝治疗。
虽然已有确凿研究证据表明,为血栓栓塞事件风险增高的房颤患者进行规范化抗凝治疗可以显著改善患者预后,但我国大多数房颤患者并未应用抗凝药物。而在应用华法林的患者中,多数未系统监测国际标准化比率(INR),或INR保持在无效的低水平(1.3-1.5)。导致这一现状的原因是多方面的,其中临床医生对于血栓栓塞性并发症危害性的认识不足以及对传统抗凝药物华法林治疗所伴随的出血风险增加的过度担忧可能是其主要原因。实际上,只要遵照相关指南原则正确掌握适应证并按要求监测凝血功能,房颤患者抗凝治疗的获益远超过其抗凝治疗相关并发症的风险。
2 房颤患者的抗凝治疗
2.1 华法林在房颤患者抗凝治疗中的应用
60余年以来,华法林一直广泛应用于临床,在房颤患者缺血性卒中的预防中一直发挥着重要作用。该药通过减少凝血因子II、VII、IX与X的合成等环节发挥抗凝作用。只有所有依赖于维生素K的凝血因子全部被抑制后才能发挥充分的抗凝作用,因此华法林的最大疗效多于连续服药4-5天后达到,停药5-7天后其抗凝作用才完全消失。
2.1.1 研究证据
迄今已有多项随机化临床研究论证了华法林在房颤患者卒中一级预防与二级预防中的作用,结果显示在密切监测INR的情况下,为中高危房颤患者长期应用华法林治疗可以有效降低患者发生缺血性卒中的风险,其疗效显著优于安慰剂、阿司匹林、以及阿司匹林联合氯吡格雷[9-11]。对现有研究进行荟萃分析表明[12],华法林治疗可使房颤患者发生卒中的相对危险度降低64%,每年发生卒中的绝对风险降低2.7%。若仅计算缺血性卒中,应用剂量调整的华法林治疗可使其相对风险降低67%,且在预防卒中初发与复发时获益幅度相同。华法林治疗可使全因死亡率显著降低26%,而颅内出血发生率很低。这项荟萃分析同时发现,房颤患者应用华法林治疗过程中中断用药或抗凝强度不足可显著增高发生卒中的风险。
2.1.2 用药方法
虽然美国等指南推荐华法林的起始治疗剂量为5mg/d-10mg/d[13],但由于种族和体重差异,我国人群达到INR目标值所需的华法林剂量可能低于欧美国家患者,因此在应用华法林治疗时应从较低剂量(如1.5mg/d-3.0mg/d)开始。初始剂量治疗INR不达标时,可按照1.0mg/d-1.5mg/d的幅度逐渐递增并连续检测INR,直至其达到目标值。特殊人群(如老年人、体质虚弱、营养不良、心力衰竭、肝脏疾病、近期曾进行手术治疗、或正在服用可增强华法林作用的药物者)应从更低剂量(如<1.5mg/d)开始用药。
在应用华法林治疗过程中,应定期监测INR并据此调整华法林剂量,将INR控制在2.0-3.0之间。虽然上述INR的目标值主要来自于欧美国家的临床研究结果,但目前并无证据显示中国患者需要采用较低的INR目标值。若INR不达到上述范围,可能会因抗凝作用不足而不能有效的预防血栓栓塞事件。一些学者认为老年患者应用华法林治疗时宜采用较低的INR目标值(1.8-2.5),但这一观点缺乏大型临床研究证据。队列研究提示,接受华法林治疗的房颤患者,INR在1.5-2.0范围时卒中风险增加2倍。因此,本共识推荐老年患者应与一般成年人采取相同的INR目标值(2.0-3.0)。
INR的监测频度应视患者具体情况而定。应用华法林治疗初期,至少应每3-5日检测一次INR。当INR达到目标值、华法林剂量相对固定后,每4周检测一次即可。如患者在接受华法林治疗过程中患者应用了可能影响华法林作用的药物或发生其他疾患,则应增加检测频度,并视情况对华法林剂量做出调整。增强华法林抗凝作用的常用药物主要包括:抗血小板药,非甾体类抗炎药, 奎尼丁,水合氯醛,氯霉素,丙咪嗪,西咪替丁等。一些广谱抗菌素可因减少维生素K的合成而增强华法林的作用。减弱华法林抗凝作用的常用药物包括:苯巴比妥,苯妥英钠,维生素K,雌激素,制酸剂,缓泻剂,利福平,氯噻酮,螺内酯等。一些中药(如丹参、人参、当归、银杏等)可对华法林的抗凝作用产生明显影响,故同时接受中药治疗时亦应加强监测。一些食物(如葡萄柚、芒果、大蒜、生姜、洋葱、海带、花菜、甘蓝、胡萝卜等)也可增强或减弱华法林的抗凝作用,在用药过程中也需予以注意。
2.1.3 INR增高或发生出血性并发症的处理
在华法林治疗过程中,若患者INR高于目标值或出现出血性并发症,应予以积极处理。具体处理方法参见表2。
2.1.4 禁忌证
下列情况下暂不宜应用华法林治疗:1)围手术期(含眼科与口腔科手术)或外伤;2)明显肝肾功能损害;3)中重度高血压(血压≥160/100 mmHg);4)凝血功能障碍伴有出血倾向;5)活动性消化性溃疡;6)妊娠;7)其他出血性疾病。
2.1.5 局限性
虽然华法林的抗凝效果肯定,但该药也存在一些局限性。首先,不同个体之间应用华法林后凝血机制受影响的程度存在很大差异且无法预测,因此其有效剂量变异幅度较大。其次,该药的抗凝作用易受多种食物和药物的影响,在用药过程中需要频繁监测凝血功能并及时调整药物剂量,这可影响患者长期治疗的依从性。建立健全房颤门诊或抗凝治疗门诊,由经验丰富的专科医师对接受抗凝治疗的房颤患者进行系统化管理,有助于在一定程度上克服其局限性。
2.1.6 应用口服抗凝药物时出血风险的评估
抗凝治疗可增加患者出血性并发症风险,因此在治疗前以及治疗过程中应注意对患者出血风险进行评估,并据评估结果确定相应的治疗方案。目前有多种评估方法应用于临床,其中HAS-BLED评分系统被认为是最为简便可靠的方案(表3)。评分为0~2分者属于出血低风险患者,评分≥3分时提示患者出血风险增高。
说明:"高血压"系指收缩压>160 mm Hg;"肾功能异常"系指长期透析或肾移植或血清肌酐≥200μmol/L者;"肝功能异常"指慢性肝病(例如肝硬化)或具有肝功能明显受损的生化证据(胆红素高于正常上限的2倍,谷草转氨酶/谷丙转氨酶/碱性磷酸酶高于正常上限的3倍等);"药物"是指同时应用抗血小板药物、非甾体类抗炎药物、皮质激素等增强华法林作用的药物。
需要指出的是,出血风险增高者发生血栓栓塞事件的风险往往也增高,这些患者接受抗凝治疗的静获益可能更大。因此,只要患者具备抗凝治疗适应证(CHADS2评分≥2分)仍应进行抗凝药物治疗,而不应将HAS-BLED评分增高视为抗凝治疗禁忌证。对于此类患者应注意筛查并纠正增加出血风险的可逆性因素,并需进一步加强监测。华法林治疗的初始剂量宜更低(1.0mg/d-1.5mg/d),对凝血指标的监测频度亦应增加。启动华法林治疗时或调整剂量期间需要每1-2日检测INR,INR达标后每2周检测1次。
2.2 INR的即时检测与患者自我管理
按要求监测INR是房颤患者安全有效的抗凝治疗的重要保障。目前我国房颤患者的INR检测主要在医院的中心实验室完成,这种模式虽然能够保证监测质量,但因流程较为复杂、等候时间较长、需使用静脉血标本等局限性,在一定程度上影响了患者的依从性。新近我国开始引进INR即时检测技术(point-of-care test, POCT),该技术易于操作,只需一滴指血,可即时报告检测结果,大大简化了抗凝治疗的检测流程,为INR的门诊、急诊快速检测以及患者家庭监测提供了便利。临床研究显示,与每月进行一次高质量的临床检测相比,服用华法林的患者应用POCT技术进行家庭自我监测同样有效[14]。
规范化的POCT技术操作时保证检测结果可靠性的关键,因此需对POCT仪器使用者进行必要的技术培训,确保其技术操作的标准化。若发现POCT结果异常增高或降低,建议在医院中心实验室采集静脉血复核检测结果,并视情况对抗凝治疗方案作出必要的调整。
欧美国家的经验表明,建立房颤专科门诊或抗凝治疗门诊是提高房颤患者抗凝治疗覆盖率、预防血栓栓塞并发症的有效措施。目前我国部分大型医院已对此进行了有益的尝试与探索,并取得了较好效果,值得在国内大中型医院继续推广。
2.3 阿司匹林在预防房颤患者血栓栓塞事件中的作用
关于阿司匹林用于房颤患者血栓栓塞事件的价值一直存在争议。虽然一些学者认为对于血栓风险较低(CHADS2评分0-1分)者可考虑选择阿司匹林治疗,但这一建议缺乏充分证据。新近一项纳入132,372例非瓣膜性房颤患者的大型队列研究提示,无论阿司匹林单独应用或与华法林联合应用,均不具有显著的抗栓疗效,却增加出血风险[15]。因此,关于阿司匹林在房颤患者血栓事件预防中的作用仍有待进一步探讨。
2.4 新型口服抗凝剂
新型抗凝药物可特异性阻断凝血瀑布中某一关键性的环节,在保证抗凝疗效的同时显著降低出血风险。目前正在研发或已经上市的新型抗凝药物主要包括直接凝血酶抑制剂、Xa因子抑制剂、IX因子抑制剂、组织因子抑制剂以及新型维生素K拮抗剂,其代表药物包括直接凝血酶抑制剂达比加群酯以及直接Xa因子抑制剂利伐沙班与阿哌沙班。新型口服抗凝药物治疗过程中无需常规监测凝血功能,更便于患者长期治疗。
2.4.1 达比加群酯
直接凝血酶抑制剂达比加群酯作用于凝血酶(即IIa因子)发挥抗凝疗效[16, 17]。达比加群酯为前体药物,其活性形式是达比加群。RE-LY研究(Randomized evaluation of long term anticoagulant therapy)提供了达比加群酯在房颤患者长期抗凝治疗中的临床证据[18]。该研究旨在评估房颤患者应用两种剂量的达比加群的疗效和安全性及其与华法林的比较。共入选18,113例患者,研究前6个月之内经心电图证实存在房颤,受试者CHADS2评分平均为2.1。将患者随机分为三组,分别接受达比加群酯110mg bid、150mg bid以及华法林治疗,根据INR值(目标值2.0-3.0)调整华法林剂量,中位数随访时间2.0年。研究结果显示,达比加群酯110 mg bid组、150 mg bid 组和华法林组一级有效性终点(卒中或体循环血栓)发生率分别为1.53%、1.11%、1.69%。华法
林组的一级安全性终点(大出血)发生率高于达比加群酯110 mg组(p=0.003),但达比加群150 mg 组与华法林组大出血事件发生率没有统计学差异(p=0.31)。在二级终点卒中发生率方面,达比加群酯150mg组低于华法林组(p<0.001),但110 mg组与华法林组比较没有减少卒中发生率(p=0.41)。本研究提示,在房颤患者中应用达比加群酯(150 mg bid)的疗效优于华法林,其出血并发症发生率与华法林治疗组相似;达比加群酯剂量为110 mg bid时出血并发症有所减少,而其疗效与华法林治疗组相似。
达比加群酯治疗过程中无需常规监测凝血功能,但对于高龄(≥75岁)、肾功能减退、体质虚弱以及存在其他出血高危因素者需减小剂量并加强监测,以免引起严重出血事件[19, 20]。
2.4.2 利伐沙班
利伐沙班对游离型和结合型Xa因子以及凝血酶原酶复合物均有强效的抑制作用,因而具有显著的抗凝疗效[21-24]。ROCKET-AF研究(Rivaroxaban once-daily oral direct factor Xa inhibition compared with vitamin K antagonism for prevention of stroke and embolism trial in atrial fibrillation)对利伐沙班预防房颤患者血栓栓塞事件的疗效进行了评估[25]。该研究采用随机化、双盲、双模拟、临床终点事件驱动设计,旨在论证利伐沙班在预防非瓣膜性房颤患者卒中事件方面的疗效不劣于华法林。共纳入14,264例受试者,入选的房颤患者均有卒中、短暂脑缺血发作或体循环栓塞病史、或存在至少2种发生卒中的独立危险因素(包括慢性心力衰竭、高血压、年龄≥75岁、糖尿病)。将受试者随机分配至利伐沙班组(20 mg qd)或华法林组(根据INR[目标值为2.0-3.0]调整华法林剂量),随访至共发生405次主要终点事件时研究结束。结果显示,与调整剂量的华法林组患者相比,利伐沙班组主要有效性终点事件(卒中与非中枢神经系统栓塞事件)发生率降低21%(p<0.001);利伐沙班组患者血管性死亡、卒中与非中枢神经系统栓塞发生率降低14%(p=0.034),且出血性卒中和非中枢神经系统栓塞事件发生率均显著降低。在安全性终点方面,利伐沙班组患者大出血和有临床意义的非大出血事件发生率与华法林组相当(p=0.442)。利伐沙班治疗组患者颅内出血的发生率降低33%(p=0.019),关键器官出血发生率降低31%(p=0.007),出血相关死亡减少50%(p=0.003)。现有证据表明利伐沙班在预防非瓣膜性房颤患者血栓栓塞事件方面的疗效不劣于、甚至优于华法林,且具有更好的安全性。
2.4.3 阿哌沙班
阿哌沙班是另一种直接Xa因子抑制剂。AVERROES研究(Apixaban versus acetylsalicylic acid to prevent strokes in AF patients who have failed or are unsuitable for vitamin K antagonist treatment)表明,对于不适于华法林治疗的患者,应用阿哌沙班能够较阿司匹林更为有效的预防卒中与全身血栓栓塞事件,且不增加严重出血的风险[26]。该研究共纳入5,599例至少存在1种卒中危险因素且不适合接受华法林治疗的房颤患者,随机分为阿哌沙班(5 mg,b.i.d)治疗或阿司匹林(81~324 mg/d)治疗,平均随访期为1.1年。结果发现阿哌沙班组患者主要终点(卒中和体循环栓塞)发生率为每年1.6%,显著低于阿司匹林组(每年3.7%,p<0.001)。阿哌沙班组与阿司匹林组大出血发生率相似(分别为每年1.4%与1.2%,p=0.57)。由于中期分析结果显示阿哌沙班组获益幅度显著优于阿司匹林组,本研究被提前终止。ARISTOTLE(Apixaban for reduction in stroke and other thromboembolic events in atrial fibrillation)研究采用双盲双模拟随机化对照研究设计,其主要目的旨在论证阿哌沙班预防主要复合终点(缺血性或出血性卒中与体循环栓塞)的疗效不劣于华法林,次要目标是探讨阿哌沙班是否较华法林更为有效的预防由缺血性或出血性卒中、体循环栓塞以及全因死亡所组成的复合终点事件的发生[27]。共纳入18,201例具有卒中高危因素的房颤患者,将其随机分配至阿哌沙班(5 mg,bid,部分患者应用剂量为2.5 mg,bid)治疗组或剂量调整的华法林治疗组(INR目标值为2.0-3.0),最短治疗时间为12个月。平均随访1.8年后显示,与华法林组相比,阿哌沙班可使主要复合终点风险降低21%(p<0.001),严重出血风险降低31%(p<0.001),全因死亡率降低11%(p=0.047),出血性脑卒中减少49%(p<0.001),颅内出血减少58%(p<0.001)。这一研究结果表明,与调整剂量的华法林相比,阿哌沙班能够更为有效的降低卒中或体循环血栓发生率与出血事件危险性,并降低全因死亡率。
毋庸置疑,新型口服抗凝剂的临床应用为房颤患者血栓栓塞并发症的预防提供了安全有效的新选
择。然而,由于此类药物上市时间尚短,仍需加强上市后安全性监测并积累临床应用经验。此外,迄今关于新型口服抗凝剂的临床研究证据主要来自于非瓣膜性房颤患者,关于其在瓣膜性房颤与人工瓣膜置换和瓣膜修补术后患者的应用价值尚有待探讨,这些患者的抗凝治疗仍应选择剂量调整的华法林。在我国(特别是经济不发达地区)仍然存在为数众多的瓣膜性房颤患者,因而华法林仍然具有重要临床地位与广泛应用价值。在现阶段,新型口服抗凝剂主要适用于非瓣膜性房颤患者。
3 特殊人群的抗凝治疗
目前关于特殊人群抗凝治疗的研究证据主要来自于关于华法林的临床试验,在此领域尚缺乏关于新型口服抗凝剂的大型临床研究。参照2010年欧洲房颤治疗指南[7],对特殊人群的抗凝治疗作出如下推荐:
3.1 围手术期抗凝治疗
正在接受华法林治疗的房颤患者在手术或介入性操作前需暂时停药,并应用肝素过渡性治疗。若非急诊手术,一般需要在术前5天左右(约5个半衰期)停用华法林,使INR降低至1.5以下。若INR>1.5但患者需要及早手术,可予患者口服小剂量(1-2mg)维生素K,使INR尽快恢复正常。对于植入机械心脏瓣膜或存在其他血栓高危因素的房颤患者围术期的抗凝治疗尚存争议,一般认为应停用华法林并使用低分子量肝素或普通肝素进行过渡性抗凝治疗。
3.2 稳定型心绞痛与外周动脉疾病
房颤患者合并稳定型心绞痛、颈动脉粥样硬化性疾病或外周动脉疾病时,其最佳抗凝治疗策略尚有待探讨。虽然一些学者建议为此类患者联合应用抗血小板药(特别是阿司匹林)与华法林,但现有研究提示在华法林治疗基础上加用阿司匹林并不能进一步降低卒中与心肌梗死发生率,却显著增加出血事件风险。稳定性冠心病患者单独应用华法林进行二级预防至少与阿司匹林等效,因此建议此类患者仅应用华法林治疗。
3.3 急性冠状动脉综合征和/或经皮冠状动脉介入术
不稳定型心绞痛与冠状动脉支架置入术后的患者应用双联抗血小板治疗(阿司匹林加氯吡格雷;金属裸支架4周,药物洗脱支架6-12个月)可显著降低不良心血管事件风险。当房颤患者合并上述情况时,在华法林治疗基础上加用双联抗血小板药物治疗亦可减少血栓栓塞事件的发生。现有证据提示,与仅应用双联抗血小板药物治疗者相比,短期(如4周)加用华法林并不会显著增加出血事件风险,具有可接受的获益/风险比,但长期应用三联抗栓药物的安全性尚有待论证。置入金属裸支架的房颤患者可短期(4周)进行三联抗栓治疗,随后应用华法林与一种抗血小板药物(阿司匹林或氯吡格雷)治疗。12个月后若患者病情稳定,则参照稳定性冠心病患者的治疗原则仅使用华法林抗凝治疗。置入药物洗脱支架后需要进行更长时间的三联抗栓治疗(西罗莫司、依维莫司和他克莫司洗脱支架应治疗≥3个月,紫杉醇洗脱支架应治疗至少6个月),之后给予华法林加氯吡格雷(75mg/日)或阿司匹林(75-100mg/日)治疗,必要时可联用质子泵抑制剂或H2受体拮抗剂。12个月后若病情稳定,可单独应用华法林抗凝治疗。
若无禁忌证,非ST抬高心肌梗死患者应联合应用阿司匹林与氯吡格雷进行双重抗血小板疗法。若患者伴有房颤且具有中至高度脑卒中风险,还需同时进行抗凝治疗。急性期患者可选用阿司匹林、氯吡格雷、普通肝素或低分子肝素、或比伐卢定和/或糖蛋白IIb/IIIa抑制剂,随后应用三联抗栓治疗(华法林、阿司匹林和氯吡格雷)至少3-6个月。若患者出血风险较低而血栓栓塞风险较高,可应用华法林与氯吡格雷(75mg/日)或阿司匹林(75-100mg/日加胃粘膜保护剂)治疗12个月。此后单独应用华法林长期治疗。
急性ST段抬高心肌梗死需应用阿司匹林、氯吡格雷和肝素联合治疗。当患者具有高血栓负荷时,可临时给予比伐卢定或糖蛋白IIb/IIIa抑制剂。由于这种联合抗栓疗法可显著增加出血风险,在INR>2时不应常规使用糖蛋白IIb/IIIa抑制剂或比伐卢定。此类患者的中长期抗栓治疗原则与非ST 抬高心肌梗死相同。
3.4 急性缺血性卒中
迄今关于缺血性卒中急性期抗栓治疗的研究尚少。急性脑卒中常作为房颤患者的首发表现,且心源性卒中后的最初2周内卒中复发的风险最高,然而在卒中急性期进行抗凝治疗将会增加颅内出血
或梗死后出血的风险,因此不推荐为发病2周以内的缺血性卒中患者进行抗栓治疗。发病2周以后若无禁忌证应开始抗栓治疗,其治疗原则与一般房颤患者相同。
3.5 心房扑动
回顾性研究显示,心房扑动患者发生血栓栓塞并发症的风险与房颤患者相同,因此应遵循房颤患者的抗栓治疗原则对此类患者进行处理。
3.6 房颤复律
在房颤持续时间>48小时或持续时间不明的患者中,拟行择期心脏复律前建议行经食道超声检查以了解是否存在左心房或心耳血栓。无条件进行经食道超声检查时应使用剂量调整的华法林(INR2.0-3.0)进行至少3周的抗栓治疗。由于复律后常存在左心房功能障碍(心房顿抑),患者发生心房内血栓的风险显著增加,故复律后应继续进行约4周的抗凝治疗。房颤发作<48小时的患者可直接进行心脏复律,但须同时应用普通肝素预防血栓。具有脑卒中高风险因素的患者中应在复律后开始应用口服抗凝药物并持续终生,无血栓栓塞高危因素者中无需常规应用口服抗凝药物。房颤发生>48小时且伴血流动力学不稳定(心绞痛、心肌梗死、休克或肺水肿)时应立即进行心脏复律,且在复律前应用肝素治疗,复律后继续口服抗凝药物治疗。口服抗凝治疗的持续时间(4周或终生)取决于患者是否存在脑卒中的高危因素。
4 结语
脑卒中等血栓栓塞性并发症是房颤患者致死致残的主要原因,合理的抗凝治疗对于改善房颤患者生活质量和远期预后具有重要意义。虽然国内外相关指南均建议为高危房颤患者进行血栓预防治疗,但迄今多数患者并未得到相应处理,因此在今后临床工作中应着力加强房颤患者的规范化抗凝治疗,降低血栓栓塞事件的危险性。新型口服抗凝药物的临床应用将为房颤患者的血栓栓塞并发症的预防提供新手段。这些药物具有用法简便、药代动力学特性稳定、不需要常规监测凝血指标、药物作用较少受食物和其他药物影响等优点,对于有效提高房颤患者的抗凝治疗覆盖率和依从性必将起到积极促进作用。
参考文献
1. 周自强,胡大一,陈捷,等. 中国心房颤动现状的流行病学研究. 中华内科杂志 2004,43:491
2. Hu D and Sun Y. Epidemiology, Risk Factors for Stroke, and Management of Atrial Fibrillation in China. J Am Coll Cardiol 2008, 52: 865
3. Levy S, Maarek M, Coumel P, et al. for the College of French Cardiologists Characterization of different subsets of atrial fibrillation in general practice in France: The ALFA study. Circulation 1999, 99: 3028
4. Krahn AD, Manfreda J, Tate RB, et al. The natural history of atrial fibrillation: incidence, risk factors, and prognosis in the Manitoba Follow-Up Study. Am J Med 1995, 98: 476
5. Atrial Fibrillation Investigators. Risk factors for stroke and efficacy of antithrombotic therapy in atrial fibrillation: Analysis of pooled data from five randomized controlled trials. Arch Intern Med 1994, 154: 1449
6. Flegel KM, Shipley MJ, Rose G. Risk of stroke in non-rheumatic atrial fibrillation. Lancet 1987,1: 526
7. Camm AJ, Kirchhof P, Lip GY, et al. Guidelines for the management of atrial fibrillation: the Task Force for the Management of Atrial Fibrillation of the European Society of Cardiology (ESC). Eur Heart J 2010,31:2369
8. Gage BF, Waterman AD, ShannonW, et al. Validation of clinical classification schemes for predicting stroke: results from the National Registry of Atrial Fibrillation. JAMA 2001, 285:2864
9. Mant J, Hobbs FD, Fletcher K, et al. BAFTA investigators; Midland Research Practices Network (MidReC). Warfarin versus aspirin for stroke prevention in an elderly community population with atrial fibrillation (the Birmingham Atrial Fibrillation Treatment of the Aged Study, BAFTA): A randomised controlled trial. Lancet 2007, 370: 493
10. Group on behalf of the ACTIVE Investigators. Clopidogrel plus aspirin versus oral anticoagulation for atrial fibrillation in the Atrial fibrillation Clopidogrel Trial with Irbesartan for prevention of Vascular Events (ACTIVE W): A randomised controlled trial. Lancet 2006, 367: 1903
11. Pérez-Gómez F, Alegría E,Berjón J, et al. Comparative effects of antiplatelet, anticoagulant, or combined therapy in patients with valvular and nonvalvular atrial fibrillation: A randomized multicenter study. J Am Coll Cardiol 2004, 44: 1557
12. Hart RG, Pearce LA, Aguilar MI. Meta-analysis: Antithrombotic therapy to prevent stroke in patients who have nonvalvular atrial fibrillation. Ann Intern Med 2007, 146: 857
13. Ansell J, Hirsh J, Hylek E, et al. Pharmacology and management of the vitamin K antagonists: American College of Chest Physicians Evidence-Based Clinical Practice Guidelines (8th Edition). Chest 2008,133(6 Suppl):160S
14. Matchar DB, Jacobson A, Dolor R, et al. Effect of Home Testing of International Normalized Ratio on Clinical Events. N Engl J Med 2010; 363:1608-1620
15. Olesen JB, Lip GYH, Lindhardsen J, et al. Risks of thromboembolism and bleeding with thromboprophylaxis in patients with atrial fibrillation: A net clinical benefit analysis using a 'real world' nationwide cohort study. Thromb Haemost 2011, 106: 739
16. Gross PL, Weitz JI. New anticoagulants for treatment of venous thromboembolism. Arterioscler Thromb Vasc Biol 2008, 28: 380
17. Weitz J, Hirsh J. New anticoagulant drugs. Chest 2001, 119(Suppl): 95S
18. Connolly SJ, Ezekowitz MD, Yusuf S, et al. Dabigatran versus warfarin in patients with atrial fibrillation. N Engl J Med 2009, 361: 1139
19. Legrand M, Mateo J, Aribaud A, et al. The use of dabigatran in elderly patients. Arch Intern Med 2011, 171:1285.
20. Jacobs JM and Stessman J. New anticoagulant drugs among elderly patients. Is caution necessary? Arch Intern Med 2011, 171:1287
21. Perzborn E, Strassburger J, Wilmein A, et al. In vitro and in vivo studies of the novel antithrombotic agent BAY 59-7939: An oral, direct factor Xa inhibitor. J Thromb Haemost 2005, 3: 514
22. Mueck W, Becka M, Kubitza D, et al. Population model of the pharmacokinetics and pharmacodynamics of rivaroxaban—an oral, direct factor Xa inhibitor—in healthy subjects. Int J Clin Pharmacol Therap 2007, 45: 335
23. Kubitza D, Becka M, Wensing G, et al. Safety, pharmacodynamics, and pharmacokinetics of BAY 59-7939—an oral, direct factor Xa inhibitor—after multiple dosing in healthy male subjects. Eur J Clin Pharmacol 2005, 61: 873
24. Kubitza D, Becka M, Zuehlsdorf M, et al. Effect of food, an antacid, and the H2 antagonist ranitidine on the absorption of BAY 59-7939 (rivaroxaban), an oral, direct factor Xa inhibitor, in healthy subjects. J Clin Pharmacol 2006, 46: 549
25. Patel MR, Mahaffey KW, Garg J, et al. Rivaroxaban versus warfarin in nonvalvular atrial fibrillation. N Engl J Med 2011,365:883
26. Connolly SJ, Eikelboom J, Joyner C, et al. Apixaban in patients with atrial fibrillation. N Engl J Med 2011,364:806
27. Granger CB, Alexander JH, McMurray JJ, et al. Apixaban versus warfarin in patients with atrial fibrillation.N Engl J Med 2011,365:981
中华医学会心血管病学分会
中华医学会心电生理和起搏分会
中国老年学学会心脑血管病专业委员会
中国生物医学工程学心律分会
中国医师协会循证医学专业委员会
心律失常联盟(中国)
房颤抗凝
近年来,卒中风险评估系统的细化与严格化在房颤的整体治疗中的重要性得以提升。早在2006年,ACC/AHA/ESC颁布的房颤指南中就已推荐使用CHADS2评分系统,其中充血性心力衰竭,高血压病史,年龄≥75岁,糖尿病史各为1分,既往卒中或短暂性脑缺血发作为2分,总分为6分。而后,在对5项房颤卒中的风险分析的随机对照研究中(AFASAK,SPAF,BAATAF,CAFA和SPINAF)一致发现,年龄是卒中的重要危险因素,并可以成为卒中独立预测因子。而对3项房颤卒中风险分析的随机对照研究(AFI,ATRIA,APAF)以及Framingham研究,欧洲心脏调查及哥本哈根城市心脏研究中均提示,女性性别因素也是房颤卒发生的独立危险因素之一。因此,2010年的ESC房颤指南中,把CHADS2评分系统改进为CHA2DS2-V ASC评分系统。该系统增加了血管性疾病(1分),年龄65-74岁(1分)以及女性性别(1分),并将年龄≥75岁的分值提升为2分,总分增加到9分。该评分系统相比既往的CHADS2评分系统,在高危风险组患者中抗凝治疗指征的确立更具优势,同时也能更加准确地指导评估真正意义上的低风险患者。 2012年的ESC房颤指南中,进一步推荐CHA2DS2-V ASc 评分系统作为非瓣膜性房颤患者卒中风险的评估工具(I A类推荐)。对于CHA2DS2-VASc 评分为0分的无卒中危险因素的低危患者(如年龄<65岁的孤立房颤患者),不推荐抗栓治疗(I A类推荐);对于CHA2DS2-V ASc 评分≧2分的房颤患者,除有禁忌症,推荐使用华法林或新型口服抗凝药物(达比加群、利伐沙班、阿哌沙班)抗凝治疗(I A类推荐);对于CHA2DS2-VASc 评分1分的患者,根据患者出血风险评估及自身选择,可考虑给予华法林或新型口服抗凝药物抗凝治疗(IIa A类推荐)。 值得注意的是,抗血小板治疗在新指南中的推荐较2010年指南进一步降低,仅当患者拒绝使用任何口服抗凝药物(包括华法林或新型口服抗凝药物)时,才考虑给予抗血小板疗法,且推荐阿司匹林+氯吡格雷双联抗血小板治疗优于阿司匹林(IIa B类推荐) 2 新型口服抗凝药物得到了新指南的强力推荐 华法林属于维生素K拮抗剂,长期以来用于房颤的抗凝治疗,其能有效地降低房颤患者的脑卒中发生率及相关死亡率。循证医学证据表明其抗栓作用优于阿司匹林或双联抗血小板药物阿司匹林与氯吡格雷的联合使用。然后,不能不正视的是,华法林治疗伴有较高的出血率,而且需要严密监测INR,给服药患者和临床医生都增加了不便。 2012年ESC房颤指南中,正式对新型口服抗凝药物(达比加群、利伐沙班、阿哌沙班)给出了推荐。除了上文中依据CHA2DS2-V ASc 评分选择抗凝策略外,新指南中还提出,当口服抗凝药物适用时,由于副作用、不耐受、难以维持治疗窗内时间或者无法监测INR导致无法使用经剂量调整的华法林时,推荐给予直接凝血酶抑制剂(达比加群)或口服Xa因子抑制剂(如利伐沙班、阿哌沙班)抗凝治疗(I B类推荐);且基于大多数非瓣膜性房颤患者的临床净获益,推荐新型口服抗凝药物优于经剂量调整的华法林(IIa A类推荐)。 对于接受任何新型口服抗凝药物治疗的患者,推荐进行肾功能基线和常规的一年一次评估(使用CrCl),其中,对于中度肾功能不全的患者,其频率应增加为每年2–3次。对于出血风险较高或中度肾功能不全(CrCl 30–49 mL/min)的患者,达比加群获得了更高的证据级别推荐。不推荐新型口服抗凝药物(达比加群、利伐沙班和阿哌沙班)用于重度肾功能不全的患者(CrCl <30 mL/min)。
心房颤动抗凝治疗中国专家共识
心房颤动抗凝治疗中国专家共识 心房颤动(房颤)是最常见的心律失常之一。根据2004年所发表的数据,我国30岁至85岁居民中房颤患病率为0.77%,其中80岁以上人群中患病率达30%以上[1,2]。血栓栓塞性并发症是房颤致死致残的主要原因,而脑卒中则是最为常见的表现类型。在非瓣膜性房颤患者中,缺血性卒中的每年发生率(约5%)是非房颤患者的2~7倍[3-6]。预防卒中的新发与复发应成为房颤患者综合管理策略中的主要内容。越来越多的研究证实,对于发生卒中风险增高的患者,合理应用抗凝药物有助于显著降低缺血性卒中的发生率,然而在我国大多数房颤患者未得到抗凝治疗[1, 2]。 进一步增强对房颤及其并发症危害性的认识、加强血栓栓塞并发症(特别是卒中)的预防对于改善患者预后进而减轻与之相关的社会经济和家庭负担具有重要意义。目前已有多种口服抗凝药物应用于临床,如华法林、达比加群、利伐沙班、阿哌沙班等。为促进与规范房颤患者的抗凝治疗,降低缺血性卒中等血栓栓塞性并发症的发生率,中华医学会心血管病学分会、中华医学会心电生理和起搏分会、中国老年学学会心脑血管病专业委员会、中国生物医学工程学心律分会、中国医师协会循证医学专业委员会、与心律失常联盟(中国)组织国内专家制定了此专家共识。 1 房颤患者卒中和血栓栓塞的危险分层与抗凝治疗原则 合理的抗凝治疗是预防房颤患者血栓栓塞事件的有效措施,但与此同时亦将增加出血性并发症的风险。因此,在确定患者是否适于进行抗凝治疗前应评估其获益风险比,只有预防血栓栓塞事件的获益明显超过出血性并发症的风险时方可启动抗凝治疗。房颤患者发生缺血性卒中的风险水平与其基线特征密切相关,根据基线特征对患者进行危险分层是制定正确的抗凝治疗策略的基础[7]。目前CHADS2评分系统是临床应用最为广泛的评估工具,其计分方法如表1所示[8]。随着CHADS2评分的增高,房颤患者未来发生缺血性卒中的风险逐渐增高。若无禁忌证,所有CHADS2评分≥2分的房颤患者均应进行长期口服抗凝药治疗。若房颤患者CHADS2评分为1分,可应用阿司匹林(100mg—300mg, qd)治疗,部分患者也可考虑应用口服抗凝药治疗。CHADS2评分为0分时一般无需抗凝治疗。 虽然已有确凿研究证据表明,为血栓栓塞事件风险增高的房颤患者进行规范化抗凝治疗可以显著改善患者预后,但我国大多数房颤患者并未应用抗凝药物。而在应用华法林的患者中,多数未系统监测国际标准化比率(INR),或INR保持在无效的低水平(1.3-1.5)。导致这一现状的原因是多方面的,其中临床医生对于血栓栓塞性并发症危害性的认识不足以及对传统抗凝药物华法林治疗所伴随的出血风险增加的过度担忧可能是其主要原因。实际上,只要遵照相关指南原则正确掌握适应证并按要求监测凝血功能,房颤患者抗凝治疗的获益远超过其抗凝治疗相关并发症的风险。 2 房颤患者的抗凝治疗 2.1 华法林在房颤患者抗凝治疗中的应用 60余年以来,华法林一直广泛应用于临床,在房颤患者缺血性卒中的预防中一直发挥着重要作用。该药通过减少凝血因子II、VII、IX与X的合成等环节发挥抗凝作用。只有所有依赖于维生素K的凝血因子全部被抑制后才能发挥充分的抗凝作用,因此华法林的最大疗效多于连续服药4-5天后达到,停药5-7天后其抗凝作用才完全消失。
心房颤动抗凝治疗指南解读(最全版)
心房颤动抗凝治疗指南解读(最全版) 心房颤动(以下简称房颤)是最常见的心律失常之一,根据2012年欧洲心脏病协会(European Society of Cardiology,ESC)发布的房颤指南(以下简称2012 ESC指南)的统计数据[1],估计发达国家房颤患病率为1.5%~2.0%,患者平均年龄75~85岁,且患病率有持续升高的趋势。在我国,根据2004年的发布数据,30~85岁居民中房颤患病率为0.77%,其中80岁以上人群患病率达30%。作为脑卒中的独立危险因素,房颤患者每年的缺血性脑卒中发病率是非房颤患者的2~7倍。 抗凝治疗是房颤患者脑卒中预防的核心策略,但我国房颤患者的抗凝治疗严重不足。为此,本文将详细分析各国新版房颤抗凝指南,了解全球各国房颤抗凝治疗现状。各国指南包括:2012 ESC指南,2014年美国心脏协会(American Heart Association,AHA)、美国心脏病学会(American College of Cardiology,ACC)、美国心律学会(Heart Rhythm Society,HRS)和美国胸外科医师学会(Society of Thoracic Surgeons,STS)联合发布的房颤患者管理指南(以下简称2014 AHA/ACC指南)[2],2014年英国国家卫生与临床优化研究所(National Institute for Health and Clinical Excellence,NICE)发布的房颤诊疗指南(以下简称2014 NICE指南)[3],2014年加拿大心脏病学会(Canadian Cardiovascular Society,CCS)发布的房颤管理指南(以下简称2014 CCS 指南)[4],以及2012年美国胸科医师协会(American College of Chest Physicians,ACCP)发布的第9版抗栓治疗及预防血栓形成指南(以下
加强和规范心房颤动的抗凝治疗(全文)
加强和规范心房颤动的抗凝治疗(全文) 心房颤动(简称房颤)是临床上最常见的心律失常之一。房颤增加缺血性脑卒中及体循环动脉栓塞的风险,其缺血性脑卒中的风险是非房颤患者的4-5倍,且将导致近20%的致死率及近60%的致残率。预防房颤引起的血栓栓塞事件,是房颤治疗策略中重要环节。在血栓栓塞危险较高的房颤患者中,应用华法林或新型口服抗凝药物(NOAC)抗凝可明显减少血栓栓塞事件,并改善患者的预后。但我国不少房颤患者并未应用抗凝治疗,接受抗血小板治疗的比率仍然较高。即使应用华法林抗凝治疗,多数患者未系统监测国际标准化比值(INR),或INR 保持在无效的低水平。导致这一现状的原因是多方面的,其中临床医生对于血栓栓塞性并发症危害性认识不足以及对传统抗凝药物华法林增加出血风险过度担忧可能是其主要原因。实际上,只要遵循相关临床实践指南、正确掌握适应证、动态评估栓塞及出血风险、注意监测,脑卒中风险高的房颤患者抗凝治疗的获益将远远超过其风险。 目前临床上权衡房颤患者血栓栓塞/出血风险的临床评估工具主要是CHA2DS2-VASc评分和HAS-BLED评分。CHA2DS2-VASc积分≥2分的男性或≥3分的女性房颤患者血栓事件的年发生率较高,抗凝治疗带来的临床净获益明显。阵发性房颤与持续性或永久性房颤具有同样的危险性,其抗凝治疗的方法均取决于危险分层。
出血和血栓具有很多相同的危险因素,例如老龄和血栓栓塞史,既是卒中同时也是出血的重要危险因素。出血风险增高者发生血栓栓塞事件的风险往往也高,这些患者接受抗凝治疗的临床净获益可能更大。因此,只要患者具备抗凝治疗的适应证仍应进行抗凝治疗,而不应将HAS-BLED评分增高视为抗凝治疗的禁忌证。 临床上应用的口服抗凝药(OAC)主要分为两类:(1)维生素K拮抗剂(VKA):华法林。(2)非维生素K拮抗剂(NOAC):①直接凝血酶抑制剂:达比加群酯;②Ⅹa因子抑制剂:利伐沙班、阿哌沙班、依度沙班。 华法林是临床上常用的口服抗凝药,随机对照研究的荟萃分析表明,华法林可使房颤患者发生卒中的相对危险度降低64%,每年发生卒中的绝对危险度降低2.7%,可使全因死亡率降低26%。其经胃肠道吸收迅速,生物利用度高,口服90 min后血药浓度达峰值,半衰期36-42 h。但华法林存在如治疗窗口窄、出血风险高、容易受其他药物与食物影响、治疗剂量个体差异大、需要定期监测INR等缺点。华法林抗凝治疗的效益和安全性取决于抗凝治疗的强度和稳定性。临床研究证实抗凝强度为INR2.0-3.0时,华法林可有效预防卒中事件,并不明显增加出血的风险。华法林抗凝治疗的稳定性常用INR在治疗目标范围内的时间百分比(time within therapeutic range, TTR)表示。一般情况下, 应尽量使TTR>65%。INR在治疗
房颤抗凝治疗指南最新修订
---------------------------------------------------------------最新资料推荐------------------------------------------------------ 房颤抗凝治疗指南最新修订 房颤抗凝治疗指南最新修订房颤抗凝治疗指南最新修订随着科技的进步和生产力的发展,人类社会正逐步进入老龄化社会发展阶段。 心房颤动(房颤, AF)的发生率随着年龄的增长而显著增加,而由房颤所致的脑栓塞带来的致残率(高达 60%)和致死率(高达20%)也随之升高。 因此,通过抗凝治疗预防卒中越来越成为广大医务工作者临床工作的重中之重。 早在 2010 年欧洲心脏病学会(ESC)颁布的房颤治疗指南中,已将房颤的抗凝治疗摆在了房颤治疗的三大方面之首,这足以显示抗凝治疗在整个房颤治疗过程中的重要地位。 而刚刚在德国慕尼黑落下帷幕的 2019 年的 ESC 大会,最大的亮点之一便是房颤指南更新的颁布,此次指南更新主要对房颤抗凝治疗的部分进行了修订,内容如下: 1 肯定了以 CHA2DS2-VASc 评分系统作为非瓣膜性房颤患者卒中风险的评估工具近年来,卒中风险评估系统的细化与严格化在房颤的整体治疗中的重要性得以提升。 早在 2006 年, ACC/AHA/ESC 颁布的房颤指南中就已推荐使用CHADS2 评分系统,其中充血性心力衰竭,高血压病史,年龄75 岁,糖尿病史各为 1 分,既往卒中或短暂性脑缺血发作为 2分,总分 1 / 5
为 6 分。 而后,在对 5 项房颤卒中的风险分析的随机对照研究中(AFASAK, SPAF, BAATAF, CAFA 和 SPINAF)一致发现,年龄是卒中的重要危险因素,并可以成为卒中独立预测因子。 而对 3 项房颤卒中风险分析的随机对照研究(AFI, ATRIA,APAF)以及 Framingham研究,欧洲心脏调查及哥本哈根城市心脏研究中均提示,女性性别因素也是房颤卒发生的独立危险因素之一。 因此, 2010 年的 ESC 房颤指南中,把 CHADS2 评分系统改进为 CHA2DS2-VASC 评分系统。 该系统增加了血管性疾病(1 分),年龄 65-74 岁(1 分)以及女性性别(1分),并将年龄75 岁的分值提升为 2 分,总分增加到 9 分。 该评分系统相比既往的 CHADS2 评分系统,在高危风险组患者中抗凝治疗指征的确立更具优势,同时也能更加准确地指导评估真正意义上的低风险患者。 2019 年的 ESC 房颤指南中,进一步推荐 CHA2DS2-VASc 评分系统作为非瓣膜性房颤患者卒中风险的评估工具(I A 类推荐)。 对于CHA2DS2-VASc 评分为 0 分的无卒中危险因素的低危患者(如年龄65岁的孤立房颤患者),不推荐抗栓治疗(I A 类推荐);对于CHA2DS2-VASc 评分≧2 分的房颤患者,除有禁忌症,推荐使用华法林或新型口服抗凝药物(达比加群、利伐沙班、阿哌沙班)抗凝治疗(I A 类推荐);对于 CHA2DS2-VASc 评分 1 分的患者,根
老年心房颤动的华法林抗凝治疗
老年心房颤动的华法林抗凝治疗 目的:了解临床实践中心房颤动(房颤)患者接受抗凝治疗的具体情况。方法:每日晚饭后服华法林,起始剂量3.0 mg/d,每5~7天测量1次INP,使INR在2.0-2.5。INP<2.0时,华法林剂量每3-5天增加0.5 mg,直至达标,当INP>2.5时,当日起药物剂量减0.5 mg,直至达标。结果:维持剂量为(2.35~0.44)nag,最高3.5 mg,最低1.5 mg,其中87.5%患者维持用量为2.0-3.0 mg。达标时间为(10.5±3.4]d,最高21 d,最低5 d,其中74.5%在14 d内达标。结论:当前基层医院房颤抗凝治疗率极低,应提高广大医务人员与患者对房颤并发栓塞的危险性的认识,减少房颤患者栓塞事件的发生。 标签:心房颤动;华法林;抗凝治疗;老年 [文献标识码]B [文章编号]1674-4721(2009)03(b)-050-02 心房颤动是临床最常见的持续性心律失常,其发生率随年龄而增加。房颤患者的病死率是无房颤者的2倍。而栓塞是房颤的重要并发症,其中脑栓塞是房颤致死及致残的最主要原因之一。因此抗凝是治疗房颤的重要目标。我们对106例老年心房颤动患者给予华法林抗凝治疗,现总结如下: 1资料与方法 1.1一般资料 2004年8月-2007年8月老年心房颤动住院患者共106例,男57例,女49例,年龄最大75岁,最小61岁,平均(67.7±4.1)岁,其中61-64岁36例,65-69岁38例,70-75岁32例,病史平均(3.3±1.8)年。冠心病68例,风心病17例(其中二尖瓣金属瓣置换术后3例,生物瓣置换术后1例),高血压性心脏病11例,扩张性心肌病8例,肺心病2例。全部患者中并发高血压病19例。 1.2入选标准 年龄60-75岁,依据病史、体检及心电图诊断为永久性心房颤动,病史>0.5年。排除标准:①明确的易出血性疾病,如活动性溃疡、支气管扩张等;②严重肝、肾功能不全;③血液病,凝血系统障碍;④脑卒中2.5时,当日起药物剂量减0.5 mg,直至达标。达标后每月复查1次INR,观察华法林达标剂量、维持剂量、达标时间和副作用,观察期为6个月。对于心功能不全、心律失常、高血压等给予相应治疗。 1.4统计学方法
抗凝治疗对于心房颤动
抗凝治疗对于心房颤动(房颤)非常重要。前面曾经提到,CHA2DS2-VASc评分≥2分的患者都推荐抗凝治疗,而华法林是目前临床应用最为广泛的口服抗凝药,也是长期抗凝治疗的基础。该药已经有60余年的历史了,通过作用于维生素K依赖性的凝血因子而发挥作用,可以使房颤患者的脑卒中风险降低64%,可以说是心血管医师和房颤患者的“好朋友”。但由于这位“朋友”的一些特性,使其有时候看起来似乎不太“友善”,甚至成了“敌人”。的确,服用华法林有一些特殊要求,但只要了解了以下这些注意事项并按医嘱服用,华法林对房颤患者还是非常有益的。 首先,华法林最突出的特点就是服用期间需要定期抽血化验。这是因为华法林体内代谢个体差异较大,还会受到多种因素影响,所以究竟用多大剂量合适人与人之间并不相同,甚至同一患者在不同时期也不一样。华法林是抗凝药,服用时会部分抑制凝血功能,通俗讲,就是让血液与不吃药的人相比“不那么容易凝了”。剂量不足达不到效果,而过量又可能产生出血风险。所以需要通过抽血化验反映凝血功能的指标来决定药物的剂量。对于华法林,我们关注的指标是国际标准化比值(INR)(正常值是0.8~1.2),用药期间应使其轻度升高,维持在2~3的范围内(对于部分患者国内也有专家提倡1.8~2.5,但缺少证据支持)。这样既能达到抗凝效果,出血风险又不会很高,即“有效且安全”。若INR<2,即抗凝不足,药物需要加量;反之,若INR>3,出血风险升高,则需要减量。因此,用药期间定期监测INR 十分重要,千万不要因为怕麻烦而忽略。此外,华法林代谢也比较慢,通常连续服药4~5 天后起效,停药后5~7天作用才能消失。因此,用药初期抽血化验的次数要多一些,3~5天1次,直到INR上升并稳定在要求范围后,可以逐步延长至每4周监测1次。 其次,华法林在体内的代谢受到多种食物、药物,甚至是身体状况的影响。可能增强华法林效果的药物主要有阿司匹林、奎尼丁(抗心律失常药)、吲哚美辛(退热镇痛药)、对乙酰氨基酚(退热镇痛药)、某些抗生素、西米替丁(抑制胃酸药)、水合氯醛(麻醉药)等;减弱华法林作用的药物包括苯妥英钠(抗癫痫药)、巴比妥类(抗癫痫药)、雌激素、利福平(抗结核药)、维生素K、螺内酯(利尿剂)等。另外,一些中药成分也会对华法林的代谢产生影响,如丹参、人参、当归、银杏等。而影响华法林作用的食物(富含维生素K 可降低INR)有猪肝、胡萝卜、菜花、大蒜、生姜、绿叶蔬菜(菠菜、油菜、生菜、圆白菜)、柚子、橘子等。发热、肿瘤等疾病也可以增强华法林的效果。那是否就是说,上述药物或食物在用药期间就都不能吃了呢?并不绝对。影响华法林作用的食物成分很多,若严格限制,甚至可能造成营养失衡。只要规律膳食,每天合理搭配各种食物成分,使蔬菜、水果及肉类的比例相对稳定,一般不会引起INR的较大波动。每天规律服用的药物对华法林的影响也相对恒定,只要定期监测即可。当然,如果不是必须的药物,还是建议不要同期服用。特别要注意的情况是因突发情况而发生用药的变化,如感染发热时短期应用抗生素、关节痛短期服用镇痛药等,由于这种影响是短期的,故需要密切监测INR变化直至停用有影响的药物或INR稳定。
