离子半径数据
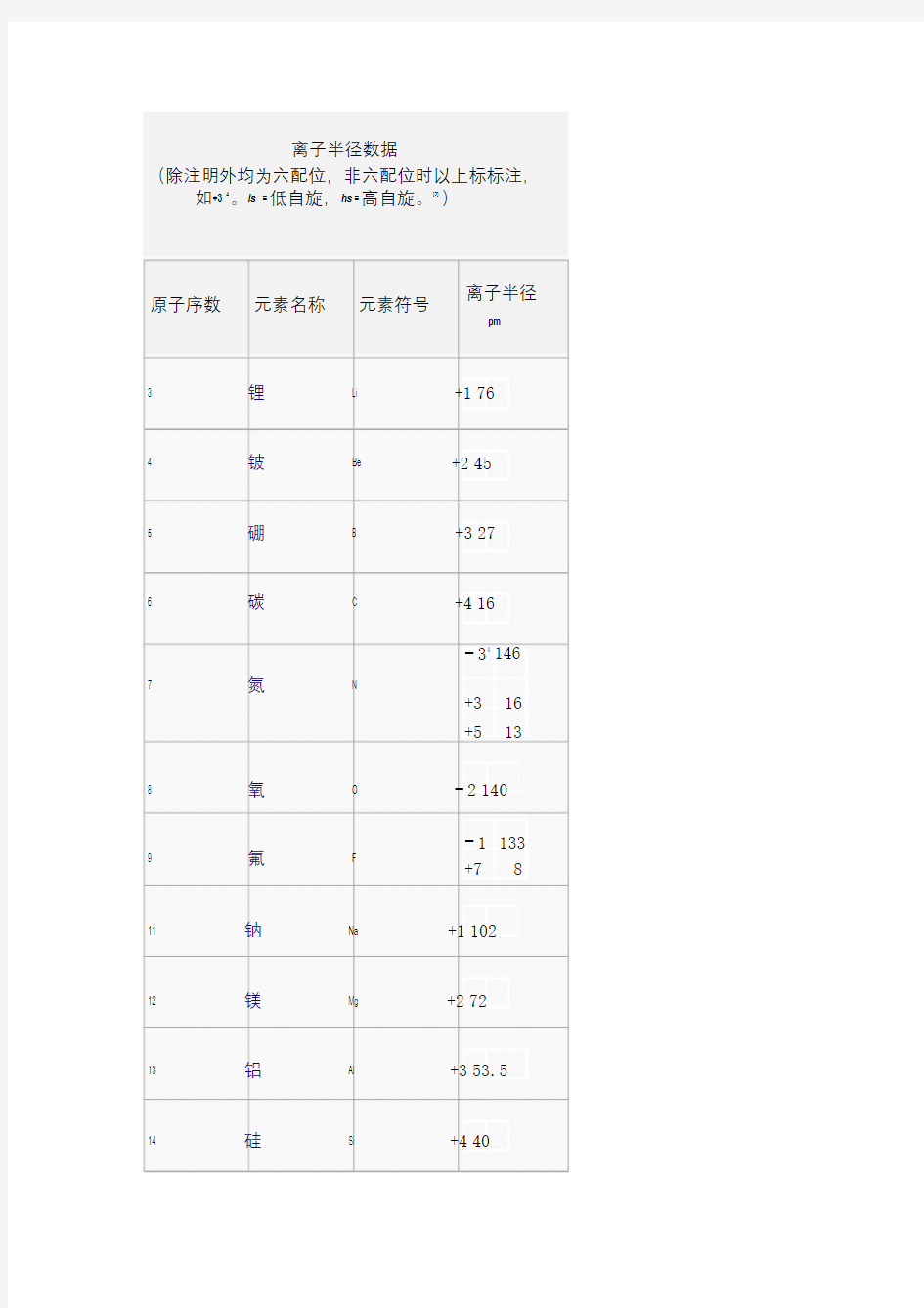

离子半径数据
(除注明外均为六配位,非六配位时以上标标注,如+34。ls=低自旋,hs=高自旋。[2])
原子序数元素名称元素符号离子半径
pm
3 锂Li +1 76
4 铍Be +2 45
5 硼 B +3 27
6 碳 C +4 16
?34 146 7 氮N
+3 16
+5 13 8 氧O ?2 140
9 氟 F ?1 133 +7 8
11 钠Na +1 102
12 镁Mg +2 72
13 铝Al +3 53.5
14 硅Si +4 40
离子半径数据
(除注明外均为六配位,非六配位时以上标标注,如+34。ls=低自旋,hs=高自旋。[2])
原子序数元素名称元素符号离子半径
pm
15 磷P +3 44
+5 38 ?2 184
16 硫S
+4 37
+6 29
?1 181 17 氯Cl
+5 12
+7 27
19 钾K +1 138
20 钙Ca +2 100
21 钪Sc +3 74.5
+2 86
22 钛Ti
+3 67
+4 60.5
+2 64
23 钒V
+4 58
+5 54
+2 73 ls
+2 80 hs 24 铬Cr
+3 61.5
+4 55
+5 49
离子半径数据
(除注明外均为六配位,非六配位时以上标标注,
如+34。ls =低自旋,hs =高自旋。[2])
原子序数 元素名称 元素符号
离子半径 pm
+6 44
+2 67
+3 58 ls
+3 64.5 hs
25 锰 Mn +4 53
+54
33 +64
25.5 +7 46
+2 61 ls
+2 78 hs
26 铁 Fe
+3 55 ls
+3 64.5 hs
+4 58.5
+64 25 +2 65 ls
+2 74.5 hs
27 钴 Co +3 54.5 ls
+3 61 hs
+4 53
+2 6 9 +3 56 ls 28 镍 Ni
+3 60 hs
+4 48 ls
29 铜 Cu
+1 7 7
+27
离子半径数据
(除注明外均为六配位,非六配位时以上标标注,如+34。ls=低自旋,hs=高自旋。[2])
原子序数元素名称元素符号离子半径
pm
3
+3 54 ls
30 锌Zn +2 74
31 镓Ga +3 62
32 锗Ge +2 73 +4 53
33 砷As +3 58
+5 46 ?2 198
34 硒Se
+4 50
+6 42
?1 196
35 溴Br +34sq 59 +54 31
+7 39
37 铷Rb +1 152
38 锶Sr +2 118
39 钇Y +3 90
离子半径数据
(除注明外均为六配位,非六配位时以上标标注,如+34。ls=低自旋,hs=高自旋。[2])
原子序数元素名称元素符号离子半径
pm
40 锆Zr +4 72
+3 72 41 铌Nb
+4 68
+5 64
+3 69
42 钼Mo +4 65 +5 61 +6 59
+4 64.5
43 锝Tc
+5 60
+7 56
+3 68
+4 62 44 钌Ru
+5 56.5
+74 38
+84 36
+3 66.5 45 铑Rh
+4 60
+5 55
+12 59
46 钯Pd +2 86 +3 76 +4 61.5
离子半径数据
(除注明外均为六配位,非六配位时以上标标注,如+34。ls=低自旋,hs=高自旋。[2])
原子序数元素名称元素符号离子半径
pm
+1 115
47 银Ag
+2 94
+3 75
48 镉Cd +2 95
49 铟In +3 80
50 锡Sn +2 112 +4 69
51 锑Sb +3 76
+5 60 ?2 221
52 碲Te
+4 97
+6 56
?1 220 53 碘I
+5 95
+7 53
54 氙Xe +8 48
55 铯Cs +1 167
56 钡Ba +2 135
离子半径数据
(除注明外均为六配位,非六配位时以上标标注,如+34。ls=低自旋,hs=高自旋。[2])
原子序数元素名称元素符号离子半径
pm
57 镧La +3 103.2
58 铈Ce +3 102 +4 87
59 镨Pr +3 99 +4 85
60 钕Nd +28 129 +3 98.3
61 钷Pm +3 97
62 钐Sm +24 122 +3 95.8
63 铕Eu +2 117 +3 94.7
64 钆Gd +3 93.8
65 铽Tb +3 92.3 +4 76
66 镝Dy +2 107 +3 91.2
67 钬Ho +3 90.1
离子半径数据
(除注明外均为六配位,非六配位时以上标标注,如+34。ls=低自旋,hs=高自旋。[2])
原子序数元素名称元素符号离子半径
pm
68 铒Er +3 89
69 铥Tm +2 103 +3 88
70 镱Yb +2 102 +3 86.8
71 镥Lu +3 86.1
72 铪Hf +4 71
+3 72 73 钽Ta
+4 68
+5 64
+4 66 74 钨W
+5 62
+6 60
+4 63
75 铼Re +5 58
+6 55
+7 53
+4 63 +5 57.5
76 锇Os
+6 54.5
+7 52.5
+84 39
离子半径数据
(除注明外均为六配位,非六配位时以上标标注,如+34。ls=低自旋,hs=高自旋。[2])
原子序数元素名称元素符号离子半径
pm
+3 68
77 铱Ir
+4 62.5
+5 57
+2 86 78 铂Pt
+4 62.5
+5 57
+1 137 79 金Au
+3 85
+5 57
80 汞Hg +1 119 +2 102
81 铊Tl +1 150 +3 88.5
82 铅Pb +2 119 +4 77.5
83 铋Bi +3 103 +5 76
84 钋Po +4 94 +6 67
85 砹At +7 62 87 钫Fr +1 180
离子半径数据
(除注明外均为六配位,非六配位时以上标标注,如+34。ls=低自旋,hs=高自旋。[2])
原子序数元素名称元素符号离子半径
pm
88 镭Ra +28 148
89 锕Ac +3 112
90 钍Th +4 94
+3 104 91 镤Pa
+4 90
+5 78
+3 102.5
92 铀U +4 89 +5 78 +6 73
+2 110 +3 101
93 镎Np +4 87 +5 75 +6 72 +7 71
+3 100
94 钚Pu +4 86 +5 74 +6 71
95 镅Am +28 126 +3 97.5
离子半径数据
(除注明外均为六配位,非六配位时以上标标注,如+34。ls=低自旋,hs=高自旋。[2])
原子序数元素名称元素符号离子半径
pm
+4 85
96 锔Cm +3 97 +4 85
97 锫Bk +3 96 +4 83
98 锎Cf +3 95 +4 82.1
离子半径大小的比较规律
离子半径大小的比较规律 Prepared on 22 November 2020
粒子半径大小的比较规律 1.同种元素粒子半径大小比较: 同种元素原子形成的粒子,核外电子数越多,粒子半径越大。阳离子半径小于相应原子半径。如r(Na+)
离子半径大小的比较规律
粒子半径大小的比较规律 1.同种元素粒子半径大小比较: 同种元素原子形成的粒子,核外电子数越多,粒子半径越大。阳离子半径小于相应原子半径。如r(Na+)
化学离子半径比较专题讲解及习题(含答案)
离子半径比较专题 一、规律方法总结 1、微粒半径大小的比较一般要掌握以下规律: (1).对原子来说:①同周期元素的原子(稀有气体除外),从左到右原子半径逐渐▁▁ ; ②同主族元素的原子,从上到下原子半径逐渐▁▁▁▁。 ③稀有气体元素的原子半径▁▁▁同周期元素原子半径。 (2).对离子来说:除符合原子半径递变规律外,经常使用的比较原则是: ①同种元素的原子和离子相比较,阳离子比相应原子半径▁▁,阴离子比相应原子半 径▁▁; ②电子层结构相同的粒子(如O F Na Mg Al 223--+++、、、、),随着核电荷数的▁▁ ▁▁,离子半径▁▁▁▁。 2、微粒半径大小判断简易规律: (1)、同元素微粒:r 阳离子 ? r 原子 ? r 阴离子 (2)、同主族微粒:电子层数越多,半径越大 (3)、电子层数相同的简单微粒:核电荷数越大,半径越小 3、判断三部曲 第一步... 先看电子层数,因为其半径大小的决定因素是电子层数。电子层数越多,其半径越大。 第二步... 在电子层数相同的情况下看核电荷数,因为核电荷数的多少是影响半径大小的次要因素。而核电荷数越多,其半径越小。 第三步... 在电子层数和核电荷数相同的情况下看电子数,核外电子数是影响半径大小的最小因素。核外电子数越多,其半径越大。 值得注意的是此三步不可颠倒。 4、填空 1)、同周期原子半径随原子序数的递增而 r(Na) r(Mg) r(Al) r(Si) r(P) r(S) r(Cl) 2)、同主族原子半径随原子序数的递增而 r(Li) r(Na) r(K) r(Rb) r(F) r(Cl) r(Br) r(I) 3)、同周期阳(阴)离子半径随原子序数的递增而 。 r(Na +) r(Mg 2+) r(Al 3+) r(P 3-) r(S 2-) r(Cl -) 4)、同主族阳(阴)离子半径随原子序数的递增而 r(Li +) r(Na +) r(K +) r(F -) r(Cl -) r(Br -) r(I -) 5)、同种元素的原子、离子,其电子数越多半径就 r(Fe 3+) r(Fe 2+) r(Fe) r(Cl -) r(Cl) 6)、电子层结构相同的离子,核电荷数越大,离子的半径 r(O 2-) r(F -) r(Na +) r(Mg 2+) r(Al 3+) 二、例题部分 例1:下列化合物中,阴离子和阳离子的半径之比最大的是( )
(完整版)粒子半径大小的比较规律
粒子半径大小的比较规律 原子和简单离子半径大小的比较是高考的一个重要考点,掌握比较的方法和规律,才能正确判断粒子半径的大小。中学化学里常见粒子半径大小比较,规律如下: 1.同种元素粒子半径大小比较: 同种元素原子形成的粒子,核外电子数越多,粒子半径越大。阳离子半径小于相应原子半径。如r(Na+)
离子半径
一、原子或离子半径大小比较 电子层数相同条件下,电子层越多,半径越大。 判断的依据核电荷数相同条件下,核电荷数越多,半径越小。 最外层电子数相同条件下,最外层电子数越多,半径越大。 微粒半径的比较1、同周期元素的原子半径随核电荷数的增大而减小(稀有气体除外) 2、同同周期元素的离子半径 3同主族元素的原子半径随核电荷数的增大而增大。 具体规律4、同主族元素的离子半径随核电荷数的增大而增大 5、电子层结构相同的离子半径随核电荷数的增大而减小。 6、同一元素不同价态的微粒半径,价态越高离子半径越小 比较下列微粒的半径大小 ①比较Na原子与Mg原子的原子半径大小②比较Na原子与Li原子的原子半径大小③比较Na与Na+的半径大小④比较Cl-与Cl的半径大小 ⑤比较Fe、Fe2+与Fe3+的半径大小⑥比较Na+与Mg2+半径大小 ⑦比较O2-与F-半径大小⑧写出下列微粒的半径由大到小的顺序:F-、O2-、Na+、Mg2+⑨在Na、K、O、N、C.Li、F、H八种元素中,原子半径由小到大的顺序为____ ____ ⑩下列化合物中,阳离子与阴离子半径比最小的是()A.NaF B.LiI C.CsF D.LiF 二、有关的微粒电子层结构 1.下列微粒中,电子层结构完全相同的一组是()A.S2-、Cl-、K+B.Cl-、Br-、I-C.Na+、 Mg2+、F-D.O2-、Mg2+、Cl- 2.下列各组微粒具有相同的质子数和电子数的是 A.OH-、H2O、F-B.NH3、NH4+、NH2-C.H3O+、NH4+、NH2-D.HCl、F2、H2S 3.A和B是前三周期的元素,它们的离子A2+和B3+具有相同的核外电子层结构,下列说法正确的是A.原子半径:A>B B.原子序数:A>B C.离子半径:A2+>B3+D.质量数:A>B 4.A元素的阳离子和B元素的阴离子具有相同的电子层结构。下列叙述正确的是 A.原子半径:AB C.原子最外层上电子数:B>A D.A的正价与B的负价的绝对值相等 5.已知元素X、Y的核电荷数分别是a和b,且它们的离子X m+和Y n-的核外电子排布相同,则下列关系式中正确的是 A.a=b+m+n B.a=b-m+n C.a=b+m-n D.a=b-m-n 6.a、b、c三种元素的原子序数均小于20,a、b两元素的阳离子和c元素的阴离子都有相同的电子层结构,a原子的半径大于b原子的半径,则三种元素的原子序数的关系是()A.a>b>c B.b >a>c C.c>b>a D.a>c>b 7.A.B均为原子序数1~20的元素,已知A的原子序数为n,A2+离子比B2-离子少8个电子,则B的原子序数是 A.n+4 B.n+6 C.n+8 D.n+10 三、元素性质递变规律 1、下列各组元素中,按最高正价递增顺序排列的是()A.C.N、O、F B.K、Mg、C.S C.F、
离子半径大小的比较规律
离子半径大小的比较规 律 Document number:WTWYT-WYWY-BTGTT-YTTYU-2018GT
粒子半径大小的比较规律 1.同种元素粒子半径大小比较: 同种元素原子形成的粒子,核外电子数越多,粒子半径越大。阳离子半径小于相应原子半径。如r(Na+)
高中化学粒子半径大小的比较专题辅导
粒子半径大小的比较 粒子半径大小的比较是考试中常见题型, 也是同学们容易出错的试题。出错的原因主要是未能掌握粒子半径大小的比较规律。 本文从影响粒子半径大小的原因着手分析,总结出比较规律,以便于运用。 一、不同元素 1、同周期元素的原子和离子。 从左到右,随着核电荷数的递增, 元素的原子半径依次减小,阳离子半径依次减小,阴离子半径也依次减小。如Cl S ,Al Mg Na ,Si Al Mg Na 232。 2、同主族元素的原子和离子。 从上到下,随着核电荷数的递增,元素的原子半径依次增大,离子半径依次增大。如 I Br Cl F ,Cs Rb K Na Li ,Cs Rb K Na Li 。3、电子层结构相同的离子。随着核电荷数的递增,离子半径依次减小。如:Na F ,Ca K Cl S 2222Mg 3Al 。 4、无法直接比较的粒子。 可借助参照物进行比较,如2S 与3Al 的离子半径大小的比较,可借助于2O ,由于,S O Al 223所以23S Al 。 二、同种元素 1、阳离子<中性原子<阴离子。 2、元素价态越高的粒子,半径越小,如H H H ,Fe Fe Fe 23。 综上所述,可以得到以下规律:要判断粒子半径的大小,首先应看电子层数。一般情况 下,电子层数越多,半径越大;若电子层数相同,则看核电荷数,核电荷数越大,半径越小;若电子层数相同,核电荷数也相同,则看核外电子数,核外电子数越多,半径越大。 三、示例分析 [题目]下列有关粒子半径的大小关系正确的是( )A. 钠离子半径大于氧离子半径 B. 硫原子半径大于锂原子半径 C. 氢原子半径大于H 的半径 D. 氯原子半径大于氯离子半径 [解析]A 项中,钠离子与氧离子的电子层结构相同,钠的核电荷数较大,所以其离子 半径较小;B 项中,虽然硫原子比锂原子多一个电子层,但由于一种为金属元素,另一种为 非金属元素,所以二者的关系不能仅仅从电子层的多少进行判断,实际上原子半径:S Li ;C 项中,氢原子比H 多一个电子层,所以氢原子半径较大;D 项中,氯原子与氯离子的电子层数相同,但由于氯离子的核外电子数较多,电子间的排斥作用强,所以氯离子半径较大。故答案为C 。 [点评]对于同周期或同主族的元素,要利用同周期、同主族元素性质的递变规律进行分析;对于不同周期、不同主族的元素,要借助其他相关元素进行分析;对于同一种元素, 要利用电子层数或核外电子数的大小关系进行分析。
元素周期律——原子、离子半径比较
元素周期律——原子、离子半径比较 原子半径比较 同周期从左到右依次减小,同主族从上到下依次增大(稀有气体除外) 1、为什么原子半径同周期从左到右依次减小? 同周期元素的原子,电子层数一样,随核电荷数的增大,原子核对核外电子的吸引增强,原子半径逐渐减小。(核外电子数增加了,吸得越紧了) 2、为什么原子半径同主族从上到下依次增大? 同一主族元素,从上到下,原子核的质子逐渐增多,核外电子数也逐渐增多,核外排布的电子层也逐渐增多,电子层的多少影响原子的半径大小,电子层的增多,意味着原子直径的增大,所以同一主族元素,原子半径从上到下逐渐增大。 离子半径比较 (1)同一元素的微粒,电子数越多,半径越大。 如:钠原子>钠离子,氯原子<氯离子 (2)同一周期内元素的微粒,阴离子半径大于阳离子半径。 如:氧离子>锂离子(电子层影响) (3)同类离子与原子半径比较相同。 如:钠离子>镁离子>铝离子,氟离子<氯离子<溴离子 (4)具有相同电子层结构的离子(单核),核电荷数越小,半径越大。 如:氧离子>氟离子>钠离子>镁离子>铝离子;硫离子>氯离子>钾离子>钙离子 (5)同一元素高价阳离子半径小于低价阳离子半径,又小于金属的原子半径。(越负越勇)如:铜离子<亚铜离子<铜原子负二价硫>硫原子>四价硫>六价硫 比较微粒(原子、离子)半径大小的依据——“三看规则” 一看电子层数:在电子层数不同时,电子层数越多,半径越大; 二看核电荷数:在电子层数相同时,核电荷数越大,半径越小; 三看电子数:在电子层数和核电荷数都相同时,电子数越多,半径越大.(同种元素,非金属)1.根据表1信息,判断以下叙述正确的是___C__. 表1 部分短周期元素的原子半径及主要化合价 A.R6+比R2-半径大 B.单质与稀盐酸反应的速率为L<Q C.M与T形成的化合物具有两性 D.M3+比T2-的半径小 2、已知短周期元素的离子aAm+、bBn +、cCm-、dDn-(m<n)都具有相同的电子层结构,则下列叙述正确的是( D )
区别金属原子半径、离子半径、共价半径和范德华半径和碳材料的分类及应用
区别金属原子半径、离子半径、共价半径和范德华半径根据量子力学,核外电子运动没有固定轨道,没有明确的界限,只有几率密度的分布。通常把核到最外层电子的平均距离定义为原子半径。现代的科学技术 还无法精确测定一个单独原子的半径,只能用实验方法,如X射线衍射法,测定出晶体中相同原子核间距离,或用同核双原子分子键长,被2相除得出。不同元素原子有不同的存在形式,就是同一元素的原子也可能形成不同化学键的分子和晶体。因而不同元素的原子半径可能表现形式不同,就是同一元素的原子半径也可能有不同形式。根据测定方法的不同,通常有3种原子半径: ①金属半径:金属晶体中相邻两金属原子核间距离的一半,称做该元素原子的金属半径,如铜的金属半径r 金 =127.8pm。 ②共价半径:同种元素的两原子以共价键结合时,其共价键键长的一半称做该元素原子的共价半径,符号表示为pm 或?,其数值与几重键结合有关,如碳原子的共价半径r共,单键时为77pm,双键时为67pm,三键时为60pm。金属元素原子在一定条件下也可形成共价的双原子分子,金属元素原子也有共价 半径,如铜的共价半径r 共 为117pm。由于形成共价键时,总会发生原子轨道重叠,通常同一金属元素的金属半径比其单键共价半径要大10%~15%。同周期元素的单键共价半径的变化规律为从左至右逐渐缩小,可认为是原子核对电子引力增大的缘故 ③范氏半径:(范德华氏 半径的简称) 非金属元素和 有些金属元素所形成的分子 间或稀有气体单原子分子间 靠分子间力(范德华力) 相 互吸引,其不同分子中两个相 同原子核间距离的一半,称做 该元素原子的范氏半径,如氯 原子的范氏半径r 范 为 181pm。如左图所示,表示了氯原子的共价半径和范氏半径。 原子半径数据只有相对的、近似的意义,而且同一元素的不同半径,数值不 同(r 范>r 金 >r 共 ),而且相差较大。使用时不要同时用不同半径的数据。在一般的 资料里,金属元素有金属半径和共价半径的数据,非金属元素则有共价半径和范氏半径的数据,稀有气体只有范氏半径的数据。 而离子半径是表示离子大小的一个物理量。在离子型晶体中,组成晶格的质点是大小不等的圆球状的正负离子,因为具有稀有气体电子层结构的离子,都有球面对称性,而且离子间极化影响不大,可把晶体中离子看做圆球。在晶体中,两个带异号电荷的圆球互相接触,到一定平衡距离时就不再接近了。现代测试手段还不能直接量取正负离子球体的半径。一般所说的离子半径是:离子晶体中正负离子的核间距离是正负离子的半径之和。正负离子的核间距为d,则d=r++r-。数值d可通过晶体的X射线衍射分析实验测得。并以氟离子F-半径=133pm,或氧离子O2-半径=132pm作为标准,然后再推算出其他离子半径。如实验测得的氟化钠的d=230pm,则Na+的半径是230-133=97pm。离子半径的大小还要受离子化合物构型的影响。一般以氯化钠构型的半径作为标准,即以配位数为6作标准(在每一个钠离子周围直接连有6个氯离子,反之亦然。将与钠离子或氯离子直接相连的带异电荷的离子数称为配位数)。如离子实际配位数
