元素在周期表中位置的判断

元素在周期表中位置的判断
元素在周期表中位置的判断,是一个考点,掌握方法,解题非常快捷。
1.根据原子结构示意图判断
此法适用于主族元素。电子层数对应周期数,最外层电子数对应主族序数。
例:判断Cl元素的位置:
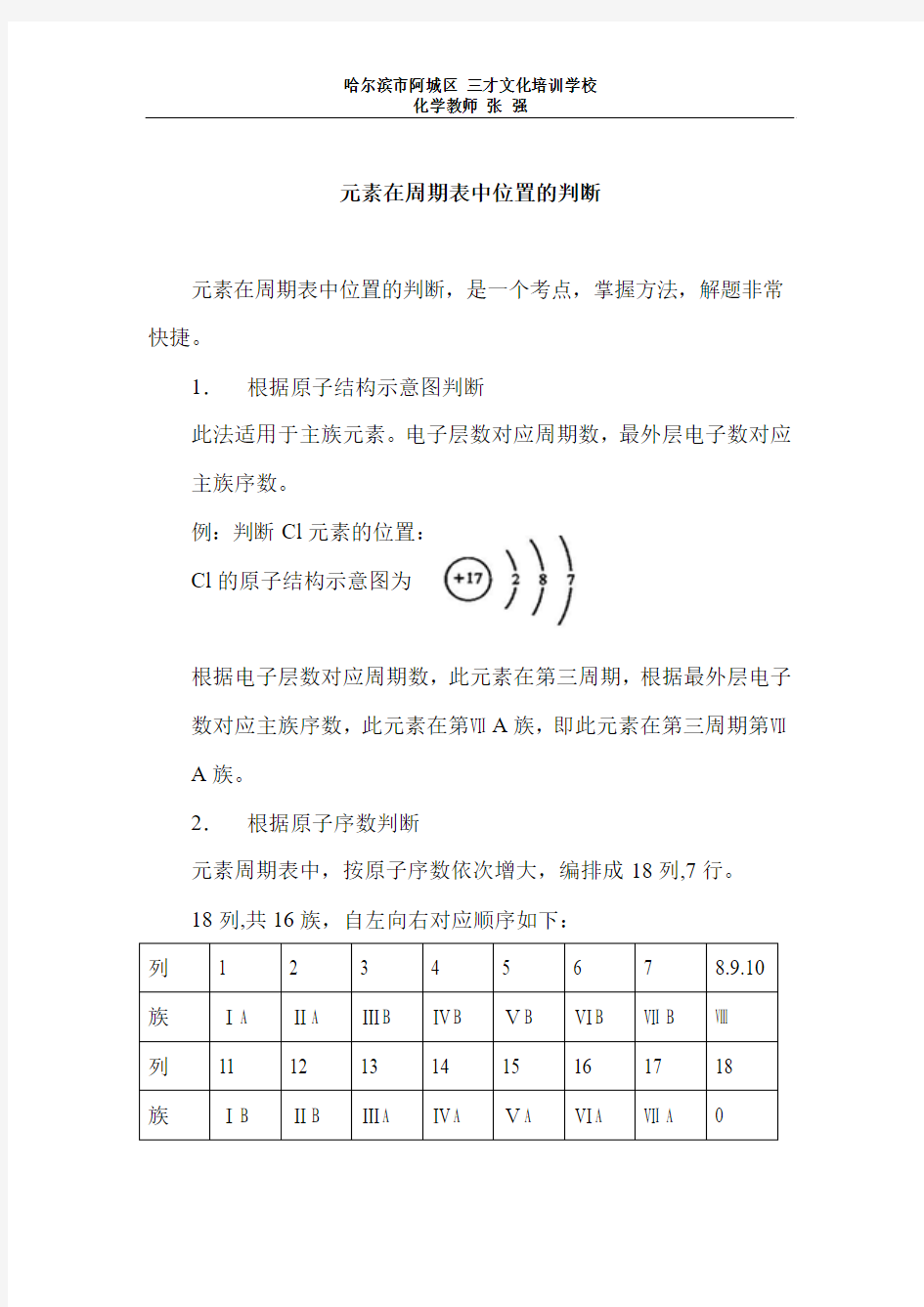
Cl的原子结构示意图为
根据电子层数对应周期数,此元素在第三周期,根据最外层电子数对应主族序数,此元素在第ⅦA族,即此元素在第三周期第ⅦA族。
2.根据原子序数判断
元素周期表中,按原子序数依次增大,编排成18列,7行。
18列,共16族,自左向右对应顺序如下:
7行,共七个周期,自上向下对应顺序如下:
例:原子序数为39的元素:
39在36与54之间,所以此元素在第五周期。
39与36接近,36对应18列,则37对应1列,以此类推,39对应3列,即第ⅢB族。即此元素在第五周期第ⅢB族。
注:(1)第六周期中,镧系57-71号只占据第ⅢB族一个位置,所以72-86号之间的元素须先减去14,然后再对应列。
(2)第七周期中,锕系89-103号只占据第ⅢB族一个位置,所以103号以上的元素须先减去14,然后再对应列。3.根据原子电子排布式判断:
元素周期表根据价电子特征分成5个区:
根据价电子先判断区,无论哪一区,价电子中的n值对应周期。S区中,价电子数对应主族序数。
d区中,价电子数对应副族序数,但价电子数为8,9,10的在第Ⅷ族。
ds 区中,价电子的s上的电子数对应副族序数。
P区中,价电子数对应主族序数,但价电子数为8的在0族。
f区包括镧系和锕系,都在第ⅢB族,只需根据价电子的n值判断周期即可。
例:价电子为5d66s2的元素在周期表中的位置?
根据价电子,首先可判断在d区,则价电子对应副族序数,价电子数为4,在第ⅣB族。
再根据n值为6,所以在第六周期,即此元素在第六周期第ⅣB 族。
类题训练:
根据所给信息,判断元素在周期表中的位置
(1)判断C元素的位置
(2)判断90号元素的位置
(3)判断价电子为3d104s1元素的位置
答案:
(1)C元素的位置:第二周期第ⅣA族。
(2)90号元素的位置:第七周期第ⅢB族。
(3)价电子为3d104s1元素的位置:第四周期第ⅠB族。
元素周期率与元素周期表
专题六元素周期率与元素周期表 【考点分析】 1.掌握元素周期率的实质,了解元素周期表(长式)的结构(周期、族)。 2.以第3周期为例,掌握同一周期内元素性质(如:原子半径、化合价、单质及化合物性质)的递变规律与原子结构的关系;以ⅠA和ⅦA族为例,掌握同一主族内元素性质递变规律与原子结构的关系。 3.以上知识是高考必考内容,常以选择题、简答题和推断填空题的形式出现。 【典型例题】 【例1】例1(2003上海理综)在人体所需的16种微量元素中有一种被称为生命元素的R 元素,对延长人类寿命起着重要的作用。已知R元素的原子有四个电子层,其最高价氧化物分子式为RO3,则R元素的名称 A.硫B.砷C.硒D.硅 【备选1】:周期表前20号元素中,某两种元素的原子序数相差1,它们形成化合物时,原子数之比为1﹕2,写出这些化合物的化学式______________ 【备选2】:X、Y、Z为短周期元素,这些元素原子的最外层电子数分别为1、4、6,则由这三种元素组成的化学式不可能是 A. XYZ B.X2YZ C.X2YZ2 D.X3YZ3 【例2】下列有关物质的性质比较正确的是 (1)同主族元素的单质从上到下,非金属性减弱,熔点增高 (2)元素的最高正化合价在数值上等于它所在的族序数 (3)同周期主族元素的原子半径越小,越难失去电子 (4)元素的非金属性越强,它的气态氢化物水溶液的酸性越强 (5)还原性:S2->Se2->Br->Cl- (6)酸性:HClO4>H2SO4>H3PO4>H2SiO3 A.(1)(3) B.(2)(4) C.(3)(6) D.(5)(6) 【备选1】下表是X、Y、Z三种元素的氢化物的某些性质: 元素熔点/℃沸点/℃与水的反应导电性(纯液体) X -283 -162 不反应不导电 Y -102 19 放热反应,形成酸性溶液不导电 Z 680 / 剧烈反应,生成H2,并形成碱性溶液导电 若X、Y、Z这三种元素属于周期表中的同一周期,则它们的原子序数递增的顺序是
门捷列夫与元素周期表的小故事
门捷列夫与元素周期表不得不说的故事宇宙万物是由什么组成的?古希腊人以为是水、土、火、气四种元素,古代中国则相信金、木、水、火、土五种元素之说。到了近代,人们才渐渐明白:元素多种多样,决不止于四五种。18世纪,科学家已探知的元素有30多种,如金、银、铁、氧、磷、硫等,到19世纪,已发现的元素已达54种。 人们自然会问,没有发现的元素还有多少种?元素之间是孤零零地存在,还是彼此间有着某种联系呢? 门捷列夫发现元素周期律,揭开了这个奥秘。 原来,元素不是一群乌合之众,而是像一支训练有素的军队,按照严格的命令井然有序地排列着,怎么排列的呢?门捷列夫发现:元素的原子量相等或相近的,性质相似相近;而且,元素的性质和它们的原子量呈周期性的变化。 门捷列夫激动不已。他把当时已发现的60多种元素按其原子量和性质排列成一张表,结果发现,从任何一种元素算起,每数到8个就和第一个元素的性质相近,他把这个规律称为“八音律”。 门捷列夫是怎样发现元素周期律的呢? 1834年2月7日,伊万诺维奇·门捷列夫诞生于西伯利亚的托波尔斯克,父亲是中学校长。16岁时,进入圣彼得堡师范学院自然科学教育系学习。毕业后,门捷列夫去德国深造,集中精力研究物理化学。1861年回国,任圣彼得堡大学教授。 在编写无机化学讲义时,门捷列夫发现这门学科的俄语教材都已陈旧,外文教科书也无法适应新的教学要求,因而迫切需要有一本新的、能够反映当代化学发展水平的无机化学教科书。 这种想法激励着年轻的门捷列夫。当门捷列夫编写有关化学元素及其化合物性质的
章节时,他遇到了难题。按照什么次序排列它们的位置呢?当时化学界发现的化学元索已达63种。为了寻找元素的科学分类方法,他不得不研究有关元素之间的内在联系。研究某一学科的历史,是把握该学科发展进程的最好方法。门捷列夫深刻地了解这一点,他迈进了圣彼得堡大学的图书馆,在数不尽的卷帙中逐一整理以往人们研究化学元素分类的原始资料…… 门捷列夫抓住了化学家研究元素分类的历史脉络,夜以继日地分析思考,简直着了迷。夜深人静,圣彼得堡大学主楼左侧的的门捷列夫的居室仍然亮着灯光,仆人为了安全起见,推开了门捷列夫书房的门。 “安东!”门捷列夫站起来对仆人说:“到实验室去找几张厚纸,把筐也一起拿来。” 安东是门捷列夫教授家的忠实仆人。他走出房门,莫名其妙地耸耸肩膀,很快就拿来一卷厚纸。“帮我把它剪开。” 门捷列夫一边吩咐仆人,一边动手在厚纸上画出格子。 “所有的卡片都要像这个格于一样大小。开始剪吧,我要在上面写字。” 门捷列大不知疲倦地工作着。他在每一张卡片上都写上了元素名称、原于量、化合物的化学式和主要性质。筐里逐渐装满了卡片。门捷列夫把它们分成几类,然后摆放在一个宽大的实验台上。接下来的日子,门捷列夫把元素卡片进行系统地整理。门捷列夫的家人看到一向珍惜时间的教授突然热衷于“纸牌”感到奇怪。门捷列夫旁若无人,每天手拿元素卡片像玩纸牌那样,收起、摆开,再收起、再摆开,皱着眉头地玩“牌”…… 冬去春来。门捷列夫没有在杂乱无章的元素卡片中找到内在的规律。有一天,他又坐到桌前摆弄起“纸牌”来了,摆着,摆着,门捷列夫像触电似的站了起来,在他面前出现了完全没有料到的现象,每一行元素的性质都是按照原子量的增大而从上到下地逐渐变化着。门捷列夫激动得双手不断颤抖着。“这就是说,元素的性质与它们的原子量呈周期性
第七讲 元素周期表的九大规律
第七讲元素周期表和元素周期律 一、分析热点把握命题趋向 热点内容主要集中在以下几个方面:一是元素周期律的迁移应用,该类题目的特点是:给出一种不常见的主族元素,分析推测该元素及其化合物可能或不可能具有的性质。解该类题目的方法思路是:先确定该元素所在主族位置,然后根据该族元素性质递变规律进行推测判断。二是确定“指定的几种元素形成的化合物”的形式,该类题目的特点是:给出几种元素的原子结构或性质特征,判断它们形成的化合物的形式。解此类题的方法思路是:定元素,推价态,想可能,得化学式。三是由“位构性”关系推断元素,该类题目综合性强,难度较大,一般出现在第Ⅱ卷笔答题中,所占分值较高。 二.学法指导:1、抓牢两条知识链 (1)金属元素链:元素在周期表中的位置→最外层电子数及原子半径→原子失去电子的能力→元素的金属性→最高价氧化物对应水化物的碱性→单质置换水(或酸)中氢的能力→单质的还原性→离子的氧化性。 (2)非金属元素链:元素在周期表中的位置→最外层电子数及原子半径→原子获得电子的能力→元素的非金属性→最高价氧化物对应水化物的酸性→气态氢化物形成难易及稳定性→单质的氧化性→离子的还原性。 2、理解判断元素金属性或非金属性强弱的实验依据
(1)金属性强弱的实验标志 ①单质与水(或酸)反应置换氢越容易,元素的金属性越强。②最高价氧化物对应的水化物的碱性越强,元素的金属性越强。③相互间的置换反应,金属性强的置换弱的。④原电池中用作负极材料的金属性比用作正极材料的金属性强。⑤电离能 (2)非金属性强弱的实验标志 ①与氢气化合越容易(条件简单、现象明显),元素的非金属性越强。②气态氢化物越稳定,元素的非金属性越强。③最高价氧化物对应的水化物的酸性越强,元素的非金属性越强。④相互间置换反应,非金属性强的置换弱的。⑤电负性 三.规律总结: 1、同周期元素“四增四减”规律 同周期元素从左至右:①原子最外层电子数逐渐增多,原子半径逐渐减小;②非金属性逐渐增强,金属性逐渐减弱;③最高价氧化物对应的水化物的酸性逐渐增强,碱性逐渐减弱;④非金属气态氢化物的稳定性逐渐增强,还原性逐渐减弱。 2、同主族元素“四增四减四相同”规律 同主族元素从上到下:①电子层数逐渐增多,核对外层电子的引力逐渐减弱;②金属性逐渐增强,非金属性逐渐减弱;③非金属气态氢化物的还原性逐渐增强,稳定性减弱;④最高价氧化物对应的水化
确定元素在元素周期表中的位置
稀有气体定位法确定元素在元素周期表中的位置 同学们还在为无法确定元素是第几周期第几族而苦恼吗?今天凹凸个性教育化学系的王玉帅老师就来教大家如何利用稀有气体元素来给元素进行定位。 首先大家要牢牢记住稀有气体元素的原子序数2,10,18,36,54,86,118,(简单记忆稀有气体元素原子序数的方法:记住第一个数是2,依次加8/8/18/18/32/32就可以推算出后面的数了)这7个元素位于每个周期的最后一个位置上,也就是说每个周期的元素排列如下所示: 第一周期:1-2 第二周期:3-10 第三周期:11-18 第四周期:19-36 第五周期:37-54 第六周期:55-86 第七周期:87-118 我们得到一个化学元素根据上面编列情况就可以判断出该元素所属的周期,如铁元素的原子序数是26,26在19-36这个范围内,也就是说铁是第四周期的元素。铂的原子序数是78,78在55-86这个范围内,也就是说铂是第六周期的元素。 然后大家要记住元素周期表族排列的规律:ⅠA,ⅡA、ⅢB、ⅣB、ⅤB、ⅥB、ⅦB、Ⅷ、ⅠB,ⅡB、ⅢA、ⅣA、ⅤA、ⅥA、ⅦA,0 需要特殊注意以下几点: 1.短周期元素(前18号元素)直接靠我们初中背诵的口诀进行记忆。 2.第Ⅷ族的有3个列需要注意,第六周期和第七周期的第ⅢB族会有15个列(锕 系元素镧系元素) 接下来判断族的方法如下: 比如铁是26号元素,我们上面讲过自己根据稀有元素的原子序数列出一个上述的表格,26属于19-36这个范围即是属于第四周期的元素,然后将第四周期的元素展开即是19、20、21、22、23、24、25、26、根据元素周期表族排列的规律,19对应ⅠA,20对应ⅡA、21对应ⅢB,22对应ⅣB,23对应ⅤB、24对应ⅥB、25对应ⅦB,26,27,28这三个对应着Ⅷ,29对应着ⅠB,30对应着ⅡB,31对应着ⅢA,32对应着ⅣA,33对应着ⅤA,34对应着ⅥA、35对应着ⅦA、36对应着0族,可以判断出铁元素是Ⅷ族的。 比如金元素的原子序数是79,根据周期元素的排列规律,79属于55-86范围内,所以金元素是第六周期的元素。将第六周期的元素展开为:55,56,57,58,59,60,61,62,63,64,65,66,67,68,69,70,71,72,73,74,75,76,77, 78,79…之前和大家说过六七周期要考虑锕系元素和镧系元素(都是ⅢB有15位),即55是ⅠA,56对应ⅡA,57-71这15个都是ⅢB,72对应ⅣB,73对应ⅤB、74对应ⅥB、75对应ⅦB,,76,77,78这三个对应着Ⅷ,79对应着ⅠB,所以79号金元素是第ⅠB族的元素。 再举一个例子来分析,如锡元素是50号元素,(即原子序数50),50根据周期排列规律,50属于37-54这个范围即是第五周期的元素。将第五周期元素展开,37,38,39,40,41,41,43,44,45,46,47,48,49,50…,37ⅠA,38ⅡA、39ⅢB,40ⅣB,41ⅤB、42ⅥB、43ⅦB,44-46这三个对应着Ⅷ,47ⅠB,48ⅡB,49ⅢA,
元素周期表与元素周期律专题复习
元素周期表与元素周期律专题复习 【考点突破】 一、高考风向标 物质结构与元素周期律这部分知识主要出现在选择题及填空题中。在选择题中,主要是有关原子结构的计算、同位素、元素周期律中物质或元素性质的递变规律、元素在周期表中的位置与其性质的关系、化合物中原子的电子排布、分子的结构、晶体的结构和性质、新发现的元素等。在非选择题中,主要考查元素的推断,物质的结构、性质、位置三者的关系。在高考卷中,本部分试题一般3个左右,分值为25分(03年,3道27分;04,2道12分;05年,三套试题中:第I套3道27分;第II套3道25分;第III套没有出现)由于本章内容是对元素化合物知识的概括和总结,同时对元素化合物性质的学习和归纳又具有积极的指导意义,所以我们在复习本章知识时,一定要注意总结规律、找出特例,明确失分点及其产生的原因,有目的、有针对性地进行复习。 可以预测2006年高考试题中,元素位、构、性三者的关系仍是高考命题的主要依据,对这三者的关系,高考常以原子序数大小、原子或离子半径大小、离子氧化性或还原性强弱等比较型试题和物质的组成、元素位置及化合价、化合物的性质、结构推断等题型进行考查,此类知识点常以选择题和推断题的形式出现。 二、高考考点逐个突破 1. 考查原子结构 例1. (05上海高考)下列离子中,电子数大于质子数且质子数大于中子数的是() A. D3O+ B. Li+ C. OD- D. OH- 解析:对于中性微粒,质子数等于电子数;对于阳离子,由于失电子,造成质子数大于电子数;对于阴离子,质子数小于电子数。“电子数大于质子数”的只可能为C、D,但能满足“质子数大于中子数”的只有D。答案为D 评析:电子数与质子数的大小关系,不需要看具体的数据,只需看离子所带电荷的性质。对于中性的分子或原子来说,质子数与电子数相等;对于阳离子来说,质子数大于电子数;对于阴离子来说,质子数小于电子数。至于质子数与中子数的关系,必须知道粒子的质子数和质量数,只要有一个不清楚,二者的关系就不能确定。 2. 考查原子半径 例2. (02江苏综合)下列叙述正确的是() A. 同周期元素中VIIA族元素的原子相对质量大 B. VIA族元素的原子,其半径越大,越容易得到电子 C. 室温时,零族元素的单质都是气体 D. 所有主族元素的原子,形成单原子离子时的化合价和它的族序数相等 解析:此题主要考查元素周期表中,同周期同主族元素性质的一些递变规律,在同周期中零族元素的原子半径最大,而在同主族中,半径越大,越难得到电子。单原子离子的化合价和它的族序数不一定相等,如IV A族铅形成的Pb2+。答案为C。 评析:对于同主族元素来说,从上到下,原子半径及相对应的离子半径依次增大;总的来说,相对原子质量依次增大;零族元素的单质全部为气体,IIA族、IIIA族、IV A族元素的单质全部为固体,V A、VIA族元素中只有氮气和氧气常温下呈气态(其余都为固态),VIIA族元素的单质既有气体、液体、还有固体。
门捷列夫的化学元素周期表与卡片分析法
中国职工科技报/2007年/4月/20日/第004版 科普家园 门捷列夫的化学元素周期表与卡片分析法 王振宇 卡片时于研究文学艺术和社会科学很重要,对于研究自然科学特别是发明创造也同样重要。运用卡片分析法取得重大成果的最著名的事例。就是俄国化学家门捷列夫发现化学元素周期率。1869年,为了研究已发现的60多种元素之间的关系,研究元素的质量和化学性质的关系,门捷列夫将搜集来的各种元素的名称写在纸上,并记下它们的原子量和基本性质,把相似的元素和相近的原子量排列在一起:他又从最小的原子量开始选取元素,并把它们按原子量的顺序排列,经过分析研究,终于发现了元素的性质存在着周期性,从而发现了化学元素周期律,并根据周期率编制了第一张化学元素周期表。 从以上事例可以看出,卡片分析法的基础是要有卡片。卡片大小自便,扑克牌大小也可,稍大也可,能在上面记录信息即可。卡片上面都记录什么呢?以下方面可供参考:突然涌现的想法:由谈话、读书、观察等产生的设想或注意到的问题;图书、杂志、人名、地址、电话号码;被记述或证实的信息;从智力激励法等创造性开发会议中产生的新设想:有关行动计划。的基本设想:使数据系统化的各种形式:发现数据存在的场所、收集的来源以及技法;数据的种类:意想不到的偶然事件;从大脑中一闪即过的有创意的新设想,等等。 卡片分析法是一种发挥综合思维作用的方法,通过将所得到的记录有有关信息或设想的卡片。进行分析,进行整理排列,以寻找各部分之间的有机联系,从整体上把握事物,最后形成比较系统的新设想。该法作为分析整理资料获得启发的有效途径,可用于解决问题的各个阶段中。在分析中要把对象的各个部分、各个方面和种种因素联系起来考虑。综合不是主观地、任意地把对象的各部分捏合在一起,也不是各个部分的机械相加,不是各种因素的简单堆砌,而是按照对象各部分间的有机联系,从总体上把握事物的一种方法。它不是抽象地、从外部现象的联结上来认识事物,而是抓住事物的本质,即抓住事物在总体上相互联结而又矛盾的特殊性,研究这一矛盾怎样制约着事物丰富多彩的属性,怎样在事物的运动中展现出整体的特征。 卡片分析法具有以下一些特点:首先,这是一种在比较分类的基础上,由综合进行创新的方法比较和分类是运用此法时要做的基本工作,然而,真正有创意的工作在于时各类资料的综合:其次,运用这种方法时,不只是对卡片的理性分析和综合,还需要综合地发挥运用者的各种心理因素,如感受、感情、直观、意志等,因为对卡片的分析整理直接受到这些圆素的影响:第三,此法借助于卡片分析事理发现其内在联系,具有直观、方便、灵活的特点。既可单人应用,也可集体进行,应用范围广,几乎适用于各领域的创造性活动。 卡片分析法在各种研究和发明创造过程中,有着特殊的作用。将待处理的信息卡片化,具有克服人脑思维限度的功能,从而成为整理分析资料获得启发的有效方法。人的思维能力虽然是无限的,但一个人在思维中同时操作的思维元素数是很有限的,实验证明,一般人当同时思维操作的信息元素超过10个时,要在脑内同时操作加工这些信息显得很困难。而通过卡片,把各种信息或设想转移到脑外,变成能稳定地呈现在眼前的外存信息,这样既可把在头脑中借助记忆进行的思维操作转为脑外自理卡片,来减轻思维负担,又可使注意力集中,从而提高了思维效率。 (四十五) 第1页共1页
元素周期表的规律总结
元素周期表的规律 一、原子半径 同一周期(稀有气体除外),从左到右,随着原子序数的递增,元素原子的半径递减;同一族中,从上到下,随着原子序数的递增,元素原子半径递增。 二、主要化合价(最高正化合价和最低负化合价) 同一周期中,从左到右,随着原子序数的递增,元素的最高正化合价递增(从+1价到 +7价),第一周期除外,第二周期的0、F元素除外最低负化合价递增(从-4价到-1价)第 一周期除外,由于金属元素一般无负化合价,故从W A族开始。元素最高价的绝对值与最低价的绝对值的和为8 三、元素的金属性和非金属性 同一周期中,从左到右,随着原子序数的递增,元素的金属性递减,非金属性递增; 同一族中,从上到下,随着原子序数的递增,元素的金属性递增,非金属性递减; 四、单质及简单离子的氧化性与还原性 同一周期中,从左到右,随着原子序数的递增,单质的氧化性增强,还原性减弱;所 对应的简单阴离子的还原性减弱,简单阳离子的氧化性增强。同一族中,从上到下,随着原子序数的递增,单质的氧化性减弱,还原性增强;所对应的简单阴离子的还原性增强, 简单阳离子的氧化性减弱。元素单质的还原性越强,金属性就越强;单质氧化性越强,非金属性就越强。 五、最高价氧化物所对应的水化物的酸碱性 同一周期中,从左到右,元素最高价氧化物所对应的水化物的酸性增强(碱性减弱); 同一族中,从上到下,元素最高价氧化物所对应的水化物的碱性增强(酸性减弱)。 元素的最高价氢氧化物的碱性越强,元素金属性就越强;最高价氢氧化物的酸性越强, 元素非金属性就越强。 六、单质与氢气化合的难易程度 同一周期中,从左到右,随着原子序数的递增,单质与氢气化合越容易; 同一族中,从上到下,随着原子序数的递增,单质与氢气化合越难。 七、气态氢化物的稳定性 同一周期中,从左到右,随着原子序数的递增,元素气态氢化物的稳定性增强; 同一族中,从上到下,随着原子序数的递增,元素气态氢化物的稳定性减弱。 此外还有一些对元素金属性、非金属性的判断依据,可以作为元素周期律的补充: 随同一族元素中,由于周期越高,价电子的能量就越高,就越容易失去,因此排在下面 的元素一般比上面的元素更具有金属性。元素的气态氢化物越稳定,非金属性越强。 同一族的元素性质相近。 以上规律不适用于稀有气体。 八、位置规律判断元素在周期表中位置应牢记的规律: (1)元素周期数等于核外电子层数; (2 )主族元素的族数等于最外层电子数。 九、阴阳离子的半径大小辨别规律 三看: 一看电子层数,电子层数越多,半径越大, 二看原子序数,当电子层数相同时,原子序数越大半径反而越小三看最外层电子数,当电子层数和原子序数相同时最外层电子书越多半径越小 + 2+ 3+ 2- - r(Na)>r(Mg)>r(AI)>r(S)>r(CI)、r(Na ) >r(Mg )>r(AI 卜 r(0 ) >r(F) r(S2—)>r(CI—)>r(Ar) >r(K+)>r(Ca2+)、r(02—)> r(F—)> r ( Na+) > r ( Mg2+) > r (Al3+)
元素周期表中知识点及误区判断
元素周期表中知识点及误区判断 高中化学作为高中生必修课程,主要目的是提高学生的化学素质、创 新能力和实践能力,其中对化学方程式的掌握是至关重要的。下面有途高考 网小编整理了《元素周期表中知识点及误区判断》,希望对你有帮助。 ?1、原子结构(1).所有元素的原子核都由质子和中子构成。正例:612C 、613C 、614C三原子质子数相同都是6,中子数不同,分别为6、7、8。反例1:只有氕(11H)原子中没有中子,中子数为0。(2).所有原子的中子数都大 于质子数。正例1:613C 、614C 、13H 等大多数原子的中子数大于质子数。正例2:绝大多数元素的相对原子质量(近似等于质子数与中子数之和)都大于 质子数的2倍。反例1:氕(11H)没有中子,中子数小于质子数。反例2:氘(11H)、氦(24He)、硼(510B)、碳(612C)、氮(714N)、氧(816O)、氖(1020Ne)、镁(1224Mg)、硅(1428Si)、硫(1632S)、钙(2040Ca)中子数等于质子数,中子数不大于质子数。(3).具有相同质子数的微粒一定属于同一种元素。正例:同一 元素的不同微粒质子数相同:H+ 、H- 、H等。反例1:不同的中性分子可以质子数相同,如:Ne、HF、H2O、NH3、CH4 。反例2:不同的阳离子可以质子数相同,如:Na+、H3O+、NH4+ 。反例3:不同的阴离子可以质子数相同,如:NH4+ 、OH-和F-、Cl和HS。2、电子云(4).氢原子电子云图中,一个小黑点就表示有一个电子。含义纠错:小黑点只表示电子在核外该处空 间出现的机会。3、元素周期律(5).元素周期律是指元素的性质随着相对原子 质量的递增而呈周期性变化的规律。概念纠错:元素周期律是指元素的性质 随着原子序数的递增而呈周期性变化的规律。(6).难失电子的元素一定得电子 能力强。反例1:稀有气体元素很少与其它元素反应,即便和氟气反应也生
阅读材料:门捷列夫与元素周期表
门捷列夫与元素周期表 在化学教科书中,都附有一张“元素周期表”。这张表揭示了物质世界的秘密,把一些看来似乎互不相关的元素统一起来,组成了一个完整的自然体系。它的发明,是近代化学史上的一个创举,对于促进化学的发展,起了巨大的作用。看到这张表,人们便会想到它的最早发明者——门捷列夫。 门捷列夫生平简介 德米特里·伊万诺维奇·门捷列夫生于一八三四年二月七日俄国西伯利亚的托波尔斯克市。这个时代,正是欧洲资本主义迅速发展时期。生产的飞速发展,不断地对科学技术提出新的要求。化学也同其它科学一样,取得了惊人的进展。门捷列夫正是在这样一个时代,诞生到人间。门捷列夫从小就热爱劳动,热爱学习。他认为只有劳动,才能使人们得到快乐、美满的生活;只有学习,才能使人变得聪明。 门捷列夫在学校读书的时候,一位很有名的化学教师,经常给他们讲课。热情地向他们介绍当时由英国科学家道尔顿始创的新原子论。由于道尔顿新原于学说的问世,促进了化学的发展速度,一个一个的新元素被发现了。化学这一门科学正激动着人们的心。这位教师的讲授,使门捷列夫的思想更加开阔了,决心为化学这门科学献出一生。 门捷列夫在大学学习期间,表现出了坚韧、忘我的超人精神。疾病折磨着门捷列夫,由于丧失了无数血液,他一天一天的消瘦和苍白了。可是,在他贫血的手里总是握着一本化学教科书。那里面当时有很多没有弄明白的问题,缠绕着他
的头脑,似乎在召呼他快去探索。他在用生命的代价,在科学的道路上攀登着。他说,我这样做“不是为了自己的光荣,而是为了俄国名字的光荣。”——过了一段时间以后,门捷列夫并没有死去,反而一天天好起来了。最后,才知道是医生诊断的错误,而他得的不过是气管出血症罢了。 由于门捷列夫学习刻苦和在学习期间进行了一些创造性的研究工作,一八五五年,他以优异成绩从学院毕业。毕业后,他先后到过辛菲罗波尔、敖德萨担任中学教师。这期间,他一边教书,一边在极其简陋的条件下进行研究,写出了《论比容》的论文。文中指出了根据比容进行化合物的自然分组的途径。一八五七年一月,他被批准为彼得堡大学化学教研室副教授,当时年仅二十三岁。 攀登科学高峰的路,是一条艰苦而又曲折的路。门捷列夫在这条路上,也是吃尽了苦头。当他担任化学副教授以后,负责讲授《化学基础》课。在理论化学里应该指出自然界到底有多少元素?元素之间有什么异同和存在什么内部联系?新的元素应该怎样去发现?这些问题,当时的化学界正处在探索阶段。近五十多年来,各国的化学家们,为了打开这秘密的大门,进行了顽强的努力。虽然有些化学家如德贝莱纳和纽兰兹在一定深度和不同角度客观地叙述了元素间的某些联系,但由于他们没有把所有元素作为整体来概括,所以没有找到元素的正确分类原则。年轻的学者门捷列夫也毫无畏惧地冲进了这个领域,开始了艰难的探索工作。 他不分昼夜地研究着,探求元素的化学特性和它们的一般的原子特性,然后将每个元素记在一张小纸卡上。他企图在元素全部的复杂的特性里,捕捉元素的共同性。但他的研究,一次又一次地失败了。可他不屈服,不灰心,坚持干下去。 为了彻底解决这个问题,他又走出实验室,开始出外考察和整理收集资料。一八五九年,他去德国海德尔堡进行科学深造。两年中,他集中精力研究了物理化学,使他探索元素间内在联系的基础更扎实了。一八六二年,他对巴库油田进行了考察,对液体进行了深入研究,重测了一些元素的原子量,使他对元素的特性有了深刻的了解。一八六七年,他借应邀参加在法国举行的世界工业展览俄罗斯陈列馆工作的机会,参观和考察了法国、德国、比利时的许多化工厂、实验室,大开眼界,丰富了知识。这些实践活动,不仅增长了他认识自然的才干,而且对他发现元素周期律,奠定了雄厚的基础。
元素周期表规律总结
元素周期表规律总结 一。主族元素的判断方法:符合下列情况的均是主族元素 1. 有1~3个电子层的元素(除去He、Ne、Ar); 2。次外层有2个或8个电子的元素(除去惰性气体); 3. 最外层电子多于2个的元素(除去惰性气体); 二。电子层结构相同的离子或原子(指核外电子数与某种惰性元素的电子数相同而且电子层排布也相同的单核离子或原子) (1)2个电子的He型结构的是:H-、He、Li+、Be2+; (2)10个电子的Ne型结构的是:N3—、O2-、F—、Ne、Na+、Mg2+、Al3+ (3)18个电子的Ar型结构的是:S2—、Cl-、Ar、K+、Ca2+ 三。电子数相同的微粒(包括单核离子、原子、也包括多原子分子、离子) 1。2e—的有:H-、H2、He、Li+、Be2+; 2. 10e-的有:N3-、O2-、F—;Na+、Mg2+、Al3+;Ne、HF、H2O、NH3、CH4(与Ne同周期的非金属的气态氢化物)NH4-、NH2-、H3O+、OH—; 3. 18e-的有:S2—、CL-、Ar、K+、CA2+;SiH4、PH3、H2S、HCl(与Ar同周期的非金属的气态氢化物);HS—、PH4+及、H2O2、F2、CH3-OH、CH3—CH3、CH3-F、CH3-NH2、NH2—NH2、NH2-、OH—等. 四. 离子半径的比较: 1. 电子层结构相同的离子,随原子序数的递增,离子半径减小. 2。同一主族的元素,无论是阴离子还是阳离子,电子层数越多,半径越大。即从上到下,离子半径增大. 3。元素的阳离子半径比其原子半径小,元素的阴离子半径比其原子半径大。 五。同一主族的相邻两元素的原子序数之差,有下列规律: 1。同为IA、IIA的元素,则两元素原子序数之差等于上边那种元素所在周期的元素种类数。
第1节 元素周期表(带详细解析)_
第一章 物质结构 元素周期律 第一节 元素周期表 重难点一 元素周期表 1.构成原子(离子)的微粒间关系 (1)原子序数=核电荷数=核内质子数=核外电子数(原子中)。 (2)离子电荷数=质子数-核外电子数。 (3)质量数(A)=质子数(Z)+中子数(N)。 (4)质子数(Z)=阳离子的核外电子数+阳离子的电荷数。 (5)质子数(Z)=阴离子的核外电子数-阴离子的电荷数。 2.元素周期表的结构 (1)周期 周期 短周期 长周期 一 二 三 四 五 六 七 对应行数 1 2 3 4 5 6 7 所含元素种 类 2 8 8 18 18 32 32 (排满时) 元素原子序数起止号(若排满) 1~2 3~10 11~18 19~36 37~54 55~86 87-118 每周期0族元素原子序 数 2 10 18 36 54 86 (2)族 族 主族(A) 副族(B) Ⅷ 0 族数 7 7 1 1 列序号 1 2 13 14 15 16 17 3 4 5 6 7 11 12 8 9 10 18 族序号 ⅠA ⅡA ⅢA ⅣA ⅤA ⅥA ⅦA ⅢB ⅣB ⅤB ⅥB ⅦB ⅠB ⅡB Ⅷ (3)过渡元素 元素周期表中从ⅢB 到ⅡB 共10个纵行,包括了第Ⅷ族和全部副族元素,共60多种元素,全部为金属元素,统称为过渡元素。
特别提醒 族序数为Ⅱ、Ⅲ的地方是主族和副族的分界线,第一次分界时主族在副族的前面,第二次分界时副族在主族的前面。 “第一次”指ⅠA ⅡA ⅢB ⅣB ⅤB ⅥB ⅦB Ⅷ依次排列。 “第二次”指ⅠB ⅡB ⅢA ⅣA ⅤA ⅥA ⅦA 0依次排列。 重难点二 零族定位法确定元素的位置 1.明确各周期零族元素的原子序数 周期 一 二 三 四 五 六 七 原子序数 2 10 18 36 54 86 118 2.比大小定周期 比较该元素的原子序数与0族元素的原子序数大小,找出与其相邻近的两种0族元素,那么该元素就和序数大的0族元素处于同一周期。 3.求差值定族数 (1)若某元素原子序数比相应的0族元素多1或2,则该元素应处在该0族元素所在周期的下一个周期的ⅠA 族或ⅡA 族。 (2)若比相应的0族元素少1~5时,则应处在同周期的ⅢA ~ⅦA 族。 (3)若差其他数,则由相应差值找出相应的族。 重难点三 元素的性质与原子结构 1.碱金属单质的相似性和递变性 (1)相似性 ①与O 2反应生成相应的氧化物,如Li 2O 、Na 2O 等。 ②与Cl 2反应生成RCl ,如NaCl 、KCl 等。 ③与H 2O 反应,能置换出H 2O 中的氢,反应通式为2R +2H 2O===2ROH +H 2↑。 ④与非氧化性酸反应,生成H 2,反应通式为2R +2H +===2R + +H 2↑。(R 表示碱金属元素) (2)递变性 从Li 到Cs ,随着核电荷数的增加,碱金属元素原子的电子层数逐渐增多,原子核对核外电子的吸引能力逐渐减弱,失电子能力逐渐增强,金属性逐渐增强。表现为: ①与O 2的反应越来越剧烈,产物更加复杂,如Li 与O 2反应只能生成Li 2O ,Na 与O 2反应还可以生成Na 2O 2,而K 与O 2反应能够生成KO 2等。 ②与H 2O 的反应越来越剧烈,如K 与H 2O 反应可能会发生轻微爆炸,Rb 与Cs 遇水发生剧烈爆炸。 ③对应离子的氧化性依次减弱,即氧化性:Li +>Na +>K +>Rb +>Cs + 。 ④最高价氧化物对应水化物的碱性逐渐增强,CsOH 的碱性最强。 特别提醒 (1)碱金属单质性质的相似性和递变性是其原子结构的相似性和递变性的必然结果。 (2)因Na 、K 等很活泼的金属易与H 2O 反应,故不能从溶液中置换出不活泼的金属。 2.卤素单质的相似性、递变性和特性 (1)相似性 ①与H 2反应生成相应的氢化物:X 2+H 2===2HX 。 ②与活泼金属(Na 等)反应生成相应的金属卤化物: 2Na +X 2=====点燃 2NaX 。
门捷列夫与元素周期表
门捷列夫与元素周期表 在十九世纪初期,人们已经发现了不少元素。在这些元素的状态和性质方面,有些极为相似,有些则完全不同,有些元素在某些性质方面很相似,但 在另一些方面却又差别很大。化学家们很自然地产生了一种寻求 元素相之间内在联系从而把元素作一科学分类的要求。科学家们 在这方面作了不少的工作,曾发表了部分元素间相互联系的论 述。 1829年德国段柏莱纳根据元素性质的相似性,提出“三素 组”的分类法,并指出每组中间元素的原子量大约等于两端的元 素原子量的平均值。但他当时只排了五个三素组,还有许多元素 没找到其间相互联系的规律。 1864年德国迈耶按元素的原子量顺序把元素分成六组,使化学性质相似的元素排在同一纵行里。但也没有指出原子量跟所有元素之间究竟有什么联系。 1865年英国纽兰兹把当时所知道的元素按原子量增加的顺序排列,发现每个元素它的位置前后的第七个元素有相似的性质。他称这个规律叫“八音律”。他的缺点在于机械地看待原子量,把一些元素(Mn、Fe等)放在不适当的位置上而把表排满,没有考虑发现新元素的可能性。 直到1868年,迈耶发表了著名的原子体积周期性图解。都末找出元素间最根本的内在联系,但却一步步地向真理逼近,为发现元素周期律开辟了道路。 与迈耶尔相似,以先行者提供的借鉴为基础,门捷列夫通过自己顽强的努力,于1869年2月编成了他的第一张元素周期表。1869年3月18日,俄国化学会举行学术报告会,门捷列夫因病未能出席,他委托他的同事、彼得堡大学化学教授门许特金代他宣读他的论文《元素性质和原子量的关系》。在论文中,他指出: (1)按照原子量大小排列起来的元素,在性质上呈现明显的周期性变化。 (2)化学性质相似的元素,或者是原子量相近(如Pt,Ir,Os),或者是依次递增相同的数量(如K,Rb,Cs)。 (3)各族元素的原子价(化合价)一致。 (4)分布在自然界的元素都具有数值不大的原子量值,具有这样的原子量值的一切元素都表现出特有的性质,因此可以称它们是典型的元素。 (5)原子量的大小决定元素的特征。 (6)应该预料到许多未知元素将被发现,例如排在铝和硅后面的、性质类似铝和硅的、原子量位于65~75之间的两种元素。 (7)当我们知道了某些元素的同类元素的原子量后,有时可借此修正该元素的原子量。 (8)一些类似的元素能根据其原子量的大小被发现出来。 正如门捷列夫所指出的,周期律的全部规律性都表述在这些原理中。其中最主要的是元素的物理和化学性质随着原子量的递增而做着周期性的变化。他的卓见没有立即被接受。他的老师、俄国化学家齐宁甚至训诫他是不务正业。在这种压力下,门捷列夫没有象纽兰兹那样伤心地放弃对新理论的研究,他不顾名家的指责和嘲笑,继续为周期律的揭示而奋斗。经过两年的努力,1871年他发表了关于周期律的新论文。文中他果断地修正了前一个元素周期表。例如在前一表中,性质类似的各族是横排,周期是竖排;而在新表中,族是竖排,周期是横排,这样各族元素化学性质的周期性变化就更为清晰。同时他象迈耶尔那样,将那些当时性质尚不够明确的元素集中在表格的右边,形成了各族元素的副族。在前表中为尚未发现的元素留下的4个空格,在新表中则变成了6个。 门捷列夫深信他所发现的周期律是正确的。他以周期律为依据,大胆指出某些元素的原子量是不准确的,应重新测定。例如当时公认金的原子量为169.2,按此,在周期表中,金应排在锇、铱、铂(当时认为它们的原子量分别是198.6,196.7,196.7)的前面。而门捷列夫根据金的性质认为金在周期表中应排在这些元素的后面,所以它们的原子量应重新测定。重新测定的结果是:锇为190.9,铱为193.1,铂为195.2,金为197.2。实验证明了门捷列夫的意见是对的。又例如,当时铀公认的原子量是116,是三价元素。门捷列夫则根据铀的氧化物与铬、钼、钨的氧化物性质相似,认为它们应属于一族,因此铀应为六
元素周期律和元素周期表知识总结
元素周期律和元素周期表知识总结 考试大纲要求 1.理解原子的组成及同位素的概念。掌握原子序数、核电荷数、质子数、中子数、核外电子数,以及质量数与质子数、中子数之间的相互关系。 2.以第1、2、3周期的元素为例,掌握核外电子排布规律。 3.掌握元素周期律的实质及元素周期表(长式)的结构(周期、族)。 4.以第3周期为例,掌握同一周期内元素性质(如:原子半径、化合价、单质及化合物性质)的递变规律与原子结构的关系;以ⅠA族和ⅦA族为例,掌握同一主族内元素性质递变规律与原子结构的关系。 知识规律总结 一、原子结构 1.几个量的关系() 质量数(A)=质子数(Z)+中子数(N) 质子数=核电荷数=原子序数=原子的核外电子数 离子电荷数=质子数-核外电子数 2.同位素 (1)要点:同——质子数相同,异——中子数不同,微粒——原子。 (2)特点:同位素的化学性质几乎完全相同;自然界中稳定同位素的原子个数百分数不变。 注意:同种元素的同位素可组成不同的单质或化合物,如H2O和D2O是两种不同的物质。 3.相对原子质量 (1)原子的相对原子质量:以一个12C原子质量的1/12作为标准,其它原子的质量跟它相比较所得的数值。它是相对质量,单位为1,可忽略不写。 (2)元素的相对原子质量:是按该元素的各种同位素的原子百分比与其相对原子质量的乘积所得的平均值。元素周期表中的相对原子质量就是指元素的相对原子质量。 4.核外电子排布规律 (1)核外电子是由里向外,分层排布的。 (2)各电子层最多容纳的电子数为2n2个;最外层电子数不得超过8个,次外层电子数不得超过18个,倒数第三层电子数不得超过32个。 (3)以上几点互相联系。 核外电子排布规律是书写结构示意图的主要依据。 5.原子和离子结构示意图 注意:①要熟练地书写1~20号元素的原子和离子结构示意图。 ②要正确区分原子结构示意图和离子结构示意图(通过比较核内质子数和核外电子数)。 6.微粒半径大小比较规律 (1)同周期元素(稀有气体除外)的原子半径随原子核电荷数的递增逐渐减小。 (2)同主族元素的原子半径和离子半径随着原子核电荷数的递增逐渐增大。 (3)电子层结构相同的离子,核电荷数越大,则离子半径越小。 (4)同种元素的微粒半径:阳离子<原子<阴离子。 (5)稀有气体元素的原子半径大于同周期元素原子半径。 (6)电子层数多的阴离子半径一定大于电子层数少的阳离子半径,但电子层数多的阳离子半径不一定大于电子层数少的阴离子半径。 二、元素周期律和周期表 1.位、构、性三者关系
元素在周期表中位置的计算
元素在周期表中位置的计算 在历届的高考题中,找出元素在周期表中的位置曾出现过几次,为了便于同学们在高考中迅速找到元素在周期表中的位置,现总结出如下的计算方法:在使用该计算方法之前首先要熟练知道稀有气体的原子序数及其所在的周期,如下表: 稀有气体所在的周期数稀有气体的原子序数 1 2 3 4 5 6 2 10 18 36 54 86 表1 稀有气体的原子序数及其所在的周期 族序数Ⅰ A Ⅱ A Ⅲ B Ⅳ B Ⅴ B Ⅵ B Ⅶ B Ⅰ B Ⅱ B Ⅲ A Ⅳ A Ⅴ A Ⅵ A Ⅶ A 纵列数 1 2 3 4 5 6 7 11 12 13 14 15 16 17 表2 每一纵列所对应的族序数 其中,第Ⅷ族所对应的是8、9、10列。 公式: 所求元素的纵列数= 所求元素的原子序数—与其接近的稀有气体的原子序数 所求元素的周期数= 稀有气体所在的周期数+1 例: ①求35号元素在周期表中的位置? 35–18 = 17 3 + 1 = 4(说明该元素在第四周期,第ⅦA族) ②求40号元素在周期表中的位置? 40 –36 = 4 4 + 1 = 5(说明该元素在第五周期,第ⅣB族) ③求45号元素在周期表中的位置? 45–36 = 9
4 + 1 = 5(说明该元素在第五周期,第Ⅷ族) 若所求差值超过了18,说明该元素的原子序数跨过了镧系或锕系,那么将所得的差值再减去14,所得数值就是该元素所在的纵列数,例: ①求79号元素在周期表中的位置? 79 –54 = 25 25 –14 = 11 5 + 1 =6(说明该元素在第六周期,第ⅠB族) ②求114号元素在周期表中的位置? 114 –86= 28 28 –14 = 14 6 + 1 = 7(说明该元素在第七周期,第ⅣA族) 若所求元素的原子序数为镧系(57~71)或锕系(89~103),可直接写出其所在的周期和族数,上述公式不适用。
化学元素周期表变化规律
主族元素原子依次增大 同 同周期相同 主 族 依 同周期依次增多 相 次 同 增 由 同周期依次减小(0族除外) 多 小 到 同 大 主 族 由 小 到 大 同周期最高正价依次升高负价=n-8(F 除外) 同周期金属性逐渐减弱非金属性增强 同周期增强 同周期酸性逐渐增强碱性减弱 同主族酸性减弱碱性增强 同主族逐渐减弱 同主族金属性逐渐增强;非金属性逐渐 减弱 同主族最高正价相同 原子半径 核电荷数 电子层数最外层电子数 化合价 金属性非金属性 气态氢化物稳定性 最高价氧化物对应水化物酸碱性
元素周期表中元素及其化合物的递变性规律 1 原子半径 (1)除第1周期外,其他周期元素(惰性气体元素除外)的原子半径随原子序数的递增而减小; (2)同一族的元素从上到下,随电子层数增多,原子半径增大。 注意:原子半径在VIB族及此后各副族元素中出现反常现象。从钛至锆,其原子半径合乎规律地增加,这主要是增加电子层数造成的。然而从锆至铪,尽管也增加了一个电子层,但半径反而减小了,这是与它们对应的前一族元素是钇至镧,原子半径也合乎规律地增加(电子层数增加)。然而从镧至铪中间却经历了镧系的十四个元素,由于电子层数没有改变,随着有效核电荷数略有增加,原子半径依次收缩,这种现象称为“镧系收缩”。镧系收缩的结果抵消了从锆至铪由于电子层数增加到来的原子半径应当增加的影响,出现了铪的原子半径反而比锆小的“反常”现象。 2 元素化合价 (1)除第1周期外,同周期从左到右,元素最高正价由碱金属+1递增到+7,非金属元素负价由碳族-4递增到-1(氟无正价,氧无+6价,除外); (2)同一主族的元素的最高正价、负价均相同 (3) 所有单质都显零价 3 单质的熔点 (1)同一周期元素随原子序数的递增,元素组成的金属单质的熔点递增,非金属单质的熔点递减; (2)同一族元素从上到下,元素组成的金属单质的熔点递减,非金属单质的熔点递增 4 元素的金属性与非金属性 (1)同一周期的元素电子层数相同。因此随着核电荷数的增加,原子越容易得电子,从左到右金属性递减,非金属性递增; (2)同一主族元素最外层电子数相同,因此随着电子层数的增加,原子越容易失电子,从上到下金属性递增,非金属性递减。 5 最高价氧化物和水化物的酸碱性 元素的金属性越强,其最高价氧化物的水化物的碱性越强;元素的非金属性越强,最高价氧化物的水化物的酸性越强。 6 非金属气态氢化物 元素非金属性越强,气态氢化物越稳定。同周期非金属元素的非金属性越强,其气态氢化物水溶液一般酸性越强;同主族非金属元素的非金属性越强,其气态氢化物水溶液的酸性越弱。 7 单质的氧化性、还原性 一般元素的金属性越强,其单质的还原性越强,其氧化物的阳离子氧化性越弱;元素的非金属性越强,其单质的氧化性越强,其简单阴离子的还原
元素周期表中规律总结.pdf
“知识梳理”栏 元素周期表中规律的总结 一、编排规律 1、原子序数=质子数=核电荷数=原子核外电子数 2、周期序数=原子核外电子层数 3、主族序数=最外层电子数=价电子数 4、1到7周期可容纳元素种数分别为2、8、8、18、18、32、32(目前7周期只有26种)。 5、主族(除ⅠA族)中,非金属元素种数=族序数-2。 二、“定性”规律 1、若主族元素族数为m,周期数为n,则: ①m-n<0时为金属,且值越小,金属性越强; ②m-n>0时是非金属,越大非金属性越强; ③m-n=0时多为两性元素。 如钫位于第7周期第ⅠA族,m-n=-6<0,钫的金属性最强;F位于第二周期VIIA族,m-n=5>0,F的非金属性最强;铝位于第3周期IIIA族,m-n=0,铝为两性元素。 2、对角线规律:左上右下的两主族元素性质相似。如铍与铝的化学性质相似,均能与 强酸和强碱反应。 3、金属与非金属的分界线附近,金属大都有两性,非金属及其某些化合物大都为原子 晶体(如晶体硼、晶体硅、二氧化硅晶体、碳化硅晶体等)。 4、若将表中第ⅤA与ⅥA之间分开,则左边元素氢化物的化学式,是将H写在后边(如SiH4、PH3、CaH2等);而右边元素氢化物的化学式,是将H写在前边(如H2O、HBr等)。 5、符合下列情况的均是主族元素: ①有1~3个电子层的元素(He、Ne、Ar除外)。 ②次外层有两个或8个电子的元素(稀有气体除外)。 ③最外层电子数多于2个的元素(稀有气体除外)。 三、“序差”规律 1、同一周期IIA、IIIA族元素的原子序数相差可能是1、11或25。 2、同一主族相邻周期元素的原子序数之差可能是2、8、18、32。 3、“左上右下”规律:上下相邻两元素,若位于ⅢB之左(如ⅠA、IIA族),则原子序数之差等于上一元素所在周期的元素种数;若位于ⅢB之右(如IIIA~0族),则原子序数之差等于下一元素所在周期的元素种数。 四、“定位”规律 1、比大小定周期。比较该元素的原子序数与0族元素的序数大小,找出与之相邻的0族元素,那么该元素就和序数大的0族元素处于同一周期。 2、求差定族数。若该元素的原子序数比相应的0族元素多1或2时,则分别位于0族元素下周期的第IA或IIA族;若少1、2、3或4时,则分别位于同周期的第VIIA、VIA、VA、IVA族。 五、性质递变性规律 1、原子(离子)的半径 ①同一周期元素(惰性气体元素除外)从左到右,原子半径逐渐减小。 ②同一主族元素从上到下,原子(或离子)半径逐渐增大。 ③同种元素,阳离子半径<原子半径,阴离子半径>原子半径。
