化学平衡高考汇编

化学平衡高考汇编
1.[2020全国新课标Ⅰ28](14分)
硫酸是一种重要的基本化工产品,接触法制硫酸生产中的关键工序是SO2的催化氧化:SO2(g)+
1
2
O2(g)SO3(g) ΔH=?98 kJ·mol?1。回答下列问题:
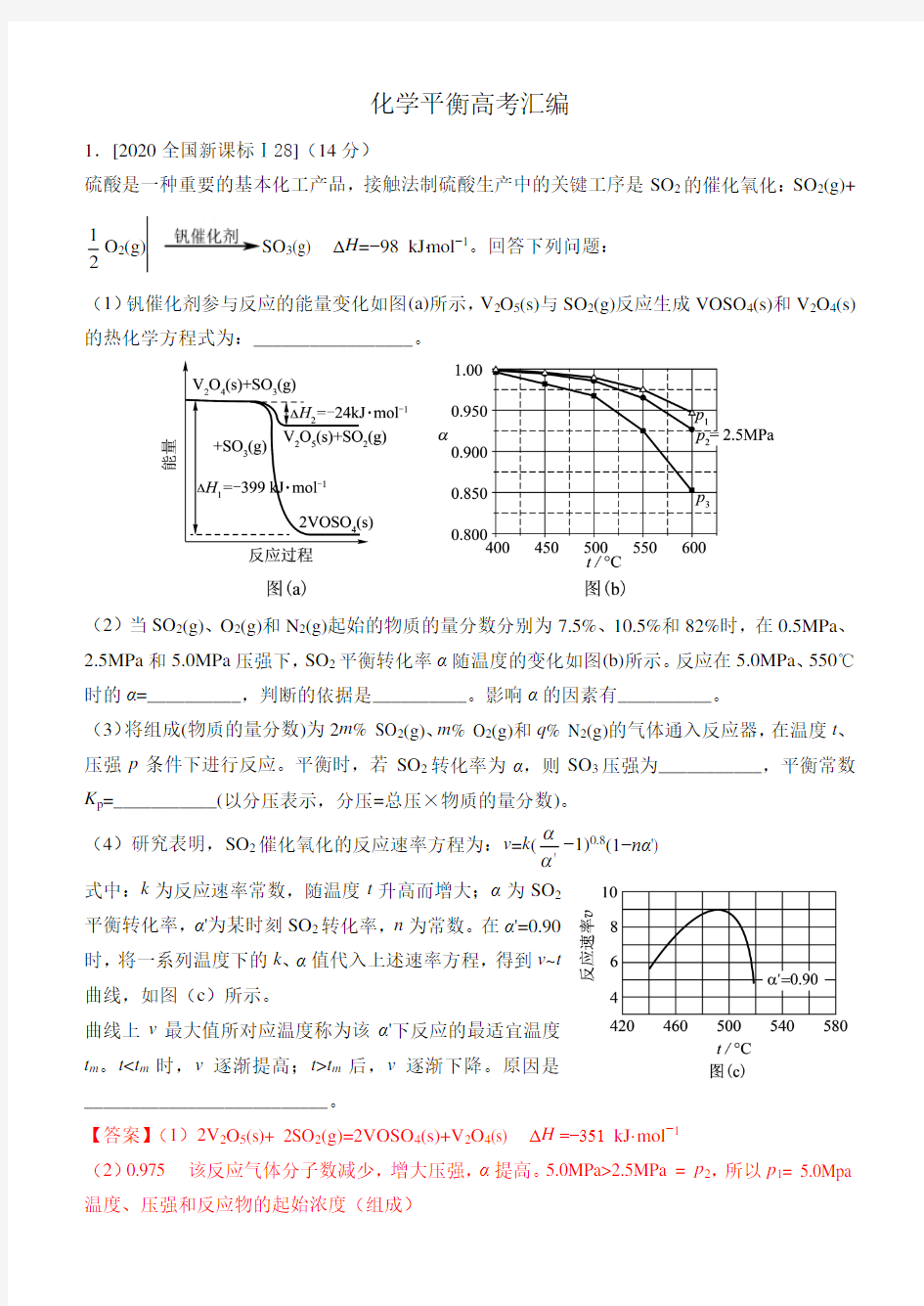
(1)钒催化剂参与反应的能量变化如图(a)所示,V2O5(s)与SO2(g)反应生成VOSO4(s)和V2O4(s)的热化学方程式为:_________________。
(2)当SO2(g)、O2(g)和N2(g)起始的物质的量分数分别为7.5%、10.5%和82%时,在0.5MPa、2.5MPa和5.0MPa压强下,SO2平衡转化率α随温度的变化如图(b)所示。反应在5.0MPa、550℃时的α=__________,判断的依据是__________。影响α的因素有__________。
(3)将组成(物质的量分数)为2m% SO2(g)、m% O2(g)和q% N2(g)的气体通入反应器,在温度t、压强p条件下进行反应。平衡时,若SO2转化率为α,则SO3压强为___________,平衡常数K p=___________(以分压表示,分压=总压×物质的量分数)。
(4)研究表明,SO2催化氧化的反应速率方程为:v=k(α
α'
?1)0.8(1?nα')
式中:k为反应速率常数,随温度t升高而增大;α为SO
2
平衡转化率,α'为某时刻SO2转化率,n为常数。在α'=0.90
时,将一系列温度下的k、α值代入上述速率方程,得到v~t
曲线,如图(c)所示。
曲线上v最大值所对应温度称为该α'下反应的最适宜温度
t m。t
__________________________。
【答案】(1)2V2O5(s)+ 2SO2(g)=2VOSO4(s)+V2O4(s) ΔH=?351 kJ·mol?1
(2)0.975 该反应气体分子数减少,增大压强,α提高。5.0MPa>2.5MPa = p2,所以p1= 5.0Mpa 温度、压强和反应物的起始浓度(组成)
(3)2100m m p α
α- 1.50.5
(1)()100p m m α
αα--
(4)升高温度,k 增大使v 逐渐提高,但α降低使v 逐渐下降。t
2.[2020全国新课标Ⅱ 28](14分)
天然气的主要成分为CH 4,一般还含有C 2H 6等烃类,是重要的燃料和化工原料。
(1)乙烷在一定条件可发生如下反应:C 2H 6(g)= C 2H 4(g)+H 2(g) ΔH ,相关物质的燃烧热数据如下表所示:
①ΔH 1=_________ kJ·mol 1。
②提高该反应平衡转化率的方法有_________、_________。
③容器中通入等物质的量的乙烷和氢气,在等压下(p )发生上述反应,乙烷的平衡转化率为α。反应的平衡常数K p =_______(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。 (2)高温下,甲烷生成乙烷的反应如下:2CH 4???
→高温
C 2H 6+H 2。反应在初期阶段的速率方程为:r =k ×4CH c ,其中k 为反应速率常数。
①设反应开始时的反应速率为r 1,甲烷的转化率为α时的反应速率为r 2,则r 2=_____ r 1。
②对于处于初期阶段的该反应,下列说法正确的是_________。
A .增加甲烷浓度,r 增大
B .增加H 2浓度,r 增大
C .乙烷的生成速率逐渐增大
D .降低反应温度,k 减小
(3)CH 4和CO 2都是比较稳定的分子,科学家利用电化学装置实现两种分子的耦合转化,其原理如下图所示:
①阴极上的反应式为_________。
②若生成的乙烯和乙烷的体积比为2∶1,则消耗的CH 4和CO 2体积比为_________。
3.[2020全国新课标Ⅲ 28](14分)
二氧化碳催化加氢合成乙烯是综合利用CO 2的热点研究领域。回答下列问题:
(1)CO 2催化加氢生成乙烯和水的反应中,产物的物质的量之比n (C 2H 4)∶n (H 2O)=__________。当反应达到平衡时,若增大压强,则n (C 2H 4)___________(填“变大”“变小”或“不变”)。
(2)理论计算表明,原料初始组成n (CO 2)∶n (H 2)=1∶
3,在体系压强为0.1MPa ,反应达到平衡时,四种
组分的物质的量分数x 随温度T 的变化如图所示。
图中,表示C 2H 4、CO 2变化的曲线分别是______、
______。CO 2催化加氢合成C 2H 4反应的
ΔH ______0(填“大于”或“小于”)。
(3)根据图中点A(440K ,0.39),计算该温度时反
应的平衡常数K p =_________(MPa)?3(列出计算式。以分压表示,分压=总压×物质的量分数)。
(4)二氧化碳催化加氢合成乙烯反应往往伴随副反应,生成C 3H 6、C 3H 8、C 4H 8等低碳烃。一定温度和压强条件下,为了提高反应速率和乙烯选择性,应当___________________。
【答案】(14分)(1)1∶4 变大(2)d c 小于(3)39140.039?或43620.39
0.39140.390.10.39()3?
??等(4)选择合适催化剂等
4.[2020山东卷 18](12分)
探究CH 3OH 合成反应化学平衡的影响因素,有利于提高CH 3OH 的产率。以CO 2、H 2为原料合成CH 3OH 涉及的主要反应如下:
Ⅰ. 2232CO (g)3H (g)
CH OH(g)H O(g)++ 1149.5kJ mol H -?=-? Ⅱ. 23CO(g)2H (g)
CH OH(g)+ 1290.4kJ mol H -?=-? Ⅲ. 222CO (g)H (g)
CO(g)H O(g)++ 3H ?
回答下列问题:
(1)13______kJ mol H -?=?。 (2)一定条件下,向体积为V L 的恒容密闭容器中通入1 mol CO 2和3 mol H 2发生上述反应,达到平衡时,容器中CH 3OH(g)为ɑ mol,CO 为b mol ,此时H 2O(g)的浓度为 mol ﹒L -1(用含a 、b 、V 的代数式表示,下同),反应Ⅲ的平衡常数为 。
(3)不同压强下,按照n (CO 2):n (H 2)=1:3投料,实验测定CO 2的平衡转化率和CH 3OH 的平衡产率随温度的变化关系如下图所示。
已知:CO 2的平衡转化率=()()()22 2 CO CO 100%CO
n n n -?平衡
初始初始 CH 3OH 的平衡产率=()()32CH OH
100%CO
n n ?平衡初始 其中纵坐标表示CO 2平衡转化率的是图 (填“甲”或“乙”);压强p 1、p 2、p 3由大到小的顺序为 ;图乙中T 1温度时,三条曲线几乎交于一点的原因是 。
(4)为同时提高CO 2的平衡转化率和CH 3OH 的平衡产率,应选择的反应条件为 (填标号)。
A .低温、高压
B .高温、低压
C .低温、低压
D .高温、高压
【答案】.(1)+40.9(2)a b V
+;()(1)(33)b a b a b a b +----(3)乙;p 1、p 2、p 3;T 1时以反应Ⅲ为主,反应Ⅲ前后气体分子数相等,压强改变对平衡没有影响(4)A
5.[2019新课标Ⅰ]水煤气变换[CO(g)+H 2O(g)=CO 2(g)+H 2(g)]是重要的化工过程,主要用于合成氨、制氢以及合成气加工等工业领域中。回答下列问题:
(1)Shibata 曾做过下列实验:①使纯H 2缓慢地通过处于721 ℃下的过量氧化钴CoO(s),氧化钴部分被还原为金属钴Co(s),平衡后气体中H 2的物质的量分数为0.0250。
②在同一温度下用CO 还原CoO(s),平衡后气体中CO 的物质的量分数为0.0192。
根据上述实验结果判断,还原CoO(s)为Co(s)的倾向是CO______H 2(填“大于”或“小于”)。
(2)721 ℃时,在密闭容器中将等物质的量的CO(g)和H 2O(g)混合,采用适当的催化剂进行反应,则平衡时体系中H 2的物质的量分数为_________(填标号)。
A .<0.25
B .0.25
C .0.25~0.50
D .0.50
E .>0.50
(3
)我国学者结合实验与计算机模拟结果,研究了在金催化剂表面上水煤气变换的反应历程,
如图所示,其中吸附在金催化剂表面上的物种用?标注。
可知水煤气变换的ΔH ________0(填“大于”“等于”或“小于”),该历程中最大能垒(活化能)E 正=_________eV ,写出该步骤的化学方程式_______________________。
(4)Shoichi 研究了467 ℃、489 ℃时水煤气变换中
CO 和H 2分压随时间变化关系(如下图所示),催化剂
为氧化铁,实验初始时体系中的2H O p 和CO p 相等、
2CO p 和2H p 相等。
计算曲线a 的反应在30~90 min 内的平均速率v
(a)=___________kPa·min ?1。467 ℃时2H p 和CO p 随时
间变化关系的曲线分别是___________、___________。
489 ℃时2H p 和CO p 随时间变化关系的曲线分别是
___________、___________。
【答案】(1)大于(2)C (3)小于 2.02 COOH*+H*+H 2O*
COOH*+2H*+OH*(或
H 2O*H*+OH*)(4)0.0047 b c a d 6.[2019新课标Ⅱ节选]环戊二烯(
)是重要的有机化工原料,广泛用于农药、橡胶、塑
料等生产。回答下列问题: (1)已知:
(g) (g)+H 2(g) ΔH 1=100.3 kJ·mol ?1 ① H 2(g)+ I 2(g) 2HI(g) ΔH 2=?11.0 kJ ·mol ?1 ②
对于反应:(g)+ I 2(g)(g)+2HI(g) ③ΔH3=________kJ·mol?1。
(2)某温度下,等物质的量的碘和环戊烯()在刚性容器内发生反应③,起始总压为105Pa,平衡时总压增加了20%,环戊烯的转化率为_________,该反应的平衡常数K p=_________Pa。达到平衡后,欲增加环戊烯的平衡转化率,可采取的措施有__________(填标号)。
A.通入惰性气体B.提高温度C.增加环戊烯浓度D.增加碘浓度
(3)环戊二烯容易发生聚合生成二聚体,该反应为可逆反应。不同温度下,溶液中环戊二烯浓度与反应时间的关系如图所示,下列说法正确的是__________(填标号)。
A.T1>T2 B.a点的反应速率小于c点的反应速率
C.a点的正反应速率大于b点的逆反应速率
D.b点时二聚体的浓度为0.45 mol·L?1
【答案】(1)89.3 (2)40% 3.56×104BD (3)CD
7.[2019新课标Ⅲ节选]近年来,随着聚酯工业的快速发展,氯气的需求量和氯化氢的产出量也随之迅速增长。因此,将氯化氢转化为氯气的技术成为科学研究的热点。回答下列问题:(1)Deacon发明的直接氧化法为:
4HCl(g)+O2(g)=2Cl2(g)+2H2O(g)。下图为刚
性容器中,进料浓度比c(HCl) ∶c(O2)分别
等于1∶1、4∶1、7∶1时HCl平衡转化率
随温度变化的关系:
可知反应平衡常数K(300℃)
____________K(400℃)(填“大于”或“小
于”)。设HCl初始浓度为c0,根据进料浓度比c(HCl)∶c(O2)=1∶1的数据计算K(400℃)=____________(列出计算式)。按化学计量比进料可以保持反应物高转化率,同时降低产物分离的能耗。进料浓度比c(HCl)∶c(O2)过低、过高的不利影响分别是____________。
(2)Deacon直接氧化法可按下列催化过程进行:
CuCl2(s)=CuCl(s)+1
2
Cl2(g) ΔH1=83 kJ·mol-1
CuCl(s)+1
2
O2(g)=CuO(s)+
1
2
Cl2(g) ΔH2=-20 kJ·mol-1
CuO(s)+2HCl(g)=CuCl2(s)+H2O(g) ΔH3=-121 kJ·mol-1
则4HCl(g)+O2(g)=2Cl2(g)+2H2O(g)的ΔH=_________ kJ·mol-1。
(3)在一定温度的条件下,进一步提高HCl的转化率的方法是___________。(写出2种)
【答案】(1)大于O2和Cl2分离能耗较高、HCl转化率较低
(2)﹣116 (3)增加反应体系压强、及时除去产物
8.【2018新课标1卷】采用N2O5为硝化剂是一种新型的绿色硝化技术,在含能材料、医药等工业中得到广泛应用。回答下列问题
(1)1840年Devil用干燥的氯气通过干燥的硝酸银,得到N2O5。该反应的氧化产物是一种气体,其分子式为___________。
(2)F.Daniels等曾利用测压法在刚性反应器中研究了25℃时N2O5(g)分解反应:
其中NO2二聚为N2O4的反应可以迅速达到平衡。体系的总压强p随时间t的变化如下表所示(t=∞时,N2O5(g)完全分解):
①已知:2N2O5(g)=2N2O4(g)+O2(g) ΔH1=?4.4kJ·mol?1
2NO2(g)=N2O4(g) ΔH2=?55.3kJ·mol?1
则反应N2O5(g)=2NO2(g)+ 1
2
O2(g)的ΔH=_______ kJ·mol?1。
②研究表明,N 2O 5(g )分解的反应速率()2531210?min N O p kPa υ--=??。t =62 min 时,测得体
系中2O p p O2=2.9 kPa ,则此时的25N O p =________kPa ,v =_______kPa ·min ?1。
③若提高反应温度至35℃,则N 2O 5(g )完全分解后体系压强p ∞(35℃)____63.1 kPa (填“大于”“等于”或“小于”),原因是________。
④25℃时N 2O 4(g )2NO 2(g )反应的平衡常数K p =_______kPa (K p 为以分压表示的平衡常数,计算结果保留1位小数)。
(3)对于反应2N 2O 5(g )→4NO 2(g )+O 2(g ),R .A .Ogg 提出如下反应历程:
第一步 N 2O 5NO 2+NO 3 快速平衡
第二步 NO 2+NO 3→NO +NO 2+O 2 慢反应
第三步 NO +NO 3→2NO 2 快反应
其中可近似认为第二步反应不影响第一步的平衡。下列表述正确的是_______(填标号)。
A .v (第一步的逆反应)>v (第二步反应)
B .反应的中间产物只有NO 3
C .第二步中NO 2与NO 3的碰撞仅部分有效
D .第三步反应活化能较高
【答案】 O 2 53.1 30.0 6.0×10-
2 大于 温度提高,体积不变,总压强提高;NO 2二聚为放热反应,温度提高,平衡左移,体系物质的量增加,总压强提高 13.4 AC
9.【2018新课标2卷】CH 4-CO 2催化重整不仅可以得到合成气(CO 和H 2),还对温室气体的减排具有重要意义。回答下列问题:
(1)CH 4-CO 2催化重整反应为:CH 4(g )+CO 2(g )=2CO (g )+2H 2(g )。
已知:C (s )+2H 2(g )=CH 4(g ) ΔH =-75 kJ ·mol ?1
C (s )+O 2(g )=CO 2(g ) ΔH =-394 kJ ·mol ?1
C (s )+1/2O 2(g )=CO (g ) ΔH =-111 kJ ·mol ?1
该催化重整反应的ΔH ==____ kJ ·mol ?1。有利于提高CH 4平衡转化率的条件是__(填标号)。
A .高温低压
B .低温高压
C .高温高压
D .低温低压
某温度下,在体积为2 L 的容器中加入2 mol CH 4、1 mol CO 2以及催化剂进行重整反应,达到平衡时CO 2的转化率是50%,其平衡常数为_______mol 2·L ?2。
(2)反应中催化剂活性会因积碳反应而降低,同时存在的消碳反应则使积碳量减少。 相关数据如下表:
积碳反应
CH4(g)=C(s)+2H2(g) 消碳反应
CO2(g)+C(s)=2CO(g )
ΔH/(kJ·mol?1) 75172
活化能/ (kJ·mol?1) 催化剂X3391催化剂Y4372
①由上表判断,催化剂X____Y(填“优于”或“劣于”),理由是_________________。在反应进料气组成、压强及反应时间相同的情况下,某催化剂表
面的积碳量随温度的变化关系如图所示。升高温度时,下列
关于积碳反应、消碳反应的平衡常数(K)和速率(v)的叙
述正确的是________填标号)。
A.K积、K消均增加B.v积减小,v消增加
C.K积减小,K消增加D.v消增加的倍数比
v积增加的倍数大
②在一定温度下,测得某催化剂上沉积碳的生成速率方
程为v=k·p(CH4)·[p(CO2)]-0.5(k为速率常数)。在
p(CH4)一定时,不同p(CO2)下积碳量随时间的变化趋势
如图所示,则p a(CO2)、p b(CO2)、p c(CO2)从大到小的
顺序为________________。
【答案】247A劣于相对于催化剂X,催化剂Y积碳反应的活化能大,积碳反应的速率小;而消碳反应活化能相对小,消碳反应速率大AD p c(CO2)、p b(CO2)、p a(CO2) 10.【2018新课标3卷】三氯氢硅(SiHCl3)是制备硅烷、多晶硅的重要原料。回答下列问题:(1)SiHCl3在常温常压下为易挥发的无色透明液体,遇潮气时发烟生成(HSiO)2O等,写出该反应的化学方程式__________。
(2)SiHCl3在催化剂作用下发生反应:
2SiHCl3(g)SiH2Cl2(g)+ SiCl4(g) ΔH1=48kJ·mol?1
3SiH2Cl2(g)SiH4(g)+2SiHCl3 (g) ΔH2=?30kJ·mol?1
则反应4SiHCl 3(g)SiH4(g)+ 3SiCl4(g)的ΔH=__________ kJ·mol?1。
(3)对于反应2SiHCl 3(g)SiH2Cl2(g)+SiCl4(g),采用大孔弱碱性阴离子交换树脂催化剂,在323K和343K时SiHCl3的转化率随时间变化的结果如图所示。
①343K时反应的平衡转化率α=_________%。平衡常数K343K=__________(保留2位小数)。
②在343K下:要提高SiHCl3转化率,可采取的措施是___________;要缩短反应达到平衡的时间,可采取的措施有____________、___________。
③比较a、b处反应速率大小:υa________υb(填“大于”“小于”或“等于”)。反应速率υ=υ正?υ逆=?,k正、k逆分别为正、逆向反应速率常数,x为物质的量分数,
计算a处=__________(保留1位小数)。
【答案】2SiHCl3+3H2O(HSiO)2O+6HCl114①220.02②及时移去产物改进催化剂提高反应物压强(浓度)③大于1.3
浙江省2021年高考化学真题分类汇编专题07:化学平衡
浙江省2021年高考化学真题分类汇编专题07:化学平衡 姓名:________ 班级:________ 成绩:________ 一、单选题 (共1题;共6分) 1. (6分)大气中的SO2是造成酸雨的主要污染物.最新研究表明,[N(CH3)4]2SO4(s)能与SO2进行如下可逆反应,使其可能成为绿色的SO2吸收剂[N(CH3)4]2SO4(s)+SO2(g)?[N(CH3)4]2S2O6(s)△H<0则用[N(CH3)4]2SO4(s)吸收SO2的适宜条件为() A . 高温高压 B . 低温高压 C . 高温低压 D . 低温低压 二、多选题 (共1题;共4分) 2. (4分)下列做法的目的与反应速率有关的是() A . 用冰箱冷藏食物 B . 在糖果制作过程中添加着色剂 C . 向食盐中添加碘酸钾 D . 在化学反应中加入合适的催化剂 三、实验探究题 (共2题;共30分) 3. (15.0分) (2018高二上·广安期末) 某探究性学习实验小组做了如下实验: 实验一:利用H2C2O4 溶液和酸性KMnO4溶液之间的反应来探究“外界条件改变对化学反应速率的影响”,实验如下:
A29320.0250.13t1 B T120.0230.1V18 C31320.02V20.15t1(1)通过实验A、B,可探究出________ (填外部因素)的改变对反应速率的影响,其中V1=________,T1=________;通过实验________可探究出温度变化对化学反应速率的影响。 (2)若t1<8,则由此实验可以得出的结论是________;利用实验B 中数据计算,用KMnO4的浓度变化表示的反应速率为v(KMnO4)= ________。 (3)实验二:探究酸的强弱对酸与镁条反应速率的影响。 实验步骤: (a)检查装置的气密性后,添加药品; (b)反应开始后,每隔1min 记录一次生成H2的体积; (c)将所记录的数据转化为曲线图(上图乙)。 根据反应的图像(图乙)分析:0-lmin盐酸与镁反应比1-2min反应快的原因:________。 (4)对照实验:用20mL 水代替酸进行实验。 实验现象:当水滴入锥形瓶中,注射器的活塞________(填“会”或“不会”)向右移动。 问题分析:针对上述现象,上图中气体发生装置是否合理:________(填“合理”或“不合理”)若合理,则忽略下问;若不合理,请改进上述装置使其变成合理的装置图:________ (用必要的文字或装置图进行回答)。 4. (1 5.0分)碳、氮、硫是中学化学重要的非金属元素,在工农业生产中有广泛的应用。 (1) 用于发射“天宫一号”的长征二号火箭的燃料是液态偏二甲肼(CH3)2N-NH2,氧化剂是液态四氧化二氮。二
2020年高考化学试题分类汇编——化学反应速率和化学平衡
2020年高考化学试题分类汇编——化学反应速率和化学平衡 化学反应速率和化学平稳 〔2018天津卷〕6.以下各表述与示意图一致的是 A .图①表示25℃时,用0.1 mol·L -1 盐酸滴定20 mL 0.1 mol·L - 1 NaOH 溶液,溶液的pH 随加入酸体积的变化 B .图②中曲线表示反应2S O 2(g) + O 2(g) 2S O 3(g);ΔH < 0 正、逆反应的平稳常数 K 随温度的变化 C .图③表示10 mL 0.01 mol·L -1 KM n O 4 酸性溶液与过量的0.1 mol·L -1 H 2C 2O 4溶液混合时,n(Mn 2+) 随时刻的变化 D .图④中a 、b 曲线分不表示反应CH 2=CH 2 (g) + H 2(g)?? →C H 3C H 3(g);ΔH< 0使用和未使用催化剂时,反应过程中的能量变化 解析:酸碱中和在接近终点时,pH 会发生突变,曲线的斜率会专门大,故A 错;正逆反应的平稳常数互为倒数关系,故B 正确;反应是放热反应,且反应生成的Mn 2+对该反应有催化作用,故反应速率越来越快,C 错;反应是放热反应,但图像描述是吸热反应,故D 错。 答案:B 命题立意:综合考查了有关图像咨询题,有酸碱中和滴定图像、正逆反应的平稳常数图像,反应速率图像和能量变化图像。 〔2018重庆卷〕10.()()()22COCl g CO g +Cl g ;0.H ??→?←??> 当反应达到平稳时,以下措施:①升温 ②恒容通入惰性气体 ③增加CO 的浓度 ④减压 ⑤加催化剂 ⑥恒压通入惰性气体,能提高COCl 2转化率的是 A .①②④ B .①④⑥ C .②③⑥ D .③⑤⑥ 10. 答案B 【解析】此题考查化学平稳的移动。该反应为体积增大的吸热反应,因此升温顺减压均能够促使反应正向移动。恒压通入惰性气体,相当于减压。恒容通入惰性气体与加催化剂均对平
化学平衡高考题(含答案)
化学平衡 1.(08年全国理综I ·11)已知:4NH 4(g)+5O 2(g) = 4NO(g)+6H 2O(g),ΔH=-1025kJ ·mol - 1 ,该反应是一个可逆反应。若反应物起始物质的量相同,下列关于该反应的示意图不正.. 确. 的是C 2.(08年全国理综II ·13)在相同温度和压强下,对反应 CO 2 ( g ) + H 2 ( g ) CO(g ) + H 2O( g ) 进行甲、乙、丙、丁四组实验,实验起始时放入容器内各组分的物质的量见下表: 物质 物质的量 ) 实验 CO 2 H 2 CO H 2O 甲 a mol a mol ^ 0 mol 0 mol 乙 2a mol a mol 0 mol 0 mol 丙 } 0 mol 0 mol a mol a mol 丁 a mol 0 mol a mol 、 a mol C . D . 1200℃ N O 含量 时间 ) N O 含量 时间 1000℃ 催化剂 1000℃ 无催化剂 N O 含量 时间 10×105Pa < A . B . N O 含量 时间 1000℃ 1200℃
上述四种情况达到平衡后, n ( CO )的大小顺序是 A A .乙=丁>丙=甲 B .乙>丁>甲>丙 C .丁>乙>丙=甲 D .丁>丙>乙>甲 3.(08年天津理综·8)对平衡CO 2(g )CO 2(aq ) .△H =·mol - 1,为增大二氧化碳 气体在水中的溶解度,应采用的方法是D A .升温增压 B .降温减压 C .升温减压 D .降温增压 ' 4.(08年山东理综·14)高温下,某反应达到平衡,平衡常数) H ()CO () O H ()CO (222c c c c K ??=。恒容 时,温度升高,H 2浓度减小。下列说法正确的是A A .该反应的焓变为正值 B .恒温恒容下,增大压强,H 2浓度一定减小 C .升高温度,逆反应速率减小 D .该反应的化学方程式为CO +H 2O CO 2+H 2 5.(08年宁夏理综·12)将固体NH 4I 置于密闭容器中,在一定温度下发生下列反应: } ①NH 4I(s) NH 3(g)+HI(g);②2HI(g) H 2(g)+I 2(g) 达到平衡时,c (H 2)=·L -1,c (H I )=4mol ·L -1,则此温度下反应①的平衡常数为C A .9 B .16 C .20 D .25 6.(08年四川理综·8)在密闭容器中进行如下反应:H 2(g) +I 2(g) 2HI(g),在温度T 1和T 2时,产物的量与反应时间 的关系如下图所示.符合图示的正确判断是D < A .T 1>T 2,ΔH >0 B .T 1>T 2,ΔH <0 C .T 1<T 2,ΔH >0 D .T 1<T 2,ΔH <0 7.(08年广东理基·36)对于反应2SO 2(g)+O 2(g) 2SO 3(g)能增大正反应速率的措施是 催化剂 高温 T 1碘化氢的量 时 间 T 2
高考化学知识点专题汇编 (11)
课时跟踪检测(五十三)陌生有机物的结构与性质 1.(2020·茂名模拟)轴烯是一类独特的星形环烃。下列关于三元轴烯()说法不正确的是() A.可以使酸性高锰酸钾溶液褪色 B.所有原子在同一平面 C.与1,3-丁二烯()互为同系物 D.与苯互为同分异构体 解析:选C该分子中含有C===C双键,所以能使酸性高锰酸钾溶液褪色,A正确;由于C===C双键构成的平面结构,所以该分子的所有原子在同一平面上,B正确;该分子含有三个C===C双键和一个碳环,而只有两个C===C双键,所以二者结构不相似,不是同系物,C错误;该分子的化学式为C6H6,与苯的化学式相同,但结构不同,所以二者互为同分异构体,D正确。 2.化合物X()是一种医药中间体。下列有关化合物X的说法正确的是() A.该物质分子式为C10H9O4 B.在酸性条件下水解,水解产物只有一种 C.分子中所有原子处于同一平面 D.1mol化合物X最多能与2mol NaOH反应 解析:选B A项,由化合物X的结构简式可知该有机物分子式为C10H8O4,错误;B 项,该有机物具有环酯结构,则水解产物只有一种,正确;C项,含有饱和烃基,具有甲烷的结构特点,则所有原子不可能在同一个平面上,错误;D项,含有羧基、酯基,且酯基可水解生成酚羟基和羧基,则1mol化合物X最多能与3mol NaOH反应,错误。3.牛至是一种质地坚硬、树枝茂密的多年生药草,下列三种结构简式表示的物质是从牛至中提取出来的活性成分。下列有关说法正确的是() A.c分子中最多有7个碳原子共平面 B.可用溴的CCl4溶液将a、b两种物质区别开 C.完全燃烧1mol三种物质时消耗氧气的量:a>c>b D.a分子与HCl发生加成反应时可得到四种以上产物
化学平衡高考题(含答案)
化学平衡 1.(08年全国理综I ·11)已知:4NH 4(g)+5O 2(g) = 4NO(g)+6H 2O(g),ΔH=-1025kJ ·mol -1 ,该反应是一个可逆反应。若反应物起始物质的量相同,下列关于该反应的示意图不. 正确.. 的是C 2.(08年全国理综II ·13)在相同温度和压强下,对反应 CO 2 ( g ) + H 2 ( g ) CO(g ) + H 2O( g )进行甲、乙、丙、丁四组实验,实验起始时放入容器内各组分的物质的量见下 表: 上述四种情况达到平衡后, n ( CO )的大小顺序是 A A .乙=丁>丙=甲 B .乙>丁>甲>丙 物质 物质的量 实验 CO 2 H 2 CO H 2O 甲 a mol a mol 0 mol 0 mol 乙 2a mol a mol 0 mol 0 mol 丙 0 mol 0 mol a mol a mol 丁 a mol 0 mol a mol a mol C . D . 1200℃ N O 含量 时间 1000℃ N O 含量 时间 1000℃ 催化剂 1000℃ 无催化剂 N O 含量 时间 10×105Pa 1×105Pa A . B . N O 含量 时间 1000℃ 1200℃
C .丁>乙>丙=甲 D .丁>丙>乙>甲 3.(08年天津理综·8)对平衡CO 2(g ) CO 2(aq ) .△H =-19.75kJ·mol - 1,为增大 二氧化碳气体在水中的溶解度,应采用的方法是D A .升温增压 B .降温减压 C .升温减压 D .降温增压 4.(08年山东理综·14)高温下,某反应达到平衡,平衡常数) H ()CO () O H ()CO (222c c c c K ??=。恒容 时,温度升高,H 2浓度减小。下列说法正确的是A A .该反应的焓变为正值 B .恒温恒容下,增大压强,H 2浓度一定减小 C .升高温度,逆反应速率减小 D .该反应的化学方程式为CO +H 2O CO 2+H 2 5.(08年宁夏理综·12)将固体NH 4I 置于密闭容器中,在一定温度下发生下列反应: ①NH 4I(s) NH 3(g)+HI(g);②2HI(g) H 2(g)+I 2(g) 达到平衡时,c (H 2)=0.5mo l ·L -1,c (H I )=4mo l ·L -1,则此温度下反应①的平衡常数为C A .9 B .16 C .20 D .25 6.(08年四川理综·8)在密闭容器中进行如下反应:H 2(g) +I 2(g) 2HI(g),在温度T 1和T 2时,产物的量与反应时 间的关系如下图所示.符合图示的正确判断是D A .T 1>T 2,ΔH >0 B .T 1>T 2,ΔH <0 C .T 1<T 2,ΔH >0 D .T 1<T 2,ΔH <0 7.(08年广东理基·36)对于反应2SO 2(g)+O 2(g) 2SO 3(g)能增大正反应速率的措施是 A .通入大量O 2 B .增大容器容积 C .移去部分SO 3 D .降低体系温度 8.(08年广东化学·8)将H 2(g)和Br 2(g)充入恒容密闭容器,恒温下发生反应H 2(g )+Br 2(g) 2HBr (g )△H <0,平衡时Br 2(g)的转化率为a ;若初始条件相同,绝热下进行上述反应,平衡时Br 2(g)的转化率为b 。a 与b 的关系是A 催化剂 高温 T 1碘化氢的量 时 间 T 2
高考总复习化学平衡移动
高考总复习化学平衡移动 【考纲要求】 1.了解化学平衡移动的概念、条件、结果。 2.理解外界条件(浓度、压强、催化剂等)对反应速率和化学平衡的影响,认识其一般规律并能用相关理论解释其一般规律。。 3.理解勒夏特列原理,掌握平衡移动的相关判断,解释生产、生活中的化学反应原理。 【考点梳理】 考点一、化学平衡移动的概念: 1、概念:可逆反应达到平衡状态后,反应条件(如浓度、压强、温度)改变,使v正和v逆不再相等,原平衡被破坏,一段时间后,在新的条件下,正、逆反应速率又重新相等,即v正'=v逆',此时达到了新的平衡状态,称为化学平衡的移动。应注意此时v正'≠v正,v逆'≠v逆。 V正=V逆改变条件 V正=V逆 一段时间后 V正=V逆 平衡状态不平衡状态新平衡状态 2、平衡发生移动的根本原因:V正、V逆发生改变,导致V正≠V逆。 3、平衡发生移动的标志:新平衡与原平衡各物质的百分含量发生了变化。 要点诠释: ①新平衡时:V′正=V′逆,但与原平衡速率不等。 ②新平衡时:各成分的百分含量不变,但与原平衡不同。 ③通过比较速率,可判断平衡移动方向: 当V正>V逆时,平衡向正反应方向移动; 当V正<V逆时,平衡向逆反应方向移动; 当V正=V逆时,平衡不发生移动。 考点二.化学平衡移动原理(勒夏特列原理): 1、内容:如果改变影响平衡的条件之一(如:温度、浓度、压强),平衡就将向着能够“减弱”这种改变的方向移动。 要点诠释: (1)原理的适用范围是只有一个条件变化的情况(温度或压强或一种物质的浓度),当多个条件同时发生变化时,情况比较复杂。 (2)注意理解“减弱”的含义: 定性的角度,平衡移动的方向就是能够减弱外界条件改变的方向。平衡移动的结果能减弱外界条件的变化,如升高温度时,平衡向着吸热反应方向移动;增加反应物,平衡向反应物减少的方向移动;增大压强,平衡向体积减少的方向移动等。 定量的角度,平衡结果只是减弱了外界条件的变化而不能完全抵消外界条件的变化量。 (3)这种“减弱”并不能抵消外界条件的变化,更不会“超越”这种变化。如:原平衡体系的压强为p,若其他条件不变,将体系压强增大到2p,平衡将向气体体积减小的方向移动,达到新平衡时的体系压强将介于p~2p之间。又如:若某化学平衡体系原温度为50℃,现升温到100℃(其他条件不变),则平衡向吸热方向移动,达到新平衡时体系温度变为50℃~100℃。 2、适用范围:已达平衡状态的可逆反应 3、推广:该原理适用于很多平衡体系:如化学平衡、溶解平衡、电离平衡、水解平衡、络合平衡等。 考点三.影响化学平衡的外界条件:
化学平衡高考题含答案
化学平衡 1.(08 年全国理综I ·11)已知:4NH 4(g)+5O 2(g) = 4NO(g)+6H 2O(g), ΔH=-1025kJ ·mol -1,该反应是一个可逆反应。若反应物起始物质的量相同,下列关于该反应的示意图不正确... 的是C 2.(08 年全国理综II ·13)在相同温度和压强下,对反应 CO 2 ( g ) + H 2 ( g ) CO(g ) + H 2O( g )进行甲、乙、丙、丁四组实验, 物质 物质的量 实验 CO 2 H 2 CO H 2O 甲 a mol a mol 0 mol 0 mol 乙 2a mol a mol 0 mol 0 mol 丙 0 mol 0 mol a mol a mol 丁 a mol 0 mol a mol a mol C . D . 1200℃ N O 含量 时间 1000℃ N O 含量 时间 1000℃ 催化剂 1000℃ 无催化剂 N O 含量 时间 10×105Pa 1×105Pa A . B . N O 含量 时间 1000℃ 1200℃
实验起始时放入容器内各组分的物质的量见下表: 上述四种情况达到平衡后, n ( CO )的大小顺序是 A A .乙=丁>丙=甲 B .乙>丁>甲>丙 C .丁>乙>丙=甲 D .丁>丙>乙>甲 3.(08 年天津理综·8)对平衡CO 2(g ) CO 2(aq ) .△ H =-19.75kJ·mol -1,为增大二氧化碳气体在水中的溶解度,应采 用的方法是D A .升温增压 B .降温减压 C .升温减压 D .降温增压 4.(08 年山东理综·14)高温下,某反应达到平衡,平衡常数 ) H ()CO () O H ()CO (222c c c c K ??= 。恒容时,温度升高,H 2浓度减小。下列说法正 确的是A A .该反应的焓变为正值 B .恒温恒容下,增大压强,H 2浓度一定减小 C .升高温度,逆反应速率减小 D .该反应的化学方程式为CO +H 2O CO 2+H 2 5.(08 年宁夏理综·12)将固体NH 4I 置于密闭容器中,在一定温度 下发生下列反应: ①NH 4I(s) NH 3(g)+HI(g);②2HI(g) H 2(g)+I 2(g) 达到平衡时,c (H 2)=0.5mol ·L -1,c (H I )=4mol ·L -1,则此温度下反应①的平衡常数为C A .9 B .16 C .20 D .25 催化剂 高温
高考化学知识点专题汇编 (10)
课时跟踪检测(五十七)物质制备类综合实验 1.二氯化一氯五氨合钴(Ⅲ),化学式为[Co(NH3)5Cl]Cl2,摩尔质量为250.5g·mol-1,常温下为紫红色固体,难溶于水,不溶于乙醇,工业上可用作聚氯乙烯(PVC)的染色剂和稳定剂。实验室制备二氯化一氯五氨合钴(Ⅲ)的流程如下: 已知:[Co(NH3)5H2O]Cl3===[Co(NH3)5H2O]3++3Cl-; [Co(NH 3)5Cl]2++H2O[Co(NH3)5H2O]3++Cl-; [Co(NH3)5H2O]3+受热可以产生氨。 (1)往黄红色沉淀[Co(NH3)6]Cl2中加H2O2时发生的离子反应方程式为 ________________ __________________________________________________________________________。 (2)下列操作或描述正确的是________。 A.步骤②,过滤得到黄红色沉淀[Co(NH3)6]Cl2,往该沉淀中加双氧水溶液 B.步骤②,双氧水溶液要缓慢滴加,是为了控制反应温度,防止温度过高发生副反应C.步骤④,水浴温度低于85℃时产率下降,可能是因为温度对反应速率的影响比较大D.步骤⑥,抽滤之后,吸滤瓶中的滤液应从吸滤瓶的支管倒出 (3)在步骤⑥中对产品进行抽滤,选择正确操作的编号,将下列步骤补充完整:组装好装 置,将滤纸置于布氏漏斗内,用少量蒸馏水润湿→________→用倾析法将溶液转移入布氏漏斗中→________→将烧杯中剩余沉淀转移入布氏漏斗中,抽滤至干燥→________→取下吸滤瓶,用滤液冲洗烧杯中残留固体,再重新抽滤。 a.微开水龙头;b.开大水龙头;c.微关水龙头;d.关闭水龙头,拔下橡皮管;e.拔下橡皮管,关闭水龙头;f.不对水龙头进行操作。 (4)在步骤⑥中洗涤操作为先用冷水洗涤,再用乙醇洗涤。用乙醇洗涤的目的是 ____________。 (5)最终得到产品的质量为21.4g,则该实验的制备产率为__________。 解析:(1)由流程图可知[Co(NH3)6]Cl2被H2O2氧化为[Co(NH3)5H2O]3+,反应的离子方程式为2[Co(NH3)6]Cl2+H2O2+2NH+4===2[Co(NH3)5H2O]3++4NH3↑+4Cl-或2[Co(NH3)6]Cl2+H2O2+4H+===2[Co(NH3)5H2O]3++2NH+4+4Cl-。(2)A项,步骤①过滤得到黄红色沉淀[Co(NH3)6]Cl2,错误;B项,反应速率过快短时间内放出的热量过多,而由信息可知温度过高[Co(NH3)5H2O]3+会分解,所以应缓慢滴加,正确;D项,吸滤瓶中的液体应直接倒出,错误。(3)抽滤开始和结束打开水龙头都应该先慢后快。(4)由于
2019年高考化学真题分类汇编专题09 反应速率、化学平衡(解析版)
专题09 反应速率、化学平衡 1.[2019江苏]在恒压、NO和O2的起始浓度一定的条件下,催化反应相同时间,测得不同温度下NO转化为NO2的转化率如图中实线所示(图中虚线表示相同条件下NO的平衡转化率随温度的变化)。下列说法正确的是 A.反应2NO(g)+O2(g)2NO2(g)的ΔH>0 B.图中点所示条件下,延长反应时间能提高NO转化率 C.图中Y点所示条件下,增加O2的浓度不能提高NO转化率 D.380℃下,c起始(O2)=5.0×10?4 mol·L?1,NO平衡转化率为50%,则平衡常数>2000 【答案】BD 【解析】A.随温度升高NO的转化率先升高后降低,说明温度较低时反应较慢,一段时间内并未达到平衡,分析温度较高时,已达到平衡时的NO转化率可知,温度越高NO转化率越低,说明温度升高平衡向逆方向移动,根据勒夏特列原理分析该反应为放热反应,?H<0,故A错误; B.根据上述分析,点时,反应还未到达平衡状态,反应正向进行,所以延长反应时间能提高NO的转化率,故B正确; C.Y点,反应已经达到平衡状态,此时增加O2的浓度,使得正反应速率大于逆反应速率,平衡向正反应方向移动,可以提高NO的转化率,故C错误; D.设NO起始浓度为amol/L,NO的转化率为50%,则平衡时NO、O2和NO2的浓度分别为0.5amol/L、(5×10-4-0.25a)mol/L、0.5amol/L,根据平衡常数表达式 = 22 2 224 2 c(NO)0.5) c(NO)c(O)0.5)(5100.5) a a a - = ???- ( ( > 4 1 510- ? =2000,故D正确; 故选BD。 【点睛】解本题时需要注意:实线中在最高点之前反应没有达到平衡状态,主要讨论温度对化学反应速率的影响;最高点之后反应达到平衡状态,可以研究温度对化学平衡的影响。
高考化学平衡移动练习题-
化学平衡移动专题练习 1.在已经处于化学平衡状态的体系中,如果下列量发生变化,其中一定能表明平衡移动的是() A.反应混和物的浓度B.反应物的转化率 C.正、逆反应速率D.反应混和物的压强 2.在下列平衡体系中,保持温度一定时,改变某物质的浓度,混合气体的颜色会改变;改变压强时,颜色也会改变,但平衡并不移动,这个反应是() A.2NO+O22NO2B.Br2(g)+H22HBr C.N2O42NO2 D.6NO+4NH35N2+3H2O 3.在某温度下,反应ClF(g) + F2(g)ClF3(g)(正反应为放热反应)在密闭容器中达到平衡。下列说法正确的是()A.温度不变,缩小体积,Cl F的转化率增大 B.温度不变,增大体积,Cl F3的产率提高 C.升高温度,增大体积,有利于平衡向正反应方向移动 D.降低温度,体积不变,F2的转化率降低 4.已建立化学平衡的可逆反应,当改变条件使化学反应向正反应方向移动时,下列有关叙述正确的是()①生成物的百分含量一定增加②生成物的产量一定增加 ③反应物转化率一定增大④反应物浓度一定降低 ⑤正反应速率一定大于逆反应速率⑥使用了合适的催化剂 A.①②B.②⑤C.③⑤D.④⑥ 5.在一密闭容器中,反应aA(g) bB(g)达平衡后,保持温度不变,将容器体积增加一倍,当达到新平衡时,B的浓度是原来的60%,则() A.平衡向逆反应方向移动了B.物质B的质量分数增加了C.物质A的转化率减小了D.a>b 6.在一固定容积的密闭容器中充入2mol NO2,一定温度下建立如下平衡:2NO2(g) N2O4此时平衡混合气体中NO2的体积分数为x%;若再充入1mol N2O4,在温度不变的情况下,达到新平衡时,测得NO2的体积分数为y%,则x和y的大小关系正确的是() A.x>y B.x=y C.x<y D.不能确定 7.下列事实中,不能用列夏特列原理解释的是( )A.溴水中有下列平衡:Br2+H2O HBr+HBrO当加入AgNO3溶液后溶液颜色变浅 B.对二氧化硫的品红溶液加热可使颜色变深 C.反应CO+NO2CO2+NO(正反应放热),升高温度可使平衡向逆反应方向移动 D.合成氨反应N2+3H 22NH3(正反应放热)中使用催化剂8.在密闭容器中进行H2(g)+Br2(g) 2HBr(g)+Q;反应达到平衡后,欲使颜色加深,应采取的措施是 () A.升温B .降温C.减小容器体积D.增大容器体积 9.在体积可变的密闭容器中,反应mA(g)+nB(s)pC (g)达到平衡后,压缩容器的体积,发现A的转化率随之降低。 下列说法中,正确的是() A.(m+n)必定小于p B.(m+n)必定大于p C.m必定小于p D.n必定大于p 10.某温度下,体积一定的密闭容器中进行如下可逆反应:X(g)+Y(g) Z(g)+W(s);△H>0,下列叙述正确的是() A.加入少量W,逆反应速率增大 B.当容器中气体压强不变时,反应达到平衡 C.升高温度,平衡逆向移动 D.平衡后加入X,上述反应的△H增大 11.一定条件下将2mol SO2和2mol SO3气体混合于一固定容积的密闭容器中,发生反应2SO2+O22SO3平衡时SO3为n mol,在相同温度下,分别按下列配比在上述容器中放入起始物质,平衡时SO3的物质的量可能大于n的是()A.1 mol SO2+1 mol O2+1 mol SO3 B.4 mol SO2+1 mol O2 C.2 mol SO2+1 mol O2+2 mol SO3 D.2 mol SO2+1 mol O2 12.下列说法中正确的是()A.可逆反应的特征是正反应速率和逆反应速率相等B.其他条件不变时,升高温度可使化学平衡向放热反应的方向移动C.其他条件不变时,增大压强会破坏有气体存在的反应的平衡状态D.在其他条件不变时,使用催化剂可以改变化学反应速率,但不能改变化学平衡状态 13.在一定条件下,向5L密闭容器中充入2mol A气体和1mol B气体,发生可逆反应: 2A(g)+B(g) 2C(g),达到平衡时容器内B的物质的量浓度为L,则A的转化率为() A.67%B.50%C.25%D.5% 14.对于平衡体系:aA(g)+bB(g) cC(s)+dD(g)+Q;有下列判断,其中不正确的是() A.若容器容积不变,升高温度。各气体的相对分子质量一定增大B.若从正反应开始,平衡时A、B的转化率相等,则A、B的物质的量之比为a∶b C.达到平衡时,有amol A消耗的同时有b mol B生成 D.若容器为体积不变的密闭容器且a+b=c+d,则当升高容器内温度时。平衡向左移动,容器中气体的压强增大 15.某温度下,在一容积可变的容器中,反应2A(g)+B(g) 2C(g)达到平衡时,A、B和C的物质的量分别为4 mol、
年高考化学真题分类汇编-专题02-化学计量与化学计算解析版-Word版含解析
专题二化学计量与化学计算 1.【2016年高考海南卷】利用太阳能分解制氢,若光解0.02 mol水,下列说法正确的是() A.可生成H2的质量为0.02g B.可生成氢的原子数为2.408×1023个 C.可生成H2的体积为0.224L(标准情况) D.生成H2的量理论上等于0.04mol Na与水反应产生H2的量 【答案】D 考点:考查水的分解及简单方程式的计算 【名师点睛】本类题的解题策略:(1)掌握基本概念,找出各化学量之间的关系;(2)加强与原子结构、元素化合物性质、有机物结构性质等相关知识的横向联系;(3)找出解题的突破口,在常规解法和计算技巧中灵活选用。顺利解答该类题目的关键是:一方面要仔细审题,注意关键字词,熟悉常见的“陷阱”;另一方面是要把各种量转化为物质的量,以此为中心进行计算。 2.【2016年高考江苏卷】下列说法正确的是() A.氢氧燃料电池工作时,H2在负极上失去电子 B.0.1mol/LNa2CO3溶液加热后,溶液的pH减小 C.常温常压下,22.4LCl2中含有的分子数为6.02×1023个 D.室温下,稀释0.1mol/LCH3COOH溶液,溶液的导电能力增强 【答案】A 【解析】
试题分析:A、氢氧燃料电池工作时,H2发生氧化反应,在负极上失去电子,A正确;B、升高温度,促进碳酸钠的水解,溶液的pH增大,B错误;C、常温常压下,气体的摩尔体积大于22.4L/mol,22.4LCl2中的物质的量小于1mol,含有的分子数小于6.02×1023个,C 错误;D、室温下,稀释稀醋酸,虽然电离平衡正向移动,自由移动离子的数目增加,但溶液体积的增大起主导作用,自由移动离子的浓度减小,溶液的导电能力减弱,D错误。答案选A。 【考点定位】本题主要是考查燃料电池,电解质溶液中的离子平衡,阿伏加德罗常数计算等【名师点晴】该题考查的知识点较多,综合性较强,但难度不大。明确原电池的工作原理、碳酸钠的水解、气体摩尔体积以及弱电解质的电离是解答的关键,易错选项是D,注意理解溶液导电性影响因素,溶液的导电能力强弱取决于溶液中离子浓度的大小和离子所带电荷的多少,离子浓度越大,离子所带的电荷越多,溶液的导电性越强。若强电解质溶液中离子浓度很小,而弱电解质溶液中离子浓度大,则弱电解质溶液的导电能力强,因此电解质的强弱与电解质溶液的导电性并无必然联系。 3.【2016年高考四川卷】N A为阿伏伽德罗常数的值。下列说法正确的是() A.2.4g镁在足量的氧气中燃烧,转移的电子数为0.1N A B.标准状况下,5.6L二氧化碳气体中含有的氧原子数为0.5N A C.氢原子数为0.4N A的甲醇分子中含有的σ键数为0.4N A D.0.1L0.5mol/LCH3COOH溶液中含有的氢离子数为0.05NA 【答案】B 【考点定位】考查阿伏加德罗常数、以物质的量为中心的计算、相关物质的结构与性质。【名师点睛】本题型为新课标高考的常见题型。解答本类题目要审清选项中涉及的以下几个方面:①要审清所求粒子的种类,如分子、原子、离子、质子、中子、电子等,②涉及物质的体积时要审清物质的状态和温度、压强,③涉及中子数和化学键的计算,要审清相关物质的结构和特殊物质的摩尔质量,④涉及化学反应要明确相关反应的特点和电子转移; ⑤涉及溶液中的微粒要关注电离和水解;⑥要注意审清运算公式。 4.【2016年高考新课标Ⅰ卷】设N A为阿伏加德罗常数值。下列有关叙述正确的是( )
2017年高考化学真题分类汇编(13个专题)及5套高考试卷烃
专题9 有机化合物 Ⅰ—生活中常见的有机物 1.(2017?北京-7)古丝绸之路贸易中的下列商品,主要成分属于无机物的是 A.瓷器B.丝绸C.茶叶D.中草药 A.A B.B C.C D.D 【答案】A 【解析】含有碳元素的化合物为有机物,有机物大多数能够燃烧,且多数难溶于水;无机 物指的是不含碳元素的化合物,无机物多数不能燃烧,据此分析。 A、瓷器是硅酸盐产品,不含碳元素,不是有机物,是无机物,故A正确; B、丝绸的主要成分是蛋白质,是有机物,故B错误; C、茶叶的主要成分是纤维素,是有机物,故C错误; D、中草药的主要成分是纤维素,是有机物,故D错误。 【考点】无机化合物与有机化合物的概念、硅及其化合物菁优网版权所有 【专题】物质的分类专题 【点评】本题依托有机物和无机物的概念考查了化学知识与生活中物质的联系,难度不大,应注意有机物中一定含碳元素,但含碳元素的却不一定是有机物。 Ⅱ—有机结构认识 2.(2017?北京-10)我国在CO2催化加氢制取汽油方面取得突破性进展,CO2转化过程示意图如下。下列说法不正确的是 A.反应①的产物中含有水 B.反应②中只有碳碳键形式
C.汽油主要是C5~C11的烃类混合物 D.图中a的名称是2﹣甲基丁烷 【答案】B 【解析】A.从质量守恒的角度判断,二氧化碳和氢气反应,反应为CO2+H2=CO+H2O,则产物中含有水,故A正确; B.反应②生成烃类物质,含有C﹣C键、C﹣H键,故B错误; C.汽油所含烃类物质常温下为液态,易挥发,主要是C5~C11的烃类混合物,故C正确;D.图中a烃含有5个C,且有一个甲基,应为2﹣甲基丁烷,故D正确。 【考点】碳族元素简介;有机物的结构;汽油的成分;有机物的系统命名法菁优网版权【专题】碳族元素;观察能力、自学能力。 【点评】本题综合考查碳循环知识,为高频考点,侧重考查学生的分析能力,注意把握化 学反应的特点,把握物质的组成以及有机物的结构和命名,难度不大。 C H, 3.(2017?新课标Ⅰ-9)化合物(b)、(d)、(p)的分子式均为66 下列说法正确的是 A. b的同分异构体只有d和p两种 B. b、d、p的二氯代物均只有三种 C. b、d、p均可与酸性高锰酸钾溶液反应 D. b、d、p中只有b的所有原子处于同一平面 【答案】D 【解析】A.(b)的同分异构体不止两种,如,故A错误 B.(d)的二氯化物有、、、、、, 故B错误 KMnO溶液反应,故C错误 C.(b)与(p)不与酸性4 D.(d)2与5号碳为饱和碳,故1,2,3不在同一平面,4,5,6亦不在同 一平面,(p)为立体结构,故D正确。 【考点】有机化学基础:健线式;同分异构体;稀烃的性质;原子共面。 【专题】有机化学基础;同分异构体的类型及其判定。 【点评】本题考查有机物的结构和性质,为高频考点,侧重考查学生的分析能力,注意把 握有机物同分异构体的判断以及空间构型的判断,难度不大。 Ⅲ—脂肪烃
高考试题汇编化学平衡
高考试题汇编—化学反应原理 1.(2012海南?15)己知A(g) + B(g) C(g) + D(g)反应的平衡常数和温度的关系 如下: 温度/℃ 700 800 830 1000 1200 平衡常数 1.7 1.1 1.0 0.6 0.4 回答下列问题: (1)该反应的平衡常数表达式K= ,△H= 0(填“<”“>”“=”); (2) 830℃时,向一个5L 的密闭容器中充入0.20 mol 的A 和0.80mol 的B ,如 反应初始6s 内A 的平均反应速率v (A) = 0.003 mol ·L -1·s - 1,则6s 时c(A) = mol ·L - 1,C 的物质的量为 mol ;若反应经一段时间后,达到平衡时A 的转化率为 ,如果这时向该密闭容器中再充入1mol 氩气,平衡时A 的转化率为 ; (3)判断该反应是否达到平衡的依据为 (填正确选项前的字母): a .压强不随时间改变 b .体系的密度不随时间改变 c .c(A)不随时间改变 d .单位时间里生成C 和A 的物质的量相等 (4) 1200℃时反应C(g)+D(g)A(g)+B(g)的平衡常数的值为 。 2.(2012山东?29)偏二甲肼与N 2O 4是常用的火箭推进剂,二者发生如下化学反应:(CH 3)2NNH 2(l)+2N 2O 4(1)=2CO 2(g)+3N 2(g)+4H 2O(g) (I) (1)反应(I)中氧化剂是 。 (2)火箭残骸中常现红棕色气体,原因为:N 2O 4(g)2NO 2(g) (Ⅱ) 当温度升高时,气体颜色变深,则反应(Ⅱ)为 (填“吸热”或“放热”)反应。 (3)一定温度下,反应(II)的焓变为△H 。现将1molN 2O 4充入一恒压密闭容器中,下列示意图正确且能说明反应达到平衡状态的是 。 若在相同沮度下,上述反应改在体积为IL 的恒容密闭容器中进行,平衡常数 (填“增大” “不变”或“减小”),反应3s 后NO 2的物质的 量为0.6mol ,则0~3s 的平均反应速率v (N 2O 4)= mol·L -1·s - 1。 a 气体密度 b △H /K J ?m o l d N 2O 4转化率 c v (正) NO 2 N 2O 4
高考化学试题分类汇编化学平衡
【十年高考】2006-2015年高考化学试题分类汇编——化学平衡 天津卷.2015.T9.下列说法不正确 ...的是 A.Na与H2O的反应是熵增的放热反应,该反应能自发进行 B.饱和Na2SO4溶液或浓硝酸均可使蛋白质溶液产生沉淀,但原理不同 C.FeCl3和MnO2均可加快H2O2分解,同等条件下二者对H2O2分解速率的改变相同 D.Mg(OH)2固体在溶液中存在平衡:Mg(OH)2(s)Mg2+(aq)+2OH-(aq),该固体可溶于NH4Cl 溶液 【答案】C 【解析】A项,△S>0、△H<0有利于反应的自发进行,A选项两条都满足,结合Na与H2O反应的实验常识,选项正确; B项,饱和Na2SO4溶液使蛋白质溶液聚沉,是物理变化,浓硝酸使蛋白质溶液变性而产生沉淀,是化学变化,故原理不一样;C项,控制变量后,结合常识,二氧化锰对双氧水的催化能力较强,故错误;D项,NH4+可以跟Mg(OH)2溶解出的OH- 反应生成弱电解质NH3·H2O,进而促进了Mg(OH)2的溶解,故正确。 天津卷.2015.T12.某温度下,在2L的密闭容器中,加入1molX(g)和2molY(g)发生反应:X (g)+m Y(g)3Z(g),平衡时,X、Y、Z的体积分数分别为30%、60%、10%。在此平衡体系 中加入1molZ(g),再次达到平衡后,X、Y、Z的体积分数不变。下列叙述不正确 ...的是 A.m=2 B.两次平衡的平衡常数相同 C.X与Y的平衡转化率之比为1:1 D.第二次平衡时,Z的浓度为0.4 mol·L-1 【答案】D 【解析】A项,根据题意,在此平衡系中加入1molZ(g),再次达到平衡后,X、Y、Z的体积分数不变,反应又是在恒温恒容条件下进行的,说明此平衡为等效平衡,根据恒温恒容条件下等效平衡的原理,反应前后气体的系数应相等,因此m=2,选项正确; B项,平衡常数的变化只与温度的变化有关,此反应是在恒温条件下进行,故两次平衡的平衡常数相同,选项正确;C项,平衡转化率等于变化量跟起始量之比,根据三段式原理,X与Y的变化量是1:2关系,而题目中给定的X与Y 起始量也是1:2关系,因此X与Y的平衡转化率之比为1:1选项正确,; D项,根据三段式,结合第一次平衡时Z的体积分数为10%,可以计算出c(Z)=0.15 mol·L-1,两次平衡为等效平衡,因此第二次平衡时,Z的浓度也为0.15 mol·L-1 ,选项错误。 四川卷.2015.T7.一定量的CO2与足量的碳在体积可变的恒压密闭容器中反应:C(s)+CO2(g)2CO(g)。平衡时,体系中气体体积分数与温度的关系如下图所示:
2020年高考化学试题分类汇编专题05 元素及其化合物 (解析版)
专题05 元素及其化合物 1.[2019新课标Ⅰ] 固体界面上强酸的吸附和离解是多相化学在环境、催化、材料科学等领域研究的重要课 题。下图为少量HCl 气体分子在253 K 冰表面吸附和溶解过程的示意图。下列叙述错误的是 A .冰表面第一层中,HCl 以分子形式存在 B .冰表面第二层中,H +浓度为5×10?3 mol·L ?1(设冰的密度为0.9 g·cm ?3) C .冰表面第三层中,冰的氢键网络结构保持不变 D .冰表面各层之间,均存在可逆反应HCl 垐?噲?H ++Cl ? 【答案】D 【解析】 【分析】由示意图可知,在冰的表面第一层主要为氯化氢的吸附,第二层中氯化氢溶于水中并发生部分电离,第三层主要是冰,与氯化氢的吸附和溶解无关。 【详解】A 项、由图可知,冰的表面第一层主要为氯化氢的吸附,氯化氢以分子形式存在,故A 正确; B 项、由题给数据可知,冰的表面第二层中氯离子和水的个数比为10—4:1,第二层中溶解的氯化氢分子应少于第一层吸附的氯化氢分子数,与水的质量相比,可忽略其中溶解的氯化氢的质量。设水的物质的量为1mol ,则所得溶液质量为18g/mol× 1mol=18g ,则溶液的体积为18g/mol 1m 0.9ol g/mL ?×10—3L/ml=2.0×10—2L ,由第二层氯离子和水个数比可知,溶液中氢离子物质的量 等于氯离子物质的量,为10 —4 mol ,则氢离子浓度为-4-2102.l 010L mo ?=5×10—3mol/L ,故B 正确;
C项、由图可知,第三层主要是冰,与氯化氢的吸附和溶解无关,冰的氢键网络结构保持不变,故C正确; D项、由图可知,只有第二层存在氯化氢的电离平衡HCl H++Cl—,而第一层和第三层均不存在,故D错误。 故选D。 【点睛】本题考查氯化氢气体在冰表面的吸附和溶解。侧重考查接受、吸收、整合化学信息的能力及分析和解决化学问题的能力,注意能够明确图像表达的化学意义,正确计算物质的量浓度为解答关键。 2.[2019江苏]下列有关物质的性质与用途具有对应关系的是 A.NH4HCO3受热易分解,可用作化肥 B.稀硫酸具有酸性,可用于除去铁锈 C.SO2具有氧化性,可用于纸浆漂白 D.Al2O3具有两性,可用于电解冶炼铝 【答案】B 【解析】A.NH4HCO3受热易分解和用作化肥无关,可以用作化肥是因为含有氮元素; B.铁锈的主要成分为Fe2O3,硫酸具有酸性可以和金属氧化物反应,具有对应关系; C.二氧化硫的漂白原理是二氧化硫与有色物质化合成不稳定的无色物质,不涉及氧化还原,故和二氧化硫的氧化性无关; D.电解冶炼铝,只能说明熔融氧化铝能导电,是离子晶体,无法说明是否具有两性,和酸、碱都反应可以体现Al2O3具有两性。 故选B。 3.[2019江苏]下列有关化学反应的叙述正确的是 A.Fe在稀硝酸中发生钝化B.MnO2和稀盐酸反应制取Cl2 C.SO2与过量氨水反应生成(NH4)2SO3D.室温下Na与空气中O2反应制取Na2O2 【答案】C 【解析】 【分析】相同的反应物,条件不同(如温度、浓度、过量与少量),反应有可能也不同; A.钝化反应应注意必须注明常温下,浓硝酸与Fe发生钝化; B.实验室制备氯气的反应中应注意盐酸的浓度和反应温度; C.过量与少量问题应以少量物质为基准书写产物;
20092012年高考化学试题分类汇编工艺流程
2012年高考化学分类汇编---工艺流程 福建 24. (16分) (1)电镀时,镀件与电源的极连接。 (2)化学镀的原理是利用化学反应生成金属单质沉积在镀件表面形成 镀层。 ①若用铜盐进行化学镀铜,应选用_(填“氧化剂”或“还原剂”) 与之反应。 ②某化学镀铜的反应速率随镀液pH 变化如右图所示。该镀铜过程中,镀液pH 控制在12.5左右。据图中信息,给出使反应停止的方法: (3)酸浸法制取硫酸铜的流程示意图如下 ①步骤(i)中Cu2(OH) 2CO3发生反应的化学方程式为。 ②步骤(ii)所加试剂起调节pH 作用的离子是(填离子符号)。 ③在步骤(iii)发生的反应中,1 mol MnO2转移2 mol 电子,该反应的离子方程式为。 ④步骤(iv)除去杂质的化学方程式可表示为 3Fe3+ + NH4++2SO42-+6H2O= NH4Fe3 (SO4)2(OH)6+6H + 过滤后母液的pH = 2.0 , c (Fe3+) =a mol·L-1,, c ( NH4+)=b mol·L-1,, c ( SO42-)= d mol·L-1,该反应的平衡常数K=_(用含a 、b 、d 的代数式表示)。 答案:
广东 32.(17分)难溶性杂卤石(K2SO4·MgSO4·2CaSO4·2H2O)属于“呆矿”,在水中存在如下平衡 为能充分利用钾资源,用饱和Ca(OH)2溶液溶浸杂卤石制备硫酸钾,工艺流程如下: (1)滤渣主要成分有和以及未溶杂卤石。 (2)用化学平衡移动原理解释Ca(OH)2溶液能溶解杂卤石浸出K+的原因:。 (3)“除杂”环节中,先加入溶液,经搅拌等操作后,过滤,再加入溶液调滤液PH至中性。 (4)不同温度下,K+的浸出浓度与溶浸时间的关系是图14,由图可得,随着温度升高, ①② (5)有人以可溶性碳酸盐为溶浸剂,则溶浸过程中会发生:
