河南省镇平县第一高级中学高一重点班分班考试化学试题

河南省镇平县第一高级中学高一重点班分班考试化学试题
一、选择题
1.下列各组内物质间的转化关系中,存在不能一步转化的是()
A. B.
C. D.
2.在相同的温度和压强下,相同体积的气体具有相同的分子数,反之亦然。取20℃和101kPa下相同体积的CH4和O2混合,在一定条件下充分反应,恢复到初始温度和压强。下列说法正确的是()
A.参加反应的CH4和O2的体积比为1:1
B.生成的CO2分子个数为原来气体分子数的三分之一
C.反应后气体的体积为原来的二分之一
D.反应后的气体中C、O原子的个数比为1:2
3.除去物质中的少量杂质,下列方法不能达到目的的是()
选项物质杂质除去杂质的方法
A CaO CaCO3高温充分煅烧
B KCl溶液CaCl2通入足量的CO2,过滤
C CO2CO通过足量的灼热氧化铜
D H2HCl依次通过足量的NaOH溶液和浓硫酸
A.A B.B C.C D.D
4.现有表面被氧化的镁条样品6g,加入到盛有73g质量分数为19%的稀盐酸的烧杯中恰好完全反应,得到0.2g气体。則原镁条样品中镁元素的质量分数为( )
A.48% B.60% C.76% D.84%
5.除去下列各物质中少量杂质,所选用的试剂和操作方法均正确的是()
选项物质(括号内为杂质)试剂操作方法
A Fe 粉(CuSO4)加水溶解、过滤、洗涤、干燥
B MnO2固体(KC1)加水溶解、过滤、洗涤、干燥
C CO2 (H2)足量氧气点燃
D KNO3溶液(K2SO4)过量Ba(NO3)2溶液过滤
A.A B.B C.C D.D
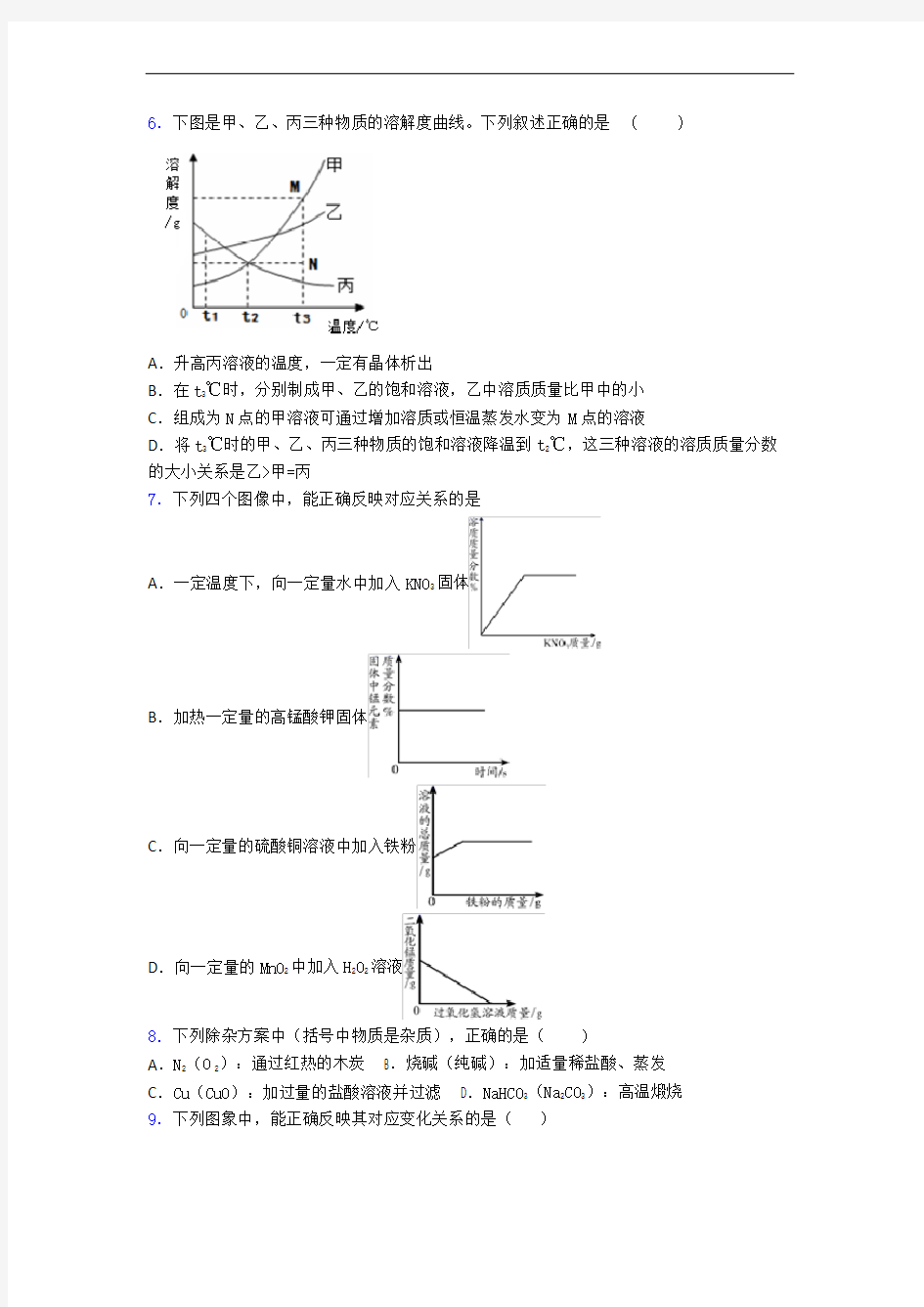
6.下图是甲、乙、丙三种物质的溶解度曲线。下列叙述正确的是 ( )
A.升高丙溶液的温度,一定有晶体析出
B.在t3℃时,分别制成甲、乙的饱和溶液,乙中溶质质量比甲中的小
C.组成为N点的甲溶液可通过增加溶质或恒温蒸发水变为M点的溶液
D.将t3℃时的甲、乙、丙三种物质的饱和溶液降温到t2℃,这三种溶液的溶质质量分数的大小关系是乙>甲=丙
7.下列四个图像中,能正确反映对应关系的是
A.一定温度下,向一定量水中加入KNO3固体
B.加热一定量的高锰酸钾固体
C.向一定量的硫酸铜溶液中加入铁粉
D.向一定量的MnO2中加入H2O2溶液
8.下列除杂方案中(括号中物质是杂质),正确的是()
A.N2(O 2):通过红热的木炭 B.烧碱(纯碱):加适量稀盐酸、蒸发
C.Cu(CuO):加过量的盐酸溶液并过滤 D.NaHCO3(Na2CO3):高温煅烧
9.下列图象中,能正确反映其对应变化关系的是()
A.服用胃舒平[主要成分是Al(OH)3]治疗胃酸过多,胃液pH的变化
B.向一定质量的稀盐酸和氯化铜的混合溶液中加入氢氧化钠溶液
C.将等质量的镁和铁分别投入到盛有足量同种稀硫酸的两个容器中
D.浓盐酸敞口放置
10.除去下列物质中所含的杂质,选用的试剂(括号内的物质)正确的是:()A.CaO中混有少量CaCO3(盐酸) B.CO2中混有HCl气体(NaOH溶液)
C.Cu(NO3)2溶液中混有AgNO3(铜粉) D.CO2中混有少量CO(氧气)
11.除去下列物质中的杂质所用的试剂和方法不正确的是 ( )。
物质杂质除去杂质所用的试剂和方法
A Cu Fe加入足量的稀硫酸,过滤,洗涤,干燥
B Cu(OH)2固体CuCl2加入适量稀盐酸,过滤
C HNO3溶液HCl加适量的AgNO3溶液,过滤
D CO气体CO2通过足量的氢氧化钠溶液,干燥
A.A B.B C.C D.D
12.将a g铁粉和锌粉的混合物加入到b g AgNO3和Cu(NO3)2组成的混合溶液中,充分反应后过滤,得到滤液和滤渣。判断下列有关说法中,不正确
...的是
A.滤渣的质量一定大于a g
B.若滤渣中含有单质Zn,则滤液一定是无色溶液
C.若向滤渣中加入足量的稀盐酸有气泡冒出,则滤渣中一定含有Ag、Cu、Fe
D.若向滤液中加入足量的稀盐酸有白色沉淀产生,则滤液中的一定含有四种金属阳离子13.除去下列物质中混有的少量杂质(括号内为杂质),所用方法正确的是()A.CaCO3固体(CaO固体)—高温煅烧
B.N2气体(O2气体)——通过灼热的铜网
C.CO2气体(CO气体)——在氧气中点燃
D.KCl溶液(CaCl2溶液)——加碳酸钠溶液至恰好完全反应,过滤
14.实验室有一包含有少量氯化钠杂质的硝酸钾固体,为提纯硝酸钾,设计如下图所示操作,
有关分析中正确的是
A.操作Ⅰ~Ⅲ分别是加热浓缩、蒸发结晶、过滤
B.操作Ⅰ是过滤,将氯化钠固体从溶液中分离除去
C.操作Ⅱ是加热浓缩,趁热过滤,除去杂质氯化钠
D.操作Ⅲ是过滤,将硝酸钾晶体从溶液中分离出来
15.如图中X、Y、Z是初中化学常见物质,箭头表示物质之间可以向箭头方向一步转化,下列说法中不正确的是()
A.若X是SO2,则Z可能是O2
B.若X是H2O,则Z可能是O2
C.若X是O2,则Z可能是CO2
D.若X是CO2,则Z可能是H2CO3
16.向一定质量AgNO3和Cu(NO3)2的混合溶液中加入Zn,溶液质量与加入Zn的质量关系如图所示。下列说法正确的是
A.取a点溶液,滴加稀盐酸,无白色沉淀
B.c点溶液中溶质为Zn(NO3)2
C.若取b~c段固体,滴加稀盐酸,有气泡产生
D.取d点的固体有2种
17.除去下列物质中混有的少量杂质(括号内为杂质),所用方法及主要操作步骤均正确的是
A.CuO固体[Cu2(OH)2CO3]——充分加热固体
B.KCl溶液(CaCl2)——加入过量的K2CO3溶液,过滤
C.FeCl2溶液(CuCl2) ——加入过量的铁粉
D.CO2(HCl气体)——先通过足量的NaOH溶液,再通过浓硫酸
18.下列四个图像分别表示对应的四种操作过程,其中正确的是:
A.加热等质量的氯酸钾制氧 B.含有水蒸气的氢气通过浓硫酸
C.引淡水浸泡盐碱地 D.向硝酸钡溶液中滴加稀硫酸
19.三种都能与酸反应的金属共2.3克,与足量的稀盐酸反应,生成氢气0.1克。则这三种金属可能是:
A.Mg、Na、Al B.Zn、Na、Fe
C.Zn、Na、Al D.Cu、Na、Al
20.如图所示,其中甲、乙、丙、丁、戊分别是铁、盐酸、氢氧化钙、二氧化碳、碳酸钠中的一种。图中相连的两圆表示相应物质能发生反应,已知乙是铁。下列说法错误的是
A.五种物质中,只有铁是单质
B.丙是氢氧化钙
C.戊是二氧化碳、甲是碳酸钠
D.甲、丙、丁之间的反应属于复分解反应
21.化学实验室要从X、银、铜、锌四种金属混合物中分离某贵重金属。流程如下:
其中正确的是
A.固体丙中一定只含银 B.四种金属活动性强弱顺序Zn、X、Cu、Ag
C.固体甲中一定含有Cu和Ag,可能含有X D.滤液A中含有两种溶质
22.除去下列各组物质中少量的杂质,所用试剂或方法正确的是
选项物质杂质除杂所用试剂或方法
A.CO2CO点燃
B.Ag粉Mg粉适量稀硫酸
C.NaOH溶液Na2CO3适量稀盐酸
D.NaCl KNO3冷却结晶
A.A B.B C.C D.D 23.下列各组对比实验,能达到实验目的的是:
实验目的
实验方案
实验①实验②
A 探究碘在汽油和植物油中的溶解性
B 探究温度对反应剧烈程度的影响
C 探究催化剂对反应快慢的影响
D探究CO2的化学性质
A.A B.B C.C D.D 24.下列实验能达到目的的是
A.分离溶液中的NaCl和CuSO4
B.检验蜡烛燃烧生成的水
C.检验CO32-的存在
D.测溶液pH
25.除去下列各组物质中的杂质,所用试剂和方法均正确的是
物质杂质除杂所用的试剂和方法
A CaO CaCO3加入适量的稀盐酸,蒸发
B H2HCl依次通过NaOH溶液、浓硫酸
C NaOH溶液Ca(OH)2先加入过量的Na2CO3溶液,再过滤
D KCl溶液CuCl2加入氢氧化钠溶液至不再产生沉淀,过滤
A.A B.B C.C D.D
二、流程题
26.氯化铜晶体(CuCl2·2H2O,为结晶水合物)常用作玻璃、陶瓷着色剂和饲料添加剂等。它在潮湿空气中易潮解。易溶于水,能溶于乙醇,受热容易失去结晶水。一种以辉铜矿石为原料制备CuCl2·H2O晶体的工艺流程如下:
查阅相关资料得知:
①辉铜矿主要含有硫化亚铜(Cu2S)、还有Fe2O3,SiO2及一些不溶性杂质。
②常温下,Cu2+、Fe3+的氢氧化物开始沉淀和沉淀完全时的pH见下表:
金属离子Fe3+Cu2+
氢氧化物开始沉淀时的pH 1.9 4.7
氢氧化物完全沉淀时的pH 3.2 6.7
回答问题:
(1)高温焙烧中有黑色固体生成,反应的化学方程式为______。
(2)焙烧时产生的二氧化硫对环境有污染,会导致______。
(3)滤液1中加入试剂X可以调节溶液pH,控制pH的取值范围为______,从而除去Fe3+而不引入杂质,试剂X可选用下列物质中的______(填字母)。
A CuO
B NaOH
C Cu
D Cu(OH)2
(4)操作a包含蒸发浓缩、______、过滤、洗涤、干燥等,洗涤CuCl2晶体时,用乙醇代替蒸馏水的目的是______。
(5)用含Cu2S 80%的辉铜矿a吨,按上述流程最多可制得CuCl2·2H2O的质量为______吨(列出算式即可)。
(6)氯化铜可用于制取氢氧化铜,一定温度下,往含一定量氯化铜的溶液中加入适量氢氧化钠,再经过滤、洗涤得到氢氧化铜,为探宄获得较高氢氧化铜转化率条件,该同学进行如下对比实验,数据如下:
实验编号CuCl2溶液溶质质量分数反应温度/℃Cu(OH)2转化率/%
a10%3027.06
b15%3056.77
c15%4069.64
d15%6054.30
e20%6060.60
由实验可知,能够得到最多Cu(OH)2的实验组是______(填编号),为探究获得更高Cu(OH)2晶体转化率条件,下列设计合理的是______(填字母)。
A 氯化铜浓度15%,温度35℃
B 氯化铜浓度15%,温度45℃
C 氯化铜浓度20%,温度40℃
D 氯化铜浓度10%,温度40℃
27.氯化亚铜(CuC1)是一种工业催化剂,不溶于水、乙醇(沸点是78.2℃)及稀硫酸熔点422℃,沸点1366℃,在空气中迅速被氧化成绿色。以粗盐水(含氯化钙、硫酸镁等杂质)、Cu、稀硫酸、SO2等为原料合成CuCl的工艺流程如图:
(1)反应I加入过量A溶液中溶质的化学式是___反应I中加入①②③三种试剂的顺序还可以是___(填写一种即可)。
(2)反应Ⅱ过程中发生中和反应的化学方程式是___。
(3)写出反应Ⅲ的化学方程式___。
(4)反应Ⅵ的化学方程式是:2NaCl+2CuSO4+SO2+2H20=2CuCl↓+2X+Na2SO4,则X的化学式为___该反应中化合价升高的元素是___。
(5)本工艺中可循环利用的物质是___。
(6)反应Ⅵ后,过滤得到的CuCl2沉淀,用无水乙醇洗涤沉淀,在真空干燥机内于70℃干燥2小时,冷却密封包装即得产品。70℃真空干燥的目的是___。
28.工业上利用某废渣(含FeSO4、Fe2(SO4)3及少量CaO和MgO)制备高档颜料铁红(主要成分为Fe2O3)和回收(NH4)2SO4。具体生产流程如下:
(背景信息)
a.氧化还原反应中,会有元素化合价发生变化。
b.3Fe2(SO4)3+12NH3?H2O=(NH4)2Fe6(SO4)4(OH)12↓+5(NH4)2SO4
c.(NH4)2Fe6(SO4)4(OH)12 叫做“铵黄铁矾晶体”
(1)该流程中回收的(NH4)2SO4在实际生活中常用作_____。
(2)加入物质X溶解废渣,X应选用_____(填序号)。
A 盐酸
B 硫酸
C 氨水
D 氢氧化钠
步骤①酸浸时,生成盐的化学方程式为_______(任写一个)。
(3)步骤②通入氧气氧化的目的是_____;工业上对该操作控制在4小时左右为宜,根据如图有关数据分析,影响Fe2+氧化率的变化规律:_________
29.氯化亚铜(CuCl)广泛应用于冶金、电镀、医药等行业。已知CuCl难溶于水和乙醇,在潮湿空气中易变质。CuCl的制备流程如下:
(1)“滤液1”中除了Na+、SO42-外,还存在较多的离子是_____、______(写离子符号)(2)“反应”中发生的化学变化是2CuCl2+Na2SO3=2CuCl↓+2NaCl+SO3,产生的SO3迅速与水化合生成一种酸,该反应的化学方程式为_____________________________________。(3)“操作a”的名称是_________。本流程中可以循环利用的物质(水除外)是
_________。(写化学式)
(4)可用“水洗”的原因是_________,“醇洗”的目的是_____________。
(5)160g CuSO4与足量NaCl经上述制备流程,可生成的CuCl最多是_________g。30.碲(Te)广泛用于彩色玻璃和陶瓷工艺,难溶与水。用某工业废渣(主要含有TeO2、少量Ag、Au)为原料制备碲的一种工艺流程如下:
回答下列问题:
(1)类比CO2与NaOH的反应,写出“碱浸”时发生反应的化学方程式:_____,产物盐中Te元素的化合价是_____。
(2)滤液1中的两种溶质是H2SO4和_____(填化学式)。
(3)上述工艺流程中设计“废渣→……→TeO2”的目的是_____。
(4)“酸溶”后,在TeCl4溶液中通入SO2,反应生成碲和初中化学中两种常见的酸,则该反应的化学方程式是_____。
【参考答案】***试卷处理标记,请不要删除
一、选择题
1.D
解析:D
【解析】根据题意,一步反应实现即原物质只发生一个反应即可转化为目标物质,根据物质的性质及变化规律,分析变化能否只通过一个反应而实现。
解:A.铜与氧气反应生成氧化铜,氧化铜与硫酸反应生成硫酸铜,可以一步转化,故A不符合题意;
B.过氧化氢分解生成水和氧气,氧气与磷反应生成五氧化二磷,可以一步转化,故B不符合题意;
C.氧化铁与一氧化碳反应生成铁,铁与盐酸反应生成氯化亚铁,可以一步转化,故C不符合题意;
D.二氧化碳与碳反应生成一氧化碳,一氧化碳不能一步转化为碳,故选D。
2.C
解析:C
【解析】
【分析】
反应的化学方程式:CH4+2O22H2O+CO2。
A.根据反应的化学方程式,判断反应中两气体的分子个数关系,利用相同体积的气体具有相同的分子数,确定参加反应的CO和O2的体积比;
BC.根据反应的化学方程式,判断反应中反应前后气体的分子个数关系,利用相同体积的气体具有相同的分子数,确定生成的CO2分子个数与原来气体分子数关系;
D.根据化学反应中甲烷与氧气的分子个数关系来分析。
【详解】
A.由化学方程式可知,参加反应的CH4和O2的分子个数比为1:2,则参加反应的CH4和O2的体积比为1:2;故A错误;
B.每1个CH4分子与1个O2分子反应生成2个CO2分子,而原混合气体中CH4和O2分子个数相等,则生成的CO2分子个数为原来气体分子数的四分之一,而不是三分之一;故B 不正确;
C.由B可知,C正确;
D.由化学方程式中参加反应的甲烷分子与氧气分子的个数比可知,反应后的气体中C、O 原子的个数比为1:1,故D不正确.
通过准确理解所给的重要信息,利用该信息实现分子个数与气体体积之间的转换,体现出获取信息与处理信息的能力。
3.B
解析:B
【解析】
利用混合物中两种物质的性质差别,分析除杂方法对混合物组成的影响,判断该方法是否能达到除去杂质的目的,选出不能达到的选项。
A. 高温充分煅烧CaCO3,生成氧化钙和二氧化碳,正确;
B. CaCl2溶液不与二氧化碳反应,故错误;
C. CO2(CO)通过足量的灼热氧化铜,CO与氧化铜反应,生成CO2,正确;
D. HCl气体溶于水与NaOH溶液反应生成氯化钠和水,氢气不与氢氧化钠反应,然后通过浓硫酸干燥,正确。
点睛:除去混合物中的杂质,所选用的试剂或方法应对杂质有作用,不影响主要成分,并且过程中不能产生新的杂质。
4.C
解析:C
【解析】表面被氧化的镁条其成分有氧化镁和镁,其中镁与盐酸反应生成氯化镁和氢气,氧化镁和盐酸反应生成氯化镁和水;表面被氧化的镁条样品6g,加入到盛有73g质量分数为19%的稀盐酸的烧杯中恰好完全反应,所以反应后镁元素都以氯化镁的形式存在;由氯化镁的化学式MgCl2-可得镁元素与氯元素的关系式如下:Mg---2Cl- MgCl2-2HCl,Mg--- -2HCl,设样品中镁元素的质量为x,Mg---2HCl
24 73
x 73g×19%
x=4.56g 則原镁条样品中镁元素的质量分数为4.56g÷6g×100%=76%
点睛:利用反应前后元素的种类质量不变计算使计算题变得简单。
5.B
解析:B
【解析】
硫酸铜易溶于水,而铁不溶,所以加水溶解过滤后可将二者分离,洗涤干燥后,可得纯的铁粉;二氧化锰不溶于水,氯化钾易溶于水,所以加水溶解过滤后可将二者分离,洗涤干燥后,可得纯的二氧化锰;二氧化碳不可燃、不助燃,无法将其中的氢气点燃,不能达到除杂的目的;硝酸钡和硫酸钾反应生成硫酸钡沉淀和硝酸钾,但是由于硝酸钡过量,会引入新的杂质硝酸钡。选B
点睛:除杂的原则:只除杂,不引杂。即所加试剂只能与杂质反应,不能与想要的主要成分反应,同时不能引入新的杂质
6.C
【解析】A、在溶解度曲线图上,横坐标是温度,纵坐标是溶解度。溶解度是一定温度下,100g溶剂里达到饱和时,所溶解的溶质的质量。饱和溶液是在一定温度下、一定量的溶剂里不能再溶解某物质的溶液叫该物质的饱和溶液,反之为不饱和溶液。由图知,丙的溶解度随温度的升高而减小,所以将丙的饱和溶液升温时会有晶体析出;B. 在t3℃时,分别制成等质量的甲、乙的饱和溶液,乙中溶质质量比甲中的小;C. M点和N点溶剂的质量相等,M中溶质的质量比N点溶质多,即M点溶液的质量分数比N的大,所以组成为N点的甲溶液可通过增加溶质或恒温蒸发水变为M点的溶液;D. 饱和溶液溶质的质量分数=溶解度÷(溶解度+100g)×100% ,将t3℃时的甲、乙、丙三种物质的饱和溶液降温到t2℃,甲乙的溶解度减小,析出晶体,得t2℃时的饱和溶液,t2℃时,乙的溶解度大于甲的溶解度,质量分数乙>甲;降温时丙的溶解度增大,溶质的质量等于t3℃时的溶解度,而丙
t3℃时的溶解度小于t2℃时甲的溶解度,这三种溶液的溶质质量分数的大小关系是乙>甲>丙;选C
点睛:在溶解度曲线图上,溶剂的量都是100g,所以分析溶质的质量分数时,只需要比较溶质的多少即可。溶解度变大时,溶质不变,溶解度减小时溶质质量等于减小后的溶解度7.A
解析:A
【解析】A. 一定温度下,向一定量水中加入KNO3固体,随固体溶解,溶质增多,溶质的质量分数增大,饱和后,溶质质量分数不再改变。 B. 高锰酸钾在加热条件下分解生成锰酸钾、二氧化锰、氧气,所以反应中固体减少,完全反应后固体的质量为二氧化锰和锰酸钾的质量和。C. 向一定量的硫酸铜溶液中加入铁粉,溶质硫酸铜转化成硫酸亚铁,二者的质量比为160:152,而溶剂不变,所以反应中溶液质量减少; D. 向一定量的MnO2中加入H2O2溶液,二氧化锰是反应的催化剂,质量不变。选A
8.C
解析:C
【解析】A氮气不可燃不助燃,使氮气中的少量氧气不能与木炭充分接触,不能使氧气转化成二氧化碳,不能除杂;B盐酸能与氢氧化钠反应;C盐酸与氧化铜反应生成氯化铜溶液,铜不与盐酸反应,过滤后固体只有铜;D碳酸氢钠在加热条件下分解生成碳酸钠。选C
点睛:除杂的原则:只除杂,不引杂。即所加试剂只能与杂质反应,不能与想要的主要成分反应,同时不能引入新的杂质
9.C
解析:C
【解析】
A、胃液的pH<7,图像应该从小于7开始逐渐增大,但最后也应该是酸性,错误;
B、氢氧化钠溶液与稀盐酸反应无沉淀生成,当稀盐酸反应完以后,氢氧化钠溶液才与氯化铜反应产生沉淀,错误;
C、等质量的镁和铁分别投入到足量同种稀硫酸中,镁与稀硫酸反应生成的氢气多,镁的金属活动性比铁强,故在开始的相等时间内,镁与稀硫酸反应生成的氢气多,正确;
D、浓盐酸具有挥发性,敞口放置溶质质量分数减小,错误。故选C。
解析:C
【解析】A 、氧化钙、碳酸钙都能盐酸反应;B 、氢氧化钠溶液与二氧化碳和氯化氢都能反应;C 铜的金属活动性比银强,铜和硝酸银反应生成硝酸铜和银,过滤后溶液中溶质只有硝酸铜;D 二氧化碳不可燃不助燃,不能将二氧化碳中的一氧化碳点燃,不能达到除杂要求;选C
点睛:除杂的原则:只除杂,不引杂。即所加试剂只能与杂质反应,不能与想要的主要成分反应,同时不能引入新的杂质
11.B
解析:B 【解析】
A 、Fe 是活泼金属,加入足量的稀硫酸,能反应生成易溶于水的氯化亚铁,铜不与酸反应,过滤,洗涤,干燥后得到金属铜;
B 、Cu(OH)2固体,加入适量稀盐酸,氢氧化铜会被反应生成易溶的氯化铜;
C 、HCl 和AgNO 3溶液反应生成氯化银沉淀和硝酸,过滤溶液中溶质只有硝酸;
D 、CO 2 和氢氧化钠溶液反应生成碳酸钠和水,一氧化碳不反应,然后将气体干燥,得纯净的一氧化碳。选B
点睛:除杂的原则:只除杂,不引杂。即所加试剂只能与杂质反应,不能与想要的主要成分反应,同时不能引入新的杂质
12.A
解析:A 【解析】 【分析】
四种金属的活动性顺序为:锌>铁>铜>银,将a g 铁粉和锌粉的混合物加入到b g AgNO 3和Cu(NO 3)2组成的混合溶液中,反应顺序是,锌先与盐溶液反应,锌完全反应后,如果硝酸银或硝酸铜有剩余,铁在与两溶液反应;①锌和硝酸银反应生成硝酸锌和银,②锌和硝酸铜反应生成铜和硝酸锌,反应中金属的质量关系如下:
3322AgNO +Zn =Zn NO +2A 6()g
5216
3232Cu NO +Zn =()()Zn NO +Cu
6564
3232Cu NO +Fe =()()Fe NO +Cu
5664
【详解】
A 、铁和硝酸银、硝酸铜反应时,随着反应的进行,溶液质量减小,固体质量增加,锌和硝酸银反应时,随着反应的进行,溶液质量减小,固体质量增加,锌和硝酸铜反应时,随着反应的进行,溶液质量增加,固体质量减小,当锌和硝酸铜的质量远远大于铁和硝酸银的质量时,滤渣的质量会小于ag ,该选项说法不正确; B. 若滤渣中含有单质Zn ,则滤液一定是无色溶液;
C. 若向滤渣中加入足量的稀盐酸有气泡冒出,则滤渣中一定含有Ag、Cu、Fe,由于锌先反应,锌可能剩余,也可能反应完;
D. 若向滤液中加入足量的稀盐酸有白色沉淀产生,则硝酸银有剩余,硝酸铜没反应,锌和铁都反应完,则滤液中的一定含有银离子,四种金属阳离子。选A
【点睛】
金属活动顺序表:K Ca Na Mg Al Zn Fe Sn Pb H Cu Hg Ag Pt Au,在金属活动顺序表中,排在氢前边的金属能和酸发生置换反应生成盐和氢气。金属的位置越靠前,金属的活动性越强。位置靠前的金属能将位于其后的金属从它的盐溶液中置换出来。
13.B
解析:B
【解析】
【分析】
根据原物质和杂质的性质选择适当的除杂剂和分离方法,所谓除杂(提纯),是指除去杂质,同时被提纯物质不得改变.除杂质题至少要满足两个条件:①加入的试剂只能与杂质反应,不能与原物质反应;②反应后不能引入新的杂质。
【详解】
A、CaCO3固体高温下分解生成氧化钙和二氧化碳,反而会把原物质除去,不符合除杂原则,故选项所采取的方法错误;
B、氧气通过灼热的铜网时可与铜发生反应生成氧化铜,而氮气不与铜反应,能除去杂质且没有引入新的杂质,故选项所采取的方法正确;
C、方法不正确的原因为:1、一氧化碳在高二氧化碳浓度的情况下无法被点燃,2、有氧气容易导致气体不纯净,3、无法收集二氧化碳,故选项所采取的方法错误;
D、CaCl2溶液能与碳酸钠溶液反应生成碳酸钙沉淀和氯化钠,能除去杂质但引入了新的杂质氯化钠,不符合除杂原则,故选项所采取的方法错误。
故选B。
【点睛】
除去混合物中的杂质,所选用的试剂或方法应对杂质有作用,不影响主要成分,并且过程中不能产生新的杂质。
14.D
解析:D
【解析】
提纯含少量氯化钠杂质的硝酸钾,结合流程可知,操作Ⅰ为溶解,二者溶解度受温度影响不同,采取冷却热饱和溶液法分离出硝酸钾,则操作Ⅱ为蒸发浓缩,冷却结晶,操作Ⅲ是过滤、洗涤;A、提纯含少量氯化钠杂质的硝酸钾,结合流程可知,操作Ⅰ为溶解,操作Ⅱ为蒸发浓缩,冷却结晶,操作Ⅲ是过滤、洗涤,错误;B、提纯含少量氯化钠杂质的硝酸钾,结合流程可知,操作Ⅰ为溶解,错误;C、提纯含少量氯化钠杂质的硝酸钾,结合流程可知,操作Ⅱ为蒸发浓缩,冷却结晶,错误;D、提纯含少量氯化钠杂质的硝酸钾,结合流程可知,操作Ⅲ是过滤,将硝酸钾晶体从溶液中分离出来,正确。故选D。
15.B
【解析】A、氧气与硫反应可得二氧化硫,二氧化硫与碱反应生成水,水电解可得氧气,故正确;
B、氢气在氧气中燃烧生成水,水无法转化为一种物质,且能生成氧气,故错误;
C、二氧化碳与水通过光合作用可得氧气,碳与氧气不完全燃烧生成一氧化碳,一氧化碳燃烧可得二氧化碳,故正确;
D、碳酸受热分解为二氧化碳,二氧化硫与碱反应生成水,水与二氧化碳反应生成碳酸,故正确。
16.B
解析:B
【解析】
【分析】
【详解】
A、a点硝酸银没有反应完全,取a点溶液,滴加稀盐酸,有白色沉淀,选项A不正确;
B、金属锌加入硝酸银和硝酸铜的溶液,先于硝酸银反应,反应到b点硝酸银反应完全,达到C点时,硝酸铜反应完全,c点溶液中溶质为Zn(NO3)2,选项B正确;
C、b~c段固体为银和铜的混合物,若取b~c段固体,滴加稀盐酸,有气泡产生,选项C 不正确;
D、金属锌加入硝酸银和硝酸铜的溶液,先于硝酸银反应,反应到b点硝酸银反应完全,达到C点时,硝酸铜反应完全,故d点时固体为3种,选项D不正确。故选B。
17.A
解析:A
【解析】A碱式碳酸铜在加热条件分解生成氧化铜、二氧化碳、水,所以加热后固体只有氧化铜;碳酸钾和氯化钙反应生成碳酸钙沉淀和氯化钾,但是碳酸钾过量,会引入新的杂质。C、铁和氯化铜反应生成氯化亚铁和铜,反应后应将铜、过量的铁通过过滤除掉;D氢氧化钠溶液与二氧化碳反应,不符合除杂要求。选A
点睛:除杂的原则:只除杂,不引杂。即所加试剂只能与杂质反应,不能与想要的主要成分反应,同时不能引入新的杂质
18.C
解析:C
【解析】A. 催化剂只改变反应速率,不改变生成物质量,加热等质量的氯酸钾制氧气,加不加催化剂,最后生成氧气的量相同 B. 含有水蒸气的氢气通过浓硫酸,水被吸收,气体质量减少;
C. 引淡水浸泡盐碱地,碱性变弱,但始终呈碱性,pH始终大于7;
D. 向硝酸钡溶液中滴加稀硫酸,两种立刻反应生成硫酸钡沉淀,选C
点睛:图像的问题主要是结合化学反应分析图的起点的位置,变化趋势,终点的位置是否正确
19.C
解析:C
【详解】
铜不与盐酸反应。设2.3g铁、铝、钠,镁、锌与酸反应分别生成氢气的质量为x、m、n、a、b
Fe +2HCl== FeCl2+H2↑
56 2
2.3g x 56/2.3g=2/x x=0.082g
2Al+6HCl==2AlCl3+3H2↑
54 6
2.3g m
54/2.3g=6/m m=0.26g
2Na+2HCl== 2NaCl+H2↑
46 2
2.3g n 46/2.3g=2/n n=0.1g
Mg+2HCl== MgCl2+H2↑
24 2
2.3g a 24/2.3g=2/a a=0.19g
Zn+2HCl==ZnCl2+H2↑
65 2
2.3g b 65/2.3g=2/b b=0.07g
选C
点睛:混合物生成氢气的能力吧介于相混合的金属各自生成氢的范围之内
20.B
解析:B
【解析】
甲、乙、丙、丁、戊分别是铁、盐酸、氢氧化钙、二氧化碳、碳酸钠中的一种,铁会与盐酸反应,盐酸会与氢氧化钙、碳酸钠反应,氢氧化钙会与盐酸、二氧化碳、碳酸钠反应,二氧化碳会与氢氧化钙反应,乙是铁,所以丙是盐酸,故B错误;甲、丁是碳酸钠或氢氧化钙,如果甲是碳酸钠,丁就是氢氧化钙,戊就是二氧化碳,合理;如果甲是氢氧化钙,丁是碳酸钠,二氧化碳不会与碳酸钠反应,不合理,所以甲是碳酸钠,丁是氢氧化钙,戊是二氧化碳,所以C正确;五种物质中,只有铁是单质所以A正确;碳酸钠和氢氧化钙,盐酸之间的反应属于复分解反应,所以D正确。故选B
21.B
解析:B
【解析】金属活动顺序表:K Ca Na Mg Al Zn Fe Sn Pb H Cu Hg Ag Pt Au,在金属活动顺序表中,排在氢前边的金属能和酸发生置换反应生成盐和氢气。金属的位置越靠前,金属的活动性越强。位置靠前的金属能将位于其后的金属从它的盐溶液中置换出来。根据金属的活泼性顺序:锌>氢>铜>银,故向锌、X、铜、银的金属混合物中加入稀硫酸,锌一定参加反应产生气泡,而铜和银一定没反应,得到的滤液A再加入过量的锌得到固体混合物
乙和滤液B,说明锌除了和过量的硫酸反应产生气体外,还和盐溶液发生了置换反应,而铜和银没有参加反应,因此是锌和X的盐溶液发生的反应,因此说明锌的活动性比X强,且X位于氢前;铜和硝酸银反应产生硝酸铜和银,因此:A、由于硝酸银是一定量,可能不足,所以固体丙中一定含有的金属是被置换出的银及原有的银,及可能有剩余的铜,错误;B、四种金属的活动性顺序由强到弱的是Zn、X、Cu、Ag,正确;C、由于硫酸过量,固体甲中只含有铜和银,没有活泼金属锌和X,错误;D、滤液A中一定有X的硫酸盐和硫酸锌,滤液A中加入锌后有气体生成,说明滤液中还有硫酸,所以溶质有三种,错误。故选B。
点睛:分析反应后的成分时除考虑生成物外,还要考虑剩余的反应物。
22.B
解析:B
【解析】
A二氧化碳不可燃不助燃,不能将二氧化碳中的少量一氧化碳点燃,不能达到除杂目的;B没有硫酸反应,银不与硫酸反应;C稀盐酸与氢氧化钠和碳酸钠都反应;D、氯化钠的溶解度受温度很小,应该用蒸发结晶提纯。选B
点睛:除杂的原则:只除杂,不引杂。即所加试剂只能与杂质反应,不能与想要的主要成分反应,同时不能引入新的杂质
23.A
解析:A
【解析】
A、食盐和高锰酸钾都能溶于水,能够达到实验目的;
B、铜和盐酸不能发生反应,不能够达到实验目的;
C、由于温度不一样,因此无法比较催化剂对反应快慢的影响,该选项不能达到实验目的;
D、实验1中蜡烛由下而上依次熄灭,说明二氧化碳密度比空气大,不燃烧,也不支持燃烧,实验2中澄清石灰水变浑浊,说明二氧化碳能使澄清石灰水变浑浊,实验1和实验2探究的化学性质不同,不能够达到实验目的。故选A。
24.B
解析:B
【解析】A、氯化钠和硫酸铜都溶于水,所以不能用过滤的方法分离,错误;B、干燥的烧杯内壁出现水雾即可检验蜡烛燃烧生成的水,正确;C、未知物中滴加盐酸产生气体,不一定含有碳酸根离子,还有可能是金属,错误;D、测定溶液的pH值不能将pH试纸湿润,否则使测量结果不准确,错误。故选B。
25.B
解析:B
【解析】
根据原物质和杂质的性质选择适当的除杂剂和分离方法,所谓除杂(提纯),是指除去杂质,同时被提纯物质不得改变.除杂质题至少要满足两个条件:①加入的试剂只能与杂质反应,不能与原物质反应;②反应后不能引入新的杂质。
A. CaO能与稀盐酸反应生成氯化钙,会把原物质除去,不符合除杂原则,故选项所采取的方法错误;
B. HCl 气体能与氢氧化钠溶液反应生成氯化钠和水,氢气不与氢氧化钠溶液反应,再通过浓硫酸除去水分,能除去杂质且没有引入新的杂质,符合除杂原则,故选项所采取的方法正确;
C. 过量的Na 2CO 3溶液是杂质,不符合除杂原则,故选项所采取的方法错误;
D.氢氧化钠溶液与氯化铜反应生成氢氧化铜沉淀和氯化钠。生成的氯化钠是杂质,不符合除杂原则,故选项所采取的方法错误。 故选B 。
点睛:解决除杂问题时,抓住除杂质的必需条件(加入的试剂只与杂质反应,反应后不能引入新的杂质)是正确解题的关键。
二、流程题
26.22
2Cu S+2O 2CuO+SO 高温
酸雨 3.2≤pH <4.7 AD 降温结晶 氯化铜晶体在乙
醇中溶解度较小,可减少晶体溶解损失,缩短干燥时间 80%342
160
a c BC
【解析】 【分析】 【详解】
(1)辉铜矿的主要成分是Cu 2S ,高温焙烧中有黑色固体生成,由图可知,还有二氧化硫生成,根据质量守恒定律,化学反应前后,元素的种类不变,反应物中含Cu 、S 、O ,生成物中含S 、O ,故生成物中还应含Cu ,故生成的黑色固体应是氧化铜,反应的化学方程式为:22
2Cu S+2O 2CuO+SO 高温
;
(2)二氧化硫能与水反应生成亚硫酸,导致酸雨的产生;
(3)滤液1中加入试剂X 调节溶液pH ,目的是使铁离子转化为沉淀,而铜离子不能形成沉淀,故控制pH 的取值范围为:3.2≤pH <4.7
A 、加入试剂X 的目的是调节pH 值,除去铁离子,得到氯化铜,但是不能引入新的杂质,氧化铜能与盐酸反应生成氯化铜和水,可以消耗盐酸,调节pH 值,且不会引入新的杂质,符合题意;
B 、氢氧化钠与盐酸反应生成氯化钠和水,虽然可以调节pH 值,但是引入了新的杂质氯化钠,不符合题意;
C 、铜与盐酸不反应,无法调节pH 值,不符合题意;
D 、氢氧化铜能与盐酸反应生成氯化铜和水,可以消耗盐酸,调节pH 值,且不会引入新的杂质,符合题意。 故选AD ;
(4)由图可知,操作a 是将滤液转化为氯化铜晶体,故是蒸发,包括:蒸发浓缩、降温结晶、过滤、洗涤、干燥等;
氯化铜易溶于水,能溶于酒精,故氯化铜在酒精中的溶解度小,可以减少晶体损失,同时
酒精易挥发,可以缩短干燥时间,故洗涤CuCl 2晶体时, 用乙醇代替蒸馏水的目的是:氯化铜晶体在乙醇中溶解度较小,可减少晶体溶解损失,缩短干燥时间; (5)222Cu S+2O 2CuO+SO 高温
,22CuO+2HCl=CuCl +H O ,故可得关系式:Cu 2S ~
2CuCl 2﹒2H 2O 。
解:设按上述流程最少可制得CuCl 2·
2H 2O 的质量为x 222Cu S 2CuCl 2H O 160
34280%a
x
?
16080%342a x = x =80%342
160
a ?; (6)由表中数据可知,能够得到最多Cu (OH )2的实验组是:c ;
A 、该实验已经设计了氯化铜浓度15%,温度40℃的实验组。且从30℃~40℃,转化率升高,无需设计氯化铜浓度15%,温度35℃的实验中,不符合题意;
B 、由表中数据可知,氯化铜浓度为15%,温度为40℃时,转化率最高,氯化铜浓度为15%,温度升到60℃时,转化率反而降低,故可设计氯化铜浓度15%,温度45℃,寻找最合适的温度,符合题意;
C 、由表中数据可知,氯化铜浓度越大,转化率越高,在已有的实验组中,氯化铜浓度为15%,温度为40℃时,转化率最高,故可设计氯化铜浓度20%,温度40℃的实验中,看是否能获得更高的转化率,符合题意;
D 氯化铜浓度越大,转化率越高,氯化铜浓度10%,温度40℃肯定比氯化铜浓度为15%,温度为40℃时,转化率低,无需设计该实验,不符合题意。 故选BC 。
27.Na 2CO 3 ①③② NaOH+HCl =NaCl+H 2O 2NaCl+2H 2O
通电
2NaOH+Cl 2↑+H 2↑ H 2SO 4
S NaOH 、H 2SO 4 是加快乙醇和水的蒸发,防止CuCl 被空气氧化 【解析】 【分析】 【详解】
(1)加入氯化钡溶液可以除去硫酸根离子,加入碳酸钠溶液可以除去钙离子和过量的钡离子,加入氢氧化钠溶液可以除去镁离子,因此A 溶液是碳酸钠溶液,碳酸钠的化学式是Na 2CO 3;碳酸钠溶液必须在氯化钡溶液后面加入,才能除去过量的钡离子,三种溶液的加入顺序可以①③②,也可以③①②;
(2)氢氧化钠和盐酸反应生成氯化钠和水,化学方程式为:NaOH+HCl =NaCl+H 2O ; (3)氯化钠和水电解生成氢氧化钠和氯气还有氢气,化学方程式为:2NaCl+2H 2O
通电
2NaOH+Cl 2↑+H 2↑;
(4)在化学方程式2NaCl+2CuSO 4+SO 2+2H 2O =2CuCl↓+2X+Na 2SO 4中,在反应物中:2个Na ,
