药品不良反应报告表填写模板

药品不良反应/ 事件报告表
首次报告 跟踪报告 编码:
报告类型:新的□严重□一般 报告单位类别:医疗机构 经营企业□生产企业□个人□其他□
药品不良反应报告表 填写示例及填写说明
药品不良反应/ 事件报告表 首次报告□跟踪报告□编码: 报告类型:新的□严重□一般□报告单位类别:医疗机构□经营企业□生产企业□个人□
药品不良反应/ 事件报告表示例 首次报告□跟踪报告□编码:
1.《药品不良反应/事件报告表》应填写真实事件,报表所列患者信息及怀疑药品信息项目必须真实、完整、准确。 2.《药品不良反应/事件报告表》填写字迹要清晰,其中选择项画“√”,叙述项应准确、简明,不得有缺漏项。 3. 新的□严重□一般□ (1)新的药品不良反应:是指药品说明书中未载明的不良反应。说明书中已有描述,但不良反应发生的性质、程度、后果或者频率与说明书描述不一致或者更严重的,按照新的药品不良反应处理。 根据不良反应/事件损害的严重程度,不良反应/事件可能是新的严重的,也可能是新的一般的。(2)严重药品不良反应,是指因使用药品引起以下损害情形之一的反应: 1) 导致死亡; 2)危及生命; 3)致癌、致畸、致出生缺陷; 4)导致显着的或者永久的人体伤残或者器官功能的损伤; 5)导致住院或者住院时间延长; 6)导致其他重要医学事件,如不进行治疗可能出现上述所列情况的。 (3)一般:指新的、严重的药品不良反应以外的所有不良反应。 4. 单位名称:必须填写单位的完整全称,如日照市人民医院。 5. 部门:应填写科室的标准全称,如:消化内科、普外三科等。 6. 电话:填写报告部门(即科室)的电话。 7. 报告日期:指上交不良反应/事件报告的时间。新的或严重的药品不良反应/事件应于发现之日起15日内报告,其中死亡病例须立即报告,其他药品不良反应应30日内报告。有随访信息的,应当及时报告。 8. 患者姓名:填写患者真实全名。 9. 体重:以千克为单位。如果不知道准确体重,请做一个最佳的估计。 10. 联系方式:最好填写患者的联系电话,也可填写患者的通信地址。 11. 家族药品不良反应/事件及既往药品不良反应/事件情况:请选择正确选项。如果选择“有”,则在报告的空白处清晰叙述。 12. 不良反应/事件名称:应填写不良反应中最主要、最明显的症状。 13. 不良反应/事件发生时间:应填写发生不良反应/事件的确切时间。 14. 病历(门诊)号:请如实填写,便于查找病例,具体分析不良反应/事件。 15. 不良反应/事件过程描述(包括症状、体征、临床检验等)及处理情况: 不良反应过程描述应具体、规范,须体现出“3个时间、3个项目和2个尽可能”。 *3个时间:①不良反应发生的时间;②采取措施干预不良反应的时间;③不良反应终结的时间; *3个项目:①第一次药品不良反应出现时的相关症状、体征和相关检查;②药品不良反应动态变化的相关症状、体征和相关检查;③发生药品不良反应后采取的干预措施结果;
药品不良反应分析结果汇报实例
药品不良反应分析报告 (20 年月--20 年月) 生产企业:(盖章) 地址: 联系人: 电话: 报告日期: 一、企业监测体系建设概况
我司于2006年已建立药品不良反应报告和监测体系,并有效实施。2012年按《药品不良反应报告和监测管理办法》(卫生部令第81号)》和《浙江省药品不良反应报告和监测管理实施细则》完善我司药品不良反应监测体系、组织机构,明确其职责。 我司监管网络为一线销售人员从医院收集药品不良反应报告,汇总至市场部相关人员。市场部相关人员将数据汇总至相应QA人员,QA人员将数据上报至国家药品不良反应监测系统中。 组织机构: 我司处理药品不良反应/事件的专职部门为质量保证部,监测部门为市场部。 组成人员: 质量负责人、质保部负责人、一名市场部人员、一名QA人员。 职责: (1)市场部人员和QA人员及时收集与公司生产的药品有关的安 全性信息,发现与公司有关的药品不良反应,及时通过药品不良反应监测信息网络报告。每年向所在地药品不良反应监测机构提交药品不良反应监测工作报告; (2)对严重药品不良反应或者药品群体不良事件进行调查,必要时对药品采取紧急控制措施,如召回; (3)配合各级食品药品监督管理局、卫生行政部门和药品不良反应监测机构对药品不良反应或者群体不良事件的调查,并提供调查所需的资料,并填写《药品不良反应/事件报告表》,填报内容应真实、完整、准确。 (4)开展药品不良反应报告数据与药品质量的关联性研究,必要时进行重点监测或再评价;
(5)按要求撰写和提交定期安全性更新报告; (6)正确介绍药品的使用要求和注意事项等,将说明书修改等安全性信息及时告知相关药品经营企业和医疗机构。 (7)经常查阅国家食品药品监督管理局定期通报国家药品不良反应报告和监测情况。 二、公司品种概况 我司现有1个品种:****(批准文号:国药准字*****)。20**年1月1日至9月30日,我司对该品种进行了生产......... 无监测期品种和重点监测品种。 三、产品基本信息和不良反应收集情况 (一)不良反应反馈数据核实情况: 无。 (二)反馈数据涉及产品的基本信息: 产品的批准文号、通用名称、剂型、统计周期内的销量、不良反应报告例数、严重的不良反应例数及其构成比、新的一般的不良反应例数及其构成比、死亡病例数见附表1。 我司无文号转入或转出情况。 (三)其他不良反应信息收集情况: 在此次报告时间段内,我司未收集到到涉及本企业药品的不良反应或可疑不良反应信息情况。
药品不良反应报告表填写示例及填写说明
药品不良反应/ 事件报告表 首次报告□ 跟踪报告□ 编码: 报告类型:新的□ 严重□ 一般□ 报告单位类别:医疗机构□ 经营企业□ 生产企业□ 个人□ 不良反应事件名称:不良反应事件发生时间:年月日不良反应/ 事件过程描述(包括症状、体征、临床检验等)及处理情况(可附页) 不良反应/ 事件的结果:痊愈□好转□ 未好转□ 不详□ 有后遗症□ 表现: 死亡□ 直接死因:死亡时间:年月日 停药或减量后,反应/ 事件是否消失或减轻?是□ 否□不明□ 未停药或未减量□再次使用可疑药品后是否再次出现同样反应/ 事件?是□ 否□ 不明□ 未再使用□
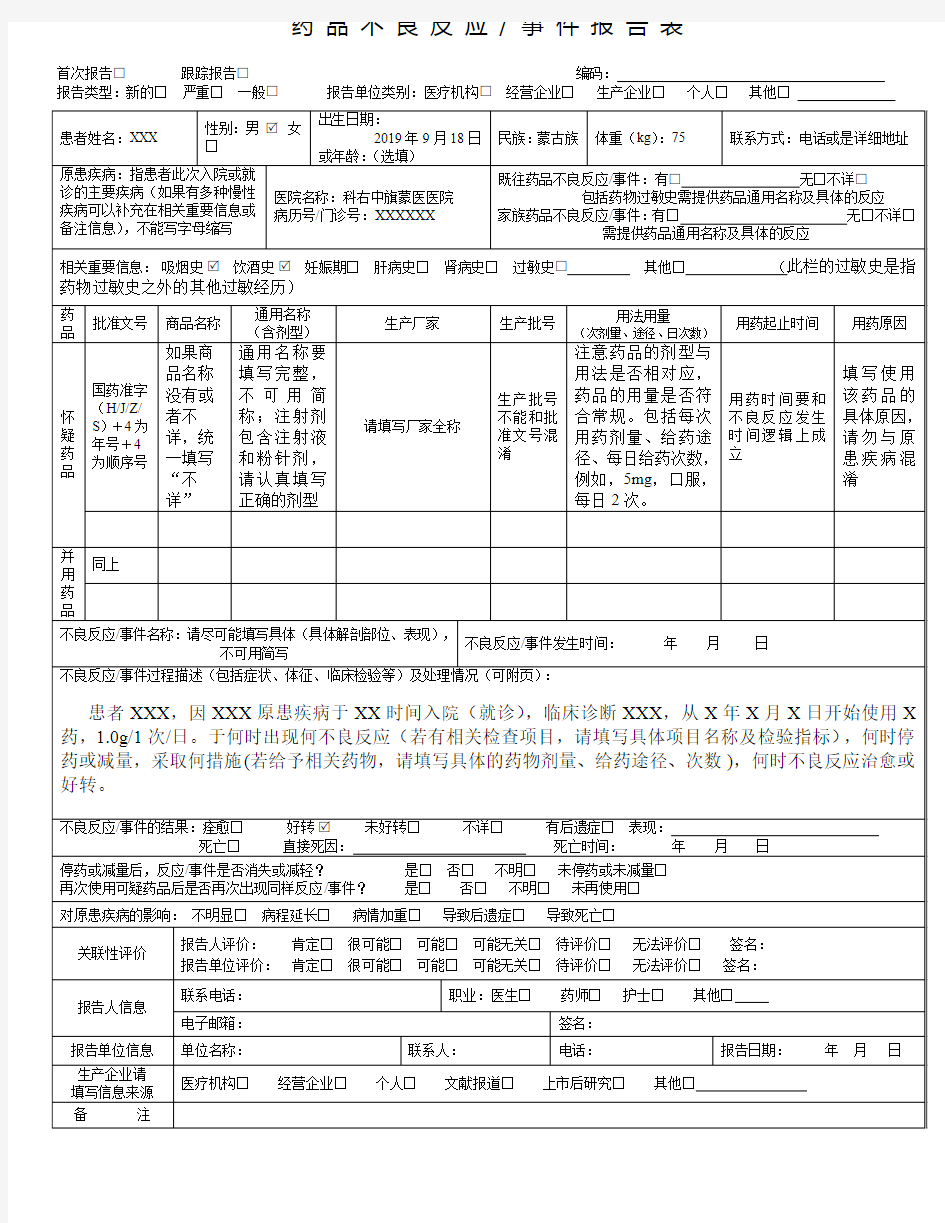
电子邮箱: 签名:××× 药 品 不 良 反 应 / 事 件 报 告 表示例 不良反应 / 事件过程描述(包括症状、体征、临床检验等)及处理情况(可附页) 一般格式为:患者因×××疾病于×××月×××日(必要时应详细到×××时分)以×××途径给予×××药品,×××剂量,用药×× ×时间出现×××反应(反应描述须明确、具体) ,×××时间后给予是否停药及×××处理(包括以×××途径给予×××药品及×××剂 和其他处理措施) ,处理后×××时间患者转归情况。 对原患疾病的影响: 不明显□ 病程延长□ 病情加重□ 导致后遗症□ 导致死亡□ 报告人评价: 肯定□ 很可能□ 可能□ 可能无关□ 待评价□ 无法评价□ 签名:××× 报告单位评价: 肯定□ 很可能□ 可能□ 可能无关□ 待评价□ 无法评价□ 签名:××× 报告人信息 患者姓名:××× 性别:男□女□ 出生日期: 年 月 日 或年龄: ×× 民族:×× 体重( kg ):×× 联系方式:×××××× 原患疾病:指患者此次入 诊的主要疾病(如果有多 疾病可以补充在相关重要 是备注里面),不能写字 院或就 种慢性 信息或 母缩写。 医院名称:三亚市中医院 病历号 / 门诊号:××××(务必 填写) 既往药品不良反应 / 事件:有□需提供药品通用名称及具体反应 无□ 不详□ 家族药品不良反应 / 事件:有□需提供药品通用名称及具体反应 无□ 不详□ 报告单位类别:医疗机构□ 其他□ 相关重要信息: 吸烟史□ 饮酒史□ 妊娠期□ 肝病史□ 肾病史□ 过敏史□此处是提供有否食物等过敏史 首次报告□ 跟踪报告□ 报告类型:新的□ 严重□ 一般□ 编码: 经营企业□ 生产企业□ 个人□ 其他□ 药 品 批准文号 商品 名称 通用名称 (含剂型) 生产厂 家 生产批号 用法用量 (次剂量、 途径、 日次数) 用药起止时 间 用药原因 怀 疑 药 品 国药准字 此处填写药品的 通用名 称。注射剂 包含注射液和粉 针剂,请认真选择 正确剂型 本次使用药 物的生产批 号 包括每次用药剂 量、 给药途径、 每日给药 次数, 例如,5mg , 口服, 每日 2 次。 指使用药品 的同 一剂量 的开始时 间 和停止时间 填写使用该药品的原因,应详 细填 写。例如:患者高血压病 史,此次因肺部感染而注射氨 苄青霉素引起不良反应,用药 原因栏应填写肺部 感染 并 用 药 品 同上 量, 不良反应 / 事件的结果:痊愈□ 死亡□ 好转□ 直接死因: 未好转□ 不详□ 有后遗症□ 表现: 死亡时间:× 年 × 月 × 日 停药或减量后,反应 / 事件是否消失或减轻? 再次使用可疑药品后是否再次出现同样反应 / 事件? 是□ 否□ 是□ 否□ 不明□ 不明□ 未停药或未减量□ 未再使用□ 关联性评价 联系电话:务必正确填写 职业:医生□ 药师□ 护士□ 其他□ 不良反应 / 事件名称:应填写不良反应中最主要、最明显的症状。 不良反应 / 事件发生时间:× 年 × 月× 日(应填写发生不良反应 / 事件 的确切时间)
关于实行《药品不良反应病例报告规范分级标准》(试行)
关于实行《药品不良反应病例报告规范分级标准》 (试行) 附录八: "药品不良反应/事件报告表"规范分级标准 0级:缺少单位名称(医院名称/企业名称)、患者姓名、不良反应/事件名称(不良反应名称)或不良反应/事件过程描述及处理情况(不良反应表现)、商品名称/通用名称(药品名称)中的任何一项视为无效报告 级:单位名称(医院名称/企业名称)、患者姓名、不良反应/事件名称(不良反应名称)或不良反应/事件过程描述及处理情况(不良反应表现)、商品名称/通用名称(药品名称) 级:级+不良反应/事件发生时间(不良反应发生时间)、用药起止时间 级:级+用法用量(日剂量)、用药原因 4级:报表中所有项目填写齐全 注:一、各级别中所列的项目均为必要条件,缺少任何一项归为下一级,关于实行《药品不良反应病例报告规范分级标准》(试行)。 二、括号中的内容,为998年版药品不良反应报告表中的相应项目。 三、单位名称项空白或填写"不详"、"不知道"、"不清
楚"、"不清"、"不明"等视为缺项。 四、患者姓名项空白或填写"不详"、"不知道"、"不清楚"、"不清"、"不明"等视为缺项。 五、不良反应/事件名称(不良反应名称)项空白或填写"不详"、"不知道"、"不清楚"、"不清"、"不明"等视为缺项;或者不良反应/事件过程描述及处理情况(不良反应表现)项空白或填写"不详"、"不知道"、"不清楚"、"不清"、"不明"等视为缺项。 六、怀疑引起不良反应的商品名称/通用名称(药品名称)项空白或填写"不详"、"不知道"、"不清楚"、"不清"、"不明"等视为缺项。 七、不良反应/事件发生时间(不良反应发生时间)项空白,视为缺项。录入数据库时填写为上报当年月日。 八、用药起止时间项空白,视为缺项。录入时填写为上报当年月日。 九、用法用量(日剂量)项空白或填写"不详"、"不知道"、"不清楚"、"不清"、"不明"者视为缺项。 十、用药原因项空白或填写"不详"、"不知道"、"不清楚"、"不清"、"不明"者视为缺项。 十一、关联性评价中省级药品不良反应监测机构项选择未评价(待评价)/无法评价时,视为缺项。 附件:
药品不良反应分析报告报告材料
药品不良反应分析报告 药品不良反应(ADR)监测是合理用药的重要依据,是关系到广大患者用药安全,减少医患纠纷的一项重要工作。我院2019年第一季度共收集报告146例,现就2019年第一季度的ADR报告进行统计、分析,了解ADR发生的一般规律和特征,为临床合理用药提供参考。 一、ADR监测统计结果及分析 1、性别与年龄分布 我院2019年第一季度共收到146例ADR报告,其中男性66人,占比45.21 %,女性80人,占比54.79%。患者的年龄分布见表1: 表1 发生ADR患者的年龄分布 年龄/岁例数/n 构成比/% 0~10 32 21.92 11~20 4 2.74 21~30 8 5.48 31~40 14 9.59 41~50 24 16.44 51~60 19 13.01 > 60 45 30.82
合计146 100.00 2、患者家族史、既往史情况 146例ADR报告中,患者既往有过敏史的26例,占17.81%;无过敏史的113例,占77.40%;不详的7例,占4.79%。146例患者中有家族药物过敏史的0例,占0%;无家族药物过敏史的51例,占34.93%;不详的95例,占65.07%。
3、患者转归情况 146例ADR中,其中痊愈77例,占52.74%;好转45例,占30.82%;不详24例,占16.44%。大多数患者经积极治疗均好转或痊愈(占83.56%),不详占16.44%,主要因为观察时间不够长,说明我院医务人员发现药品不良反应能够及时上报。 4、药品剂型及用药途径分布 药品剂型 146例病例报告涉及药品剂型17种,以注射剂为主。本季度涉及药品剂型分布及所占比例见表2。 表2 药物剂型分布 剂型例次/n 构成比/% 注射剂142 64.25 粉针剂21 9.50
药品不良反应报告表的填写要求
药品不良反应报告表的填写要求《药品不良反应/事件报告表》是药品安全性监测工作的重要档案资料,需要永久保存,务必要用钢笔填写。填写的内容和字迹要清楚、整洁;不用不规范的符号、代号,不用草体签名。报告表中选择项划√,叙述项应准确、简明。 1. 药品不良反应/事件报告表的填写 每一个患者填写一张报告表。个人报告建议由专业人员填写,可以是诊治医务人员、生产企业、经营企业专(兼)职人员及专业监测机构人员。尽可能详细填写所有项目。无法获得的项目,填写“不详”。空间不够时可附页,注明“附件”。所有附件应按顺序表明页码,并指出所描述的项目的名称。 如果报告的是补充报告请填写与原始报告相同的编号并在报告左上 方注明“补充报告”与原始报告重复的部分可不必再填写。补充报告也可不填写报告表只需要对补充部分附纸说明即可。 填写详细要求: (1)新的□严重□一般□ “一般”是指新的、严重的药品不良反应以外的所有药品不良反应。“新的”可与“严重”或“一般”复选,而“严重”与“一般”只能二选一。 (2)编码 编码为各级药品不良反应监测机构在网络报告时自动生成。 (3)单位名称 填写发现并报告药品不良反应的单位名称,要求填写全称,如不可填“人民医院”,应填写“﹡﹡省人民医院”,“﹡﹡省﹡﹡市人民医院”。 (4)部门 部门应填写标准全称或简称,如“普通外科二病房”或“普外二”,“质保部”。 (5)电话 电话号码应填写报告部门电话,注意填写区号,如:。 (6)报告日期 报告日期应为填写报告日期,如:2004年3月3日。 (7)患者姓名 填写患者真实全名。 当新生儿被发现有出生缺陷时,如果报告者认为这种缺陷可能与孕妇在怀孕期间服用药品有关,患者为新生儿。
《药品不良反应事件报告表》的填写要求
《药品不良反应/事件报告表》填写要求 《药品不良反应报告和监测管理办法》第十三条明确规定:药品生产、经营企业和医疗卫生机构必须指定专(兼)职人员负责本单位生产、经营、使用药品的不良反应报告和监测工作,发现可能与用药有关的不良反应应详细记录、调查、分析、评价、处理,并填写《药品不良反应/事件报告表》,每季度集中向所在地的省、自治区、直辖市药品不良反应监测中心报告,其中新的或严重的药品不良反应应于发现之日起15日内报告,死亡病例须及时报告。 (一)填写注意事项: 1.《办法》第十四条规定:《药品不良反应/事件报告表》的填报内容应真实、完整、准确。 2.《药品不良反应/事件报告表》是药品安全性监测工作的重要档案资料,手工报表需要长期保存,因此需用钢笔、签字笔书写,填写内容、签署意见(包括有关人员的签字)字迹要清楚,不得用报告表中未规定的符号、代号、不通用的缩写形式和花体式签名。其中选择项画“√”,叙述项应准确、完整、简明,不得有缺漏项。 3.每一个病人填写一张报告表。 4.个人报告建议由专业人员填写,可以是诊治医务人员、药品生产、经营企业专(兼)职人员及专业监测机构人员。 5.尽可能详细地填写报告表中所要求的项目。有些内容无法获得时,填写“不详。 6.对于报告表中的描述性内容,如果报告表提供的空间不够,可另附A4纸说明。在纸的顶部注明“附件”,所有的附件应按顺序标明页码,附件中必须指出描述项目的名称。
7.补充报告:如需作补充报告时,请注意与原报表编号保持一致,并在报告左上方注明“补充报告”,与原报表重复的部分可不必再填写。补充报告也可不填写报告表,只需附纸说明补充内容即可,但须注明原报表编号、单位名称、补充报告时间、报告人。 (二)填写详细要求 1.新的、严重、一般: 新的ADR:是指药品说明书中未载明的ADR。 严重ADR:是指因服用药品引起以下损害情形之一的反应: ⑴引起死亡; ⑵致癌、致畸、致出生缺陷; ⑶对生命有危险并能够导致人体永久的或显著的伤残; ⑷对器官功能产生永久损伤; ⑸导致住院或住院时间延长。 一般的ADR:是指除新的、严重的ADR以外的所有ADR。 2.单位名称:填写医疗卫生机构、药品生产企业或经营企业的完整全称。如:“镇江市第一人民医院”,不可填“一院”。 3.部门:填写报告单位的具体报告部门, 应填写标准全称或简称,如:“普通外科二病房”或“普外二”,如连锁药店应填具体的门店,零售药店可填写药店名称。
药物不良反应报告的判断
药物不良反应报告的判断、评价及 药物不良反应(Adverse Drug Reactions,ADRs)监测,在欧洲国家也习惯称为“上市后药 物监测(Postmarketing Drug Surveillance,PMDS)”,以1964年英国黄卡制度(Yellow card system)的问世而宣告诞生。ADRs监测有志愿报告体系(SPontaneous Reporting system,SRS)、集中(或强化)监测体系(intensivereporting system)等多种方式。由于SRS一直是ADRs监测的主要方式,近年来,似乎已约定俗成,ADRs监测一般指的即是SRS。SRS主要目标是尽早获得药物安生性问题的信号,为药政管理提供依据以及向卫生专业人员传递信 息。 药品不良反应常成为医疗、科学、道德、商业与诉讼的焦点。法律判决依据的事实。而 药品不良反应监测报告的不确切性,常使得问题的讨论难以为继。 ADR报告的获得过程可分析如下:(1) 不良反应事件的发生和发现;(2) 把事件的发生归因于药物,这一判断很多源于经验,通常考虑的是时间上有联系,以及没有混杂因素等; (3) 把归咎于药物的不良事件以可疑的ADR的名义向卫生行政部门或制药公司报告。而报 告的只占实际发生的不良反应事件的极少部分。 为了减少漏报,提高检测的灵敏性,一般都提倡“有疑即报”,即不必在肯定了药物与 不良事件的因果关系后再报告。 监测方法的优劣,不但要看其灵敏性,还要看其特异性。70年代后期以来,为了提高 药品不良反应监测的特异性,许多专家探讨、研究了各种因果判断方法,有的国家将其作为对厂方报告ADR时的一种要求。这一倾向曾使人们以为应用这些方法能测定具体病人或个 例报告的因果关系,能解决不确定性问题。现在已逐渐认识到这是一种偏向,但“因果”方 法也并非一无是处,它们可以告诉初报者如何考虑这是一起ADR,该收集哪些资料,该从 哪些方面描述。 为了更准确、更有质量地报告ADR,系统地了解药物不良反应判断的思路十分必要。而为 了高屋建瓴,从战略角度全面地了解药品不良反应监测的作用与地位,探讨药物警戒中的信号问题就十分必需。 1 药物不良反应报告归因判断 1.1 因果性质的标准——ADR判断时的考虑因素 ①与现有资料要有一致性(或生物学合理性) 即从已有的文献资料中其他类型信息的观点看因果联系的合理性。其他类型信息是指其他人体研究的数据,其他有关问题研究的数据,动物实验的数据以及科学的病理生理学理论。 如果某项发现能为已有的资料和理论所解释,一般就会更令人信服。 ②以往的经验,即是否已有该药反应的报道、评述等——联系的一贯性
医院药品不良反应总结分析报告
医院药品不良反应总结分析报告 年药品不良反应分析、反馈报告2014监测是合理用药的重)药品不良反应(ADR减少医患是关系到广大患者用药安全,要依据,年共收集上报2014纠纷的一项重要工作。我院
。例增加了年的7190.14%135例ADR,较2013了解ADR报告进行统计、分析,现就2014年的的一般规律和特征,为临床合理用药提供ADR 依据。报告人包括医生报告人职业和科室分布;药份,占90.37%和药师,其中医生上报12218ADR报告来自全院份,占9.63%。13师上报例门诊患者。详见3个科室,132例住院患者,。表1上报科室排序1 2014年ADR表例数(例)构成比科室11.85% 16 外三病区
11.11% 15 内一病区 11.11% 15 内二病区 10.37% 14 内四病区 8.89% 12 内三病区 7.41% 临床药学室10 5.93% 8 外一病区 5.83% 8 儿科病区 5.19% (肛中医二病区7 肠)5.19% 7 中医一病区 3.70% 5 外四病区 3.70% (康中医二病区5 复)
2.96% 4 ICU综合组 1.48% 2 妇产科病区 1.48% 2 住院药房 1.48% 2 门诊急诊科 1.48% 2 外二病区0.74% 门诊西药房 1 100% 135 合计 发AD的患者性别及年龄分布情例,中,男81例,女54ADR在报告的135例 1-95
岁,情况详见表2。年龄分布区间为表2 患者年龄分布情况百分比年龄例数1.48% 2 1小于岁2.22% 1-4岁 3 2.96% 4 5-14岁22.96% 31 岁 15-4428.15% 岁38 45-6442.22% 6557 岁及其以上100% 总计135 用药情况分析用药途径包括静脉给药及 口服、皮下注射等。最常见仍为静脉滴注,占. 3:74.85%。详细统计见表表3:给药途 径统计排名 给药途径一般严重总计 例次百分例次百分比例次
药品不良反应报告材料表填写要求
药品不良反应报告表填写要求 (试用教案) 培训题目:药品不良反应报告表如何填写 培训学时:1个学时 培训方式:集中授课 主要容: 第一部分:药品不良反应/事件的填写要求 第二部分:药品群体不良事件基本信息表的填写要求 药品不良反应报告表填写要求 一、药品不良反应报告表填写要求 《药品不良反应报告和监测管理办法》(以下简称《办法》)(卫生部令第81号)2011年05月04日发布,《办法》中针对不同报告类型提供了三份表格,分别是《药品不良反应/事件报告表》、《群体不良事件基本信息表》和《境外发生品不良反应/事件报告表》;为全面贯彻落实《办法》,下面将分别对三份表格填写要求进行详细的说明。 二、《药品不良反应/事件报告表》 1.法规依据 《药品不良反应报告和监测管理办法》 第十九条药品生产、经营企业和医疗机构应当主动收集药品不良反应,获知或者发现药品不良反应后应当详细记录、分析和处理,填写《药品不良反应/事件报告表》(见附表1)并报告。 第二十条新药监测期的国产药品应当报告该药品的所有不良反应;其他国产药品,报告新的和严重的不良反应。 进口药品自首次获准进口之日起5年,报告该进口药品的所有不良反应;满5年的,报告新的和严重的不良反应。 第二十一条药品生产、经营企业和医疗机构发现或者获知新的、严重的药品不良反应应当在15日报告,其中死亡病例须立即报告;其他药品不良反应应当在30日报告。有随访信息
的,应当及时报告。 2.新旧表格的不同--详见ppt 3.填写详细要求 目前国家药品不良反应监测中心制定的《药品不良反应/事件报告表》可大致分为报告基本情况、患者基本情况、使用药品情况、ADR过程描述、关联性评价、报告人报告单位信息六部分。 3.1报告的基本信息 首次报告□跟踪报告□ 如果报告的是跟踪报告,如果报告的是跟踪报告,搜索到原始报告后在原始报告上进行修改,补充资料后保存。 编码 是报告单位部编码,电子上报后自动形成的编码,报告单位要记录在纸制报告上 报告类型 新的□严重□一般□ 新的药品不良反应,是指药品说明书中未载明的不良反应。说明书中已有描述,但不良反应发生的性质、程度、后果或者频率与说明书描述不一致或者更严重的,按照新的药品不良反应处理。 (原:新的药品不良反应是指药品说明书中未载明的不良反应。) 严重药品不良反应,是指因使用药品引起以下损害情形之一的反应: 1.导致死亡; 2.危及生命; 3.致癌、致畸、致出生缺陷; 4.导致显著的或者永久的人体伤残或者器官功能的损伤; 5.导致住院或者住院时间延长; 6.导致其他重要医学事件,如不进行治疗可能出现上述所列情况的。 一般:新的、严重的药品不良反应以外的所有不良反应 报告单位类别 医疗机构□生产企业□经营企业□个人□其他 选择药品不良反应报告表的填报单位的类型
药品不良反应报告表(模版)
附表1 药品不良反应/ 事件报告表(书写模版)首次报告□跟踪报告□编码:
药品不良反应报告表 部分项目填报注意事项 一、药品不良反应事件名称及描述 1.如果患者出现皮疹伴瘙痒,不要把二者同时列为一个不良反应,应当分类描述为“皮疹;瘙痒”, 对于皮疹得发生部位、大约形态进行描述; 2.如果患者发生多种过敏反应,就不用分类描述,直接描述为“过敏反应”或就是“过敏样反应”;不属于过敏反应得其她症状,应当分类描述; 3.如果患者出现过敏性休克,就必须描述患者得临床表现(包含呼吸道阻塞、微循环障碍、中枢神经系统症状及皮肤过敏症状)及体征; 例如头晕、面色苍白、呼吸困难、胸闷、腹痛、出汗、脉搏增快及血压下降等;此时相应得体征进行描述,如体温、心率、血压、呼吸频率等;还包含不良反应发生前后得症状与体征得动态变化。 4.如果患者出现血象异常,要将不良反应发生前后相应指标、实验室检查进行描述; 例如患者白细胞降低,此时就需要提供患者入院时(或服药前)白细胞指数,服药后发生不良反应就是监测得白细胞指数以及采取措施停药后患者白细胞有所
恢复得指数。 5.如果患者出现消化道反应,例如腹泻、呕吐等,请具体描述一哈相关得症状; 例如腹泻,一日几次、什么性状;呕血,一日几次、颜色等性状;呕吐,一日几次、内容物就是什么。 二、药品不良反应发生后采取得措施及转归 1、药品不良反应发生以后,主要采取得治疗措施要进行描述。例如立即停药,给与抗过敏治疗(过敏反应)、给与升白细胞治疗(白细胞下降)、给与物理降温(高热)等对症治疗。具体得治疗措施,例如给与地塞米松10mg肌肉注射,要尽量详细描述对症治疗得药物及剂量。 2、药品不良反应得转归,要尽量描述采取对症治疗之后患者得转归。有得医疗机构在患者刚刚发生不良反应,采取措施尚未缓解得时候就立即上报,这种就是不规范得。 国家规定药品不良反应报告得上报时限。大家应当按照规定时限完整得对药品不良反应进行上报。
药品不良反应报告和监测体系运行(修订版)【新版】
目的:确保药品不良反应报告和监测工作的有效开展,有效控制药品风险,保障公众用药安全,建立药品不良反应组织机构及运行体系。 适用范围:适用于公司药品不良反应报告和监测工作。 责任人:药品不良反应办公室、质量保证部、后勤部、销售公司、科研中心 内容: 1.组织机构简图 2. 体系运行 2.1 信息采集途径 2.1.1 信息采集途径包括被动收集:销售人员、400热线投诉电话,和主动收集:上市前和上市后的临床研究、文献检索、国内外政府网站。 2.1.2 信息采集技巧:第一时间了解:判断事情的严重性。是否停药?是否上报?是否召回? 第一时间控制:控制医生态度,控制患者情绪; 第一时间反馈:及时反馈至ADR管理员或药品不良反应办公室主任; 长期应对准备:掌握我公司产品主要不良反应及质量特性等,并具有一定的ADR判断能力,若不能独立解答患者疑问,切忌给予医疗服务建议,药品不良反应办公室给予支持。 信息收集要全:因其他原因不能全面收集ADR信息,至少收集以上四要素及时反馈至ADR管理员处,协助做好相关沟通工作。 2.2 单个病例管理 2.2.1 单个病例处理流程:收集(多渠道)→报告公司关联性评价→随访→上报ADR监测系统→纳入公司不良反应病例数据库。 2.2.2 出现药品不良反应及出现其他情况均应报告,即使没有伴随具体的不良事件,如: ·说明书已知一般不良反应、严重不良反应和新的不良反应 ·因药品停用而发生的事件 ·超适应症用药 ·孕妇暴露
·药品无效 ·用药错误 ·死亡结局 ·出现未预期的治疗/临床益处 2.2.3 临床试验安全性信息报告 临床试验定义:任何在人体(病人或健康志愿者)进行的药物系统性研究,以证实或揭示试验药物的作用、不良反应或试验药物吸收、分布、代谢和排泄,其目的是确定试验药物的疗效与安全性。 临床试验类别:I、Ⅱ、Ⅲ、IV期临床试验、生物等效性试验、重点监测、一致性评价、临床有效性试验及其他安全与疗效对比研究等。 上报流程: 研究者上报所有不良事件;申办方上报严重不良事件(时限:死亡和危及生命为7天,其他情况15天),以电话、传真或EMS邮寄的形式向CFDA注册司、BFDA注册处及卫计委提交首次报告,及时提交随访报告,并将收集的所有不良事件报告1个工作日内反馈至公司不良反应办公室;不良反应办公室按法规时限要求上报上市后临床研究不良反应,上市前不良反应长期保存,待产品上市后纳入不良反应数据库并带入PSUR中。 2.2.4 个例不良反应/事件评价、上报 2.2.4.1 不良反应/事件类型: 依据《药品不良反应和监测管理办法》对一般的、新的和严重的不良反应的定义,对比说明书中不良反应描述,确定不良反应/事件的类型。 2.2.4.2 不良反应/事件关联性评价: 从时间相关性、药理作用/同类药物反应、去激发、再激发、剂量等方面对不良事件与药品之间关系进行评定。同时考虑的其他因素:原患疾病、相互作用、伴随药物、伴发疾病。时间相关性:用药前、用药过程中或延迟发生不良反应的可能。 2.2.4.3 药理作用/同类药物反应:不良事件发生时间是否与药理/毒理反应一致,同类药物的不良反应。 去激发:停药观察,去激发是否为阳性 再激发:去激发后再次给药观察,再激发是否为阳性。 给药剂量:规定给药剂量与实际给药剂量是否一致。 原患疾病:分析不良事件是否为原患疾病的症状,或治疗适应症的自然进程。 药物相互作用:协同作用、拮抗作用、配伍禁忌。 伴随药物/伴发疾病:是否导致不良事件的发生。 其他因素:是否存在其他风险因素,如吸烟史、饮酒史、过敏史、家族病史及不良反应病史等。
药品不良反应事件报告登记本.doc
药品不良反应/事件报告登记本 年
药剂科
药品不良反应/事件报告登记本 ADR信息监测员: 赠送资料 青花鱼(北京)健康产业科技有限公司 2018年财务分析报告 1 .主要会计数据摘要 2 . 基本财务情况分析 2-1 资产状况 截至2011年3月31日,公司总资产20.82亿元。 2-1-1 资产构成 公司总资产的构成为:流动资产10.63亿元,长期投资3.57亿元,固定资产净值5.16亿元,无形资产及其他资产1.46亿元。主要构成内容如下:
(1)流动资产:货币资金7.01亿元,其他货币资金6140万元,短期投资净值1.64亿元,应收票据2220万元,应收账款3425万元,工程施工6617万元,其他应收款1135万元。 (2)长期投资:XXXXX2亿元,XXXXX1.08亿元,XXXX3496万元。 (3)固定资产净值:XXXX净值4.8亿元,XXXXX等房屋净值2932万元。 (4)无形资产:XXXXXX摊余净值8134万元,XXXXX摊余净值5062万元。 (5)长期待摊费用:XXXXX摊余净值635万元,XXXXX摊余净值837万元。 2-1-2 资产质量 (1) 货币性资产:由货币资金、其他货币资金、短期投资、应收票据构成,共计9.48亿元,具备良好的付现能力和偿还债务能力。 (2) 长期性经营资产:由XXXXX构成,共计5.61亿元,能提供长期的稳定的现金流。 (3) 短期性经营资产:由工程施工构成,共计6617万元,能在短期内转化为货币性资产并获得一定利润。 (4) 保值增值性好的长期投资:由XXXX与XXXX的股权投资构成,共计3.08亿元,不仅有较好的投资回报,而且XXXX的股权对公司的发展具有重要作用。 以上四类资产总计18.83亿元,占总资产的90%,说明公司现有的资产具有良好的质量。2-2 负债状况 截至2011年3月31日,公司负债总额10.36亿元,主要构成为:短期借款(含本年到期的长期借款)9.6亿元,长期借款5500万元,应付账款707万元,应交税费51万元。 目前贷款规模为10.15亿元,短期借款占负债总额的93%,说明短期内公司有较大的偿债压力。结合公司现有7.62亿元的货币资金量来看,财务风险不大。 目前公司资产负债率为49.8%,自有资金与举债资金基本平衡。 2-3 经营状况及变动原因
药品不良反应填写规范
药品不良反应病例报告填写录入规范 (试行) 总则 1.目的:为了规范报表填写录入,提高报表质量,加快上报效率,提取有效预警信号,综合我院日常报表填写录入存在的问题和药品不良反应监测报告填报要求,特制定本规范。 2.依据:《药品不良反应报告和监测管理办法》和《江苏省药品不良反应监测工作暂行规定》。第二章基本要求 3.《药品不良反应报告表》的填报内容应真实、完整、准确,符合规定时限。 新的、严重的药品不良反应应当在15日内报告,其中死亡病例须立即报告;其他药品不良反应应当在30日内报告。有随访信息的,应当及时报告。(此为上报监测中心时限) 4.药品不良反应名称填写应准确、完整。新的药品不良反应要认真核对说明书。 5.所有的不良反应要核对是否有并用药品。 6.不良反应过程描述及处理情况应详细规范填写,如有并用药品,则应包含并用药品使用情况。 7.药品信息项下的怀疑和并用药品的药品通用名称、药品生产企业名称、药品生产批号应真实、完整、准确。生产批号应认真核对,必要时进行核实。有并用药品的,药品信息项不能缺少并用药品信息。 8.审核员在收到报告表之后,要对报告表进行认真审核,如发现生产企业名称相同、不良反应表现类似、不良反应发生时间和地点比较集中、药品名称和批号相同等聚集性特点的报告,应密切关注,及时进行核实,报告医院药品不良反应监测办公室,由医院药品不良反应监测办公室报告市级药品监督管理部门,上报省药品不良反应监测中心。 第三章一般信息 9.报告类别:新的□严重□一般□ 分一般的、严重的、新的一般、新的严重四类。 (1)一般的:是指药品说明书中载明的不良反应; (2)严重的:是指药品说明书中载明且符合严重药品不良反应判定5条标准之一的;
药品不良反应报告表模板
药品不良反应报告表 部分项目填报注意事项 一、药品不良反应事件名称及描述 1.如果患者出现皮疹伴瘙痒,不要把二者同时列为一个不良反应,应当分类描述为“皮疹;瘙痒”, 对于皮疹的发生部位、大约形态进行描述; 2.如果患者发生多种过敏反应,就不用分类描述,直接描述为“过敏反应”或是“过敏样反应”;不属于过敏反应的其他症状,应当分类描述; 3.如果患者出现过敏性休克,就必须描述患者的临床表现(包含呼吸道阻塞、微循环障碍、中枢神经系统症状及皮肤过敏症状)及体征; 例如头晕、面色苍白、呼吸困难、胸闷、腹痛、出汗、脉搏增快及血压下降等;此时相应的体征进行描述,如体温、心率、血压、呼吸频率等;还包含不良反应发生前后的症状和体征的动态变化。 4.如果患者出现血象异常,要将不良反应发生前后相应指标、实验室检查进行描述; 例如患者白细胞降低,此时就需要提供患者入院时(或服药前)白细胞指数,服药后发生不良反应是监测的白细胞指数以及采取措施停药后患者白细胞有所恢复的指数。
5.如果患者出现消化道反应,例如腹泻、呕吐等,请具体描述一哈相关的症状; 例如腹泻,一日几次、什么性状;呕血,一日几次、颜色等性状;呕吐,一日几次、内容物是什么。 二、药品不良反应发生后采取的措施及转归 1、药品不良反应发生以后,主要采取的治疗措施要进行描述。例如立即停药,给与抗过敏治疗(过敏反应)、给与升白细胞治疗(白细胞下降)、给与物理降温(高热)等对症治疗。具体的治疗措施,例如给与地塞米松10mg肌肉注射,要尽量详细描述对症治疗的药物及剂量。 2、药品不良反应的转归,要尽量描述采取对症治疗之后患者的转归。有的医疗机构在患者刚刚发生不良反应,采取措施尚未缓解的时候就立即上报,这种是不规范的。 国家规定药品不良反应报告的上报时限。大家应当按照规定时限完整的对药品不良反应进行上报。 备注:提供一个药品不良反应/事件报告表填写模板(见附表),供大家参考。
药品不良反应报告表
药品不良反应/ 事件报告表 ※新的□严重□一般□医疗卫生机构□生产企业经营企业□个人□编码□□□□□□□□□□□□□□□□□□□单位名称:部门:※电话:※报告日期:年月日 ※电话: ◇不良反应/事件分析
※停药或减量后,反应/事件是否消失或减轻?是□否□不明□未停药或未减量□ ※再次使用可疑药品后是否再次出现同样反应/事件?是□否□不明□未再使用□ PS: 用法用量: 用量:___(毫升、微升、毫克、微克、粒、片、等……) 给药途径:____(静滴、肌注、皮下注射、口服、含服、外用等……) 不良反应/事件需填写具体症状,如: 皮肤反应:皮疹、斑丘疹、皮炎、荨麻疹、风团、水疱、瘙痒、面部水肿、眼睑水肿、皮肤红肿、硬结、局部发热、皮肤发冷、出汗、出血点、皮肤潮红等 胃肠道反应:恶心、反胃、反酸、呕吐、腹痛、腹胀、腹泻、大便次数增加、胃不适、便秘、便血、口干、口(舌)麻木、口腔金属味、消化道出血、胃溃疡、大小便失禁等 全身系统:胸闷、发热、寒战、颤抖、抖动、乏力、食欲不振等 神经系统:头晕、头痛、麻木、抽搞、癒痛、感觉异常、意识模糊、意识丧失、晕厥、牙关紧闭、反应迟钝、嗜睡、兴奋、坐立不安、烦躁、幻觉等 心血管系统:心慌、心悸、心律失常、心电图异常、心区不适、心动过缓、心脏停搏、紫绀、血压降低、血压升高、休克等 呼吸系统:呼吸困难、呼吸急促、咽喉不适、喉头水肿、咽喉发紧、喉部窒息感、舌水肿、哮喘等 肾功能:肾功能异常、无尿、少尿、排尿困难、肾衰竭等 肝功能:肝功能异常、转氨酶升高、黄疸、肝功能衰竭等。 其他:静脉炎、注射部位疼痛、红肿、硬结;牙龈出血、鼻出血(主要针对抗凝血药和容易导致出血的药面色苍白、月经紊乱、耳鸣、味觉异常、肌肉疼痛、骨髓抑制(血小板、白细胞、粒细胞等减少)、 肌肉痛、胸痛、腰痛等。 皮肤及其附件损害:渗出性红斑、多形性红斑、剥脱性皮炎 ?胃肠系统损害:消化性溃疡、胃肠道出血、呕血、肠梗阻 ?呼吸系统损害:支气管痉挛、哮喘、呼吸抑制、呼吸困难、喉水肿、肺水肿 ?中枢及外周神经系统损害:锥体外系病、张力亢进、语言障碍、舌麻痹、脑水肿、惊厥、昏迷 ?红细胞异常:溶血性贫血、全血细胞减少、骨髓抑制 ?心率及心律紊乱:心脏停搏、房颤 ?心血管系统一般损害:紫绀、体位性低血压、高血压、低血压 ?白细胞和网状内皮系统异常:粒细胞减少、白细胞减少 ?心外血管损害:脑出血、过敏性紫癜 ?肝胆系统损害:肝炎、肝细胞损害、肝功能异常 ?神经紊乱:谵妄、意识模糊 ?血小板和出血,凝血障碍:紫癜、血小板减少性紫癜、血小板减少、凝血障碍、非特异性出血 ?泌尿系统损害:血尿、肾功能异常、排尿困难、尿潴留、急性肾衰竭 ?代谢和营养障碍:痛风、高血糖、高尿酸血症、低血糖昏迷、低血糖、低血钾、低钠血症 ?肌肉骨骼系统损害:肌痛、肌病、横纹肌溶解
药品不良反应检测报告管理规程
发放部门: 1.目的:用于规范公司药品不良反应信息的收集、调查、处理、上报等内容,以提高药品质量及时、有效控制药品风险,保障公众用药安全有效。 2.范围:适用于公司生产的药品不良反应报告和监测。 3.定义 3.1 药品不良反应:是指合格药品在正常用法用量下出现的与用药目的无关的有害反应。 3.2 药品不良反应报告和监测:是指药品不良反应的发现、报告、评价和控制的过程。 3.3 严重药品不良反应:是指因使用药品引起以下损害情形之一的反应:①导致死亡;②危及生命;③致癌、致畸、致出生缺陷;④导致显著的或者永久的人体伤残或者器官功能的损伤;⑤导致住院或者住院时间延长;⑥导致其他重要医学事件,如不进行治疗可能出现上述所列情况的。 3.4 新的药品不良反应:是指药品说明书中未载明的不良反应。说明书中已有描述,但不良反应发生的性质、程度、后果或者频率与说明书描述不一致或者更严重的,按照新的药品不良反应处理。
3.5 药品群体不良事件:是指同一药品在使用过程中,在相对集中的时间、区域内,对一定数量人群的身体健康或者生命安全造成损害或者威胁,需要予以紧急处置的事件。 3.6 同一药品:指同一生产企业生产的同一药品名称、同一剂型、同一规格的药品。 3.7 药品重点监测:是指为进一步了解药品的临床使用和不良反应发生情况,研究不良反应的发生特征、严重程度、发生率等,开展的药品安全性监测活动。 3.8 怀疑药品:是指患者使用的怀疑与不良反应发生有关的药品。 3.9 并用药品:指发生此药品不良反应时患者除怀疑药品外的其他用药情况,包括患者自行购买的药品或中草药等。 3.10 用法用量:包括每次用药剂量、给药途径、每日给药次数,例如,5mg,口服,每日2 次。 4.职责 4.1 药品不良反应监测部负责药品不良反应信息的收集、整理和上报工作。4.2 质量部、销售部负责协助不良反应监测部完成需相关工作。 4.3 质量受权人负责所有上报文件的签批。 5.内容 5.1 不良反应报告与处置 5.1.1 基本要求 5.1.1.1 在获知或者发现可能与用药有关的不良反应,应当通过国家药品不良反应监测信息网络报告;不具备在线报告条件时,应当通过纸质报表报所在地药品不良反应监测机构,由所在地药品不良反应监测机构代为在线报告。 5.1.1.2 出现不良反应或者群体不良事件时,应当配合药品监督管理部门、卫生行政部门和药品不良反应监测机构对药品不良反应或者群体不良事件的调查,并提供调查所需的资料。
药品不良反应报告表填写注意事项
药品不良反应报告表填写注意事项 一、报告的基本信息 首次报告□跟踪报告□ 如果报告的是跟踪报告,搜索到原始报告后在原始报告上进行修改,补充资料后保存。 二、编码 是报告单位内部编码,电子上报后自动形成的编码,报告单位要记录在纸制报告上 三、报告类型 新的□严重□一般□ 新的药品不良反应,是指药品说明书中未载明的不良反应。说明书中已有描述,但不良反应发生的性质、程度、后果或者频率与说明书描述不一致或者更严重的,按照新的药品不良反应处理。 严重药品不良反应,是指因使用药品引起以下损害情形之一的反应: 1.导致死亡; 2.危及生命; 3.致癌、致畸、致出生缺陷; 4.导致显著的或者永久的人体伤残或者器官功能的损伤; 5.导致住院或者住院时间延长; 6.导致其他重要医学事件,如不进行治疗可能出现上述所列情况的。 一般:新的、严重的药品不良反应以外的所有不良反应 四、原患疾病:患者所患的所有疾病。疾病诊断应填写标准全称,如急性淋巴细胞白血病,不能写ALL。
填写中容易出现的问题:原患疾病:即病历中的诊断,首先审核原患疾病的名称是否规范,是否存在缩写、英文符号;若同时患有几种疾病,尽量完整填写所有疾病。 五、病历号/门诊号(企业填写医院名称): ①认真填写患者的病历号(门诊号),以便于对病历详细资料的查找。 ②企业填写须填写病例发生的医院名称。 六、怀疑药品:报告人认为可能与不良反应/事件发生有关的药品。 批准文号:这是一个新增栏目,增加的目的是减少电子报表录入的工作量。因为药品批准文号是药品生产合法性的标志。《药品管理法》规定,生产药品“须经国务院药品监督管理部门批准,并发给药品批准文号”。药品生产企业的每种药品的每一规格有一个批准文号。也就是说每个批准文号是与药品生产企业、药品名称、规格对应的。药品批准文号格式:国药准字+1位字母+8位数字,试生产药品批准文号格式:国药试字+1位字母+8位数字。化学药品使用字母“H”,中药使用字母“Z”,生物制品使用字母“S”,进口分包装药品使用字母“J”。在产品的说明书和外标签上都可以找到批准文号。
