高考全国2卷化学试题及答案

绝密★启用前
2018年普通高等学校招生全国统一考试
理科综合能力测试试题卷(化学)
注意事项:
1.答卷前,考生务必将自己的姓名、准考证号填写在答题卡上。
2.作答时,务必将答案写在答题卡上。写在本试卷及草稿纸上无效。
3.考试结束后,将本试卷和答题卡一并交回。
可能用到的相对原子质量:H 1 C 12 N 14 O 16 Na 23 P 31 S 32 Fe 56
一、选择题:本题共7个小题,每小题6分,共42分。在每小题给出的四个选项中,只有一项是符合题
目要求的。
1. 化学与生活密切相关。下列说法错误的是
A. 碳酸钠可用于去除餐具的油污
B. 漂白粉可用于生活用水的消毒
C. 氢氧化铝可用于中和过多胃酸
D. 碳酸钡可用于胃肠X射线造影检查
【答案】D
2. 研究表明,氮氧化物和二氧化硫在形成雾霾时与大气中的氨有关(如下图所示)。下列叙述错误的是
A. 雾和霾的分散剂相同
B. 雾霾中含有硝酸铵和硫酸铵
C. NH3是形成无机颗粒物的催化剂
D. 雾霾的形成与过度施用氮肥有关
【答案】C
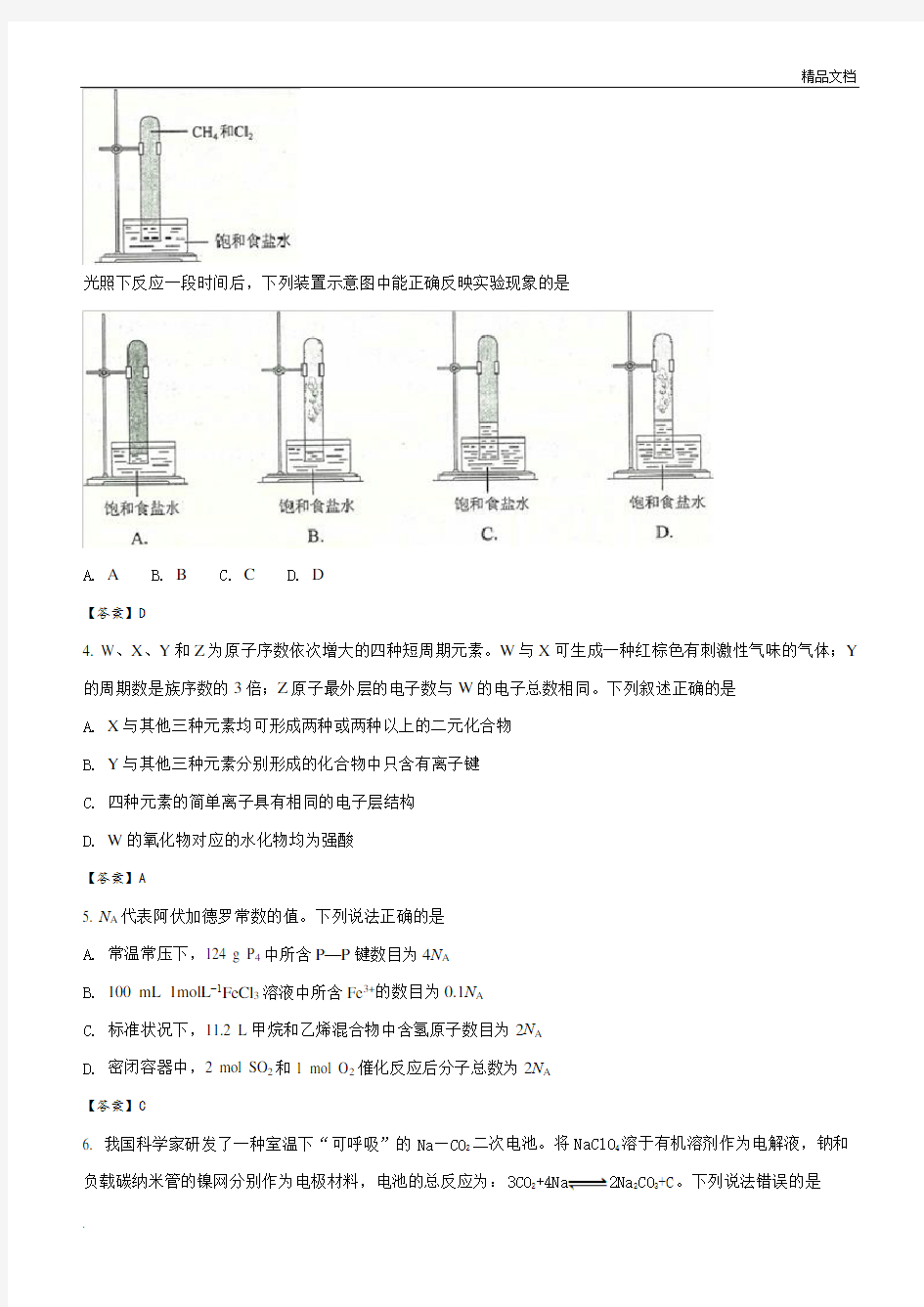
3. 实验室中用如图所示的装置进行甲烷与氯气在光照下反应的实验。
光照下反应一段时间后,下列装置示意图中能正确反映实验现象的是
A. A
B. B
C. C
D. D
【答案】D
4. W、X、Y和Z为原子序数依次增大的四种短周期元素。W与X可生成一种红棕色有刺激性气味的气体;Y 的周期数是族序数的3倍;Z原子最外层的电子数与W的电子总数相同。下列叙述正确的是
A. X与其他三种元素均可形成两种或两种以上的二元化合物
B. Y与其他三种元素分别形成的化合物中只含有离子键
C. 四种元素的简单离子具有相同的电子层结构
D. W的氧化物对应的水化物均为强酸
【答案】A
5. N A代表阿伏加德罗常数的值。下列说法正确的是
A. 常温常压下,124 g P4中所含P—P键数目为4N A
B. 100 mL 1mol·L?1FeCl3溶液中所含Fe3+的数目为0.1N A
C. 标准状况下,11.2 L甲烷和乙烯混合物中含氢原子数目为2N A
D. 密闭容器中,2 mol SO2和1 mol O2催化反应后分子总数为2N A
【答案】C
6. 我国科学家研发了一种室温下“可呼吸”的Na—CO2二次电池。将NaClO4溶于有机溶剂作为电解液,钠和负载碳纳米管的镍网分别作为电极材料,电池的总反应为:3CO2+4Na2Na2CO3+C。下列说法错误的是
A. 放电时,ClO4-向负极移动
B. 充电时释放CO2,放电时吸收CO2
C. 放电时,正极反应为:3CO2+4e?=2CO32-+C
D. 充电时,正极反应为:Na++e?=Na
【答案】D
7. 下列实验过程可以达到实验目的的是
编号实验目的实验过程
A
配制0.4000 mol·L?1
的NaOH溶液称取4.0 g固体NaOH于烧杯中,加入少量蒸馏水溶解,转移至250 mL容量瓶中定容
B 探究维生素C的还原性
向盛有2 mL黄色氯化铁溶液的试管中滴加浓的维
生素C溶液,观察颜色变化
C 制取并纯化氢气
向稀盐酸中加入锌粒,将生成的气体依次通过NaOH
溶液、浓硫酸和KMnO4溶液
D
探究浓度对反应速率
的影响向2支盛有5 mL不同浓度NaHSO3溶液的试管中同时加入2 mL 5%H2O2溶液,观察实验现象
A. A
B. B
C. C
D. D
【答案】B
二、非选择题:共58分。第8~10题为必考题,每个试题考生都必须作答。第11、12题为选考题,考生根据要求作答。
(一)必考题(共43分)
8. 我国是世界上最早制得和使用金属锌的国家,一种以闪锌矿(ZnS,含有SiO2和少量FeS、CdS、PbS杂质)为原料制备金属锌的流程如图所示:
相关金属离子[c0(M n+)=0.1 mol·L-1]形成氢氧化物沉淀的pH范围如下:
金属离子Fe3+Fe2+Zn2+Cd2+
开始沉淀的pH 1.5 6.3 6.2 7.4
沉淀完全的pH 2.8 8.3 8.2 9.4
回答下列问题:
(1)焙烧过程中主要反应的化学方程式为_______________________。
(2)滤渣1的主要成分除SiO2外还有___________;氧化除杂工序中ZnO的作用是____________,若不通入氧气,其后果是________________。
(3)溶液中的Cd2+可用锌粉除去,还原除杂工序中反应的离子方程式为_________________。
(4)电解硫酸锌溶液制备单质锌时,阴极的电极反应式为______________;沉积锌后的电解液可返回_______工序继续使用。
【答案】 (1). ZnS+O2ZnO+SO2 (2). PbSO4 (3). 调节溶液的pH (4). 无法除去杂质Fe2+ (5). Zn+Cd2+Zn2++Cd (6). Zn2++2e-Zn (7). 溶浸
9. CH4-CO2催化重整不仅可以得到合成气(CO和H2),还对温室气体的减排具有重要意义。回答下列问题:(1)CH4-CO2催化重整反应为:CH4(g)+CO2(g)=2CO(g)+2H2(g)。
已知:C(s)+2H2(g)=CH4(g) ΔH=-75 kJ·mol?1
C(s)+O2(g)=CO2(g) ΔH=-394 kJ·mol?1
C(s)+1/2O2(g)=CO(g) ΔH=-111 kJ·mol?1
该催化重整反应的ΔH==______ kJ·mol?1。有利于提高CH4平衡转化率的条件是____(填标号)。
A.高温低压B.低温高压C.高温高压D.低温低压
某温度下,在体积为2 L的容器中加入2 mol CH4、1 mol CO2以及催化剂进行重整反应,达到平衡时CO2的转化率是50%,其平衡常数为_______mol2·L?2。
(2)反应中催化剂活性会因积碳反应而降低,同时存在的消碳反应则使积碳量减少。
相关数据如下表:
积碳反应
CH4(g)=C(s)+2H2(g) 消碳反应
CO2(g)+C(s)=2CO(g)
ΔH/(kJ·mol?1) 75 172
活化能/ (kJ·mol?1) 催化剂X 33 91 催化剂Y 43 72
①由上表判断,催化剂X____Y(填“优于”或“劣于”),理由是_________________。在反应进料气组成、压强及反应时间相同的情况下,某催化剂表面的积碳量随温度的变化关系如图所示。升高温度时,下列关于积碳反应、消碳反应的平衡常数(K)和速率(v)的叙述正确的是________填标号)。
A.K积、K消均增加B.v积减小,v消增加
C.K积减小,K消增加D.v消增加的倍数比v积增加的倍数大
②在一定温度下,测得某催化剂上沉积碳的生成速率方程为v=k·p(CH4)·[p(CO2)]-0.5(k为速率常数)。在p(CH4)一定时,不同p(CO2)下积碳量随时间的变化趋势如图所示,则p a(CO2)、p b(CO2)、p c(CO2)从大到小的顺序为________________。
【答案】 (1). 247 (2). A (3). (4). 劣于 (5). 相对于催化剂X,催化剂Y积碳反应的活化能大,积碳反应的速率小;而消碳反应活化能相对小,消碳反应速率大 (6). AD (7). p c(CO2)、p b(CO2)、p a(CO2)
10. K3[Fe(C2O4)3]·3H2O(三草酸合铁酸钾)为亮绿色晶体,可用于晒制蓝图。回答下列问题:
(1)晒制蓝图时,用K3[Fe(C2O4)3]·3H2O作感光剂,以K3[Fe(CN)6]溶液为显色剂。其光解反应的化学方程式为:2K3[Fe(C2O4)3]2FeC2O4+3K2C2O4+2CO2↑;显色反应的化学方程式为______________。
(2)某小组为探究三草酸合铁酸钾的热分解产物,按下图所示装置进行实验。
①通入氮气的目的是________________________________________。
②实验中观察到装置B、F中澄清石灰水均变浑浊,装置E中固体变为红色,由此判断热分解产物中一定含有___________、___________。
③为防止倒吸,停止实验时应进行的操作是_____________________________。
④样品完全分解后,装置A中的残留物含有FeO和Fe2O3,检验Fe2O3存在的方法是:________________。(3)测定三草酸合铁酸钾中铁的含量。
①称量m g样品于锥形瓶中,溶解后加稀H2SO4酸化,用c mol·L-1 KMnO4溶液滴定至终点。滴定终点的现象是___________________________。
②向上述溶液中加入过量锌粉至反应完全后,过滤、洗涤,将滤液及洗涤液全部收集到锥形瓶中。加稀H2SO4酸化,用c mol·L-1 KMnO4溶液滴定至终点,消耗KMnO4溶液V mL。该晶体中铁的质量分数的表达式为
________________________________。
【答案】 (1). 3FeC2O4+2K3[Fe(CN)6]Fe3[Fe(CN)6]2+3K2C2O4 (2). 隔绝空气、使反应产生的气体全部进入后续装置
(3). CO2 (4). CO (5). 先熄灭装置A、E的酒精灯,冷却后停止通入氮气 (6). 取少许固体粉末于试管中,加稀硫酸
溶解,滴入1~2滴KSCN溶液,溶液变红色,证明含有Fe2O3 (7). 粉红色出现 (8).
(二)选考题:共15分。请考生从2题中任选一题作答。如果多做,则按所做的第一题计分。
11. 硫及其化合物有许多用途,相关物质的物理常数如下表所示:
H2S S8FeS2SO2SO3H 2SO4
熔点/℃?85.5 115.2
>600(分解)
?75.5 16.8 10.3
沸点/℃?60.3 444.6 ?10.0 45.0 337.0
回答下列问题:
(1)基态Fe原子价层电子的电子排布图(轨道表达式)为__________,基态S原子电子占据最高能级的电子云轮廓图为_________形。
(2)根据价层电子对互斥理论,H2S、SO2、SO3的气态分子中,中心原子价层电子对数不同于其他分子的是_________。
(3)图(a)为S8的结构,其熔点和沸点要比二氧化硫的熔点和沸点高很多,主要原因为__________。
(4)气态三氧化硫以单分子形式存在,其分子的立体构型为_____形,其中共价键的类型有______种;固体三氧化硫中存在如图(b)所示的三聚分子,该分子中S原子的杂化轨道类型为________。
(5)FeS2晶体的晶胞如图(c)所示。晶胞边长为a nm、FeS2相对式量为M,阿伏加德罗常数的值为N A,其晶体密度的计算表达式为___________g·cm?3;晶胞中Fe2+位于所形成的正八面体的体心,该正八面体的边长为______nm。
【答案】 (1). (2). 哑铃(纺锤) (3). H2S (4). S8相对分子质量大,分子间范德华力强 (5). 平面三角 (6). 2 (7). sp3 (8). (9).
12. 以葡萄糖为原料制得的山梨醇(A)和异山梨醇(B)都是重要的生物质转化平台化合物。E是一种治疗心绞痛的药物,由葡萄糖为原料合成E的过程如下:
回答下列问题:
(1)葡萄糖的分子式为__________。
(2)A中含有的官能团的名称为__________。
(3)由B到C的反应类型为__________。
(4)C的结构简式为__________。
(5)由D到E的反应方程式为______________。
(6)F是B的同分异构体,7.30 g的F与足量饱和碳酸氢钠反应可释放出2.24 L二氧化碳(标准状况),F 的可能结构共有________种(不考虑立体异构),其中核磁共振氢谱为三组峰,峰面积比为3∶1∶1的结构简式为_________。
【答案】 (1). C6H12O6 (2). 羟基 (3). 取代反应 (4). (5).
(6). 9 (7).
近五年高考真题化学大题
近五年高考真题化学大题 (2013年全国卷1,13分)醇脱水是合成烯烃常用的方法。实验室合成环己烯的反应和实验装置如下: 相对分子质量密度/(g·cm-3)沸点/(0C)溶解性 环己醇1000.9618161微溶于水 环己烯820.810283难溶于水 在a中加入20 g环己醇和2小片碎瓷片,冷却搅动下慢慢加入1 mL浓硫酸。b中通入冷却水后,开 始缓慢加热a,控制馏出物的温度不超过900C。 分离提纯:反应粗产物倒入分液漏斗中分别用少量5%碳酸钠溶液和水洗涤,分离后加入无水氯化钼颗粒,静置一段时间后弃去氯化钙。最终通过蒸馏得到纯净环己烯10g。 回答下列问题: (1)装置b的名称是。 (2)加入碎瓷片的作用是;如果加热一段时间后发现忘记加瓷片,应该采取的正确操作是。 A.立即补加 B.冷却后补加 C.不需补加 D.重新配料 (3)本实验中最容易产生的副产物的结构简式为。 (4)分液漏斗在使用前须清洗干净并;在本实验分离过程,产物应该从分液漏斗的(填“上口倒出”或“下口放出”)。 (5)分离提纯过程中加入无水氯化钙的目的是。 (6)在环己烯粗产物蒸馏过程中,不可能用到的仪器有(填正确答案标号) A.圆底烧瓶 B.温度计 C.吸滤瓶 D.球形冷凝管 E.接收器 (7)本实验所得到的环己烯产率是(填正确答案标号) A.41% B.50% C.61% D.70% 答案:(1)直形冷凝管(2)防液体暴沸;B(3)(4)检漏;上品倒出。 (5)干燥(或除不除醇)(6)CD(7)C (2014年全国卷1,13分)乙酸异戊酯是组成蜜蜂信息素的成分之一,具有香蕉的香味。实验室制备乙酸 异戊酯的反应、 装置示意图和有关数据如下:
2018年高考化学全国II卷解析版
2017年普通高等学校招生全国统一考试 化学试题(全国II) 7.下列说法错误得就是 A.糖类化合物也可称为碳水化合物 B.维生素D可促进人体对钙得吸收 C.蛋白质就是仅由碳、氢、氧元素组成得物质 D.硒就是人体必需得微量元素,但不宜摄入过多 【解析】 A、糖类化合物也可称为碳水化合物,就是沿用下来得叫法,故A正确; B、维生素D可促进人体对钙得吸收,故B正确; C、蛋白质含有C、H、O、N、S等元素,故C错误; D、硒就是人体必需得微量元素,但不宜摄入过多,摄入过多可能会导致脱发等,故D正确; 【答案】C 8.阿伏加德罗常数得值为。下列说法正确得就是 A.1 L 0、1 mol·NH4Cl溶液中, 得数量为0、1 B.2、4 g Mg与H2SO4完全反应,转移得电子数为0、1 C.标准状况下,2、24 L N2与O2得混合气体中分子数为0、2 D.0、1 mol H2与0、1 mol I2于密闭容器中充分反应后,其分子总数为0、2 【解析】 A、NH4+能够发生水解,故NH4+得数量小于0、1N A,故A错误; B、 2、4 g Mg与H2SO4完全反应,转移得电子数为0、2N A,故B错误; C、标准状况下,2、24LN2与O2得混合气体得物质得量为0、1mol,故混合气体得分子数为0、1N A; D、 H2 + I22HI,反应前后气体分子数不变,故其分子总数为0、2N A,故D正确; 【答案】D 9.a、b、c、d为原子序数依次增大得短周期主族元素,a原子核外电子总数与b原子次外层得电子数相同;c所在周期数与族数相同;d与a同族。下列叙述正确得就是 A.原子半径:d>c>b>a B.4种元素中b得金属性最强 C.c得氧化物得水化物就是强碱 D.d单质得氧化性比a单质得氧化性强 【解析】 a、b、c、d为短周期主族元素,且a原子核外电子总数与b原子次外层得电子数相同,故a为O,d与a 同族,故d为S,c所在周期数与族数相同,故c为Al,则b为Na或Mg; A、原子半径b>c>d>a,故A错误; B、4种元素种b得失电子能力最强,故其金属性最强,故B正确; C、c得氧化物得水化物就是氢氧化铝,为两性氢氧化物,故C错误; D、O2得氧化性强于S,故D错误; 【答案】B 10.下列由实验得出得结论正确得就是
2019年高考理综化学部分-全国卷I
2019年普通高等学校招生全国统一考试(全国卷I) 理科综合【化学部分】 可能用到的相对原子质量: H 1 Li 7 C 12 N 14 O 16 Na 23 S 32 Cl 35.5 Ar 40 Fe 56 I 127 一、选择题(共7小题,每小题6分,共42分,每题只有一个选项符合题意) 7.陶瓷是火与土的结晶,是中华文明的象征之一,其形成、性质与化学有着密切的关系。下列说法错误的是 A.“雨过天晴云破处”所描述的瓷器青色,来自氧化铁 B.闻名世界的秦兵马俑是陶制品,由黏土经高温烧结而成 C.陶瓷是应用较早的人造材料,主要化学成分是硅酸盐 D.陶瓷化学性质稳定,具有耐酸碱侵蚀、抗氧化等优点 8.关于化合物2?苯基丙烯(右图),下列说法正确的是 A.不能使稀高锰酸钾溶液褪色 B.可以发生加成聚合反应 C.分子中所有原子共平面 D.易溶于水及甲苯 9.实验室制备溴苯的反应装置如下图所示,关于实验操作或叙述错误的是 A.向圆底烧瓶中滴加苯和溴的混合液前需先打开K B.实验中装置b中的液体逐渐变为浅红色 C.装置c中的碳酸钠溶液的作用是吸收溴化氢 D.反应后的混合液经稀碱溶液洗涤、结晶,得到溴苯 10.固体界面上强酸的吸附和离解是多相化学在环境、催化、材料科学等领域研究的重要课题。下图为少量HCl气体分子在253 K冰表面吸附和溶解过程的示意图。下列叙述错误的是
A.冰表面第一层中,HCl以分子形式存在 B.冰表面第二层中,H+浓度为5×10?3 mol·L?1(设冰的密度为0.9 g·cm?3) C.冰表面第三层中,冰的氢键网格结构保持不变 D.冰表面各层之间,均存在可逆反应HCl H++Cl? 11.NaOH溶液滴定邻苯二甲酸氢钾(邻苯二甲酸氢钾H2A的K a1=1.1×10?3 ,K a2=3.9×10?6)溶液,混合溶液的相对导电能力变化曲线如图所示,其中b点为反应终点。下列叙述错误的是 A.混合溶液的导电能力与离子浓度和种类有关 B.Na+与A2?的导电能力之和大于HA?的 C.b点的混合溶液pH=7 D.c点的混合溶液中,c(Na+)>c(K+)>c(OH?) 12.利用生物燃料电池原理研究室温下氨的合成,电池工作时MV2+/MV+在电极与酶之间传递电子,示意图如下所示。下列说法错误的是 A.相比现有工业合成氨,该方法条件温和,同时还可提供电能 B.阴极区,在氢化酶作用下发生反应H 2+2MV2+2H++2MV+ C.正极区,固氮酶为催化剂,N2发生还原反应生成NH3 D.电池工作时质子通过交换膜由负极区向正极区移动 13.科学家合成出了一种新化合物(如图所示),其中W、X、Y、Z为同一短周期元素,Z核外最外层电子数是X核外电子数的一半。下列叙述正确的是 A.WZ的水溶液呈碱性 B.元素非金属性的顺序为X>Y>Z C.Y的最高价氧化物的水化物是中强酸 D.该新化合物中Y不满足8电子稳定结构 二、非选择题 (一)必考题(本题包括3小题,共43分) 26.(14分)硼酸(H3BO3)是一种重要的化工原料,广泛应用于玻璃、医药、肥料等工艺。一种以硼镁矿(含Mg2B2O5·H2O、SiO2及少量Fe2O3、Al2O3)为原料生产硼酸及轻质氧化镁的工艺流程如下:
全国卷高考化学选择题汇编
1.[化学常识]下列叙述正确的是A.锥形瓶可用作加热的反应器 B.室温下,不能将浓硫酸盛放在铝桶中 C.可以使用碱式滴定管量取高锰酸钾溶液 D.用蒸馏水润湿的试纸测溶液的pH,一定会使结果偏低 2.化学与生活密切相关,下列有关说法错误的是 A.用灼烧的方法可以区分蚕丝和人造纤维 B.食用油反复加热会产生稠环芳香烃等有害物质 C.加热能杀死流感病毒是因为蛋白质受热变性 D.医用消毒酒精中乙醇的浓度为85% 3.下列关于有机化合物的说法正确的是 A.2-甲基丁烷也称为异丁烷 B.由乙烯生成乙醇属于加成反应 C.C4H9Cl有3种同分异构体 D.油脂在酸性条件下水解叫做皂化反应 4.下列叙述错误的是 A.SO使溴水褪色与乙烯使KMnO溶液褪色的原理相同 B.制备乙酸乙酯时可用热的NaOH溶液收集产物以除去其中的乙酸 C.用饱和食盐水替代水跟电石反应,可以减缓乙炔的产生速率 D.用AgNO溶液可以鉴别KC1和KI 5.下列叙述中,错误 ..的是 A.苯与浓硝酸、浓硫酸共热并保持55~60℃反应生成硝基苯 B.苯乙烯在合适条件下催化加氢可生成乙基环己烷 C.乙烯和溴的四氯化碳溶液反应生成1,2-二溴乙烷
D.甲苯与氯气在光照下反应主要生成2,4-二氯甲苯 6、[离子方程]能正确表示下列反应的离子方程式是 A.用过量氨水吸收工业尾气中的SO2:2NH3·H20+SO22NH4++SO32-+H2O B.氯化钠与浓硫酸混合加热:H2SO4+2Cl-SO2↑+Cl2↑+H2O C.磁性氧化铁溶于稀硝酸:3Fe2++4H++NO3-3Fe3++NO↑+3H2O D.明矾溶液中滴入Ba(OH)2溶液使SO42-恰好完全沉淀: 2Ba2++3OH-+Al3++2SO42-2BaSO4↓+Al(OH)3↓ 7.下列离子方程式错误的是 A.向Ba(OH)2溶液中滴加稀硫酸:Ba2++2OH-+2H++SO42—=BaSO4↓+2H2O B.酸性介质中KMnO4氧化H2O2:2MnO4-+5H2O2+6H+=2Mn2++5O2↑+8H2O C.等物质的量的MgCl2、Ba(OH)2和HC1溶液混合:Mg2++2OH-=Mg(OH)2↓ D.铅酸蓄电池充电时的正极反应:PbSO4+2H2O-2e-=PbO2+4H++SO42— 8.[阿伏伽德罗常数]NA表示阿伏加德罗常数,下列叙述正确的是A.lmolFeI与足量氯气反应时转移的电子数为2N B.2L0.5mol?L硫酸钾溶液中阴离子所带电荷数为N C.1molNaO固体中含离子总数为4N A D.丙烯和环丙烷组成的42g混合气体中氢原子的个数为6N 9.设N A为阿伏加德罗常数值。下列有关叙述正确的是 A.14 g乙烯和丙烯混合气体中的氢原子数为2N A B.1molN2与4molH2反应生成的NH3分子数为2N A C.1molFe溶于过量硝酸,电子转移数为2N A D.标准状况下,2.24LCCl4含有的共价键数为0.4N A 10.设N A为阿伏加德罗常数,下列叙述中正确的是 A.0.1mo l·L-1的NH4NO3溶液中含有的氮原子数为0.2N A B.1mol氯气分别与足量铁和铝完全反应时转移的电子数均为3N A
高考化学历年(2018)真题及答案
2018年真题 (全国1卷)7.硫酸亚铁锂(LiFePO4)电池是新能源汽车的动力电池之一,采用湿法冶金工艺回收废旧硫酸亚铁锂电池正极片中的金属,其流程如下: 下列叙述错误的是() A. 合理处理废旧电池有利于保护环境和资源再利用 B. 从“正极片”中可回收的金属元素有AL、Fe、Li C. “沉淀”反应的金属离子为Fe3+ D. 上述流程中可用硫酸钠代替碳酸钠 8.下列说法错误的是() A. 蔗糖,果糖和麦芽糖均为双糖 B. 酶是一类具有高选择催化性能的蛋白质 C. 植物油含不饱和脂肪酸酯,能使Br/CCl4色 D. 淀粉和纤维素水解的最终产物均为葡萄糖 9.在生成和纯化乙酸乙酯的实验过程中,下列操作未涉及的是() A. B. C. D. 10. 11. 12. 主族元素W、X、Y、Z的原子序数依次增加,且均不大于20,W、X、Z最外层电子数之和为10:W与Z形成的化合物可与浓硫酸反应,其生成物可腐蚀玻璃。下列说法正确的是() A. 常温常压下X的单质为气态 B. Z的氢化物为离子化合物 C. Y和Z形成的化合物的水溶液呈碱性 D. W与Y具有相同的最高化合价 13.
26.(14分) (1)实验中所用蒸馏水均需经煮沸后迅速冷却,目的是_________,仪器a的名称是 _______。 (2)将过量锌粒和氯化铬固体置于c中,加入少量蒸馏水,按图连接好装置,打开 ,关闭K3。①c中溶液由绿色逐渐变为亮蓝色,该反应的离子方程式为____。 ②同时c中有气体产生,该气体的作用是____。 (3)打开K3,关闭K1和K2。c中亮蓝色溶液流入d,其原因是____;d中析出砖红色沉淀,为使沉淀充分析出并分离,需采用的操作是____、_________、洗涤、干燥。 (4)指出装置d可能存在的缺点____。 27.(14分)
高考化学真题全国卷Ⅲ
2017年普通高等学校招生全国统一考试(全国Ⅲ卷) 理科综合能力测试(化学部分)可能用到的相对原子质量:H-1 Li-7 C-12 N-14 O-16 S-32 K-39 Cr-52 Mn-55 Fe-56 第Ⅰ卷 7.化学与生活密切相关。下列说法错误的是() A.是指粒径不大于μm的可吸入悬浮颗粒物 B.绿色化学要求从源头上消除或减少生产活动对环境的污染 C.燃煤中加入CaO可以减少酸雨的形成及温室气体的排放 D.天然气和液化石油气是我国目前推广使用的清洁燃料 8.下列说法正确的是() A.植物油氢化过程中发生了加成反应 B.淀粉和纤维素互为同分异构体 C.环己烷与苯可用酸性KMnO4溶液鉴别 D.水可以用来分离溴苯和苯的混合物 10.N A为阿伏加德罗常数的值。下列说法正确的是() A.mol 的11B中,含有个中子 B.pH=1的H3PO4溶液中,含有个H+ C.L(标准状况)苯在O2中完全燃烧,得到个CO2分子 D.密闭容器中1 mol PCl3与1 mol Cl2反应制备PCl5(g),增加2N A个P-Cl 键 11.全固态锂硫电池能量密度高、成本低,其工作原理如图所示,其中电极a常用掺有石墨烯的S8材料,电池反应为:16Li+x S8 = 8Li2S x(2≤x≤8)。下列说法错误的是()
A.电池工作时,正极可发生反应:2Li2S6+2Li++2e- = 3Li2S4 B.电池工作时,外电路中流过mol电子,负极材料减重g C.石墨烯的作用主要是提高电极a的导电性 D.电池充电时间越长,电池中的Li2S2量越多 12.短周期元素W、X、Y和Z在周期表中的相对位置如表所示,这四种元素原子的最外电子数纸盒为 W X Y Z A.氢化物沸点:Y>W C.化合物熔点:Y2X3 2020年全国I高考化学试题点评 点评一: 广西南宁三中化学老师蓝宇认为,今年高考理综化学试题,大部分连续了历年的特点,总分依旧占108 分,题量没有多大变化,题目难度比去年略低,深浅层次明显。其中与去年不太一样的是,运算量有所增加,而且有关氧化还原的运算题替换成了电化学原理及运算。 主观题题号也由原先的26?29题改为27?30题。 今年高考化学试题给人的整体感受是坚持学科内综合为主的原那么,注重考查化学学科主干知识、考查学科内各知识板块的综合应用能力、考查内容源于课本但又高于课本。 蓝宇认为,试题中能力的考查是以知识为载体,通过灵活的解决咨询题的方法来实现。假如平常学生不注重基础、训练表达能力,就觉得不易下手。他从每个题型分析了今年化学考试的特点。 今年的化学题型包括选择题、实验题、无机和有机推断题、电化学原理及运算。选择题的命题是以考查化学差不多概念、差不多理论为主。强调化学概念、理论、元素化合物、有机基础等知识点的综合,要紧考察传统题型,这些题型差不多上烂熟于心的,难度并不大。然而8道选择题里有第7题、第9题、第11题和第13题4道题目涉及运算。运算能力不是专门突出的同学在选择题上会用比较多时刻。 27 题实验题要紧以考查综合实验设计能力为主。要求把握常见物质检验方法,具有规 范的实验操作能力、能依照实验目的进行实验设计。此题比较新颖,有一定的开放性。不仅需要自己设计流程、选择装置,还要选药品,而且还需要大量的文字描述。 28 题电化学原理咨询题一直是化学中的难点,但近几年涉及到的知识点主观题考得少,而今年以大题的形式显现,难度尽管不大,但专门多学生把握得不是专门扎实,会在运算和文字表述上失分。它要紧考查了电解原理及有关运算,能够较好地区分学生的水平,涉及的知识点有正负极判定、电极反应书写、电极产物运算等。 29 题无机推断题,要紧以结合元素周期表并以元素化合物知识为载体,考查学生多方面的综合能力。此题涉及三大强酸、晶体结构、熔沸点及生疏反应的书写等知识点的考查,有专门好的选拔功能。 30 题有机推题,以框图的形式出现,考查有机化学基础的综合能力为主。命题时适当 给出新的信息即一个新的反应条件。以考查学生应用信息、解决咨询题的能力。设咨询时,将结合运算等内容,考查有机分子式的推断,化学方程式、结构简式的书写以及有机反应的差不多类型,同分异构体书写等,此题对学生的推理能力要求较高,第⑵咨询给B和C命 名时专门容易失分。 总体上分析,蓝宇老师认为今年高考化学科试题稳中有变,变的是更加突出对学科能力的考查,加大了知识的覆盖面,加大了试题的思维容量,重点考查学生的思维过程以及解决实际咨询题的能力。 考生印象:绝大部分的考生讲,关于像27 题如此的题型来讲,他们并可不能感到生疏,但大量文字的描述让他们觉得无从下手,看起来如何讲都沾边,但又如何讲都讲不清晰。且,在答题时,每道题目都考查了好几个知识点,有时想起了那个点,就不记得了那个点,做起来不如何顺手。 2016年高考化学试题全国II卷(含答案) word版 7.下列有关燃料的说法错误的是 A.燃料燃烧产物CO2是温室气体之一 B.化石燃料完全燃烧不会造成大气污染 C.以液化石油气代替燃油可减少大气污染 D.燃料不完全燃烧排放的CO是大气污染物之一 【答案】B 8.下列各组中的物质均能发生加成反应的是 A.乙烯和乙醇B.苯和氯乙烯C.乙酸和溴乙烷D.丙烯和丙烷 【答案】B 9.a、b、c、d为短周期元素,a的原子中只有1个电子,b2-和C+离子的电子层结构相同,d与b同族。下列叙述错误的是 A.a与其他三种元素形成的二元化合物中其化合价均为+1 B.b与其他三种元素均可形成至少两种二元化合物 C.c的原子半径是这些元素中最大的 D.d和a形成的化合物的溶液呈弱酸性 【答案】A 10.分子式为C4H8Cl2的有机物共有(不含立体异构) A.7种B.8种C.9种D.10种 【答案】C 11.Mg-AgCl电池是一种以海水为电解质溶液的水激活电池。下列叙述错误的是 A.负极反应式为Mg-2e-=Mg2+ B.正极反应式为Ag++e-=Ag C.电池放电时Cl-由正极向负极迁移 D.负极会发生副反应Mg+2H2O=Mg(OH)2+H2↑ 【答案】B 12.某白色粉末由两种物质组成,为鉴别其成分进行如下实验: ①取少量样品加入足量水仍有部分固体未溶解;再加入足量稀盐酸,有气泡产生,固体全部溶解; ②取少量样品加入足量稀硫酸有气泡产生,振荡后仍有固体存在。 该白色粉末可能为 A.NaHCO3、Al(OH)3B.AgCl、NaHCO3C.Na2SO3、BaCO3D.Na2CO3、CuSO4 【答案】C 13.下列实验操作能达到实验目的的是 【答案】D 26.联氨(又称联肼,N2H4,无色液体)是一种应用广泛的化工原料,可用作火箭燃料,回答下列问题: (1)联氨分子的电子式为_________,其中氮的化合价为______。 (2)实验室可用次氯酸钠溶液与氨反应制备联氨,反应的化学方程式为_____ ______。(3)①2O2(g)+N2(g)=N2O4(l) △H1 ②N2(g)+2H2(g)=N2H4(l) △H2 ③O2(g)+2H2(g)=2H2O(g) △H3 ④2 N2H4(l) + N2O4(l)= 3N2(g)+ 4H2O(g) △H4=-1048.9kJ/mol 上述反应热效应之间的关系式为△H4=________________,联氨和N2O4可作为火箭推进剂的主要原因为_________________________________________________。 (4)联氨为二元弱碱,在水中的电离方程式与氨相似,联氨第一步电离反应的平衡常数值为_______(已知:N2H4+H+N2H5+的K=8.7×107;K W=1.0×10-14)。联氨与硫酸形成的酸式盐的化学式为。 (5)联氨是一种常用的还原剂。向装有少量AgBr的试管中加入联氨溶液,观察到的现象是。联氨可用于处理高压锅炉水中的氧,防止锅炉被腐蚀。理论上1kg的联氨可除去水中溶解的O2kg;与使用Na2SO3处理水中溶解的O2相比,联氨的优点是。【答案】26、(1);-2 (2)NaClO+2NH3=N2H4+NaCl+H2O (3)△H4=2△H3-2△H2-△H1;反应放热量大、产生大量气体 2018年全国统一高考化学试卷(新课标Ⅰ) 一、选择题(共7小题,每小题6分,满分42分) 1.(6分)磷酸亚铁锂(LiFePO4)电池是新能源汽车的动力电池之一,采用湿法冶金工艺回收废旧磷酸亚铁锂电池正极片中的金属,其流程如下: 下列叙述错误的是() A.合理处理废旧电池有利于保护环境和资源再利用 B.从“正极片”中可回收的金属元素有Al、Fe、Li C.“沉淀”反应的金属离子为Fe3+ D.上述流程中可用硫酸钠代替碳酸钠2.(6分)下列说法错误的是() A.蔗糖、果糖和麦芽糖均为双糖 B.酶是一类具有高选择催化性能的蛋白质C.植物油含不饱和脂肪酸酯,能使Br2/CCl4褪色 D.淀粉和纤维素水解的最终产物均为葡萄糖 3.(6分)在生成和纯化乙酸乙酯的实验过程中,下列操作未涉及的是() A.B. C.D. 4.(6分)N A是阿伏加德罗常数的值,下列说法正确的是() A.16.25gFeCl3,水解形成的Fe(OH)3为胶体粒子数为0.1N A B.22.4L(标准状况)氩气含有的质子数为18N A C.92.0g甘油(丙三醇)中含有羟基数为1.0N A D.1.0molCH4与Cl2在光照下生成CH3Cl的分子数为1.0N A 5.(6分)环之间共用一个碳原子的化合物称为螺环化合物,螺(2,2)戊烷()是最单的一种,下列关于该化合物的说法错误的是() A.与环戊烯互为同分异构体 B.二氯化物超过两种 C.所有碳原子均处同一平面 D.生成1molC5H12,至少需要2molH2 6.(6分)主族元素W、X、Y、Z的原子序数依次增加,且均不大于20.W、X、Z最外层电子数之和为10;W与Y同族;W与Z形成的化台物可与浓硫酸反应,其生成物可腐蚀玻璃。下列说法正确的是() A.常温常压下X的单质为气态 B.Z的氢化物为离子化合物 C.Y和Z形成的化合物的水溶液呈碱性 D.W与Y具有相同的最高化合价 7.(6分)最近我国科学家设计了一种CO2+H2S协同转化装置,实现对天然气中CO2和H2S的高效去除。示意图如右所示,其中电极分别为ZnO@石墨烯(石墨烯包裹的ZnO)和石墨烯,石墨烯电极区发生反应为: ①EDTA﹣Fe2+﹣e﹣=EDTA﹣Fe3+ ②2EDTA﹣Fe3++H2S=2H++S+2EDTA﹣Fe2+该装置工作时,下列叙述错误的是() A.阴极的电极反应:CO2+2H++2e﹣═CO+H2O B.协同转化总反应:CO2+H2S═CO+H2O+S C.石墨烯上的电势比ZnO@石墨烯上的低 D.若采用Fe3+/Fe2+取代EDTA﹣Fe3+/EDTA﹣Fe2+,溶液需为酸性 二、解答题(共3小题,满分43分) 8.(14分)醋酸亚铬[(CH3COO)2Cr?2H2O]为砖红色晶体,难溶于冷水,易溶于酸,在气体分析中用作氧气吸收剂。一般制备方法是先在封闭体系中利用金属锌作还原剂,将三价铬还原为二价络;二价铬再与醋酸钠溶液作用即可制得醋酸亚铬。实验装置如图所示。回答下列问题: (1)实验中所用蒸馏水均需经煮沸后迅速冷却,目的是仪器a的名称是。(2)将过量锌粒和氯化铬固体置于c中,加入少量蒸馏水,按图连接好装置。打开K1、K2,关闭K3。 ①c中溶液由绿色逐渐变为亮蓝色,该反应的离子方程式为 ②同时c中有气体产生,该气体的作用是 (3)打开K3,关闭K1和K2.c中亮蓝色溶液流入d,其原因 是;d中析出砖红色沉淀。为使沉淀充分析出并 分离,需采用的操作是、洗涤,干燥。 (4)指出装置d可能存在的缺点 2019 年高考试题—理综化学(山东卷)解析版 注意事项 :认真阅读理解,结合历年的真题,总结经验,查找不足!重在审题,多思考,多 理解! 无论是单选、多选还是论述题, 最重要的就是看清题意。 在论述题中, 问题大多具有委 婉性, 尤其是历年真题部分, 在给考生较大发挥空间的同时也大大增加了考试难度。 考生要 认真阅读题目中提供的有限材料, 明确考察要点, 最大限度的挖掘材料中的有效信息, 建议 考生答题时用笔将重点勾画出来, 方便反复细读。 只有经过仔细推敲, 揣摩命题老师的意图, 积极联想知识点,分析答题角度,才能够将考点锁定,明确题意。 7、以下与化学概念有关的说法正确的选项是 A 、化合反应均为氧化还原反应 B 、金属氧化物均为碱性氧化物 C 、催化剂能改变可逆反应达到平衡的时间 D 、石油是混合物,其分馏产品汽油为纯净物 【解析】此题考查化学基本概念。有单质参加的化合反应为氧化还原反应, A 项错误; Mn 2O 7 为酸性氧化物, Al O 为两性氧化物, B 项错误;催化剂能影响反应速率,改变可逆反应达到 2 3 平衡的时间, C 项正确;石油的分馏产物汽油为混合物, D 项错误。 答案: C 8、以下与含氯化合物有关的说法正确的选项是 A 、 HClO 是弱酸,所以 NaClO 是弱电解质 B 、向沸水中逐滴加入少量饱和 FeCl 3 溶液,可制得 Fe(OH)3 胶体 C 、 HCl 溶液和 NaCl 溶液均通过离子导电,所以 HCl 和 NaCl 均是离子化合物 D 、电解 NaCl 溶液得到 22.4LH 2 ( 标准状况 ) ,理论上需要转移 N 个电子 (N 表示阿伏加德 A A 罗常数 ) 【解析】 NaClO 属于盐, 为强电解质, A 项错误; 向沸水中滴加饱和 FeCl 3 制备 Fe(OH)3 胶体, B 项正确; HCl 属于共价化合物, C 项错误;根据电解 NaCl 溶液的阴极反应 :2H + +2e -2 =H ↑, 产生标准状况下 22.4LH 2,转移 2N A 个电子, D 项错误。 答案: B 9、以下关于原子结构、元素性质的说法正确的选项是 A 、非金属元素组成的化合物中只含共价键 B 、 IA 族金属元素是同周期中金属性最强的元素 C 、同种元素的原子均有相同的质子数和中子数 D 、Ⅶ A 族元素的阴离子还原性越强,其最高价氧化物对应水化物的酸性越强 【解析】 NH 4Cl 全部由非金属元素组成,但含有离子键和共价键, A 项错误;同周期元素从 左到右金属性逐渐减弱,各周期中Ⅰ A 族元素的金属性最强, B 项正确;同种元素的原子的 质子数相同,但中子数不同, C 项错误;Ⅶ族元素的阴离子还原性越强,那么元素的金属性 越弱,其最高价氧化物对应水化物的酸性越弱, D 项错误。 答案: B 10、以下与有机物的结构、性质有关的表达正确的选项是 A 、苯、油脂均不能使酸性 KMnO,溶液褪色 B 、甲烷和 Cl 2 的反应与乙烯和 Br 2 的反应属于同一类型的反应 C 、葡萄糖、果糖的分子式均为 C 6H 12O 6,二者互为同分异构休 D 、乙醇、乙酸均能与 Na 反应放出 H 2,二者分子中官能团相同 2018年高考理综试题(全国新课标卷)化学部分 1.(2018全国大纲卷)下列有关化学键的叙述,正确的是 A.离子化合物中一定含有离子键 B.单质分子均不存在化学键 C.含有极性键的分子一定是极性分子 D.含有共价键的化合物一定是共价化合物 2.(2018全国大纲卷)能正确表示下列反应的离子方程式是 A.硫酸铝溶液中加入过量氨水:Al3++3OH-= Al(OH)3↓ B.碳酸钠溶液中加入澄清石灰水:Ca(OH)2+CO32-= CaCO3↓+2OH- C.冷的氢氧化钠溶液中通入氯气:Cl2+2OH-= ClO-+Cl-+H2O D.稀硫酸中加入铁粉:2Fe+6H+= 2Fe3++3H2↑ 3.(2018全国大纲卷)合成氨所需的氢气可用煤和水作原料经过多步反应制得,其中的 一步反应为:CO(g)+H2O(g)CO2(g)+H2(g) △H < 0 反应到达平衡后,为提高CO的转化率,下列措施中正确的是 A.增加压强B.降低温度C.增大CO的浓度 D.更换催化剂 4.(2018全国大纲卷)反应A+B→C(△H<0)分两步进行:①A+B→X(△H>0),②X→C(△H<0)。下列示意图中,能正确表示总反应过程中能量变化的是 A B C D 5.(2018全国大纲卷)元素X形成的离子与钙离子的核外电子排布相同,且X的离子半径小于负二价硫离子的半径。X元素为 A.Al B.P C.Ar D.K 6.(2018全国大纲卷)①②③④四种金属片两两相连浸入稀硫酸中都可组成原电池,①②相连时,外电路电流从②流向①;①③相连时,③为正极;②④相连时,②上有气泡逸出;③④相连时,③的质量减少。据此判断这四种金属活动性由大到小的顺序是 A.①③②④ B.①③④② C.③④②① D.③①②④7.(2018全国大纲卷)在常压和500℃条件下,等物质的量的Ag2O、Fe(OH)3、NH4HCO3、NaHCO3完全分解,所得气体体积依次为V1、V2、V3、V4,体积大小顺序正确的是 A.V3>V2 >V4 >V1 B.V3>V4 >V2 >V1 C.V3>V2 >V1 >V4D.V2>V3 >V1 >V4 8.(2018全国大纲卷)橙花醇具有玫瑰及苹果香气,可作为香料,其结构简式如下: 下列关于橙花醇的叙述,错误的是 A.既能发生取代反应,也能发生加成反应 B.在浓硫酸催化下加热脱水,可以生成不止一种四烯烃 C.1mol橙花醇在氧气中充分燃烧,需消耗470. 4L氧气(标准状况) D.1mol橙花醇在室温下与溴的四氯化碳溶液反应,最多消耗 240g溴 2018年普通高等学校招生全国统一考试 理科综合能力测试 可能用到的相对原子质量:H 1 C 12 N 14 O 16 Na 23 Mg 24 Al 27 S 32 Cr 52 Zn 65 I 127 一、选择题:本题共13个小题,每小题6分,共78分。在每小题给出的四个选项中,只有一项是符合题目要求的。 7.化学与生活密切相关。下列说法错误的是 A.泡沫灭火器可用于一般的起火,也适用于电器起火 B.疫苗一般应冷藏存放,以避免蛋白质变性 C.家庭装修时用水性漆替代传统的油性漆,有利于健康及环境 D.电热水器用镁棒防止内胆腐蚀,原理是牺牲阳极的阴极保护法 8.下列叙述正确的是 A.24 g 镁与27 g铝中,含有相同的质子数 B.同等质量的氧气和臭氧中,电子数相同 C.1 mol重水与1 mol水中,中子数比为2∶1 D.1 mol乙烷和1 mol乙烯中,化学键数相同 9.苯乙烯是重要的化工原料。下列有关苯乙烯的说法错误的是 A.与液溴混合后加入铁粉可发生取代反应 B.能使酸性高锰酸钾溶液褪色 C.与氯化氢反应可以生成氯代苯乙烯 D.在催化剂存在下可以制得聚苯乙烯 10.下列实验操作不当的是 A.用稀硫酸和锌粒制取H2时,加几滴CuSO4溶液以加快反应速率 B.用标准HCl溶液滴定NaHCO3溶液来测定其浓度,选择酚酞为指示剂 C.用铂丝蘸取某碱金属的盐溶液灼烧,火焰呈黄色,证明其中含有Na+ D.常压蒸馏时,加入液体的体积不超过圆底烧瓶容积的三分之二 11.一种可充电锂-空气电池如图所示。当电池放电时,O2与Li+在多孔碳材料电极处生成Li2O2-x(x=0或1)。下列说法正确的是 A.放电时,多孔碳材料电极为负极 B.放电时,外电路电子由多孔碳材料电极流向锂电极 C.充电时,电解质溶液中Li+向多孔碳材料区迁移 D.充电时,电池总反应为Li2O2-x=2Li+(1-x/2)O2 12.用0.100 mol·L-1 AgNO3滴定50.0 mL 0.0500 mol·L-1 Cl-溶液的滴定曲线如图所示。下列有关描述错误的是 2015年普通高等学校招生全国统一考试(新课标Ⅰ) 理科综合能力测试(化学部分) 7.我国清代《本草纲目拾遗》中记叙无机药物335种,其中“强水”条目下写道:“性最烈,能蚀五金…… 其水甚强,五金八石皆能穿第,惟玻璃可盛。”这里的“强水”是指( ) A .氨水 B . 硝酸 C .醋 D .卤水 8.N A 为阿伏伽德罗常数的值。下列说法正确的是( ) A .18gD 2O 和18gH 2O 中含有的质子数均为10N A B .2L0.5mol/L 亚硫酸溶液中含有的H +种数为2N A C .过氧化钠与水反应时,生成0.1mol 氧气转移的电子数为0.2N A D .密闭容器中2molNO 与1molO 2充分反应,产物的分子数为2N A 9.乌洛托品在合成、医药、染料等工业中有广泛用途,其结构式如图所示。将甲醛水溶液 与氨水混合蒸发可制得乌洛托品。若原料完全反应生成乌洛托品,则甲醛与氨的物质的量之比为( ) A .1:1 B .2:3 C .3:2 D .2:1 10.下列实验中,对应的现象以及结论都正确且两者具有因果关系的是( ) 11.微生物电池是指在微生物的作用下将化学能转化为电能的装置,其工作原理如图所示。下列有关微生 物电池的说法错误的是( ) A .正极反应中有CO 2生成 B .微生物促进了反应中电子的转移 C .质子通过交换膜从负极区移向正极区 D .电池总反应为C 6H 12O 6+6O 2=6CO 2+6H 2O 12.W 、X 、Y 、Z 均为的短周期元素,原子序数依次增加,且原子核外L 电子层的电子数分别为0、5、8、 8,它们的最外层电子数之和为18。下列说法正确的是( ) N N N N 2017全国卷二理综--化学 一、选择题(每题6分,共42分) 7、下列说法错误的是() A. 糖类化合物也称碳水化合物 B. 维生素D可促进人体对钙的吸收 C. 蛋白质是仅由碳、氢、氧元素组成的物质 D. 硒是人体必须的微量元素,但不宜摄入过多 【考点】化学与生活中基本营养物质糖类、蛋白质、维生素、无机盐。 正确答案:C 解析: A选项:糖类通式:C n(H20)m又称碳水化合物,故A正确; B选项:维生素D是固醇类衍生物,属于脂溶性维生素,最重要的生理功能是促进钙的吸收与利用,故B正确; C选项蛋白质中主要元素为:C、H、O、N,还含P、S等,故C错误; D选项,硒是人体必须的微量元素(缺少硒会降低祛病能力),但硒有毒,不易摄入过多,故D正确。 8、阿伏伽德罗常数是N A,下列说法正确的是() A. 1L 0.1mol/L NH4Cl溶液中,NH4+的数目为0.1N A B. 2.4g Mg与H2SO4完全反应,转移电子数为0.1N A C. 标准状况下,2.24L N2和O2的混合气体中分子数为0.2N A D. 0.1mol H2和0.1mol I2于密闭容器中充分反应后,其分子总数为0.2N A 【考点】关于阿伏伽德罗常数N A的计算,涉及:盐类水解、氧化还原反应、可逆反应、混合气体计算。 正确答案:D 解析: A选项NH4+易水解,则1L 0.1mol/L NH4Cl溶液中,NH4+的数目小于0.1N A,故A错误; B选项:Mg与H2SO4反应:Mg – 2e- == Mg2+,1molMg完全反应转移电子2mol, 2.4g Mg 与H2SO4完全反应转移电子数为0.2N A,故B错误; C选项:标准状况下,2.24L N2和O2的混合气体物质的量为1mol,则分子数为N A,故C错误; 2009-2013年高考化学试题分类解析汇编:电化学基础 2009年高考化学试题 1.(09广东理科基础?25)钢铁生锈过程发生如下反应: ①2Fe +O 2+2H 2O =2Fe(OH)2; ②4Fe(OH)2+O 2+2H 2O =4Fe(OH)3; ③2Fe(OH)3=Fe 2O 3+3H 2O 。下列说法正确的是 A .反应①、②中电子转移数目相等 B .反应①中氧化剂是氧气和水 C .与铜质水龙头连接处的钢质水管不易发生腐蚀 D .钢铁在潮湿的空气中不能发生电化学腐蚀 2.(09安徽卷?12)Cu 2O 是一种半导体材料,基于绿色化学理念设计的制取。Cu 2O 的电解池示意图如下,点解总反应:2Cu +H 2O Cu 2O +H 2O ↑。下列说法正确的是 A .石墨电极上产生氢气 B .铜电极发生还原反应 C .铜电极接直流电源的负极 D .当有0.1mol 电子转移时,有0.1molCu 2O 生成。 2.(09江苏卷?12)以葡萄糖为燃料的微生物燃料电池结构示意图如图所示。关于该电池的叙述正确的是 A .该电池能够在高温下工作 B .电池的负极反应为: C 6H 12O 6+6H 2O -24e - =6CO 2↑+24H + C .放电过程中,+ H 从正极区向负极区迁移 D .在电池反应中,每消耗1mol 氧气,理论上能生成标准状况下CO 2气体22.4 6 L 3.(09浙江卷?12)市场上经常见到的标记为Li —ion 的电池称为“锂离子电池”。它的负极材料是金属锂和碳的复合材料(碳作为金属锂的载体),电解质为一种能传导Li + 的高分子材料。这种锂离子电池的电池反应为: Li +2Li 0.35NiO 2 2Li 0.85NiO 2 下列说法不正确的是 A .放电时,负极的电极反应式:Li ? e -=Li + B .充电时,Li 0.85NiO 2既发生氧化反应又发生还原反应 C .该电池不能用水溶液作为电解质 D .放电过程中Li + 向负极移动 4.(09广东理科基础?34)下列有关电池的说法不正确的是 A .手机上用的锂离子电池属于二次电池 B .铜锌原电池工作时,电子沿外电路从铜电极流向锌电极 C .甲醇燃料电池可把化学能转化为电能 D .锌锰干电池中,锌电极是负极 5.(09福建卷?11) 控制适合的条件,将反应2Fe 3+ +2I - 2Fe 2+ +I 2设计成如右图所示的原电池。下列判断不 正确的是 A .反应开始时,乙中石墨电极上发生氧化反应 B .反应开始时,甲中石墨电极上Fe 3+ 被还原 C .电流计读数为零时,反应达到化学平衡状态 D .电流计读数为零后,在甲中溶入FeCl 2固定,乙中石墨电极为负极 6.(09广东化学?10)出土的锡青铜(铜锡合金)文物常有Cu 2(OH)3Cl 覆盖在其表面。下列说法正确的是 A .锡青铜的熔点比纯铜高 B .在自然环境中,锡青铜中的锡对铜起保护作用 C .锡青铜文物在潮湿环境中的腐蚀比干燥环境中快 放电 充电 2019年普通高等学校招生全国统一考试理科化学II卷 可能用到的相对原子质量:H 1 C 12 N 14 O 16 F 19 Na 23 S 32 Cl35.5 As 75 I 127Sm 150 7.“春蚕到死丝方尽,蜡炬成灰泪始干”是唐代诗人李商隐的著名诗句,下列关于该诗句中所涉及物质的说法错误的是 A.蚕丝的主要成分是蛋白质 B.蚕丝属于天热高分子材料 C.“蜡炬成灰”过程中发生了氧化反应 D.古代的蜡是高级脂肪酸酯,属于高分子聚合物 8.已知N A是阿伏加德罗常数的值,下列说法错误的是 A.3g 3He含有的中子数为1N A B.1 L 0.1 mol·L?1磷酸钠溶液含有的PO3- 4 数目为0.1N A C.1 mol K2Cr2O7被还原为Cr3+转移的电子数为6N A D.48 g正丁烷和10 g异丁烷的混合物中共价键数目为13N A 9.今年是门捷列夫发现元素周期律150周年。下表是元素周期表的一部分,W、X、Y、Z为短周期主族元素,W与X的最高化合价之和为8。下列说法错误的是 A.原子半径:W 2019年全国卷Ⅱ理综化学 可能用到的相对原子质量:H 1 C 12 N 14 O 16 F 19 Na 23 S 32 Cl 35.5 As 75 I 127 Sm 150 一、选择题:本题共13个小题,每小题6分。共78分,在每小题给出的四个选项中,只有一项是符合题 目要求的。 7.“春蚕到死丝方尽,蜡炬成灰泪始干”是唐代诗人李商隐的著名诗句,下列关于该诗句中所涉及物质的说法错误的是 A.蚕丝的主要成分是蛋白质 B.蚕丝属于天热高分子材料 C.“蜡炬成灰”过程中发生了氧化反应 D.古代的蜡是高级脂肪酸酯,属于高分子聚合物 8.已知N A是阿伏加德罗常数的值,下列说法错误的是 A.3g 3He含有的中子数为1N A PO 数目为0.1N A B.1 L 0.1 mol·L?1磷酸钠溶液含有的3 4 C.1 mol K2Cr2O7被还原为Cr3+转移的电子数为6N A D.48 g正丁烷和10 g异丁烷的混合物中共价键数目为13N A 9.今年是门捷列夫发现元素周期律150周年。下表是元素周期表的一部分,W、X、Y、Z为短周期主族元素,W与X的最高化合价之和为8。下列说法错误的是 A.原子半径:W C 向盛有饱和硫代硫酸钠溶液的试管中滴加稀 盐酸 有刺激性气味气体产生,溶液变浑浊 D 向盛有FeCl3溶液的试管中加过量铁粉,充分 振荡后加1滴KSCN溶液 黄色逐渐消失,加KSCN后溶液颜色不变11.下列化学方程式中,不能正确表达反应颜色变化的是 A.向CuSO4溶液中加入足量Zn粉,溶液蓝色消失 Zn+CuSO4Cu+ZnSO4 B.澄清的石灰水久置后出现白色固体 Ca(OH)2+CO2CaCO3↓+H2O C.Na2O2在空气中放置后由淡黄色变为白色 2Na2O22Na2O+O2↑ D.向Mg(OH)2悬浊液中滴加足量FeCl3溶液出现红褐色沉淀 3Mg(OH)2+2FeCl32Fe(OH)3+3MgCl2 12.绚丽多彩的无机颜料的应用曾创造了古代绘画和彩陶的辉煌。硫化镉(CdS)是一种难溶于水的黄色颜料,其在水中的沉淀溶解平衡曲线如图所示。下列说法错误的是 A.图中a和b分别为T1、T2温度下CdS在水中的溶解度 B.图中各点对应的K sp的关系为:K sp(m)=K sp(n)2020年全国Ⅰ高考化学试题点评
2016年高考化学试题全国II卷 含答案 word版
2018年高考化学试卷(全国卷1)
(完整版)2019年高考试题—理综化学(山东卷)解析版.doc
历年化学高考试题.doc
高考化学全国卷3
2015高考化学全国卷一(含答案)
2020全国卷2高考化学
高考电化学历年真题汇编练习版
2019年高考理综化学全国2卷含答案
2019年高考化学试卷-(全国II卷与答案)
