坡长坡度因子的生成过程

坡长坡度因子的生成过程如下:
1、要估算坡长因子,可以利用ARCGIS中的水文模块提取流水累积量。
流水累积量的计算,要先建立无洼地的DEM。(见水文分析过程)
利用 jx_srtm 数据,先生产任意流向图:flowdir,再寻找洼地:sink,并计算洼地流域贡献围:sink_watersh 。再计算每个洼地的最低高程和出水口高程:zonalmin ,zonalmax,并可以求出洼地深度:sinkdep = zonalmax – zonalmin。
填充洼地:fill_jx_srtm。并计算无洼地的dem的水流流向:flowdir_fill1。然后计算流水累积量:flowacc。
2、根据坡长因子公式(参考文献:土壤侵蚀研究中的坡长因子评价问题):
L=(λ/22.13) m, λ=flowacc * cell size
其中:m=n/(1+n),n=(sinθ/0.0896)/(3.0*sin0.8θ+0.56)
这里的θ用“jx_slope.img *3.1415926/180”替代
依次得到图:n、 m、 l_yinzi
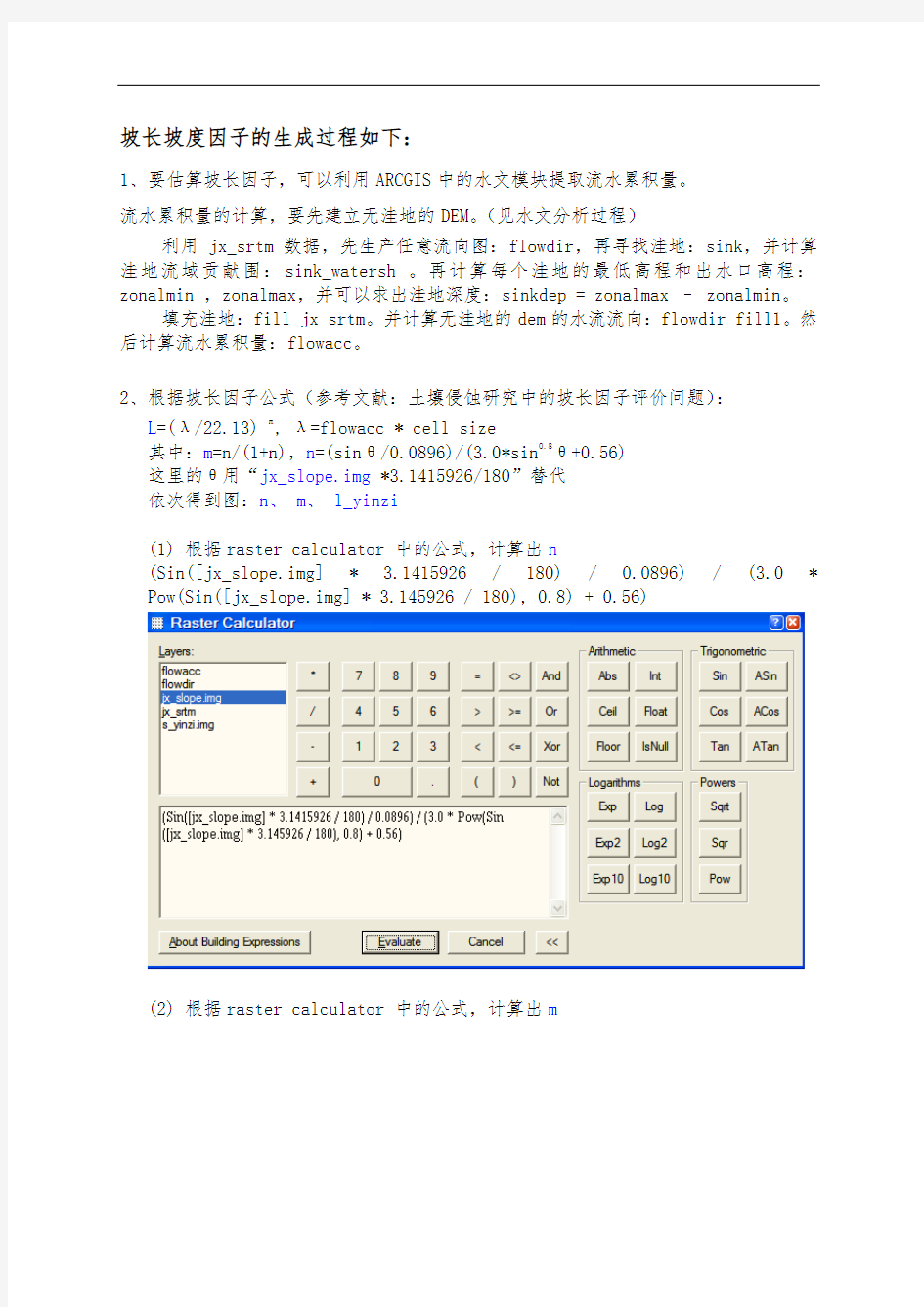
(1) 根据raster calculator 中的公式,计算出n
(Sin([jx_slope.img] * 3.1415926 / 180) / 0.0896) / (3.0 * Pow(Sin([jx_slope.img] * 3.145926 / 180), 0.8) + 0.56)
(2) 根据raster calculator 中的公式,计算出m
(3) 根据raster calculator 中的公式,计算出l_yinzi Pow([flowacc] * 87.72085638 / 22.13, [m])
对得到的l_yinzi(l_yinzi1.img)进行去除异常值:
利用ERDAS中的图像增强工具,对异常值进行平滑处理。
这里,我们选择以下的运算模板:
因此,得到图:l_yinzi_convolution.img。
再利用建模工具,对l_yinzi1.img和l_yinzi_convolution.img求值。(参考文献:GIS支持下的土壤侵蚀量估算_以省泰和县灌溪乡为例)
得到图:l_yinzi_model.img,为最后的L因子图。
3、根据坡度因子公式:S= 10.8*sinθ+ 0.03 (θ<5),
16.8*sinθ- 0.50 (5<=θ<10),
21.9*sinθ- 0.96 (θ>=10)
利用建模工具,得到s_yinzi.img
肿瘤血管生成与血管生成抑制因子的研究进展
肿瘤血管生成与血管生成抑制因子的研究进展 摘要:肿瘤血管生成在肿瘤的生长和转移中起着重要的作用,是肿瘤生长、侵袭、转移和复发的先决条件。肿瘤的血管生成是一个复杂的生物学过程,包括血管内皮细胞的增殖、出芽和迁移等。这一过程中有众多肿瘤血管生成因子和抑制因子参与调节和激活血管生成的开关。因此, 研究肿瘤血管生成相关分子在肿瘤血管生成中的作用机制, 及其对肿瘤血管生成的调控,形成一种抗血管生成疗法,来达到控制肿瘤血管生长和转移的目的, 对肿瘤的治疗具有重要意义。 关键词:肿瘤血管生成;血管生成因子;血管生成抑制因子;血管生成开关恶性肿瘤的生长和转移依赖于血管生成。当肿瘤体积超过2-3mm3后局部缺血缺氧[ 1] , 需要产生新的毛细血管以维持肿瘤的生长, 丰富的血管可向肿瘤提供足够的营养物质, 清除各种降解产物, 肿瘤细胞亦经血管进入血液循环发生血行转移, 否则肿瘤将发生退行性坏死[ 2].新血管的形成发展取决于血管生成生长因子和血管生成抑制因子之间的动态平衡,当血管生长因子与血管抑制因子达到平衡时,血管生成不被启动; 当此平衡趋向于血管生成时,血管开关被开启,新生血管开始生成。在正常组织中, 由于缺少血管生成生长因子或生长因子被高水平的血管生成抑制因子严格控制,血管生成的开关处于关闭状态;但在肿瘤组织中, 生长因子过度表达, 抑制因子表达过低, 改变了这个平衡, 开启了肿瘤血管生成的表型, 导致新血管的生长。因此,有学者认为肿瘤血管形成的始动因素是血管生长因子和血管抑制因子失衡,并且这种失衡会持续出现在肿瘤生长过程中,并提出了通过抑制血管生长因子信号通路,来抑制肿瘤生长和转移。[3]1.肿瘤血管生成开关机制 实验和临床数据表明,大多数人类肿瘤生成早期不诱导血管生成和并存在于原位,在无血供数月至数年后,肿瘤中的一些细胞向血管生成的表型转变,这种现象称为血管生成开关。这一机制的分子基础可能是血管生成抑制剂的减少以及血管生成因子产量增加所致[4]。因此,血管生成表型的开关是由血管生成因子与血管生成抑制因子的动态变化来调节。
SPSS探索性因子分析报告地过程
现要对远程学习者对教育技术资源和使用情况进行了解,设计一个李克特量表,如下图所示: 问题题项从未使用很少使用有时使用经常使用总是使用 1 2 3 4 5 a1 电脑 a2 录音磁带 a3 录像带 a4 网上资料 a5 校园网或因特网 a6 电子邮件 a7 电子讨论网 a8 CAI课件 a9 视频会议 a10 视听会议 一.因子分析的定义 在现实研究过程中,往往需要对所反映事物、现象从多个角度进行观测。因此研究者往往设计出多个观测变量,从多个变量收集大量数据以便进行分析寻找规律。多变量大样本虽然会为我们的科学研究提供丰富的信息,但却增加了数据采集和处理的难度。更重要的是许多变量之间存在一定的相关关系,导致了信息的重叠现象,从而增加了问题分析的复杂性。 因子分析是将现实生活中众多相关、重叠的信息进行合并和综合,将原始的多个变量和指标变成较少的几个综合变量和综合指标,以利于分析判定。用较少的综合指标分析存在于各变量中的各类信息,而各综合指标之间彼此是不相关的,代表各类信息的综合指标成为因子。因子分析就是用少数几个因子来描述许多指标之间的联系,以较少几个因子反应原资料的大部分信息的统计方法。
二.数学模型 i m im i i i i U F F F F Z +++++=αααα · · · 332211 i Z 为第i 个变量的标准化分数;(标准分是一种由原始分推导出来的相对地位量数,它是用来说明原始分在所属的 那批分数中的相对位置的。) m F 为共同因子; m 为所有变量共同因子的数目; i U 为变量i Z 的唯一因素; im α为因子负荷。(也叫因子载荷,统计意义就是第i 个变量与第m 个公共因子的相关系数,它反映了第i 个变量在 第m 个公共因子上的相对重要性也就是第m 个共同因子对第i 个变量的解释程度。) 因子分析的理想情况,在于个别因子负荷im α不是很大就是很小,这样每个变量才能与较少的共同因子产生密切关联,如果想要以最少的共同因素数来解释变量间的关系程度,则i U 彼此间不能有关联存在。 所谓的因子负荷就是因子结构中原始变量与因子分析时抽取出共同因子的相关,即在各个因子变量不相关的情况下,因子负荷im α就是第i 个原有变量和第m 个因子变量间的相关系数,也就是i Z 在第m 个共同因子变量上的相对重要性,因此,im α绝对值越大则公共因子和原有变量关系越强。在因子分析中有两个重要指针:一为“共同性”,二为“特征值”。 所为共同性,也称变量共同度或者公共方差,就是每个变量在每个共同因子的负荷量的平方总和(一横列中所有因子负荷的的平方和),也就是个别变量可以被共同因子解释的变异量百分比,这个值是个别变量与共同因子间多元相关的平方。从共同性的大小可以判断这个原始变量与共同因子间的关系程度。如果大部分变量的共同度都高于0.8,则说明提取出的共同因子已经基本反映了各原始变量80%以上的信息,仅有较少的信息丢失,因子分析效果较好。而各变量的唯一因素就是1减掉该变量共同性的值,就是原有变量不能被因子变量所能解释的部分。 所谓特征值,是每个变量在某一共同因子的因子负荷的平方总和(一直行所有因子负荷的平方和),在因子分析的的共同因子抽取中,特征值最大的共同因子会最先被抽取,其次是次大者,最后抽取的共同因子的特征值会最
肿瘤细胞诱导血管生成模型具体步骤及详细说明
肿瘤细胞诱导血管生成模型具体步骤及详细说明 肿瘤血管生成是指肿瘤微环境诱导的在原有血管基础上生成以毛细血管为主的血管系统,并在肿瘤组织内建立血液循环的过程。肿瘤血管生成与肿瘤微环境密切相关,受多种促血管生成因子和(或)血管生成抑制因子的调节。 1、鸡胚准备和接种组织:选择北京白鸡种蛋,洗净,用l:1000苯扎溴铵(新洁尔灭)液浸泡3分钟,置37.8土0.5℃培养箱中孵育。鸡胚发育第7天,蛋壳消毒后,标记制作2cmX3cm左右观察窗。接种组织视研究目的而定,一定要在接种当日取材,充分清洗除去血污和粘液,再剪成1——2mm 组织小块。 2、组织接种:在制备鸡胚观察窗的次日,即鸡胚发育第8天进行组织接种。每个鸡胚可接种5—7个组织小块于接种部位CAM表面,再用透明胶纸封好,继续孵育。 3、接种组织的收获与观察:组织接种后每12小时观察一次,到组织接种第11天(鸡胚发育第18天)收获接种组织,取出鸡胚,置接种组织连同周围的CAM于解剖显微镜下观察,并用10%甲醛固定保存,部分组织可作石蜡切片,用作血管生成研究的免疫组化染色等。 4、CAM的血管生成表现:组织接种24小时后,CAM血管开始向接种组织生长,随培养时间的延长,血管数目及直径均明显增加;第2天,新细小血管直接趋向组织;第3天,新生血管形成以接种组织为中心,10——20条放射状
血管网;尔后,CAM血管继续明显增加。非接种部位与接种部位比较,CAM 血管数目少,大血管与小血管呈脉样均匀分布;而接种部位的CAM血管在接种组织周围弥散样增加,以组织为中心向周围呈放射状分布,在首先与组织发生联系的区域CAM血管更多。第4天,可见新生细小CAM血管生长形成中、粗血管,并在中、粗血管继续分支出细小血管,形成新的血管网。CAM血管管腔结构清晰,可区别动、静脉。 注意事项 该类体外实验研究,有很多人为因素影响,不能代表体内生理反应,因为内皮细胞在生长因子存在的条件下培养了很长一段时间,已被激活。因此,有必要建立一类与体内生理反应有关的血管生成实验方法,尤其是与人类血管生成有关的血管生成实验。 CAM血管生成模型用于血管生成的研究,可取得两方面结果: ①检测评价接种物刺激CAM血管增生的血管生成作用,用于分析研究血管生成促进因子、抑制因子的活性和作用的检测,如肿瘤血管生成的研究等; ②对接种物,如肿瘤组织、自身的血管生成进行研究,用于分析不同组织的血管生成活性和作用,如肿瘤组织有引发新生血管生成的作用。
血管内皮因子综述
血管内皮生长因子与肿瘤治疗的研究进展 【摘要】肿瘤生长和转移依赖于血管生成,肿瘤血管生成是受多种细胞因子、生长因子及其受体调控,其中血管内皮生长因子(VEGF)及其受体(VEGFR)被认为是最关键的调控因子, 以VEGF及其受体作用途径中的任一环节为靶点,阻断VEGF对肿瘤血管的作用,都可以达到遏制肿瘤生长和转移的目的。VEGF靶向抗肿瘤血管生成成为抗肿瘤的新策略。 【关键词】VEGF 肿瘤靶向治疗 血管内皮生长因子(vascular endothelial growth factor,VEGF),也叫做血管通透因子(vascular permeability factor,VPF),在正常胚胎发育时有广泛的表达,但正常成年者的组织中呈低水平表达,在肿瘤等病理情况下其表达异常升高。VEGF是一种高度特异性的血管内皮细胞有丝分裂因子,通过与其特异性受体(VEGFR)结合,引起一系列的信号转导,释放多种细胞因子与生长因子,刺激血管内皮细胞增殖和迁移,促进新生血管生成,在肿瘤的生长和转移中起重要作用。 1.VEGF生物学功能 VEGF的功能包括:①诱导内皮细胞钙浓度短暂升高、形态改变、分裂及运动,影响内皮细胞基因表达,加快基底膜降解,从而发挥促血管生成功能。②增加血管通透性,使血浆蛋白外渗,形成血管化纤维蛋白基质,为内皮细胞迁移形成网架。血管内物质外漏也为肿瘤转移提供基质,这对于肿瘤发展和转移可能比促内皮细胞增生更重要。另外,肿瘤细胞分泌的VEGF弥散作用于肿瘤周围组织的毛细血管,使其通透性增加造成瘤周水肿。③改变内皮细胞基因表达,诱导其合成大量蛋白水解酶,加速血管构建。④抑制宿主抗原呈递细胞成熟,使肿瘤细胞得以逃避免疫监视。⑤诱导血管内皮细胞bcl-2基因表达,提高诸如放射损伤细胞、血管内皮细胞抗凋亡的能力。 2.VEGF促进肿瘤生长、侵袭、转移的机制 肿瘤的侵袭、转移涉及到多个步骤:包括在局部生长到一定大小后瘤细胞从原发灶脱落,细胞外基质和基底膜的降解,瘤细胞进入血循环后逃脱宿主的免疫监控而存活下来, 瘤细胞达远处组织器官后粘附, 继而新生血管形成, 最后继发成瘤。VEGF几乎参与了此过程中的各个步骤,而不仅仅只作为促血管生成因子和血管通透性因子。 2.1 VEGF通过对内皮细胞的增殖、迁移、粘附的调节而促进新生血管的形成。 2.2 肿瘤细胞分泌的VEGF通过自分泌机制与瘤细胞上的VEGFR-2(KDR)结合,调控下游基因的表达而促进瘤细胞的生长、侵袭、转移。 2.3 VEGF通过抑制树突细胞的分化、成熟,减少树突细胞的生成从而降低宿主免疫功能。3.VEGF肿瘤治疗中的应用 3.1 基因治疗 3.1.1 反义寡核苷酸 反义寡核苷酸可抑制VEGF基因水平的分泌,也可特异性降低细胞中VEGFR mRNA水平。高渝等利用超声微泡介导VEGF反义寡核苷酸转染作用于人膀胱癌裸鼠移植瘤模型,
血管生成(Angiogenesis)信号通路图
本实验技术来源于SciMall科学在线 血管生成(Angiogenesis)信号通路图 血管生成是通过人体中存在的诸多互补和复杂的信号途径调节的.血管内皮生长因子(VEGF)-血管内皮生长因子受体(VEGFR)、血管生成素(Ang)-Tie2轴和Dll4-Notch这3个复杂的、相辅相成的信号传导通路可在调节血管生成中发挥重要作用. VEGF与内皮细胞上的两种受体KDR和Flt-1高亲和力结合后,直接刺激血管内皮细胞增殖,并诱导其迁移和形成官腔样结构;同时还可增加微血管通透性,引起血浆蛋白(主要是纤维蛋白原)外渗,并通过诱导间质产生而促进体内新生血管生成。VEGF在血管发生和形成过程中起着中枢性的调控作用,是关键的血管形成刺激因子。碱性成纤维细胞生长因子(bFGF)。TNF-α是一类具有血管活性的细胞因子,可诱导异位子宫内膜炎性细胞因子MCP-1,IL-6和IL-8等的释放,促进异位内膜及基质细胞增殖及炎性细胞浸润,新生血管形成,组织粘连,从而形成异位病灶。 (来源:Scimall科学在线) 本信号转导涉及的信号分子主要包括: HIF1α,PHDs,HIF1β,PI3K,Akt,mTOR,S6K,4E-BP1,eIF4E1,elF4E1,Ras,MEK1,MEK2,Erk1,Erk2,MNK,CBP,P300,TCEB1,TCEB2,Rbx1,Cul2,VHL,MMP,Cox2,PAI-1,VEGF,PDGFR-β,VEGFR2,Tie2,FGFR,IGFR,TGFα-R,SLIT,ROBO,Src,FAK,p38,MAPK,Smad2,Smad3,PLCγ,NOS等。 点击图中信号分子,自动寻找相关试剂
赤魟软骨血管生成抑制因子的制备【开题报告】
开题报告 药学 赤魟软骨血管生成抑制因子的制备 一、综述本课题国内外研究动态,说明选题的依据和意义 作为拥有1.8万公里海岸线的国家,我国的渔业资源非常丰富,赤魟就是这丰富资源中的一种。 魟鱼[1] (Ray)俗称鯆鱼,草帽鱼,蒲扇鱼,黄貂鱼。英文名:Red stingray。它属暖温类底层鱼,属于脊椎动物门Verterata,软骨鱼纲Chondrichthyes,板鳃亚纲Elasmobranchii,鳐目(或魟目)Rajiformes,魟科Dasyatidae和燕魟科Myliobatidae。全世界共有六个科158种。赤魟主要分布于我们南海和东海,长江口咸谈水中亦有分布。浙江沿海拥有丰富的海洋资源,其中以赤魟(Dasyatis akajei)资源最为丰富。 魟软骨味尚佳,皮厚实,无血有光泽,含丰富的胶质,水发后烹制成“大扒鱼皮”,味道鲜美,是宴席上的珍品。此外,作为药用,其肉性味甘、咸平,无毒,具有健脾补气、滋补强身之功效。用其熬油,主治小儿疳积。尾毒的毒液是一种氨基酸和多肽类的蛋白质,其药性咸、寒,有小毒,对于中枢神经和心脏具有一定的效应,有清热消炎、化结、除癥之功效。尾刺研末入药,对治疗胃癌、食道癌、肺癌、乳腺炎、咽喉炎、疟疾、牙痛、魟鱼尾刺刺伤均有一定疗效。其肝除作为制作鱼肝油的原料外,煮食后能治夜盲症。 但是,国内外对赤魟的生物活性研究还处于起步阶段,其应用研究和应用基础几乎空白,资源量丰富、营养药用价值高的赤魟仅处于被人们日常食用的阶段。上文所述赤魟的药用价值大多都是对赤魟尾刺提取物、赤魟肝脏活性蛋白、赤魟软骨多糖或其软骨活性蛋白的研究。 如肖湘等对赤魟肝脏活性蛋白体外抗氧化作用的研究[2],采用硫酸铵沉淀、Sephadex-G150柱层析的方法从赤魟肝脏分离活性蛋白,测定活性蛋白清除超氧阴离子自由基、羟自由基和抑制脂质过氧化作用,结果显示分离得到的三个蛋白峰均具有很强的抗氧化作用。 罗红宇等对赤魟软骨黏多糖的制备研究[3],探索利用碱浸提和酶法去蛋白从赤魟
银屑病与血管生成因子(一)
银屑病与血管生成因子(一) 摘要:银屑病是一种炎症性疾病,血管生成是银屑病病理改变的特征之一。作为银屑病发生发展必不可少的条件,血管生成相关因子在银屑病发病机制中的研究日益受到重视。现就目前若干银屑病血管生成研究中较热点的血管生成相关因子:血管内皮生长因子,肝细胞生长因子,胸苷磷酸化酶,血小板反应蛋白等的研究进展作一综述。 银屑病是一种常见的复发性、炎症性皮肤病。以角质形成细胞(KC)过度增生、炎症细胞浸润、新生血管形成为其组织病理三要素。目前研究表明:银屑病皮损处的真皮乳头层微血管扩张迂曲,通透性增高,血管数量增多,并认为这种变化主要发生在毛细血管后微静脉1]。银屑病中最先发生的病理改变是血管的分布和形成的改变1,2]。在银屑病患者非皮损皮肤中亦常能见到异常扩张的血管2]。银屑病的复发则与皮损内真皮乳头内皮细胞的过度表达有关。且银屑病患者皮肤血管生成只与表皮变化有关,而与真皮无关3]。微血管是皮肤组织与循环血液进行物质交换的场所。因此对银屑病血管生成的研究有助于揭示银屑病的发病机制,并指导临床治疗。目前有关银屑病血管生成,特别是一些血管生成相关因子以及抗血管生成药物治疗银屑病的研究日益受到重视。 促血管生成物质诱导血管生成的过程大致可分解为以下几步:①内皮细胞激活;②基底膜和细胞外基质降解;③内皮细胞增生,并迁移到血管周围基质形成管腔;④新生血管网络系统形成。现就近几年在银屑病研究中的若干热点血管生成因子的研究进展综述如下4,5]。 一、血管内皮生长因子 血管内皮生长因子(VEGF)又名血管通透性因子(VPF),有4种不同的亚型,在人类细胞中的氨基酸残基数分别为121,165,189,2066],是由同一基因因mRNA剪接差异而生成的不同表达产物。VEGF在体内可以增加血管通透性,促进血管生成;在体外则作为内皮细胞选择性的有丝分裂原。VEGF是内皮细胞特异性的,它能改变内皮细胞的基因表达。VEGF 与血管内皮细胞表面的两个酪氨酸激酶受体kdr与flt-1结合,使胞浆内Ca++浓度上升,刺激三磷酸肌醇(IP3)聚集,这一作用被认为与磷酸肌醇特异性的磷脂酶C有关6,7]。Siemeister 等8]报道:人工合成的VEGF变异体能抑制VEGF介导的受体自动磷酸化和内皮细胞增生。其增加血管通透性的作用可能是通过囊泡-液泡细胞器(vesicular-vacuolarorganelleVVO)起效的6]。VEGF能上调囊泡-液泡细胞器功能,调节血管基底膜上窗孔的开放或关闭,它的促血管通透性增加的作用较组胺强50000倍9]。另有报道,VEGF在冠状动脉内皮细胞中可能是通过一氧化氮/鸟苷酸环化酶信号级联(guanylatecyclasesignalingcascade)放大起作用的10]。Detmar等9]报道,VEGFmRNA及蛋白表达水平在银屑病患者皮损中明显增加,而在正常人皮肤中几乎没有VEGFmRNA表达。患者非皮损处VEGFmRNA及蛋白水平表达亦增加,且出现银屑病早期病理改变。研究发现VEGF染色位于基底层上(suprabasal)的KC胞浆内,kdr 与flt-1的mRNA则表达于活动期皮损的真皮乳头层微血管内皮细胞上,在正常人或皮损更深部位则无kdr与flt-1的mRNA表达。同时发现,转化生长因子/表皮生长因子(TGF-α/EGF)对培养的人KC中VEGFmRNA的表达有剂量依赖的诱导上调作用,TGF-α/EGF受体在银屑病皮损中表达也明显增高。TGF-α能刺激VEGF合成分泌。另外VEGFmRNA和TGF-αmRNA在表皮KC的相同定位也在一定程度上证实了上述观点。最近有研究表明,KC通过自分泌成纤维细胞生长因子FGF-4(bFGF)上调VEGFmRNA来表达其血管生成活性11]。 由此可见VEGF所介导的银屑病血管生成过程是:表皮KC在受到刺激后能通过自分泌或旁分泌的形式释放细胞因子,促进VEGF表达,而VEGF则通过内皮细胞上的特异性受体kdr 和flt-1使胞内发生一系列改变,促使血管通透性增加及血管内皮细胞增生、迁移,最终导致新生血管形成。 二、肝细胞生长因子 肝细胞生长因子(HGF)又名扩散因子(SF),是由基质细胞(stromalcell)、成纤维细胞及
中药抗肿瘤血管生成研究进展
中药抗肿瘤血管生成研究进展 (作者:__________ 单位: __________ 邮编:____________ ) 【摘要】抗肿瘤血管生成为肿瘤的治疗提供了新的契机,中药均为有效的血管生成抑制剂,具有廉价无毒等优点,随着其抗肿瘤,血管生成等机制方面研究的不断深入,中草药极有希望成为理想 而全面的癌症预防和治疗药物。 【关键词】肿瘤血管抑制因子综述 近年来中药或有效成分抑制肿瘤血管生成研究非常活跃,也具有明显的广度和深度。 1中草药研究动态 1.1去甲斑蝥素范跃祖等观察了去甲斑蝥素(NCTD对胆囊癌肿瘤血管生成的抑制作用及其机制NCTD可有效抑制、破坏胆囊癌肿瘤血管生成,进而抑制胆囊癌的增殖与生长。其机制可能与NCTD诱导血管内皮细胞凋亡、直接破坏血管内皮细胞、改变血管内皮细胞PCNA/凋亡比、下调血管生成因子VEGFA n期2和上调血管抑制因子TSP TIMP2表达有关[1]。 1.2小檗碱小檗碱(berberine)为黄连(毛茛科植物)、黄柏等
(芸香科植物)植物的一种生物碱,作为抗菌药已有悠久的历史。初步研究表明它在体内、体外对多种肿瘤细胞具有较强的抑制和杀伤作用 :2]。娄金丽等研究小檗碱对bFGF活化人脐静脉内皮细胞(HUVEC)增殖、细胞周期及细胞凋亡的影响,探讨其对肿瘤新生血管形成作用的机制。方法:MTT法检测小檗碱对bFGF活化HUVEC勺增殖作用;流式细胞仪检测用药后细胞周期的变化;激光共聚焦扫描显微镜下观察药物对细胞形态、细胞内钙的影响;流式细胞仪检测小檗碱对细胞凋亡的作用。结果:小檗碱能明显抑制bFGF活化的HUVE(增殖,且存在剂量依赖关系;使细胞在GG以G1期的比例明显增多;使细胞核浓缩、甚至裂解成碎块,同时使细胞内钙增多;并诱导活化HUVEC 发生细胞凋亡。结论:小檗碱可能通过将bFGF活化的HUVEC田胞周期阻滞在G期G1期,抑制活化HUVEC勺增殖;诱导活化HUVEC田胞发生凋亡等机制,阻止新生血管形成,发挥其抗肿瘤作用]3]。 1.3白藜芦醇白藜芦醇是广泛存在于葡萄、花生和多种药用植物中的一种多酚类化合物,目前至少已经在21个科,31个属的72 种植物中发现了白藜芦醇。早期研究发现,白藜芦醇具有保护心血管, 调节血脂、抗病原微生物、护肝等多种生物学作用。自从Jang等于1997年系统报道了白藜芦醇的抗肿瘤作用后,迄今已发现白藜芦醇能通过多种途径抑制肿瘤细胞的起始,促进,发展三个阶段,而且可以抑制肿瘤血管形成。1.对内皮细胞的作用,能够直接抑制血管内皮细胞的增生,迁移及诱导其凋亡,从而抑制血管的生成。 2.对血管生
血管生成实验模型研究进展
血管生成实验模型研究进展 吴家明1 ,陆 茵 1,2 ,郜 明1,张伟伟 1 (1.南京中医药大学中医药研究院,江苏南京 210029;2.江苏省方剂研究重点实验室,江苏南京 210029) 收稿日期:2007-09-21,修回日期:2007-11-01 基金项目:国家自然科学基金资助项目(No 30371727,30772766);江 苏省自然科学基金资助项目(No BK2003113) 作者简介:吴家明(1980-),男,硕士生,研究方向:肿瘤血管生成与 抗肿瘤转移研究,E 2mail:nj w ujia m ing@https://www.360docs.net/doc/8810224486.html,; 陆 茵(1963-),女,教授,博士生导师,研究方向:肿瘤血管生成与抗肿瘤转移研究,通讯作者,Tel:0252 86798154,E 2mail:luyingreen@https://www.360docs.net/doc/8810224486.html, 中国图书分类号:R 205;R 332;R 3632332;R 36413 文献标识码:A 文章编号:1001-1978(2008)01-0011-04摘要:抗血管生成已经成为治疗肿瘤转移、糖尿病视网膜病变、风湿性关节炎等疾病的重要策略之一。血管生成模型作为一种研究工具在探讨血管形成机制、发现促进或抑制血管生成药物等研究中发挥十分积极的作用。如何寻找适合的血管生成模型是研究人员在研究中常遇到的问题。该文就主要常用模型做较全面的介绍,并对其优缺点进行评价。关键词:血管生成;模型 血管生成(angi ogenesis )是指在原有的毛细血管和(或)微静脉基础上通过血管内皮细胞的迁移和增殖,从已存在的血管处以芽生或非芽生(套迭)形式形成新的、以毛细血管为主的血管系统过程 [1] 。血管生成是许多促进或抑制血管 生成的分子参与调节的一个平衡过程[2]。血管生成过多与肿瘤、糖尿病性视网膜病变等疾病有关[3],抑制血管生成已经成为治疗这些疾病的重要策略。因此寻找血管生成抑制剂成为研究热点。血管生成研究需借助血管生成模型进行,血管形成的许多过程都可以在血管生成模型中模拟完成,包括内皮细胞增殖、迁移、毛细血管网状结构的形成等。本文就常用体内、体外及整体模型进行综述。 1 体外模型 体外模型主要分为细胞水平及组织学水平两类,常用的体外模型有以下4种。 1.1 内皮细胞增殖实验(cell proli fera ti on a ss ay) 内皮细 胞活化增殖是血管生成的起始阶段。目前主要有两种测定细胞增殖的方法即净细胞数测定和细胞周期分析。 1.1.1 净细胞数测定 M TT 法(四甲基偶氮唑比色法)是 测定活细胞数的化学定量方法,操作简便,价格低廉。但它不适合测定对细胞代谢有影响的药物,因为这类药物能影响 MTT 测定的活细胞数。另外通过胸腺嘧啶核苷参入法测定DNA 合成来测定细胞增殖能力。抑制细胞增殖可能是由于 药物的抑制作用,也可能是药物的毒性作用引起。因此,这种方法常需要结合细胞凋亡实验的数据才可以更好地评价药物对细胞增殖的影响。 1.1.2 细胞周期分析 近年来有报道通过细胞周期分析来 评价药物对细胞增殖的影响,细胞短时间暴露到溴脱氧尿苷 (B rd U )中可以促使B rdU 参入细胞DNA 中。碘化丙啶(P I ) 染色后测定细胞的总DNA 量,再用荧光激活细胞分析仪测定细胞中B rd U 和P I 的量可得出细胞周期信息[4]。但实验用的内皮细胞处于增殖状态,与体内静止状态的内皮细胞是不同的,实验结果与体内还是存在一定差异。 1.2 内皮细胞迁移实验(cell m i gra ti on a ss ay) 常用迁移 模型有两种:①细胞损伤模型:在培养血管内皮细胞的培养皿上用刀片划出#形区,经P BS 洗涤后再用含011%明胶的 ME M 培养20h,细胞用甲醇固定,Gie m sa 染色。在光镜下计 数从损伤边缘迁移出的细胞数,需要注意的是划出的损伤区域一定要精确。②Boyden 室模型,Boyden 室由两层组成,两层之间为胶原包被的多孔的多聚碳酸盐滤膜;血管内皮细胞放于上层,同时加入待测药物,共同培养6h 后,除去上层的细胞,下层细胞用甲醇固定,HE 染色,光镜下计算下层的血管内皮细胞数。龙淼云等[5]采用本模型研究证明了血管生成抑制因子arresten 对huvec 迁移有抑制作用。Boyden 室模型优点在于它对药物浓度梯度差异很敏感。但对实验技术要求较高且计数方法不同可能会造成统计结果误差较大。因此有必要建立一个严格的计数标准以减少因方法不同产生的误差。 1.3 小管形成实验(tube for ma ti on a ss ay) 小管形成实验 能模拟人体内毛细血管生成的过程,包括内皮细胞出芽增殖和毛细血管网结构形成等步骤,接近人体内血管生成的实际过程。内皮细胞在基质胶、纤维蛋白胶、胶原等基质上培养时能形成网状结构。用电子显微镜来分析小管间的紧密连接,从而定量血管生成情况[6]。需要指出的是似乎所有的内皮细胞都能在细胞外基质上形成管状结构,有些非内皮细胞也能在基质胶上形成管腔结构[7]。实验一般采用24孔培养板,但它底面积大,Matrigel 用量多,计数区域大只能随机选择几个典型区域且数据分析耗时长。Sanz 等[8]采用384孔和1536孔培养板培养可节约胶的用量,借助计算机可以计算整个孔的小管及小管之间的连接数及小管的长度和面积。改进方法后减少了原来分析困难及重现性差的缺点。 1.4 大鼠动脉环实验(ra t aorti c r i n g a ss ay) 1990年N ic 2osia 等首次将此模型应用于血管生成研究中。取下大鼠主 动脉后,剪成1mm 宽的血管环,再用纤维蛋白胶或胶原蛋白胶包埋,然后以无血清的MC DB131培养液培养。培养过程中每天计算主动脉环产生的新生微血管数并进行定量分析。用不同胶培养的大鼠主动脉环新生血管的生长曲线不同。胶原包埋的主动脉环,培养1wk 时血管数达到顶峰,第 2wk 开始萎缩。用纤维蛋白胶包埋时能使血管数顶峰期维 ? 11?中国药理学通报 Chinese Phar m acological B ulletin 2008Jan;24(1):11~4
血管新生概念及其调控因子网络
血管新生概念及其调控因子网络 1.1病理性血管新生与治疗性血管新生 任何组织损伤后的修复都离不开血管生成,血管生成是组织修复的中心。血管生成过程包括血管新生、血管发生和原已存在的血管剪切重构形成的成熟毛细血管网。血管新生,是指毛细血管从原血管以出芽方式形成新血管床的过程。通常存在于胚胎形成和产后组织正常生长的过程中,成年女性生殖系统子宫内膜血管的周期性反复重建和组织受损后正常的修复也有血管生成的参与。在这些过程中,血管生成的启动受到多种因素的控制,仅随刺激信号的出现开启短暂时间,然后即被关闭。所以,体内血管的生长与抑制处于动态平衡,以保持相对静止状态,当这一状态一旦被打破,即导致许多疾病的发生[5]。在创伤、缺血、炎症、伤口愈合、肿瘤生长、糖尿病性视网膜病、风湿性关节炎、牛皮癣等许多病理条件下亦可发生新的血管形成。血管新生包括以下几个过程[6]:①小血管(常常为毛细血管后静脉)基底膜和基质的降解,参与这一过程的有胶原酶、尿激酶型纤溶酶原激活物等;②内皮细胞在趋化因子的作用下发生迁移,bFGF、VEGF、IL-8等对这一过程均具有促进作用;③内皮细胞增殖;④在内皮芽生的基础上形成管腔;⑤芽生的管腔相互融合成环状血管分支,形成三维管状结构,允许血流通过;⑥血管周细胞进一步构建血管结构;⑦血管周围基膜的形成。 血管新生性疾病即指与微血管异常生长有关的疾病,表现为血管生成的过度与缺陷。自1971年Folkman[7]提出:“三维生长的肿瘤 2mm×2mm×2mm之后是绝对血管生成依赖性”的观点后,血管生成的研究受到了广泛的关注,并取得飞速进步。探讨血管生成发生机理和研制逆转血管生成病变的治疗方法和药物是近年医学研究的热点课题。其中,抑制血管新生(抗病理性血管新生)研究与肿瘤的治疗密切相关;而对促进血管新生(治疗性血管新生)的研究多围绕冠状动脉侧枝循环的治疗展开。冠状动脉粥样硬化和渐进型冠状动脉闭塞常能形成侧枝循
神经生长因子与血管生成的相关性研究进展.
.138? 中国现代医药杂志2009年8月第11卷第8期MMJC,Aug2009.Vol11,No.8 神经生长因子与血管生成的相关性研究进展 于一凡综述孙晋民审校 神经生长因子f nerve growth factor,NGF)作为一种传统 意义上的神经营养因子,具有多方面的作用,它能促进中枢及外周神经系统的 发育与分化.维持神经系统的正常功能,促进神经维的再生,并对神经元有保护作用。有两种膜受体介导NGF的信号,即高亲和性的TrkA受体。和低亲和性的 p75受体。近来研究表明NGF还具有促周围再生神经…和非神经组织12t31的血管生成作用。研究发现NGF不仅可以通过调节血管内皮细胞生长因子(v ascular endothelial growthfactor, VEGF)的表达间接地促进血管形成141,NGF还具有直接促进血管形 成的作用阁。1血管生成的机制 血管生成是新血管形成的主要过程。它在机体胚胎发育中起着重要作用,参与 人体正常的生理活动,而且血管生成也是很多病理情况的重要标志.包括糖尿病和 癌症.在创伤修复、缺血缺氧、慢性炎症和癌症等情况下,原有微血管内皮细胞经
过生芽、迁移、增殖及基质重塑等形成新毛细血管问.血管生成受促血管生成因子和相应受体间的相互作用调节。在新血管形成过程的不同阶段中均有参与。 2 NGF促进血管生成的作用 2.1 NGF与血管内皮细胞的相互作用Tanaka等同研究发 现,大鼠主动脉内皮细胞可产生并释放NGF,从而确认血管内皮细胞是NGF的又一重要来源。Dolle7等【{I用人类主动脉内皮细胞human aorticendothelial cells.HAECs)I羞行全方位迁 移分析.发现NGF刺激了HAECs的迁移,这和血管内皮生长因子vascularendothelialgrowthfaetor,VEGF).基本成纤维 细胞生长因子(basicfibroblast growth factor,bFGn的作用相 似。NGF介导的HAEC迁移可被NC胁kA受体拮抗剂 K252a阻断。而不被VEGF,F1k受体拮抗剂SU一5416阻断,说明了NGF通过TrkA受体直接激活了HAEC迁移,数据还显示HAEC表达p75NTR。此外,有研究显示mGF促进血管内皮增生,提高了胰岛移植的
血小板第四因子抗肿瘤血管生成研究进展
?2948?[22] [23] [24] [25] [26]匡堂筮述!Q塑生!Q旦箜!!鲞笙!!翅丛!ii型塾!!!唑!!!塑:Q堕!Q鲤:!!!:!§,盟!:!! proteinincreasesdoxorubicin sensitivity andnuclearaccumulation anddisruptsitssequestrationinlysosomes[J].MolCancerTher,200r7,6(6):1804.1813. HuhHJ。ParkCJ,JangS,eta1.Prognosticsignificanceofmultidrug resistancegenel(MDRl),muhidrugresistance—relatedprotein(MRP)andlungresistanceprotein(LRP)mRNAexpressionina—cuteleukemia[J].JKoreanMedSci,2006,21(2):253-258. BergerW,Spiegl—KreineckerS,BuchroithnerJ。eta1.Overexpres—sionofthehumanmajorvaultproteininastracyticbraintumorcells[J].InlJCancer.2001,94(3):377-382. BergerW,ElbtingL,MickscheM.ExpressionofthemajorvaultproteinLRPinhumannon—small—celllungcancercells:activationbyshort—termexposaretoantineoplasticdrugs[J].IntJCancer。2000,88(2):293-300. SteinU,BergmannS,sche艉rGL,eta1.YB—lfacilitatesbasaland5-fluorouraeil-inducihleexpressionofthehumanmajorvaultpro-tein(MVP)gene[J].Oncogene,2005,24(22):3606-3618. 1kutaK,TakemuraK,SasakiK,eta1.Expressionofmuhidrugre- sistaneeproteinsandaccumulationofcisplatininhumannon—smallcelllung cancercells[J].BiolPharmBull,2005,28(4):707-712.[271I(jtazonoM,Sumiz.awaT,TakebayashiY,da/.Muhidrugresistanceandthelungresistance—relatedproteininhumancoloncarcinoma SW-620cellslJ1.JNatlCancerlnst,1999。91(19):1647-1653.[28】LewinJM,LwaleedBA,CooperAJ,eta1.Thedirecteffectofnacle— arporesoilnuclearchemotherapeuticconcentrationinmuhidrug resistantbladdercancer:thenuclearsparingphenomenonJ】.J Urol。2007.177(4):1526一1530. [29】YasunamiT,WangYH,TsujiK,eta1.Multidrugresistanceprotein expressionofaduhT-cellleukemia/lymphoma【J1.kukRes, 2007.31(4):465-470. [30]樊娟,周慧,张丽,等.急性白JlIL病细胞肺耐药相关蛋白的表达及其临床意义[J].中华肿瘤防治杂志,2007,14(19): 1477-1479. [31]KourtiM,VavatsiN,GombakisN,eta1.Expressionofmultidrug resistance1(MDRI),multidrugresistance—relatedprotein1 (MRPI),lungresistanceprotein(LRP),andbreastcancerre? sistanceprotein(BCRP)genesandclinicaloutcomeinchild— hoodacutelymphoblasticleukemia[J].IntJHematol,2007, 86(2):166-173. 收稿日期:2009-03-30修回日期:2009-07-10 血小板第四因子抗肿瘤血管生成研究进展 张华1△(综述),任宏轩h,伍治平2(审校) (1.云南省肿瘤医院内二科,昆明650018;2.云南省肿瘤研究所,昆明650018) 中图分类号:R730.5文献标识码:A文章编号:1006-2084(2009)19-2948-03 摘要:血小板因子4是由活化的血小板ot颗粒分泌的趋化因子,属于CXC4家族,具有抗肿瘤血管生成的活性,属于内源性的血管生成抑制因子。其可以通过多种机制抑制肿瘤的血管生成,如抑制血管内皮细胞生长园子、碱性成纤维细胞生长园子介导的血管内皮的增殖;削弱p21的下调,抑制内皮细胞分裂、增殖;抑制基质金属蛋白酶的表达,防止新生血管向周围组织的蔓延等。从而有效抑制肿瘤的新生血管形成。 关键词:血小板因子4;肿瘤血管生成;抗血管生成 ResearchProgressinAnti—tulnorAngiogenesisofPlateletFactor.4Z托4NGHual.兄FNHong.z“Ⅱ,l‘.删Zhi-pin92.(1.DepartmentofInternalMedicine,ynn,zⅡnProvinceTumorHospital。Kunmin9650018,傩i—w;2.CancerResearchInstituteofy“n№n,Kunming650018.吼ina) Abstract:Plateletfactor-4isachemokinereleasedbytheactivatedplateletintheplasma.whichisin.dexedintheCX(=4 superfamily.It hasanti?angiogenesisactivity.istheantiangiogenesisinvivo.ThrotIghavarietyofmechanisms,plateletfactor-4caninhibittumorangiogenesis.SU(-hasinhihitingVECF。bFGF-medi.atedproliferationofvascularendothelial.weakenthedownwardofp21.inhibitedendothelialeelldivisionandproliferation;inhibitingtheexpressionofmatrixmetalloproteinases.topreventneovascularizationspreada.roundtheorganizatinnsoastoeffectivelyinhibittumorangiogenesis. Keywords:Plateletfactor-4;Angiogenasis;Anti—angiogenesis 目前恶性肿瘤已成为威胁人类健康最严重的一 类疾病,肿瘤的发病率和病死率都日益增高。临床 上绝大多数的肿瘤患者死于肿瘤的远处转移。血管 生成在肿瘤转移中起到了非常重要的作用。同时也 是肿瘤转移的必需条件…。血小板因子4(platelet factor-4,PF4)属于内源性血管生成抑制因子,它可以 通过多种机制抑制肿瘤的血管生成,是近几年研究 的热点[23。 1PF4及其生物学活性 早在1948年,Conley就发现血小板减少患者对肝素的敏感性异常增加,从而推测血小板可能释放某种具有中和肝素抗凝活性的因子,此后被其他学者陆续证实,并部分纯化了这种血小板蛋白,并命名为PF4。因其有中和肝素的作用又称其为肝素结合蛋白或抗肝素因子。PF4是由巨核细胞合成的,生理状态下存在于巨核细胞及血小板at颗粒致密体中,在血小板黏附、聚集等 活化状态下以高分子质量蛋白多糖一PF4复合物的形 式释放。因此,它可以作为巨核细胞分化成熟以及 血小板活化的一种标志物∞J,但是最近研究显示单 核.巨噬细胞在细菌、真菌、脂多糖、酵母多糖及血小 板碱性蛋白等的刺激下也可以分泌PF4HJ。酶联免 疫吸附法测定其在正常人血浆中的浓度为0.9 ~5.5斗g/LⅢ。 PF4属于人趋化因子超家族C.x—C亚族,含有 70个氨基酸,由4个单体组成,每个单体相对分子质 量为7.8×103,单体是N端的可变区通过二硫键锚万方数据
抑制血管生成与肿瘤治疗
抑制血管生成与肿瘤治疗 肿瘤的生长是血管生成依赖性的,通过抑制肿瘤血管的生成应该可以达到抑制肿瘤生长和转移的目的。肿瘤血管的生成是一个多步骤的过程,阻断其中任何一步,都将可能阻止肿瘤血管生成,因此肿瘤的血管系统己成为一个崭新的抗肿瘤治疗靶点。如抑制促血管生成因子与相应受体结合,阻断信号传导通路,抑制内皮细胞的生长;抑制降解基底膜的酶的活性,组织内皮细胞向外移动形成细胞索,抑制血管形成;抑制破坏茹附分子,使内皮细胞无法与基底膜乳附,抑制形成管腔等,这些手段均可有效阻断血管的生成。肿瘤血管生成抑制剂作用于肿瘤内皮细胞,阻止其增殖、迁移、出芽及形成新生血管,并诱导不成熟内皮细胞趋向凋亡,抑制肿瘤生成和转移,具有良好的特异性和针对性。近年来,这类抑制剂的研究已取得新的进展,有望成为抗肿瘤治疗的新方法。虽然到目前为止,还没有一种抗血管生成的药物能够单独消退肿瘤,但这些药物能够延缓肿瘤生长进程,使其更加稳定,而且和别的抗肿瘤药物合用,有明显的协同作用。 一、血管内皮生长因子与肿瘤治疗 由于VEGF是目前发现的诱导肿瘤血管形成作用最强和最具特异性的生长因子,故VEGF/VEGFR信号转导通路被认为是最有前途
的靶点。而大量的研究结果也表明,抑制VEGF的表达或者活性在动物以及人类肿瘤中均能取得直接迅速的抗血管生成的作用。 对目前正在进行临床前期研究以及临床试验的VEGF药物,根据其作用靶点的部位不同分为以下几类:①针对内源性VEGF的抗体,如bevacizumab ( BV ).BV 是一种人工合成的VEGF单抗,2004年被美国食品药物管理局批准与5-氟尿啼陡合用作为转移性结直肠癌的一线用药。除了结直肠癌,BV在治疗转移性乳腺癌、进展型或转移性非小细胞型肺癌等应用中也取得了一定的疗效。研究者认为,BV 主要是通过抑制新生血管生成,阻断肿瘤血供,进而诱导肿瘤细胞凋亡,并认为这样的治疗效果更加符合生理性细胞的死亡过程,减少了传统化疗药物的毒副作用。②针对血管内皮生长因子受体(VEGFR)并与之相结合的小分子VEGF抑制物,这类药物能竞争性地与VEGFR相结合,并阻断VEGF信号转导。如BA Y43一9006,SU541fi, SLi11248, PTK787/K222;i84等。BAY43一9006已干2005年被美国食品药物管理局批准应用于进展型肾癌等。SU5416是一种新合成的VEGF受体VEGFR一2酩氨酸激酶抑制物,可明显抑制肿瘤血管生成,阻断其血供,进而诱导肿瘤细胞凋亡,使肿瘤从大到小处于休眠状态,目前川期临床试验正在进行中。③可溶性VEGF受体类似物,如VEGF Trapo VEGF Trap,是由VEGFRI,VEGFR2的胞外段与人Y 免疫球蛋白Fc段融合产生的蛋白,其与VEGF有极强的结合能力,并抑制其活性,目前已经应用于多种实体癌和淋巴瘤的I期实验研究。
