大学有机化学第五版天津大学版5第五章教学要点和复习
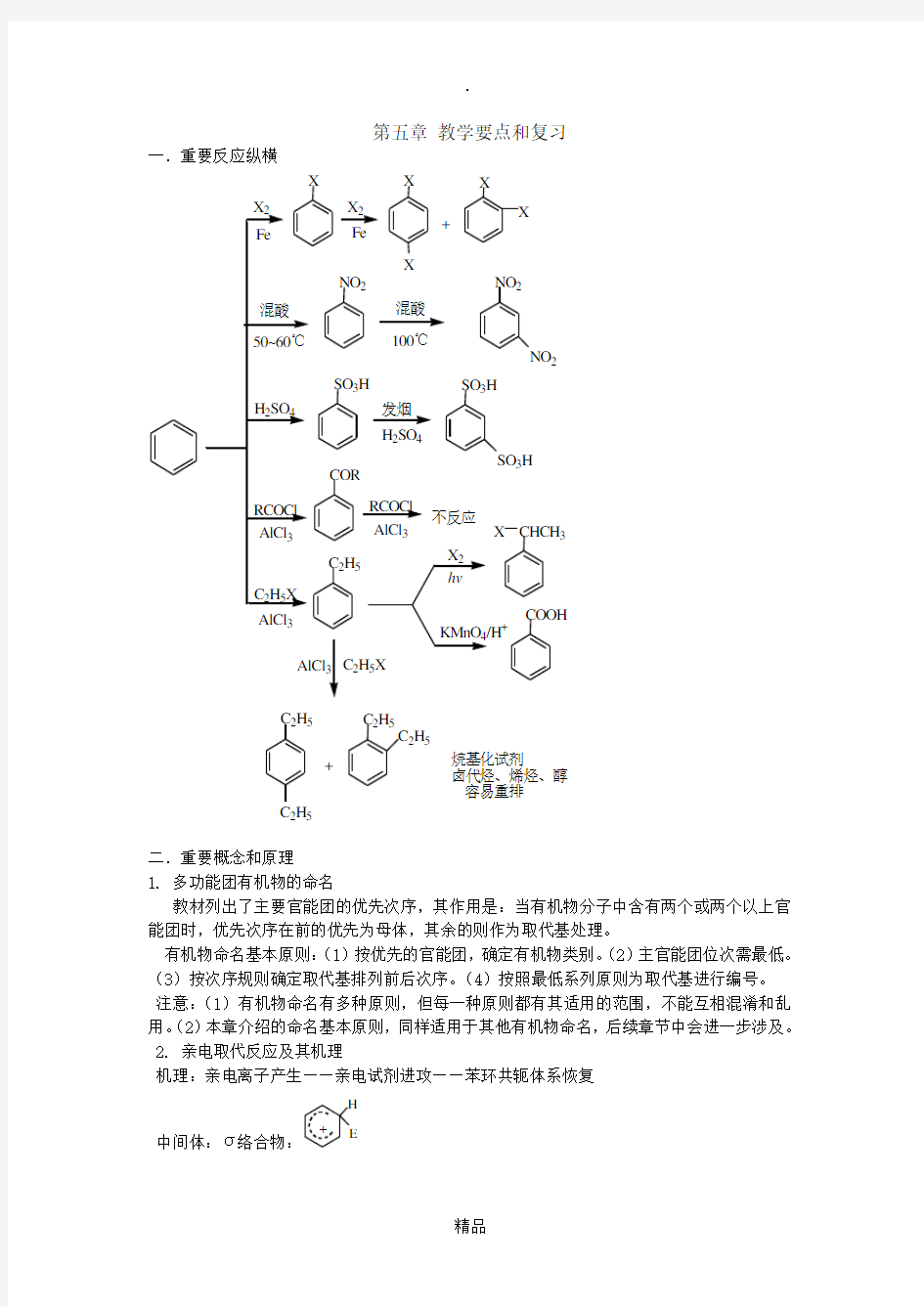

第五章教学要点和复习一.重要反应纵横
+
C2H5C2H5 C2H5C2H5
3
烷基化试剂
卤代烃、烯烃、醇
容易重排
二.重要概念和原理
1. 多功能团有机物的命名
教材列出了主要官能团的优先次序,其作用是:当有机物分子中含有两个或两个以上官能团时,优先次序在前的优先为母体,其余的则作为取代基处理。
有机物命名基本原则:(1)按优先的官能团,确定有机物类别。(2)主官能团位次需最低。(3)按次序规则确定取代基排列前后次序。(4)按照最低系列原则为取代基进行编号。
注意:(1)有机物命名有多种原则,但每一种原则都有其适用的范围,不能互相混淆和乱用。(2)本章介绍的命名基本原则,同样适用于其他有机物命名,后续章节中会进一步涉及。
2. 亲电取代反应及其机理
机理:亲电离子产生——亲电试剂进攻——苯环共轭体系恢复
中间体:σ络合物:
H
E +
理解:(1)环状碳正离子,但很难说E +从某一个碳原子上得到π电子。
(2)可看作亲电加成产物产物,但不会停留于此:σ络合物失去质子可以恢复为稳定的苯环结构。
3. 苯取代定位规律及其解释
本章重点和难点,教材以共振论结合电子效应解释。教学中主要以电子效应进行解释。 理解:(1)苯环上的取代基,改变了苯环上电子云密度分布。(2)供电子取代基,苯环上电子云密度分布提高,且邻对位上提高更多;吸电子取代基,苯环上电子云密度分布降低,但间位上降低较少。(3)诱导和共轭效应均有供和吸电子两类,效应不一样的主要是卤素(吸电子诱导和供电子共轭)
4. 芳香性及其判断
原则:体系平面(碳杂化为SP 2),π电子符合:4n+2
注意:π电子计算:碳碳双键每一个碳1个,碳正离子0个,碳负离子2个
三.重要考点示范
1. 下列亲电取代反应速率由快到慢的顺序为 。 (A) NO 2 (B) CH 3 (C) OCH 3 (D)
答案: (C) (B) (D) (A)
注意:亲电取代反应的速率主要与苯环上电子云密度有关,第一类定位基,且定位效应越强,则亲电取代反应速率越快。
2. 写出下列反应主要产物: 3)3CH 2CH 3
NBS
答案:3)3CHCH 3
Br
注意:(1)NBS 是自由基反应中常用的溴源,自由基取代和自由基加成反应均可以用NBS 发生溴自由基。
(2)苯环侧链α-H 优先发生自由基取代。
3. 写出下列反应主要产物:
CH 2CH 3O CH 3O
CH CH 2
3 答案:CH 3O
CH 3O O 2
注意:分子内的F-K 酰基化反应,优先发生在电子云密度大的苯环上。
4. 写出:C CH 2O
一次硝化的主要产物 答案:C CH 2O NO 2 C
CH 2O
NO 2
注意:(1)苯环上电子云密度越大,越容易进行亲电取代反应。(2)化合物左边苯环与吸电子羰基相连,右边苯环与供电子亚甲基相连,因此亲电取代反应应发生在右边苯环上。(3
)由于空间效应的影响,邻位取代产物可能教少。
5. 下列分子或离子中,具有芳香性的是 :
(A
答案:(D )
如有侵权请联系告知删除,感谢你们的配合!
有机化学_第五版答案(完整版)
《有机化学》(第五版,李景宁主编)习题答案 第一章 3、指出下列各化合物所含官能团的名称。 (1) CH 3CH=CHCH 3 答:碳碳双键 (2) CH 3CH 2Cl 答:卤素(氯) (3) CH 3CHCH 3 OH 答:羟基 (4) CH 3CH 2 C=O 答:羰基 (醛基) H (5) CH 3CCH 3 答:羰基 (酮基) (6) CH 3CH 2COOH 答:羧基 (7) NH 2 答:氨基 (8) CH 3-C ≡C-CH 3 答:碳碳叁键 4、根据电负性数据,用和标明下列键或分子中带部分正电荷和负电荷的原子。 答: 6、下列各化合物哪个有偶极矩?画出其方向 (1)Br 2 (2) CH 2Cl 2 (3)HI (4) CHCl 3 (5)CH 3OH (6)CH 3OCH 3 答:以上化合物中(2)、(3)、(4)、(5)、(6)均有偶极矩 (2) H 2C Cl (3 )I (4 ) Cl 3 (5)H 3C OH (6) H 3C CH 3 7、一种化合物,在燃烧分析中发现含有84%的碳[Ar (C )=12.0]和16的氢[Ar (H )=1.0],这个化合物的分子式可能是
(1)CH 4O (2)C 6H 14O 2 (3)C 7H 16 (4)C 6H 10 (5)C 14H 22 答:根据分析结果,化合物中没有氧元素,因而不可能是化合物(1)和(2); 在化合物(3)、(4)、(5)中根据碳、氢的比例计算(计算略)可判断这个化合物的分子式可能是(3)。 第二章 习题解答 1、用系统命名法命名下列化合物 (1)2,5-二甲基-3-乙基己烷 (3)3,4,4,6-四甲基辛烷 (5)3,3,6,7-四甲基癸烷 (6)4-甲基-3,3-二乙基-5-异丙基辛烷 2、写出下列化合物的构造式和键线式,并用系统命名法命名之。 (3)仅含有伯氢和仲氢的C 5H 12 答:符合条件的构造式为CH 3CH 2CH 2CH 2CH 3; 键线式为; 命名:戊烷。 3、写出下令化合物的构造简式 (2)由一个丁基和一个异丙基组成的烷烃 (4) 相对分子质量为100,同时含有伯、叔、季碳原子的烷烃 答:该烷烃的分子式为C 7H 16。由此可以推测同时含有伯、叔、季碳原子的烷烃的构造式为(CH 3)3CCH(CH 3)2 (6) 2,2,5-trimethyl-4-propylnonane (2,2,5-三甲基-4-丙基壬烷) CH 3CH 2CH 2CH 2CHCHCH 2CCH 3 CH 3 CH 3CH 3 nC 3H 7
(完整版)无机化学(天津大学第四版答案)
第1章 化学反应中的质量关系和能量关系 习题参考答案 1.解:1.00吨氨气可制取2.47吨硝酸。 2.解:氯气质量为2.9×103g 。 3.解:一瓶氧气可用天数 33111-1 222()(13.210-1.0110)kPa 32L 9.6d 101.325kPa 400L d n p p V n p V -???===?? 4.解:pV MpV T nR mR = = = 318 K 44.9=℃ 5.解:根据道尔顿分压定律 i i n p p n = p (N 2) = 7.6?104 Pa p (O 2) = 2.0?104 Pa p (Ar) =1?103 Pa 6.解:(1)2(CO )n = 0.114mol; 2(CO )p = 42.87 10 Pa ? (2)222(N )(O )(CO )p p p p =--43.7910Pa =? (3)4224(O )(CO ) 2.6710Pa 0.2869.3310Pa n p n p ?===? 7.解:(1)p (H 2) =95.43 kPa (2)m (H 2) = pVM RT = 0.194 g 8.解:(1)ξ = 5.0 mol (2)ξ = 2.5 mol 结论: 反应进度(ξ)的值与选用反应式中的哪个物质的量的变化来进行计算无关,但与反应式的写法有关。 9.解:?U = Q p - p ?V = 0.771 kJ 10.解: (1)V 1 = 38.3?10-3 m 3= 38.3L (2) T 2 = nR pV 2 = 320 K (3)-W = - (-p ?V ) = -502 J (4) ?U = Q + W = -758 J (5) ?H = Q p = -1260 J
2015年天津大学无机化学期中试卷
无机化学期中试卷 2015.11.17 班级 姓名 学号 分数 一、 选择题 ( 共10题 20分 ) 1. 2 分 (3778) 3778 对于一个氧化还原反应,下列各组中所表示的 m r G ?, E 和K 的关系应 是…………………………………………………………………………………………… ( ) (A) m r G ?>0; E <0;K <1 (B) m r G ?>0; E >0;K >1 (C) m r G ?<0; E <0;K >1 (D) m r G ?<0; E >0;K <1 2. 2 分 (0438) 0438 关于熵,下列叙述中正确的是…………………………………………………………( ) (A) 298K 时,纯物质的 m S = 0 (B) 一切单质的 m S = 0 (C) 对孤立体系而言, m r S ?> 0的反应总是自发进行的 (D) 在一个反应过程中,随着生成物的增加,熵变增大 3. 2 分 (3515)
25℃,2NO 2(g)N 2O 4(g),K c 与K p ( K )的比值( p = 100 kPa )K c /K p 等于… ( ) (A) 298 0831.01 ?= 0.0404 (B) 8.31 ? 25 = 207.8 (C) 0.0831 ? 298 = 24.8 (D) 0.0821 ? 298 = 24.5 4. 2 分 (3871) 3871 HI 的生成反应的焓变为负值,HI 的分解反应的焓变为正值,则HI 分解反应的活化能 E a ……………………………………………………………………………………………( ) (A) E a <ΔH 分解 (B) E a >ΔH 分解 (C) E a = 0 (D) E a =ΔH 分解 5. 2 分 (6709) 6709 常用的三种甘汞电极,即 (1) 饱和甘汞电极 (2) 摩尔甘汞电极 (3) 0.1 mol ·dm -3 甘汞电极 其电极反应为:Hg 2Cl 2(s) + 2e - = 2Hg(l) + 2Cl - (aq),在25℃ 时三种甘汞电极的 ?的大小次序为………………………………………………………………………………… ( ) (A) 1?> 2?> 3? (B) 2?> 1?> 3? (C) 3?> 2?> 1? (D) 1?= 2?= 3? 6. 2 分 (0436)
Removed_有机化学(第五版)下册课后答案 李景宁
第十二章羧酸(P32-33) 1.命名下列化合物或写出结构式: (1) 3-甲基丁酸 (2) 3-对氯苯基丁酸(3) 间苯二甲酸 (4) 9,12-十八碳二烯酸 (5) 4-甲基己酸CH3CH2CH(CH3)CH2CH2COOH (6) 2-羟基丁二酸HOOCCH(OH)CH2COOH (7) 2-氯-4-甲基苯甲酸 (8) 3,3,5-三甲基辛酸 2.试以反应式表示乙酸与下列试剂的反应 3.区别下列各组化合物:
4.指出下列反应的主要产物:(第四版保留) 4.完成下列转变: 5、怎样由丁酸制备下列化合物?
6、解: 7、指出下列反应中的酸和碱。 按lewis酸碱理论:凡可接受电子对的分子、离子或基团称为酸,凡可给予电子对的分子、离子或基团成为碱。 8.(1)按酸性降低的次序排列下列化合物: ①酸性: 水>乙炔>氨; ②酸性: 乙酸>环戊二烯>乙醇>乙炔 (2)按碱性降低的次序排列下列离子: >> ①碱性:CH3HC C CH3O ②碱性:(CH3)3CO>(CH3)2CHO>CH3O 9. 解:化合物A有一个不饱和度,而其氧化产物B含有两个不饱和度。产物DC5H10有一个不饱和度。从题意可知:D的结构式可能为环戊烷;C的结构为环戊酮;B的结构为己二酸;A的结构式为环己醇。 10.解:
(1)由题意:该烃氧化成酸后,碳原子数不变,故为环烯烃,通式为CnH2n-2。 (2)该烃有旋光性,氧化后成二元酸,所以分子量=66*2=132。故二元酸为CH3CH(CH2COOH)COOH 11.由题意:m/e=179,所以马尿酸的分子量为179,它易水解得化合物D和E,D 的IR谱图:3200-2300cm-1为羟基中O-H键的伸缩振动。1680为共扼羧酸的>C=O的伸缩振动;1600-1500cm-1是由二聚体的O-H键的面内弯曲振动和C-O 键的伸缩振动之间偶合产生的两个吸收带;750cm -1和700cm-1是一取代苯的C-H键的面外弯曲振动。再由化学性质知D为羟酸,其中和当量为 121±1,故D的分子量为122,因此,又由题意:E为氨基酸,分子量为75,所以E的结构为H2NCH2COOH。 第十三章羧酸衍生物(P77-78) 1.说明下列名词: 酯、油脂、皂化值、干性油、碘值、非离子型洗涤剂。 酯:是羧酸分子和醇分子间脱水形成的产物。 油脂:是高级脂肪酸的甘油醇酯。 皂化值:是指完全皂化1克油脂所需的KOH的质量(以mg为单位)。 干性油:是指那些在空气中放置后能逐渐变成有韧性的固态薄膜的油。 碘值:是指100克油脂完全加成时所能吸收的碘的质量(以克为单位)。 非离子型洗涤剂:此处实指非离子型表面活性剂,即在水溶液中不离解出正负离子的表面活性剂(此处的非离子型表面活性剂起主要的洗涤去污作用)。 2.试用方程式表示下列化合物的合成路线: (1)由氯丙烷合成丁酰胺;
天津大学无机化学教研室《无机化学》复习全书(分子的结构与性质)
第6章分子的结构与性质 6.1 复习笔记 一、键参数 1.键能 (1)定义 键能是指气体分子每断裂单位物质的量的某键(6.022×1023个化学键)时的焓变。(2)特性 ①键能可作为衡量化学键牢固程度的键参数,键能越大,键越牢固; ②对双原子分子,键能在数值上等于键解离能(D); ③多原子分子中若某键不止一个,则该键键能为同种键逐级解离能的平均值; ④可通过光谱实验测定键解离能以确定键能,还可利用生成焓计算键能。 2.键长(L b) (1)定义 键长是指分子内成键两原子核间的平衡距离。一些双原子分子的键长如表6-1所示: 表6-1 一些双原子分子的键长
(2)特性 ①一个键的性质主要取决于成键原子的本性; ②两个确定的原子之间,如果形成不同的化学键,其键长越短,键能就越大,键就越牢固。 ③键长可以用分子光谱或X射线衍射方法测得。 3.键角 (1)定义 键角是指在分子中两个相邻化学键之间的夹角。 (2)特性 ①键角可以用分子光谱或X射线衍射法测得; ②可以通过分子内全部化学键的键长和键角数据来确定这个分子的几何构型。 二、价键理论 1.共价键 (1)共价键的形成 共价键是指原子间由于成键电子的原子轨道重叠而形成的化学键。 (2)价键理论要点 ①两原子接近时,自旋方向相反的未成对的价电子可以配对,形成共价键; ②成键电子的原子轨道如能重叠越多,则所形成的共价键就越牢固(最大重叠原理)。 (3)共价键的特征 ①共价键具有饱和性; ②共价键具有方向性。
(4)原子轨道的重叠 ①两个原子轨道以对称性相同的部分相重叠(正重叠) 图6-1所示为原子轨道几种正重叠的示意图。 (a)s-s (b)p x-s (c)p y-p y(d)d xy-p y 图6-1 原子轨道几种正重叠示意图 ②两个原子轨道以对称性不同部分相重叠(负重叠) 图6-2所示为原子轨道几种负重叠的示意图。 (a)p x-p y(b)p x-s (c)p y-p y(d)p x-d xy 图6-2 原子轨道几种负重叠示意图 (5)共价键的类型 ①按是否有极性来分类: ②按原子轨道重叠部分的对称性来分类: a.键 若原子轨道的重叠部分,对键轴(两原子的核间连线)具有圆柱形对称性,所形成的键称为键。图6-3给出了几种不同组合形成的键示意图。
天津大学制药工程专业卓越工程师培养方案
制药工程专业卓越工程师培养计划 2011年11月
天津大学制药工程专业卓越工程师 培养计划学校培养标准 一、总体要求 本培养标准在国家通用标准的指导下,按照行业专业标准的基本要求,结合天津大学特色、办学理念和人才培养定位,制定本校制药工程专业的卓越工程师培养标准。天津大学制药工程专业将按照此标准培养学生,突出“创新性、重实践、国际化”特色,培养基础宽、素质高、具有创新精神和实践能力强的制药工程师,使学生具备较强的综合素质、能力和知识。 二、专业特征目标 培养适应社会主义现代化建设需要的,德智体美等全面发展的,具备制药工程方面的知识和设计研究能力的基础宽、素质高、具有创新精神和实践能力强的制药工程师。具体的专业特征目标包括: 1. 个人综合素质培养 1.1 积极乐观与理性思维的人生态度 积极乐观与理性思维的人生态度 1.2 探究真理百折不挠的毅力 实事求是、探求真理的毅力 克服困难的顽强意志 1.3 很强的自制力 自制力,为人处事,遵纪守法 组织纪律观念,遵从自然规律,培养科学精神
1.4 成就宏伟事业的自信心 认识历史发展规律,树立远大理想 认识学科发展前沿,树立在科学领域做出突出成果的勇气和决心1.5 诚实守信严谨求真的职业道德 诚实守信的人生态度 严谨求真的科学态度和职业道德 增强严谨求真的职业素养 1.6 敬业精神、社会责任感和工作责任心 爱岗敬业、踏实肯干的职业素养 增强社会责任感 1.7 包容心与团队精神 包容心,增强团队意识 增强学生的合作和团队意识 加强集体观念、团队精神熏陶 1.8 爱国奉献精神与谋求人类福祉的志向 爱国奉献精神,以谋求人类福祉为远大志向 1.9 优良的身体素质 加强学生的身体素质训练 养成良好的生活工作习惯,增强学生的身体素质 2. 个人能力培养 2.1 善于学习,独立获取知识的能力 自主学习、独立获取知识能力 2.2 分析问题能力 分析问题能力 2.3 计划与综合能力 规划、设计和综合能力
有机化学第五版下册课后答案 李景宁
) 羧酸(P第十二章32-33: 1.命名下列化合物或写出结构式 (2) 3-对氯苯基丁酸甲基丁酸(1) 3-十八碳二烯酸12-(3) 间苯二甲酸 (4) 9,CH(5) 4-甲基己酸CHCH(CH)CHCHCOOH22332COOH (6) 2-羟基丁二酸 HOOCCH(OH)CH2 甲基苯甲酸(7) 2-氯-4- (8) 3,3,5-三 甲基辛酸 2.试以反应式表示乙酸与下列试剂的反应 : 3.区别下列各组化合物
(第四版保留)4.指出下列反应的主要产物: (1) CO干醚2MgClCHCH ClHCCH(1)265(2) HO2562MgSOCl2CHCHCOOHCHCHCOCl256265 4.完成下列转变: 、怎样由丁酸制备下列化合物?
5. :6、解 、指出下列反应中的酸和碱。7酸碱理论:凡可接受电子对的分子、离子或基团称为酸,凡可给予电子lewis按对的分子、离子或基团成为碱。 : )按酸性降低的次序排列下列化合物8.(1 ; 乙炔>氨①酸性: 水> 乙炔乙醇>: 乙酸>环戊二烯>酸性②: )按碱性降低的次序排列下列离子(2>OHCCHCH>C:①碱性33CHO(CH)OCHCO(CH>)>23② :碱性3339. 解:化合物A有一个不饱和度,而其氧化产物B含有两个不饱和度。产物DCH有一个不饱和度。从题意可知:D的结构式可能为环戊烷;C的结构为105环戊酮;B的结构为己二酸;A的结构式为环己醇。 .解:10. (1)由题意:该烃氧化成酸后,碳原子数不变,故为环烯烃,通式为CnH2n-2。。故二元酸为(2)该烃有旋光性,氧化后成二元酸,所以分子量 =66*2=132CH3CH(CH2COOH)COOH ,,它易水解得化合物D和E11.由题意:m/e=179,所以马尿酸的分子量为179-1>1680为共扼羧酸的D 的IR谱图:3200-2300cm为羟基中O-H键的伸缩振动。 -1键C-O O-HC=O的伸缩振动;1600-1500cm键的面内弯曲振动和是由二聚体的-1-1C-H的伸缩振动之间偶合产生的两个吸收带;750cm 是一取代苯的和700cm 分1其中和当量为121±,故D的键的面外弯曲振动。再由化学性质知D为羟 酸,又由题意:E为氨基酸,分子量为75,因此,,122子
天津大学无机化学第一章__思考题
第一章思考题 1.一气柜如下图所示: A 假设隔板(A)两侧N2和CO2的T, P相同。试问: (1)隔板两边气体的质量是否相等? 浓度是否相等?物质的量不等而浓度相等 (2)抽掉隔板(假设不影响气体的体积和气柜的密闭性)后,气柜内的T和P 会改变?N2、CO2物质的量和浓度是否会改变?T和P 会不变,N2、CO2物质的量不变而浓度会改变 2.标准状况与标准态有何不同? 标准状况指气体在27.315K和101325Pa下的理想气体,标准态是在标准压力下(100kPa)的纯气体、纯液体或纯固体 3.化学反应方程式的系数与化学计量数有何不同?对某一化学反应方程式来说,化学反应方程式的系数和化学计量数的绝对值相同,但化学反应方程式的系数为正值,而反应物的化学计量数为负值,生成物的化学计量数为正值 4.热力学能、热量、温度三者概念是否相同? 试说明之。 5.试用实例说明热和功都不是状态函数。
6.判断下列各说法是否正确: (1)热的物体比冷的物体含有更多的热量。× (2)甲物体的温度比乙物体高,表明甲物体的热力学能比乙物体大。× (3)物体的温度越高,则所含热量越多。× (4)热是一种传递中的能量。√ (5)同一体系: (a)同一状态可能有多个热力学能值。× (b)不同状态可能有相同的热力学能值。√ 7.判断下列各过程中,那个ΔU最大: (1)体系放出了60kJ热,并对环境做了40kJ功。 (2)体系吸收了60kJ热,环境对体系做了40kJ功。√ (3)体系吸收了40kJ热,并对环境做了60kJ功。 (4)体系放出了40kJ热,环境对体系做了60kJ功。 根据ΔU=Q+W, (1) ΔU=-60+(-40)=-100KJ (2) ΔU=+60+40=+100KJ ,(3) ΔU=+40+(-60)=-20KJ (4) ΔU=-40+60=+20KJ因此通过计算可以看出,(2)过程的ΔU最大. 8.下列各说法是否正确: (1)体系的焓等于恒压反应热。× (2)体系的焓等于体系的热量。× (3)体系的焓变等于恒压反应热。√
最新-天津大学无机化学第五版习题答案 精品
第1章 化学反应中的质量关系和能量关系 习题参考答案 1.解:1.00吨氨气可制取2.47吨硝酸。 2.解:氯气质量为2.9×103 g 。 3.解:一瓶氧气可用天数 33111-1 222()(13.210-1.0110)kPa 32L 9.6d 101.325kPa 400L d n p p V -???= ==?? 4.解:pV MpV T nR mR = = = 318 K 44.9=℃ 5.解:根据道尔顿分压定律 i i n p p n = p (N 2) = 7.6?104 Pa p (O 2) = 2.0?104 Pa p (Ar) =1?103 Pa 6.解:(1)2(CO )n = 0.114mol; 2(CO )p = 42.87 10 Pa ? (2)222(N )(O )(CO )p p p p =--43.7910Pa =? (3) 4224(O )(CO ) 2.6710Pa 0.2869.3310Pa n p n p ?===? 7.解:(1)p (H 2) =95.43 kPa (2)m (H 2) = pVM RT = 0.194 g 8.解:(1)ξ = 5.0 mol (2)ξ = 2.5 mol 结论: 反应进度(ξ)的值与选用反应式中的哪个物质的量的变化来进行计算无关,但与反应式的写法有关。 9.解:?U = Q p - p ?V = 0.771 kJ 10.解: (1)V 1 = 38.3?10-3 m 3 = 38.3L (2) T 2 = nR pV 2 = 320 K (3)-W = - (-p ?V ) = -502 J (4) ?U = Q + W = -758 J (5) ?H = Q p = -1260 J 11.解:NH 3(g) + 45O 2(g) 298.15K ????→标准态 NO(g) + 2 3H 2O(g) m r H ?= - 226.2 kJ ·mol -1 12.解:m r H ?= Q p = -89.5 kJ m r U ?= m r H ?- ?nRT = -96.9 kJ 13.解:(1)C (s) + O 2 (g) → CO 2 (g)
大学无机化学期末考试(天津大学第四版)归纳.doc
第一章 化学反应中的质量和能量关系 重要概念 1.系统:客观世界是有多种物质构成的,但我们可能只研究其中一种或若干物质。人为地将一部分物质与其他物质分开,被划分的研究对象称为系统。 2.相:系统中具有相同物理性质和化学性质的均匀部分称为相。 3.状态:是指用来描述系统的诸如压力P 、体积V 、温度T 、质量m 和组成等各种宏观性质的综合表现。 4.状态函数:用来描述系统状态的物理量称为状态函数。 5.广度性质:具有加和性,如体积,热容,质量,熵,焓和热力学能等。 6.强度性质:不具有加和性,仅决定于系统本身的性质。如温度与压力,密度等。 系统的某种广度性质除以物质的量或者质量之后就成为强度性质。强度性质不必指定物质的量就可以确定。 7.热力学可逆过程:系统经过某种过程由状态1到状态2之后,当系统沿着该过程的逆过程回到原来状态时,若原来的过程对环境产生的一切影响同时被消除(即环境也同时复原),这种理想化的过程称为热力学的可逆过程。 8.实际过程都是不可逆的,可逆过程是一种理想过程。 9.化学计量数:0=∑B VB B表示反应中物质的化学式,VB是B 的化学计量数, 量纲为一;对反应物取负值,生成物取正值。 10.化学计量数只表示当安计量反应式反应时各物质转化的比例数,并不是各反应物质在反应过程中世界所转化的量。 11.反应进度ξ:b b v /n ?=?ξ 对于化学反应来讲,一般选未反应时,0=ξ 引入反应进度这个量最大的优点是在反应进行到任意时刻时,可用任一反应物或产物来表示反反应进行的程度,所得的值总是相等的。 12.习惯对不注明温度和压力的反应,皆指反应是在298.15K ,100kPa 下进行的。 13.一般没有特别的注明,实测的反应热(精确)均指定容反应热,而反应热均指定压反应热。 14.能量守恒定律:在任何过程中,能量不会自生自灭,只能从一种形式转化为另一种形式,在转化过程中能量的总值不变。也叫做热力学第一定律。ΔU=Q+W 15.热力学能具有状态函数的特点:状态一定,其值一定。殊途同归,值变相等。周而复始,值变为零。 16.系统与环境之间由于存在温差而交换的热量称为热。若系统吸热值为正,若系统放热值为负。 17.系统与环境之间除了热以外其他形式传递的能量都称为功。系统得功为正,系统做功为负。在一定条件下由于系统体积的变化而与环境交换的功称为体积功?-=pdV W ,除体积功以外的一切功称为非体积功如电功。 18.功和热都是过程中被传递的能量,它们都不是状态函数,其数值与途径有关。而热力学第一定律中的热力学能的改变量只有过程的始态和终态决定,而与过程的具体途径无关。 19.化学反应热是指等温过程热,即当系统发生了变化后,使反应产物的温度回到反应前始态的温度,系统放出或吸收的热量。
天津大学349药学综合考研红宝卷
天津大学349药学综合考研红宝卷 考研冲刺阶段是考研的攻坚期,在短时间内查漏补缺、实地演练成为制胜的关键。历年考研真题是考研冲刺阶段复习的不二法宝,但是大多数研友在前期已经看过真题,再做真题已经起不到实战的效果,而市面上的各种习题集和模拟卷又不能解决各校侧重点不同的问题。基于此,天津考研网为满足研友需求,特推出《天津大学349药学综合考研红宝卷》。以下复习方法摘自《天津大学349药学综合考研红宝卷》资料部分。 一、备考建议 考研是一场对心理和身体双重考验的战役,要想学好知识打赢这场战役就必须要有充分的准备。天津大学药学院初试成绩主要是由英语、政治、专业课三部分组成。英语、政治满分都是100,专业课满分300分,每场3个小时。 (1)向师兄师姐请教 (2)上网寻找信息 (3)不要做资料帝 天津大学349药学综合考研真题复习宝典 天津大学349药学综合考研红宝书 天津大学349药学综合考研红宝卷 349药学综合是4选2的科目 二、生物化学 参考书目:1. 化学工业出版社的《现代生物化学》,于自然,黄若泰 2. 王镜岩的《生物化学》 复习时间规划:第一次整体看一遍(不要看考纲),一边看一边做习题集, 第二次按考纲总结,做真题; 第三遍,只看重点+补充部分就行了。 1.初次复习阶段(7月-9月)
2.强化复习阶段(10月-11月) 3. 巩固复习阶段(12月-考试) 真题题型:选择、填空、名词、简答、论述。 考题特点:考的面比较广,题目出的比较大 真题举例:例如:10年真题 比较DNA RNA的区别(化学结构上、功能上) 三、生物学: 参考书目: 胡玉佳主编的《现代生物学》 细胞生物学+生物化学+植物动物学+免疫学 复习时间规划:第一遍按考纲总结,做笔记 第二遍,做真题,找重点,进行强化记忆 第三遍,背熟重点+补充部分, 1.初次复习阶段(10月-11月) 2.强化复习阶段(11月-12月) 3. 巩固复习阶段(12月-考试) 真题题型:判断、选择、填空、名词、简答、论述。 考题特点:题目比较细致,好好看书,背熟重点 真题举例:例如:10年真题 含氮激素和类固醇激素的作用机制 书上原话,背下来。重点是含氮激素与受体偶联的三种方式和类固醇激素以复合物形式进入细胞,与非组蛋白相互作用,通过调节转录来调节生理效应。 四、有机化学: 参考书目: 1.邢其毅等,基础有机化学《第二版》(上、下册),北京:高等教育出版社,1993。 2. 倪沛洲主编,《有机化学》(供药学类专业用),人民卫生出版社,最新版。
有机化学第五版下册课后答案李景宁
第十二章羧酸(P32-33) 1.命名下列化合物或写出结构式: (1) 3-甲基丁酸 (2) 3-对氯苯基丁酸 (3) 间苯二甲酸 (4) 9,12-十八碳二烯酸 (5) 4-甲基己酸 CH 3CH 2 CH(CH 3 )CH 2 CH 2 COOH (6) 2-羟基丁二酸 HOOCCH(OH)CH 2 COOH (7) 2-氯-4-甲基苯甲酸 (8) 3,3,5-三甲基辛酸 2.试以反应式表示乙酸与下列试剂的反应 3.区别下列各组化合物: 4.指出下列反应的主要产物:(第四版保留) 4.完成下列转变: 5、怎样由丁酸制备下列化合物? 6、解: 7、指出下列反应中的酸和碱。 按lewis酸碱理论:凡可接受电子对的分子、离子或基团称为酸,凡可给予电子对的分子、离子或基团成为碱。 8.(1)按酸性降低的次序排列下列化合物: ①酸性: 水>乙炔>氨; ②酸性: 乙酸>环戊二烯>乙醇>乙炔 (2)按碱性降低的次序排列下列离子: ①碱性:CH3HC C CH3O >>
②碱性:(CH3)3CO>(CH3)2CHO>CH3O 9. 解:化合物A有一个不饱和度,而其氧化产物B含有两个不饱和度。产物DC 5H 10 有一个不饱和度。从题意可知:D的结构式可能为环戊烷;C的结构为环戊酮;B的结构为己二酸;A的结构式为环己醇。 10.解: (1)由题意:该烃氧化成酸后,碳原子数不变,故为环烯烃,通式为CnH2n-2。(2)该烃有旋光性,氧化后成二元酸,所以分子量=66*2=132。故二元酸为 CH3CH(CH2COOH)COOH 11.由题意:m/e=179,所以马尿酸的分子量为179,它易水解得化合物D和E,D 的IR谱图:3200-2300cm-1为羟基中O-H键的伸缩振动。1680为共扼羧酸的>C=O的伸缩振动;1600-1500cm-1是由二聚体的O-H键的面内弯曲振动和C-O 键的伸缩振动之间偶合产生的两个吸收带;750cm -1和700cm-1是一取代苯的 C-H键的面外弯曲振动。再由化学性质知D为羟酸,其中和当量为121±1,故D的分子量为122,因 此,又由题意:E为氨基酸,分子量为75,所以E的结构为 H 2NCH 2 COOH。 第十三章羧酸衍生物(P77-78) 1.说明下列名词: 酯、油脂、皂化值、干性油、碘值、非离子型洗涤剂。 酯:是羧酸分子和醇分子间脱水形成的产物。 油脂:是高级脂肪酸的甘油醇酯。 皂化值:是指完全皂化1克油脂所需的KOH的质量(以mg为单位)。 干性油:是指那些在空气中放置后能逐渐变成有韧性的固态薄膜的油。 碘值:是指100克油脂完全加成时所能吸收的碘的质量(以克为单位)。 非离子型洗涤剂:此处实指非离子型表面活性剂,即在水溶液中不离解出正负离子的表面活性剂(此处的非离子型表面活性剂起主要的洗涤去污作用)。 2.试用方程式表示下列化合物的合成路线: (1)由氯丙烷合成丁酰胺; (2)由丁酰胺合成丙胺 (3)由邻氯苯酚、光气、甲胺合成农药“害扑威”
天津大学无机化学考试试卷下册 及 答案
天津大学无机化学考试试卷(下册)答案 一、是非题(判断下列叙述是否正确,正确的在括号中画√,错误的画X)(每小题1分,共10分) 1、(X)在周期表中,处于对角线位置的元素性质相似,这称为对角线规则。 2、(X)SnS溶于Na2S2溶液中,生成硫代亚锡酸钠。 3、(X)磁矩大的配合物,其稳定性强。 4、(X)氧族元素氢化物的沸点高低次序为H2O>H2S>H2Se>H3Te。 5、(√)已知[HgCl4]2-的K=1.0?10-16,当溶液中c(Cl)=0.10mol·L-1时,c(Hg2+)/c([HgCl4]2-) 的比值为1.0?10-12。 6、(√)如果某氢化物的水溶液为碱性,则此氢化物必为离子型氢化物。 7、(X)硼是缺电子原子,在乙硼烷中含有配位键。 8、(√)在浓碱溶液中MnO4-可以被OH-还原为MnO42-。 9、(√)配合物Na3[Ag(S2O3)2]应命名为二硫代硫酸根合银(Ⅰ)酸钠。 10、(X)Pb(OAc)2是一种常见的铅盐,是强电解质。 二、选择题(在下列各题中,选择出符合题意的答案,将其代号填入括号内)(每小题1分,共20分) 1、在下列各种酸中氧化性最强的是...............(B)。 (A)HClO3;(B)HClO;(C)HClO4;(D)HCl。 2、下列浓酸中,可以用来和KI(s)反应制取较纯HI(g)的是...............(C)。 (A)浓HCl;(B)浓H2SO4;(C)浓H3PO4;(D)浓HNO3。 3、用于说明Pb(Ⅳ)具有强氧化性的是...............(D)。 (A)熵效应;(B)螯合效应;(C)屏蔽效应;(D)惰性电子对效应。 4、美国的阿波罗飞船上的天线是用钛镍合金制成的,这是因为钛镍合金................(C)。 (A)机械强度大;(B)熔点高;(C)具有记忆性能;(D)耐腐蚀。 5、在一溶液中加入淀粉溶液和少量NaClO溶液,得到蓝色溶液(a),继续加入NaClO后得一无色溶液,然后加入适量Na2SO3溶液,又复原为(a),Na2SO3溶液逐渐过量时,蓝色褪去,成为一无色溶液(b)。由此可推断,(a)和(b)溶液含有...............(B)。 (A)(a)I2,(b)SO42-、IO3-;(B)(a)I2,(b)SO42-、I-; (C)(a)I-,(b)H2S、IO3-;(D)(a)I-,(b)H2S、I-。 6、下列各组离子中每种离子分别与过量NaOH溶液反应时,都不生成沉淀的是...............(B)。 (A)Al3+、Sb3+、Bi3+;(B)Be2+、Al3+、Sb3+; (C)Pb2+、Mg2+、Be2+;(D)Sn2+、Pb2+、Mg2+。
天津大学无机化学思考题完整版
天津大学无机化学思考 题 集团标准化办公室:[VV986T-J682P28-JP266L8-68PNN]
第一章思考题 1.一气柜如下图所示: A 假设隔板(A)两侧N2和CO2的T, P相同。试问: (1)隔板两边气体的质量是否相等浓度是否相等物质的量不等而浓度相等 (2)抽掉隔板(假设不影响气体的体积和气柜的密闭性)后,气柜内的T和P 会改变?N2、CO2物质的量和浓度是否会改变?T和P 会不变,N2、CO2物质的量不变而浓度会改变 2.标准状况与标准态有何不同 标准状况指气体在27.315K和101325Pa下的理想气体,标准态是在标准压力下(100kPa)的纯气体、纯液体或纯固体 3.化学反应方程式的系数与化学计量数有何不同?对某一化学反应方程式来说,化学反应方程式的系数和化学计量数的绝对值相同,但化学反应方程式的系数为正值,而反应物的化学计量数为负值,生成物的化学计量数为正值
4.热力学能、热量、温度三者概念是否相同 试说明之。 5.试用实例说明热和功都不是状态函数。 6.判断下列各说法是否正确: (1)热的物体比冷的物体含有更多的热量。× (2)甲物体的温度比乙物体高,表明甲物体的热力学能比乙物体大。× (3)物体的温度越高,则所含热量越多。× (4)热是一种传递中的能量。√ (5)同一体系: (a)同一状态可能有多个热力学能值。× (b)不同状态可能有相同的热力学能值。√ 7.判断下列各过程中,那个ΔU最大: (1)体系放出了60kJ热,并对环境做了40kJ功。 (2)体系吸收了60kJ热,环境对体系做了40kJ功。√ (3)体系吸收了40kJ热,并对环境做了60kJ功。
无机化学(天津大学第四版答案)
第1章化学反应中的质量关系和能量关系习题参 考答案 1.解:1.00吨氨气可制取2.47吨硝酸。 2.解:氯气质量为2.9×103g。 3.解:一瓶氧气可用天数 4.解: = 318 K ℃ 5.解:根据道尔顿分压定律 p(N2) = 7.6104 Pa p(O2) = 2.0104 Pa p(Ar) =1103 Pa 6.解:(1) 0.114mol;
(2) (3) 7.解:(1)p(H2) =95.43 kPa (2)m(H2) = = 0.194 g 8.解:(1) = 5.0 mol (2) = 2.5 mol 结论: 反应进度()的值与选用反应式中的哪个物质的量的变化来进行计算无关,但与反应式的写法有关。 9.解: U = Qp p V = 0.771 kJ 10.解:(1)V1 = 38.3 10-3 m3= 38.3L (2) T2 =
= 320 K (3)W = (pV) = 502 J (4) U = Q + W = -758 J (5) H = Qp = -1260 J 11.解:NH3(g) + O2(g) NO(g) + H2O(g) = 226.2 kJ·mol1 12.解: = Qp = 89.5 kJ = nRT = 96.9 kJ 13.解:(1)C (s) + O2 (g) → CO2 (g) =
(CO2, g) = 393.509 kJ·mol1 CO2(g) + C(s) → CO(g) = 86.229 kJ·mol1 CO(g) + Fe2O3(s) → Fe(s) + CO2(g) = 8.3 kJ·mol1 各反应 之和 = 315.6 kJ·mol1。 (2)总反应方程式为 C(s) + O2(g) + Fe2O3(s) → CO2(g) +
大学无机化学期末考试复习资料(天津大学第四版)
第一章化学反应中的质量和能量关系 重要概念 1.系统:客观世界是有多种物质构成的,但我们可能只研究其中一种或若干物质。 人为地将一部分物质与其他物质分开,被划分的研究对象称为系统。 2.相:系统中具有相同物理性质和化学性质的均匀部分称为相。 3.状态:是指用来描述系统的诸如压力P、体积 V、温度 T、质量 m 和组成等各 种宏观性质的综合表现。 4.状态函数:用来描述系统状态的物理量称为状态函数。 5.广度性质:具有加和性,如体积,热容,质量,熵,焓和热力学能等。 6.强度性质:不具有加和性,仅决定于系统本身的性质。如温度与压力,密度等。 系统的某种广度性质除以物质的量或者质量之后就成为强度性质。强度性质不必 指定物质的量就可以确定。 7.热力学可逆过程:系统经过某种过程由状态 1 到状态 2 之后,当系统沿着该过 程的逆过程回到原来状态时,若原来的过程对环境产生的一切影响同时被消除 (即环境也同时复原),这种理想化的过程称为热力学的可逆过程。 8.实际过程都是不可逆的,可逆过程是一种理想过程。 9.化学计量数: 0= VBB表示反应中物质的化学式,VB是B的化学计量数, B 量纲为一;对反应物取负值,生成物取正值。 10.化学计量数只表示当安计量反应式反应时各物质转化的比例数,并不是各反 应物质在反应过程中世界所转化的量。 11. 反应进度:n b / v b对于化学反应来讲,一般选未反应时,0 引 入反应进度这个量最大的优点是在反应进行到任意时刻时,可用任一反应物或产
物来表示反反应进行的程度,所得的值总是相等的。 12.习惯对不注明温度和压力的反应,皆指反应是在 298.15K ,100kPa 下进行的。 13.一般没有特别的注明,实测的反应热(精确)均指定容反应热,而反应热均 指定压反应热。 14.能量守恒定律:在任何过程中,能量不会自生自灭,只能从一种形式转化为 另一种形式,在转化过程中能量的总值不变。也叫做热力学第一定律。 U=Q+W 15.热力学能具有状态函数的特点:状态一定,其值一定。殊途同归,值变相等。 周而复始,值变为零。 16.系统与环境之间由于存在温差而交换的热量称为热。若系统吸热值为正,若系 统放热值为负。 17.系统与环境之间除了热以外其他形式传递的能量都称为功。系统得功为正, 系统做功为负。在一定条件下由于系统体积的变化而与环境交换的功称为体积功 W pdV ,除体积功以外的一切功称为非体积功如电功。 18.功和热都是过程中被传递的能量,它们都不是状态函数,其数值与途径有关。而热力学第一定律中的热力学能的改变量只有过程的始态和终态决定,而与过程的具体途径无关。 19.化学反应热是指等温过程热,即当系统发生了变化后,使反应产物的温度回 到反应前始态的温度,系统放出或吸收的热量。 20. U Q v令H U pV 定压反应热,在恒压,只做体积功的条件下, H 2H1 则Q p 是焓的增量,称为焓变。如果<0 表示系统放热,>0 表示系统吸热, 为吸热反应。 21.对于只有凝聚相的系统即液态和固态的系统, Q p Q v,对于有气态物质参与
有机化学-第五版答案完整版
《有机化学》(第五版,李景宁主编)习题答案 第一章 3、指出下列各化合物所含官能团的名称。 (1) CH 3CH=CHCH 3 答:碳碳双键 (2) CH 3CH 2Cl 答:卤素(氯) (3) CH 3CHCH 3 OH 答:羟基 (4) CH 3CH 2 C=O 答:羰基 (醛基) H (5) CH 3CCH 3 O 答:羰基 (酮基) (6) CH 3CH 2COOH 答:羧基 (7) NH 2 答:氨基 (8) CH 3-C ≡C-CH 3 答:碳碳叁键 4、根据电负性数据,用和标明下列键或分子中带部分正电荷和负电荷的原子。 答: 6、下列各化合物哪个有偶极矩?画出其方向 (1)Br 2 (2) CH 2Cl 2 (3)HI (4) CHCl 3 (5)CH 3OH (6)CH 3OCH 3 答:以上化合物中(2)、(3)、(4)、(5)、(6)均有偶极矩 (2) H 2C Cl (3 )I (4 ) Cl 3 (5) H 3C OH (6)H 3C CH 3 7、一种化合物,在燃烧分析中发现含有84%的碳[Ar (C )=12.0]和16的氢[Ar (H )=1.0],这个化合物的分子式可能是 (1)CH 4O (2)C 6H 14O 2 (3)C 7H 16 (4)C 6H 10 (5)C 14H 22 答:根据分析结果,化合物中没有氧元素,因而不可能是化合物(1)和(2); 在化合物(3)、(4)、(5)中根据碳、氢的比例计算(计算略)可判断这个化合物的分子式可能是(3)。
第二章 习题解答 1、用系统命名法命名下列化合物 (1)2,5-二甲基-3-乙基己烷 (3)3,4,4,6-四甲基辛烷 (5)3,3,6,7-四甲基癸烷 (6)4-甲基-3,3-二乙基-5-异丙基辛烷 2、写出下列化合物的构造式和键线式,并用系统命名法命名之。 (3)仅含有伯氢和仲氢的C5H12 答:符合条件的构造式为CH3CH2CH2CH2CH3; 键线式为;命名:戊烷。 3、写出下令化合物的构造简式 (2)由一个丁基和一个异丙基组成的烷烃 (4) 相对分子质量为100,同时含有伯、叔、季碳原子的烷烃 答:该烷烃的分子式为C7H16。由此可以推测同时含有伯、叔、季碳原子的烷烃的构造式为(CH3)3CCH(CH3)2 (6) 2,2,5-trimethyl-4-propylnonane (2,2,5-三甲基-4-丙基壬烷) 8、将下列烷烃按其沸点由高至低排列成序。 (1)2-甲基戊烷(2)正已烷(3)正庚烷(4)十二烷 答:对于饱和烷烃,随着分子量的逐渐增大,分子间的范德华引力增大,沸点升高。支链的存在会阻碍分子间的接近,使分子间的作用力下降,沸点下降。由此可以判断,沸点由高到低的次序为:十二烷>正庚烷>正己烷>2-甲基戊烷。[(4)>(3)>(2)>(1)] 10、根据以下溴代反应事实,推测相对分子质量为72的烷烃异构式的构造简式。答:相对分子质量为72的烷烃的分子式应该是C5H12。溴化产物的种类取决于烷烃分子内氢的种类(指核磁共振概念中的氢),既氢的种类组与溴取代产物数相同。 (1)只含有一种氢的化合物的构造式为(CH3)3CCH3
天津大学无机化学考试试卷(上册) 答案
天津大学无机化学考试试卷(上册)答案 一、填表题(20分) 1. (g) 2CO2 (g) (?r H m<0),在密闭容器中达到平衡: 2. 反应2CO (g) + O 3. 4. 5. 在0.1mol?L-1NH3?H2O中加入下列物质,写出NH3?H2O的解离度α和pH值变化趋势 二、填空题(20分) 1. 随着溶液的pH值增加,下列电对Cr2O72-/Cr3+、Cl2/Cl-、MnO4-/MnO42-的E值将分别减小、 不变、不变。 2. MgO晶体比金属Mg的延展性差;石墨晶体比金刚石晶体的导电性好;SiO2晶体比SiF4晶 体的硬度大;I2晶体比NaI晶体在水中的溶解度小。 3. 健康人血液的pH值为7.35~7.45。患某种疾病的人的血液pH可暂时降到5.90,此时血液中c(H+)为正常状态的28~35 倍。 4. 已知B2轨道的能级顺序为σ1sσ*1sσ2sσ*2sπ2pyπ2pzσ2pxπ*2pyπ*2pzσ*2px,则B2的分子轨道分布式为
(σ1s )2(σ*1s )2(σ2s )2(σ*2s )2(π2py )1(π2pz )1,成键数目及名称两个单电子π键,价键结构式为 。 5. 根据E θ(PbO 2/PbSO 4) >E θ(MnO 4-/Mn 2+) >E θ(Sn 4+/Sn 2+),可以判断在组成电对的六种物质中,氧化性最 强的是 PbO 2 ,还原性最强的是 Sn 2+ 。 6. 表示θm r H ?=θ m f H ?(AgBr, s)的反应式为 Ag(s) + 1/2 Br 2(l) → AgBr(s) 。 7. 用电对MnO 4-/Mn 2+,Cl 2/Cl -组成的原电池,其正极反应为 MnO 4- + 8H + + 5e → Mn 2+ + 4H 2O ,负极反 应为 2 Cl - -2 e → Cl 2 ,电池的电动势等于0.15V ,电池符号为(-)Pt,Cl 2(p θ)|Cl -‖MnO 4-,Mn 2+,H +|Pt(+)。(E θ4;E θ(Cl 2/Cl -)=1.36V ) 8. 下列各溶液浓度均为0.1 mol ?L -1,按pH 值从小到大顺序排列NH 4NO 3, NH 4F, NH 4OAc, KCN, Na 2CO 3。 KCN, NH 4F, NH 4OAc, NH 4NO 3, Na 2CO 3。 (已知K θ(NH 3?H 2O)=1.8×10-5, K θ(HF)=6.6×10-4, K θ(HCN)=6.2×10-10, K θ(HOAc)=1.8×10-5, θ1K (H 2CO 3)=4.4×10-7, θ2K (H 2CO 3)=4.8×10-11) 9. 已知V E A /θ:Cr 2O 72- +1.36 Cr 3+ -0.41 Cr 2+ -0.86 Cr ,则E θ(Cr 2O 72- / Cr 2+)= 0.917 V ,Cr 2+能否发生歧化反应 不能 。 10. 已知氨水溶液中,c(OH -)=2.4×10-3 mol ?L -1, 则此氨水的浓度为0.32 mol ?L -1。(K θ(NH 3?H 2O)=1.8×10-5) 11. 因为SnCl 2强烈水解,在配制其溶液时应加入HCl ,水解反应式为 SnCl 2+H 2O Sn(OH)Cl+HCl 。 12. K θ、θi K 、Δχ分别用来衡量 反应限度的大小、 电解质强弱 、 键的极性 。 13. HF 的沸点比HI 高,主要是由于 HF 中存在氢键 。 14. 物质NaCl 、MgO 、Na 2O 、KCl 的熔点由低到高的顺序是KCl 、NaCl 、Na 2O 、MgO 。 15. 在元素周期表中,同一主族自上而下,元素第一电离能的变化趋势是逐渐 减小 ,因而其金属性依次 增强 ;在同一周期中自左向右,元素的第一电离能的变化趋势是逐渐 增大 ,元素的金属性逐渐 减弱 。 三、是非题(判断下列叙述是否正确,正确的在括号中画√,错误的画×) (10分) 1. 乙烷裂解生成乙烯:C 2H 6 (g) C 2H 4 (g) + H 2 (g) 。在实际生产中常在恒温恒压下采用加入过 量水蒸汽的方法来提高乙烯的产率,这是因为随着水蒸汽的加入,同时以相同倍数降低了p (C 2H 6)、 p (C 2H 4)、p (H 2),使平衡向右移动。………………………………………………………………………( √ ) 2. 波函数ψ表明微观粒子运动的波动性,其数值可大于零,也可小于零,2 ψ表示电子在原子核外空间出现的几率密度。…………………………………………………………………………………….…..(√ ) 3. 因为I - 的极化率大于Cl -,所以θsp K (AgI) <θsp K (AgCl)。 ……………………………………………( √ ) 4. 在298K 时,最稳定纯态单质的θ θθm m f m f S G H ,,??均为零。…………………………………….. ( × ) 5. Δr G m 代数值越小,K θ就越大,反应进行得越完全。……………………………………..…………….. ( × ) 6. 在相同温度下,纯水或0.1 mol ?L -1HCl 或0.1 mol ?L -1NaOH 溶液中,水的离子积都相同。………. ( √ ) 7. 在氧化还原反应中,如果两个电对的电极电势相差越大,反应就进行得越快。…………………. ( × ) 8. 当溶液中含有多种离子均可与沉淀剂发生沉淀反应时,溶度积小的对应离子一定先沉淀。……. ( × ) 9. 溶度积规则适用于任何难溶电解质,质量作用定律只适用于基元反应。………………………. ( √ ) 10. 偶极矩可衡量分子极性大小,极化率可衡量分子变形性大小,晶格能可衡量离子晶体的稳定性。( √ )
