临床试验运行管理流程图
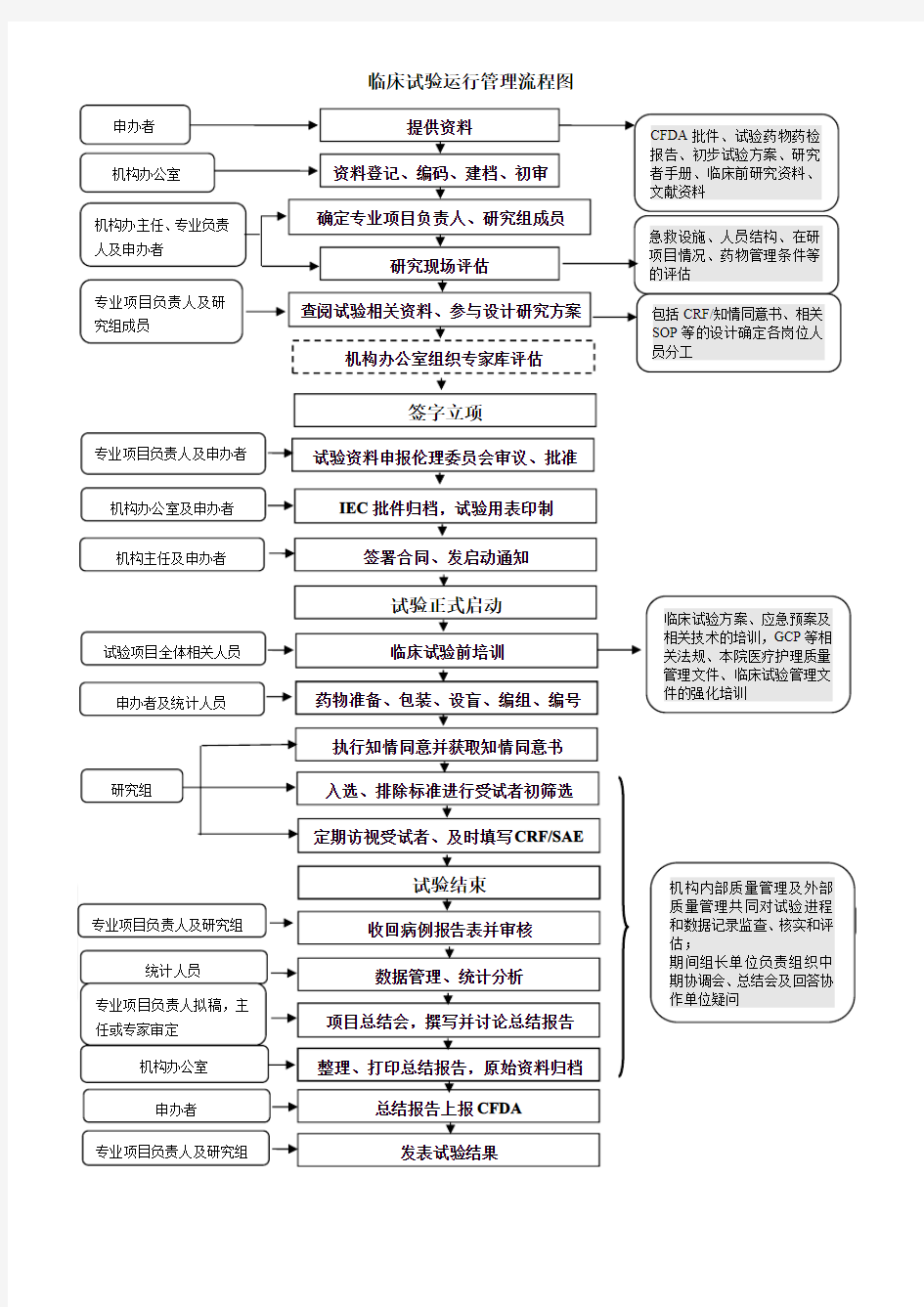
临床试验运行管理流程图
提供资料
资料登记、编码、建档、初审确定专业项目负责人、研究组成员
CFDA 批件、试验药物药检报告、初步试验方案、研究者手册、临床前研究资料、文献资料
研究现场评估
查阅试验相关资料、参与设计研究方案
机构办公室组织专家库评估
申办者机构办公室
机构办主任、专业负责人及申办者
专业项目负责人及研究组成员
试验正式启动
临床试验前培训
药物准备、包装、设盲、编组、编号入选、排除标准进行受试者初筛选执行知情同意并获取知情同意书
定期访视受试者、及时填写CRF/SAE
试验结束
收回病例报告表并审核数据管理、统计分析
项目总结会,撰写并讨论总结报告整理、打印总结报告,原始资料归档
总结报告上报CFDA
发表试验结果
试验资料申报伦理委员会审议、批准
IEC 批件归档,试验用表印制
签署合同、发启动通知
研究组
急救设施、人员结构、在研项目情况、药物管理条件等的评估
试验项目全体相关人员
申办者及统计人员
专业项目负责人及申办者
机构办公室及申办者
机构主任及申办者
专业项目负责人及研究组
统计人员
专业项目负责人拟稿,主任或专家审定
机构办公室申办者
专业项目负责人及研究组
包括CRF/知情同意书、相关SOP 等的设计确定各岗位人员分工
临床试验方案、应急预案及
相关技术的培训,GCP 等相关法规、本院医疗护理质量管理文件、临床试验管理文件的强化培训
机构内部质量管理及外部质量管理共同对试验进程和数据记录监查、核实和评估;
期间组长单位负责组织中期协调会、总结会及回答协作单位疑问
签字立项
药物临床试验运行管理制度和流程
药物临床试验是指任何在人体(病人或健康志愿者)进行的药物的系统性研究,以证实或发现试验药物的临床、药理和/或其他药效学方面的作用、不良反应和/或吸收、分布、代及排泄,目的是确定试验药物的安全性和有效性。遵照《药物临床试验质量管理规》及ICH GCP要求,参照国外开展药物临床试验的经验,制定本制度与流程。 1.步骤一:立项准备 1.1.申办者/CRO与机构共同商定主要研究者(PI)。 1.2.PI提出研究小组成员,根据项目的具体情况并参照如下人员组成组 建研究团队:⑴临床医师;⑵病区护士;(3)研究护士;(4)药物管理人 员;(5)药代研究人员(如必要);(6)相关科室人员(如必要)。 1.3.研究人员的资质:⑴研究团队成员必须经GCP培训并获取证书;⑵ 临床医务人员必须为本院在职在岗人员。 1.4.如需机构派出研究护士的项目,请递交《研究护士申请》(附件6)。 1.5.若本中心为组长单位,申办方/CRO协助PI主持召开研究者会议,机 构应派人参议;若为参加单位,PI等研究人员参加研究者会议。 1.6.申办者/CRO按照附件1准备申请临床试验的相关材料,由监查员交 机构办公室秘书(5)进行形式审查,正式受理后通知PI。 2.步骤二:立项审核 机构对送审材料及研究小组成员资质进行审核、立项。(具体事项可参考《立项审核的SOP》)。 3.步骤三:伦理审核
3.1 申办者按伦理委员会的要求准备材料,将申报材料交伦理委员会进 行伦理审评。 3.2 最终的“伦理委员会审批件”交机构办公室秘书存档。 4.步骤四:合同审核 4.1申办者/CRO与PI拟订合同/经费预算,按《临床试验合同签订SOP》的 要求,递交机构办公室秘书。 4.2经费管理小组审核合同/经费预算,通过后由机构办公室秘书交主管院长 签字盖章生效。 4.3协议正式签署后,方能开始临床试验。 5.步骤五:项目实施 5.1申办者/CRO应尽快将临床试验材料交研究小组。 5.2申办者/CRO按照《药物的接收、保存、分发、回收、退还的SOP》将药 物交予药学部临床试验药房(药物管理员,7)。如有特殊保管需求的,需报机构办公室和药学部。 5.3申办者/CRO协助PI主持项目启动会,具体事宜可参照《药物临床试验 项目启动的SOP》。 5.4项目管理实行PI负责制。PI对受试者安全、研究质量、进度负全责。 5.5研究者遵照《药物临床试验质量管理规》及ICH-GCP、试验方案及相关 SOP,实施临床试验。涉及知情同意、医疗判断、医嘱等环节,须由本院注册的,经PI授权的临床医生负责执行;临床试验相关医疗病历、文书的书写,需由PI授权的临床医生签名确认。 5.6试验过程中,若发生AE,参照《不良事件及严重不良事件处理与记录 的标准操作规程》;如判断为SAE,按照《药物临床试验SAE报告的标准操作规程》及时上报,并同时报告机构SAE专员(:6)。 6.步骤六:质量管理
皮试流程说明
皮试流程说明 一、医生首先要下达一条临时的皮试医嘱(通知护士需要做皮试) (1)皮试医嘱的下达: 注意事项:1、给药途径中要选择包含“皮试费用” 2、父医嘱皮试选项务必要选择“无需皮试” 3、需作皮试的子医嘱务必要选择“皮试” (2)保存: 保存后状态为“新增未提交”(医生仍可以对其进行修改) (3)提交(医生) 医生提交的新增医嘱状态为“新增未确认”
二、领皮试药(护士) 1、护士到老的YZ系统里面生成费用细目。 注意:需要皮试的临时医嘱在医生提交之后,护士在海泰系统无需进行医嘱确认,直接到老的YZ系统里面生成后,发送药品单拿药。如下图: 2、在老的YZ系统医嘱记价中可对生成的药品进行查询: 3、生成领药单:发送可到药房拿药
三、录皮试结果(护士) 1、做完皮试后进行“皮试结果录入”(选中前面的复选框,录入皮试结果,右键保存) 2、皮试结果确认(勾选前面的复选框,右键确认) 完成皮试结果确认后,医嘱状态变为:“已执行” 四、皮试完使用此药品 正式给使用此药品操作:给病人下达一条药品医嘱,选择【无需皮试】(表示病人做过皮试,皮试结果显示可以用该类药品),如下图: (1)药品医嘱的下达; (2)保存提交(医生)
(3)护士在海泰系统护士站确认接收这条医嘱:(勾选前面的复选框,右键医嘱确认),只有进行“确认”,医嘱才会传到老YZ系统中。 确认后的医嘱状态为“已确认” (4)生成执行单(一旦生成执行单,医嘱状态即变为【长期的“正在执行”,临时的“已执行”】) (5)打印执行单(只有先生成执行单,才能打印执行单【打印执行单时可选择不同的类型:卡、执行单、瓶签】) (6)、到老YZ系统中操作“医嘱生成”,才会生成费用明细,打印药品单。
机器设备管理流程图
机器设备管理流程 图 1
机器设备管理流程图 为了加强设备全过程管理,提高企业装备水平,保证安全生产和设备正常、经济运行,特制订本标准。本标准对原设备管理通则的主要修改内容如下: ——理顺了设备管理从规划选型、维护管理、检修到更新全过程的管理流程,新增了管理流程图。 ——强调了设备管理的主要指标纳入方针目标和经济责任制考核。各级责任和要求。 设备管理通则 1 范围 本标准规定了设备规划、选型、使用、检修、改造、更新一生管理的基本任务和管理原则。 2 规范性引用文件 国务院《全民所有制工业交通企业设备管理条例》 3 术语和定义 3.1 设备 是固定资产的主要组成部分,是工业企业中可供长期使用并在使用中基本保持原有实物形态的物资资料的总称。 3.2 设备管理 是以企业经营目标为依据,经过一系列的技术、经济、组织措施,对设备的规划、设计、制造、选型、购置、安装、使用、维护、修理、改造及更新、调拨,直至报废全过程的管理活动。 4 职责
4.1 装备环保部负责公司从选型到报废的全过程管理。 4.2 计划财务部、安全生产管理部、培训中心等部门协助装备环保部做好设备的计划、资金、考核、安全、培训等管理。 4.3 各分厂(部门)负责本部门设备的组织、协调及日常管理。 5 管理业务流程(见下页图) 6 管理内容与方法 6.1 设备管理准则 6.1.1设备管理的基本任务是经过对设备实行技术和经济的综合管理,以达到设备寿命周期费用最低,设备的综合效能最高,企业经济效益最好的目的。 6.1.2 设备管理应当依靠技术进步、促进生产发展和预防为主,坚持设计、制造与使用结合,维护与计划检修相结合,修理、改造与更新相结合,专业管理与群众管理相结合,技术管理与经济管理相结合的原则。 6.1.3 对工艺发生明显变化或有特殊要求,以及质量不稳定时应经过对设备的检修和改造或采取其它有效措施,以保持对生产工艺的适用性。 6.1.4 设备管理实行主管副总经理统一领导,建立公司、分厂(部门)分级管 设备管理流程图
医疗器械临床试验运行管理制度及流程
医疗器械临床试验运行管理制度和流程 医疗器械的临床试验是对申办方申请注册的医疗器械的临床试用或验证的过程。本机构按照国务院颁发的《医疗器械监督管理条例》,以及国家食品药品监督管理总局制定的《医疗器械注册管理办法》,并参照国内、外开展临床试验的规范和要求,制定本制度与流程。 1. 步骤一:立项准备 1.1申办者与机构共同商定主要研究者(PI)。 1.2 PI提出研究小组成员,PI及至少两名研究成员应接受过GCP培训,并提供证 书。 1.3若本单位为该项目的组长单位,PI主持召开研究者会议;若为参加单位, PI、机构代表应参加研究者会议。 1.4申办者按照附件1准备申请临床试验的相关材料,交机构办公室秘书(电话020- 87343565 )进行形式审查,正式受理后通知PI。 2. 步骤二:立项审核 机构对送审材料及研究小组成员资质进行审核、立项。(具体事项可参考《立
项审核的SOP》)。 3. 步骤三:伦理审核 3.1 申办者按照伦理委员会的要求准备材料,将申报材料交伦理委员会进行伦理审 评。 3.2 最终的“伦理委员会审批件”交机构办公室秘书存档。 4. 步骤四:合同审核 4.1申办者与PI拟订合同/经费预算,按《临床试验合同签订SOP》的要求, 递交 机构办公室秘书。 4.2 经费管理小组审核合同/经费预算。 4.3 取得伦理委员会审批件后,审核通过后的合同由机构办公室秘书交主管院长签 字盖章生效。 4.4 如为第二类医疗器械,申办者还应向申请人所在地食品药品监督管理部门备 案,将备案回执或相关证明交机构办公室存档。 5. 步骤五:项目实施 5.1 PI 参照“ PI 工作指引”开展临床试验工作。 5.2 申办者将试验用医疗器械及相关材料交项目研究小组,由研究者派专人负责接 收、保管、使用、回收和退还并记录。 5.3 申办者和研究者共同召开启动会。 5.4 研究者遵照GCP 规范、试验方案及相关SOP 实施临床试验。
临床试验观察表crf讲解
阿美宁病例报告表 (Case Report Form) 受试者姓名: 家庭地址: 联系电话: 试验中心名称: 申办单位:江苏豪森药业股份有限公司 在正式填表前请认真阅读下列填表说明 病例报告表填写说明: 1.筛选合格者填写病例报告表。 2.病例报告表填写务必准确、清晰,不得任意涂改,错误之处纠正时需用横线居中化出,并签署修改者姓名缩写及修改时间。 3.填写记录一律用钢笔或碳素签字笔。 4.患者姓名拼音缩写四个需填满,两字姓名填写两字拼音前两个字母;三字姓名填写三字首字母及第三字第二字母;四字姓名填写每个字的首字母。
5.表中凡有“□”的项,请在符合的条目上划“√”。表格中所有栏目均应填写相应的文字或数字,不得留空。 6.所有检验项目因故未查或漏查,请填写ND;具体合并用药剂量和时间不明,请先写NK。 7.试验期间应如实填写合并用药记录表、不良事件记录表。记录不良事件的发生时间、严重程度、持续时间、采取的措施和转归。如有严重不良事件发生(包括临床验证过程中发生需住院治疗、延长住院时间、伤残、影响工作能力危及生命或死亡、导致先天畸形等事件),必须立即通知主要研究单位伦理委员会及申办单位。 8.临床试验应严格按照临床试验方案要求进行。试验不同时期需完成的检查和需记录的项目,请对照临床流程图执行。
受试者知情同意书 敬爱的患者: 我们现在正在进行一项临床研究,该项临床研究是经吉林省药品监督管理局备案的,研究的目的是评价物理治疗的高科技产品----温热电位治疗仪的疗效和安全性。 温热磁疗仪是XXX医疗器械有限公司根据韩国专利技术研制生产的医疗器械,本治疗仪是通过XXXXXXXXXXXXXXXXXXXXXXXXXXXXXX机理,主要用于XXXXXXXXXXXXX治疗。具有平衡机体阴阳,增强脏腑机能,促进新陈代谢,调节植物神经,改善心脑血管血液供应,促进血液循环,调节血管张力,降低血液粘稠度,防治动脉粥样硬化,促进组织的再生修复功能,增强机体免疫功能及消炎止痛等作用。其注册标准已经XX省食品药品监督管理局备案,其技术指标经XX省医疗器械检验所检测合格。现拟进行临床验证。
药物临床试验运行管理制度和流程
临床试验运行流程 吉林大学第一医院药物临床试验机构,遵照中国GCP及ICH GCP要求,参照国内、外开展药物临床试验的经验,结合我机构药物临床试验的特点,制定本制度与流程。 步骤一:申办者/CRO若有意在我院开展药物临床试验,请首先与本机构就研究科室、PI等相关问题进行商洽。 步骤二:申办者/ CRO递交临床试验申请材料 申办者或CRO按照(附件1)准备申请临床试验的相关材料,并提交《伦理审核申请书》(附件2)递交机构办公室秘书。 步骤三:审核 1.申办者/CRO与临床科室和机构共同商定主要研究者(PI) 2.PI提出研究小组成员 3.机构对送审材料及研究小组成员资质进行审核 步骤四:主持或召开研究者会议 1.PI遵照“PI指引”开展临床试验工作。 2.若本单位为该项目的组长单位,PI主持召开研究者会议;若为参加单 位,主要研究者、机构代表应参加研究者会议。 步骤五:伦理委员会审核 由申办者/CRO按照(附件1)要求,将伦理申报材料递交给机构办公室秘书,秘书审核资料齐全后,转交伦理委员会进行伦理评审,最终将审批意见交机构办公室秘书存档。 步骤六:临床协议及经费审核
伦理委员会讨论同意并取得伦理批件后,申办者/CRO与研究者初步拟定协议和经费预算,签字确定后递交机构办公室秘书,并呈交机构负责人(主管院长)签字生效。 步骤七:临床试验材料及药物的交接 申办者/CRO应尽快将临床试验材料交项目研究小组,按照“吉林大学第一医院临床试验用药品管理制度”和“药物的接收、保存、分发、回收、退还的SOP”的原则,将试验药物交予药剂科保管(苏兴国) 步骤八:临床启动会的召开 协议签署后,由申办者/CRO负责召集、PI主持本研究单位现场项目启动会,对GCP等法规、试验方案及相关SOP进行培训。所有该项目的成员均应参加。 步骤八:项目实施 1.实施项目管理、PI负责制。PI对研究质量、进度、协调负全责。 2.研究小组遵照GCP规范、试验方案及相关SOP,实施临床试验。 3.机构将定期对试验项目质量、项目进度进行监督管理,对存在的问题提 出书面整改意见,研究者予以整改并给予书面答复。对违背方案并造成 严重后果者,机构办公室将与相关部门协商,采取相应的处理措施。 4.在试验过程中,若发生SAE,PI按照相关的SOP积极处理,并及时通 报机构及伦理委员会。 5.项目执行过程中如遇管理部门或申办方发出稽查通知,本项目的PI应会 同研究小组和机构成员共同参加稽查,并将稽察结果交机构备案。 6.如本单位为组长单位,机构将协助申办者/CRO在临床试验中召开项目 中期总结会、电话会等。 7.临床试验进行超过1年以上,申办者/CRO须向伦理委员会和机构办公 室递交年度总结报告。 步骤九:药物回收与材料归档
药物皮试液配制操作规程
药物皮试液配制操作规程 一、青霉素类 按《中国药典》2000年版临床用药须知规定,使用青霉素类抗生素前均需做青霉素皮肤试验,阳性反应者禁用。 青霉素类药物在应用前可用青霉素G钠皮试液进行皮试。另外也可用青霉素类原药做皮试(供选用的试液浓度为300μg/ml或按说明书规定)。 青霉素G钠皮试液的配制方法如下: 规格:80万单位 配制方法:取注射用青霉素钠80万单位加生理盐水至4ml溶解摇匀,用1ml注射器取稀释液0.1ml加生理盐水稀释至1ml;取稀释液0.1ml加生理盐水稀释至1ml;取稀释液0.25ml加生理盐水稀释至1ml(每ml稀释液含青霉素钠500单位);将0.1ml注入皮内。 规格:160万单位 配制方法:取注射用青霉素钠160万单位加生理盐水至8ml溶解摇匀,用1ml 注射器取稀释液0.1ml加生理盐水稀释至1ml;取稀释液0.1ml加生理盐水稀释至1ml;取稀释液0.25ml加生理盐水稀释至1ml(每ml稀释液含青霉素钠500单位);将0.1ml注入皮内。 其他青霉素类原药皮试液的配制方法如下: 1、注射用氨苄青霉素钠 (1)规格:0.5g (即50万μg) 配制方法:取0.5 g注射用氨苄青霉素钠加生理盐水至5ml溶解摇匀,用1ml 注射器取稀释液0.1ml加生理盐水稀释至1ml;取稀释液0.1ml加生理盐水稀释至1ml;取稀释液0.3ml加生理盐水稀释至1ml(每ml稀释液含氨苄青霉素钠300μg);将0.1ml注入皮内。 (2)规格:1.0g(即100万μg) 配制方法:取1.0 g注射用氨苄青霉素钠加生理盐水至5ml溶解摇匀,用1ml 注射器取稀释液0.1ml加生理盐水稀释至1ml;取稀释液0.1ml加生理盐水稀释至1ml;取稀释液0.15ml加生理盐水稀释至1ml(每ml稀释液含氨苄青霉素钠300μg);将0.1ml注入皮内。 2、注射用苯唑西林钠 规格:0.5g (即50万μg)
药物临床试验运行管理制度和流程-
药物临床试验就是指任何在人体(病人或健康志愿者)进行得药物得系统性研究,以证实或发现试验药物得临床、药理与/或其她药效学方面得作用、不良反应与/或吸收、分布、代谢及排泄,目得就是确定试验药物得安全性与有效性。遵照《药物临床试验质量管理规范》及ICH GCP要求,参照国内外开展药物临床试验得经验,制定本制度与流程。 1.步骤一:立项准备 1.1.申办者/CRO与机构共同商定主要研究者(PI)。 1.2.PI提出研究小组成员,根据项目得具体情况并参照如下人员组成组建 研究团队:⑴临床医师;⑵病区护士;(3)研究护士;(4)药物管理人员;(5) 药代研究人员(如必要);(6)相关科室人员(如必要)。 1.3.研究人员得资质:⑴研究团队成员必须经GCP培训并获取证书;⑵临 床医务人员必须为本院在职在岗人员。 1.4.如需机构派出研究护士得项目,请递交《研究护士申请》(附件6)。 1.5.若本中心为组长单位,申办方/CRO协助PI主持召开研究者会议,机 构应派人参议;若为参加单位,PI等研究人员参加研究者会议。 1.6.申办者/CRO按照附件1准备申请临床试验得相关材料,由监查员交机 构办公室秘书(电话)进行形式审查,正式受理后通知PI。 2.步骤二:立项审核 机构对送审材料及研究小组成员资质进行审核、立项。(具体事项可参考《立项审核得SOP》)。 3.步骤三:伦理审核 3.1 申办者按伦理委员会得要求准备材料,将申报材料交伦理委员会进行 伦理审评。 3.2 最终得“伦理委员会审批件”交机构办公室秘书存档。
4.步骤四:合同审核 4.1申办者/CRO与PI拟订合同/经费预算,按《临床试验合同签订SOP》得要 求,递交机构办公室秘书。 4.2经费管理小组审核合同/经费预算,通过后由机构办公室秘书交主管院长 签字盖章生效。 4.3协议正式签署后,方能开始临床试验。 5.步骤五:项目实施 5.1申办者/CRO应尽快将临床试验材料交研究小组。 5.2申办者/CRO按照《药物得接收、保存、分发、回收、退还得SOP》将药 物交予药学部临床试验药房(药物管理员,电话)。如有特殊保管需求得, 需报机构办公室与药学部。 5.3申办者/CRO协助PI主持项目启动会,具体事宜可参照《药物临床试验 项目启动得SOP》。 5.4项目管理实行PI负责制。PI对受试者安全、研究质量、进度负全责。 5.5研究者遵照《药物临床试验质量管理规范》及ICH-GCP、试验方案及相 关SOP,实施临床试验。涉及知情同意、医疗判断、医嘱等环节,须由本院注册得,经PI授权得临床医生负责执行;临床试验相关医疗病历、文书得书写,需由PI授权得临床医生签名确认。 5.6试验过程中,若发生AE,参照《不良事件及严重不良事件处理与记录得 标准操作规程》;如判断为SAE,按照《药物临床试验SAE报告得标准操作规程》及时上报,并同时报告机构SAE专员(电话:)。 6.步骤六:质量管理 6.1.申办者派出合格得、为研究者所接受得监查员,参照GCP要求对整个试验 过程进行监查。 6.2.机构质量管理员对试验项目进行质量检查,对存在得问题提出书面整改 意见,研究者予以整改并给予书面答复。具体要求可参考《临床研究质量检查得SOP》与《临床研究得问题分级与处理SOP》。对违背方案并造成严重后果者,机构办公室将与相关部门协商,采取相应得处理措施。具体措施可参考《临床研究缺陷管理办法》。
各种药物的皮试方法
各种药物的皮试方法 青霉素皮试药液配制方法: 青霉素1瓶80万u,注入4ml生理盐水,则1ml含20万u 取0. 1ml,加生理盐水至1ml,则1ml含2万u 取0. 1ml,加生理盐水至1ml,则1ml含2000u 取0. 25ml,加生理盐水至1ml,则1ml含500u,即成青霉素皮试液。皮内注射0. 1ml含50 u 破伤风抗毒素(TAT)皮试液的配制方法: TAT 每支1500IU约0.7 ml,加水至1ml,抽取0. 1ml,加生理盐水稀释至1ml(含150IU),皮内注射0. 1ml含15IU。 细胞色素C皮试液的配制方法: 细胞色素C 每支2 ml含15mg,取0. 1ml,加生理盐水至1ml(1ml含0.75 mg), 皮内注射0. 1ml含0.075 mg。 先锋酶素皮试液的配制方法: 先锋酶素0.5 g加生理盐水2 ml,则1ml含250mg 取0.2ml,加生理盐水至1ml,则1ml含30mg 取0. 1ml,加生理盐水至1ml,则1ml含3mg(3000 ug) 取0. 1ml,加生理盐水至1ml,则1ml含300 ug 皮内注射0. 1ml含30ug 长效青霉素皮试液的配制方法; 长效青霉素1瓶120万u,注入4ml生理盐水,则1ml含30万u 取0. 1ml l含3万u,作画痕试验。 碘过敏试验:
30%泛影葡胺1ml缓慢静脉注射 链霉素皮试液的配制方法: 链霉素1瓶1g(100万u),加生理盐水至3. 5ml溶解后为4ml,则1ml含0.25 g(25万u) 取0. 1ml,加生理盐水至1ml,则1ml含2. 5万u 取0. 1ml,加生理盐水至1ml,则1ml含2500u 皮内注射0. 1ml含250万 精制抗狂犬病血清皮试液的配制方法: 抗血清每支400IU, 取0. 1ml,加生理盐水0·9ml,皮内注射0. 05ml,观察30分钟。 头孢唑啉钠皮试液的配制 0.5g/瓶头孢唑啉钠加等渗盐水至5ml -→0.1g/ml 取0.1ml瓶加4.9ml等渗盐水至5ml -→2mg/ml 取0.15g/瓶加4.85ml等渗盐水至5ml -→60μg/ml 取头孢唑啉钠皮试液0.1ml(含6μg)作皮内注射,观察20分钟后,判断试验结果。头孢曲松皮试液的配置 在1 g的头孢曲松钠中加入生理盐水4 ml,充分溶化,使每毫升浓度为250 mg/ml。 用1 ml注射器从上液中抽取0.2 ml,加生理盐水至1 ml,使其浓度为50 mg/ml。 取0.1 ml,加生理盐水至1 ml,使其浓度为5 mg/ml。 取0.1 ml,加生理盐水至1 ml,即成浓度为500 μg/ml的皮试液。
设备管理流程图
设备管理方案总经理副总经理需求部设备部采购部相关文件表设备请购单设备开箱验收移交单设备台帐固定资产登记表年度设备维护计划设备点检卡设备检查日志设备完整性检查记录定期检查并记录设备管理方案,设备部财务部负责人,执行本岗位、设备经理、设备技术员、设备经理、设备技术员的相关文件和表格,固定资产登记表,财务经理负责设备经理,设备管理计划,设备部,生产部负责执行相关部门主管部门主管部门主管设备经理部门设备采购申请管理工艺机械设备标识卡(代码)设备故障/事故记录表设备事故处理工艺设备事故/故障处理表阶段工艺设备事故报告组织事故分析资产登记列入设备文件工艺设备要求申请设备购置评估设备维修计划定期维修设备安装验收固定资产登记设备分类/记录设备记录归档设备使用和管理审批统计设备需求审核选择/安装位置/电源配置审批设备日常维护固定资产登记表,设备使用和管理在ERP 文件中,设备经理相关人员,设备经理相关人员、设备管理程序、设备部、生产部主管、执行岗位相关文件和表格、设备经理、设备修理工、年度维修计划、设备经理、设备维修人员、设备经理,相关人员设备经理维修人员设备经理维修人员定期检查记录表设备
经理设备经理设备维修人员设备管理程序物资管理部设备部采购部主管岗位实施岗位相关文件和表格设备经理设备技术员备件管理计划采购经理设备技术员仓库管理员仓库管理员仓库管理员仓库管理员仓库管理员仓库管理员组织事故分析、事故处理,改进/预防程序、关键设备维修计划和维修项目应通知使用部门根据维修情况达成A协议,编制记录分析等级,完善维修备件发放计划,对备件采购进行备件验收分析,完善备品备件计划的储存,录入、保存和下达预定级别的维修记录归档计划,填写设备经理、设备技术员分析和改进备件计划,设备管理程序,设备部、需求部、采购部负责岗位实施后的相关文件。使用部门主管、使用部门经理、使用部门经理、使用部门主管、用户设备经理、设备经理、采购经理、仓库管理员、采购经理、采购经理,零星采购申请表设备经理维修人员设备经理设备经理维修人员使用部门设备经理设备管理程序设备部门需求部门采购部门负责人执行本岗位相关文件表格,使用部门负责人负责设备故障处理流程、设备维修人员、设备维修设备故障/事故处理表、设备维修管理流程、总经理/副总经理流程,临时采购流程、维修统计分析、大修决策、设备异常、设备维修需求申请
皮内注射操作流程培训资料
皮内注射操作流程
皮内注射操作流程 尊敬的评委老师好,我是××科的×××,今天被考核的项目是皮内注射(青霉素皮试),现在我已准备完毕,请问可以开始吗? 1、查看体温单无药物过敏史,核对医嘱:“2床,李岚,青霉素皮试”。 2、到病人床前进行评估:“您好,是2床李岚李大姐吗?”核对床头卡,昏迷患者核对腕带。“李大姐,因为您需要使用抗生素,我来给您做个青霉素皮试。请问您或家人对青霉素过敏吗?对酒精过敏吗?哦,没有,请伸出手臂让我看一下”。“注射部位无皮疹、炎症、硬结、瘢痕”“李岚大姐,我回去准备用物,请您稍等,马上回来”。 3、回治疗室:“按六步洗手法洗手,戴好口罩”。 4、按要求准备用物。 ⑴核对:分别用纱布擦去青霉素、生理盐水、肾上腺素的浮土,检查治疗卡与药物。“生理盐水有效期×××,肾上腺素有效期×××,安瓿无裂痕、药液无变色、变质、混浊、沉淀、絮状物,可以使用”,弹下安瓿尖端药液。“青霉素的批号×××,有效期×××,瓶口无松动、瓶身无裂痕、药物无变色、变质。 ⑵去除青霉素铝盖中心部分,常规消毒瓶盖,将青霉素放于治疗台的左上方。常规消毒安瓿颈部及砂轮,在安瓿颈部划一锯痕,再次消毒青霉素及安瓿后放于治疗台左上方。 (3)检查一次性注射器及针头:“注射器有效期×××,包装无破损、无漏气,可以使用,针头有效期×××,外包装无破损、潮湿,可以使用。”折断安瓿,置于治疗台左上方。 ⑷打开5ml注射器,拧紧针头并使斜面向下,左手食指固定针栓,右手抽拉活塞检查无漏气,正确抽吸盐水3.2ml注入青霉素瓶中,回抽等量气体后将注射器弃于弯盘,摇匀,使药物完全溶解。 打开1ml注射器,使针头斜面向下,(检查方法同上)按要求抽吸药液0.1ml,依次稀释,配置为每ml内含500u的皮试液。更换一次性针头(使针头斜面向上,与刻度在同一水平),将皮试液、青霉素药瓶、肾上腺素放于治疗盘内。分类处理弯盘内垃圾。应用消毒剂消毒双手。 5、携用物(1ml与5ml注射器各1个及其他治疗用物)至床旁,“李岚大姐,您准备好了吗?我来为您做皮试”,再次核对床头卡。取舒适体位,“请伸出手臂,注射部位在前臂掌侧内下1/3处”。 6、用75%酒精点状消毒皮肤,面积不小于5×5cm,核对注射卡与药物。排尽注射器内气体。 7、“李大姐,请放松,不要紧张”,左手拇指、食指固定注射部位皮肤,右手持注射器,食指固定针栓,呈5°角刺入,使针头斜面完全刺入皮肤,放平注射器,左手拇指固定针栓,其余四指固定前臂,右手推动针芯,注入0.1ml药液,(注射局部隆起一圆形皮丘,毛孔变大,皮肤变白),拔出针头,查看皮试时间,再次核对注射卡、药物。 8、协助取舒适体位:“李岚大姐,皮试为您做完了,20分钟我来看结果,在此期间,请您不要外出,不要按压或搔抓皮丘部位,如果您感觉有胸闷、气短或口角发麻等不适症状时,请您及时呼叫我们,呼叫器就放在您床头,我也会常过来看您的,谢谢您的配合”。 9、分类清理用物,六步洗手法洗手并记录(皮试药名、日期、时间、病人反应等)。
中山大学附属肿瘤医院药物临床试验运行管理制度和流程-发布版
药物临床试验就是指任何在人体(病人或健康志愿者)进行的药物的系统性研究,以证实或发现试验药物的临床、药理与/或其她药效学方面的作用、不良反应与/或吸收、分布、代谢及排泄,目的就是确定试验药物的安全性与有效性。遵照《药物临床试验质量管理规范》及ICH GCP要求,参照国内外开展药物临床试验的经验,制定本制度与流程。 1.步骤一:立项准备 1.1.申办者/CRO与机构共同商定主要研究者(PI)。 1.2.PI提出研究小组成员,根据项目的具体情况并参照如下人员组成组建 研究团队:⑴临床医师;⑵病区护士;(3)研究护士;(4)药物管理人员;(5) 药代研究人员(如必要);(6)相关科室人员(如必要)。 1.3.研究人员的资质:⑴研究团队成员必须经GCP培训并获取证书;⑵临 床医务人员必须为本院在职在岗人员。 1.4.如需机构派出研究护士的项目,请递交《研究护士申请》(附件6)。 1.5.若本中心为组长单位,申办方/CRO协助PI主持召开研究者会议,机 构应派人参议;若为参加单位,PI等研究人员参加研究者会议。 1.6.申办者/CRO按照附件1准备申请临床试验的相关材料,由监查员交机 构办公室秘书(电话)进行形式审查,正式受理后通知PI。 2.步骤二:立项审核 机构对送审材料及研究小组成员资质进行审核、立项。(具体事项可参考《立项审核的SOP》)。 3.步骤三:伦理审核 3.1 申办者按伦理委员会的要求准备材料,将申报材料交伦理委员会进行 伦理审评。 3.2 最终的“伦理委员会审批件”交机构办公室秘书存档。
4.步骤四:合同审核 4.1申办者/CRO与PI拟订合同/经费预算,按《临床试验合同签订SOP》的要 求,递交机构办公室秘书。 4.2经费管理小组审核合同/经费预算,通过后由机构办公室秘书交主管院长 签字盖章生效。 4.3协议正式签署后,方能开始临床试验。 5.步骤五:项目实施 5.1申办者/CRO应尽快将临床试验材料交研究小组。 5.2申办者/CRO按照《药物的接收、保存、分发、回收、退还的SOP》将药 物交予药学部临床试验药房(药物管理员,电话)。如有特殊保管需求的, 需报机构办公室与药学部。 5.3申办者/CRO协助PI主持项目启动会,具体事宜可参照《药物临床试验 项目启动的SOP》。 5.4项目管理实行PI负责制。PI对受试者安全、研究质量、进度负全责。 5.5研究者遵照《药物临床试验质量管理规范》及ICH-GCP、试验方案及相 关SOP,实施临床试验。涉及知情同意、医疗判断、医嘱等环节,须由本院注册的,经PI授权的临床医生负责执行;临床试验相关医疗病历、文书的书写,需由PI授权的临床医生签名确认。 5.6试验过程中,若发生AE,参照《不良事件及严重不良事件处理与记录的 标准操作规程》;如判断为SAE,按照《药物临床试验SAE报告的标准操作规程》及时上报,并同时报告机构SAE专员(电话:)。 6.步骤六:质量管理 6.1.申办者派出合格的、为研究者所接受的监查员,参照GCP要求对整个试验 过程进行监查。 6.2.机构质量管理员对试验项目进行质量检查,对存在的问题提出书面整改 意见,研究者予以整改并给予书面答复。具体要求可参考《临床研究质量检查的SOP》与《临床研究的问题分级与处理SOP》。对违背方案并造成严重后果者,机构办公室将与相关部门协商,采取相应的处理措施。具体措施可参考《临床研究缺陷管理办法》。
药物临床试验运行管理制度和流程1通用.doc
药物临床试验运行管理制度和流程1 临床试验运行流程 吉林大学第一医院药物临床试验机构,遵照中国GCP及ICH GCP要求,参照国内、外开展药物临床试验的经验,结合我机构药物临床试验的特点,制定本制度与流程。 步骤一:申办者/CRO若有意在我院开展药物临床试验,请首先与本机构就研究科室、PI等相关问题进行商洽。 步骤二:申办者/ CRO递交临床试验申请材料 申办者或CRO按照(附件1)准备申请临床试验的相关材料,并提交《伦理审核申请书》(附件2)递交机构办公室秘书。 步骤三:审核 1.申办者/CRO与临床科室和机构共同商定主要研究者(PI) 2.PI提出研究小组成员 3.机构对送审材料及研究小组成员资质进行审核 步骤四:主持或召开研究者会议 1.PI遵照“PI指引”开展临床试验工作。 2.若本单位为该项目的组长单位,PI主持召开研究者会议;若为参加单 位,主要研究者、机构代表应参加研究者会议。
步骤五:伦理委员会审核 由申办者/CRO按照(附件1)要求,将伦理申报材料递交给机构办公室秘书,秘书审核资料齐全后,转交伦理委员会进行伦理评审,最终将审批意见交机构办公室秘书存档。 步骤六:临床协议及经费审核 伦理委员会讨论同意并取得伦理批件后,申办者/CRO与研究者初步拟定协议和经费预算,签字确定后递交机构办公室秘书,并呈交机构负责人(主管院长)签字生效。 步骤七:临床试验材料及药物的交接 申办者/CRO应尽快将临床试验材料交项目研究小组,按照“吉林大学第一医院临床试验用药品管理制度”和“药物的接收、保存、分发、回收、退还的SOP”的原则,将试验药物交予药剂科保管(苏兴国) 步骤八:临床启动会的召开 协议签署后,由申办者/CRO负责召集、PI主持本研究单位现场项目启动会,对GCP等法规、试验方案及相关SOP进行培训。所有该项目的成员均应参加。 步骤八:项目实施 1.实施项目管理、PI负责制。PI对研究质量、进度、协调负全责。 2.研究小组遵照GCP规范、试验方案及相关SOP,实施临
临床试验观察表(CRF)29652
病例报告表(Case Report Form) 受试者姓名: 家庭地址: 联系电话: 试验中心名称: 申办单位:延吉喜来健医疗器械有限公司
在正式填表前请认真阅读下列填表说明 病例报告表填写说明: 1.筛选合格者填写病例报告表。 2.病例报告表填写务必准确、清晰,不得任意涂改,错误之处纠正时需用横线居中化出,并签署修改者姓名缩写及修改时间。 3.填写记录一律用钢笔或碳素签字笔。 4.患者姓名拼音缩写四个需填满,两字姓名填写两字拼音前两个字母;三字姓名填写三字首字母及第三字第二字母;四字姓名填写每个字的首字母。5.表中凡有“□”的项,请在符合的条目上划“√”。表格中所有栏目均应填写相应的文字或数字,不得留空。 6.所有检验项目因故未查或漏查,请填写ND;具体合并用药剂量和时间不明,请先写NK。 7.试验期间应如实填写合并用药记录表、不良事件记录表。记录不良事件的发生时间、严重程度、持续时间、采取的措施和转归。如有严重不良事件发生(包括临床验证过程中发生需住院治疗、延长住院时间、伤残、影响工作能力危及生命或死亡、导致先天畸形等事件),必须立即通知主要研究单位伦理委员会及申办单位。
8.临床试验应严格按照临床试验方案要求进行。试验不同时期需完成的检查和需记录的项目,请对照临床流程图执行。
受试者知情同意书 敬爱的患者: 我们现在正在进行一项临床研究,该项临床研究是经吉林省药品监督管理局备案的,研究的目的是评价物理治疗的高科技产品----温热电位治疗仪的疗效和安全性。 温热磁疗仪是XXX医疗器械有限公司根据韩国专利技术研制生产的医疗器械,本治疗仪是通过XXXXXXXXXXXXXXXXXXXXXXXXXXXXXX机理,主要用于XXXXXXXXXXXXX 治疗。具有平衡机体阴阳,增强脏腑机能,促进新陈代谢,调节植物神经,改善心脑血管血液供应,促进血液循环,调节血管张力,降低血液粘稠度,防治动脉粥样硬化,促进组织的
机器设备现场管理流程图
机器设备管理流程图 为了加强设备全过程管理,提高企业装备水平,保证安全生产和设备正常、经济运行,特制订本标准。本标准对原设备管理通则的主要修改内容如下: ——理顺了设备管理从规划选型、维护管理、检修到更新全过程的管理流程,新增了管理流程图。 ——强调了设备管理的主要指标纳入方针目标和经济责任制考核。各级责任和要求。 设备管理通则 1 范围 本标准规定了设备规划、选型、使用、检修、改造、更新一生管理的基本任务和管理原则。 2 规范性引用文件 国务院《全民所有制工业交通企业设备管理条例》 3 术语和定义 3.1 设备 是固定资产的主要组成部分,是工业企业中可供长期使用并在使用中基本保持原有实物形态的物资资料的总称。 3.2 设备管理 是以企业经营目标为依据,通过一系列的技术、经济、组织措施,对设备的规划、设计、制造、选型、购置、安装、使用、维护、修理、改造及更新、调拨,直至报废全过程的管理活动。 4 职责 4.1 装备环保部负责公司从选型到报废的全过程管理。 4.2 计划财务部、安全生产管理部、培训中心等部门协助装备环保部做好设备的计划、资金、考核、安全、培训等管理。 4.3 各分厂(部门)负责本部门设备的组织、协调及日常管理。 5 管理业务流程(见下页图) 6 管理内容与方法 6.1 设备管理准则 6.1.1设备管理的基本任务是通过对设备实行技术和经济的综合管理,以达到设备寿命周期费用最低,设备的综合效能最高,企业经济效益最好的目的。 6.1.2 设备管理应当依靠技术进步、促进生产发展和预防为主,坚持设计、制造与使用结合,维护与计划检修相结合,修理、改造与更新相结合,专业管理与群众管理相结合,技术管理与经济管理相结合的原则。
药物临床试验运行管理制度与工作流程
药物临床试验运行管理制度与工作流程 Ⅰ.概念: 药物临床试验是指任何在人体(病人或健康受试者)进行的药物的系统性研究,以证实或发现试验药物的临床、药理和/或其他药效学方面的作用、不良反应和/或吸收、分布、代谢及排泄,目的是确定试验药物的安全性和有效性。 Ⅱ.管理部门: 药物临床试验机构(以下简称“机构”)对我院药物临床试验实行管理。 Ⅲ.工作程序: 1.立项准备 1.1.申办者/CRO(合同研究者组织)联系机构办、意向科室共同确定主要研究者。CRA提交“药 物临床试验立项申请表”(附件1),并按照“药物临床试验报送资料目录”(附件2)准备临床试验相关完整材料一份,交机构办公室。 1.2.PI提出研究小组成员,填写“主要研究者履历”(附件3)“项目研究团队成员表”(附件4), 由CRA连同试验资料一起递交机构办公室。 研究小组人员的资质必须符合以下要求: ?研究团队成员必须经GCP培训并获取证书; ?主要研究者组建研究团队,包括:①临床医师;②病区护士;③研究护士;④药物管理人员;⑤药物代谢研究人员(如需要);⑥其他相关科室人员(如需要) 1.3. 一页均为文件目录,每项文件中间用带数字标识的隔页纸分隔。请按文件目录所列文件顺序排列各项文件,文件夹中不包括的文件无需列入目录。文件多的项目请准备多个“机构文件夹”,编号“①,②,③……”。 2.受理立项 机构对送审材料及研究小组成员资质进行审核,决定是否同意立项。若同意,则向伦理委员会发出“临床试验审批受理通知”(附件5)。 3.伦理审核 3.1.申请者持“临床试验审批受理通知”(附件5)按照伦理委员会要求准备材料,将申报材料 交伦理委员会进行伦理评审。
常用药皮试配置方法
部分药品皮试液配制方法 1.注射用盐酸头孢吡肟规格0.5g(皮试液浓度为500ug/ml) 取0.9%氯化钠注射液10ml稀释原药后,抽取0.1ml,再用0.9%氯化钠注射液稀释至10ml,抽取0.1ml皮内注射。 2.注射用盐酸头孢吡肟规格1g(皮试液浓度为500ug/ml) 取0.9%氯化钠注射液20ml稀释原药后,抽取0.1ml,再用0.9%氯化钠注射液稀释至10ml,抽取0.1ml皮内注射。 3.注射用哌拉西林钠规格0.5g(皮试液浓度为500ug/ml) 取0.9%氯化钠注射液10ml稀释原药后,抽取0.1ml,再用0.9%氯化钠注射液稀释至10ml,抽取0.1ml皮内注射。 4.注射用哌拉西林他唑巴坦钠规格1.25g(1g:0.25g)(皮试液浓度为500ug/ml) 取0.9%氯化钠注射液20ml稀释原药后,抽取0.1ml,再用0.9%氯化钠注射液稀释至10ml,抽取0.1ml皮内注射。 5.注射用哌拉西林舒巴坦钠规格2.5g(2g:0. 5g)(皮试液浓度为500ug/ml) 取0.9%氯化钠注射液20ml稀释原药后,抽取0.05ml,再用0.9%氯化钠注射液稀释至10ml,抽取0.1ml皮内注射。 6.注射用哌拉西林舒巴坦钠规格1.5g(1g:0. 5g)(皮试液浓度为500ug/ml) 取0.9%氯化钠注射液20ml稀释原药后,抽取0.1ml,再用0.9%氯化钠注射液稀释至10ml,抽取0.1ml皮内注射。 7.注射用头孢哌酮钠他唑巴坦钠规格2.5g(2g:0.5g)(皮试液浓度为500ug/ml) 取0.9%氯化钠注射液20ml稀释原药后,抽取0.05ml,再用0.9%氯化钠注射液稀释至10ml,抽取0.05ml皮内注射。 8.注射用头孢哌酮舒巴坦钠规格3g(2g:1g)(皮试液浓度为500ug/ml) 取0.9%氯化钠注射液20ml稀释原药后,抽取0.05ml,再用0.9%氯化钠注射液稀释至10ml,抽取0.05ml皮内注射。 9.注射用盐酸头孢替安规格1.0g(皮试液浓度为500ug/ml) 取0.9%氯化钠注射液20ml稀释原药后,抽取0.1ml,再用0.9%氯化钠注射液稀释至10ml,抽取0.1ml皮内注射。 10.注射用盐酸头孢替安规格2.0g(皮试液浓度为500ug/ml) 取0.9%氯化钠注射液20ml稀释原药后,抽取0.05ml,再用0.9%氯化钠注射液稀释至10ml,抽取0.05ml皮内注射。 11.注射用氨苄西林钠舒巴坦钠规格3g(2g﹕1g)(皮试药液浓度为500ug/ml) 取0.9%氯化钠注射液20ml稀释原药后,抽取0.05ml,再用0.9%氯化钠注射液稀释至10ml,抽取0.1ml皮内注射。 12..注射用头孢甲肟规格0.5g(皮试药液浓度为500ug/ml) 取0.9%氯化钠注射液10ml稀释原药后,抽取0.1ml,再用0.9%氯化钠注射液稀释至10ml,抽取0.1ml皮内注射。 13.注射用青霉素规格80万U(皮试药液浓度为500U/ml) 取0.9%氯化钠注射液8ml稀释原药后,抽取0.1ml,再用0.9%氯化钠注射液稀释至20ml,抽取0.1ml皮内注射。 14.注射用青霉素规格400万U(皮试药液浓度为500U/ml) 取0.9%氯化钠注射液8ml稀释原药后,抽取0.1ml,用0.9%氯化钠注射液稀释至10ml,
体外诊断试剂临床试验运行管理制度和工作流程
体外诊断试剂临床试验运行管理制度和工作流程
体外诊断试剂临床试验运行管理制度和工作流程 Ⅰ.目的: 为保证我院体外诊断试剂临床试验科学、规范和有序进行,充分保障受试者的权益。 Ⅱ.范围:适用于我院开展的体外诊断试剂临床试验。 Ⅲ.规程: 遵照《体外诊断试剂注册管理办法》、《体外诊断试剂临床研究技术指导原则》等法律法规的相关要求,参照国内外开展器械临床试验的经验,制定本制度与流程。 本院的体外诊断试剂临床试验由药物临床试验机构办公室(以下简称机构办)组织相关专业实施,实行“准入制”,未经GCP 机构办同意进行的临床试验,概不予认可。 1.立项准备。 1.1.申办者/CRO(合同研究者组织)联系机构办、意向科室共同 确定主要研究者。CRA提交“体外诊断试剂临床试验立项申请表”(附件1),并按照“体外诊断试剂临床试验机构立项文件列表”(附件2)准备临床试验相关完整材料一份,交机构办公室。 1.2.PI提出研究小组成员,填写“主要研究者履历”(附件3) “项目研究团队成员表”(附件4),由CRA连同试验资料一起递交机构办公室。 研究小组人员的资质必须符合以下要求:
?研究团队成员必须经GCP培训并获取证书; ?主要研究者组建研究团队,包括:检验医学、临床医学、流行病学、统计学等人员;药物代谢研究人员(如需要);其它相关科室人员(如需要) 1.3.文件资料请用黑色、厚壳、双孔文件夹装订,文件夹侧标使 用统一的模板(附件9),第一页均为文件目录,每项文件中间用带数字标识的隔页纸分隔。请按文件目录所列文件顺序排列各项文件,文件夹中不包括的文件无需列入目录。文件多的项目请准备多个“机构文件夹”,编号“①,②, ③……”。 2.受理立项。 机构对送审材料及研究小组成员资质进行审核,决定是否同意立项。若同意,则向伦理委员会发出“临床试验审批受理通知”(附件5)。 3.伦理委员会审核。 3.1.申请者持“临床试验审批受理通知”(附件5)按照伦理委 员会要求准备材料,将申报材料交伦理委员会进行伦理评审3.2.评审结束后,将“伦理委员会接受临床试验回执”(附件 5)和“伦理委员会审批件”原件交回机构办公室。若按伦理委员会要求所提交项目资料有所修订,要将已修订的项目资料补交到机构办公室备案。 4.协议签订。
