三种大肠杆菌高效感受态的制备及转化

第34卷 第4期2006年 4月 华 中 科 技 大 学 学 报(自然科学版)
J.Huazhong Univ.of Sci.&Tech.(Nature Science Edition )Vol.34No.4 Apr. 2006
收稿日期:2005203207.
作者简介:涂知明(19652),男,副教授;武汉,华中科技大学生命科学与技术学院(430074).
E 2m ail :hegy @https://www.360docs.net/doc/9216453114.html, (何光源)
基金项目:国家高技术研究发展计划资助项目(2002AA224031);华中科技大学博士论文基金资助项目.
三种大肠杆菌高效感受态的制备及转化
涂知明 陈明洁 何光源 常俊丽
(华中科技大学生命科学与技术学院,湖北武汉430074)
摘要:描述了一种改良的高效细菌感受态的制备和感受态细胞的保藏及细菌的转化方法.三种不同的大肠杆菌分别是D H5
α,T G1和XL1blue ,其中最有效的是XL1blue.每种菌株的感受态细胞制备的最佳光密度(OD 600值)不同.对感受态细胞的存储时间及其与转化效率之间的关系也进行了研究,结果显示感受态细胞可
以在-20℃存储7d ,在-70℃存储15d.将常见的方法做了三种改进:首先是将CaCl 2溶液改为TB 溶液;其次是将培养基由LB 换成S.O.C ;再就是在质粒对感受态细胞的转化过程中加入DMSO 或PEG 8000.改良的细菌转化系统比常见的方法能提高转化效率约1000倍,是一种高效的细菌转化系统.关 键 词:感受态细胞;大肠杆菌;质粒;保藏;转化
中图分类号:Q943.2 文献标识码:A 文章编号:167124512(2006)0420112204
Competent cells preparation and plasmid transformation
for three Escherichia coli strains
T u Zhi mi ng Chen M i nj ie He Guang y uan Chang J unli
Abstract :An efficient bacterial t ransformation system was described for t he preparation of competent cells ,plasmid preparation ,and for t he storage in bacterial stocks.Three different st rains of Esche 2
richi a coli t hat were tested were D H5
α,T G1and XL1blue ,and t he most efficient st rain being XL1blue.The optimal optical density (OD 600)range for co mpetent cell p reparatio n varied for each of t he st rains.The storage time of competent cells and it s correlation to transformation efficiency were st ud 2ied.Three critical alterations to p revious met hods were made ,which were t he changing of t he normal CaCl 2solution to TB solution ,t he changing of t he medium f rom LB to S.O.C ,and addition of DMSO or PEG 8000during t ransformation.The t ransformatio n efficiency was increased by about 1000times by t he use of t his improved bacterial t ransformation system.
K ey w ords :competent cells ;Escherichi a coli (E.coli );plasmid ;storage ;t ransformation
Tu Zhiming Assoc.Prof.;College of Life Sci.&Tech.,Huazhong Univ.of Sci.&Tech.,Wuhan
430074,China.
质粒转化进入细菌的感受态细胞是分子克隆
的关键技术.在20世纪70年代早期科恩成功地转化了R 因子并且利用氯化钙法将质粒重组进入大肠杆菌的细胞内,由于其方便性,这种方法从那时起被广泛应用.电穿孔技术是另一种转化方法,其转化效率可以高至1×109~1×1010转化株/μg DNA.然而很多实验室没有电穿孔技术所
需要的特殊仪器.Tsen 等发现大肠杆菌的某些菌株可以自然地在细胞质中与细胞外质粒低频率结合[1].Chen 等提出一种方便快捷的质粒转化大肠杆菌的方法[2],它几乎与传统的钙转化方法有相同的转化效率,而且这种方法大约只需要2min.基于这种方法,建立了一个利用大肠杆菌感受态细胞转化质粒的系统,感受态细胞和质粒能长期
储存,而且便于以后实验的扩增和利用[3].
1 实验材料
菌株:E.coli D H5α和 E.coli T G1由武汉大学提供,E.coli XL1blue由湖北大学提供.
质粒:标记基因质粒p UC18,pD E4, pD E108,pDE110,pA HC25,pA HC20, p U GFP和高分子量麦谷蛋白基因质粒1Ax1, p1Dx5,p1Dy10,为本实验室所保存.
细菌培养基:LB培养基和S.O.C培养基.
TB(CaCl2)溶液:Pipes3.021g/L,CaCl2?2H2O 2.205g/L,KCl18.637g/L,MnCl2?4H2O10.885g/L.所有成分除了MnCl2外被混合并且用KO H将p H值调至6.7.然后将MnCl2溶解,溶液通过0.45μm的过滤器过滤灭菌并于4℃储存.
DMSO(二甲基亚砜)购自AL P HA L TD生物技术公司(SigmaD5879).
PEG8000购自华美公司,PEG8000(40%)溶液储存于-20℃.
2 方法
2.1 感受态细胞的制备
感受态细菌细胞的转化采用氯化钙的方法.不含有质粒的大肠杆菌菌株在室温下使其解冻并加入40mL S.O.C的液体培养基.在37℃培养1h,然后将其转移到37℃摇床上以200r/min速度培养2~3h,直到OD600达到0.2~0.4.不同细菌菌株的最适宜OD600是不同的.在4℃下以8000r/min的速度离心1min,然后用一半体积(20mL)已灭菌的预冷的TB(CaCl2)溶液进行悬浮,并在冰上保存25min.如上进行另一次离心后,所得到的细胞沉淀用十分之一体积(4mL)预冷的TB(CaCl2)溶液进行悬浮获得感受态细胞.感受态细胞可于4℃下保存3d.
2.2 感受态细胞的储存
转移1.6mL的感受态细胞悬浮液至已消过毒的冷藏管内,并加入已灭菌的0.4mL甘油使最终浓度达到20%,混匀.甘油储液可在-4℃, -20℃和-70℃下分别储存待用.
2.3 细菌的转化
氯化钙法使细菌产生感受态的细胞,该细胞在热震惊后吸收DNA,然后DNA分子会在宿主细胞中复制.在热震惊后,为帮助细菌细胞恢复,细胞被暂时放在无选择性的培养基上培养.然而,由于只有少数细菌细胞被转化,并且不是所有的质粒都能遗传给每一个子细胞,因此必须对含有质粒的细菌进行抗生素选择.大肠杆菌菌株如XL1blue,D H5α和T G1对普通的抗生素如氨苄青霉素敏感.质粒带有抗生素抗性的基因,因而转化之后,细菌被涂在含有氨苄青霉素的培养基上,只有转入外源质粒的细菌才能对氨苄青霉素产生抗性并形成菌落.
优化的细菌转化步骤:37℃下预热固体S.O.C和含氨苄青霉素的S.O.C(最终浓度100μg/mL)平板1h;取100μL感受态细胞并加入1μg/μL质粒0.5μL;加入DMSO或PEG8000 (40%)1μL;在冰上放置30min;42℃处理90s (更快的转化方法,此步可以忽略);冰上放置30 min;加入400μL液体S.O.C培养基;37℃下在摇床上培育45min;将混合液的一半(50μL)涂在含有氨苄青霉素的预热的平板上,另一半混合液涂在没有氨苄青霉素的对照板上;在S.O.C 平板培养基上37℃培养过夜(12~16h).
3 结果
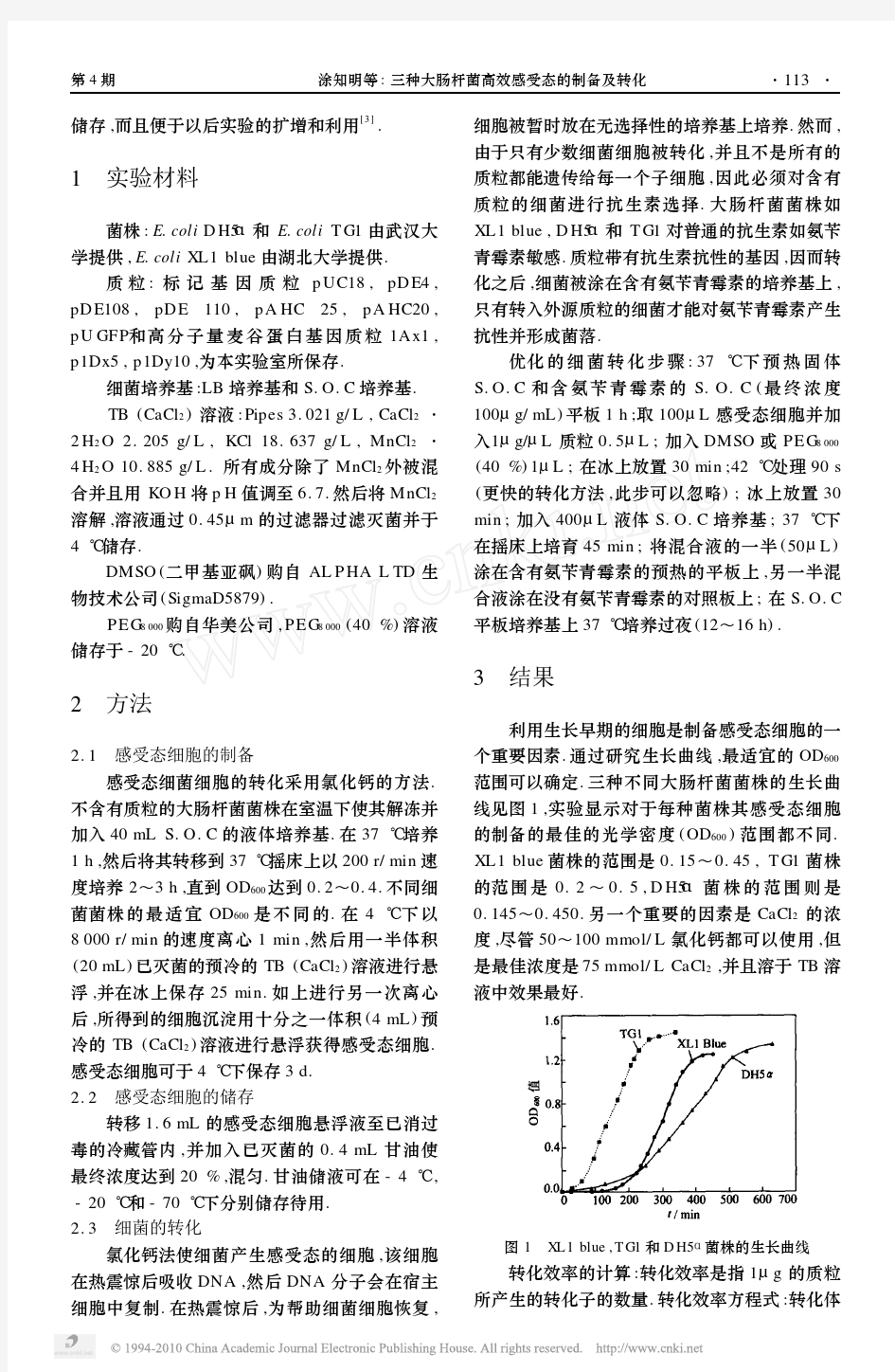
利用生长早期的细胞是制备感受态细胞的一个重要因素.通过研究生长曲线,最适宜的OD600范围可以确定.三种不同大肠杆菌菌株的生长曲线见图1,实验显示对于每种菌株其感受态细胞的制备的最佳的光学密度(OD600)范围都不同. XL1blue菌株的范围是0.15~0.45,T G1菌株的范围是0.2~0.5,D H5α菌株的范围则是0.145~0.450.另一个重要的因素是CaCl2的浓度,尽管50~100mmol/L氯化钙都可以使用,但是最佳浓度是75mmol/L CaCl2,并且溶于TB溶液中效果最好
.
图1 XL1blue,T G1和D H5α菌株的生长曲线
转化效率的计算:转化效率是指1μg的质粒所产生的转化子的数量.转化效率方程式:转化体
?
3
1
1
?
第4期 涂知明等:三种大肠杆菌高效感受态的制备及转化
总数=菌落数×稀释倍数×转化反应原液总体积/涂板菌液体积,例如:稀释1000倍的转化菌有21个菌落,其转化子总数=4.2×104个.
转化效率=转化子总数/质粒DNA加入量.若加入0.5μL(1μg/μL)DNA质粒,则转化效率为8.4×105cf u/μg,每个质粒DNA的转化效率在各不同菌株中差异由表1列出,这是六组重复所得的平均值.通过利用不同的方法作用于不同的菌株,其不同的质粒的转化效率见表1.用p UC18建立系统,并且用p U GFP,pA HC25, p1Ax1,p1Dx5,p1Dy10来测试,然后计算转化效率的平均值.接着用这种改进方法来扩增其他质粒如pD E110,pA HC20等,显示XL1是最有效的菌株而且改进方法比普通的方法[4]的转化效
表1 几种不同质粒对三种菌株的转化率的比较
质粒
XL1blue菌株D H5α菌株T G1菌株常规方法快速方法本文方法常规方法快速方法本文方法常规方法快速方法本文方法pUC18 6.51×1067.10×1058.18×108 2.31×106 3.50×105 4.15×108 2.01×106 3.80×105 4.50×108 pU GFP7.79×106 6.70×1058.85×108 1.66×106 3.20×105 2.63×108 1.25×106 2.20×105 4.72×108 pA HC25 6.86×1067.80×1059.09×108 1.56×106 2.70×105 4.13×108 1.46×106 2.90×105 5.39×108 p1Ax17.13×106 6.40×1058.60×108 1.25×106 2.30×105 4.52×108 1.08×106 2.70×105 4.26×108 p1Dx57.09×106 6.98×1058.90×108 1.31×106 2.08×105 3.99×108 1.21×106 2.08×105 4.19×108 p1Dy108.17×106 6.75×1057.80×108 1.20×106 1.97×105 3.56×108 1.31×106 1.97×105 3.25×108
率提高了大约1000倍.
不同温度下感受态细胞储存时间的不同对转化率有影响,用pA HC25质粒转化已分别在-4℃,-20℃和-70℃储存了1h,0.5d,1d,2 d,3d,5d,7d,10d,15d,20d的感受态细胞XL1 blue.用普通的方法测试,结果显示感受态细胞XL1blue可以在-20℃被储存并在1h到7d之内不会有明显的转化率的下降,相反,其转化率从第3d到第7d还有所升高,然后缓慢降低.在不同温度下感受态细胞的储存时间对转化率的影响结果显示,感受态细胞在-20℃下储存7d以下与在-70℃下储存15d以下都不会影响它们的转化能力.
4 讨论
转化效率受很多因素的影响,最重要的因素是细菌细胞必须处在它们的对数生长早期.能够吸收DNA的细菌称为感受态细菌,可以通过氯化钙处理产生.细菌膜可以透过氯离子,但是不能透过钙离子.当氯离子进入细胞,水分子也伴随进入.流入的水使细胞膨胀并导致DNA的吸收.实验显示具有不同生长特性的大肠杆菌,如XL1 blue,T G1和D H5α,其感受态细胞的制备的最佳的光学密度OD600范围都不同,从生长过度或发育不全的细菌制备的感受态细胞,转化能力将会减退或丧失.
第二个会影响转化效率的因素是感受态细胞的储存期间.Dargert M[4]报告感受态细胞能被储存在4℃的氯化钙溶液中24~48h.在最初的12~24h之间,其转化效率提高3~5倍,而后减低到平均水平.本实验显示感受态细胞可以在-70℃下保存15d而没有明显的转化力的下降.若感受态细胞在-20℃下保存,最高的转化效率出现在2~7d内.如果储存时间超过7d,转化效率会急剧下降.若感受态细胞在4℃下储存,他们会在3d内失去转化能力.
另一个重要的因素是氯化钙的浓度.尽管50~100mmol/L氯化钙都能使用,但最佳浓度是75mmol/L CaCl2溶于TB溶液中.Brian和Heler第一次使用TFB替换传统的氯化钙溶液[5].用TB溶液使转化效率提高了一百多倍.在37℃使用传统的CaCl2方法,转化子总数/质粒DNA加入量为1×105~10×105cf u/μg.在同样条件下用TB法导致转化子总数/质粒DNA加入量是1×107~9×107cf u/μg.
在细菌转化过程中加入DMSO或PEG8000也能影响转化效率.Hanahan发现加入DMSO可极大地提高转换效率[6],作者过去也发现PEG8000有同样效果[7,8].本实验显示在细菌转化过程中加入DMSO或PEG8000可以使转化效率比文献[2]的方法提高100~300倍.
细菌的培养基也可以影响转化的效率[9]. S.O.C比LB培养基更有营养,因此导致细菌的快速生长;相对于LB培养基,S.O.C培养基中转化株不仅可以在其后的12h就观察到,而且转化效率较高,S.O.C培养基比LB培养基的效率高出10~30倍.
热震惊对DNA的吸收的作用有一些争论,但通过加热,氯化钙的效果会增强.当大肠杆菌被
?
4
1
1
? 华 中 科 技 大 学 学 报(自然科学版) 第34卷
加热至42℃时,一系列的热休克基因会表达.42℃以上细菌吸收DNA 的能力下降,更极端的温度下细菌会死亡.尽管不是很必要,但热震惊的确能提高转化效率.文献[2]提出的方法省略了热休克,但转化效率降低了近两个数量级,因此要提高转化效率还需要热休克.
参
考
文
献
[1]Tsen S D ,Heler M K.Natural plasmid transforma 2
tion in Escherichia coli [J ].J Biomed Sci ,2002,9(3):2462252
[2]Chen X ,Guo P ,Xie Z ,et al.A convenient and rapid
method for genetic transformation of E.coli with plasmids [J ].Antonie Van Leeuwenhoek ,2001,80(324):2972300.
[3]陈明洁,刘 勇,涂知明,等.多重PCR 法快速鉴定转
基因小麦植株及后代[J ].华中科技大学学报:自然科学版,2004,32(9):1052107.
[4]Sambrook J ,Fritsch E D ,Maniatis T.Molecular clo 2
ning :a laboratory manual [M ].2nd ed.New Y ork :Cold Spring Harbor Laboratory Press ,1989:49255.[5]Brian P ,Heler M K.High efficiency 5min transfor 2
mation of E.coli [J ].Nucl Acids Res ,1996,24(3):5362537.
[6]Hanahan D ,Jessee J ,Bloom F R.Plasmid transfor 2
mation of Escherichia coli and other bacteria [J ].Methods Enzymol ,1991,20(4):63265,113.[7]涂知明,柯丽华.酶标HBV DNA 探针的研制及应
用[J ].病毒学杂志,1991,6(2):1322137.
[8]Tu Zhiming ,Ke Lihua ,He Guangyuan.The applica 2
tion of Alkaline Phosphatase labeled HBV probe in serum detection[J ].Virus Genes ,2004,28(2):1532158.
[9]宋 洁,涂知明.非嗜碱性突变株的筛选[J ].湖北医
科大学学报,1998,19(2):1062107.
(上接第111页)
[2]Philip J ,Davies A ,Richard H ,et al.The sensitiza 2tion of thermal decomposition of ammonium polyphos 2phate by selected metal ions and their potential for im 2proved cotton fabric flame retardancy [J ].Polymer Degradation and Stability ,2005,88:1142122.[3]苗国平.中聚合度磷酸铵的合成及其对木材阻燃处理
的研究[J ].东北林业大学学报,1995,23(4):72277.
[4]Riva A ,Camino G ,Fomperie L ,et al.Fire retardant
mechanism in intumescent ethylene vinyl acetate com 2positions [J ].
Polymer Degradation and Stability ,
2003,82:3412346.
[5]肖新颜,涂伟萍,杨卓如,等.膨胀型防火涂料的阻燃
机理研究[J ].华南理工大学学报:自然科学版,1998,
26(12):77282.
[6]肖新颜,涂伟萍,杨卓如,等.阻燃体系对涂料防火性
能影响的研究[J ].化学工业与工程,1998,15(2):62
11.
[7]廖凯荣,卢泽俭,苏 瑾.聚磷酸铵型膨胀阻燃剂对聚
丙烯酸的阻燃作用[J ].高分子材料科学与工程,
1999,15(2):59262.
[8]Levchik S ,Levchik G F ,Balabanovich A I.Mecha 2nistic study of combustion performance and thermal decomposition behaviour of nylon 6with added halo 2gen 2f ree fire retardants [J ].Polymer Degradation and Stability ,1996,54:2172222.
[9]Matsuda N ,Shirasaka H.Thermal degradation and flame retardancy of ethylene 2vinyl alcohol copolymer blended with ammonium polyphosphate [J ].Polymer Degradation and Stability ,2003,79:13220.
?
511?第4期 涂知明等:三种大肠杆菌高效感受态的制备及转化
CaCl2法制备大肠杆菌感受态细胞
CaCl2法制备大肠杆菌感受态细胞 原理: 转化(Transformation):将外源DNA分子引入受体细菌,使之获得新的遗传性状。 受体细菌一般是限制修饰系统缺陷的变异株,不含限制性内切酶和甲基化酶的突变体(R-,M-),可以容忍外源DNA分子进入体内并稳定地遗传给后代。受体细胞经过一些特殊方法,如电击或CaCl2、RbCl/KCl等化学试剂的处理后,细胞膜的通透性增高,成为感受态细胞(Compenent cells),使外源DNA分子得以进入。 目前常用的感受态细胞制备方法有CaCl2和RbCl/KCl法,RbCl/KCl法制备的感受态细胞转化效率较高,但CaCl2法简便易行,且其转化效率完全可以满足一般实验的要求,制备出的感受态细胞暂时不用时,可加入无菌甘油至总体积15%,于-70℃保存半年之久,因此CaCl2法为使用更广泛。 准备: 1、配制0.05mol/L CaCl2-15%甘油(可用0.1mol/L CaCl2和30%甘油等体积混合) 混合溶液,高温高压灭菌; 注:CaCl2必须为分析纯以上。 2、实验中所需的所有试管、培养瓶、离心管等均要用去离子水彻底清洗干净, 高温高压灭菌; 注:最好有制备感受态细菌专用的一套实验器材。 3、受体菌的培养:从非选择性LB平板上挑取E.coli单菌落,接种于3-5ml LB液 体培养基 ( )中,37℃振荡培养过 夜至对数生长中后期。将该菌悬液以1:100的比例接种于50~100ml LB液体培养基中,37℃振荡培养2.5小时至OD600=0.5。注:培养时间不宜超过2.5小时,否则不能达到最高转化效率。 实验步骤: 1、细菌的收获:培养液冰浴5分钟后,4℃5000g离心5分钟。 注:(1)冰浴时间不要超过10分钟;(2)或者4℃8000g离心2分钟,速度太快或时间太长对细菌状态不利,并且不利于下步洗涤。(3)若出现很多黑色沉淀(细菌碎片),说明有多量细菌死亡,此时细菌状态并不好,但若只有少量黑色沉淀,或对转化效率要求不高,亦可继续进行。 2、用预冷的去离子水洗涤沉淀,4℃5000g离心5分钟。 注:(1)洗去细菌碎片和残留的培养液;(2)洗涤时间宜短不宜长。 3、沉淀加入2ml预冷的0.05mol/L CaCl2-15%甘油混合溶液,轻吹散,冰浴5分 钟,4℃5000g离心5分钟。 注:此时可见细菌沉淀为白色,体积也胀大为最初沉淀体积的数倍。 4、沉淀加入2ml预冷的0.05mol/L CaCl2-15%甘油混合溶液,轻吹散,即成为感 受态细胞悬液。分装成50~100μl的小份,贮存于-70℃可保存半年。
(完整版)大肠杆菌感受态细胞的制备.doc
大肠杆菌感受态细胞的制备 标签: tr..,Ca..,co.. 分类:细胞技术> 感受态细胞 来源: 实验管理实验概要 大肠杆菌感受态细胞的CaCl2 法制备及质粒转化 实验原理 处于对数生长期的细菌经 CaCl2 处理后接受外源 DNA 的能力显著增加。细菌处于容易吸收外源DNA 的状态叫感受态。 在自然条件下,很多质粒都可通过细菌接合作用转移到新的宿主内,但在人工构建的质粒载体 中,一般缺乏此种转移所必需的 mob 基因,因此不能自行完成从一个细胞到另一个细胞的接合转 以移。如需将质粒载体转移进受体细菌,需诱导受体细菌产生一种短暂的感受态,摄取外源 DNA 。 转化( Transformation)是将外源DNA 分子引入受体细胞,使之获得新的遗传性状的一种 手段,它是微生物遗传、分子遗传、基因工程等研究领域的基本实验技术。转化过程所用的受体细胞一般是限制修饰系统缺陷的变异株,即不含限制性内切酶和甲基化酶的突变体 (R-,M- ),它可以容忍外源DNA 分子进入体内并稳定地遗传给后代。受体细胞经过一些 特殊方法(如电击法, CaCl2 ,RbCl(KCl) 等化学试剂法)的处理后,细胞膜的通透性发生 了暂时性的改变,成为能允许外源DNA 分子进入的感受态细胞( Compenent cells )。进入受体细胞的 DNA 分子通过复制、表达实现遗传信息的转移,使受体细胞出现新的遗传性状。 将经过转化后的细胞在筛选培养基中培养,即可筛选出转化子(Transformant ,即带有异 源 DNA 分子的受体细胞)。目前常用的感受态细胞制备方法有CaCl2 和 RbCl(KCl) 法,RbCl(KCl) 法制备的感受态细胞转化效率较高,但CaCl2 法简便易行,且其转化效率完全可 以满足一般实验的要求,制备出的感受态细胞暂时不用时,可加入占总体积15%的无菌甘油于-70 ℃保存(半年),因此CaCl2 法使用更广泛。 主要试剂 (1)0.1mol/L CaCl2溶液 (2)LB 液体培养基
农杆菌感受态细胞的制备原理和实验步骤及验证
农杆菌电击感受态的制备及电击转化 表达载体pB-2mb-FRO-1.7A和pB-2mb-1.7A空载体的农杆菌(EHA105)电击转化 (1)抽提纯化pB-2mb-FRO-1.7A和pB-2mb-1.7A空载体的重组质粒 pB-2mb-FRO-1.7A重组载体和pB-2mβ-1.7A空载体的(DH5α)菌种接种于5ml LB(含卡那霉素50mg/L)液体培养基中,37℃,200rpm震荡培养过夜。按V-GENE公司的质粒提取试剂盒提取pB-2mb-FRO-1.7A重组质粒。 (2)取200ml型号的电击杯用无水乙醇浸泡,晾干。 (3)农杆菌EHA105电击预备处理。 I. 接种于5ml YEP(含链霉素Sm50mg/L)液体培养基中,28℃,200rpm震荡培养过夜至OD600值为0.4。EHA105 II. 离心管中收集1ml菌液,4℃,8000rpm,离心30s。1.5ml III. 去残液,沉淀用200μl ddH2O充分悬浮,4℃,8000rpm,离心30s。 IV. 重复步骤ⅲ三次。 V. 去残液,沉淀用200ml ddH2O充分悬浮,即为电击用农杆菌EHA105感受态。加入200μl灭菌甘油混匀后置于-80℃备用。 (4)电击 I. 分别取10ml pB-2mb-FRO1-1.7A和pB-2mb-1.7A重组质粒至200μl EHA105感受态中,轻打混匀,然后转移至电击杯中,置冰上。 II. 准备好电击装置(BioRad),电压为2.5V,用手按住电击按钮,直到啪的一声电击完毕。 III. 室温静置2min后加入800ml YEP培养液,28℃静置1h,然后28℃,200rpm培养2h。IV. 离心30s,收集菌液,沉淀用200ml ddH2O悬浮,用玻璃棒涂布含含卡那霉素50mg/L 和含链霉素Sm50mg/L的YEP固体培养基平板,28℃培养48h。8000rpm 1.制备农杆菌电转感受态 (1)挑取根癌农杆菌EHA 105单菌落,接种于5mlLB〔含利福平(Rif) 50mg/L,;链霉素 100mg/L)液体培养基中,28'C, 220rpm震荡培养过夜。 (2)将2m1过夜培养的菌液加到50ml含同样抗生素的LB培养基中,28'C, 220rpm震荡 3-4小时,至OD560=0.5左右。 (3) 5000rpm离心5分钟,去上清。 (4) 加入40m1 10%甘油悬浮菌体,冰浴30min. (5) 4'C, 5000rpm离心5分钟,去上清。 (6 加入30mL10%甘油重悬浮菌体,4'C, 5000rpm离心5分钟, (7)重复步骤6一次,去上清,加入2ml10%甘油悬浮,分装于1.5ml的离心管中(200 p 1/ 管)备用。 2 农杆菌感受态的电转化 〔I)取2 ul质粒加到200 u I EHA 105感受态细胞中,轻轻混匀,冰浴 30分钟。 (2)把质粒和感受态混合液吸入电极杯,电击转化。 (3)马上加入lml新鲜的LB液体培养基,28'C, 150rpm轻摇4-6小时。 (4)收集菌体涂布于含有链霉素100mg/L),利福平(50mg/L)及质粒所含的抗性的LB固体培
大肠杆菌感受态细胞的制备实验具体步骤及说明
大肠杆菌感受态细胞的制备实验具体步骤及详细说明 带有外源DNA 的重组质粒,在体外构建后,导入宿主细胞,随着细胞的大量复制、繁殖,才能够有机会获得纯的重组质粒DNA,该过程称之为转化过程。受体细胞经过一些特殊方法(如:CaCl2,RuCl 等化学试剂)的处理后,细胞膜的通透性发生变化,能容许外源DNA 的载体分子通过。 带有外源DNA 的重组质粒,在体外构建后,导入宿主细胞,随着细胞的大量复制、繁殖,才能够有机会获得纯的重组质粒DNA,该过程称之为转化过程。受体细胞经过一些特殊方法(如:CaCl2,RuCl 等化学试剂)的处理后,细胞膜的通透性发生变化,能容许外源DNA 的载体分子通过。 具体步骤 1、从37℃培养16-20 h的平板中挑取一个单菌落(直径2-3 mm),转到一个含有100 ml LB或SOB培养基的1L烧瓶中。于37℃剧烈振摇培养3 h。一般经验,1 OD600约含有大肠杆菌DH5α 109个/mL。 2、将细菌转移到一个无菌、一次性使用的、用冰预冷的50 ml聚丙烯管中,在冰上放置10 min,使培养物冷却至0℃。 3、于4℃用Sorvall GS3特头(或与之相当的转头)以4 100 r/min离心10 min,以回收细胞。 4、倒出培养液,将管倒置1 min以使最后的痕量培养液流尽。
5、每50 ml初始培养液用30 ml预冷的0.1 mol/LCaCl2-MgCl2溶液(80 mmol/L MgCl2,20 mmol/L CaCl2)重悬每份细胞沉淀。 6、于4℃用Sorvall GS3转头(或与之相当的转头)以41 00 r/min离心10 min,以回收细胞。 7、倒出培养液,将管倒置1 min以使最后的痕量培养液流尽。 8、每50 ml初始培养物用2 ml用冰预冷的0.1 mol/L CaCl2(或TFB)重悬每份细胞沉淀。 9、此时,可以用新鲜制备的感受态细胞直接做转化实验,也可以将细胞冻存于- 70℃。 注意事项 1. 为达到高效转化,活细胞数务必少于108个细胞/mL,对于大多散大脑杆菌来说,这相当于OD值为0.4左右。为保证细菌培养物的生长密度不致过高,可每隔15-20 min测定OD600值来监测,用监测的时间及OD值列一个图表,以便预测培养物的OD600值到0.4的时间,当OD600值达到0.35时,收获细菌培养物。 2. 在菌株与菌株之间,OD值与每毫升中活细胞散间的关系变化很大,因此有必要通过漶量特定脑杆菌的生长培养物在生长周期的不同时相的OD600值,并
农杆菌感受态制备与转化
农杆菌感受态制备与转化 普通农杆菌感受态制备与转化:方案一 1. 挑单菌落于2ml YEP培养基(含Rif20mg/ml)中28℃过夜活化。 2. 取2ml过夜菌液接种于50ml YEP培养基中28℃生长至OD600约等于0.5左右(4hr)。 3. 5k rpm离心5分钟。 4. 在10ml 0.15M NaCl中悬浮细胞。 5. 5 krpm离心5分钟,悬浮细胞于20ml冰预冷的CaCl2。 如不是马上使用,可以将之按200ul分裝储存于-80℃待用。 6. 加1ug DNA于200ul感受态细胞中,冰上放置30分钟。 7. 液氮中冷冻1分钟。 8. 37℃水浴溶化细胞。 9. 加1ml YEP培养基,28℃摇床培养2-4hr(低速)。 10. 离心1分钟,悬浮细胞在100ul YEP培养基中。 11. 涂板,28℃培养2-3天。 电转农杆菌感受态细胞制备与转化方案二 1.挑取单克隆接种于2mlYEP(含50mg/l链霉素)液体培养基,28℃,250rpm,振荡培养过夜。(如用5mlYEP,需培养36h) 2.将菌液按1:100转移至200mlYEP(含50mg/l链霉素)培养液中,28℃,250rpm,振荡培养至OD=0.3(约4~5h)。 3.转入50ml的无菌离心管,4℃,4000rpm离心10min,弃上清。4.用20ml冰浴的HEPES(1mM,PH-7.0)重悬。 5.4℃,4000rpm离心10min,弃上清。 6.重复4、5步骤2~3次。 7.用2ml冰浴的10%甘油重悬。 8.每管100μl分装于1.5ml无菌的Eppendorf管中,-70℃保存。 1mM HEPES的配制:称取0.119gHEPES(MW 238.3)粉末,加水溶解,定容至500ml,用NaOH调pH至7.0,灭菌后待用。 注:HEPES需现用现配。 电击法转化农杆菌感受态细胞 1.取出农杆菌感受态细胞于冰上冻融。 2.加2μl质粒DNA于100μl感受态细胞中,用枪头轻轻搅拌混匀。3.取出细胞与质粒的混合物转入电击杯中(电击杯-20℃预冷),在2500V高压下电击。 4.取出电击杯,加入500μl预冷的YEP培养液(不含抗生素),轻轻吹打混匀,吸出菌液转入1.5ml离心管中,28℃,200rpm振荡培养5h。 5.取30-40μl菌液涂在含相应抗生素的YEP平板上,28℃倒置培养
实验三 大肠杆菌感受态细胞的制备(新)
实验三大肠杆菌感受态细胞的制备 【课前预习】 1、大肠杆菌感受态细胞的制备及转化的基本原理是什么? 2、大肠杆菌感受态细胞的制备可以采用哪些方法? 【目的要求】 1、了解感受态细胞生理特性及制备条件; 2、掌握大肠杆菌感受态细胞制备方法; 【基本原理】 所谓感受态,是指细菌生长过程中的某一阶段的培养物,只有某一生长阶段中的细菌才能作为转化的受体,能接受外源DNA而不将其降解的生理状态。它是由受体菌的遗传性状所决定的,同时也受菌龄、外界环境因子的影响。cAMP可以使感受态水平提高一万倍,而Ca2+也可大大促进转化的作用。细胞的感受态一般出现在对数生长期,新鲜幼嫩的细胞是制备感受态细胞和进行成功转化的关键。感受态形成后,细胞生理状态会发生改变,出现各种蛋白质和酶,负责供体DNA 的结合和加工等。细胞表面正电荷增加,通透性增加,形成能接受外来的DNA 分子的受体位点等。 基因工程技术中最常用的是氯化钙转化技术,虽然对其基本原理仍然不完全清楚,但是比较认同的看法是,细菌处干0℃、CaCl2低渗溶液中,细胞膨胀形成球状,转化混合物中的DNA形成抗DNase的羟基-钙磷酸复合物粘附与细胞表面,经42℃短时间热冲击处理,促进细胞吸收DNA复合物,之后细菌在富含营养的培养基上生长,球状细胞复原并分裂繁殖,重组质粒在转化的细菌中,表达目的基因,因而在选择性培养基平板中,可以选出阳性细菌转化子。Ca2+处理的感受态细胞,一般每微克DNA能转化105-106个细菌、环化的质粒DNA 愈小,转化率愈高。环化的DNA分子比线性DNA分子转化率高1000倍。CaCl2转化法的优点是:简单快速,重复性好,菌株适用范围广。 另外,电击法也可用于转化过程,电击法不需要预先诱导细菌的感受态,依赖短暂的电击,利用瞬时高压电流(数千伏特)处理细胞悬浮液,使微生物细胞膜在高压电作用下发生去极化,产生微孔,悬液中溶解的核酸即可通过细胞膜上的空洞进入细胞内部,转化率最高达109-1010转化子/μg闭环DNA。 制备出的感受态细胞暂时不用时,可加入占总体积15%的无菌甘油或-70℃保存(有效
感受态细胞的制备(DH5α大肠杆菌)
感受态细胞的制备(DH5α) 一、准备工作 所有试剂、容器均需提前预冷。 1、实验器械 4℃离心机(50ml离心管),37℃恒温箱,37℃摇床,超净台(使用前需要紫外消毒15min 至少);0.22μm的滤器2个(过滤灭菌TfB2种溶液),10ml注射器2个;冰盒;高压灭菌的1.5mlEP管1盒,与离心机配套的50ml离心管6个(高压灭菌),高压灭菌的500ml 锥形瓶2个,高压灭菌的100ml玻璃瓶2个,高压灭菌的1ml枪头和200μl枪头各一盒。 2、试剂配制(甘油特别难吸,用蓝枪头慢慢吸吧) ① LB平板:单纯LB平板,加有amp或有kana的(制板时需标注好类型,时间)。 ② SOB培养基(Super Optimal Broth) ③ TfBⅠ:(100ml制备量)分别称取乙酸钾0.294g,MnCl2 0.99g,KCl 0.146g,CaCl2 0.111g,置于200ml烧杯中,加入15ml甘油和85mlDDW,摇晃,使其全部溶解。然后在安全橱中用孔径为0.22μm的滤器过滤混合液,置于高压灭菌的100ml玻璃瓶中,4℃保存,使用前必须预冷。(装在50ml离心管,封口4度保存) ④ TfBⅡ(20ml制备量,每次现用现配,装在50ml离心管):分别称取MOPS 0.046g,CaCl2 0.167g,KCl 0.015g,置于50ml烧杯中,加入3ml甘油和17mlDDW, 摇晃,使其全部溶解。然后在安全橱中用孔径为0.22μm的滤器过滤混合液,使用前必须预冷。
配制量 1 L 配制方法 1.配制250 mM KCl溶液。(50ml离心管分装) 在90 ml的去离子水中溶解l.86 g KCl后,定容至100 ml。 2.配制2 M MgCl2溶液。(50ml离心管分装) 在90 ml去离子水中溶解4.06g MgCl2 6H2O后,定容至100 ml,高温高压灭菌。 5.量取10 m1 250 mM KCl溶液,加入到烧杯中。 6.滴加NaOH小块,调节pH值至 7.0。 7.加入去离子水将培养基定容至l L。 8.高温高压灭菌后,4℃保存。 9.使用前加入5 ml灭菌的2 M MgCl2溶液。 LB培养基 配制量 1 L 配制方法 3.滴加固体NaOH,调节pH值至7.0。 4.加去离子水将培养基定容至1 L。 5高温高压灭菌后,4度保存。
农杆菌感受态细胞的制备及转化
农杆菌感受态细胞的制备及转化、浸润烟草 1)挑取农杆菌单菌落于3 ml Sm(1000倍稀释)抗性的LB液体培养基中,28o C振荡培养过夜; 2)取过夜培养菌液500μl加入到50ml的Sm抗性的LB液体培养基中,28o C振荡培养至OD600为0.5; 3)5000rpm离心5min,倒掉培养液; 4)加入10ml 0.15M NaCl悬浮农杆菌细胞,5000rpm 5min; 5)倒掉上清,加入1ml 预冷的20mM CaCl2悬浮细胞,冰浴24h内使用,或者分装成每管200μl,液氮中速冻,保存于-70 o C备用。 取200μl感受态细胞,加入1ug质粒DNA,液氮中速冻1min,37o C水浴5min,加入1ml LB,28o C慢速振荡培养4-6h后,涂布于含有相应抗生素的固体培养基平板上,28o C 培养约48h。挑取平板上长出的单菌落,接种于LB液体培养基(含有50μg/ml Kan和100μg/ml sm)中,28℃振荡培养过夜,碱裂解法小量提取质粒DNA,进行PCR及酶切鉴定。 用于浸润的菌液制备 MMA buffer:10mmol/L MgCl2(95.21),10mmol/L MES(195.23),100μmol/L 乙酰丁香酮(196.20)(Acetosyringone)(MgCl2 :2g MES :2g 乙酰丁香酮:50ul) 1)取单菌落接种于3ml LB(含有50μg/ml Kan和100μg/ml SM)培养基中28℃振荡培养过夜; 2)取1ml活化后的菌液接入50ml LB(含有50μg/ml Kan和100μg/ml SM)中,28℃振荡培养至合适浓度OD600约0.8-1.0; 3)4℃,4000rpm离心15min,沉淀用MMA buffer重悬,菌液终浓度为OD600约1.0-2.0; 4)室温静置2hr以上,用1ml注射器对合适苗龄的本生烟进行浸润。
大肠杆菌和农杆菌感受态的制备
A 大肠杆菌感受态的制备(CaCl2法)(《水稻NR和NIR基因启动子的克隆及功能验证》第38页) 1 材料、设备及试剂 1.1材料 大肠杆菌DH5α、BL21、Rossette、JM109菌株 1.2试剂 LB液体培养基: 蛋白胨10g/L 酵母提取物5g/L NaCl 10g/L NaOH(1mol/L)1mL/L 400mL 0.1M/L预冷的CaCl2溶液(高温高压灭菌) 50%甘油 75%酒精 95%酒精 液氮 1.3 实验设备 接种环、酒精灯,打火机,75%酒精,95%酒精,50mL灭菌三角瓶4个,250mL灭菌的三角瓶4个,移液抢(5mL、200μL,1000μL),灭菌的枪头(5mL、200μL,1000μL),离心管(1.5mL,50mL)恒温摇床,灭菌锅,紫外分光光度计,超净工作台,制冰机,冰盒,高速冷冻离心机。 2 实验步骤 1、从新鲜培养的大肠杆菌DH5α平板上挑取一个单菌落,接种于5mL新鲜LB培液体养基中,于37℃,200rpm振荡培养过夜。 2、培养12~16h,取1ml培养物加入到100mL新鲜LB培液体养基中,于37℃,200rpm振荡培养至OD=0.4~0.6(3~4h) 3、在无菌条件下将菌液转移到250mL离心管中,置于冰上10min. 4、于4℃,3000rpm离心5~10 min,弃上清,收集菌体。 5、加入20mL预冷的0.1M/L CaCl2溶液重新悬沉淀,至于冰上30min(严格) 6、于4℃,3000rpm离心5~10 min,弃上清,收集菌体。 7、加入4 mL0.1M/L CaCl2溶液及15%(最终浓度)甘油(50%的甘油1.71428 mL),重悬沉淀。 8、以100μL每管分装于1.5mL冻存管中保存于液氮。 3 试验结果 4 注意事项
大肠杆菌感受态细胞的制备和转化原理
大肠杆菌感受态细胞的制备和转化(原理) 感受态细胞的概念重组DNA分子体外构建完成后,必须导入特定的宿主(受体)细胞,使之无性繁殖并高效表达外源基因或直接改变其遗传性状,这个导入过程及操作统称为重组DNA分子的转化。在原核生物中,转化是一个较普遍的现象,在细胞间转化是否发生,一方面取决于供体菌与受体菌两者在进化过程中的亲缘关系,另一方面还与受体菌是否处于一种感受状态有着很大的关系。 1、感受态细胞的概念 所谓的感受态,即指受体(或者宿主)最易接受外源DNA片段并实现其转化的一种生理状态,它是由受体菌的遗传性状所决定的,同时也受菌龄、外界环境因子的影响。cAMP可以使感受态水平提高一万倍,而Ca2+也可大大促进转化的作用。细胞的感受态一般出现在对数生长期,新鲜幼嫩的细胞是制备感受态细胞和进行成功转化的关键。 制备出的感受态细胞暂时不用时,可加入占总体积15%的无菌甘油或-70℃保存(有效期6个月)。 2、转化的概念及原理 在基因克隆技术中,转化特指将质粒DNA或以其为载体构建的重组DNA导入细菌体内,使之获得新的遗传特性的一种方法。
它是微生物遗传、分子遗传、基因工程等研究领域的基本实验技术之一。 受体细胞经过一些特殊方法(如:电击法,CaCl2等化学试剂法)处理后,使细胞膜的通透性发生变化,成为能容许外源DNA分子通过的感受态细胞。进入细胞的DNA分子通过复制、表达实现遗传信息的转移,使受体细胞出现新的遗传性状。 大肠杆菌的转化常用化学法(CaCl2法),该法最先是由Cohen 于1972年发现的。其原理是细菌处于0℃,CaCl2的低渗溶液中,菌细胞膨胀成球形,转化混合物中的DNA形成抗DNase(DNA酶)的羟基--钙磷酸复合物粘附于细胞表面,经42℃短时间热冲击处理,促使细胞吸收DNA复合物,在丰富培养基上生长数小时后,球状细胞复原并分裂增值。被转化的细菌中,重组子中基因得到表达,在选择性培养基平板上,可选出所需的转化子。 Ca2+处理的感受态细胞,其转化率一般能达到5×106--2×107转化子/质粒DNA,可以满足一般的基因克隆试验。如在Ca2+的基础上,联合其它的二价金属离子(如Mn2+、Co2+)、DMSO或还原剂等物质处理细菌,则可使转化率提高100--1000倍。 化学法简单、快速、稳定、重复性好,菌株适用范围广,感受态细菌可以在-70℃保存,因此被广泛用于外源基因的转化。
农杆菌感受态的制备方法
农杆菌感受态细胞制备 第一天晚至第三天晚: 1)取-80℃保存的GV3101于含50μg/ml 利福平的LB (千分之一的利福平)平板划线,28℃培养(一般要两天)。 注意:划线的时候要少沾一点原菌株,不必等到菌株融化就可轻轻沾一点,一定要少量,然后轻轻地划在板上。挑得太多不容易长出单菌落,如果太用力也容易伤到菌株。 第三天下午或晚: 2) 挑取单菌落接种于灭菌的50ml 新管子加10ml 50μg/ml (千分之一)利福平的LB 液体培养基中,200rpm 28℃振荡培养12-16 hr (过夜可以)。 注意:管子最好用灭菌过的报纸包一下,摇菌时。 第四天早: 3) 取1-2ml (按1:50或者1:100的比例)菌液转接于含有50μg/ml (千分之一)利福平的100ml LB 液体培养基中(用500 ml 的三角瓶来摇菌28℃,200rpm 振荡培养至OD 600=0.5)。 注意:摇菌的过程可能需要3-4小时,要随时监控菌的浓度,可以平行的摇两瓶,其中一瓶用来测浓度,避免污染;并且为了保证检测菌液与未检测菌液的一致性,平行的两瓶菌液,最好来源于同一个50 ml 管子的菌液。 摇菌的过程中可以预先把NaCl 置于冰上预冷。 4) 转移菌液到新的灭过菌的50 ml 离心管中,冰上30min ; 5) 4℃,5000rpm 离心5min 。 6) 在超净台中弃上清,将管子倒立在灭过菌的吸水纸上,尽量倒干,可以用预冷的NaCl 快速冲洗一遍。 7) 加入10ml 预冷的0.15M 的NaCl 溶液,轻轻悬浮细胞,冰上放置20min 。 注意:要用5ml 枪调到3ml 挡,轻轻抽打。 8) 4℃,5000rpm 离心5min 。 9) 在超净台中弃上清,将管子倒立在灭过菌的吸水纸上,尽量倒干。 10)加入2 ml 预冷的含15%甘油的20mM 的CaCl 2溶液,轻轻悬浮。 注意:要用1ml 枪轻轻抽打。 11)按200ul 的量分装到1.5 ml 无菌Eppendorf tube 中,液氮速冻,-80℃保存,一般不要存放超过2-3个月。
大肠杆菌感受态细胞的制备和转化原理及注意事项
大肠杆菌感受态细胞的制备和转化原理及注意事项1、感受态细胞的概念 重组DNA分子体外构建完成后必须导入特定的宿主(受体细胞)使之无性繁殖并高效表达外源基因或直接改变其遗传性状,这个导入过程及操作统称为重组DNA分子的转化。在原核生物中,转化是一个较普遍的现象,在细胞间转化是否发生,一方面取决于供体菌与受体菌两者在进化过程中的亲缘关系,另一方面还与受体菌是否处于一种感受状态有着很大的关系。所谓的感受态:即指受体或者宿主最易接受外源DNA 片段并实现其转化的一种生理状态,是由受体菌的遗传性状所决定的同时也受菌龄、外界环境因子的影响。cAMP可以使感受态水平提高一万倍,而Ca2+也可大大促进转化的作用。细胞的感受态一般出现在对数生长期新鲜幼嫩的细胞是制备感受态细胞和进行成功转化的关键。制备出的感受态细胞暂时不用时可加入占总体积15%的无菌甘油或-70℃保存有效期6 2、转化的概念及原理 在基因克隆技术中,转化特指将质粒DNA或以其为载体构建的重组DNA导入细菌体内使之获得新的遗传特性的一种方法。它是微生物遗传、分子遗传、基因工程等研究领域的基本实验技术之一。受体细胞经过一,如电击法、CaCl2等化学试剂法处理后,使细胞膜的通透性发生变化,成为能容许外源DNA 分子通过的感受态细胞。进入细胞的DNA分子通过复制、表达实现遗传信息的转移,使受体细胞出现新的遗传性状。大肠杆菌的转化常用化学法CaCl2法该法最先是由Cohen于1972年发现的。其原理是细菌处于0℃CaCl2的低渗溶液中,菌细胞膨胀成球形,转化混合物中的DNA形成抗DNase的羟基-钙磷酸复合物粘附于细胞表面,经42℃短时间热冲击处理,促使细胞吸收DNA复合物,在丰富培养基上生长数小时后,球状细胞复原并分裂增值,被转化的细菌中重组子中基因得到表达,在选择性培养基平板上可选出所需的转化子。Ca2+处理的感受态细胞其转化率一般能达到5×106~2×107转化子/ug质粒DNA可以满足一般的基因克隆试验。如在Ca2+的基础上联合其它的二价金属离子如Mn2+、Co2+、DMSO或还原剂等物质处理细菌,则可使转化率提高100~1000倍。化学法简单、快速、稳定、重复性好,菌株适用范围广,感受态细菌可以在-70℃保存,因此被广泛用于外源基因的转化。除化学法转化细菌外,还有电击转化法,电击法不需要预先诱导细菌的感受态,依靠短暂的电击,促使DNA进入细菌,转化率最高能达到109~1010转化子/ug闭环DNA。因操作简便愈来愈为人们所接受。 3、感受态细胞制备及转化中的影响因素 ⑴、细胞的生长状态和密度 最好从-70℃或-20℃甘油保存的菌种中直接转接用于制备感受态细胞的菌液。不要用已经过多次转接及贮存在4℃的培养菌液。细胞生长密度以每毫升培养液中的细胞数在5×107
农杆菌感受态细胞的制备原理和实验步骤(精)
一、目的及要求 了解和掌握农杆菌感受态细胞制备的原理和方法。 二、实验原理 在利用根癌农杆菌介导的基因转化中,首先要获得含有目的基因的农杆菌工程菌株。 在基因工程操作中,感受态细胞的制备和质粒的转化是一项基本技术。感受态是细菌细胞具有的能够接受外源DNA 的一种特殊生理状态。农杆菌的感受态可用CaCl2 处理而诱导产生。将正在生长的农杆菌细胞在加入到低渗的氯化钙溶液中,0℃下处理便会使细菌细胞膜的透性发生改变,此时的细胞呈现出感受态。 制备好的农杆菌感受态细胞迅速冷冻于70℃可保存相当一段时间而不会对其转化效率有太大影响。 三、实验仪器、材料和试剂 仪器:超净工作台,恒温摇床,冷冻高速离心机,高压灭菌锅,冰箱,70℃超低温冰柜,分光光度计,接种针,10ml 试管,50ml 离心管,1.5ml 离心管,冰浴,微量进样器及吸头。以上玻璃仪器和离心管需在用前灭菌,灭菌条件:120℃,15分钟。 材料:土壤农杆菌LBA4404菌株或其它农杆菌菌株 试剂: YEB 液体培养基(1升):酵母提取物1g ,牛肉膏5g ,蛋白胨5g ,蔗糖 5g , MgSO4.7H2O 0.5g, pH7.0,高压灭菌; 链霉素(Sm )储液:125mg/ml
0.15 N NaCl,高压灭菌。 20mM CaCl2,高压灭菌。 四、实验步骤 1. 挑取根癌农杆菌LBA4404 单菌落于3ml 的YEB 液体培养基(含Sm 125mg/l)中,28°C 振荡培养过夜; 2. 取过夜培养菌液0.5ml 接种于50mlYEB(Sm 125mg/l液体培养基中,28°C 振荡培养至OD600为0.5; 3. 5000rpm, 离心5min ; 4. 加入10ml 0.15N NaCl,使农杆菌细胞充分悬浮,5000rpm, 离心5min ; 5. 弃上清,置于冰上,加入1ml 预冷的20mM CaCl2,充分悬浮细胞,冰浴中保存,24小时内使用,或分装成每管200ml ,液氮中速冻1 分钟,置70°C 保存备用。
大肠杆菌感受态
大肠杆菌感受态细胞的制备和转化 概述 在自然条件下,很多质粒都可通过细菌接合作用转移到新的宿主内,但在人工构建的质粒载体中,一般缺乏此种转移所必需的mob基因,因此不能自行完成从一个细胞到另一个细胞的接合转移。如需将质粒载体转移进受体细菌,需诱导受体细菌产生一种短暂的感受态以摄取外源DNA。 转化(Transformation)是将外源DNA分子引入受体细胞,使之获得新的遗传性状的一种手段,它是微生物遗传、分子遗传、基因工程等研究领域的基本实验技术。 转化过程所用的受体细胞一般是限制修饰系统缺陷的变异株,即不含限制性内切酶和甲基化酶的突变体(Rˉ,Mˉ),它可以容忍外源DNA分子进入体内并稳定地遗传给后代。受体细胞经过一些特殊方法(如电击法,CaCl2 ,RbCl(KCl)等化学试剂法)的处理后,细胞膜的通透性发生了暂时性的改变,成为能允许外源DNA分子进入的感受态细胞(Compenent cells)。进入受体细胞的DNA分子通过复制,表达实现遗传信息的转移,使受体细胞出现新的遗传性状。将经过转化后的细胞在筛选培养基中培养,即可筛选出转化子(Transformant,即带有异源DNA分子的受体细胞)。目前常用的感受态细胞制备方法有CaCl2和RbCl(KCl)法,RbCl(KCl)法制备的感受态细胞转化效率较高,但CaCl2 法简便易行,且其转化效率完全可以满足一般实验的要求,制备出的感受态细胞暂时不用时,可加入占总体积15%的无菌甘油于-70℃保存(半年),因此CaCl2法为使用更广泛。本实验室一般用TSS 法制备感受态。 为了提高转化效率, 实验中要考虑以下几个重要因素: 1. 细胞生长状态和密度: 不要用经过多次转接或储于4℃的培养菌,最好从-70℃或-20℃甘油保存的菌种中直接转接用于制备感受态细胞的菌液。细胞生长密度以刚进入对数生长期时为好,可通过监测培养液的OD600 来控制。DH5α菌株的OD600为0.5时,细胞密度在5×107 个/ml左右(不同的菌株情况有所不同),这时比较合适。密度过高或不足均会影响转化效率。 2. 质粒的质量和浓度: 用于转化的质粒DNA应主要是超螺旋态DNA(cDNA)。转化效率与外源DNA的浓度在一定范围内成正比,但当加入的外
大肠杆菌感受态细胞的制备原理、步骤以及重组质粒转化解析
一、目的 1.了解感受态细胞生理特性及制备条件,掌握大肠杆菌感受态细胞制备方法。 2.掌握质粒DNA 转化大肠杆菌的方法,了解转化的条件和利用半乳糖苷酶基因插入失活选择重组质粒DNA 的原理。 二、原理 (一)大肠杆菌感受态细胞制备的原理 所谓感受态,是指细菌生长过程中的某一阶段的培养物,只有某一生长阶段中的细菌才能作为转化的受体,能接受外源DNA而不将其降解的生理状态。感受态形成后,细胞生理状态会发生改变,出现各种蛋白质和酶,负责供体DNA 的结合和加工等。细胞表面正电荷增加,通透性增加,形成能接受外来的DNA 分子的受体位点等。本实验为了把外源DNA(重组质粒)引入大肠杆菌,就必须先制备能吸收外来DNA分子 的感受态细胞。在细菌中,能发生感受态细胞是占极少数。而且,细菌的感受态是在短暂时间内发生。 目前对感受态细胞能接受外来DNA 分子的本质看法不一。主要有两种假说: 1、局部原生质体化假说――细胞表面的细胞壁结构发生变化,即局部失去细胞壁或局部溶解细胞壁,使DNA 分子能通过质膜进细胞。证据有: (1)发芽的芽孢杆菌容易转化; (2)大肠杆菌的原生质体不能被噬菌体感染,却能受噬菌体DNA 转化; (3)适量的溶菌酶能提高转化率。 2、酶受体假说――感受态细胞的表面形成一种能接受DNA 的酶位点,使DNA分子能进入细胞。证据是:(1)蛋白质合成的抑制剂如氯霉素,可以抑制转化作用;
(2)细胞分裂过程中,一直有局部原生质化,但感受态只在生长对数期的中早期出现;(3)分离到感受态因子,能使非感受态细胞转变为感受细胞。 目前对感受态细胞的转化理论尚未有统一结论,但是许多实验室一直进行探索,试图从实验中获得明确回答。有人根据pBR322 质粒DNA对E?coli K――12X1776菌株的转化结果,认为: 近来,在许多研究室都发现CaCl2对受体菌处理,可提高转化效率几十倍,通常把细胞悬浮在pH6.0 的100mmol/L CaCl2中,在冰浴条件下,放置过夜,转化率转高,但一过24小时,转化率测恢复为原来的水平。 (二)重组DNA 的转化原理 我们已经制备好大肠杆菌感受态细胞,接下的实验是把重组的DNA 引入受体细胞,使受体菌具有新的遗传特性,并从中选出转化子。作为受体的大肠杆菌C600 或DH5α,必须不同外来DNA分子发生遗传重组,通常是rec基因缺陷型的突变体,同时它们必须是限制系统缺陷或限制与修饰系统均缺陷的菌株。这样外来的DNA分子不会受其限制酶的降解。保持外来DNA 分子在受体细胞中的稳定性。制备的大肠杆菌细胞就具有这三种缺陷(rk- mk- rec-)同时此受体细胞还是氨苄青霉素敏感(Ap)。 在体外构建好的重组分子上具有分解氨苄青霉素(Ap)基因存在,当它导入受体细胞后,就赋于这些受体细胞新的特性,即Ap 抗性。同时载体质粒上具有乳糖操纵的β一半乳糖苷酶基因(lacZ,我们可以利用外源基因插入载体β一半乳糖苷酶基因(lacZ,使其失去β一半乳糖苷酶活性的原理来选择新构建的重组子。
常用大肠杆菌感受态JM109,DH5a,BL21等的区别-用途-特征
常用大肠杆菌感受态JM109,DH5a,BL21等的区别 1:DH5a菌株 DH5a是一种常用于质粒克隆的菌株。E.coli DH5a在使用pU C系列质粒载体转化时,可与载体编码的β-半乳糖苷酶氨基端实现α-互补。可用于蓝白斑筛选鉴别重组菌株。 基因型:F-,φ80dlacZΔM15,Δ(lacZYA-argF)U169,deoR,recA1,endA1,hsdR17(rk-,mk+),phoA,supE44,λ-,thi-1,gy rA96,relA1 2:BL21(DE3) 菌株 该菌株用于高效表达克隆于含有噬菌体T7启动子的表达载体(如pET系列)的基因。T7噬菌体RNA聚合酶位于λ 噬菌体DE3区,该区整合于BL21的染色体上。该菌适合表达非毒性蛋白。 基因型:F-,ompT,hsdS(rBB-mB-),gal,dcm(DE3) 3:BL21(DE3) pLy sS菌株 该菌株含有质粒pLy sS,因此具有氯霉素抗性。PLy sS含有表达T7溶菌酶的基因,能够降低目的基因的背景表达水平,但不干扰 目的蛋白的表达。该菌适合表达毒性蛋白和非毒性蛋白。 基因型:F-,ompT hsdS(rBB-mB-),gal,dcm(DE3,pLy sS ,C amr 4:JM109菌株 该菌株在使用pU C系列质粒载体进行DNA转化或用M13 phage载体进行转染时,由于载体DNA产生的LacZa多肽和JM09编码的La cZΔM15进行α-互补,从而显示β-半乳糖苷酶活性,由此很容易鉴别重组体菌株 基因型:recA1,endA1,gy r A96,thi-1,hsdR17,supE44,re lA1,Δ(lac-proA B)/F’[traD36,proAB+,lacIq,lacZΔM15] 5:TO P10菌株 该菌株适用于高效的DNA克隆和质粒扩增,能保证高拷贝质粒的稳定遗传。 基因型:F- ,mcr AΔ(mrr-hsd RMS-mcrBC),φ80 ,lacZΔM15,△lacⅩ74,recA1 ,araΔ139Δ(ara-leu)7697,galU,galK ,rps,(Strr) endA1,nupG 6:HB101菌株 该菌株遗传性能稳定,使用方便,适用于各种基因重组实验 基因型:supE44,hsdS20(rB-mB-),recA13,ara-14,proA2,lacY1,galK2,rpsL20,xy l-5,mtl-1,le uB6,thi-1 7:M110或SCS110 大多数大肠杆菌菌株中含有Dam甲基化酶和Dcm甲基化酶,前者可以在GA TC序列中腺嘌呤N-6位上引入甲基,后者在CCA/TGC 序列的第一个胞嘧啶C-5位置上引入甲基。常用的菌株都会产生dam,dcm,从而受到甲基化的影响. 部分限制性内切酶对甲基化的DNA不能切割,如F baI和MboI等,一般生物公司提供的内切酶说明中均有说明。 大多数酶切位点的甲基化不影响切割,而有些会影响,如XbaI, BclI等。而且甲基化只发生在特定序列,以XbaI为例,只有在位点序列旁出现GA或TC,该XbaI位才会被甲基化。 而要解除这种限制修饰作用通常有两种方法: (1)选用上述酶的同功酶,如Sau3AI,DNA识别切割位点与MboI相同;但不受甲基化影响; (2)利用甲基化酶缺失的受体细胞进行DNA的制备,如E.coli JM110和链霉菌等,前者Dam和Dcm甲基化酶已敲出,而后者细胞内本就没有甲基化酶,从这些细胞中抽提的DNA就能被上述酶切割。 8:E.coli JM110 要排除dam,dcm甲基化的影响,需要用特定的dam-,dcm-的菌株,如JM110 如果由JM110或SCS110等甲基化缺失的菌株产生的质粒,则不会被甲基化. 各种感受态细胞的区别用途特征 Xl1-Blue菌株
农杆菌感受态细胞的制备原理和实验步骤及验证
农杆菌感受态细胞的制备原理和实验步骤发布日期:2010-04-28 发布 人:technew最后更新时间:2010-04-28 浏览次数:889 一、目的及要求 了解和掌握农杆菌感受态细胞制备的原理和方法。 二、实验原理 在利用根癌农杆菌介导的基因转化中,首先要获得含有目的基因的农杆菌工程菌株。 在基因工程操作中,感受态细胞的制备和质粒的转化是一项基本技术。感受态是细菌细胞具有的能够接受外源DNA 的一种特殊生理状态。农杆菌的感受态可用CaCl2 处理而诱导产生。将正在生长的农杆菌细胞在加入到低渗的氯化钙溶液中,0℃下处理便会使细菌细胞膜的透性发生改变,此时的细胞呈现出感受态。 制备好的农杆菌感受态细胞迅速冷冻于70℃可保存相当一段时间而不会对其转化效率有太大影响。 三、实验仪器、材料和试剂 仪器:超净工作台,恒温摇床,冷冻高速离心机,高压灭菌锅,冰箱,70℃超低温冰柜,分光光度计,接种针,10ml 试管,50ml 离心管,1.5ml 离心管,冰浴,微量进样器及吸头。以上玻璃仪器和离心管需在用前灭菌,灭菌条件:120℃,15分钟。 材料:土壤农杆菌LBA4404菌株或其它农杆菌菌株 试剂: YEB液体培养基(1升):酵母提取物1g,牛肉膏5g,蛋白胨5g,蔗糖5g, MgSO4.7H2O 0.5g, pH7.0,高压灭菌; 链霉素(Sm)储液:125mg/ml 0.15 N NaCl,高压灭菌。 20mM CaCl2,高压灭菌。
四、实验步骤 1. 挑取根癌农杆菌LBA4404 单菌落于3ml 的YEB液体培养基(含Sm 125mg/l)中,28°C振荡培养过夜; 2. 取过夜培养菌液0.5ml接种于50mlYEB(Sm 125mg/l)液体培养基中,28°C振荡培养至OD600为0.5; 3. 5000rpm, 离心5min; 4. 加入10ml 0.15N NaCl,使农杆菌细胞充分悬浮,5000rpm, 离心5min; 5. 弃上清,置于冰上,加入1ml预冷的20mM CaCl2,充分悬浮细胞,冰浴中保存,24小时内使用,或分装成每管200ml,液氮中速冻1 分钟,置70°C保存备用。 一.农杆菌感受态细胞的制备 二.双元载体转化农杆菌EHA105 三.杆菌转化子的鉴定 A.农杆菌转化子的PCR鉴定 B.农杆菌转化子的酶切鉴定 关键词:农杆菌感受态细胞转化子 一.农杆菌感受态细胞的制备(同大肠杆菌质粒DNA的提取),然后将其转化大肠杆菌,再提取大肠杆菌的质粒DNA进行酶切鉴定。 取-70℃保存的EHA105于含有50μg/ml链霉素平板划线,28℃培养2天。挑单 菌落接种于5ml YM(0.5g/L KH 2 PO 4 ,10 g/L Mannitol,2 g/L L-Glutamine,0.2 g/L NaCL,0.2 g/L MgSO 4,0.3 g/L Yeast extract,PH 7 .0)液体培养基中,220rpm, 28℃振荡培养18 hr 左右。将5ml菌液转接于100ml YM液体培养基中, 28℃,220rpm,振荡培养至OD 600 =0.5。转入无菌1.5ml的EP管,5000g离心5min, 去上清液。加入1ml预冷的0.1M的CaCl 2 溶液,轻轻悬浮细胞,冰上放置20min, 4℃下,5000g离心5min,去上清。加入200μl预冷的含15%甘油的0.1M的CaCl 2溶液,轻轻悬浮。混匀后立即冻存于-80℃。 二.双元载体转化农杆菌EHA105 取1μg左右的质粒DNA加入到200μl EHA105感受态细胞中,混匀后,冰浴30min;-70℃放置10min ;取出后37℃水浴5min或42℃水浴1min;冰浴2min;加入800μl YM液体培养基,28℃,175rpm摇培3hr;取出后涂在含50μg/ml Kanamycin 的YM平板上,28℃培养到形成单菌落。
