江苏省盐城市2016届高三年级第一学期期中考试化学试题(含答案)

反应进程
能量/k J
CH 2=CH 2(g) CH 3CH 2Br(l)
中间体
E 1
E 4
E 2 E 3
+HBr(g) 2016届江苏省盐城市高三上学期期中考试 化学
可能用到的相对原子质量:H 1 C 12 O 16 Na 23 S 32 Pb 207
选 择 题
单项选择题:本题包括10小题,每小题2分,共计20分。每小题只有一个....选项符合题意。 1.最近美国宇航局的科研人员确认火星地表含有溶有高氯酸盐的液态水。下列有关水及高氯酸盐的说法错误..的是 A .水是一种弱电解质 B .NH 4ClO 4溶液显酸性
C .NaClO 4中含有离子键和共价键
D .NH 4ClO 4只有氧化性,没有还原性 2.下列有关硫元素及其化合物的表示正确的是 A .中子数为18的硫原子:18
16S
B .CS 2分子的电子式:
C .硫离子(S
-
2)的结构示意图:
D .苯磺酸的结构简式:
OSO 2H
3.用H 2O 2溶液处理含NaCN 的废水的反应原理为:NaCN+H 2O 2+H 2O=NaHCO 3+NH 3,已知:HCN 酸性比H 2CO 3弱。下列有关说法正确的是 A .该反应中氮元素被氧化 B .该反应中H 2O 2作还原剂
C .实验室配制NaCN 溶液时,需加入适量的NaOH 溶液
D .0.1mol·L -
1NaCN 溶液中含HCN 和CN -
总数目为0.1×6.02×1023 4.下列说法正确的是
A .分子式为C 2H 4O 的有机化合物性质相同
B .同温同压下,同体积的任何气体均含有相同的原子数
C .密闭容器中1molN 2与3molH 2充分反应,产物的分子数为
2×6.02×1023
D .依据右图能量曲线可确定反应:
CH 2=CH 2(g)+HBr(g)→CH 3CH 2Br(l)的 H = (E 1+E 3-E 2-E 4)kJ·mol -1
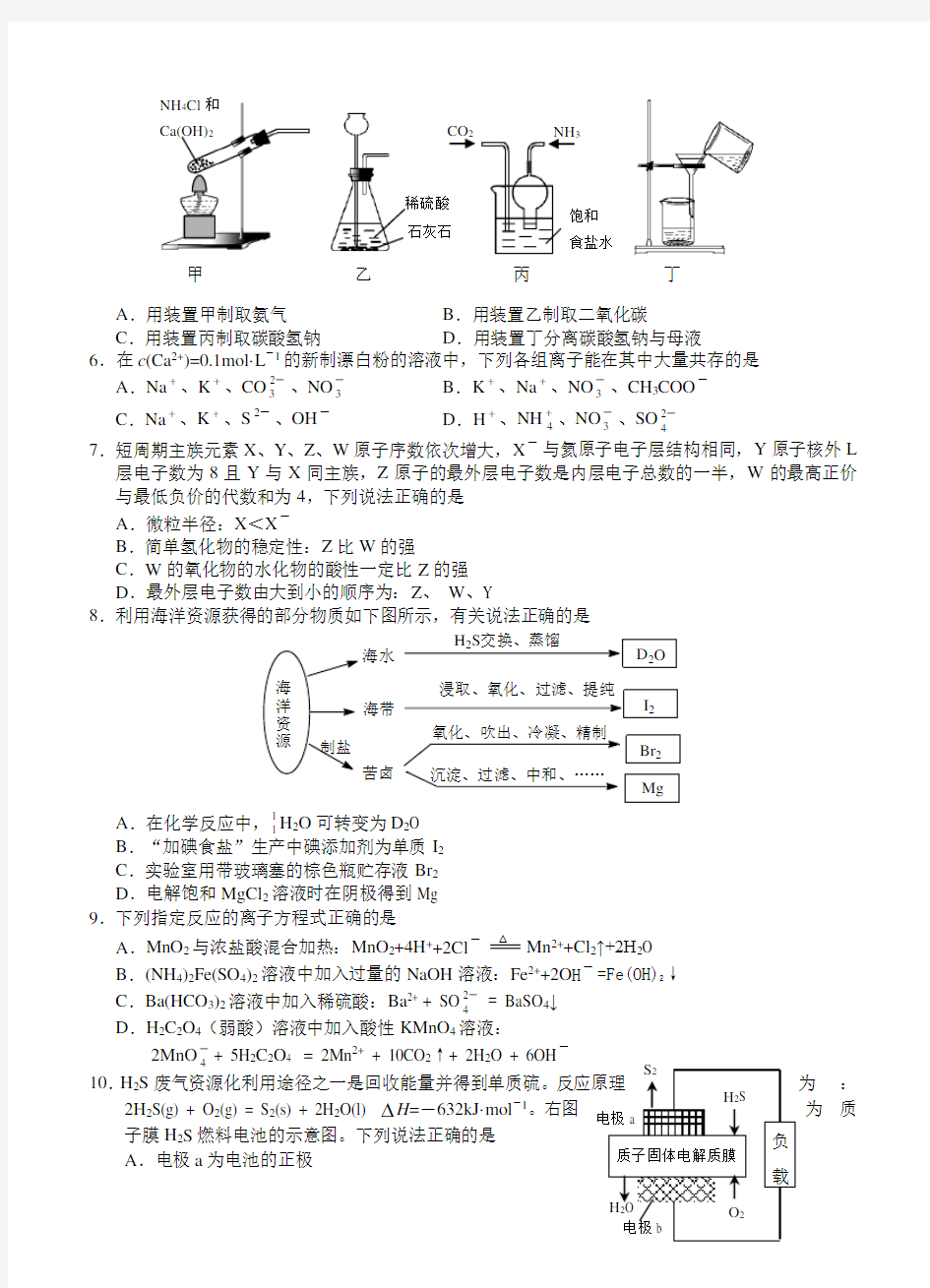
5.依据反应原理:NH 3+CO 2+H 2O+NaCl = NaHCO 3↓+NH 4Cl ,并利用下列装置制取碳酸氢钠粗品,实验装置正确且能达到实验目的的是
电极a
S 2
负
载
H 2O O 2
电极b
质子固体电解质膜 H 2S
A .用装置甲制取氨气
B .用装置乙制取二氧化碳
C .用装置丙制取碳酸氢钠
D .用装置丁分离碳酸氢钠与母液
6.在c (Ca 2+)=0.1mol·L -
1的新制漂白粉的溶液中,下列各组离子能在其中大量共存的是 A .Na +、K +、CO -
23、NO -3
B .K +、Na +、NO -
3、CH 3COO -
C .Na +
、K +
、S -2、OH
-
D .H +、NH +4 、NO -
3、SO -
24
7.短周期主族元素X 、Y 、Z 、W 原子序数依次增大,X -与氦原子电子层结构相同,Y 原子核外L
层电子数为8且Y 与X 同主族,Z 原子的最外层电子数是内层电子总数的一半,W 的最高正价与最低负价的代数和为4,下列说法正确的是
A .微粒半径:X <X -
B .简单氢化物的稳定性:Z 比W 的强
C .W 的氧化物的水化物的酸性一定比Z 的强
D .最外层电子数由大到小的顺序为:Z 、 W 、Y
8.利用海洋资源获得的部分物质如下图所示,有关说法正确的是
海洋资源
海水
D 2O 海带浸取、氧化、过滤、提纯I 2苦卤
Mg
H 2S 交换、蒸馏制盐
氧化、吹出、冷凝、精制
沉淀、过滤、中和、……
Br 2
A .在化学反应中,1
1H 2O
可转变为D 2O
B .“加碘食盐”生产中碘添加剂为单质I 2
C .实验室用带玻璃塞的棕色瓶贮存液Br 2
D .电解饱和MgCl 2溶液时在阴极得到Mg 9.下列指定反应的离子方程式正确的是 A .MnO 2与浓盐酸混合加热:MnO 2+4H ++2Cl
-
△
Mn 2++Cl 2↑+2H 2O
B .(NH 4)2Fe(SO 4)2溶液中加入过量的NaOH 溶液:Fe 2++2O H -
=Fe(OH)2↓
C .Ba(HCO 3)2溶液中加入稀硫酸:Ba 2+ + SO -
24
= BaSO 4↓ D .H 2C 2O 4(弱酸)溶液中加入酸性KMnO 4溶液:
2MnO -4
+ 5H 2C 2O 4 = 2Mn 2+ + 10CO 2↑+ 2H 2O + 6OH -
10.H 2S 废气资源化利用途径之一是回收能量并得到单质硫。反应原理
为:
2H 2S(g) + O 2(g) = S 2(s) + 2H 2O(l) ?H =-632kJ·mol -
1。右图
为质
子膜H 2S 燃料电池的示意图。下列说法正确的是
A .电极a 为电池的正极
甲 乙 丙 丁
NH 4Cl 和 Ca(OH)2
饱和 食盐水
NH 3
CO 2
稀硫酸 石灰石
B .电极b 上发生的电极反应为:O 2+2H 2O+4e -= 4 OH -
C .电路中每流过4mol 电子,电池内部释放632kJ 热能
D .每17gH 2S 参与反应,有1mol H +经质子膜进入正极区
不定项选择题:本题包括5小题,每小题4分,共计20分。每小题只有一个或两个选项符合题意。若正确答案只包括一个选项,多选时,该小题得0分;若正确答案包括两个选项,只选一个且正确的得2分,选两个且都正确的得满分,但只要选错一个,该小题就得0分。 11.下列有关氯气及其含氯分散系的说法正确的是
A .钢铁在Cl 2气氛中主要发生电化腐蚀
B .在新制氯水中加入少量CaCO 3,溶液中c (HClO)增大
C .反应3Cl 2(g) + 8NH 3(g) = 6NH 4Cl(s) + N 2(g)的?H >0,?S <0
-
1+-
12D .青蒿素在热的酸、碱溶液中均可稳定存在
13.下列图示箭头方向表示与某种常见试剂在通常条件下(不含电解)发生转化,其中6步转化均
能一步实现的一组物质是 14A .制备Fe(OH)3胶体:向0.1mol·L -1FeCl 3溶液中加入等体积0.3mol·L -
1NaOH 溶液
B .除去FeCl 3溶液中少量Cu 2+:向含有少量Cu 2+的FeCl 3溶液中加入适量铁粉,充分反应后过
滤
C .比较Fe(OH)3和Al(OH)3的溶度积:向0.1mol·L -1FeCl 3溶液中滴加0.1 mol·L -
1
氨水至不再产生沉淀,然后再滴入0.1mol·L -
1AlCl 3溶液,观察现象
D . 验证氧化性Fe 3+<Br 2<Cl 2:向试管中依次加入1mL 0.1mol·L -
1FeBr 2溶液、几滴KSCN 溶
液和1mL 苯,然后逐滴加入氯水,并缓缓振荡,直到氯水过量,观察整个过程中有机相和水相中的现象
15.一定温度下,在三个体积均为2.5L 的恒容密闭容器中发生反应:
CO 2(g)+H 2S(g) COS(g)+H 2O(g)
下列说法正确的是
A .该反应正反应为放热反应
B .607K 时该反应的平衡常数为2.50×10-
3
C .容器Ⅱ达到平衡时容器中COS 的物质的量为0.02mol
D .容器Ⅲ达平衡时,再充入少量氦气,平衡将向正反应方向移动
非选择题
16.(12分)CMA (醋酸钙、醋酸镁固体的混合物)是高速公路的绿色融雪剂。以生物质废液——
木醋液(主要成分乙酸,以及少量的甲醇、苯酚、焦油等杂质)及白云石(主要成分MgCO 3·CaCO 3,含SiO 2等杂质)等为原料生产CMA 的实验流程如下:
CMA
滤渣1
(1)步骤①发生的反应离子方程式为 ▲ 。
(2)步骤②所得滤渣1的主要成分为 ▲ (写化学式);步骤②所得滤液常呈褐色,颜色除与木醋
液中含有少量的有色的焦油有关外,产生颜色的另一主要原因是 ▲ 。 (3)已知CMA 中钙、镁的物质的量之比与出水率(与
融雪效果成正比)关系如右图所示,步骤④的目的除调节n (Ca)∶n (Mg)约为 ▲ (选填:1∶2;3∶7;2∶3)外,另一目的是 ▲ 。 (4)步骤⑥包含的操作有 ▲ 、过滤、洗涤及干燥。 17.(15分)丹参酮ⅡA 是一种治疗心血管疾病的药物,其中的一种合成路线如下:
每克C M A 出水率
n (Ca)/n (Mg)
CH 3CH 2CHO
试剂X
NCH=CHCH 3
HO
O N
HCl
O HO 亚硝基过硫酸钾
O O
O
O O
O
丹参酮ⅡA
A
B
C D
E 双烯加成
(1)丹参酮ⅡA 中含氧官能团为 ▲ 和 ▲ (写名称)。 (2)试剂X 的分子式为C 5H 11N ,则X 的结构简式为 ▲ 。 (3)C →D 的反应类型为 ▲ 。
(4)写出同时满足下列条件的E 的一种同分异构体的结构简式: ▲ 。
Ⅰ.能发生银镜反应
Ⅱ.分子中除苯环外不含其它环状结构,分子中含有4种不同化学环境的氢 (5)写出以CH 3CH=CHCH 3和CH 2=CHCHO 为原料制备
CH 2OH
的合成路线流程图(无机试剂可
任选)。合成路线流程图示例如下: CH 3CHO
O 2
催化剂,△
CH 3COOH
32浓H 2SO 4,△
CH 3COOCH 2CH 3
18.(12分)PbI 2是生产新型敏化太阳能电池的敏化剂——甲胺铅碘的原料。合成PbI 2的实验流程如下:
铅花
-1制备PbI 2
(1)将铅块制成铅花的目的是 ▲ 。
(2)31.05g 铅花用5.00mol·L -1的硝酸溶解,至少需消耗5.00 mo l ·L -1
硝酸 ▲ mL ,同时产生 ▲
L(标准状况下)NO 。
(3)取一定质量(CH 3COO)2P b ·nH 2O 样品在N 2气氛中加热,测得样品固体残留率
(%100 固体样品的起始质量
固体样品的剩余质量
)随温度
的变化如下图所示(已知:样品在75℃时已完全
失去结晶水)。
①(CH 3COO)2Pb ·nH 2O 中结晶水数目
n=
150 固体残留率/%
温度/℃
接真空泵 接真空泵 题19图-3 ▲ (填数字)。
②100~200℃间分解产物为铅的氧化物和一种有机物,则该有机物为 ▲ (写结构简式)。
(4)称取一定质量的PbI 2固体,用蒸馏水配制成室温时的饱和溶液,准确移取25.00mLPbI 2饱和溶液分次加入阳离子交换树脂RH 中,发生:2RH(s) + Pb 2+(aq) = R 2Pb(s) +2H +(aq),用锥形瓶接收流出液,最后用蒸馏水淋洗树脂至流出液呈中性,将洗涤液合并到锥形瓶中。加入2~3滴酚酞溶
液,用0.002500mol·L -
1NaOH 溶液滴定,到滴定终点时用去氢氧化钠标准溶液20.00mL 。计算室温时PbI 2 的K sp (请给出计算过程)。 19.(15分)焦亚硫酸钠(Na 2S 2O 5)在食品加工中常用作防腐剂、漂白剂和疏松剂。焦亚硫酸钠为
黄色结晶粉末,150℃时开始分解,在水溶液或含有结晶水时更易被空气氧化。实验室制备焦亚硫酸钠过程中依次..包含以下几步反应: 2NaOH + SO 2 = Na 2SO 3 + H 2O ……(a ) Na 2SO 3+ H 2O + SO 2 = 2NaHSO 3 ……(b ) 2NaHSO 3
△
Na 2S 2O 5 + H 2O …………(c )
实验装置如下:
(1)实验室可用废铝丝与NaOH 溶液反应制取H 2,制取H 2的离子方程式为 ▲ 。
(2)题19图-1装置中,导管X 的作用是 ▲ 。
(3)通氢气一段时间后,以恒定速率通入SO 2,开始的一段时间溶液温度迅速升高,随后温度缓慢变
化,溶液开始逐渐变黄。“温度迅速升高”的原因为 ▲ ; 实验后期须保持温度在约80℃,可采用的加热方式为 ▲ 。
(4)反应后的体系中有少量白色亚硫酸钠析出,参照题19图-2溶解度曲线,除去其中亚硫酸钠固体
的方法是 ▲ ;然后获得较纯的无水Na 2S 2O 5应将溶液冷却到30℃左右抽滤,控制“30℃左右”的理由是 ▲ 。 (5)用题19图-3装置干燥Na 2S 2O 5晶体时,通入H 2的目的是 ▲ ;真空干燥的优点是 ▲ 。
(6)测定产品中焦亚硫酸钠的质量分数常用剩余碘量
法。已知:S 2O 52-+2I 2+3H 2O=2SO 42-+4I -
+6H +;
2S 2O 32-+I 2 = S 4O 62-+2I -
请补充实验步骤(可提供的试剂有:焦亚硫酸钠样品、标准碘溶液、淀粉溶液、酚酞溶液、标准Na 2S 2O 3溶液及蒸馏水)。
题19图-2
0 20 40 60 80 100
2
4 6 8
10
温度
盐m o l /每100m o l 水
-20 Na 2SO 3
Na 2SO 3·7H 2O
N a 2S 2O 5·7H 2O
Na 2S 2O 5
题19图-1
导管X
温度计
控速管
175gNaOH(s) + 500mL 煮沸 过的蒸馏水
800 400 200 10S O 3的转化率/%
温度
1000 20
40 60
80 ①精确称取产品0.2000g 放入碘量瓶(带磨口塞的锥形瓶)中。
②准确移取一定体积和已知浓度的标准碘溶液(过量)并记录数据,在暗处放置5min ,然后加入5mL 冰醋酸及适量的蒸馏水。 ③用标准Na 2S 2O 3溶液滴定至接近终点....
。 ④ ▲ 。 ⑤ ▲ 。 ⑥重复步骤①~⑤;根据相关记录数据计算出平均值。 20.(14分)硫-氨热化学循环制氢示意图如下:
O 2
H 2
423
(1)反应1的离子方程式为 ▲ 。 (2)反应2能量转化主要方式为 ▲ 。
(3)反应3中控制反应条件很重要,不同条件下硫酸铵分解产物不同。若在400℃时分解,产物除水
蒸气外还有A 、B 、C 三种气体,A 是空气中含量最多的单质,B 能使湿润的红色石蕊试纸变蓝,
C 能使品红溶液褪色。则400℃时硫酸铵分解的化学方程式为 ▲ 。 (4)反应4是由(a)、(b)两步反应组成:
H 2SO 4(l) =SO 3(g) +H 2O(g) , ?H =+177kJ?mol -
1 …………(a)
2SO 3(g)2SO 2(g) + O 2(g),?H=+196 kJ?mol -
1…………(b) ①则H 2SO 4(l)分解为SO 2(g)、O 2(g)及H 2O(g)的热化学方程式为: ▲ 。
②在恒温密闭容器中,控制不同温度进行SO 3分解实验。以SO 3起始浓度均为c mol·L -
1,测定SO 3
的转化率,结果如右图,图中Ⅰ曲线为SO 3的平衡转化率与温度的关系,Ⅱ曲线表示
不同温度下反应经过相同反应时间且未达
到化学平衡时SO 3的转化率。 i )图中点X 与点Z 的平衡常数K :
K (X) ▲ K (Z)(选填:>,<,=); ii )Y 点对应温度下的反应速率: v (正) ▲ v (逆)(选填:>,<,=); iii )随温度的升高,Ⅱ曲线逼近Ⅰ曲线的原因 是: ▲ 。 21. (12分)【选做题】本题包括A 、B 两小题,请选定其中一小题........,并在相应的答题区域.........内作答...
。若多做,则按A 小题评分。 A .[物质结构与性质]
K 4[Fe(CN)6]强热可发生反应:3 K 4[Fe(CN)6]
高温
2 (CN)2↑+12 KCN +N 2↑+ Fe 3C + C
(1)K 4[Fe(CN)6]中Fe 2+的配位数为 ▲ (填数字);Fe 2+基态核外电子排布式为 ▲ 。
(2)(CN)2分子中碳原子杂化轨道类型为 ▲ ;1mol(CN)2分子中含有σ键的数目为 ▲ 。
(3)O +
22与CN -互为等电子体,则O +
22的电子式为 ▲ 。
(4)Fe 3C 的晶胞结构中碳原子的配位数为6,碳原子与紧邻的铁原子组成的空间构型为 ▲ 。 B .[实验化学]
三乙酸甘油酯是一种优良的溶剂、定香剂和增塑剂。实验室制备三乙酸甘油酯的反应原理、实验装置及相关数据如下:
3CH 3COOH
+
CH 2OH CHOH CH 2OH
CH 3COOCH 2
CH 3COOCH CH 3COOCH 2
+ 3H 2O 浓H 2SO 4
物质 相对 分子质量 密度/g·cm -3
沸点/℃ 水中 溶解性 甘油 92 1.2636 290
(分解) 溶 乙酸 60 1.0492 118 溶 三乙酸甘油酯
218
1.1596
258
不溶
实验步骤:
步骤1.在500mL 反应器中加入200g 冰醋酸,92g 甘油和100mL 苯,开动搅拌器,慢慢从插温度计
口加入3mL 浓硫酸后,缓缓加热并回流1h ,停止加热。
步骤2.用5%碳酸钠溶液洗涤,再用水洗涤,最后加入无水氯化钙。 步骤3.先进行常压蒸馏收集75~85℃馏分。
步骤4.将常压馏分再进行减压蒸馏,收集128~131℃/933Pa 馏分,最终得产品176g 。 (1)步骤1先开搅拌器后加浓硫酸的目的是 ▲ ;冰醋酸过量的目的是 ▲ 。 (2)用5%碳酸钠溶液洗涤的主要目的是 ▲ ;加无水氯化钙的目的是 ▲ 。 (3)最后用减压蒸馏而不用常压蒸馏其原因是 ▲ 。 (4)本次实验产率为 ▲ 。
盐城市2016届高三年级第一学期期中考试
化学试题参考答案
选择题(共40分)
单项选择题:本题包括10 小题, 每小题2 分, 共计20 分。 1.D 2.B 3.C 4.D 5.C 6.B 7.A 8.C 9.A 10.D
不定项选择题:本题包括5小题,每小题4分,共计20分。每小题只有一个或两个选项符合题意。若
温度计
搅拌器
冷凝器
水
正确答案只包括一个选项,多选时,该小题得0分;若正确答案包括两个选项,只选一个且正确的得2分,选两个且都正确的得满分,但只要选错一个,该小题就得0分。 11. BD 12.C 13.D 14.CD 15. BC
非选择题(共80分)
16. (12 分)
(1)MgCO 3·CaCO 3+4CH 3COOH = Ca 2++Mg 2++4CH 3COO -
+2CO 2↑+2H 2O (2分) (2)SiO 2(2分);实验过程中苯酚被空气中氧气氧化最终产生褐色物质(2分) (3)3∶7(2分);除去过量的乙酸(2分) (4)蒸发结晶(2分) 17. (15分)
(1)羰基,醚键(每空1分,共2分) (2)
N -H
(2分) (3)消去反应(1分) (4)(3分)
C ≡C -CHO OH
C ≡C -CHO HO HO
或或
C ≡C -O --H
HO
O
CHO
OHC CHO
或
等
(5)(7分)
CH 3-CH=CH -CH 3
Br 2CH 3-CH -CH -CH 3
乙醇,△
CH 2=CHCH=CH 2
CHO
CH 2OH
2
Ni ,高温高压
4
18. (12 分)
(1)增大与酸的接触面,加快溶解反应速率(1分)
(2)80.0(2分);2.24(2分) (3)①3(2分);②(CH 3CO)2O (2分) (4)n (H +
)=n (NaOH)=0.002500 mol·L -
1×20.00mL×10-3L·mL
1
-= 5.000×10-5mol
n [Pb 2+(aq)]=
)H (2
1
+n =2.500×10-5mol ………………(1分) c (Pb 2+)=
1
-3-5-mL
L 1025.00mL mol 102.500???=1.000×10-3 mol·L -
1………(共得2分)
K sp(PbI 2)=c (Pb 2+)·c 2(I -
)=4c 3(Pb 2+)=4×(1.000×10-
3)3 =4.000×10-
9……(共得3分)
19. (15分)
(1)2Al +2OH -
+2H 2O = 2AlO -
2+3H 2↑(2分) (2)排出H 2、未反应的SO 2及水蒸气等(1分)
(3)SO2与NaOH溶液的反应是放热反应(1分);80℃水浴加热(1分)
(4)趁热过滤(1分);此时溶液中Na2SO3不饱和,不析出(1分)
(5)排出空气,防止焦亚硫酸钠被氧化(2分);干燥室内部的压力低,水分在低温下就能气化,减少产品氧化(2分)
(6)④加入1~2mL淀粉溶液(2分)
⑤继续用标准Na2S2O3溶液滴定至蓝色刚好褪去且半分钟内颜色不复现,记录滴定所消耗的
体积(2分)
20. (14分)
(1)SO2+H2O+2NH3 = 2NH4++SO-2
3
(2分)
(2)太阳能转化为电能再转化为化学能(2分)
(3)3(NH4)2SO4400℃
4NH3↑+ N2↑+3SO2↑+ 6H2O↑(2分)
(4)①2H2SO4(l)2SO2(g) + O2(g) +2H2O(g) H=+550kJ?mol1-(2分)
②i)<(2分);ii)>(2分);iii)温度升高,反应速率加快,达到平衡时间缩短(2分)
21. (12 分)【选做题】
A. [物质结构与性质]
(1)6(2分);[Ar]3d6或1s22s22p63s23p63d6(2分)
(2)sp(2分);3mol(或3×6.02×1023)(2分)
(3)(2分);(4)正八面体(2分)
B. [实验化学]
(1)防止局部浓硫酸浓度过大,造成有机物脱水炭化(2分);有利于向酯化方向移动,提高甘油的转化率(2分)
(2)除去产品的硫酸、乙酸(2分) 除去有机物中的水份(2分)
(3)防止常压蒸馏温度过高导致产品分解(2分)
(4)80.7% (2分)
本卷中所有合理答案均参照给分
初三化学期中考试试卷分析
初三化学第一次月考试卷分析 一、试题特点 1.本次试卷的命题是以义务教育化学课程标准及义务教育课程标准教科书《化学》的有关内容为依据,重点考查学生化学基础知识和基本技能、基本方法和情感态度价值观,以及对化学、技术和社会之间相互关系的理解,运用化学知识解决简单实际问题的能力等。 2.试卷在重视考查基础知识的同时,加强对学生科学素养(知识与技能、过程与方法、情感态度价值观)的考查,引导学生改变学习方式。如选择题第8、9题,填空题最后一道和综合应用第一题,学生在解答这类开放性问题时,思维应该是发散的,富有创造性和个性的,同时也会明白许多科学道理,并受到潜移默化的教育。这类试题考查的不再是课程中单一的知识点,而是学生能否灵活运用所学的化学知识,分析解决实际问题的能力,同时也培养了学生的创造性思维能力。这些做法体现了初中化学课程新理念,对素质教育的推进具有导向作用。 3.体现学科渗透,融合科学精神和人文思想,也是本试题的一个特点。生活和生产中的问题大多数为学科间渗透的综合,打破学科界限,培养和提高学生解决实际问题的能力是社会、学科和学生自身发展的需要。这些综合性试题,注意学科间知识的相互渗透,体现了要培养学生综合运用各科知识分析解决实际问题能力的导向。 二、答卷中主要问题的原因分析 1.基础知识和基本技能不扎实。表现在对化学式的意义表述不清;对化学反应的量的关系不能正确理解;对物质的分类混淆不清;计算能力非常薄弱;对化学用语的表达含义不能准确理解;不会书写化学反应的表达式等等。 2.实验基本技能差。不会组合正确的实验装置和排列合适的实验操作顺序等。 3.能力与方法问题。阅读理解、综合分析与归纳、语言表达、科学探究等能力较差,对化学学科中常用的科学方法不熟悉。表现在不会进行探究性学习;根据现象总结结论的能力较差。 4.用化学知识解决实际问题的能力较差。表现在不能根据所设计的问题情境,结合自身体验来思考问题,寻求解决问题的方法。 5.语言表述不清楚,逻辑性较差,缺乏条理性。表现在不能用精练的、准确的语言来描述具体的反应现象,或对反应现象叙述不清;回答问题不能抓住重点问题去阐述,不能答出关键点。 6.计算能力薄弱。表现在根据化学式计算元素的质量分数和元素的质量比,以及化学反应中有关量的计算。 三、教学建议 1.增强质量意识
2021年江苏省盐城市大丰区第一共同体中考化学一模试卷
2021年江苏省盐城市大丰区第一共同体中考化学一模试卷 一、选择题(共30分,每题2分,只有一个选项符合题意) 1.(2分)下列措施不符合我市创建“全国卫生文明城市”要求的是()A.不向车窗外丢垃圾 B.生活污水任意排放 C.合理使用农药化肥 D.严查工厂排放的水是否达标 2.(2分)下列工艺过程中主要涉及化学变化的是() A.海水晒盐B.西瓜榨汁C.头发刺绣D.陈皮酿酒3.(2分)利用如图检查装置的气密性,手握试管一段时间后,导管口有气泡产生的主要原因是() A.分子间隔变大了B.分子体积变大了 C.分子运动加快了D.分子个数变多了 4.(2分)脑黄金在医药、食品等行业中应用前景非常广阔,脑黄金的化学式为C25H51COOH.下列对脑黄金的说法正确的是() A.物质中含有80个原子 B.该物质是由碳、氢、氧三种元素构成的 C.该物质的相对分子质量为396 D.该物质中碳、氢、氧元素质量比为13:26:1 5.(2分)下列说法正确的是() A.食盐就是盐,纯碱属于碱 B.铵态氮肥一定不能与碱性物质同时施用,但尿素可以 C.盐都含有金属元素 D.碱与非金属氧化物反应生成盐和水,所以该反应属于复分解反应 6.(2分)下列实验现象描述正确的是() A.高温条件下木炭还原氧化铜:黑色固体逐渐变成光亮的铜
B.铁丝在氧气中燃烧:银白色固体剧烈燃烧,火星四射,放出大量的热,生成黑色固体 C.电解水实验:两个电极附近产生气泡,一段时间后,正、负极产生的气体体积比约为2:1 D.铜片放入硝酸银溶液中:紫红色固体表面有银白色固体产生,溶液由蓝色逐渐变为无色 7.(2分)硒是人体必需的微量元素,被誉为“抗癌大王”.根据如图提供的硒的有关信息,下列说法中正确的是() A.硒属于金属元素 B.硒的原子核内有34个中子 C.硒原子在化学反应中易得电子 D.硒的相对原子质量是78.96g 8.(2分)某溶液由盐酸、硫酸、硫酸铜、氯化铜几种溶液中的两种混合而成,向该混合液中滴加Ba(OH)2溶液的体积与生成沉淀质量的关系如图所示,则该混合液中含有() A.HCl、H2SO4B.H2SO4、CuCl2 C.HCl、CuCl2D.H2SO4、CuSO4 9.(2分)我们学习过以下常见的酸、碱、盐:HCl、H2SO4、NaOH、Ca(OH)2、Na2CO3、NaCl,请你整理归纳,这六种物质两两相互作用能发生化学反应共有() A.7个B.6个C.5个D.4个 10.(2分)如图是甲、乙两种固体物质在水中的溶解度曲线,下列说法不正确的是()
北京市海淀区2018届高三上学期期中考试化学试卷Word版含答案
北京市海淀区2017-2018 学年度高三年级第一学期期中练习 化学 本试卷分为第Ⅰ卷(选择题)和第Ⅱ卷(非选择题)两部分,共8页。满分100分。考试时长90分钟。考生务必将答案写在答题卡和答题纸上,在试卷上作答无效。考试结束后,将本试卷、答题卡和答题纸一并交回。 可能用到的相对原子质量:H 1 C 12 O 16 S 32 Ba 137 第I卷(选择题,共42分) 本部分共14道小题,每小题3分,共42分。请在每小题列出的四个选项中,选出最符合题目要求的一项。 1.下列我国古代的技术应用中,不涉及 ...氧化还原反应的是 A. 煅烧贝壳 B. 粮食酿醋 C. 古法炼铁 D. 火药爆炸 2. “一带一路”贸易使国外的特色产品走入百姓的日常生活,下列商品的主要成分所对应 的材料类型不正确 ...的是 A B C D 泰国银饰埃及棉制品捷克水晶饰品土耳其彩瓷 金属材料天然高分子材料合成高分子材料无机非金属材料 3.下列关于硅及其化合物的说法不正确 ...的是 A.高纯硅具有良好的半导体性能,可制成硅芯片、光电池、光导纤维等
B.二氧化硅能与氢氟酸反应,可用氢氟酸刻蚀玻璃 C.向硅酸钠溶液中滴加稀盐酸有不溶物生成,实验室可用该方法制备硅酸 D.“硅胶”由硅酸凝胶经干燥、脱水制得,常用作食品、药品等的干燥剂 4. 常温下,下列各组离子在指定溶液中一定能大量共存的是 A. pH=1的溶液中:HCO 3-、SO 42-、K + 、Cl - B. 遇酚酞变红的溶液中:NO 3-、Na + 、AlO 2-、K + C. c (NO 3-) = 1 mol ·L -1 的溶液中:H + 、Fe 2+ 、Cl -、NH 4+ D. 无色透明溶液中: K + 、SO 42-、Na + 、MnO 4 - 5.通常工业上监测SO 2含量是否达到排放标准的化学反应原理是 SO 2 + H 2O 2 + BaCl 2 BaSO 4↓+ 2HCl 用N A 表示阿伏伽德罗常数的值,下列说法不正确...的是 A. mol BaCl 2中所含离子总数约为 N A B. 25 o C 时,pH=1的HCl 溶液中含有H + 的数目约为 N A C. 标准状况下,17 g H 2O 2中所含电子总数约为9 N A D. 生成 g BaSO 4沉淀时,吸收SO 2的体积在标准状况下约为 L 6. 下图表示自然界中的氮循环,相关说法正确的是 A .“雷电作用”中发生的反应是:N 2 + 2O 2 === 2NO 2 B .“人工固氮”过程中,氮元素一定被还原 C .①中涉及的反应可能有: 2 NO 2- + O 2 === 2 NO 3- D .②中涉及的反应可能有: 2NO 3- + 12H + === N 2+ 6H 2O 7.以下有关原子结构及元素周期表的叙述正确的是 放电 ① ②
(word完整版)高一化学期中考试试卷分析
武陟一中2011-2012学年上期高一期中考试化学试卷分析 一、试卷结构 1、试卷结构 本次期中考试共分Ⅰ、Ⅱ两卷,Ⅰ卷1—18题为选择题,分值54分,Ⅱ卷19、20、21为填空题,22、23题为推断题,24题为计算题,分值46分,共计100分。 2、试卷评价 试题难度适中,知识覆盖面大,基本上覆盖了期中考试前所学的所有知识,突出主干知识、基础知识、基本技能和基本方法的考查,同时也对学生运用知识的要求有一定要求,整套试卷无难题、怪题、偏题,主要目的是考查学生对最基本的知识理解和掌握情况。 二、试卷分析 选择题主要是考查学生对基础理论、概念辨析以及重要元素化合物等知识的掌握。涉及化学用语、阿伏伽德罗常数、离子共存、电解质溶液、氧化还原反应等。学科特色浓郁,知识层次鲜明,既有描述性知识又有迁移性和创新性知识,各层次的考生都有一定发挥的空间。 第12题和第14题 命题意图:本题考查溶液中的电荷守恒,要求学生能够熟练的运用物质的量和物质的量浓度来表示溶液中的电荷守恒。 试卷中反映出的主要问题:学生得分情况不是太好,经分析和调查后主要问题在于学生运用所学知识的能力较差。 第17题 命题意图:本题考查氧化还原反应中氧化性和还原性的判断,是氧化还原反应中很基本的要求,也是命题时常考的题型之一,要求学生能准确找出氧化剂和还原剂、氧化产物和还原产物,并能熟练比较其氧化性和还原性强弱。 试卷中反映出的主要问题:大部分学生能准确的找出氧化剂和还原剂,但是不能找出氧化产物和还原产物,导致出错。 相应措施:引导学生从两条线的变化来理解氧化还原反应,即在氧化还原反应中氧化剂得到电子,化合价降低,发生还原反应,得到还原产物;还原剂失去电子,发生氧化反应,得到氧化产物。 第20题
江苏省盐城市大丰市万盈第二中学2020学年八年级英语下学期第8周周末作业(无答案) 牛津版
江苏省盐城市大丰市万盈第二中学2020学年八年级英语下学期第8周周末作业一、单项选择(20分) ( )1. Quasimodo(卡西莫多) is ______ugly man, he is from ________European country,France. A. a,a B.a,an C.an,an D.an,a ( )2. Miss Li gives us lots of ________on learning English. A. tip B. advice C. way D. idea ( )3. Sally sat______ Harry and they drank tea face to face. A. beside B. next to C. opposite D. behind ( )4. He has worked in the company ___ten years and he has been a manager ____three years ago. A. for, for B. for, since C. since, for D. since, since ( )5. —I can drive you to the supermarket if you wait? —No, I'll walk.Thanks, ______. A. too B.otherwise C. anyway D.however ( )6. I have ______finished my wo rk. Have you finished yours _______? A. already, already B. yet, yet C. yet, already D. already, yet ( )7. The old man lives ____ , but he doesn’t feel_____at all .He has many hobbies. A. alone, lonely B. lonely, alone C. lonely, lonely D. alone, alone ( )8. I have only _______ money. I can’t buy that expensive dress. A. a bit B. a little C. a few D. a lot ( )9. You __________ come to my desk to renew the book. You can do it online. A. shouldn’t B.can’t C. needn’t D.mustn’t ( )10. —Where have you _________? —I’ve ________ the supermarket. A. gone, gone to B. been, been to C. gone, been at D. been, gone to ( )11.—My grandparents have been to the United States . —Really ? When _____ there ? A. will they go B. have they gone C. do they go D. did they go ( )12. I used to _________coke, but now I’m used to _________milk. A.drink,drink B.drink,drinking C.drinking, drinking D.drinking,drink ( )13. The sheep several hours ago. A.died B.has died C.has been dead D.has dead ( )14—Thank you a lot for your help.— __________________. A.All right. B.My pleasure. C. No problem. D. No, thanks. ( )15. Jacky didn’t ______ himself clearly enough. He was just too nervous. A. talk B. express C. speak D. tell ( )16. —_______ turn is it to make our daily talk today? —I t’s my turn, Mrs Lin. A. Whose B. What C. Which D. Where ( )17. Boy, didn’t you see people waiting in line? Don’t _______in. A. push B. pull C. put D. carry ( )18. —Excuse me, sir. But you’re _____ my way. —Sorry. I didn’t know you wanted to pass by. A. in B. on C. by D. with ( )19. Checking your answers before handing in your paper can help you ______mistakes. A. make B. provide C. avoid D. advise ( )20. —Sir, please don’t smoke, look at the sign. —Sorry, I __________ it. A. don’t notice B. haven’t noticed C. didn’t notice D. won’t notice 三、完形填空(15分) It was June. The sun was shining brightly in the sky. It was very 35 . Jim was 36 of school. He wanted to be at the 37 to have a swim. He could not stay in his 38 . He could
2020届高三化学上学期期中试题201912040198
2020届高三化学上学期期中试题 相对原子质量:H 1 Li 7 C 12 N 14 O 16 Na 23 Mg 24 Al 27 S 32 Fe 56 Pb207 第Ⅰ卷(选择题共42分) 一、选择题(本题包括21小题,每小题2分。每小题只有一项符合题目的要求) 1.下列有关化学用语使用正确的是() A.氯离子(Cl-)的结构示意图: B.氯化铵的电子式: C.CH4分子的比例模型: D.次氯酸的结构式:H-Cl-O 2.下列各组物质中,前者属于电解质,后者属于混合物的是() A.纯碱,饱和食盐水 B.氯水,漂白粉 C.盐酸,碱石灰 D.液氨,硫酸铵 3.下列变化过程涉及氧化还原反应的是() A.从海水中获取氯化镁B.煤的液化和气化 C.使用泡沫灭火器产生泡沫D.铝土矿用强碱溶解 4.化学与生活密切相关。下列说法错误 ..的是() A.磁性氧化铁可用作红色油漆和涂料 B.漂白粉可用于生活用水的消毒 C.氢氧化铝可用于中和过多胃酸 D.硅胶可用作袋装食品的干燥剂 5.在一定温度下,向体积不变且相同的两个容器中,一个充入NH3,另一个充入N2与H2物质的量之比为1:3的混合气,使两个容器的压强相同。则两个容器内一定相等的是()
A.原子数B.分子数C.质量D.密度 6.N A表示阿伏加德罗常数。下列叙述中正确的是() A. 标准状况下,2.24L水中含H原子的数目为0.2N A B. 1L 0.1 mol·L-1KNO3溶液里含O原子的数目为0.3N A C. 2.3g钠反应生成Na2O和Na2O2的混合物,转移电子的数目为0.1N A D. 1mol H3O+和1molNH4+中含质子的数目均为10N A 7.下列反应可用离子方程式“ H++OH-= H2O ” 表示的是() A.NaHSO4溶液与KOH溶液混合 B.NaHCO3溶液与KOH溶液混合 C.H2SO4溶液与Ba(OH)2溶液混合D.向Fe(OH)3沉淀中滴加稀硝酸 8.下列反应的离子方程式正确的是() A.氯气溶于水:Cl2+ H2O = 2H++ Cl-+ ClO- B.氧化亚铁溶于稀硝酸:FeO + 2H+=Fe2++ H2O C.向三氯化铝溶液中滴入过量氨水:Al3++3NH3·H2O =Al(OH)3↓+3NH4+ D.金属钠投入水中:Na + 2H2O =Na++ 2OH-+ H2↑ 9.某无色溶液中加入铝粉能放出氢气,在该溶液中一定可以大量共存的是() A. Na+、NH4+、SO42-、CO32-B. Na+、Cu2+、Cl-、SO42- C. Na+、K+、Cl-、SO42- D. Na+、K+、Cl-、NO3- 10.工业上处理黄铜矿(主要成分是CuFeS2)的主要反应是2CuFeS2 + 4O2= Cu2S + 3SO2 + 2FeO。 关于该反应的下列说法中,不正确 ...的是() A.CuFeS2既是氧化剂又是还原剂 B.还原产物有Cu2S、SO2、FeO C.Fe元素的化合价没有变化 D.每反应1 molCuFeS2,转移电子8 mol 11.下列事实不能 ..用元素周期律解释的是() A.原子半径:Na > O B.气态氢化物的稳定性:H2O > H2S
江苏省盐城市初级中学2019-2020学年九年级上学期期中考试化学试题(已审阅)
盐城市初级中学2019-2020学年度第一学期期中考试 九年级化学试题 (考试时间:60分钟 卷面总分:70分) 一、选择题(本大题共15小题,每小题2分,共30分,请将正确答案填写到答案纸中) 1、“做文明人,创文明城”下列做法不符合这一要求的是 ( ) A .垃圾分类回收,以保护环境 B .将工厂废液偷排入江河,以减少成本 C .禁止就地燃烧秸秆,以减轻雾霾影响 D .骑公共自行车出行,以减少污染 2、下列属于化学变化的是 ( ) A .水沸腾变成水蒸气 B .胆矾研碎 C .铁锅生锈 D .石蜡熔化 3、下列有关氢气的“自述”,错误的是 ( ) A .我难溶于水 B .我可以用向上排空气法收集 C .我通常是无色无气味的气体 D .我具有可燃性 4、如下图,这四位同学描述的可能是下面的哪一个化学符号 ( ) A .HCl B .SO 3 C .H 2O D .NO 3— 5、下列有关实验现象,描述正确的是 ( ) A .红磷在空气里燃烧产生大量的白雾 B .木炭在空气里燃烧生成了二氧化碳气体 C .硫在空气中燃烧发出淡蓝色火焰 D .铁丝在空气中燃烧火星四射,生产黑色固体 6、下列实验操作正确的是 ( ) 7、目前未计入空气污染指数的项目是 ( )
A.SO 2 B.CO 2 C.CO D.可吸入颗粒物 8、用10mL 量筒量取2mL 氢氧化钠溶液倒入试管中,然后用滴管向该试管中滴加硫酸铜溶液,产生蓝色沉淀,再将试管中的混合物加热,加热后可观察到试管中的蓝色沉淀变成( ) A.白色 B.黑色 C.无色 D.蓝色(不变色) 9、近年来,有关PX 毒性的争议源源不断,其化学式为C 8H 10,名称为对二甲苯。下列有关PX 的说法正确的是 ( ) A .PX 是由8个碳原子和10个氢原子构成的 B .PX 是由10个氢元素和8个碳元素组成的 C .PX 分子是由碳元素和氢元素组成 D .一个PX 分子含有18个原子 10、结合右图分析,下列说法错误的是( ) A .硅元素属于金属元素 B .氧原子的核电荷数为8 C .铝原子在化学反应中易失去电子形成Al 3+ D .铁的相对原子质量为55.85 11、三氧化二铬(Cr 2O 3)可用作油漆颜料,Cr 2O 3中Cr 的化合价是 ( ) A . -3 B .-2 C .+2 D .+3 12、决定元素种类的是 ( ) A .质子数 B .中子数 C .电子数 D .相对原子质量 13、下列变化不属于氧化反应的是 ( ) A .分离液态空气制氧气 B .呼吸作用 C .木炭燃烧 D .食物腐败 14、下列有关过滤的说法中错误的是( ) A.过滤可以除去水中难溶性杂质 B.过滤后的液体仍然浑浊可以再次过滤 C.过滤时液面要低于滤纸上边缘 D.过滤时玻璃棒的作用是搅拌 15、某同学用排水法收集氧气,在实验准备时向集气瓶中加入约200mL 水(集气瓶的容积为250mL ),就将集气瓶盖上玻璃片倒扣在水中,其他操作均正确,则该同学收集满氧气后可获得的氧气的体积约为( ) A.200mL B.250mL C.180.5mL D.210.5mL
高一化学学科试卷分析
宿州市十三所重点中学2020-2021学年度第一学期期中质量检测 高一化学学科试卷分析 灵璧一中高一化学学科组 一、试卷结构 1、试卷结构 本次期中考试共分Ⅰ、Ⅱ两卷,Ⅰ卷1—16题为选择题,分值48分,Ⅱ卷17、18为填空题,19题为推断题,20题为实验题,21题为计算题,分值52分,共计100分。 2、试卷评价 试卷有一定的区分度,试卷总体难度稍偏难,抽样分析难度系数在0.6左右。试卷能结合教材注重基础知识的考查,偏重于化学基础知识和化学实验运用的考查,较好体现在新课标的三维能力考查的要求。整套试卷无难题、怪题、偏题,主要目的是考查学生对最基本的知识理解和掌握情况,但试卷中基础偏易题相对较少,试卷适合对将来选修化学学生的知识和能力的考查,不太适合将来不选修化学学生学习兴趣和学习信心的培养。 二、试卷分析 1、整体分析
满分有3人,90-99有92人,80-89有187人,70-79有260人,60-69有320人,不及格有1249人,从及格以上来看符合正态分布,数据合理。 从考试情况来看,第4、9、11、12、13和20题得分率较低 选择题主要是考查学生对基础理论、概念辨析以及重要元素化合物等知识的掌握。涉及化学用语、阿伏伽德罗常数、离子共存、电解质溶液等。学科特色浓郁,知识层次鲜明,既有描述性知识又有迁移性和创新性知识,各层次的考生都有一定发挥的空间。 第4题
命题意图:本题考查分散系的相关知识,要求学生知道溶液、胶体和浊液的 区别和联系,知道肢体与其它分散系的本质区别,还要了解胶体中胶粒概念。 试卷中反映出的主要问题:学生得分情况不是很好,主要是学生不了解胶粒 的概念,误以为1molNaCl中有1mol胶粒。 第9题和第11题: 命题意图:考查物质的量相关概念。 试卷中反映出的主要问题:学生审题不清,误把原子数看成分子数做题导致 错误较多。对于气体摩尔体积与温度和压强有关,质量是物质的固有属性,不能 很好掌握标准状况和气体与22.4的关系。 第12题和第13题 命题意图:本题考查电解质的概念与离子方程式的书写,溶液中的离子共存, 要求学生能够熟练的判断离子方程式,以及运用离子共存条件判断溶液中的离子 共存情况。 试卷中反映出的主要问题:学生得分情况不是太好,经分析和调查后主要问 题在于学生运用所学知识的能力较差。 第18题 命题意图:本题是一道溶液配制的填空题。以一定物质的量浓度溶液的配制 为载体,涉及具体考点有实验仪器的使用、实验误差的判断、电解质和非电解质 的判断、物质的量浓度的相关计算等。 试卷中反映出的主要问题:1、回答言语不够严谨,如在第(2)小题中很多学生都回答出了量筒,但没有指明量筒的规格,导致失分;2、第(4)小题得分情况很不好,不理解溶液配制的具体顺序;3、误差分析中仰视与俯视导致的误差容易颠倒。 相应措施:训练学生严谨的解题习惯,化学用语要规范,不丢三拉四。 第19题 命题意图:本题为离子推断题。重点考察通过物质之间反应时的不同现象来 推断离子,特别突出常见反应的考察。 试卷中反映出的主要问题:1、不会书写离子方程式,氢氧化镁不知道写沉 淀符号。2、离子共存条件不熟练,不会根据现象判断何种离子在反应。3、离子 检验不熟悉,检验氯离子时只知道加入硝酸银而不知道加入硝酸来检验。 相应措施:离子共存和离子检验是高考的必考内容,应进行专题讲练,使学 生在熟练掌握基础知识的基础上能够准确书写离子方程式。 第20题 命题意图:本题主要考查物质探究的过程与实验顺序。 试卷中反映出的主要问题:学生对物质探究不熟悉,心生胆怯。对化学反应 实验装置看不懂,不知道各种装置的作用,不会从对比实验中得出结论,还有审 题不清,从而得出相反的结论。
最全面江苏省盐城中学期中考试初三物理试卷(精华版)
盐城市初级中学2009∕2010 学年度第一学期期中考试 初三年级物理试题(2009 .11 ) ( 考试时间:100 分钟卷面总分:100 分) 命题人:胥加波审核人:宗炜斌 一、选择题(每题 2 分,共24 分) 1. 下列各物理量中能反映物质特性的是() A. 比热容 B.内能 C.热量 D. 温度 2.如图所示的工具中,属于费力杠杆的是() A. 钢丝钳 B. 起子 C.羊角锤 D. 镊子 3.小明去商场购物,自动扶梯把他从一楼匀速送到二楼的过程中,他的() A. 动能减小 B.势能不变 C.机械能增大 D. 机械能不变 4.下列属于通过做功途径改变物体内能的是() A. 在火炉上浇水,水温升高 B. 感冒发烧,用冷毛巾敷额头 C.用气筒给轮胎打气,气筒壁发热 D. 炎热的夏天,柏油路面温度升高 5.在动滑轮上施加了10N 的力,刚好把一个物体匀速提起,那么所提的物体的重力是(动滑轮的重和摩擦 不计)() A.20N B.5N C.25N 20N D.5N 或 6.如图为某种吊车的工作示意图,利用伸缩撑杆可使吊臂绕O 点转动,伸缩撑杆为圆弧状,伸缩时对吊臂的支持力始终与吊臂垂直。下列关于这个吊车的有关说法正确() A. 吊臂是一个省力杠杆 B. 使用这种吊车,好处是可以少做功。 C.匀速顶起吊臂的过程中,伸缩撑杆的支持力大小保持不变 D. 匀速顶起吊臂的过程中,伸缩撑杆的支持力渐渐变小
7.如图所示的简单机械均不计摩擦且动滑轮不计重力, B 图中R=2r,其中最省力的是() 8.如图所示,定滑轮重2N ,动滑轮重1N,物体 A 在拉力F 的作用下,1s 内将重8N 的物体 A 沿竖直方向匀速提高了0.2m。如果不计绳重和摩擦,则以下计算结果正确的() 第8 题图 B. A. 绳子自由端移动速度为0.6m∕s 滑轮组的机械效率为80% D. C. 拉力F 的功率为 1.8W 拉力F 的大小为5N 9. 关于热机的效率,下列说法中正确的是() A. 热机做的有用功能越多,效率一定越高 B. 热机消耗的燃料越少,功率一定越高 C. 热机做的有用功一定,消耗的燃料越少,效率一定越高 D. 热机做功越快,效率一定越高 10. 一个同学在使用电流表测电路中电流时,应当使用“一”和“3”两个接线柱,但他错误地使用了“一”和“0.6 ”两个接线挂,其他操作均正确,这样做的结果是() B. A. 指针偏转的角度小了、读数不正确指针反向偏转 D. C. 指针不动、无法读数指针迅速过大偏转,电流表可能损坏 11. 小华用电流表测串联电路中的电流时,闭合开关后发现电流指针来回晃动,灯泡时亮时暗,则可能发 生故障的原因是() B. C. A. 导线断开开关断开灯泡与灯座接触不良 D. 电流表损坏 12. 小明准备在前后门安装两只声音不同的电铃,希望能从铃声分辨出是前门来客还是后门来客。下图中, 设计的电路图正确的是()
高二化学期中考试试卷分析
在反思中 -----高一化学期中检测质量分析 矿务局中学刘花 一、试题的整体结构与难度: 1、试题的结构: 试题范围包括了化学选修4《化学反应原理》中第一章《化学反应与能量》与第二章《化学反应速率与化学平衡》的内容。 2、试题的难度及特点: 本试题难度适中,考查的虽然都就是基本知识与实验,但就是比较灵活。试卷体现了新课标的教学理念,能注重基础与能力,注重考查学生知识的应用性、解题的规律性、思维的灵活性,体现了新高考对能力与素质的要求。试题既较好的检测了学生化学基础知识掌握情况,又对学生学习起到了一定的诊断、指导与激励作用。 二、试卷结构与特点 1.试卷结构 第一大题选择题1—15题共45分。第二大题填空及简答题16—19题共31分。第三题实验及探究性题20题共12分。第四题计算及分析题21题共8分。卷面分4分。本次试题总分为100分。 2.试卷特点 (1)坚持了对化学主干知识的考查 ①试卷的结构及各知识块的赋分及试题难度比例与《考试大纲》的要求基本保持一致,试卷长度适中,题量恰当,答案的书写量也较为合适,给学生留有较多分析与思考的时间。 ②化学能量与反应、化学反应速率与化学平衡等。 (2)提高了对化学学科内综合知识的考查 本份试卷不管从内容还就是形式上都有一种高考试卷的风格,试题的质量、试题的新颖度、对考点的要求、对学生能力点的要求以及对学生情感态度价值观的渗透等做的均比较到位。 3.试题分析 1、单项选择题1、 2、 3、5、8做得相对好些。 4、7、10、12、14做得较好。 5、9、11、13、15做得较差。第5小题考查同一反应中不同物质表示其反应速率的大小比较,学生算错的较多。第9题考察化学键断裂时需要吸收能量的多少。11题考察外界条件改变对可逆反映的影响。13题同11题考察内容一样形式不同。15题图像的方式考察外界条件的改变可逆反应的影响。 2、非选择题答题情况比较差。
英语_2017年江苏省盐城市大丰市中考英语二模试卷(含答案)
2017年江苏省盐城市大丰市中考英语二模试卷 一、单项选择(共 15 题,每题 1 分,计 15 分)从 A、B、C、D 四个选项中选出一个可以填入句中空白处的最佳答案. 1. Good news!We'll have ________ one﹣day holiday.Let's go on a spring outing.() A a B an C the D / 2. ﹣﹣﹣What do you think of the vegetable soup? ﹣﹣﹣Well, it________a little salty.() A looks B smells C sounds D tastes 3. If we don't pay much attention to the________,the pollution will get worse and worse.() A Development B environment C government D treatment 4. —The stuntman is planning to walk on the wings of a flying plane. —What? I've never heard of ______ idea before. A a crazier B the crazier C a craziest D the craziest 5. ﹣Jane won the first prize in the English speech contest. 一________big progress she has made!She used to be weak in English.() A How B How a C What D What a 6. ﹣Which of these shirts do you like best? ﹣I'll take ________.They are all expensive and out of fashion.() A neither B either C none D both 7. Before the match, make sure you know________your competitor's advantages and disadvantages.() A hardly B exactly C luckily D nearly 8. -As a nurse,her work goes _____ taking care of her patients. -Yes,she always thinks of others.() A beyond B beside C behind D between 9. ________he isn't rich, he keeps on giving money to charity.() A Unless B If C Though D Since 10. Before Julie left, Mrs. Griffin said, "You'd better take an umbrella with you.Look at the dark clouds in the sky. It________rain."() A can't B need C mustn't D might 11. 一 Did you watch the fashion show on TV last night? 一I wanted to,but my mother ________ her favorite TV programme.() A watched B was watching C is watching D has watched 12. 一How was your May Day holiday? 一Just so﹣so.We drove to Suzhou and tried to find a place for parking,but they were all ________.() A turned up B taken up C stayed up D put up 13. ﹣What else should we pay attention to _______ building the bridge? ﹣﹣The change of the weather,I think.() A finish B finished C to finish D finishing 14. ﹣﹣What did Tom say to you just now,John? ﹣﹣He asked _____________.()
江苏省启东市2021届高三上学期期中考试化学试题 Word版含答案
2020-2021学年第一学期期中考试 高三化学试题 本卷满分100分,考试时间90分钟。 可能用到的相对原子质量:H 1 Li 7 B 11 N 14 O 16 S 32 Cl 35.5 Cu64 选择题(共40分) 一、选择题:本题共10小题,每小题2分,共20分。每小题只有一个 ....选项符合题意。1.2020年9月,我国作出对于全球减排具有里程碑意义的承诺:2060年实现碳中和。碳中和是指直接或间接产生的温室气体排放总量,通过植树造林、节能减排、碳捕集与封存等形式,抵消自身产生的二氧化碳排放量,实现二氧化碳“零排放”。下列有关说法正确的是 A.CO2是导致温室效应和酸雨的主要气体 B.煤的液化、气化主要是为了减少CO2的排放 C.CO2催化加氢合成低碳烯烃属于化合反应 D.CO2分子间有间隔,故可将其压缩液化后封存 2.中国科学院科研团队研究表明,在常温常压和可见光下, 基于LDH(一种固体催化剂)合成NH3的原理示意图如右 所示。下列说法正确的是 A.该过程中没有非极性键的断裂与生成 B.氧化剂与还原剂的物质的量之比为3︰1 C.基于LDH合成NH3的过程不属于氮的固定 D.利用NH3容易液化的性质,将混合气体加压降温可分离出NH3 3.下列离子方程式书写正确的是 A.K2O2加入H218O中:2K2O2 + 2H218O ==4K+ + 4OH—+ 18O2↑ B.用铜作电极电解饱和食盐水:2Cl—+ 2H2O Cl2↑+ H2↑+ 2OH— C.NH4Al(SO4)2溶液与过量KOH溶液反应:Al3++ 4OH—== AlO-2+ 2H2O D.用氨水溶解AgOH沉淀:AgOH + 2NH3?H2O == [Ag(NH3)2]+ + 2H2O + OH—
江苏省盐城市初级中学2019-2020年第二学期九年级期中考试数学试卷
盐城市初级中学初三第二学期期中考试 一、选择题 1.?1 2的相反数是( ) A .-2 B.?12 C. 1 2 D.2 答案:C 2.下列各式中,计算结果为a 7的是( ) A. a 6+a B.a 2?a 5 C. (a 3)4 D. a 14?a 2 答案:B 3.一组数据:1,3,3,5,3,2的众数是 ( ) A.1 B.2 C.3 D.5 答案:C 4.下列艺术字中可以看作是轴对称图形的是( ) A.白 B.衣 C.天 D.使 答案:C 5.下列给出的几何体中,主视图和俯视图都是圆的是( ) A.球 B.正方体 C.圆锥 D.圆柱 答案:A 6.在百度搜索引擎中输入“平安盐城”,能搜索到与之相关的网页约12200000个,将这个数字用科学计数法表示为( ) A .0.122×108 B .1.22×108 C .12.2×107 D .1.22×107 答案:D 7.如果分式 x+2x 值为0,那么x 的值是( ) A.0 B.2 C.-2 D.-2或0 答案:C 8.若方程x 2?2x ?k =0没有实数根,则k 的值可以为( ) A.1 B.0 C.-1 D.-2 答案:D
二、填空题 9、因式分解:x2?1= 【答案】:(x?1)(x+1) 10、把抛物线y=x2向上平移2个单位,所得的抛物线的函数关系式为 【答案】:y=x2+2 11、如图,转盘中6个小扇形的面积都相等,任意转动转盘1次,当转盘停止转动时,指针指向红色区域的概率为 【答案】:1 3 12、如图,直线a,b被直线c所截,a//b,若∠2=40°,则∠1等于 【答案】:140° 的图形如图所示,则k 的取值范围是 13、已知反比例函数y=k?2 x 【答案】:k>2 14、如图,正方形ABCD内接于⊙O,若⊙O的半径是1,则正方形的边长是
期中考试化学试卷质量分析
期中考试化学试卷质量分析 针对我校本次期中考试试卷及学生答题情况,本组教师进行了认真分析,具体情况如下: 一、得分率及通过率 符合哈尔滨市试题题型和难度要求,试题既有利于建立科学的化学教学评价体系,又能发挥考试的选拔功能,具备较好的层次与区分度。 二、答题中体现出的教师的教学和学生学习方面的成就 1、基础知识扎实,知识掌握准确 从统计结果看第1、2、6、10题得分率和高超过了90%,第3、4、5、7、8、9、13、14题得分率比较高,超过了80%。这些题主要考察了学生对基础知识和基本技能的掌握的情况,学生的成绩较为理想,反映出学生在平时学习过程中对“双基”的掌握情况达到了课标的要求,试题将双基的考察置于问题情境中。试题注重从学生日常生活、社会生产和新闻报道的社会热点问题中提取素材,生成问题,图文并茂使学生感到亲切,增强了学生对自然和社会的责任感。 2、学生具有收集和处理信息的能力,化学语言表达能力,达到了课程改革目标之一。例如:第34题B到C 过程中气球由小变大,再由大变小图示信息提炼出镁与稀盐酸反应为放热反应,这个信息的获取,再结合理化知识来解释A到B过程中现象产生的原因,培养了学生的科学素养。 3、注意审题、思路清晰,体现出热爱祖国、热爱社会,关爱他人的积极情感。 第31题第(1)增大煤粉与氧气的接触面积,供给燃烧充足的氧气,使煤粉充分燃烧,提高燃料的利用率,在烟囱上安装净化过滤装置,建议有的同学使用清洁能源,采用脱硫没技术,风力发电,太阳能发电等。第35提连接成一个五角星,体现了公平、公正和希望,实现了知识性和思想性的结合。体现了热爱祖国的积极情感。 第29题从微观的角度解释魔术中的奥秘,体现了学生具有宏观与微观、具体与抽象的思维的结合能力,并能用较准确的化学语言来表达一个化学变化发生的实质过程。 4、学生运用知识的能力、逻辑思维能力、探究能力逐渐提高 第36题:表格部分 5、具备一定的计算能力 试卷中的第15题和37为计算题,第15题的难度不大,通过率为57%,第37题最后一问有一定的区分性,通过率为25.7%,体现了平时教学中注重了学生基本计算能力的培养,达到了考试说明的要求,学生的过程计算、综合司思维能力得到发展。 三、答卷中发现的问题与今后的对策 在成绩的背后还存在着一些问题,为全面提升学生的各项能力,更好地服务于今后的教育教
江苏省盐城市大丰市九年级化学下学期第一次调研试卷(含解析)
2015-2016学年江苏省盐城市大丰市南阳镇初级中学九年级(下)第一次 调研化学试卷 一、选择题(本题共15小题,每小题只有一个选项符合题意.每小题2分,共30分.) 1.下列物质的用途与化学性质有关的是() A.用生铁制铁锅 B.氧气供给呼吸 C.用木炭除去鞋柜、冰箱内的异味 D.用16%的食盐水来选种 2.一种“环保石头纸”的主要原料是碳酸钙和高分子材料.“环保石头纸”属于() A.单质B.化合物C.混合物D.纯净物 3.大丰区濒临黄海,物产丰富.大丰特产闻名遐迩,下列大丰特产中富含维生素的是()A. 神王麻虾酱 B. 刘庄香肚 C. 恒北早酥梨 D.
小海香干 4.下列图示的实验操作中,正确的是() A. 稀释浓硫酸 B. 称取氯化钠 C. 过滤 D. 制取氧气 5.“纸火锅”(如图)是用纸张代替金属材料做容器盛放汤料,当酒精燃烧时纸张不会燃烧.对此现象,下列解释合理的是() A.纸张不是可燃物,不能燃烧 B.纸张被水浸湿,导致着火点降低 C.水蒸发时吸热,温度达不到纸张的着火点
D.纸张没有与空气接触,不会燃烧 6.下列四种金属中,有一种金属的盐溶液与其它三种金属都能发生置换反应,这种金属是 () A.Ag B.Cu C.Fe D.Mg 7.下列各组物质的鉴别的方法不正确的是() A.用肥皂水鉴别硬水与软水 B.用灼烧的方法鉴别奶粉和淀粉 C.用酚酞试液鉴别食盐水和白醋 D.用燃着的小木条鉴别氧气与二氧化碳气体 8.某种玉石的主要成份是NaAlSi2O6.关于NaAlSi2O6的说法正确的是() A.相对分子质量为202克 B.该物质由9个原子构成 C.该物质中含有二种金属元素 D.该物质中钠元素与氧元素质量比为1:6 9.“低碳生活”简言之就是降低二氧化碳的排放,就是低能量、低消耗、低开支的生活方式.下列做法不符合低碳生活方式的是() A.骑自行车上学B.多用相对廉价的煤 C.用淘米水浇花D.减少使用塑料袋 10.下列说法正确的是() A.煤、石油、乙醇是三种重要的化石燃料 B.洗洁精能除去餐具的油污是“乳化作用”的原因 C.铁元素在自然界中主要以铁合金和钢两种形式存在 D.“白色污染”是指白色建筑材料垃圾引起的污染 11.下列化学实验中能达到预期实验结果的是() A.借助托盘天平和其他手段测定铜锌合金中锌的质量分数为36.25% B.用pH试纸测定某未知溶液的pH为5.5 C.20℃时,配制2%的氢氧化钙溶液 D.将100g 10%的稀盐酸加热蒸发掉50g水,使得稀盐酸溶质质量分数变成20% 12.如图是a、b、c三种物质的溶解度曲线.由图示判断下列说法中正确的是()
