电镀黄铜工艺培训知识

第六章电镀黄铜工艺
第一节概述
在第二章中已经介绍了黄铜镀层对钢帘线与橡胶粘合的至关重要的作用,本章将阐述获得黄铜镀层的方法,即电镀黄铜工艺。
铜含量高于锌的铜锌合金通常称为黄铜,1841年就已发明了镀黄铜。最早的镀黄铜槽液是把硫酸铜和硫酸锌转换成碳酸盐,然后再在氰化钾溶液中溶解,使用低电流密度进行电镀。这种方法一直沿用到1915年,随着科技的进步发展成为现代的氰化电镀工艺。1974年第三版《现代电镀》中提到,专家们“研究了在1960年之前研究过的所有不同类型镀黄铜槽液之后下结论说,迄今为止,还没有一种槽液能满意地代替氰化黄铜槽液”。因为氰化物剧毒,人们总想摆脱它,一直在研究非氰电镀黄铜工艺。60年代,一些欧洲国家(如前苏联、意大利等)对“两步法”(先镀铜,后镀锌,再热扩散而形成铜锌合金的方法,又称热扩散法)非氰电镀黄铜工艺进行了工业性试验,并于70年代投入了规模生产。值得一提的是,我国从60年代末开始,曾探索过“一步法”(直接镀铜锌合金的方法)非氰电镀黄铜工艺,选用焦磷酸盐一草酸镀液体系,从实验室试验到中间试验反复进行了几年时间,先后生产了Φ0.8mm镀黄铜钢丝10余吨,捻制成7×3×0.147和3+9+9×3×O.147两种结构钢帘线用于子午线轮胎,进行了里程试验,并与氰化电镀产品对照,所得数据表明其质量与氰化法不相上下。后来投入大生产时,仅连续运行几天时间便发现阳极钝化严重,经试验分析初步认定是镀液中派生物磷酸氢二钠过多所致,最后高达lOOg/l以上,而且很难除去。工程技术人员做了大量工作,企图复苏焦磷酸盐一草酸电镀液,限于当时的条件,工作未能继续下去,最后不得不终止它的应用。这种独创性的电镀黄铜工艺虽未取得最后成功,但对后人有借鉴作用。
目前,钢丝电镀黄铜工艺处于氰化法和热扩散法并存在的局面。据国外考察,意大利几乎所有的钢帘线生产厂都采用热扩散法电镀工艺;而法国米其林公司年产18.5万吨钢帘线,则全部采用氰化法电镀工艺,只有在泰国所建的一个分厂采用热扩散法。世界上许多国家包括我国,在采用热扩散法的同时,仍保留了氰化法电镀工艺。我国自80年代以来,引进两步法热扩散电镀黄铜作业线至少有6条(包括单丝电镀作业线,即单根钢丝在镀槽中来回走镀多圈以达到所需的镀层厚度,线速可达200--300m/min),几乎无一例外地费了很长的时间进行调试方达基本正常。关于氰化法和热扩散法两者的利弊,将在对两种工艺作系统阐述后再进行比较。
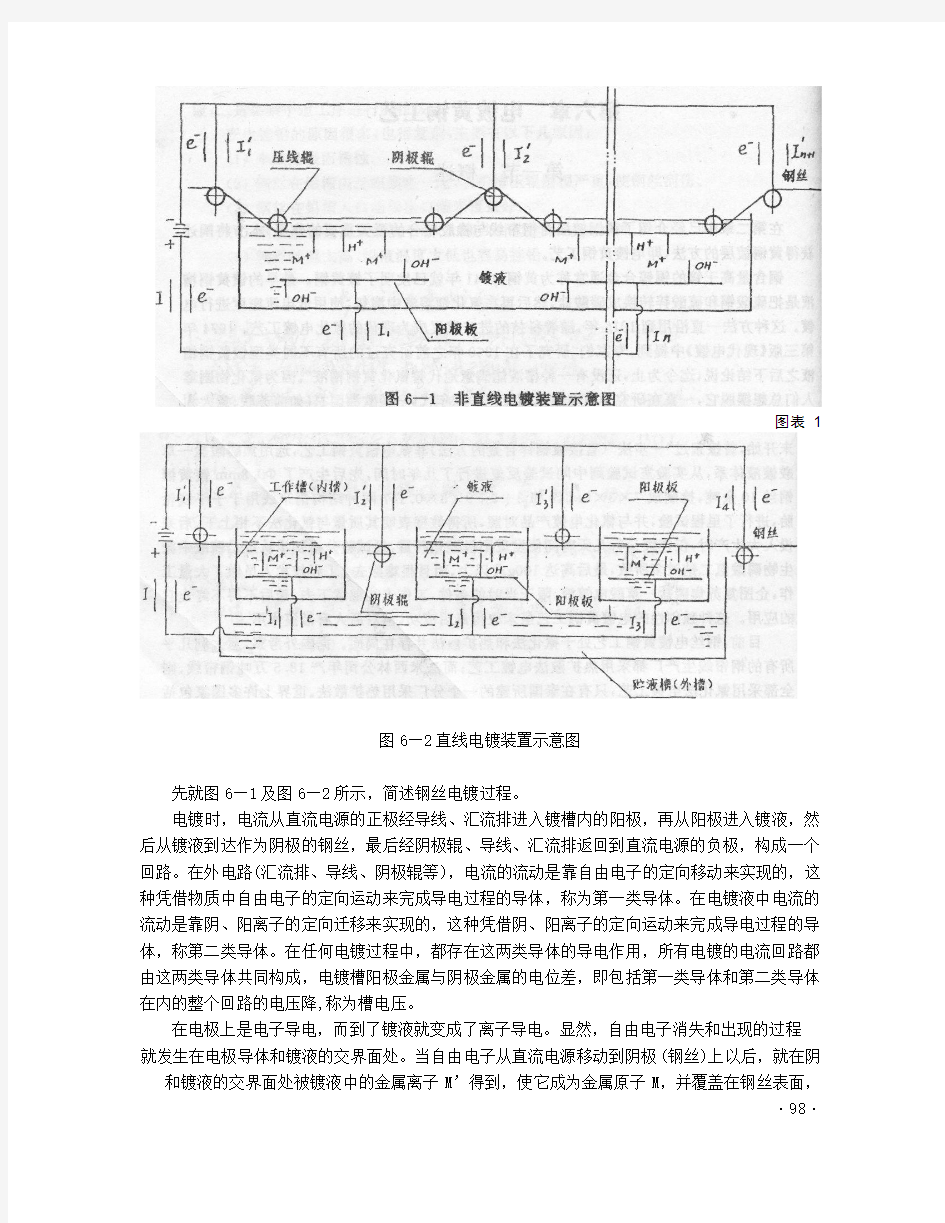
钢丝电镀不同于零件电镀,钢丝是在镀槽中不断前进的,俗称“走镀”。图6--1所示,钢丝在镀槽中是曲折前进的,钢丝所遇阻力较大,限制了线速度,影响生产率,但设备比较简单;图6—2所示,钢丝在镀槽中是直线前进的,钢丝所遇阻力较小,线速度可以大幅度提高,生产率也随之提高,但设备比较复杂。在设计电镀作业线时,必须考虑两个重要参数:一是dv值,即钢丝线速(m/min)与钢丝直径(mm)的乘积;二是穿线根数(n)。DV值与n数越大,生产率便越高。目前国外多丝电镀黄铜作业线dv值可达60,n数可达50,我国尚未达到这个水平。
·97·
图表1
图6—2直线电镀装置示意图
先就图6—1及图6—2所示,简述钢丝电镀过程。
电镀时,电流从直流电源的正极经导线、汇流排进入镀槽内的阳极,再从阳极进入镀液,然后从镀液到达作为阴极的钢丝,最后经阴极辊、导线、汇流排返回到直流电源的负极,构成一个回路。在外电路(汇流排、导线、阴极辊等),电流的流动是靠自由电子的定向移动来实现的,这种凭借物质中自由电子的定向运动来完成导电过程的导体,称为第一类导体。在电镀液中电流的流动是靠阴、阳离子的定向迁移来实现的,这种凭借阴、阳离子的定向运动来完成导电过程的导体,称第二类导体。在任何电镀过程中,都存在这两类导体的导电作用,所有电镀的电流回路都由这两类导体共同构成,电镀槽阳极金属与阴极金属的电位差,即包括第一类导体和第二类导体在内的整个回路的电压降,称为槽电压。
在电极上是电子导电,而到了镀液就变成了离子导电。显然,自由电子消失和出现的过程就发生在电极导体和镀液的交界面处。当自由电子从直流电源移动到阴极(钢丝)上以后,就在阴
和镀液的交界面处被镀液中的金属离子M’得到,使它成为金属原子M,并覆盖在钢丝表面,
即在钢丝表面镀上一层金属M,其反应式为:
M++e-→M
这是一个电化学反应,属于还原反应。它发生在电极表面,故可称为电极反应。又由于它是在阴极上发生的,故可称之为阴极反应。正是由于阴极发生的电化学反应,才使得从电源流到阴极的电子和镀液中向阴极迁移过来的金属离子都有了去路,正是阴极反应实现了电子导电与离子导电的相互转化。
阳极所发生的情况与阴极相反,在外电源的作用下,阳极金属M的电子不断流入电源,即阳极金属M在极板与溶液交界的表面放出电子,这样金属M由原子变为金属离子而进入镀液,同时向阴极迁移,其反应式为:
M+e-→M+
这个电化学反应属于氧化反应。它发生在阳极,故可称为阳极反应。正是由于阳极反应的发生,使得从阳极流入电源的电子和从阳极附近迁移的金属离子有了补充的来源,也正是阳极反应实现了离子导电与电子导电的相互转化。
在实际电镀时,阴、阳两极的反应可能并不止这些,如阴极上除了金属M的沉积之外,还有H+得到电子还原为H2析出;阳极上除了金属M的溶解之外,还可能有OH—失去电子氧化成O2析出。但不论阴、阳极上发生何种还原和氧化反应,在导电意义上都是相同的。
综上所述,钢丝电镀是指在含有被镀金属的盐溶液中,以钢丝为阴极,在外电源的作用下,通过电解反应,使金属或合金沉积在钢丝表面,以形成均匀、致密、结合力良好的金属层的表面处理方法。由于钢丝电镀是一种利用电化学方法使金属电沉积的过程,为了叙述方便和便于理解,须介绍一些电化学的基础理论知识,但限于篇幅,只能涉及最初步的知识。欲进一步深入理解,还要参阅有关电镀的教科书、专著和手册。
第二节电化学基础理论知识
一、电极电位
(1)原电池电动势
所谓原电池指的是可将化学能转变为电能的装置。例如将金属锌插在ZnS04水溶液中作为一极,将金属铜插在CuS04水溶液中作为另一极,两个溶液之间用盐桥(含有饱和KCl溶液)连通,便组成一个原电池。如果将Cu和Zn两极接通,在负载电阻不太大时,将发现外线路中有一定大小电流通过。自由电子自发地从锌电极流出,经外线路到达铜电极,这相当于电流从铜电极流向锌电极。
上述ZnS04、CuSO4,在水溶液中能够导电的物质称为电解质。电解质加入水中后,由于水分子是极性分子,它的一端呈正电性,会吸引离子化合物中的阴离子。作用的结果使阴阳离子从固体表面溶入水中,并且使溶入水中的阴、阳离子周围吸引着数目不等的水分子。这个过程称为水合作用,发生水合作用的离子称为水合离子。
溶液中大量分子和离子彼此之间总是互相牵制的,每一个离子或分子的活动能力都要受到其它离子和分子的影响,使得它们都不能充分发挥各自应当发挥的作用,这就产生了离子活度的概
·99·
念。所谓活度,可以认为是有效浓度。只有在无限稀的溶液中,活度等于浓度。
再回到原电池上来,既然两极接通后,有电流从外电路流过,这说明两极之间存在着电位差。将原电池开路时两极间的电位差,称为原电池的电动势,用E表示。
(2)相对电极电位
金属(电子导电相)和电解质(离子导电相)直接接触所构成的体系称为电化学电极,简称电极;有时也将此体系中的金属相称作电极。
上述铜一锌原电池中的电流便是两极发生的电化学反应而产生的。为什么两极会自发地发生这种电化学反应?这与金属的电极电位有关。任何金属在水溶液中或多或少地有些溶解,存在着下列反应:
M≒M++e (6—1) 当Zn置于ZnSO4溶液中,则金属相的Zn2+有逾越相界进入溶液相的趋势,溶液相中的Zn2+也有逾越相界进入金属相的趋势。究竟哪一种趋势占优势,取决于Zn2+在这两相中的化学位的高低。因为Zn2+在金属相中的化学位大于在溶液相中的化学位,则金属相中的Zn2+逾越相界进入溶液相的趋势占优势,即反应方程式(6—1)的正向反应占优势。在Zn未与外电源构成通路的情况下,必定要达到这样一种状态,即(6—1)式反应的正反速度相等,也就是Zn原子的氧化速度和还原速度相等。这时金属相的表面带负电,而溶液带正电,分别积聚在两相的界面上,如图6—3的(a)所示,这就是通常所说的“双电层”,它是自发建立的,故称自发离子双电层。
当Cu置于CuSO4溶液中,因为Cu2+在金属相中的化学位小于在溶液相中的化学位,则溶液相中的Cu2+逾越相界进入金属相的趋势占优势,即反应方程式(6-一1)的逆向反应占优势,这时金属相的表面带正电,而溶液带负电,这种在金属电极与电解质溶液界面上存在大小相等,电荷符号相反的电荷层,叫双电层。如图6—3的(b)所示。当金属的还原能力较强,溶液中离子浓度较大时,双电层较为紧密,称为“紧密双层";否则就较为分散,称为“分散双层”,图6—3的(c)所示,既有紧密双层又有分散双层.
图表2
(a)(b)(c)
图6—3双电层结构示意图
综上所述,由于双电层的存在,就使得在金属电极与溶液界面之间产生了电位差,这种电位差就叫金属的电极电位。但是,我们经常使用的电极电位值并不是这种电位的绝对值。因为现在还没有足够可靠的实验方法能准确地测出这种绝对值。但可规定一个特殊的电极作
·100·
为参比电极,让待测电极电位的电极与这个特定的参比电极组成一个特殊的原电池,测量其开路电压(电动势),从而得到一种可以表征电极体系氧化还原能力的参数——相对电极电位。
现在国际上对电极电位通用的定义表述为;若任一电极M与标准氢电极组成一特殊原电池,此电池的电动势(开路电压,无电流通过时)E即为M电极的电极电位。
E=Φ
+一Φ
-
式中: E--原电池的电动势,单位V
Φ+—正极的电极电位,单位V
Φ-—负极的电极电位,单位V
(3)平衡电极电位
在双电层的形成过程中,把金属原子失去电子进入溶液的过程称为阳极过程,把溶液中水合金属离子或其它阳离子到金属上获得电子的过程称为阴极过程。若接上外电源,则在阳极上发生氧化反应,在阴极上发生还原反应,而将电能转变成化学能,这个过程称为电解。若未接上外电源,这两个过程是可逆的,当达到动态平衡时,两过程进行的速度相等,此时既建立起物质的平衡(电荷的交换靠同种物质完成),又建立起电荷的平衡,将产生一个稳定的电极电位,这时电极的相对电极电位就称为平衡电极电位,又称为可逆电极电位,用E P表示。
在实际电镀过程中,情况往往复杂得多,在阴极上有几种离子同时放电。显然阳极过程和阴极过程的物质的迁移是不平衡的,即使两过程反应速度相等,达到电荷平衡,仍是不可逆的,此时测得的电极电位称为非平衡电极电位,又称不可逆电极电位。
(4)标准电板电位
电极在25℃、1个大气压下,离子活度等于1时的相对平衡电位,称为标准电极电位,用E0表示。还规定在任何温度下标准氢电极的相对平衡电位都为零,这就是所谓“氢标”。
标准电极电位的数值可通过实验测得,或由热力学数据计算求得。表(6--1)列出了某些电极反应的标准电极电位。
平衡电极电位的大小可以作为电极体系氧化还原反应可能性的判据:电极电位愈正,则该电极体系的氧化态愈易获得电子而还原;电极电位愈负,则其还原态愈易失去电予而氧化。如铜的氧化态获得电子(Cu2++2e一→Cu)比锌的氧化态获得电子(Zn2++2e一→Zn)容易,因为铜电极电位(E0=+O.337V)比锌电极电位(E0=-0.763V)正;锌的还原态失去电子(Zn→Zn2++2e-)比铜的还原态失去电子(Cu→Zn2++2e-)容易,因为锌电极电位比铜电极电位负。也就是说,金属的电极电位愈正就愈易沉积,愈负就愈易溶解。这可以解释在电镀锌时为什么把镀液中的铁、铜、铅离子视为有害物质。因为这些金属的电极电位都比锌的电极电位正,更容易在阴极上沉积,所以尽管它们离子浓度比锌离子浓度低,但它们还是很容易在阴极上沉积出来,夹在锌镀层中,影响镀层的质量。
(5)能斯特(Nernst)平衡电极电位方程式
电极的平衡电极电位的数值与该金属的本性、溶液中金属离子的有效浓度(活度)、温度有关,其关系可用能斯特(Nernst)平衡电极电位方程式表示。
当金属离子以简单水合离子存在时,对任一电极反应:氧化态+n·e一=还原态,其能斯
特方程式为:
图表3
E P=E0+(RT/nF)ln(a±氧/a±还)(6--2) 式中:E P——平衡电极电位,V(伏)
E0——简单金属离子M n+还原为金属的标准电极电位,v(伏)
R--气体常数,为8.315J·K-1mol-1(焦耳/度·摩尔)
T--开尔文温度,K
F--法拉第常数,为96500C·mol-(库仑/摩尔)
n--参加电极反应的电子数,即金属离子的价数
a±氧——氧化态物质的平均活度,mol/l
a±还——还原态物质的平均活度,mol/l
a±氧实际上是该电极体系溶液中的有效浓度,其值可从有关电化学手册中查得。
a±还有如下规定:纯固态和纯液态物质的活度为1;气态物质在压力不大时,可近似地认为压力等于活度,例如latm(大气压)的H2,可以认为a=1。所以在一般情况下,a±还=1。
因而式(6—2)可简化为;
E P=E0+RT/nF·㏑α(6—3)
式中:α——溶液中离子的平均活度。
以上讨论的是金属离子以简单水合离子状态存在时的平衡电极电位的计算问题。以下
讨论金属以络合离子状态存在时的平衡电极电位。
如果一个金属离子在溶液中与化学基团或配位体(除水以外)相缔合,于是就形成了络合离子。任何络合离子在溶液中均有离解成它的组成成分的现象,其离解度的大小随各种络合离子的性质而异。络合离子离解达到平衡时的平衡常数称为络合离子的不稳定常数,记作Kd,其倒数1/Kd 称为稳定常数。Kd的数值越大,表示这种络合离子越不稳定,越易离解。Kd可以从有关化学手册上查找,查找时需注意Kd给出的方式,有时以其倒数形式或对数形式给出。以锌电极为例,当Zn2+与CN-络合形成[Zn(CN)4]2-络合离子时,则有下列平衡:
[Zn(CN)
4
]2-≒Zn2++4CN-
当溶液温度一定时,[Zn(CN)4]2-、CN-以及少量未经络合的简单水合锌离子Zn2+三者的浓度有如下关系:
C Zn 2+·C4
CN-
/C[Zn(CN)
4
]2-=Kd(6—4)
根据(6—3)式,此时锌电极的平衡电极电位:
E P Zn/Zn2+= E0+RT/nF·㏑αZn2+
由于Zn2+的浓度很低,故αZn2+近似等于C Zn2+,而根据(6—4)式,C Zn2+==Kd·C[Zn(CN)4]2-/ C4
CN-,代入上式可得:
E P Zn/Zn2+= E0+ RT/nF·㏑Kd·C[Zn(CN)4]2-/ C4CN-
如果加入络合剂CN-后使所产生的C CN-与C[Zn(CN)4]2-均为1mol/l,则:
E P= E0+ RT/nF·㏑Kd (6—5)
把Zn2+形成络合物后的标准电极电位记为E0L,以区别于αZn2+=1时的标准电极电位,则:E0L= E0+ RT/nF·㏑Kd (6—6)
对于其它络合物也有(6—6)式,将有关常数代入并将自然对数换算为常用对数,则有:E0L= E0+0.059/n·lgKd (6—7)
现将几种常用的金属络合离子的不稳定常数Kd及根据(6—7)式算出的络合后电极的标准电极电位E0L列于表6—2。
从计算结果看出,Zn2+经CN-络合后,其标准电极电位负移了近0.5伏,如果络合剂加
·103·
得太少不足以充分络合溶液中的Zn2+,则其负移的值小于O.5伏。 Cu+与CN一络合后,其标准电极电龟负移得更多,可达1.8伏。
在简单盐溶液中,Zn2+的标准电极电位(一0.763)与Cu z+的标准电极电位(+O.337)相差达1.1伏(见表6~1),两者不可能同时沉积,因为电极电位较高的金属,其氧化态较易还原,铜首先在阴极上析出。
表6-2
图表4
子的活度将相差几十个数量级,这显然是不现实的。在简单盐溶液中,待到锌开始沉积时,镀
液中已经没有几个铜离子了,所以在简单盐的混合液中是不可能一次镀出黄铜层的。
二、电极的极化
(1)极化和过电位
当有电流通过电极时,电极电位就偏离平衡电极电位,这种现象称为电极的极化。当电极表面进行氧化反应,其电极电位向正方向偏移,称为阳极极化。相反,如电极进行还原反应,电极电位变得较平衡电位更负,称为阴极极化。在其它条件相同时,通过电极的电流密度愈大,电极电位偏离平衡电极电位也愈大,亦即极化作用愈大。
当某一电流流过一电极时,其电极电位E与平衡电极电位E P的差值叫做该电极在此电流密度下的过电位。过电位一般都用正值表示。
阳极过电位△E a=E—E p (6—8)
阴极过电位△E k==E p一E (6—9)
(2)极化产生的原因
电极极化的原因很多,主要有如下几个。在实际电镀过程中,它们可能同时存在,只是在不同情况,它们各占的比重不同而已。
电化学极化由于反应粒子在电极——溶液界面得失电子较慢,而使从导线流入电极的电荷在电极表面积累或不足,以致使双电层中的电位差发生变化而形成极化,称为电荷传递极化,一般叫做电化学极化。
浓差极化由于反应粒子或产物的液相传质速度缓慢,故通电后,电极表面反应粒子或生成物粒子的浓度与平衡时的浓度不同,根据平衡电极电位方程式,电极电位也将发生变化,由此而形成的极化称为浓差极化。
电阻极化电镀过程中在电极表面生成一层氧化膜或其它物质,阻碍了电流的通过而引起的极化称为电阻极化。
新相极化由于反应产物生成新相,例如生成气泡或固相沉积层等的缓慢性而引起的极化称为新相极化。
(3)极化曲线与极化度
表示电极电位随着电流密度的变化而改变的关系曲线叫做极化曲线。一般以纵坐标表示电极电位,横坐标表示电流密度。图6—4所示为两条阴极极化曲线。
从曲线可以看出:随阴极电流密度不断增大,阴极电位也不断变负。若阴极电流密度D k改变某一值,曲线I和曲线I的△E值有所不同。通常把△E K与△D k的比值称为阴极极化度,曲线愈陡,阴极极化度愈大。
(4)极化对电镀的影响
提高阴极极化作用,可以使金属电结晶的速度加快,获得结晶细致的镀层;还使电流在阴极表面的实际分布更均匀,提高镀液的分散能力和深镀能力,使镀层更均匀。在生产中一般采用以下措施提高阴极极化作用:加入络合剂、添加剂,提高阴极电流密度,适当降低电解液温度等。
阳极极化作用会引起阳极的电化学钝化,钝化能使电极电位剧烈地向正方向移动,致使阳极不能正常溶解。电镀时要想办法消除和降低不必要的阳极极化作用,生产中一般采用以下方法;
·105·
加入适量的阳极活化剂可防止阳极钝化,促使阳极 正常溶解;增大阳极面积以降低其电流密度,利用 搅拌来降低阳极极化作用。 三、氢的过电位
在电镀过程中,阴极的电流效率的高低,与析氢 的副反应直接有关。阴极析氢不仅会降低电流效率, 降低了产量,增加了能耗,而且阴极析出的氢会部 分地进入钢丝的基体引起“氯脆”。因此有必要了解 氢电极的一些情况。 (1)氢的过电位
在给定电流密度下析氢时,其平衡电位△E H p
与极 化电位E H 之差称为该电流密度下氢的过电位△E H △E H =△E H p
一E H
(6—10)
实验表明,氢在不同金属上还原时,过电位是不同的,许多金属上氢的析出过电位与阴极电流密度的关系服从塔菲尔(Tafel)公式; △E H =a+blg|D k |
(6—11)
式中:D K --阴极电流密度,A /cm 2
。
a ,b--某些金属在一定溶液组成时析氢的常数,其值可从有关化学手册上查找。表6—3列出几种金属上氢过电位塔菲尔公式常数。
表6—3
·106·
图6—4阴极极化 曲线
四、金属电沉积过程
电镀过程是一种金属电沉积过程,具体说来,它指的是电解液中的金属离子在直流电的作用下,在阴极上沉积出金属的过程。金属电沉积过程也叫金属电结晶过程,这是因为镀层金属和一般金属一样具有晶体结构。
金属电沉积过程一般包括以下几个步骤:
(1)液相传质步骤——金属的水合离子向阴极表面迁移。
(2)电子转移步骤——金属水合离子脱水并与阴极上的电子发生反应,生成金属原子。
(3)电结晶步骤——金属原子排列成一定形式的金属晶体。结晶时又分为两个步骤进行:结晶核心的形成和晶核的成长。如果晶核的形成速度较快,而晶核形成后的成长速度较慢,则生成的结晶数目较多,晶粒较细。反之,晶粒就较粗。
五、法拉第(Faraday)电解定律
(1)法拉第电解第一定律
电流通过电解液时,在电极上析出或溶解的物质的量(m)与通过电极的电量(Q)成正比。用公式表达为:
m=C·Q=C·I·t (6—15) 式中:m——电极上析出(或溶解)的物质的量,g(克)
Q——通过电解液的电量,它等于通电时间(t)和电流强度(I)的乘积;
C---比例常数,称为电化当量,g/A·h
(2)法拉第电解第二定律
电解时,在电极上每析出或溶解1克当量的任何物质所需要的电量是一个定值,这个定值就是一摩尔电子所带的电量(96500库仑)。用公式表达为:
m=Q/F(克当量)=Q/F·A/n (6—16) 式中:F--法拉第常数,等于96500库仑(或26·8A·h);
A--物质的原子量;
n--物质的化合价;
(3)物质的电化当量C
物质的电化当量(C)的物理意义是:电极通过单位电量时电极析出或溶解物质的质量。由法拉第电解第一定律和第二定律可以推出如下关系式;
C=m/I·t=A/n·F (6—17) 由(6—17)式可知,物质的电化当量与其原子量成正比,与其化合价成反比。
(4)合金的电化当量的计算
如果电极上有两种或两种以上的金属同时析出或溶解,则合金的电化当量的计算方法如下:设合金的成分为A、B二种金属组成,它们的电化当量分别为C A、C B,金属A所占的重量百分比为a%,金属B所占的重量百分比为b%,显然有a%+b%=100%。为简便起见,设合金的析出量为100g,则金属A、B的析出量分别为a克和b克。
根据公式(6—15)有:
·107·
C A -B =100/Q A -B ,又Q A -B =Q A +Q B
C A -B -C =1/(a%/C A +b%/C B +c%/C C ) (6—22) 各种金属的电化当量C 可从有关手册查得。例如,查得Cu 2+的电化当量为1.186g/A ·h ,Zn 2+
的电化当量为 1.220 g/A ·h ,可用(6—21)式求得68:32黄铜得电化当量为C Cu -Zn =1/(0.68/1.186+0.32/1.220)=1.744 g/A ·h 。
六、电流效率
法拉第定律本是很严格的定律,但在电镀时却往往会出现形式上“违反”定律的现象。例如,电镀锌时,虽然阴极上通过了1法拉第电量(96500库仑),但得不到l 克当量的锌。这是电极上存在着副反应的缘故。镀锌时,阴极反应如下: Zn 2+
+2e -
→Zn(主反应) 2H +
+2e -→H 2↑(副反应)
如果把这两个反应的产物加在一起,则仍为1克当量,符合法拉第电解定律。 在阳极,除了锌的溶解外,也同样有副反应: Zn-2e -→Zn 2+
(主反应) 40H 一
-4e -→2H 2O 十O 2
↑(副反应)
在电镀时,副反应是我们不需要的,所以对镀层重量来说,提出了电流效率的概念。电极 的电流效率是用于主反应的电量在通过电极总电量中所占的百分数,即:
·108·
η一Q,/Q×100%=m,/m×100%(6--23)
式中η——电流效率
Q’——用于主反应的电量,
Q ——主反应和副反应的总电量
m’——电极上实际析出(或溶解)物质的量
m ——按理论计算应析出(或溶解)物质的量
一般酸性镀液如酸性镀铜、酸性镀锌的电流效率都很高,接近100%;碱性镀液的电流效率较低,如焦磷酸盐镀铜通常大于90%,氰化镀黄铜通常只有50--70%,镀铬一般只有10--20%。
在电镀生产中掌握电流效率十分重要,提高阴极电流效率能节约电能并提高生产率;还要注意阴极电流效率(ηk)与阳极电流效率(ηA)的平衡,使电镀过程稳定。
七、电流密度
阴极或阳极单位表面积上分布的电流强度分别称为阴极电流密度(D K)或阳极电流密度(D A),以A/d㎡(安培/分米2)表示。
任何镀液都有一个获得良好镀层的电流密度范围,这个电流密度范围的最小值(即获得良好镀层的最小电流密度)称为电流密度下限,最大值(即获得良好镀层的最大电流密度)称为电流密度上限。
提高阴极电流密度,可以提高阴极极化,使镀层结晶细致,同时还能加快沉积速度,缩短电镀时间,但是阴极电流密度太大,往往会使镀层烧焦。
电流密度范围的大小,通常是由镀液的性质、镀液温度、搅拌和PH值等因素决定的。一般,提高主盐浓度、升高镀液温度、加速搅拌镀液(镀液循环是一种搅拌形式)及降低镀液的PH值(指弱碱性或弱酸性镀液),可以提高电流密度上限,有时向镀液中加入适量的附加盐或添加剂,也能提高电流密度上限。
阳极电流密度随阳极电位的正移而增大,溶解速度也加快。当电位到达一定值后.再升高阳极电位,电流密度非但不增加,反而急剧下降几乎到零,电极由活化状态向钝化状态过镀,这个电位值称为临界钝化电位,对应的电流密度称为临界钝化电流密度。阳极电流密度只有低于这个临界值时,阳极才能正常溶解。但电镀时往往采用较高的阳极电流密度,为了保证阳极在低于临界钝化电流密度下正常溶解,那就必须保证阳极有足够大的表面积。
八、钢丝电镀有关运算公式的推导
(1)镀层沉积量的计算
由法拉第电解第一定律,金属在阴极的实际析出量有如下关系式
m=C·I·t·ηk (6—24)
式中:m--阴极析出金属量,g
C--析出金属的电化当量,g/A·h
I--通过阴极的电流强度,A
t--电镀时间,h
ηK——阴极电流效率
现场习惯用分钟(min)作单位,将(6—24)式中的t换算成分钟为单位,则
m=1/60·C·I·t·η
K
(6—25)
(2)镀层平均厚度的计算
就单根钢丝而言,若钢丝直径为d(mm)、钢丝浸入镀液的长度为L(m),析出金属的密度为γ沉积(g/cm2)、镀层平均厚度为δ(μm),则有下式:
m=π·d·L·δ·γ沉积×10-3(6—26)
将(6—25)式代入(6—26)式,得:
1/60·C·I·t·η
K =π·d·L·δ·γ
沉积
×10-3
移项后得下式:
δ= C·I·t·ηK/(60π·d·L·γ沉积)×103(6—27)
对于电镀铜,C cu2+=1.186g/A·h,γCu=8.92g/cm2,代入(6—27)式得:
δ=0.705 I·t·ηK/(d·L)=0.705 I·ηK/(d·V)(6—28)
式中:V=L/t(m/min)为电镀钢丝线速度(下同)。
对于电镀锌,C Zn2+=1.2196g/A·h,γZn=7.14g/cm3,代入(6—27)式得:
δ=0.906 I·t·ηK/(d·L)=0.906 I·ηK/(d·V )(6—29)
对于电镀黄铜合金(Cu,68%,Zn,32%),C Cu-Zn=1.744 g/A·h,γCu-Zn=8.35 g/cm3,代入(6—27)式得:
δ=1.108I·t·ηK/(d·L)=1.108 I·ηK/(d·V)(6—30)(3)钢丝单位表面积的镀层重量
W=δ·γ
沉积
(6—31)
式中: W——镀层重量,g/m2
δ——镀层厚度,μm
γ沉积——镀层金属的密度,g/cm3
将(6—27)式代入(6—31)式,得
W= C·I·t·η
K
/(60π·d·L)×103(6—32)对于电镀铜,将C cu2+=1.186g/A·h代入(6—32)式,得:
·110·
W =6.292I·t·η
K /(d·L)=6.292 I·η
K
/(d·V ) (6—33)
对于电镀锌,将C Zn2+=1.2196g/A·h代入(6—32)式,得:
W =6.470I·t·η
K /(d·L)=6.470 I·η
K
/(d·V)(6—34)
对于电镀黄铜合金,将C Cu-Zn=1.744 g/A·h代入(6—32)式,得:
W =9.25I·t·η
K /(d·L)=9.25 I·η
K
/(d·V ) (6—35)
(4)每公斤钢丝上的镀层重量
将t=L/V代入(6—25)式,得:
m= C·I·ηK·L/60V (6—36)当长度L=1m,则以克表示的1米钢丝上的沉积量为:
m= C·I·ηK/60V (g)(6—37)令P为以公斤表示的1米钢丝的重量,则:
P=π/4·d2·γ钢×10-3(kg)(6—38)则每公斤钢丝上的镀层重量为:
G=m/p=4C·I·ηK·103/(60V·π·d2·γ钢)(g/kg)(6—39)用γ钢=7.85g/cm3代入上式,得:
G=2.70827C·I·ηK/(V·d2)(g/kg)(6—40)对于电镀铜,将C cu=1.186代入(6—39)式,得:
G=3.206 I·ηK/(V·d2)(6—41)I Cu=0.312 G·V·d2/ηK(6—42)对于电镀锌,将将C Zn=1.2196代入(6—39)式,得:
G=3.2969 I·ηK/(V·d2)(6—43)I Zn=0.303G·V·d2/ηK(6—44)对于电镀黄铜合金,将C Cu-Zn=1.744 代入(6—39)式,得:
G=4.432I·ηK/(V·d2)(6—45)I Cu-Zn=0.226G·V·d2/ηK(6—46)
·111·
(5)镀层厚度与镀层重量的相互换算从(6—39)式可得:
C·I·η
K /(60π·d·V)=G ·d·γ
钢
/4 (6—47)
将(6—47)式代入(6—27)式,可得
δ= G ·d·γ钢/4γ沉积(6—48)
已知γCu=8.92 g/cm3,γZn=7.14 g/cm3,γCu-Zn=8.35 g/cm3,γ钢=7.85 g/cm3,分别代入(6—48)式,可得:
对于钢丝电镀铜,有:
δ=0.22 G ·d(μm)(6—49)
对于钢丝电镀锌,有:
δ=0.275G ·d(μm)(6—50)
对于钢丝电镀黄铜合金,有:
δ=0.235 G ·d(μm)(6—51)
将(6—48)式代入(6—31)式,再将(6—49)、(6—50)、(6—51)分别代入,则W= G ·d·γ
钢/4,可得以下各式:
对于钢丝电镀铜,有:
W=8.92δ(g/m2)(6—52)
W=1.9625d·G(g/m2)(6—53)
对于钢丝电镀锌,有:
W=7.14δ(g/m2)(6—54)
W=1.9625d·G(g/m2)(6—55)
对于钢丝电镀黄铜合金,有:
W=8.35δ(g/m2)(6—56)
W=1.9625 d·G(g/m2)(6—57)
为了查找方便,将(6—49)式至(6—57)式的换算关系列于表6—4。
·112·
表6—4
第三节钢丝的镀前表面处理
钢丝镀前表面往往沾有油污,它来源于拉丝润滑剂等物质,油污的主要成分有硬脂酸及盐,动物油,矿物油等。这些物质不仅在酸洗时阻碍了酸液与氧化铁皮(由铅浴淬火热处理形成)的充分浸润,而且也会影响镀层质量,出现局部或大部镀不上的质量缺陷,因此镀前必须进行表面脱脂和酸洗。
一、铜丝脱脂
粘附在钢丝表面的油脂来自钢丝拉拔时的润滑剂,它们可以分为两类:一类为皂化脂,它们与碱发生皂化反应生成可溶于水的肥皂,象动、植物油均属于皂化脂;另一类为非皂化脂,它们不能与碱发生皂化反应,象矿物油(机油、石腊、凡士林等)属于此类。电镀前钢丝脱脂的方法一般有;化学脱脂、电化学脱脂、灼烧脱脂。
(一)化学脱脂
1.脱脂原理
化学脱脂是利用碱溶液对油脂的皂化作用除去皂化脂,利用表面活性剂的乳化作用除去非皂化脂。
可皂化性油脂与碱发生皂化反应,生成可溶性的肥皂和甘油,其反应方程式为:
图表5
非皂化性油脂是利用乳化作用将其去掉。钢丝进入脱脂液后,由于钢丝的运动,其表面的油膜破裂,而变成不连续的小油滴。溶液中的乳化剂使油——固界面上的表面张力降低,结果油滴进入溶液;乳化剂的憎水基团和亲水基团把进入溶液中的小油滴包围起来,使油滴不能重新聚集沾污钢丝,这样就将油除去了。
在生产中,由于皂化作用时间较长,除油大部分是乳化作用完成的。
(2)脱脂液的主要成分及其作用
氢氧化钠:碱性最强,皂化作用亦强,是脱脂液的主要成分,钢丝碱洗其浓度一般为50~120g /L,若含量太低,除油效果差;若含量过高又会降低肥皂的溶解度,进而影响除油效果。
·113·
碳酸钠:皂化能力弱,但对油脂层有润湿和分散作用,同时它还是一种PH值的缓冲剂,随着皂化反应的进行,NaOH的含量不断减少,此时Na2CO3水解从而产生NaOH。
水玻璃:呈弱碱性,有较强的乳化能力和一定的皂化能力,但其水洗性不好。
磷酸钠:主要起乳化作用。它很容易从钢丝表面洗净,同时能帮助水玻璃容易被水洗掉。
表面活性剂:降低溶液的表面张力,使非皂化脂乳化。
(3)脱脂的操作条件对脱脂速度和效果的影响
温度:脱脂液一般加热到60"C以上,以保证完全脱除皂化类和非皂化类的油污及润滑层。升高温度可使溶液的表面张力显著下降,使油脂的粘度下降;可增进碱性盐类的水解,从而提高脱脂液的碱度,加快皂化反应的进行;可以使溶液的对流、扩散、乳化、渗透能力加强。
搅拌:搅拌能加速脱脂进程,其原因是搅拌能经常更新钢丝周围的溶液,强化乳化作用;同时由于机械作用。可以从金属表面带走油滴。
化学脱脂的脱脂液成分和脱脂操作条件没有严格的规定,各厂可根据自己的实际情况确定其配方和操作条件。表6—5是碱性脱脂液的组成及工艺规范示例。
表6—5
(二)电解脱脂
(1)电解脱脂原理
化学脱脂的速度慢,时间长,在连续作业线上要占用较长的场地,为了加快脱脂的速度,常采用电解脱脂。
电解脱脂就是将钢丝置于碱液中,以钢丝作为阴极(或阳极),以另一个辅助电极为阳极(或阴极),通以直流电,此时在阴极和阳极分别发生如下电极反应:
阴极:2H++2e→H2↑
阳极:40H-一2e→02↑十2H20
不论是将钢丝作为阴极还是作为阳极,电解时所产生的H2和O2会大大地加快溶液的搅拌和乳化过程,同时还能机械地驱除粘附在钢丝表面的污物,电极反应产生的气体不但能驱除钢丝表面的润滑膜层或其它油脂,还能撕裂钢丝表面的氧化铁皮,部分地起到酸洗的作用。
·114·
钢丝在电解脱脂时,可以在阴极进行,也可以在阳极进行。阴极除油的优点是,除油速度快,这是因为阴、阳两极通过相同电量时,阴极析出的H2的体积是阳极析出的O2的体积的二倍,因而阴极除油乳化能力强;阴极除油的不足之处是阴极大量析出的氢气能向钢丝内部扩散,导致“氢脆”。阳极除油的优点是,电解时阳极释放出的是氧气,因此钢丝没有产生“氢脆”的危险;缺点是除油速度比阴极除油低。
为了发挥阴、阳极电解脱脂各自的长处,可以采用阴一阳交替电解的办法脱脂。国外很早就采用了阴一阳交替电解脱脂和阴一阳交替电解酸洗,70年代贵州钢绳厂引进东德莱比锡公司的电镀锌机组就采用了阴—阳交替电解碱洗和电解酸洗的设备和技术。
(2)影响电解脱脂的速度与效果的主要因素:
电解液中NaOH浓度:氢氧化钠有良好的导电能力,适当地提高氢氧化钠的含量可以提高除油速度。
电流密度:适当提高电流密度,因产生的气泡多,故可加快除油速度。
溶液温度:温度升高,电极反应活化能降低,反应速度加快,从而提高除油速度。
表6—6是电解脱脂液的组成及工艺规范示例。
表6—6
(三)灼烧脱脂
灼烧脱脂是指将钢丝加热到油脂燃点以上的温度,去除油脂的一种方法。如果钢丝在拉拔之后电镀之前需要正火、铅淬火等热处理时,通常都采用这种方式脱脂。由于灼烧脱脂后的钢丝表面留有残渣,尤其是润滑层较厚时,残渣较多,容易堵塞加热炉马弗管,且在后道工序不易清洗干净,因此现在不少厂家在正火、铅淬火前加化学脱脂或电解脱脂工序。
二、钢丝酸洗
经热处理后的钢丝在其表面一般都有一层氧化铁皮,它硬而脆,在电镀之前必须将这层氧化铁皮去除,否则不可能获得牢固的镀层。去除氧化铁皮的方法很多,但在连续作业线上采用的主要是两种方法:化学酸洗法和电化学酸洗法。
·115·
(一)化学酸洗
化学酸洗是让钢丝通过酸液,使钢丝表面的氧化铁皮与酸液发生化学的或电化学的反应,达到去除氧化铁皮的目的。钢丝化学酸洗常用的酸为硫酸和盐酸。在连续作用线上的化学酸洗一般都采用盐酸酸洗,这是因为:第一,盐酸在常温下具有较强的浸蚀能力,而硫酸需在50℃左右方具有这种能力;第二,盐酸对钢丝基体溶解缓慢,不易使钢丝发生过腐蚀和产生“氢脆”。盐酸酸洗的主要缺点是:易挥发,污染空气,腐蚀设备。
(1)盐酸酸洗原理
钢丝浸入盐酸液后,将发生下列反应:
Fe2O3+6HCl==2FeC13+3H2O (α) Fe304+8HCl==2FeCl3+FeCl2+4H20 (β) FeO+2HCl==FeCl2+H20 (γ) 2FeCl3+Fe==3FeCl2 (δ) Fe+2HCl==FeCl2+H2↑(ζ) 由于反应产物FeCl2的溶解度大,故(α) 、(β) 、(γ)三个反应进行较快,相对地(α)进行得较慢,因此氧化铁皮的去除主要是靠盐酸的化学溶解作用,而氢气的机械剥离作用比硫酸要小得多。据有关资料介绍:硫酸酸洗的氧化铁皮的去除,化学溶解作用只占22%,而氢气剥离作用要占78%;而盐酸酸洗的氧化铁皮的去除,化学溶解作用只占77%,氢气剥离作用占23%,这也是用盐酸酸洗比用硫酸酸洗酸耗要高的原因之一。
(2)影响盐酸酸洗速度和效果的主要因素
盐酸浓度:盐酸溶液承受亚铁离子的能力越强,酸洗的时间越短。当温度一定时,盐酸的浓度越高,FeCl2的溶解度越低;但盐酸浓度太低,氧化铁皮的溶解度又太慢。实验表明,当温度为25—35℃和盐酸浓度为15—20%时,可达到较快的酸洗速度。
酸液温度:提高酸液温度,可以提高酸洗速度,但不能为提高酸洗速度而随意提高酸液温度。因为在较低的温度时盐酸的蒸汽压已经相当大,并且随温度升高还要继续迅速增加,产生大量的酸蒸汽而影响环境;同时增加酸耗量,所以盐酸洗一般应该是在室温下进行。
铁盐含量:盐酸酸洗时,酸液中含有适量的FeCl2会强化酸洗,缩短酸洗时间,这是因为盐酸中铁盐易溶于水,而溶液中铁离子浓度增加,会使溶液的电化学反应能力增强,因此,在更换酸洗液时要留一部分老酸。但是,当FeCl2含量超过4—8%(重量)时,随着FeCl2含量增加,酸洗时间会延长。
表6--7是盐酸酸洗液的组成及工艺规范示例
表6--7
·116·
塑料电镀基础知识培训
塑料电镀基础知识培训 一.塑料电镀概述: 1.塑料电镀件的特点: 塑料件电镀后,既保持了制品重量轻,抗蚀性好的特点,又赋予其金属的导电性,耐磨性,装饰件等特点.它不仅可用于装饰品,还可用于某些具有特殊要求的零部件. 塑料电镀件的性能:塑料电镀件与金属零件相比,有许多优越性. a. 重量轻塑料的密度为0.9-2.2g/cm3,最轻的塑料是聚丙烯,密度为0.9-0.91 g/cm3,比水还轻. b. 耐蚀性好塑料件本身抗蚀性能比金属强,电镀后仍比金属强. c. 易成型塑料件易成型,一般形状的零件生产速度比金属快10倍以上.生产装饰性塑料电镀件时,只要模具的表面粗糙度适宜,成型的塑料件可获得光滑的平面,电镀前无需抛光,即可获得高装饰性外观. 二.塑料电镀件的主要性能: 塑料电镀件的主要性能是指塑料与金属的结合力,塑料电镀件的机械强度,耐热性能,抗蚀性能,生产性能等五个方面. ⑴. 结合力结合力的大小,与塑料本身的物料、化学性能有关.不同种类的塑料与金属镀层之间的结合力相差很大.目前用作装饰性塑料电镀件,主要是ABS塑料,其次是改性聚丙乙烯和聚丙烯. ⑵. 抗蚀性能: 塑料电镀件因镀层组合以及镀层厚度的不同,其抗蚀性能有很大差别. 塑料电镀件的抗蚀性之所以比具有同样镀层的金属件高,是因为塑料电镀件的腐蚀不同于金属件的腐蚀.首先,塑料电镀件是按阳极保护机理进行腐蚀的.轻者,因铜镀层的腐蚀镀层出现铜绿或暗褐色斑点.可能引起局部镀层鼓泡或起皮;重者,由于铜镀层完全被腐蚀,导致铜镀层溶解,镀层全部脱落.因此,对于要求抗蚀性能很高的塑料电镀件,应采用双层镍加微孔铬镀层.其次,塑料与金属镀层不可能形成原电池,即使出现腐蚀斑点,也不可能向深度延伸,仅作横向扩展. ⑶. 耐热性: 塑料电镀件的耐热性能,主要取决于塑料本身的耐热能力,以及金属镀层的结合强度.其次,也与金属镀层的耐热性能有关.不同种类的塑料,其耐热性能各不相同.任何一种塑料电镀后,其耐热能力都将有不同程度的提高.如下表: ABS塑料的耐热性能和变形温席 塑料名称热变形温度(℃)镀层厚度 (μm)耐热性能提高率(%) 电镀前电镀后 ABS 85.5 98.6 Cu30 Ni5 Cr0.2 15.2 ⑷. 机械强度: 塑料电镀件的机械强度与塑料的种类密切相关.一般情况下,塑料件电镀后,其刚性均有所提高. ⑸. 生产性能: 金属件的制作,一般要经过冲压、车、钳、刨、磨等繁杂的机械加工工序。而塑料件只需成型,其生产效率比金属件快10倍以上,可节省大量的机械加工工时及机械加工设备。另外,塑料密度小,比金属件成型省力、方便。 一.金属与塑料结合的机理及影响因素: 1. 金属与塑料结合的机理 ⑴. 机械结合论:目前,人们对于塑料与金属镀层间结合的机理主要有两种观点:一是机械结合,另一种是机械结合兼化学结合,而以机械结合为主. 机械结合论认为,ABS(丙烯腈-丁二烯-苯乙烯)塑料经过化学粗化后,其B组分(丁二烯)被溶解掉,形成许多燕尾形的显微凹坑(即锁扣),化学镀时,沉积出的金属微粒将填满这些凹坑,产
最新塑料电镀基础知识
塑料电镀基础知识
塑料电镀的特点 塑料电镀制品具有塑料和金属两者的特性。它的比重小,耐腐蚀性能良好,成型简便,具有金属光泽和金属的质感,还有导电、导磁和焊接等特性。它可以节省繁杂的机械加工工序、节省金属材料,而且美观,装饰性强,同时,它还提高了塑料伯的机械强度。由于金属镀层对光、大气等外界因素具有较高的稳定性,因而塑料电镀金属后,可防止塑料老 化,延长塑料件的使用寿命。 随着工业的迅速发展、塑料电镀的应用日益广泛,成为塑料产品中表面装饰的重要手段之一。目前国内外已广泛在ABS、聚丙烯、聚砜、聚碳酸酯、尼龙、酚醛玻璃纤维增强塑料、聚苯乙烯等塑料表面上进行电镀,其中尤以ABS塑料电镀应用最广,电镀效果最好。 塑料的工艺过程 塑料制件电镀的主要工艺流程。 塑料制件---机械粗化---化学除油---化学粗化 敏化处理---活化处理---还原处理---化学镍---电镀---成品 塑料电镀的主要工艺流程 1、化学除油 防止塑料变形、溶解,应考虑除油液对塑料的适应性。当用碱性除油液时,应注意使用温度,以防变形;用有机溶剂除油时,应注意其是否有溶解塑料的现象。 2、粗化
为提高结合强度,就得尽可能地增加镀层和基体间的接触面积。粗化的方法有机械粗化法和化学粗化方法两种。机械粗化如喷砂、滚磨、用砂纸打磨等。化学粗化可以迅速地使工件表面微观粗糙,粗化层均匀、细致、不影响工件的外观。 3、敏化处理 工业上常用的敏化剂为氯化亚锡或三氯化钛的水溶液。 4、活化处理所谓活化处理,就是将吸附有还原剂的制件浸入含有氧化剂的溶剂中。一般是浸入贵金属盐类水溶液,于是贵金属离子就被还原剂还原为贵金属,从而在制件表面上形成贵金属膜。这层贵金属可以起到活性催化的作用,帮也称催化膜,它可以加速化学镀的还原反应。实践证明,银、钯等贵金属都具有这种催化能力。 5、还原反应经过活化处理的塑料制件,用水清洗后,就可以进行化学镀。塑料制件进行化学镀以前,先在一定浓度的化学镀所用的还原剂溶液中浸一下,把未被水洗掉的活化剂还原,这就是还原处理。化学镀铜时,可先用次磷酸钠溶液进行还原处理。 6、化学镀到目前为止,已有很多重金属可以通过化学镀铜的方法从水溶液中沉积出来。从经济角度来看,化学镀铜成本最低,因此被广泛采用。化学镀铜层外观呈铜红色,不能作为装饰和防护层,通常用作非金属、印刷电路板孔金属化等电镀加厚镀层的导电层。化学镀铜只能给塑料制件镀上一层导电源,镀层很薄。要想继续加厚其他镀层时,要先用电镀铜将化学镀铜层加厚。电镀铜时,可以使用酸性镀铜,也可以使用碱性镀铜。塑料制件经过电镀铜以后,就可以根据需要继续电镀其他金属镀层。 金属喷镀的原理
工艺技术员电镀基本知识培训测试题附答案
工艺技术员电镀基本知识培训测试题附答案 部门:姓名:工号:分数: 一.填空题(每空2分,供16分) 1.物质在电解质溶液中的传递方式(运动方式)有三种:对流、扩散和电迁移。 2.由电子来传导电流的导体称为第一类导体,如铜、铁等金属导体。 3.主盐浓度高,一般可采用较高的阴极电流密度。溶液的导电性和阴极电流效率都较高。 4.在电镀中,常用分散能力和覆盖能力来分别评定金属镀层的在阴极上分布的均匀性和完整性。 5.在给定的电流密度下,某可逆电极的电极电位与其平衡电位之间的差值,叫做该电极在给定电流密度下的过电位。 二.判断题(每空2分,共24分)正确的打“√”,错误的打“×” 1.单金属电镀的电流效率可以大于100%。(×) 2.电镀液的覆盖能力亦称深镀能力,它是指电镀液所具有的使镀件 的深凹处沉积上金属镀层的能力。(√) 3.提高金属电结晶时的阴极极化作用,可以提高晶核的生成速度, 2便于获得结晶细致的镀层。(√) 4.阴极极化作用愈大愈好。(×)
5.依靠离子的定向移动来传导电流的导体称为第二类导体或离子导 体。(√) 6.表面活性剂是一种在低浓度下能降低水和其它溶液体系的表面张 力或界面张力的物质。(√) 7.在溶解或熔化状态下能导电的物质叫做电解质。酸、碱、盐不是 电解质。(×) 8.我们经常使用的电极电位是电位差的绝对值。(×) 9.电位越正的金属,如金、银、铜等,越容易在阴极上还原析出;而电位越负的金属,如铝、镁、钛等,则越不容易镀出来。(√) 10.标准氢电极的电极电位在任何温度下都规定为零。(√) 11.缓冲剂可以在任何pH值范围内有较好的缓冲作用。(×) 12.阴极上析出的氢,会使镀层出现针孔(或麻点)、鼓泡、氢脆 等缺陷。(√) 三.名词解释。(每题5分,共20分) 1.电镀液的分散能力。(5分) 答:电镀液的分散能力是指在特定条件下,一定溶液使电极上(通常是阴极)镀层分布比初次电流分布所获得的结果更为均匀的能力。
电镀基础知识
电镀基本知识介绍 1.电镀基本原理 电镀是一种电化学过程﹐也是一种氧化还原过程。电镀的基本过程是将零件浸在金属盐的溶液中作为阴极﹐金属板作为阳极﹐接直流电源后﹐在零件上沉积出所需的镀层。 例如﹕镀镍时﹐阴极为待镀零件﹐阳极为纯镍板﹐在阴阳极分别发生如下反应﹕阴极(镀件)﹕Ni2++2e→Ni (主反应) 2H++e→H 2 ↑ (副反应) 阳极(镍板)﹕Ni ﹣2e→Ni2+ (主反应) 4OH-﹣4e→2H 2O+O 2 +4e (副反应) 不是所有的金属离子都能从水溶液中沉积出来﹐如果阴极上氢离子还原为氢的副反应占主要地位﹐则金属离子难以在阴极上析出。根据实验﹐金属离子自水溶液中电沉积的可能性﹐可从元素周期表中得到一定的规律﹐如表1.1所示 阳极分为可溶性阳极和不溶性阳极﹐大多数阳极为与镀层相对应的可溶性阳极﹐ 如﹕镀锌为锌阳极﹐镀银为银阳极﹐镀锡-铅合金使用锡-铅合金阳极。但是少数电镀由于阳极溶解困难﹐使用不溶性阳极﹐如酸性镀金使用的是多为铂或钛阳极。镀液主盐离子靠添加配制好的标准含金溶液来补充。镀铬阳极使用纯铅﹐铅-锡合金﹐铅-锑合金等不溶性阳极。 2.★电镀基本工艺及各工序的作用 2.1 基本工序 (磨光→抛光)→上挂→脱脂除油→水洗→(电解抛光或化学抛光)→酸洗活化→(预镀)→电镀→水洗→(后处理)→水洗→干燥→下挂→检验包装 2.2 各工序的作用 2.2.1 前处理﹕施镀前的所有工序称为前处理﹐其目的是修整工件表面﹐除掉工件表 面的油脂﹐锈皮﹐氧化膜等﹐为后续镀层的沉积提供所需的电镀表面。 前处理主要影响到外观,结合力﹐据统计﹐60%的电镀不良品是由前处 理不良造成﹐所以前处理在电镀工艺中占有相当重要的地位。在电镀技 朮发达的国家﹐非常重视前处理工序﹐前处理工序占整个电镀工艺的 一半或以上﹐因而能得到表面状况很好的镀层和极大地降低不良率。 喷砂﹕除去零件表面的锈蚀﹐焊渣﹐积碳﹐旧油漆层﹐和其它干燥的油污﹔除去铸件﹐锻件或热处理后零件表面的型砂和氧化皮﹔除去零件表面 的毛刺和和方向性磨痕﹔降低零件表明的粗糙度﹐以提高油漆和其它 涂层的附着力﹔使零件呈漫反射的消光状态 磨光﹕除掉零件表明的毛刺﹐锈蚀﹐划痕﹐焊缝﹐焊瘤﹐砂眼﹐氧化皮等各种宏观缺陷﹐以提高零件的平整度和电镀质量。 抛光﹕抛光的目的是进一步降低零件表面的粗糙度﹐获得光亮的外观。有机械抛光﹐化学抛光﹐电化学抛光等方式。
电镀铜工艺
电镀铜工艺 A 电镀铜工艺部分 1问题:各镀铜层附着力不良原因: (1)除油前清洁处理不当,铜表面的氧化或钝化膜除干净 (2)除油槽液中的润湿剂被带出或水洗不足造成底铜钝化 (3)板子进入镀槽后电源并未立即打开 (4)电流密度过大 (5)过硫酸根残余物污染 (6)干膜显影后水洗不足 解决方法: (1)A)提高除油槽液温度以利去除基板表面油污和指纹 B必须经微蚀处理除去铜表面的氧化膜和污染物 C检查除油槽和微蚀槽液的活性 (2)A检查水洗程序即水量和水压 B增加水洗流量并在出槽时采用喷淋水洗,确保孔内清洗效果 C提高水洗水温度,喷淋水洗后也可采用多段式溢流水洗 (3)重新检查整流器自动程序 (4)重新检查电镀程序和被镀基板实测面积,适当降低电流密度 (5)如使用过硫酸盐微蚀后,还必须尽5-10%硫酸浸洗,以除去基板表面铜盐类。(6)A.提高喷淋压力 B.检查喷嘴是否被堵塞,并采用适当地喷嘴布置 C、增加水洗温度 2、问题:经第二次电镀铜的导线出现局部漏镀与阶梯式镀层原因: (1)干膜经性影后图像不洁 (2)板面已有指纹及油渍的污染 (3)镀液中有机物含量过多
(4)修版的油墨对待镀板子的线路部分造成意外污染 (5)镀液中的添加剂成分有问题 (6)除油槽中润湿剂被带走,并自小孔内逐渐流出而影响镀铜外观 (7)干膜表面渗出显影液的残渣 (8)显影液受到污染 解决方法: (1)A.重新检查显影程序,确保显影后图像清晰 B.检查底片电路图形布线密度,凡导线有长、线路又密时应特别小心显影操作程序 C.检查显影机显影段喷嘴是否被堵塞 (2)A.提高除油槽液的温度 B.持取班子要特别注意,绝不能用手触摸板面,只能用手掌顶两侧板边 (3)A.使用霍氏槽分析光亮剂 B.按照工艺规定进行活性碳过滤处理 C.严格控制添加剂的含量 (4)检查经修补后的线路部分状态,确保板面无异物 (5)通过工艺试验法和分析法确定添加剂质量优劣并进行调整 (6)增加水洗浸泡时间并在板子出槽时另采用强力喷淋水清洗 (7)A.曝光后须放置30分钟以使反应到达平衡 B.使用低温烘烤以加速溶剂的挥发 C.显影后加强水洗 (8)提高显影的再生速率;保持显影的洁净度 3、问题:板子正反两面镀层厚度不均匀原因: (1)板子两面的电镀面积不一致,尤其是一面是接地层面而另一面是线路面时(2)可能是某一边阳极的线路导电不良所致 解决方法: (1)A.以正反排版方式将板子两面待镀面积加以调整
电镀基本知识-电镀基本原理和方法
目录1.电镀的定义和分类 1-1.电镀的定义 1-2.电镀的分类 1-3.电镀的常见工艺过程 2.常见电镀效果的介绍 2-1.高光电镀 2-2.亚光电镀 2-3.珍珠铬 2-4.蚀纹电镀 2-5.混合电镀 3.电镀件设计的常见要求 3-1.电镀件镀层厚度对配合尺寸的影响 3-2.电镀件变形的控制 3-3.局部电镀要求的实现 3-4.混合电镀效果对设计的要求 3-5.电镀效果对设计的影响 3-6.电镀成本的大致数据
1.电镀的定义和分类 1-1.电镀的定义 随着工业化生产的不断细分,新工艺新材料的不断涌现,在实际产品中得到应用的设计效果也日新月异,电镀是我们在设计中经常要涉及到的一种工艺,而电镀效果是我们使用时间较长,工艺也较为成熟的一种效果,对于这种工艺的应用在我们的产品上已经非常多,我们希望通过总结我们已有的经验作一些设计的参考性文件,可以更好的将电镀效果应用在我们的设计上,也更合理的应用在我们的设计上,可以为以后的工作带来一些方便。通过这种工艺的处理我们通常可以得到一些金属色泽的效果,如高光,亚光等,搭配不同的效果构成产品的效果的差异性,通过这样的处理为产品的设计增加一个亮点。 1-1-1.电镀的定义 电镀就是利用电解的方式使金属或合金沉积在工件表面,以形成均匀、致密、结合力良好的金属层的过程,就叫电镀。简单的理解,是物理和化学的变化或结合。 电镀工艺的应用我们一般作以下几个用途: a.防腐蚀 b.防护装饰 c.抗磨损 d.电性能:根据零件工作要求,提供导电或绝缘性能的镀层 e.工艺要求 1-1-2.常见镀膜方式的介绍 这里从类同与电镀的一些工艺作分析介绍,以下的一些工艺都是在与我们电镀相关的一些工艺过程,通过这样的介绍给大家对这些工艺有一个感性的认识。 化学镀(自催化镀) autocalytic plating 在经活化处理的基体表面上,镀液中金属离子被催化还原形成金属镀层的过程。这是在我们的工艺过程中大多都要涉及到的一个工艺工程,通过这样的过程才能进行后期电镀等处理,多作为塑件的前处理过程。 电镀 electroplating 利用电解在制件表面形成均匀、致密、结合良好的金属或合金沉积层的过程,这种工艺过程比较烦杂,但是其具有很多优点,例如沉积的金属类型较多,可以得到的颜色多样,相比类同工艺较而言价格比较低廉。 电铸 electroforming 通过电解使金属沉积在铸模上制造或复制金属制品(能将铸模和金属沉积物分开)的过程。这种处理方式是我们在要求最后的制件有特殊表面效果如清晰明显的抛光与蚀纹分隔线或特殊的锐角等情况下使用,一般采用铜材质作一个部件的形状后,通过电镀的工艺手段将合金沉积在其表面上,通常沉积厚度达到几十毫米,之后将形腔切开,分别镶拼到模具的形腔中,注射塑件,通过这样处理的制件在棱角和几个面的界限上会有特殊的效果,满足设计的需要,通常我们看到好多电镀后高光和蚀纹电镀效果界限分明的塑胶件质量要求较高的通常都采用这样的手段作设计。如下图所见的棱角分明的按键板在制造上采用电铸工艺的话,会达到良好的外观效果。 图 1-1 按键电镀效果1
化学镀铜与直接电镀工艺
一次化学镀厚铜孔金属化工艺 不用电镀铜的一次化学镀厚铜进行双面板和多层板孔金属化,可以显著缩短加工周期,降低生产成本,用此种工艺方法很容易作出高精度的印制板。通过实践证明一次化学镀厚铜的金属化孔可靠性要超过电镀铜,因为一次化学镀厚铜孔内镀层厚度非常均匀,不存在应力集中,特别是对于高密度的印制板小孔金属化(φ0.5以下的孔),对电镀来讲很难达到孔内镀层厚度均匀一致,而用化学镀铜的方法则是轻而易举的事,下面介绍双面和多层板一次化学镀厚铜的生产工艺。 5.1 双面印制板一次化学镀厚铜 1)用液体感光胶(抗电镀印料)制作双面电路图形。然后蚀刻图形。液体感光胶可以用网印或幕帘式涂布,幕帘法生产效率高,而且涂层均匀无砂眼,网印法易产生气孔砂眼。液体抗电镀感光胶分辨率非常高,显影无底层。很容易得到精细的电路图形。价格比干膜便宜。蚀刻电路图形之后用5%NaOH去除感光胶层。 2)网印或幕帘式涂布液体感光阻焊剂,制出阻焊图形 3)再用液体感光胶涂布板面,用阻焊底片再次曝光,显影,使孔位焊盘铜裸露出来。 4)钻孔 5)化学镀厚铜。 1.酸性除油3分钟 2.H2SO4/H2O2粗化3分钟 3.预浸处理1分钟 4.胶体钯处理3分钟②③④⑤⑥⑦ ①- ④处理液均为酸性溶液,板面上的液体感光胶层不会破坏,其结果是保护板面不受浸蚀,在进行活化时,孔内和板面上的感光胶层吸附了胶体钯。 ⑤5%NaOH处理3分钟,然后水冲洗板面上的感光层,连同感光胶上的胶体钯一同被碱溶解下来。孔内的胶体钯仍然保留。 ⑥1%NaOH处理1分钟,然后水冲洗,进一步去除板面上的残胶。 ⑦化学镀厚铜4小时,铜层厚度可达到20微米,化学镀铜过程中自动分析自动补加化学成份。适用于连续化学镀厚铜的配方: CuSO4.5H2O 10g/1 EDTA.2Na 40 g/1 NaOH 15 g/1 双联呲啶10mg/1 CN-10mg/1 操作条件:温度600C,化学镀铜过程中,通空气搅拌化学镀铜溶液,并连续过滤。自动控制PH和Cu+1离子含量。
(工艺技术)电镀工艺基础知识
2、电镀新工艺介绍 2 .1合金电镀 合金电镀一直是电镀新工艺开发的重要领域。以往为取代昴贵的镀镍而开发的铜锡合金,就曾经是一种新工艺。现在的代镍和节镍镀层,也都是各种合金。因为合金可以综合单一金属的优点,并具有单一金属所不具备的新的特性,比如硬度、耐腐蚀性、功能性等。现在已经认识到,电镀作为一种湿法冶金技术,能生产出用电、热方法做不到的新合金。包括在制作非晶态材料和纳米材料方面,电镀技术都是有优势的。合金电镀的原理在传统的理论中是要求两种共沉积的金属的电极电位要接近,如果一个的电位较正,另一个的电位较负,就要采用络合剂将正电位的金属的离子络合,使之放电电位向负的方向移动,与另一金属的电位相近,达到共沉积的目的。这在现在也仍然对合金新工艺的开发有指导意义。但是现在越来越多的合金中的另一种成分的量非常小,就是这种少量的金属分散在另一金属中,却改变了金属的性能。用传统冶金学的观点是这些掺入的金属是占据在主体金属的某些晶格位上,从而改变了金属的物理性能。但实际上,用火法冶金很难把微量金属分散到另一金属中去,而采用电镀的方法则比较容易做到。不过电镀方法得到的合金的结构是否符合冶金学的原理,则是值得探讨的课题。现在已经得到应用的新合金工艺有锌系列,镍系列,铜系列,锡系列,银系列等。锌作为钢铁的优良廉价的防护性镀层被广泛地采用 , 但是自从日本汽车打进欧洲和北美市场,汽车的耐盐防护性就提到了议事日程。〈1〉在开展高耐蚀性镀层的研究中,锌合金的研究引人注目。最先出现的是锡锌合金,这种合金的含锌量在30%左右时耐盐水喷雾时间最长,出现红锈的时间可达1500个小时以上。最开始进入实用化的工艺是70年代末的有机羧酸的中性镀液,后来有柠檬酸镀液,现在我公司已经开发出硫酸盐光亮镀锡锌工艺。在锡锌工艺之后出现的是锌镍工艺。这种工艺由于含镍量在5-10%,成本比锡锌要低,因此很快得到普及。最先出现的是用于钢板连续电镀的硫酸盐工艺,这大约在1982年前后。以后开发出氯化铵型工艺,现在比较成熟的是碱性锌酸盐工艺。这种工艺的特点是抗腐蚀性能特别好,不经钝化的镀层耐盐雾到出现红锈的时间在150小时以上。在高温下也仍能维持其优良的防护性能。因此在汽车等行业有较多应用。 在锌镍开发之后两年,锌铁工艺就进入了实用化。锌铁与前面的工艺不同的是铁的含量很小,只在 0.2 到0.6 左右。虽然以前有用于钢板电镀的锌铁合金,其含铁量在10-20%,但现在进入实用的还是这种低铁含量的镀层。比较成熟的有锌酸盐工艺。其耐蚀性也很好,但一定要经过钝化才能有高的耐蚀性,当含铁量在 0. 4 左右时,出现红锈的盐水喷雾时间可达1500小时以上。现在,我公司已经开发出氯化钠型锌铁新工艺,并有黄色、彩色等高耐蚀性的钝化产品。 在欧洲还有用锌钴合金工艺的,这种工艺与锌铁一样,可以不用银盐做出黑色钝化膜。含钴量也仅在1%左右. 镍一直是电镀加工工业中的重要镀种,由于镍资源的紧张和价格昂贵,开发镍合金电镀是节镍的一种选择。同时,有些镍合金的功能性能也是市场所需要的,因此,镍基合金的应用也很广泛。镍铁合金不仅可节约部分镍,而且镀层性能也比纯镍镀层要好。这种镀层的含铁量在 7%-30% 左右,镀层中的含铁量与镀液中的镍铁比例成正比。也有采用镍锰铁合金电镀工艺的报导。 <2 >用于装饰的镍合金更多,特别是黑色镀层方面,不少是用的镍合金,比如镍锡,镍钴,镍镉等。铜镍合金更是在装饰电镀中有较多的应用。 <3 >铜合金如铜锡合金,铜锌合金,很早就有大量的应用。这方面的新工艺的主攻方向是以非氰化物络合物来取代氰化物,比如焦磷酸盐,柠檬酸盐镀铜合金等。锡作为钎焊性镀层主要是用在电子电镀行业,但也可以用在装饰和防护方面,比如代银的锡合金,用于罐头盒防腐的镀锡工艺等。但主要还是电子工业中有大量应用,现在用得最多的仍然是锡铅合金。也有锡铈,锡铋等。当前的趋势是采用无氟和无铅的新工艺取代老工艺。<4 >其它贵金属的合金主要是用在装饰和功能性方面,这里就不一一加以介绍。正如前面讲到的,由于合金电镀技术的开发可能产生出一些新的合金,这不仅在表面处理业有重要意义,对材料学科也有重要意义。因此,在新世纪,对合金电镀的研究仍会加紧进行。 特别是在多元合金,包括三元、四元合金等的开发上还有很大的空间 2.2电子电镀 如前所述,21世纪被称为高信息化世纪。所谓高信息化世纪就是以因特网为传播工具的信息爆炸的世纪。在这个世纪内,电子产品的品种和产量将有更快更大的发展,这给电子电镀业也带来很大的机遇和挑战。因此,现在新工艺的开发有很大的比重将放在电子电镀方面。 所谓电子电镀就是用于电子产品或电子工业的电镀技术。用于电子行业的镀层有很多,包括导电性镀层,钎焊性镀层,信息载体镀层,电磁屏蔽镀层,电子功能性镀层,印刷电路板电镀,电子构件防护性镀层,电子产品装饰性镀层等。电子电镀工艺除了少数是利用了传统的工艺以外,大多数是近几十年开发的新工艺。比如非金属电镀新工艺,化学镀新工艺,贵金属电镀新工艺,合金电镀新工艺等。 以印刷线路板的电镀为例,它是以孔金属化为中心的综合了前处理、化学镀、电镀、退镀等技术的工艺。印
电镀基础知识讲座
电镀基础知识讲座( 五) 电镀的分类有很多, 主要是根据镀层种类或者根据获得的镀层性能和作用来分。表1-1是根据获得的镀层为单金属或者合金镀层来分类的,也就是常说的单金属电镀和合金电镀。 表1-1 常用单金属和合金电镀的种类 单金属电镀二元合金电镀三元合金电镀四元合金电镀 Zn,Cd,Cu, Ni,Cr,Sn, Au,Ag,Pb, Fe,Pd,Pt, Co,Mn,Rh, In,Re,Ru, Sb,Bi等 Cu-Zn,Cu-Sn,Cu-Cd,Sn-Ni, Sn-Zn,Sn-Co,Sn-Cd,Sn-Bi, Au-Cu,Au-Ag,Au-Co,Au-Ni, Au-Sb,Ag-Sb,Ag-Cd,Ag-Zn, Ag-Pb,Ag-Cu,Ag-Sn,Ag-Pd, Ag-Pt,Zn-Ni,Zn-Fe,Zn-Sn, Zn-Co,Cd-Ti,Pb-Sn,Ni-Co,Ni-W, Ni-Fe,Ni-P,Ni-Mo,Ni-Cu,Cr-Ni, Cr-Mo,Cr-Fe,Pd-Ni,Pd-Pt, Co-Fe,In-Pb,Re-Fe,Re-Co等 Cu-Zn-Sn, Cu-Sn-Ni,Ni-W-B, Ni-W-P, Ni-Co-Fe, Ni-Co-Cu, Cr-Fe-Ni, Sn-Ce-Sb, Sn-Ni-Cu, Sn-Co-Zn, Au-Pd-Cu, Ag-Pt-Pd,Zn-Ni-Fe 等 Cu-Sn-In-Ni, Co-Ni-Re-P, Au-Pd-Cu-Ni 等 另外还可以根据获得的镀层功能性来分:防护性镀层、装饰性镀层、耐磨、减摩性镀层,以及抗高温氧化、耐热、电性能、磁性能、光学性能、半导体性能、超导性能、杀菌性能等镀层。也就是除了在传统的装饰、防护方面的应用外,目前的电镀技术主要是制备一些新型的功能性镀层,如目前大量应用于IT产业的印制板电镀层、磁记录介质膜层等。 还有就是根据金属电镀层的实际状态(如叠层、功能作用等)来划分一些镀层的类型(见图1-1)。 单金属镀层合金镀层复合镀层 缎面镍镀层沙面镍镀层
第六章 电镀黄铜工艺
第六章电镀黄铜工艺 第一节概述 在第二章中已经介绍了黄铜镀层对钢帘线与橡胶粘合的至关重要的作用,本章将阐述获得黄铜镀层的方法,即电镀黄铜工艺。 铜含量高于锌的铜锌合金通常称为黄铜,1841年就已发明了镀黄铜。最早的镀黄铜槽液是把硫酸铜和硫酸锌转换成碳酸盐,然后再在氰化钾溶液中溶解,使用低电流密度进行电镀。这种方法一直沿用到1915年,随着科技的进步发展成为现代的氰化电镀工艺。1974年第三版《现代电镀》中提到,专家们“研究了在1960年之前研究过的所有不同类型镀黄铜槽液之后下结论说,迄今为止,还没有一种槽液能满意地代替氰化黄铜槽液”。因为氰化物剧毒,人们总想摆脱它,一直在研究非氰电镀黄铜工艺。60年代,一些欧洲国家(如前苏联、意大利等)对“两步法”(先镀铜,后镀锌,再热扩散而形成铜锌合金的方法,又称热扩散法)非氰电镀黄铜工艺进行了工业性试验,并于70年代投入了规模生产。值得一提的是,我国从60年代末开始,曾探索过“一步法”(直接镀铜锌合金的方法)非氰电镀黄铜工艺,选用焦磷酸盐一草酸镀液体系,从实验室试验到中间试验反复进行了几年时间,先后生产了Φ0.8mm镀黄铜钢丝10余吨,捻制成7×3×0.147和3+9+9×3×O.147两种结构钢帘线用于子午线轮胎,进行了里程试验,并与氰化电镀产品对照,所得数据表明其质量与氰化法不相上下。后来投入大生产时,仅连续运行几天时间便发现阳极钝化严重,经试验分析初步认定是镀液中派生物磷酸氢二钠过多所致,最后高达lOOg/l以上,而且很难除去。工程技术人员做了大量工作,企图复苏焦磷酸盐一草酸电镀液,限于当时的条件,工作未能继续下去,最后不得不终止它的应用。这种独创性的电镀黄铜工艺虽未取得最后成功,但对后人有借鉴作用。 目前,钢丝电镀黄铜工艺处于氰化法和热扩散法并存在的局面。据国外考察,意大利几乎所有的钢帘线生产厂都采用热扩散法电镀工艺;而法国米其林公司年产18.5万吨钢帘线,则全部采用氰化法电镀工艺,只有在泰国所建的一个分厂采用热扩散法。世界上许多国家包括我国,在采用热扩散法的同时,仍保留了氰化法电镀工艺。我国自80年代以来,引进两步法热扩散电镀黄铜作业线至少有6条(包括单丝电镀作业线,即单根钢丝在镀槽中来回走镀多圈以达到所需的镀层厚度,线速可达200--300m/min),几乎无一例外地费了很长的时间进行调试方达基本正常。关于氰化法和热扩散法两者的利弊,将在对两种工艺作系统阐述后再进行比较。 钢丝电镀不同于零件电镀,钢丝是在镀槽中不断前进的,俗称“走镀”。图6--1所示,钢
从事电镀行业要知道的电镀基础知识100问
从事电镀行业要知道的电镀基础知识 100问 文章出自:深圳电镀厂 1.电解液为什么能够导电? 答:电解液导电与金属导体的导电方式是不一样的。在金属导体中,电流是靠自由电子的运动输送的,在电解液中则是由带电的离子来输送电流。在电解液中 由于正负离子的电荷相等,所以不显电性,我们叫做电中性。当我们对电解液 施加电压时,由于强大的电场的吸引力,离子分别跑向与自己极性相反的电极。阳离子跑向阴极,阴离子跑向阳极。它们的运动使电流得以通过,这就是电解 液导电的道理。 2.在电镀过程中,挂具发热烫手,是由于镀液温度太高造成的吗? 答:挂具的发热虽然与溶液的温度有关系,但主要的原因是: (1)通过挂具的电流太大。 (2)挂具上的接触不良,电阻增高而使挂具发热。 3.控制电镀层厚度的主要因素是什么? 答:控制电镀层厚度的主要因素为电流密度、电流效率与电镀时间。 4.黄铜镀层与青铜镀层是同一样的台金镀层吗? 答:不是,黄铜镀层是铜和锌的合金镀层,青铜镀层是铜和锡的合金镀层。 5.法拉第定律是表示什么关系的,试述法拉第的第一定律和第二定律? 答:法拉第定律是描述电极上通过的电量与电极反应物重量之间的关系的,又称为电解定律。 法拉第第一定律:金属在电解时所析出的重量与电解液中所通过的电流和时间成正比。 W=KIt W——析出物质的重量(g) K——比例常数(电化当量) I——电流强度(安培) t——通电时间(小时) 法拉第第二定律:同量电流通过不同电解液时,则所析出金属之重量与各电解液
之化学当量成正比。 K=CE C——比例常数。E——化学当量 6.为什么镀件从化学除油到弱酸蚀,中间要经清水洗净? 答:因为通常的化学除油溶液都是碱性的,如果把除油溶液直接带进酸腐蚀溶液中,就会起酸、碱的中和反应,降低了酸的浓度和作用。中和反应的生成物粘 附在工件上,会影响镀层的质量。故工件在化学除油后,一定要经清水冲洗干净,才能进入酸腐蚀的溶液。 7.电镀层出现毛刺、粗粒,通常是那些原因造成的,如何解决? 答:镀层出现毛刺、粗粒,主要是镀液受悬浮杂质污染所造成的。其来源是:空 气中的灰尘、阳极的泥渣、金属杂质的水解产物。此外,还有镀液成分不正常 和操作条件不合要求等等。解决的办法是:调正镀液成分和操作条件。如果是悬浮杂质所造成,则应将镀液过滤。 8.配制电镀液的基本程序如何: 答:配制电镀液的基本程序如下: (1)将汁量好的所需电镀药品先放入开料槽(小槽)内,再加入适量的清水溶解,注意勿将药品直接倒入镀槽内。 (2)溶液所含的杂质,可以先用各种化学方法清除,并以活性炭处理。 (3)已处理静置好的溶液,滤入清洁的镀槽中,加水至标准量。 (4)调节好镀液工艺规范(pH值、温度、添加剂等)。 (5)最后用低电流密度进行电解沉积,以除去其它金属离子杂质,直至溶液适合操作为止。 9.为什么桂具要涂上绝缘材料? 答:挂具制造一般除挂勾和产品接触导电部分外,其余均应涂上绝缘材料,以减少电流损耗和金属损失,确保产品有效面积电镀,提高有效电流,并使挂具耐用。 10.硫酸、盐酸除锈效果怎样?硝酸能否除锈? 答:产品除锈一般以采用浓盐酸效果最好,能达到效率高,即使时间过长了些也不致产生过腐蚀,损坏基体金属的现象。硫酸除去表面锈渍较好,但除锈很慢,而时间过长了又产生过腐蚀现象,对产品基体损坏较大。硝酸不能用于除锈, 因其氧化性很强,遇金属即进行氧化,产生大量的氧化氮剧毒气体。 11.镀前处理对电镀层的质量有何影响?
电镀银工艺规范
电镀银工艺规范编号:0TK.929.041
山东泰开电器有限公司二 五年五月一日
一、及铜合金工件表面镀银 1.金属清洗剂除油:将工件在50~90℃的金属清洗剂溶液中浸泡30分钟以上,油污严重或溶液温度低可适当延长时间,必要时可用抹布蘸取金属清洗剂液擦拭; 2.水洗:在热水槽中洗净工件上残存的清洗液; 3.化学除油:采用碱性化学除油,将工件在70~90°的除油液中浸泡30分钟以上,油污严重者可适当延长,除尽油为原则;(注:工件有厚氧化皮且油污极少时,可先在20%左右的稀硫酸中浸泡30~60分钟以松动氧化皮然后除油水洗) 4.水洗:在水洗槽中洗净工件上残存的除油液,水洗槽中的水要根据洗件的数量经常更换以保持清洁; 5.酸洗:在酸洗槽中浸泡酸洗3~10秒,使用新酸时或洗薄壁铜件时时间要短(酸洗时间1~3秒),以免工件过腐蚀; 6.水洗:工件由酸洗槽出来后应立即在水洗槽中洗净工件上残存的酸液,水洗槽中的水要根据洗件的数量经常更换以保持清洁; 7.二次酸洗:在酸洗槽中浸泡酸洗1~3秒,使用新酸时或洗薄壁铜件时时间要短,以免工件过腐蚀;(注:在当酸洗一次经水洗后工件表面已光洁无污点时,可省略第二次酸洗) 8.水洗:工件由酸洗槽出来后应立即在水洗槽中洗净工件上残存的酸液,水洗槽中的水要根据洗件的数量经常更换以保持清洁; 9.钝化:根据钝化效果在钝化槽中钝化5~25秒,一般新配钝化液钝化时间短,反之略长。钝化前一定要清洗干净,不可把上道工序残存液带入钝化液中。 10.水洗:在水洗槽中洗净工件上残存的钝化液。 11.烫干:在50~70℃的热水槽中浸烫10秒,取出晾干; 12.局部保护:需局部电镀而保护的工件干燥后施与保护,缠胶带或涂可剥漆,若涂可剥漆等干后再进行下道工序;(注:若工件表面全部镀则不进行烫干和局部保护直接进入下道工序—漂洗) 13.漂洗:在漂洗槽中浸泡漂洗3~15秒,除去钝化膜; 14.水洗:在水洗槽中彻底洗净工件上残存的漂洗液酸液,水洗槽中的水要经常更换以保持清洁; 15.浸银:在浸银槽中浸泡浸银1~2分钟,必要时可稍摇动以使工件表面浸银颜色均匀呈银白色,若出现蓝灰色应酸洗掉重新进行处理; 16.水洗:在水洗槽中彻底洗净工件上残存的浸银液,水洗槽中的水要经常更换以保持清洁,严防杂质带入镀槽; 17.予镀:清洗后的工件尽快的挂入予镀槽进行予镀,一定要带电入槽(即挂入的同时要导电);电流密度:10~35℃时,0.1~0.5A/dm2,温度低时电流密度稍低,予镀时间:5~30秒;
填孔镀铜配方组成,工艺流程及技术研究进展
填孔镀铜配方组成,工艺流程及技术研究进展 摘要:文章简述了填孔电镀的概况、工艺以及填孔工艺中的镀铜添加剂 关键词:电镀;填孔;镀铜添加剂; 1前言 从20世纪60年代开始,PCB行业就采用孔金属化和电镀技术来解决层间连接或导通的问题。实际上过去、现在和将来,在PCB进行电镀铜的最核心问题是解决孔内镀铜连通、镀铜厚度均匀性和填孔镀铜方面等问题。随着PCB行业产品的高密度化和结构多样化的发展,PCB电镀技术有了飞快的进步,但是电镀铜的核心问题仍然没有得到有效的解决。到目前为止,PCB行业电镀经历了常规直流电镀—直接电镀—脉冲电镀—新型直流电镀等过程,核心仍然是围绕着PCB层间“孔”导通的问题。 在孔金属化过程中,采用填铜工艺可以提高电路板层间的导通性能,改善产品的导热性,减少孔内孔洞,降低传输信号的损失,这将有效的提高电子产品的可靠性和稳定性。在填孔镀铜工艺中添加剂组分之间的相互作用直接影响着填铜工艺的顺利进行,因此,了解镀铜添加剂的作用原理对填孔电镀工艺非常重要。 禾川化学是一家专业从事精细化学品以及高分子分析、研发的公司,具有丰富的分析研发经验,经过多年的技术积累,可以运用尖端的科学仪器、完善的标准图谱库、强大原材料库,彻底解决众多化工企业生产研发过程中遇到的难题,利用其八大服务优势,最终实现企业产品性能改进及新产品研发。 样品分析检测流程:样品确认—物理表征前处理—大型仪器分析—工程师
解谱—分析结果验证—后续技术服务。有任何配方技术难题,可即刻联系禾川化学技术团队,我们将为企业提供一站式配方技术解决方案! 2填孔电镀的工艺流程 2.1填孔镀铜的机理 填孔电镀添加剂由三类组份组成:光亮剂(又称加速剂),其作用减小极化,促进铜的沉积、细化晶粒;载运剂(又称抑制剂),增加阴极极化,降低表面张力,协助光亮剂作用;整平剂,抑制高电流密度区域铜的沉积。微盲孔孔底和孔内沉积速率的差异主要来源于添加剂在孔内不同位置吸附分布,其分布形成过程如下: 1、由于整平剂带正电,最易吸附在孔口电位最负的位置,并且其扩散速率较慢因此在孔底位置整平剂浓度较低; 2、加速剂最易在低电流密度区域富集,并且其扩散速率快,因此,孔底加速剂浓度较高; 3、在孔口电位最负,同时对流最强烈,整平剂将逐渐替代抑制剂加强对孔口的抑制,最终使得微孔底部的铜沉积速率大于表面沉积速率,从而达到填孔的效果。 2.2填孔镀铜的过程 填孔镀铜过程主要分为四个时期:起始期、爆发期、回复期、平衡期。 (1)起始期:在此阶段,分散于电镀液中的各添加剂,如抑制剂因分子
电镀常识
电镀基础知识100问 1.电解液为什么能够导电? 答:电解液导电与金属导体的导电方式是不一样的。在金属导体中,电流是靠自由电子的运动输送的,在电解液中则是由带电的离子来输送电流。在电解液中由于正负离子的电荷相等,所以不显电性,我们叫做电中性。当我们对电解液施加电压时,由于强大的电场的吸引力,离子分别跑向与自己极性相反的电极。阳离子跑向阴极,阴离子跑向阳极。它们的运动使电流得以通过,这就是电解液导电的道理。 2.在电镀过程中,挂具发热烫手,是由于镀液温度太高造成的吗? 答:挂具的发热虽然与溶液的温度有关系,但主要的原因是: (1)通过挂具的电流太大。 (2)挂具上的接触不良,电阻增高而使挂具发热。 3.控制电镀层厚度的主要因素是什么? 答:控制电镀层厚度的主要因素为电流密度、电流效率与电镀时间。 4.黄铜镀层与青铜镀层是同一样的台金镀层吗? 答:不是,黄铜镀层是铜和锌的合金镀层,青铜镀层是铜和锡的合金镀层。 5.法拉第定律是表示什么关系的,试述法拉第的第一定律和第二定律? 答:法拉第定律是描述电极上通过的电量与电极反应物重量之间的关系的,又称为电解定律。 法拉第第一定律:金属在电解时所析出的重量与电解液中所通过的电流和时间成正比。 W=KIt W——析出物质的重量(g) K——比例常数(电化当量) I——电流强度(安培) t——通电时间(小时) 法拉第第二定律:同量电流通过不同电解液时,则所析出金属之重量与各电解液之化学当量成正比。 K=CE C——比例常数。E——化学当量 6.为什么镀件从化学除油到弱酸蚀,中间要经清水洗净? 答:因为通常的化学除油溶液都是碱性的,如果把除油溶液直接带进酸腐蚀溶液中,就会起酸、碱的中和反应,降低了酸的浓度和作用。中和反应的生成物粘附在工件上,会影响镀层的质量。故工件在化学除油后,一定要经清水冲洗干净,才能进入酸腐蚀的溶液。 7.电镀层出现毛刺、粗粒,通常是那些原因造成的,如何解决? 答:镀层出现毛刺、粗粒,主要是镀液受悬浮杂质污染所造成的。其来源是:
滚镀碱铜电镀作业指导书
1.0 目的 规范碱铜电镀工序操作,维护事项,保证该工序品质和生产秩序顺畅。 2.0 适用范围 2.1 该工序作业员、化验技术人员。 2.2 碱铜镀浴的建立维护、操作及更新。 2.3 适用于各个有碱铜电镀工艺要求的表面处理操作。 3.0 职责 3.1 技术人员负责槽液分析和调整浓度并开出相应表单。 3.2 技术人员负责生产故障排除等技术维护工作。 3.3 作业人员对工作的规范性展开。 4.0内容 4.1 流程 4.2 镀槽及附属设备 4.2.1 主槽系耐高温防腐材质PP板,容积300L,液位距槽顶部10CM。 4.2.2 附属设备 项目温控装置整流机过滤机阴极移动 数量 1 1 1 型号热泵 规格4KW 200A/12V 2T/H 4.3 镀液组成和操作规范(使用的镀槽体积不同则开缸量不同具体工艺参数一样) 碱 铜 镀液组成规格名称含量范围开缸量 氰化亚铜电镀级CuCN 50-65g/L 18kg 游离氰化钠电镀级NaCN 18-25g/L 26kg 酒石酸钾钠25KG/包30-50g/L 9KG 4.4 调制溶液 4.4.1 加DI水至体积3/4。 4.4.2 不断搅拌下慢慢加入计量好的洒石酸钾钠,氰化钾待溶解后加入氰化亚铜,要边加边搅拌。 4.4.3 边搅拌边升温到50℃,然后开启过滤机,过滤机中长期放置活性碳芯连续过滤。 4.4.4 挂上装好干净电解铜的阳极篮,每个篮用阳极袋罩上。 4.4.5试镀生产 4.5 操作标准 项目温度时间电流过滤 范围45-55℃根据要求0.3-0.7ASD 过滤清洗15日/次,每15日更换棉芯,阳极清 洗90日/次
精品文档 .
安美特 电镀基础知识培训
Atotech (China) Chemicals Ltd.SH 安美特上海青浦分公司 PRESENTS ELECTROPLATING TRAINING 电镀培训
OUTLINE 内容提要 ?INTRODUCTION 介绍 ?ELECTROCHEMISTRY 电化学 ?CLEANING & PREPLATE 清洗及预镀?NICKEL 镍 ?Copper 铜 ?DECORATIVE CHROMIUM 装饰铬 ?TESTING 测试 ?FILTRATION 过滤 ?TROUBLE SHOOTING 故障处理
WHAT IS ELECTROPLATING ? 什么是电镀? THE DEPOSITION OF A METALLIC COATING UPON A NEGATIVELY CHARGED CATHODE BY THE PASSING OF AN ELECTRIC CURRENT 在电流通过时,有金属层沉积在带负电荷的阴极表面.
WHAT IS THE PURPOSE ? 电镀的目的是什么? ?TO OBTAIN A METALLIC COATING HAVING CERTAIN PROPERTIES SUCH AS HARDNESS, BRIGHTNESS, CORROSION RESISTANCE AND TO REPRODUCE IDENTICAL FORMS IN ELECTROFORMING. ?是为了得到具有某种特性的金属层,如:硬度、光亮度、耐腐性及在电铸方面复制同样的形状.
REQUIREMENTS 要求 ?SOURCE OF DIRECT CURRENT 直流电源 ?A PLATING TANK 电镀槽 ?A SOLUTION CONTAINING THE DISSOLVED SALTS OF THE METAL TO BE PLATED 含有待镀的可溶性金属盐的溶液 ?ANODE( POSITIVE ELECTRODE )阳极(正电极) ?A PREPARED OBJECT -CATHODE ( NEGATIVE ELECTRODE ) 准备好的待镀工件--阴极(负电极)
镀铜操作规范
镀铜操作规范 一.镀前准备 1.镀液检查 a. 查看镀液液位是否正常。超出时,停止或少冲水时,通知车间加 水补充。 b.查看溶液的波美度是否在18-23Be°之间(循环测定),超出23Be°时,适量加水稀释,如波美度高出23Be°液位高时,则必须通知车间并在交接表上作好记录。 c.镀液温度要求在40℃±2℃之间,如偏差大,则立即向车间汇报并在交接表上作好记录。 2.设备检查 a.查看操作面板所有按钮是否正常。 b.对导电系统传动系统水气管道等进行细致检查,发现问题及时反映,保证设备运行正常,电镀过程中导电良好。 3.版辊检查 a.检查钢辊表面是否有划伤、碰伤、料伤、刀纹等问题。光洁度是否合格,表面是否有横纹或螺旋纹。 b.检查堵头堵孔有无严重料伤,堵孔要求无碰伤。 c.检查版辊尺寸(直径、锥度、椭圆度)是否同机加工钢辊检验单相符。 d.钢辊表面不允许有影响电镀质量的、严重表面锈蚀和严重氧化层。如有以上问题必须汇报机加工返修一支,并向车间汇报。 4.接活
a.根据生产计划,查看工票并认真审阅工票上的各项内容。注意特种 版一定要有特定人员操作。 b.根据版辊不同的尺寸(特别是补铜)合理搭配。 c.根据版辊规格计算 版辊面积(S)=直径(R)*长度(L)*3.14(∏)(单位d㎡) 版面误差1d㎡ 安培小时(A.H)=版辊面积(S)/2*厚度(丝)*电流密度*槽系数 安培小时误差≤1A.H/d㎡ 电流(A)=版辊面积(S)/2*电流密度电流误差≤1.5A/d㎡ (铜的电流密度17-22A/d㎡)施镀为半浸或以计算面积需除以2)二.装版和打天车 1.装版见(装版操作规程) a.装版前要打磨铜瓦、堵头、堵孔穿杠及适配器内孔保证电镀过程中导电良好。 b.把有键槽的一端装中间保证版辊精度。 c.铁丝要装好,防止倒角烧焦(距离2-3cmm最好) 2.打天车 a.决不允许用湿手或手套操作天车控制盒。 b.天车运行时高度要适当,行走时要与天车平行,眼睛要看着天车,以 防以外事故发生。 c.打天车时,天车下面不允许站人,防止意外事故发生。 三.清洗过程
