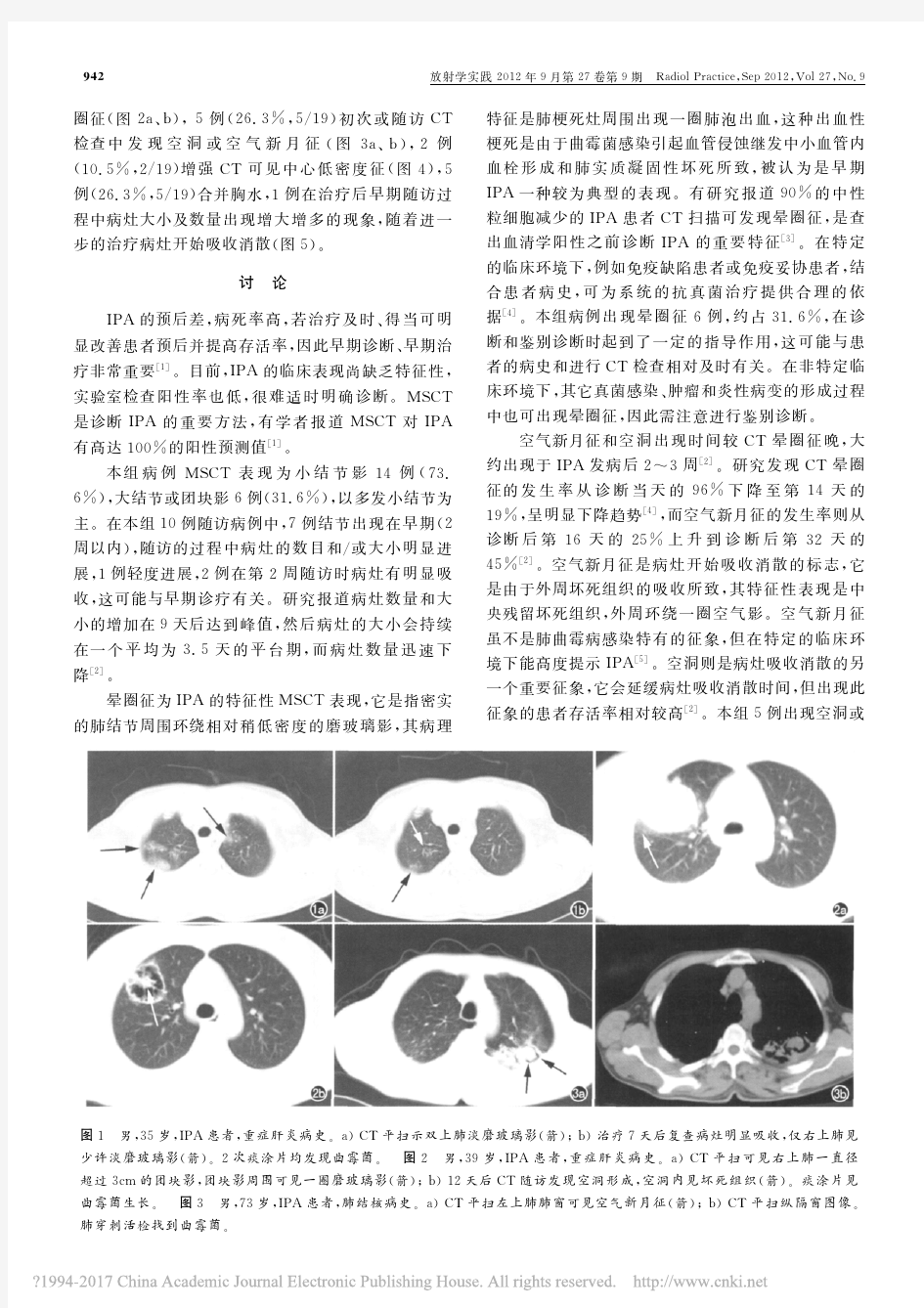
侵袭性肺曲霉菌病CT表现

侵袭性肺曲霉菌病的诊治
侵袭性肺曲霉菌病的诊治 中国医学论坛报2014-11-05发表评论 侵袭性曲霉病(Invasive Aspergillosis,IA)发病率逐年增加,病死率高。早期诊断治疗能提高生存率。医脉通小编收集侵袭性肺曲霉病诊治相关内容如下,以飨医友。 侵袭性肺曲霉病 肺曲霉病在临床上分为曲霉球、变态反应性支气管肺曲霉病(ABPA)和侵袭性肺曲霉病(IPA)等类型。 IPA是曲霉侵入肺组织所引起的深部真菌感染性疾病,以发展成坏死性出血性肺炎,形成多发性肺脓肿或肉芽肿,病灶边缘可有小动脉栓塞为特征,病情进展迅速,临床表现凶险。其主要见于免疫受损患者,常见危险因素包括中性粒细胞减少、造血干细胞移植、实体器官移植、长时间大剂量使用皮质类固醇激素、血液系统肿瘤、细胞毒性药物治疗以及罹患获得性免疫缺陷综合征(AIDS)等。 IPA初次诊断时误诊率较高,其诊断按确定程度分为确诊(proven)、临床诊断(probable)和拟似(possible)。确诊病例需要组织病理学依据或来自正常无菌部位的标本曲霉培养阳性。临床诊断病例需要有宿主因素、临床依据(症状、体征和影像学特征)及微生物学证据。 侵袭性肺曲霉病的诊断:GM试验、G试验
1,3-β-D-葡聚糖可特异性激活鲎变形细胞裂解物中的G因子,引起裂解物凝固,故常称G 试验。1,3-β-D葡聚糖是真菌的细胞壁成分,人体的吞噬细胞吞噬真菌后,会持续释放该物质,使血液及体液中含量增高(浅部真菌感染无类似现象),因此,G试验适用于深部真菌(隐球菌和接合菌除外)感染的早期诊断,尤其是念珠菌和曲霉菌,但不能确定菌种。在下列情况下会出现假阳性:①使用纤维素膜进行血透,标本或患者暴露于纱布或其他含有葡聚糖的材料;②静脉输注免疫球蛋白、白蛋白、凝血因子或血液制品;③链球菌血症;④操作者处理标本时存在污染;⑤使用多糖类抗癌药物、放化疗造成黏膜损伤导致食物中的葡聚糖或定植的念珠菌经胃肠道进入血液等;⑥食用菌类(例如蘑菇)等。G试验在不同研究中敏感性特异性差别较大,其敏感性为67%~100%,特异性为74%~90%。 GM试验检测的是半乳甘露聚糖(Galactomannan,GM)。曲霉菌特有的细胞壁多糖成分β(1-5)呋喃半乳糖残基,当菌丝生长时,半乳甘露聚糖从薄弱的菌丝顶端释放,是最早释放的抗原。GM释放量与菌量成正比,可以反映感染程度。在造血干细胞移植患者中的诊断敏感性高。值得注意的是,GM试验假阳性率较高,在如下情况下易发生:①使用半合成青霉素尤其是哌拉西林/他唑巴坦;②新生儿和儿童;③血液透析;④自身免疫性肝炎等;⑤食用可能含有GM的牛奶等高蛋白食物和污染的大米等;⑥冬虫夏草成分的虫草多糖也属于半乳甘露聚糖。在下述情况下也可出现假阴性:①释放入血循环中的曲霉GM(包括甘露聚糖)并不持续存在,而是会很快被清除;②以前使用过抗真菌药物; ③病情不严重;④非粒细胞缺乏的患者假阴性也较高。GM试验在不同人群中敏感性和特异性差别同样较大,敏感性为50% ~100%,特异性为73%~98%。 就如同其他许多血清学诊断检测方法一样,GM试验和G试验也会有一定的假阳性和假阴性情况,因此,临床上应当正确看待这两者的结果。 侵袭性肺曲霉病的治疗 根据多个IPA 诊治指南推荐,IPA患者的首选初始治疗推荐静脉或口服伏立康唑,对于病情严重患者,推荐使用静脉制剂(第1天6 mg/kg,q 12h,之后4 mg/kg,q 12h,至好转后改为口服伏
血管侵袭性肺曲霉菌病的+CT+表现
血管侵袭性肺曲霉菌病的CT表现 杨 蕾1,宋晓莉2,秦晓峰3,林吉征1 (1.青岛大学附属医院放射科 山东 青岛 266003;2.玲珑英诚医院检验科 山东 招远 265406;3.山西晋城煤业集团总医院放射科 山西 晋城 048000) 【摘 要】 目的 探讨血管侵袭性肺曲霉菌病的CT表现。方法 回顾性分析52例经病理或临床证实为血管IPA的CT表现。结果 多发35例;以双肺外周带分布为主39例;病灶形态为结节或肿块38例;伴有晕征21例,其中15例发生于血液系统恶性肿瘤患者;中心低密度征13例;反晕征5例;空气半月征或空洞28例,其中49个(67%,49/73)病灶的空气半月征或空洞位于近肺门位置;9例增强扫描病例出现环形强化。17例随访患者中,7例空气半月征、4例空洞分别出现在晕征之后的第2、4周。结论 血管IPA的CT常表现为双肺外周带多发结节或肿块影,常伴晕征或空气半月征或空洞,后二者多位于病变肺门侧;CT动态观察诊断意义较大;肿块结节内中心低密度征,反晕征以及增强扫描环形强化有助于诊断。 【关键词】 血管侵袭性肺曲霉菌病;晕征;空气半月征;体层摄影术,X线计算机 中图分类号:R379;R814.42 文献标识码:A 文章编号:1006‐9011(2015)05‐0805‐04 CTfindingsofpulmonaryangioinvasiveaspergillosis YANGLei1,SONGXiao‐li2,QINXiao‐feng3,LINJi‐zheng1 1.DepartmentofRadiology,TheAffiliatedHospitalofQingdaoUniversity,Qingdao266003,P.R.China 2.DepartmentofClinicalLaboratory,YingchengHospitalofLinglong,Zhaoyuan265406,P.R.China 3.DepartmentofRadiology,JinchengCoalGeneralHospitalofShanxi,Jincheng048000,P.R.China 【Abstract】 Objective ToanalyzetheMSCTperformanceofpulmonaryangioinvasiveaspergillosis.Methods CTap‐pearancesof52pulmonaryangioinvasiveaspergillosispatientsprovedbypathologyorclinicwereretrospectivelyanalyzed.Results Multiplelesions(35cases)mainlydistributedintheperipheralareasoflungfield(39cases).Theshapeofthelesionswerenodulesortumors(38cases)accompaniedwithhalosign(21cases),15casesofthese21caseswerehap‐penedinpatientswithhematologicmalignancies.Therewerehypodensesign(13cases),reversedhalosign(5cases),aircrescentsignorcavities(28cases),and49(67%,49/73)crescentsignorcavities.Amongthese28caseslocatednearthehilarofthelesions,9enhancedcasespresentedborderstrengthen.Thereweretotally17revisitedcases,presentingaircrescentsign(7cases)andcavities(4cases)respectivelyperformedafter2and4weeksofhalosigns.Conclusion Pul‐monaryangioinvasiveaspergillosisusuallypresentedmultiplenodulesortumorsintheperipheralareasoflungfield,usual‐lyaccompaniedwithhalosignoraircrescentsignorcavities.Thetwolattersignsusuallylocatednearthehilarofthele‐sions,CTdynamicfollow‐uphasadiagnosticsignificance.Thehypodensesign,reversedhalosignandborderstrengtheninenhancedcasesmayhelptodiagnosis. 【Keywords】 Pulmonaryangioinvasiveaspergillosis;Halosign;Aircrescentsign;Computedtomography 侵袭性肺曲霉菌病(Invasivepulmonaryasper‐gillosis,IPA)通常见于免疫抑制的患者中,例如血液系统恶性肿瘤及慢性消耗性疾病或是其他恶性肿瘤化疗后,近年来由于强效化疗药及免疫抑制剂的广泛应用,其患病率明显升高,严重威胁此类患者的生存。由于痰培养准确度低、半乳甘露聚糖测定敏作者简介:杨蕾(1986‐),女,山东招远人,青岛大学在读研究生,主要从事胸部影像诊断工作 通信作者:林吉征 副主任医师 E‐mail:linjizhd@163.com感度变数大及特异度低、霉菌DNA测定开展困难等现状,而胸部CT因为能够发现肺部感染的早期变化,成为目前检测肺曲霉菌感染的重要手段[1]。 IPA分为血管侵袭型、气道侵袭型及慢性坏死型(“半侵袭型”),其中最常见的是血管侵袭型,其重要意义不言而喻。本文搜集本院血管IPA患者52例,探讨其CT表现,旨在为该病的诊治提供有价值的依据。 1 资料与方法 508 医学影像学杂志2015年第25卷第5期 JMedImagingVol.25No.52015
变应性支气管肺曲霉菌病
变应性支气管肺曲霉菌病 变应性支气管肺曲霉病变应性支气管肺曲霉病(allergic bronchopulmonary aspergillosis,ABPA)是机体对寄生于支气管内曲霉菌(主要是烟曲霉菌)产生的变态反应性炎症。该病常在患有慢性哮喘或囊性纤维化(CF)患者的基础上发生。ABPA是1952年由英国学者Hinson等首先在哮喘患者中发现的。1968年由Patterson等报告了美国首例ABPA。过去认为ABPA是一种少见病,近年来由于血清学和影像学诊断方法的进展,ABPA的诊断率明显提高。Agarwal等最近报告在印度北部确诊的ABPA 126例。由于缺乏统一的诊断标准和标化的诊断试验,关于ABPA的发病率文献报道各异,在慢性持续性哮喘患者中发病率为1~2%,囊性纤维化患者中为2~15%。一些学者认为可将ABPA看作是哮喘的并发症。 一、发病机制 迄今为止,ABPA的发病机制尚不完全清楚。健康人由于有支气管粘膜-上皮屏障功能、粘液纤毛清除功能和肺泡巨噬细胞的吞噬作用,曲霉孢子经呼吸道吸入后即被清除,不会引起ABPA。仅特异体质者吸入曲霉孢子后才会导致ABPA。ABPA的发生也与宿主的基因表型有关。遗传学研究发现HLA-DR2和HLA-DR5基因型与易感者之间有密切关系。曲霉孢子吸入后黏附在气道上皮细胞表面或细胞之间发育生长成为菌丝。在此过程中释放蛋白水解酶和其它毒性物质,破坏气道上皮并激活上皮细胞。激活的上皮细胞释放一系列炎症前细胞因子和细胞趋化因子启动炎症反应,同时被蛋白水解酶破坏的上皮层增强了对曲霉抗原和其它变应原转运和递呈,进而诱导Th2型免疫反应,产生IL-4、IL-5、IL-13,其中IL-4和IL-13诱导B细胞产生IgE并激活肥大细胞,IL-5使嗜酸细胞脱颗粒。由特异性IgE介导的I型变态反应引起气道壁和周围组织的损害,出现支气管痉挛,腺体分泌增多,临床上表现为喘息、咳痰。此外抗原持续存在气道诱发了局部炎症,形成黏液栓,导致中心性支气管扩张,嗜酸细胞分泌多种致纤维化因子以及特异性IgG介导的Ⅲ型变态反应引起气道重构,最终致肺纤维化。 二、病理学特征 ABPA的病理改变早期主要表现为支气管壁大量单核细胞和嗜酸性细胞浸润,但不发生组织侵袭。以后出现黏液嵌塞、中心性支气管扩张和嗜酸细胞性肺炎,进一步发展为慢性细支气管炎和非干酪性支气管肉芽肿,晚期则出现广泛肺纤维化。 三、临床表现 1、症状和体征ABPA以儿童与青年人多发,患者常有哮喘或其他过敏性疾病史,儿童期间容易发病,糖皮质激素依赖的哮喘患者也易发生。临床可表现为急性或慢性过程。本病临床最常见症状为喘息,急性发作时可有发热、咳嗽、头痛、全身不适、咳白色或粘液泡沫痰,可有金棕色或墨绿色胶胨样痰栓,部分患者出现咳血。慢性期除有肺纤维化导致的呼吸困难、全身乏力和紫绀等症状外,还可出现支气管扩张合并感染的症状。体检时两肺可闻及哮鸣音,病程长的有肺气肿征象、杵状指(趾)
侵袭性肺曲霉菌病诊断及治疗进展
龙源期刊网 https://www.360docs.net/doc/9f8816489.html, 侵袭性肺曲霉菌病诊断及治疗进展 作者:李慧 来源:《健康必读(上旬刊)》2018年第11期 【摘要】肺曲霉菌病是真菌感染性疾病中的一种特殊类型,目前将其分为肺曲菌球、慢性坏死性肺曲霉菌病、变态反应性支气管肺曲霉菌病和侵袭性肺曲霉菌病。本文对侵袭性肺曲霉菌病的诊断及治疗进展进行了相关研究综述。 【关键词】肺曲霉菌病;诊断,鉴别;药物疗法;综述 【中图分类号】R969.4;;;;;;【文献标识码】B;;;;;【文章编号】1672-3783(2018)11-0192-01 在我国随着结核病、艾滋病、肿瘤的高发、器官移植的盛行及抗生素免疫抑制剂的应用增加,真菌病感染几率也在逐年增加。有文献报道继发性肺曲霉菌病的发生率为65%~96%,但诊断困难,导致误诊及延误治疗甚至致患者死亡。基于目前肺曲霉菌病发病率的上升,而临 床诊断的不重视及诊断方法导致诊断及治疗。临床表现肺结核病与肺曲霉菌感染的临床症状相似,较多临床医生对该病的认识不够,导致漏诊及误诊率较高。曲霉菌广泛分布于自然界,是一种机会致病菌,一般情况下不致病,只有在免疫力低下或长期有慢性疾病的情况下,才会引起曲霉菌感染。这可能与大量细胞毒性药物、免疫抑制剂、广谱抗生素及抗结核药的应用,或感染人类免疫缺陷病毒(HIV)或患有获得性免疫缺陷综合征(AIDS),使人体内菌群失调有关。 1;肺曲霉菌病的诊断 肺曲霉菌病的临床诊断包括痰霉菌培养、痰涂片、纤维支气管镜检、曲霉免疫学检查、经皮肺穿刺检查以及影像学检查。 诊断步骤:1)胸部X线片检查,确定大致诊断方向;2)病史和体格检查,进一步缩小诊断范围;3)无创性检查,协助诊断或确定诊断;4)有创性检查,经以上步骤不能确定诊断者,选择此方法。 诊断方法:金标准病理,诊断 I PA 的金标准金标准是组织学检测依据,包括经皮肺穿刺,开胸肺组织活检,经支气管镜肺组织活组织学标本中发现曲霉,已证实侵袭性肺曲霉菌病,血培养罕有阳性结果。 1.1;国内诊断标准 1.1.1;定义:侵袭性真菌病感染(invasive pulmonary fungal infections,IPFI)的診断有宿主因素、临床特征、微生物学检查和组织病理学四部分组成。临床诊断IPFI是要充分结合宿主
肺曲霉菌病的CT表现
肺曲霉菌病的CT表现 目的探讨肺曲霉菌病的CT影像表现特征,提高对本病认识和早期诊断。方法回顾性分析10例经病理活检、痰培养及手术证实的肺曲霉菌病的CT影像表现特征。结果10例CT表现中均不同程度地出现了结节状阴影,伴有晕征或空气半月征。结论晕征、空气半月征是侵袭型肺曲霉菌病的CT特征性表现,对肺曲霉菌病的临床诊断或早期治疗具有重要参考价值。 标签:肺;曲霉病;体层摄影术;MSCT 肺曲霉菌病是由曲霉菌引起的肺部疾病,其影像表现复杂多样,正确认识本病的影像表现对肺部疾病的鉴别诊断具有重要意义。肺曲霉菌病通过原发和继发两种不同的感染方式,主要是继发感染为主,即患者常在原发病变的基础上,如严重感染、慢性消耗性疾病,当人体抵抗力降低时使致病菌发展,引起疾病。另一方面长期大量广谱抗生素、免疫抑制剂、化疗及肾上腺皮质激素的应用,可使不敏感的曲霉菌得以繁殖。肺曲霉菌病影像学表现较复杂,缺乏特征性改变。肺曲菌病临床分为3型:曲霉菌球、侵袭性肺曲菌病(IPA)和变态反应性支气管肺曲菌病(ABPA)。本文收集了我院自2009年1月~2014年1月经临床确诊10例肺曲霉菌病例的CT资料进行总结和探讨,以提高影像对其诊断的准确性。 1资料与方法 1.1一般资料回顾性分析我院自2009年1月~2014年1月经确诊具有完整临床及CT资料的10例肺曲霉菌病中,其中男8例,女2例,年龄在42~84岁,平均年龄65岁。有7例患者有咳嗽,发热症状,3例咳血。 1.2方法CT扫描机为GE Hispeed DX/i型螺旋CT机,每例患者均采用平静呼吸状态下屏气自肺尖至肺底进行层厚10 mm,层距10 mm连续螺旋扫描,对较小病灶局部进行层厚2~5 mm,层距2~5 mm薄层扫描。 2结果 10例肺霉菌病中肺霉菌球型6例,侵袭性肺曲霉菌病4例,变态反应性支气管肺曲霉菌病1例。CT表现为多发球形或片状影4例,均可见”日晕”征;单发或多发空洞6例,且均发现6例空洞内软组织影及新月征,见图1~图4。 图1 左肺小片状阴影图2 同一患者,11 d后出现半月征及菌球 图3 空洞及洞内随体位变化之菌球图4 双肺多发空洞及”日晕征” 2.1多发球形或片状阴影4例,占40%在侵袭性肺曲霉菌病表现,多见。可累及多个肺段或肺叶,境界不清。CT表现为多在肺野中、外带,其边缘可见毛玻璃样改变,呈环或”日晕”征。
肺曲霉菌病
肺部真菌感染 肺部真菌感染是由真菌感染引起的支气管-肺部疾病。 肺部真菌感染可以通过临床表现、微生物学、免疫学检测来辅助诊断。其中免疫学检测血清中细胞壁成分(1,3)-β-D-葡聚糖抗原检测(G试验)、半乳甘露聚糖抗原检测(GM试验)阳性有重要的辅助诊断价值。 诊断: 1.肺念珠菌病 见于粒细胞缺乏、中心静脉留置导管、腹部大手术、激素和抗生素治疗、糖尿病、肾功能不全、器官移植等高危人群。临床症状有不能解释的持续发热、呼吸道症状,但体征轻微。咳嗽,甚至剧咳,咳少量白色黏液痰或浓痰。血型播散型常出现迅速进展的循环和呼吸衰竭。X线呈支气管肺炎改变或片状浸润或融合,可有空洞形成。下呼吸道分泌物、肺组织、胸水、血直接涂片或培养出念珠菌即可确诊。痰液直接涂片或培养出念珠菌并不能诊断为真菌病,因有10%~20%的正常人痰中可找到白色念珠菌,若3%双氧水含漱3次从深部咳出的痰(合格痰)连续≥2次培养出同一菌种的念珠菌则有诊断参考价值。血培养念珠菌阳性是念珠菌菌血症可靠的诊断证据。部分患者G试验阳性(需除外假阳性),可为临床诊断提供重要参考。 2.肺曲霉病 临床表现复杂,常见3种类型:过敏性支气管肺曲霉病(多见过敏体质)、曲霉球(最常见症状是咯血)和侵袭性肺曲霉病(为粒细胞缺乏或接受广谱抗生素、激素、免疫抑制剂治疗过程中出现不能解释的发热、干咳、胸痛,咯血等)。过敏性支气管肺曲霉病诊断标准包括: (1)反复哮喘样发作; (2)外周血嗜酸粒细胞增高≥1X109/L; (3)X线一过性或游走性肺部浸润; (4)血清总IgE浓度≥1000mg/ml; (5)曲霉抗原皮试阳性; (6)血清沉淀素抗体阳性; (7)特异性抗曲霉IgE和IgG滴度升高; (8)中央囊状支气管扩张。 肺曲霉球根据影像学特征可作出临床诊断,但需与其他真菌球、错构瘤、肺癌、棘球蚴囊肿、肺脓肿相鉴别。确诊需病原学和组织病理学。肺曲霉球CT特征为肺空洞或胸膜腔内圆形致密阴影,其边缘有透光晕影。若空腔较大,尚可见球形阴影有蒂与洞壁相连,形如钟摆,球形阴影可随体位变化而改变形态。如果空洞较小,球形病灶填充了大部分空腔,其晕影很小,仅呈一狭长的半月形透亮带。侵袭性肺曲霉病CT特征:早期为炎症阴影,周围呈现薄雾状渗出(“晕轮征”),随后炎症病灶出现气腔实变,可见支气管充气征,再后可见病灶呈现半月形透光区(“空气半月征”),进一步可变为完整的坏死空洞。其诊断采用上述提到的3级诊断标准。GM试验阳性提供重要参考。
侵袭性肺曲霉菌感染怎么回事
侵袭性肺曲霉菌感染怎么回事 真菌引起的疾病比较多,在对真菌引发疾病治疗上,一定要选择多种治疗方式,这样对缓解病情有很好帮助,而且真菌引发疾病,发展速度很快,患者患有后,需要及时的进行治疗,否则病情严重后,治疗上也是会很复杂,侵袭性肺曲霉菌感染是很多人不了解的,对它是怎么回事呢? 侵袭性肺曲霉菌感染怎么回事: 侵袭性肺部真菌感染,是指真菌引起的支气管肺部真菌感染,即真菌对气管支气管和肺部的侵犯,引起气道粘膜炎症和肺部炎症肉芽肿,严重者引起坏死性肺炎,甚至血行播散到其他部位。但需要注意的是,IPFI不包括真菌寄生和过敏所引起的肺部改变,分为原发性和继发性两种类型。原发性肺部真菌感染是指免疫功能正常、有或无临床症状的肺部真菌病;继发性肺部真菌感 染是指伴有宿主因素和(或)免疫功能受损的真菌感染,后者在临床上常见。IPFI常见的真菌主要是念珠菌属、曲霉属、隐球菌属、接合菌(主要指毛霉)和肺孢子菌等。
肺部真菌感染常继发于严重的原发病,症状、体征常无特征性,可有以下临床表现: (1)流感样症状:表现为发热、畏寒、头痛、流涕、关节痛、肌痛等; (2)隐匿性感染:无明显的症状和体征,可自愈; (3)肺部表现: ①肺炎或支气管炎:最常见,与一般细菌性肺炎难以鉴别。可有发热、咳嗽、咯白色粘稠痰或黄脓痰等症状,肺部可闻及湿性罗音,可伴有少至中量胸液; ②肺结核样表现:组织胞浆菌病、皮炎芽生菌病和奴卡菌病的临床表现有时酷似肺结核,可有干咳、咯血、胸痛等呼吸道症状及午后低热、盗汗等“结核中毒症状”; ③肺脓肿和脓胸:常急性起病,可有寒战、高热(多呈驰张热)、咳嗽、咯粘液脓性痰,有时痰中臭味明显,咯血多为痰中带血。放线菌病和奴卡菌病所致脓胸均易在胸壁上形成窦道;
肺曲霉病
专题笔谈 肺曲霉病病谱及其诊断策略 张静瞿介明 近年来,随着对肺曲霉病认识的增多和临床资料的积累,其分类也在不断演变。对肺曲霉病病谱的特点及其病理生理基础深入理解对疾病诊治尤为重要[1]。一方面,不同类型的肺曲霉病具有鲜明的特征,有助于早期诊断;另一方面,肺曲霉病的复杂性、多变性又阻碍了准确诊断,例如同为免疫功能低下患者,但因免疫功能抑制类型及程度不同,感染曲霉后的临床表现往往差别很大,多数缺乏典型特征;又如伴随疾病的临床表现往往掩盖了肺曲霉病演变过程中出现的蛛丝马迹。本文介绍肺曲霉病目前的常用分类及其特点,并在此基础上谈谈诊断方面需要注意的几个问题。 一、肺曲霉病病谱及其疾病特点 1.侵袭性肺曲霉病(invasive pulmonary aspergillosis, IPA):IPA多发生于免疫功能低下患者。经典的免疫功能低下指血液系统恶性肿瘤及异基因骨髓干细胞移植患者的持续粒细胞缺乏,是IPA的高危因素。非粒细胞缺乏患者,如长期应用糖皮质激素治疗、慢阻肺、营养不良、实体器官移植等也是IPA的易发人群[2]。 IPA可分为血管侵袭性曲霉病(angio-invasive aspergillosis, AGIA)和气道侵袭性曲霉病(airway invasive aspergillosis),后者根据累及的部位又可分为气管支气管炎(aspergillus tracheobronchitis, ATB)、支气管肺炎和细支气管炎。 AGIA多见于经典免疫功能低下患者,也可见于其他具有危险因素的患者。“晕征”是AGIA的早期影像学表现,在CT上表现为单个或多个结节或肿块,边缘模糊,有些聚集成簇,其病理基础是出血性肺梗死,中央的结节或肿块为坏死的肺组织,磨玻璃晕环提示肺泡出血[3]。空气新月征(air crescent)多发生于粒细胞缺乏患者AGIA中性粒细胞恢复时,一般在初发浸润的第6~26天(平均15 d)后出现,提示预后较好及免疫功能恢复。在X线胸片和CT检查均可见到环型 DOI:10.3760/cma.j.issn.1001-0939.2015.01.000 作者单位:200025上海,复旦大学附属中山医院呼吸内科(张静);上海交通大学医学院附属瑞金医院(瞿介明) 通信作者:瞿介明,Email: jmqu0906@https://www.360docs.net/doc/9f8816489.html,
变态反应性肺曲霉菌病怎么办
如对您有帮助,可购买打赏,谢谢变态反应性肺曲霉菌病怎么办 导语:变态反应性肺曲霉菌病通常情况下是伴随着肺部内出现感染的症状。而且常诱发出哮喘或者囊性纤维化等的并发症的出现。其病症会出现喘气、支气 变态反应性肺曲霉菌病通常情况下是伴随着肺部内出现感染的症状。而且常诱发出哮喘或者囊性纤维化等的并发症的出现。其病症会出现喘气、支气管扩张等现象的病情。出现病情时应当第一时间到医院进行治疗,然后搭配合理的食物进行食物治疗和药物治疗双结合的方式进行治疗,平时多参加户外运动。 变态反应性支气管肺曲霉病是哮喘和囊性纤维化患者常见的并发症,由机体对曲霉的变态反应引起,表现为喘息、肺部浸润、支气管扩张和肺纤维化;病理改变包括黏液嵌塞、中心性支气管肉芽肿、嗜酸细胞肺炎和慢性或渗出性毛细支气管炎;诊断依靠临床表现、实验室以及影像学改变等标准,并分为囊性纤维化和非囊性纤维化两组;治疗主要是口服激素联合依曲康唑。过去认为变态反应性肺曲霉菌病是一种少见病,近年来由于血清学和影像学诊断方法的进展,变态反应性肺曲霉菌病的诊断率明显提高。一些学者认为可将变态反应性肺曲霉菌病看作是哮喘的并发症。 迄今为止,变态反应性肺曲霉菌病的发病机制尚不完全清楚。健康人由于有支气管粘膜-上皮屏障功能、粘液纤毛清除功能和肺泡巨噬细胞的吞噬作用,曲霉孢子经呼吸道吸入后即被清除,不会引起变态反应性肺曲霉菌病。仅特异体质者吸入曲霉孢子后才会导致变态反应性肺曲霉菌病。变态反应性肺曲霉菌病的发生也与宿主的基因表型有关。遗传学研究发现HLA-DR2和HLA-DR5基因型与易感者之间有密切关系。曲霉孢子吸入后黏附在气道上皮细胞表面或细胞之间发育生长成为菌 预防疾病常识分享,对您有帮助可购买打赏
IDSA2016年新版曲霉菌病诊治指南
IDSA:2016年新版曲霉菌病诊治指南 曲霉菌病是感染曲霉菌引起的一种真菌病,可累及皮肤、黏膜、眼、鼻、支气管、肺、胃肠道、神经系统、骨骼等多器官系统,严重者导致败血症,病例呈世界性分布。病原体曲霉菌属丝状真菌,是一种常见的条件致病性真菌,广泛分布于自然界,其感染者并不少见。 时隔 8 年,美国感染病学会(IDSA)就曲霉菌病临床关注的热点问题,总结现有不同类型曲霉菌病相关证据,于近期发布了新版曲霉菌病诊治指南,替代2008 旧版指南,旨在为临床医生诊治管理此病提供参考。该 2016 新版指南于近期发表在 Clinical Infectious Diseases 杂志上。现将主要内容简述如下。 流行病学与感染风险因素 1. 易感者如何预防曲霉菌病?何为易感人群? (1)应将住院的异体造血干细胞移植(HSCT)接受者安置在受保护的环境中,以减少霉菌暴露机会(强烈推荐;证据级别低)。 (2)也应给予其他严重免疫功能低下的、易发生侵袭性曲霉菌病(IA)的高危患者相应防护措施,如急性白血病正在接受诱导/再诱导化疗方案治疗者(强烈推荐;证据级别低)。 (3)若住院无法提供防护病房的条件,推荐此类患者入住单独病房,且病房远离施工场地,也不允许将绿植或鲜花带入病房(强烈推荐;证据级别低)。 (4)建议对 IA 高危门诊患者采取合理防护措施,以减少霉菌暴露机会,包括避免园艺、施肥劳作或密切接触装修或施工场地(强烈推荐;证据级别低)。 (5)白血病诊疗中心与移植中心应当定期监测侵袭性霉菌感染。若发现霉菌感 染率超过基线水平,或者非高危人群发生侵袭性霉菌感染,应当立即对医源性感染情况进行评估(强烈推荐;证据级别低)。
侵袭性肺曲霉菌病15例CT分析
侵袭性肺曲霉菌病15例CT分析【关键词】肺曲霉菌病 侵袭性肺曲霉菌病(invasive pulmonary aspergillosis, IPA)的早期诊断非常困难,由于该病的早期临床表现及X线平片无特异性,痰培养的阳性率低于10%[1],血清学检查又不够可靠,因而以往确诊常依赖于有创的肺活检。随着薄层、高分辨CT扫描的广泛应用,IPA的CT表现更趋特征性[2]。作者回顾分析2000年1月至2006年5月15例经病理及实验室检查证实IPA患者的CT表现,旨在寻求该病的CT表现特点,为早期诊断及治疗提供帮助。 1 资料与方法 1.1 一般资料本组15例中男10例,女5例;年龄22~70岁,平均46岁。所有患者均有肺部感染症状,包括发热、咳嗽、咳痰、痰中带血、胸痛等。12例原发病变分别为白血病4例,肾移植术后3例,骨髓移植术后2例,淋巴瘤、糖尿病及AIDS患者各1例;无特殊病变3例。15例均经病理、实验室检查证实,其中手术后病理证实2例,CT引导下经皮穿刺肺活检6例,经纤维支气管镜活检5例,2例肺泡灌洗液培养找到典型菌丝,且治疗后症状消失。 1.2 检查方法所有患者均行胸部CT扫描,扫描机型为
SOMATOM PLUS 4 。扫描程序:先行常规胸部扫描,层厚8mm,螺距1.5,8mm层厚重建,然后对病变区进行薄层扫描,层厚2mm,层间距2mm。采用标准肺窗和纵隔窗观察病灶。
2 结果 侵袭性肺曲霉菌病的CT表现具有多样性,肺部单发或多发结节样软组织密度影或肿块影12例,表现为单发肿块或结节4例,多发肿块或结节6例,肿块合并多发结节2例,病灶多位于肺外带,靠近胸膜。其中8例结节影或肿块影周围可见“晕征”(halo sign)(图1),6例肿块或结节内形成空洞或“月芽征”(图2),胸膜下楔形实变影11例(图3),广基在胸膜侧,边缘毛糙模糊,局部胸膜增厚。其中3例单发,8例多发,多发者均合并多发结节影。 图1 白血病患者,两肺可见多发结节影,密度不均匀,结节周围绕有“晕征”;(略) 图2 中年女性患者,曾有腐烂毛霉织物接触史。两肺结节内形成空洞,右肺可见一楔形实变影;(略) 图3 糖尿病患者,左下肺可见一楔形实变影,广基在胸膜侧,右下肺可见小结节影。(略)
侵袭性肺曲霉病CT征象
侵袭性肺曲霉病CT征象 侵袭性肺曲霉病(invasive pulmonary aspergillosis,IPA)是一种种继发于免疫功能低下的严重机会性感染,多见于急性白血病并白细胞减少症、激素及其他免疫抑制剂应用、器官移植、AIDS和其他免疫抑制患者,此外,慢性重型肝炎患者也较常见。 影像学特征性表现为X线胸片以胸膜为基底的多发的楔形阴影或空洞;胸部CT早期为晕轮征(halo sign),即肺结节影(水肿或出血)周围环绕低密度影(缺血), 后期为新月体征(crescent sign)。部分患者可有中枢神经系统感染,出现中枢神经系统的症状和体征。 治疗首选两性霉素B,尤其对威胁生命的严重感染尽可能给予最大的耐受剂量[1-1.5mg/(kg·d)]。如患者不能耐受,首次宜从小剂量开始,每日0.lmg/kg 溶于5%葡萄糖溶液中缓慢避光静滴,逐日增加5-l0mg,至最大耐受剂量后维持治疗。目前对疗程、总剂量还没有统一的意见,可根据患者病情的程度、对治疗的反应、基础疾病或免疫状态个体化给予。滴液中加适量肝素有助于防止血栓性静脉炎。主要不良反应为畏寒、发热、心慌、腰痛及肝肾功能损害等。但用药过程中出现中度肾功能损害并非停药的指征。两性霉素B脂质复合体,其肾毒性较小,主要适合已有肾功能损害或用两性霉素B后出现肾毒性的患者,剂量5mg/( kg·d)。还可选用伏立康唑、卡泊芬净和米卡芬净等。【发病机制和病理】 吞噬细胞作为宿主的防御机制之一,其数量和功能在侵袭性肺曲菌病的发病中具有重意义。淋巴细胞介导的细胞免疫也是重要的。实验研究证明,中性粒细胞可阻止曲霉菌丝的形成,而单核细胞则主要影响分生孢子。病理主要表现为急性坏死性出血性肺炎。炎性浸润、化脓,进而形成肉芽肿。菌丝在肺内增殖和侵入血管,导致坏死性血管炎,造成血栓或菌栓。引起咯血和血行播散,肺外产生曲霉感染。 肺曲霉病多为局限性肉芽肿或广泛化脓性肺炎,伴脓肿形成。病灶呈急性凝固性坏死,伴坏死性血管炎、血栓及菌栓,甚至累及胸膜。 【临床表现】 是最常见的类型,肺组织破坏严重,治疗困难。典型病例为粒胞缺乏或接受广谱杭生素、免疫抑制剂和糖皮质激素过程中出现不能解释的发热,胸部症状以干咳、胸痛最常见。咯血虽不如前两种症状常见。但十分垂要,具有提示性诊断价值。当肺内病变广泛时出现气急、甚至呼吸衰竭。此外,还可以出现胃肠道出血及各种中枢神经系统症状。肺部体征取决于病变的性质和范围。 【CT表现】 1、侵袭性肺曲菌病的早期CT表现:1.包绕晕征(Halo sign)的结节:表现为肺内单发或多发类圆形结节周围绕以一独特的带或晕,密度低于结节中心而高于肺实质密度。有晕征的结节约见50%~68%的早期侵袭性肺曲菌病病例,它是侵袭性肺曲菌病早期较有特征性的CT表现(图3-131)。2.楔形实变影:表现为以胸膜而为基底的节段性实变影,边缘模糊,呈毛玻璃样改变,与栓塞性肺梗死相似,其病理基础为出血性肺梗死。楔形实变影也是侵袭性肺曲菌病早期较特征性的改变,其出现率约80%,远高于“结节加晕征”。楔型实变影可单独出现,也可合并结节影和(或)晕征。楔型实变影主要见于侵袭性肺曲菌病早期,也可见于毛霉菌病、细菌性肺炎或肺出血等疾病(图3-132)。3.其他表现:支气管周围实变和小叶中心结节代表侵袭性肺曲菌病沿气道播散。此外,胸腔积液和胸膜增厚粘连也较常见。 2、侵袭性肺曲菌病的晚期CT表现: 1.空气新月征:是指结节性病变或楔形实变中心出现新月形空洞。多见于侵袭性肺曲菌病诊断后2~3周的病例,病理特点是中心坏死组织和曲菌,周围为空气间隙。空气新月征表示感染消退期的开始。2.线条状瘢痕:与胸膜相连,见于感染恢复末期,提示病变基本痊愈(图3-134)。
治疗肺曲霉菌病需要做哪些化验检查
治疗肺曲霉菌病需要做哪些化验检查 是由曲霉菌感染或吸入曲霉菌属抗原引起的一组急、慢性肺部疾病。本病包括过敏型曲霉菌病、侵入型曲霉菌病、寄生虫型曲霉菌病,临床表现有所不同。胸部X线检查,有诊断价值。 (1)嗜酸性粒细胞(E)检测:过敏型曲霉菌病,E可增高。 (2)病原体检查:支气管一肺泡灌洗液培养可发现曲霉菌,组织学检查有菌丝入侵组织的形态学表现或 培养阳性,均可确诊。 (3)血清免疫学检测:过敏型曲霉菌病患者,血清总免疫球蛋白E(IgE)和特异性免疫球蛋白E(IgE)均明 显升高;用放免法和酶联吸附法(ELISA)检测侵入型曲霉菌病患者的循环曲霉菌抗原,为阳性。 肺曲霉菌病检查项: 1.嗜酸性粒细胞(E)直接计数 2.免疫球蛋白E(IgE) 3.呼吸道合胞病毒酶联免疫吸附试验(ELISA) 嗜酸性粒细胞(E)直接计数(正常值及其临床意义) 【单位】 个/升(个/L) 【正常值】 (50~300)×108/升 【临床意义】 同白细胞分类(DC) 免疫球蛋白E(IgE)(正常值及其临床意义) 【单位】 毫克/升(mg/L) 【正常值】 EIA法:成人为0.1~0.9毫克/升 【临床意义】 (1)增高:见于免疫球蛋白E(IgE)骨髓瘤、湿疹、支气管哮喘、过敏性疾病、寄生虫感染、药物及食物过敏 等。 (2)降低:某些进行性新生物、运动失调毛细血管扩张症及某些无丙种球蛋白血症。
呼吸道合胞病毒酶联免疫吸附试验(ELISA)(正常值及其临床意义) 【正常值】 阴性。 【临床意义】 阳性,见于婴幼儿下呼吸道感染,如细支气管炎和肺炎及成人上呼吸道感染等。原文地址:https://www.360docs.net/doc/9f8816489.html,/jibing/88.html
侵袭性肺曲霉病
侵袭性肺曲霉病 侵袭性肺曲霉病(IPA)是曲霉菌直接侵犯肺或支气管引起的肺部感染性疾病,最常见烟曲霉。主要病理改变是呈急性广泛坏死性出血性肺炎或有肉芽肿,曲霉丝侵入血管,导致坏死性血管炎。 【诊断要点】见三级诊断标准。 1.临床表现:急性肺炎症状(咳嗽、咯痰、发热、咯血),抗生素治疗无效。抗生素治疗无效的持续性发热、干咳、呼吸困难、咯血 2.辅助检查: 影像学表现:(1)急性侵袭性肺曲霉病:CT早期可见晕轮征(磨玻璃样环状阴影环绕病灶周围),2-3周出现空气新月征(原有病灶中出现新月状的低密度透光区),后期可形成曲霉球。(2)慢性坏死性肺曲霉病:CT可见上叶和下叶背段肺浸润性病变或结节影,伴有或不伴有空洞,可见曲霉球。(3)气道侵袭性肺曲霉病:影像学提示;①急性气管-支气管炎:X线多数正常;②细支气管炎:HRCT可见小叶中心性结节和“树-芽”征;③支气管肺炎:肺外周细支气管分布区小片实变影;④阻塞性支气管肺曲霉病:曲霉在官腔内呈团块状生长,好发于下叶,可有支气管扩张、大量黏液嵌塞。 微生物检查:GM试验阳性。 微生物检查:合格痰标本、支气管吸取物、BALF或胸腔积液涂片典型形态为45°分枝的有隔菌丝。
【治疗要点】 一线治疗:首选伏立康唑。 备选治疗:卡泊芬净、两性霉素B、两性霉素B脂质体。 缓解期用药:口服伏立康唑、泊沙康唑、伊曲康唑,直到临床或影像学表现缓解或者稳定。 大咯血时如有条件可行手术治疗或支气管动脉栓塞。 【药物处方】 一线治疗: 伏立康唑:第一天0.9%氯化钠/5%葡萄糖250ml+伏立康唑400mg(6mg/kg)静点12小时1次;以后0.9%氯化钠/5%葡萄糖250ml+伏立康唑 200mg(3mg/kg)静点12小时1次。 备选治疗: 处方1:卡泊芬净:第一次负荷量:0.9%氯化钠250ml+卡泊芬净70mg 静点(至少1h)。维持量:0.9%氯化钠250ml+卡泊芬净50mg 静点(至少1h) 每日1次。 处方2:两性霉素B:5%葡萄糖7-10ml/kg+两性霉素B 0.7-1mg/kg静点每日1次。
侵袭性肺曲霉病的护理查房
侵袭性肺曲霉病的护理查房 一、病理改变:主要是呈急性广泛坏死性出血性肺炎、化脓、形成脓肿或有上皮细胞和巨噬细胞组成的肉芽肿,曲霉丝在肺组织内增殖并侵入血管,导致坏死性血管炎,造成血栓和菌栓性出血,导致血行播散。IPA 的基本病理特征是化脓和梗死。其他组织病理反应还包括实 质结节性损害、支气管肉芽肿性损害和侵入性气管支气管炎等。病理组织切片可见菌丝和孢子经HE染色呈蓝灰色,略带红色背景,而PAS及嗜银染色分别呈红色和黑色。菌丝长短不一,多呈杆状,有分隔,直径为3~5卩m,并见多条菌丝沿同一方向反复分支,分支呈45 °角,呈放射状或珊瑚状排列。 二、临床表现: 1.急性侵袭性肺曲霉病本病临床表现不一,并缺乏特征性。早期,部分患者以持续性发热为唯一表现,这种发热一般对抗生素治疗无效。另有部分患者仅有干咳,提示为支气管炎症而非肺部浸润。肺部浸润病变广泛时可引起低氧血症,出现呼吸困难,病变累及胸膜时产生胸膜炎或脓胸,引起胸痛或上腹痛。随着病变进展,可有高热,出现肺部啰音和肺部浸润,少数可闻及胸膜摩擦音。可有咯血,常为少量咯血,也可出现大咯血并危及生命。白细胞减少的患者,大咯血常出现在白细胞恢复时约30%的患者。肺部和肺外可同时受累,肺外表现主要见于血流丰富的器官如胃肠道、肝、脑、肾、心脏等,偶见睾丸、横膈及皮肤受累。临床表现常与患者白细胞的数量和功能异常的程度有关。一般先有上呼吸道侵入性曲霉病,表现为会厌炎和口咽
部炎症,鼻腔和鼻旁窦受累更多见。鼻出血以及鼻腔填塞可引起局部鼻腔溃疡,可形成焦痂。若白细胞减少症患者出现鼻腔溃疡和肺部浸润高度提示本病。胸部X线片可见楔形阴影、斑片状浸润影、孤立性或多发性结节影等,病灶内可形成空洞,胸腔积液少见。胸部CT 可发现特征性的改变,疾病早期(约1周内)CT可见晕轮征(halo sign),即磨玻璃样环状阴影环绕病灶周围,因病灶周围水肿或出血所致;稍后(1周左右)可出现底边邻居胸膜、尖端朝向肺门的楔形阴影,与肺血栓栓塞症导致的肺梗死类似。空气新月征(cresce nt sign)出现较晚(2~3周左右),表现为原有病灶中出现新月状的低密度透光区,较常见于免疫抑制患者中性粒细胞恢复期,因梗死灶收缩所致。后期可在病灶内形成曲霉球。急性侵袭性肺曲霉病的进展速度快,通常在数天内病灶即可有明显增加,这也是其影像学特征之一。 2.慢性坏死性肺曲霉病 慢性坏死性肺曲霉病常见于中老年人,主要症状有咳嗽、咳痰、咯血和体征减退等,病情相对较轻,病程可长达数周至数月不等,一般可达 1~6个月。患者的基础免疫状况也相对好于急性侵袭性肺曲霉病患者,危险因素包括①慢性肺部疾病:如COPD、支气管哮喘、囊性肺纤维化、肺结核、肺部分切除术后、结节病、尘肺等;②全身性疾病;如糖尿病、类风湿关节炎、营养不良等疾病以及长期小剂量糖皮质激素治疗的患者。胸部影像学检查可见 单侧或双侧肺浸润性病变或结节影,边界常不规则,多发于上叶和下叶背段,伴有或不伴有空洞,有空洞者50%出现曲霉球,常有邻近
儿童侵袭性肺曲霉菌病诊治策略
专家经验谈 文章编号:1005-2224(2009)01-0022-04 儿童侵袭性肺曲霉菌病诊治策略 张 琪,王天有 作者单位:首都儿科研究所附属儿童医院,北京 100020电子信箱:zhangqi0355@sina .com 中图分类号:R72 文献标志码:B 张琪,副教授,主任医师,从事儿科临床工作20余年。现任首都儿科研究所附属儿童医院急诊科副主任,重症监护病房主任, 承担N I CU 和P I C U 危重患儿医疗救治工作。研究方向为小儿危重病医学。曾获北京市优秀人才资助项目、首都发展基金项目各1项,参加北京市重点学科项目、北京市优秀人 才资助项目、“十五”国家科技公关项目、北京市自然基金项目。在儿科核心期刊上发表论著30余篇,参编专著4部。 关键词:儿童;侵袭性肺曲霉菌病 Keywords :children;invasive pul m onary as pergill osis 真菌感染作为医院获得性机会性感染,已成为一类疾病引起关注。侵袭性曲霉菌感染(invasive as pergillus infec 2 ti on )尽管发生率低于白色念珠菌,但近年来病死率已升高 了3157倍,位居真菌感染中第一位[1]。肺是曲霉菌最容易侵袭的器官,一旦感染病死率可高达62%~100%,侵袭性肺曲霉菌病(invasive pul m onary as pergill osis,I P A )不仅是粒细胞缺乏、白血病、骨髓移植或实体器官移植患者等免疫受损儿童重要死亡原因之一,在I CU 危重患儿中的感染率也在上升[223]。降低儿童I P A 病死率有赖于认识风险因素、早期诊断和及时有效的治疗。 1 儿童侵袭性曲霉菌感染的现状 1995年美国学者对1941例免疫抑制儿童进行了调 查,22例确诊为侵袭性曲霉菌感染,其中15例死亡,病死率为6812%[4];2000年调查结果显示,每100000例免疫抑制或缺陷美国儿童中有437例感染曲霉,死亡相对危险率为318%~2116%;侵袭性曲霉菌病的总病死率预计为 58%,其中骨髓移植受体播散性或中枢神经系统曲霉病病 死率更高。2002—2005年美国6个中心对139例侵袭性曲霉菌病儿童进行调查,I P A 占59%,而皮肤、鼻窦、中枢、支气管、肾脏、骨骼、心内膜、血行、眼睛受累均在10%以下;即使在有效治疗甚至联合治疗下,仍有52%患儿死亡。无传统风险因素的I CU 危重患儿I P A 感染率在013%~ 518%,此类患儿所感染病原并不单一,8912%存在其他病 原微生物的感染(其中细菌5516%、病毒2714%、其他真菌 1619%) [4] ,因临床表现不典型,易被原发病或伴随感染所 掩盖,早期诊断困难,部分生前未能确诊,经尸检证实为侵袭性曲霉菌病者达59%[5]。 2 致病曲霉菌及感染途径 自然环境中曲霉菌普遍存在,目前被认识的曲霉菌有 175余种,据报道人类疾病密切相关的有19种,最常见的 致病曲霉菌包括:烟曲霉菌、黄曲霉菌、黑曲霉菌、土曲霉菌、构巢曲霉菌。感染途径有外源性和内源性2种,外源性感染由外界环境获得,通过呼吸道,消化道,皮肤,鼻窦侵入机体;内源性感染的则来自机体内部感染灶,通过血循环播散或直接扩散至邻近组织。有报道,定植先于感染发生,是否发病取决于机体免疫状态。爆发感染发生在免疫功能低下的骨髓移植、实体器官移植、白血病儿童常见,早产儿、新生儿、儿童危重病例证实为侵袭性曲霉菌感染者屡有发生。医院设施、通气设备、水源是医院获得性曲霉菌感染潜在的来源[6]。 3 曲霉菌感染的风险因素 儿童多中心大规模统计资料不多,2002—2005年美国 6个中心对139例侵袭性曲霉菌感染儿童临床研究发现,62%患者存在粒细胞缺乏症;69%儿童接受肾上腺糖皮质 激素治疗;60143%接受免疫抑制剂治疗;3413%儿童存在急、慢性移植物抗宿主反应[4]。接受免疫抑制剂、糖皮质激素、细胞毒药物及长期使用抗生素治疗的器官移植、血液病、恶性肿瘤、粒细胞减少、先天免疫缺陷病、获得性免疫缺陷病(A I D S )患儿为曲霉菌感染的高危人群已广为认可。非免疫抑制儿童,如体质虚弱(早产儿、新生儿、营养不良等)、慢性器官功能障碍(消化系统疾病、代谢紊乱疾患、糖
